Типы расчетных задач, их решение.ppt
- Количество слайдов: 61


При решении задач необходимо руководствоваться несколькими простыми правилами: 1. 2. 3. Внимательно прочитать условие задачи; 4. Записать, если это необходимо, уравнение реакции и расставить коэффициенты; 5. Решать задачу, используя понятие о количестве вещества, а не метод составления пропорций; 6. Записать ответ. Записать, что дано; Перевести, если это необходимо, единицы физических величин в единицы системы СИ (некоторые внесистемные единицы допускаются, например литры);

Вычислить относительную молекулярную массу малахита Cu. CO 3 ∙ Cu(OH)2, используемого для изготовления ювелирных изделий.

*Молярная масса – это отношение массы вещества к количеству вещества, т. е. * М(х) = m(x)/ν(x), (1) *где М(х) – молярная масса вещества Х, m(x) – масса вещества Х, ν(x) – количество вещества Х. Единица СИ молярной массы – кг/моль, однако обычно используется единица г/моль. Единица массы – г, кг. Единица СИ количества вещества – моль. * Любая задача по химии решается через количество вещества. Необходимо помнить основную формулу: * ν(x) = m(x)/ М(х) = V(x)/Vm = N/NA, (2) *где V(x) – объем вещества Х(л), Vm – молярный объем газа (л/моль), N – число частиц, NA - постоянная Авогадро.

1. Определите массу иодида натрия Na. I количеством вещества 0, 6 моль. Дано: γ(Na. I)= 0, 6 моль. Найти: m(Na. I) =? Решение. 1. Молярная масса иодида натрия составляет: M(Na. I) = Mr (Na) + Mr (I) = 23 + 127 = 150 г/моль 2. Определяем массу Na. I: m(Na. I) = γ (Na. I) • M(Na. I) = 0, 6 • 150 = 90 г.

2. Определите количество вещества атомного бора, содержащегося в тетраборате натрия Na 2 B 4 O 7 массой 40, 4 г. Дано: m(Na 2 B 4 O 7)=40, 4 г. Найти: γ(B)=? Решение. 1. Молярная масса тетрабората натрия составляет 202 г/моль. 2. Определяем количество вещества Na 2 B 4 O 7: γ(Na 2 B 4 O 7)= m(Na 2 B 4 O 7)/ М( Na 2 B 4 O 7) = 40, 4/202=0, 2 моль. 3. Вспомним, что 1 моль молекулы тетрабората натрия содержит 2 моль атомов натрия, 4 моль атомов бора и 7 моль атомов кислорода (см. формулу тетрабората натрия). Тогда количество вещества атомного бора равно: ν(B)= 4 • ν(Na 2 B 4 O 7) =4 • 0, 2 = 0, 8 моль.

1. Сколько граммов серной кислоты необходимо для получения 0, 3 моль сульфата цинка? Дано: γ(Zn. SO 4)= 0, 3 моль Найти: m(Н 2 SO 4)=?

Массовая доля вещества – отношение массы данного вещества в системе к массе всей системы, т. е. ω(Х) =m(Х)/m, где ω(X)– массовая доля вещества Х, m(X) - масса вещества Х, m - масса всей системы. Массовая доля – безразмерная величина. Её выражают в долях от единицы или в процентах. Например, массовая доля атомного кислорода составляет 0, 42, или 42%, т. е. ω(О)=0, 42. Массовая доля атомного хлора в хлориде натрия составляет 0, 607, или 60, 7%, т. е. ω(Cl)=0, 607.

1. Определите массовую долю кристаллизационной воды в дигидрате хлорида бария Ba. Cl 2 • 2 H 2 O. Дано: Ba. Cl 2 • 2 H 2 O Найти: ω(H 2 O) = ? Решение. 1. Молярная масса Ba. Cl 2 • 2 H 2 O составляет: М(Ba. Cl 2 • 2 H 2 O) = 137+ 2 • 35, 5 + 2 • 18 =244 г/моль 2. Из формулы Ba. Cl 2 • 2 H 2 O следует, что 1 моль дигидрата хлорида бария содержит 2 моль Н 2 О. Отсюда можно определить массу воды, содержащейся в Ba. Cl 2 • 2 H 2 O: m(H 2 O) = 2 • 18 = 36 г. 3. Находим массовую долю кристаллизационной воды в дигидрате хлорида бария Ba. Cl 2 • 2 H 2 O. ω(H 2 O) = m(H 2 O)/ m(Ba. Cl 2 • 2 H 2 O) = 36/244 = 0, 1475 = 14, 75%.

2. Из образца горной породы массой 25 г, содержащей минерал аргентит Ag 2 S, выделено серебро массой 5, 4 г. Определите массовую долю аргентита в образце. Дано: m(Ag )=5, 4 г; m = 25 г. Найти: ω(Ag 2 S) =? Решение. 1. Определяем количество вещества серебра, находящегося в аргентите: ν(Ag ) =m(Ag )/M(Ag ) = 5, 4/108 = 0, 05 моль. 2. Из формулы Ag 2 S следует, что количество вещества аргентита в два раза меньше количества вещества серебра. Определяем количество вещества аргентита: ν( Ag 2 S)= 0, 5 • ν (Ag) = 0, 5 • 0, 05 = 0, 025 моль 3. Рассчитываем массу аргентита: m(Ag 2 S) = ν( Ag 2 S) • М(Ag 2 S) = 0, 025 • 248 = 6, 2 г. 4. Теперь определяем массовую долю аргентита в образце горной породы, массой 25 г. ω(Ag 2 S) = m(Ag 2 S)/ m = 6, 2/25 = 0, 248 = 24, 8%.

1. Определите простейшую формулу соединения калия с марганцем и кислородом, если массовые доли элементов в этом веществе составляют соответственно 24, 7, 34, 8 и 40, 5%. Дано: ω(K) =24, 7%; ω(Mn) =34, 8%; ω(O) =40, 5%. Найти: формулу соединения.

Решение: 1. Для расчетов выбираем массу соединения, равную 100 г, т. е. m=100 г. Массы калия, марганца и кислорода составят: m (К) = m ω(К); m (К) = 100 • 0, 247= 24, 7 г; m (Mn) = m ω(Mn); m (Mn) =100 • 0, 348=34, 8 г; m (O) = m ω(O); m (O) = 100 • 0, 405 = 40, 5 г. 2. Определяем количества веществ атомных калия, марганца и кислорода: ν(К)= m(К)/ М( К) = 24, 7/39= 0, 63 моль ν(Mn)= m(Mn)/ М( Mn) = 34, 8/ 55 = 0, 63 моль ν(O)= m(O)/ М(O) = 40, 5/16 = 2, 5 моль 3. Находим отношение количеств веществ: ν(К) : ν(Mn) : ν(O) = 0, 63 : 2, 5. Разделив правую часть равенства на меньшее число (0, 63) получим: ν(К) : ν(Mn) : ν(O) = 1 : 4. Следовательно, простейшая формула соединения KMn. O 4.

2. При сгорании 1, 3 г вещества образовалось 4, 4 г оксида углерода (IV) и 0, 9 г воды. Найти молекулярную формулу вещества, если его плотность по водороду равна 39. Дано: m(в-ва) =1, 3 г; m(СО 2)=4, 4 г; m(Н 2 О)=0, 9 г; ДН 2 =39. Найти: формулу вещества.

Решение. 1. Предположим, что искомое вещество содержит углерод, водород и кислород, т. к. при его сгорании образовались СО 2 и Н 2 О. Тогда необходимо найти количества веществ СО 2 и Н 2 О, чтобы определить количества веществ атомарных углерода, водорода и кислорода. ν(СО 2) = m(СО 2)/ М(СО 2) = 4, 4/44 = 0, 1 моль; ν(Н 2 О) = m(Н 2 О)/ М(Н 2 О) = 0, 9/18 = 0, 05 моль. 2. Определяем количества веществ атомарных углерода и водорода: ν(С)= ν(СО 2); ν(С)=0, 1 моль; ν(Н)= 2 • ν(Н 2 О); ν(Н)= 2 • 0, 05 = 0, 1 моль. Следовательно, массы углерода и водорода будут равны: m(С) = ν( С) • М(С) = 0, 1 • 12 = 1, 2 г; m(Н) = ν( Н) • М(Н) = 0, 1 • 1 =0, 1 г.

3. Определяем качественный состав вещества: m(в-ва) = m(С) + m(Н) = 1, 2 + 0, 1 = 1, 3 г. Следовательно, вещество состоит только из углерода и водорода (см. условие задачи). Определим теперь его молекулярную массу, исходя из данной в условии задачи плотности вещества по водороду. М(в-ва) = 2 • ДН 2 = 2 • 39 = 78 г/моль. 4. Далее находим отношение количеств веществ углерода и водорода: ν(С) : ν(Н) = 0, 1 : 0, 1 Разделив правую часть равенства на число 0, 1, получим: ν(С) : ν(Н) = 1 : 1 Примем число атомов углерода (или водорода) за «х» , тогда, умножив «х» на атомные массы углерода и водорода и приравняв эту сумму молекулярной массе вещества, решим уравнение: 12 х + х = 78. Отсюда х= 6. Следовательно, формула вещества С 6 Н 6 – бензол.

Молярный объем газа равен отношению объема газа к количеству вещества этого газа, т. е. Vm= V(X)/ ν(x), где Vm - молярный объем газа - постоянная величина для любого газа при данных условиях; V(X) – объем газа Х; ν(x) – количество вещества газа Х. Молярный объем газов при нормальных условиях (нормальном давлении рн= 101 325 Па ≈ 101, 3 к. Па и температуре Тн= 273, 15 К ≈ 273 К) составляет Vm= 22, 4 л/моль. В расчетах, связанных с газами, часто приходится переходить от данных условий к нормальным или наоборот. При этом удобно пользоваться формулой, следующей из объединенного газового закона Бойля-Мариотта и Гей-Люссака: p. V pн. Vн ──── = ─── Т Тн где p - давление; V - объем; Т- температура в шкале Кельвина; индекс «н» указывает на нормальные условия. Состав газовых смесей часто выражают при помощи объемной доли – отношения объема данного компонента к общему объему системы, т. е. φ(Х) = V(X)/V где φ(Х) – объемная доля компонента Х; V(X) - объем компонента Х; V - объем системы. Объемная доля – безразмерная величина, её выражают в долях от единицы или в процентах.

1. Какой объем займет при температуре 20 о. С и давлении 250 к. Па аммиак массой 51 г? Дано: m(NH 3)=51 г; p=250 к. Па; t=20 o. C. Найти: V(NH 3) =? Решение. 1. Определяем количество вещества аммиака: ν(NH 3) = m(NH 3)/ М(NH 3) = 51/17 = 3 моль. 2. Объем аммиака при нормальных условиях составляет: V(NH 3) = Vm • ν(NH 3) = 22, 4 • 3 = 67, 2 л. 3. Используя формулу , приводим объем аммиака к данным условиям [температура Т= (273 +20)К = 293 К]: pн. TVн(NH 3) 101, 3 • 293 • 67, 2 V(NH 3) =──── = ───── = 29, 2 л. p. Тн 250 • 273

2. Определите объем, который займет при нормальных условиях газовая смесь, содержащая водород, массой 1, 4 г и азот, массой 5, 6 г. Дано: m(N 2)=5, 6 г; m(H 2)=1, 4 ; н. у. Найти: V(смеси)=? Решение. 1. Находим количества вещества водорода и азота: ν(N 2) = m(N 2)/ М(N 2) = 5, 6/28 = 0, 2 моль ν(H 2) = m(H 2)/ М(H 2) = 1, 4/ 2 = 0, 7 моль 2. Так как при нормальных условиях эти газы не взаимодействуют между собой, то объем газовой смеси будет равен сумме объемов газов, т. е. V(смеси)=V(N 2) + V(H 2)=Vm • ν(N 2) + Vm • ν(H 2) = 22, 4 • 0, 2 + 22, 4 • 0, 7 = 20, 16 л.

Расчеты по химическим уравнениям (стехиометрические расчеты) основаны на законе сохранения массы веществ. Однако в реальных химических процессах из-за неполного протекания реакции и различных потерь веществ масса образующихся продуктов часто бывает меньше той, которая должна образоваться в соответствии с законом сохранения массы веществ. Выход продукта реакции (или массовая доля выхода) – это выраженное в процентах отношение массы реально полученного продукта к его массе, которая должна образоваться в соответствии с теоретическим расчетом, т. е. η = [mp(X) • 100]/m(X) где η– выход продукта, %; mp(X) - масса продукта Х, полученного в реальном процессе; m(X) - рассчитанная масса вещества Х. В тех задачах, где выход продукта не указан, предполагается, что он – количественный (теоретический), т. е. η=100%.

1. Какую массу фосфора надо сжечь для получения оксида фосфора (V) массой 7, 1 г? Дано: m(P 2 O 5)=7, 1 г. Найти: m(Р) =? Решение. 1. Записываем уравнение реакции горения фосфора и расставляем стехиометрические коэффициенты. 4 P+ 5 O 2 = 2 P 2 O 5 2. Определяем количество вещества P 2 O 5, получившегося в реакции. ν(P 2 O 5) = m(P 2 O 5)/ М(P 2 O 5) = 7, 1/142 = 0, 05 моль. 3. Из уравнения реакции следует, что ν(P 2 O 5)= 2 • ν(P), следовательно, количество вещества фосфора, необходимого в реакции равно: ν(P 2 O 5)= 2 • ν(P) = 2 • 0, 05= 0, 1 моль. Отсюда находим массу фосфора: m(Р) = ν(Р) • М(Р) = 0, 1 • 31 = 3, 1 г.

2. В избытке соляной кислоты растворили магний массой 6 г и цинк массой 6, 5 г. Какой объем водорода, измеренный при нормальных условиях, выделится при этом? Дано: m(Mg)=6 г; m(Zn)=6, 5 г; н. у. Найти: V(H 2) =?

Решение. 1. Записываем уравнения реакции взаимодействия магния и цинка с соляной кислотой и расставляем стехиометрические коэффициенты. Zn + 2 HCl = Zn. Cl 2 + H 2↑ Mg + 2 HCl = Mg. Cl 2 + H 2↑ 2. Определяем количества веществ магния и цинка, вступивших в реакцию с соляной кислотой. ν(Mg) = m(Mg)/ М(Mg ) = 6/24 = 0, 25 моль ν(Zn) = m(Zn)/ М(Zn) = 6, 5/65 = 0, 1 моль. 3. Из уравнений реакции следует, что количество вещества металла и водорода равны, т. е. ν(Mg) = ν(Н 2); ν(Zn) = ν(Н 2), определяем количество водорода, получившегося в результате двух реакций: ν(Н 2) = ν(Mg) + ν(Zn) = 0, 25 + 0, 1= 0, 35 моль. 4. Рассчитываем объем водорода, выделившегося в результате реакции: V(H 2) = Vm • ν(H 2) = 22, 4 • 0, 35 = 7, 84 л.

3. При пропускании сероводорода объемом 2, 8 л (нормальные условия) через избыток раствора сульфата меди (II) образовался осадок массой 11, 4 г. Определите выход продукта реакции. Дано: V(H 2 S)=2, 8 л; m(осадка)= 11, 4 г; н. у. Найти: η =? Решение. 1. Записываем уравнение реакции взаимодействия сероводорода и сульфата меди (II). H 2 S + Cu. SO 4 = Cu. S ↓+ H 2 SO 4 2. Определяем количество вещества сероводорода, участвующего в реакции. ν(H 2 S) = V(H 2 S) / Vm = 2, 8/22, 4 = 0, 125 моль. 3. Из уравнения реакции следует, что ν(H 2 S) = ν(Сu. S) = 0, 125 моль. Значит можно найти теоретическую массу Сu. S. m(Сu. S) = ν(Сu. S) • М(Сu. S) = 0, 125 • 96 = 12 г. 4. Теперь определяем выход продукта, пользуясь формулой : η = [mp(X) • 100]/m(X)= 11, 4 • 100/ 12 = 95%.

4. Какая масса хлорида аммония образуется при взаимодействии хлороводорода массой 7, 3 г с аммиаком массой 5, 1 г? Какой газ останется в избытке? Определите массу избытка. Дано: m(HCl)=7, 3 г; m(NH 3)=5, 1 г. Найти: m(NH 4 Cl) =? m(избытка) =?

Решение. 1. Записываем уравнение реакции. HCl + NH 3 = NH 4 Cl 2. Эта задача на «избыток» и «недостаток» . Рассчитываем количества вещества хлороводорода и аммиака и определяем, какой газ находится в избытке. ν(HCl) = m(HCl)/ М(HCl) = 7, 3/36, 5 = 0, 2 моль; ν(NH 3) = m(NH 3)/ М(NH 3) = 5, 1/ 17 = 0, 3 моль. Аммиак находится в избытке, поэтому расчет ведем по недостатку, т. е. по хлороводороду. 3. Из уравнения реакции следует, что ν(HCl) = ν(NH 4 Cl) = 0, 2 моль. Определяем массу хлорида аммония. m(NH 4 Cl) = ν(NH 4 Cl) • М(NH 4 Cl) = 0, 2 • 53, 5 = 10, 7 г. 4. Мы определили, что аммиак находится в избытке (по количеству вещества избыток составляет 0, 1 моль). Рассчитаем массу избытка аммиака. m(NH 3) = ν(NH 3) • М(NH 3) = 0, 1 • 17 = 1, 7 г.

5. Технический карбид кальция массой 20 г обработали избытком воды, получив ацетилен, при пропускании которого через избыток бромной воды образовался 1, 1, 2, 2 –тетрабромэтан массой 86, 5 г. Определите массовую долю Са. С 2 в техническом карбиде. Дано: m = 20 г; m(C 2 H 2 Br 4)=86, 5 г. Найти: ω(Са. C 2) =?

Решение. 1. Записываем уравнения взаимодействия карбида кальция с водой и ацетилена с бромной водой и расставляем стехиометрические коэффициенты. Ca. C 2 +2 H 2 O = Ca(OH)2 + C 2 H 2 +2 Br 2 = C 2 H 2 Br 4 2. Находим количество вещества тетрабромэтана. ν(C 2 H 2 Br 4) = m(C 2 H 2 Br 4)/ М(C 2 H 2 Br 4) = 86, 5/ 346 = 0, 25 моль. 3. Из уравнений реакций следует, что ν(C 2 H 2 Br 4) =ν(C 2 H 2) = ν(Са. C 2) =0, 25 моль. Отсюда мы можем найти массу чистого карбида кальция (без примесей). m(Са. C 2) = ν(Са. C 2) • М(Са. C 2) = 0, 25 • 64 = 16 г. 4. Определяем массовую долю Са. C 2 в техническом карбиде. ω(Са. C 2) =m(Са. C 2)/m = 16/20 = 0, 8 = 80%.

1. Рассчитайте ∆Ho 298 химической реакции Na 2 O(т) + H 2 O(ж) = 2 Na. OH(т) по значениям стандартных теплот образования веществ ( см. таблицу приложения). Укажите тип реакции (экзо- или эндотермическая). , Решение По данным таблицы 1 приложения, стандартные энтальпии образования Na 2 O(т), H 2 O(ж) и Na. OH(т) при 298 К равны соответственно – 416, – 286 и – 427, 8 к. Дж/моль. Используя следствие из закона Гесса, рассчитываем ∆Ho 298 химической реакции: ∆Ho 298 = 2 (Na. OH, т) – [ (Na 2 O, т) + (H 2 O, ж)] = 2×(– 427, 8) – – [– 416 + (– 286)] = – 153, 6 к. Дж. Ответ: – 153, 6 к. Дж.

2. Составьте термохимическое уравнение реакции взаимодействия Na 2 O(т) и H 2 O(ж), если при этом образуется 1 моль Na. OH(т). В ответе приведите количество теплоты, указанное в термохимическом уравнении. Решение: Коэффициенты в термохимическом уравнении имеют смысл молей. Поэтому допустимы дробные значения коэффициентов. 1 моль гидроксида натрия может образоваться из 1/2 моля оксида натрия и 1/2 моля воды. В задании 1 (см. выше) рассчитано, что при образовании 2 моль Na. OH в данной реакции выделяется 153, 6 к. Дж теплоты (∆Ho 298 = – 153, 6 к. Дж). Поэтому при образовании 1 моль Na. OH количество выделившейся теплоты будет в 2 раза меньше, т. е. 76, 8 к. Дж. В термохимическом уравнении количество выделяющейся теплоты указывают со знаком “плюс”: 1/2 Na 2 O(т) + 1/2 H 2 O(ж) = Na. OH(т) + 76, 8 к. Дж. Ответ: +76, 8 к. Дж.

3. Определите, возможно ли при 95 o. С самопроизвольное протекание процесса Na 2 O(т) + H 2 O(ж) = 2 Na. OH(т). Ответ обоснуйте, рассчитав величину изменения энергии Гиббса при данной температуре. Решение: Переведем температуру в шкалу Кельвина: Т=273+95=368 К. Для расчета ∆Go 368 воспользуемся уравнением: ∆Go 368 =∆Ho – T∆So Воспользуемся табличными значениями. При этом величину изменения энтропии необходимо перевести из Дж/К в к. Дж/К, поскольку значения ∆H и ∆G обычно измеряют в к. Дж. – 17, 18 Дж/К = – 0, 01718 к. Дж/К ∆Go 368 = – 153, 6 – 368×(– 0, 01718) = – 147, 3 к. Дж. Таким образом, ∆Go 368 < 0, поэтому самопроизвольное протекание данного процесса при 95 o. С возможно. Ответ: – 147, 3 к. Дж; возможно.

Основными компонентами этого типа задач являются: а) массовая доля растворенного вещества в растворе; б) масса растворенного вещества в растворе; в) масса раствора. Предполагают, что: а) все получившиеся смеси и сплавы являются однородными; б) смешивание различных растворов происходит мгновенно; в) объем смеси равен сумме объемов смешиваемых растворов; г) объемы растворов и массы сплавов не могут быть отрицательными.

Определения и обозначения. Массовая доля растворенного вещества в растворе - это отношение массы этого вещества к массе раствора. где - массовая доля растворенного вещества в растворе; - масса раствора.

Следствия формулы (1): Основными методами решения задач на смешивание растворов являются: с помощью расчетной формулы, “Правило смешения”, “Правило креста”, графический метод, алгебраический метод.

Введем обозначения: - массовая доля растворенного вещества в первом растворе; - массовая доля растворенного вещества во втором растворе; - массовая доля растворенного вещества в новом растворе, полученном при смешивании первого и второго растворов; m 1(в-ва), m 2(в-ва), m(в-ва) - массы растворенных веществ в соответствующих растворах; m 1(р-ра), m 2(р-ра), m(р-ра) - массы соответствующих растворов.

Основные методы: 1. С помощью расчетной формулы 2. “Правило смешения” 3. “Правило креста” 4. Графический метод 5. Алгебраический метод

1. С помощью расчетной формулы В наших обозначениях, получим формулу для вычисления массовой доли вещества в смеси. 1. Масса полученного при смешивании раствора равна: m(р-ра) = m 1(р-ра) + m 2(р-ра). 2. Определим массы растворенных веществ в первом и втором растворах: m 1(в-ва)= • m 1(р-ра), m 2(в-ва)= • m 2(р-ра). 3. Следовательно, масса растворенного вещества в полученном растворе вычисляется как сумма масс веществ в исходных растворах: m(в-ва) = m 1(в-ва) + m 2(в-ва) = • m 1(р-ра) + • m 2(р-ра).

4. Таким образом, массовая доля растворенного вещества в полученном растворе равна: или где - массы соответствующих растворов.
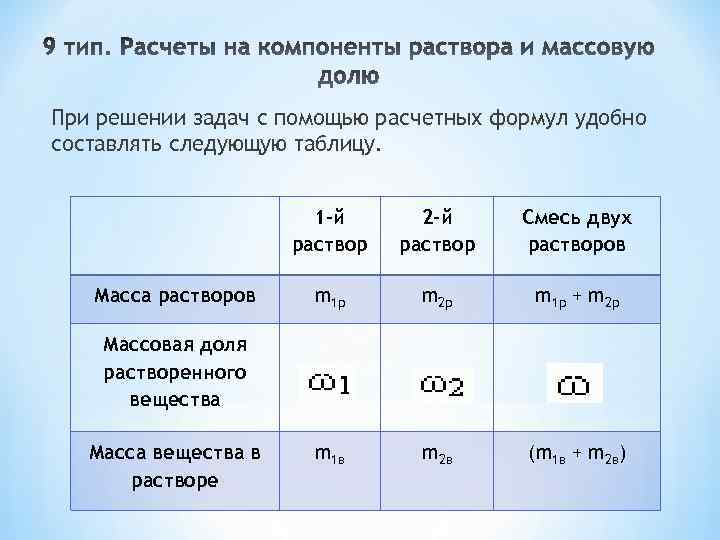
При решении задач с помощью расчетных формул удобно составлять следующую таблицу. 1 -й раствор Масса растворов 2 -й раствор Смесь двух растворов m 1 р m 2 р m 1 р + m 2 р m 1 в m 2 в (m 1 в + m 2 в) Массовая доля растворенного вещества Масса вещества в растворе

2. “Правило смешения” Воспользуемся формулой (4): тогда отсюда

Таким образом, отношение массы первого раствора к массе второго равно отношению разности массовых долей смеси и второго раствора к разности массовых долей первого раствора и смеси. Аналогично получаем, что при Замечание: Формула (5) удобна тем, что на практике, как правило, массы веществ не отвешиваются, а берутся в определенном отношении.

3. “Правило креста” “Правилом креста” называют диагональную схему правила смешения для случаев с двумя растворами. Слева на концах отрезков записывают исходные массовые доли растворов (обычно слева вверху-большая), на пересечении отрезков - заданная, а справа на их концах записываются разности между исходными и заданной массовыми долями. Получаемые массовые части показывают в каком отношении надо слить исходные растворы.

4. Графический метод Отрезок прямой (основание графика) представляет собой массу смеси, а на осях ординат откладывают точки, соответствующие массовым долям растворенного вещества в исходных растворах. Соединив прямой точки на осях ординат, получают прямую, которая отображает функциональную зависимость массовой доли растворенного вещества в смеси от массы смешанных растворов в обратной пропорциональной зависимости Полученная функциональная прямая позволяет решать задачи по определению массы смешанных растворов и обратные, по массе смешанных растворов находить массовую долю полученной смеси.

Построим график зависимости массовой доли растворенного вещества от массы смешанных растворов. На одной из осей ординат откладывают точку, соответствующую массовой доли 1 раствора, а на другой – 2 раствора. Обозначим на оси абсцисс точки А и В с координатами (0, 0) и (m 1 + m 2, 0), соответственно. На графике точка А(0, 0) показывает, что массовая доля всего раствора равна , а точка В(m 1 + m 2, 0) - массовая доля всего раствора равна. В направлении от точки А к точке В возрастает содержание в смеси 2 -го раствора от 0 до m 1+ m 2 и убывает содержание 1 -го раствора от m 1+ m 2 до 0. Таким образом, любая точка на отрезке АВ будет представлять собой смесь, имеющую одну и ту же массу с определенным содержанием каждого раствора, которое влияет на массовую долю растворенного вещества в смеси. Замечание: Данный способ является наглядным и дает приближенное решение. При использовании миллиметровой бумаги можно получить достаточно точный ответ.

5. Алгебраический метод Задачи на смешивание растворов решают с помощью составления уравнения или системы уравнений.

Задача 1. В воде массой 40 г растворили железный купорос Fe. SO 4 • 7 H 2 O массой 3, 5 г. Определите массовую долю сульфата железа (II) в полученном растворе. Дано: m(H 2 O)=40 г; m(Fe. SO 4 • 7 H 2 O)=3, 5 г. Найти: ω(Fe. SO 4) =? Решение. 1. Найдем массу Fe. SO 4 содержащегося в Fe. SO 4 • 7 H 2 O. Для этого рассчитаем количество вещества Fe. SO 4 • 7 H 2 O. ν(Fe. SO 4 • 7 H 2 O)=m(Fe. SO 4 • 7 H 2 O)/М(Fe. SO 4 • 7 H 2 O)=3, 5/278=0, 0125 моль 2. Из формулы железного купороса следует, что ν(Fe. SO 4)= ν(Fe. SO 4 • 7 H 2 O)=0, 0125 моль. Рассчитаем массу Fe. SO 4: m(Fe. SO 4) = ν(Fe. SO 4) • М(Fe. SO 4) = 0, 0125 • 152 = 1, 91 г. 3. Учитывая, что масса раствора складывается из массы железного купороса (3, 5 г) и массы воды (40 г), рассчитаем массовую долю сульфата железа в растворе. ω(Fe. SO 4) =m(Fe. SO 4)/m=1, 91 /43, 5 = 0, 044 =4, 4 %.

Задача 2. В 100 г 20%-ного раствора соли добавили 300 г её 10%-ного раствора. Определите процентную концентрацию раствора. Примеры решения с помощью следующих методов: 1. С помощью расчетной формулы 2. Графический метод 3. Последовательных вычислений 4. Алгебраический метод

Пример решения с помощью расчетной формулы
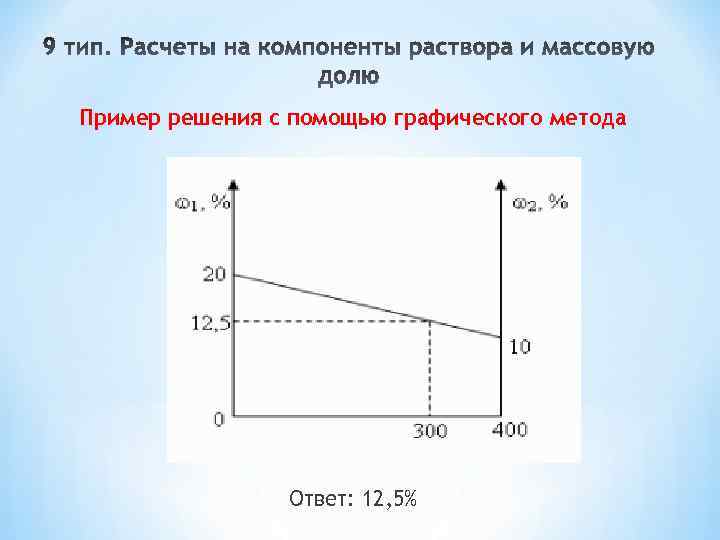
Пример решения с помощью графического метода Ответ: 12, 5%

Пример решения с помощью последовательных вычислений 1. Сколько растворенного вещества содержится: а) в 100 г 20%-ного раствора; [100 • 0, 2 = 20(г)] б) в 300 г 10%-ного раствора? [300 • 0, 1 = 30(г)] 2. Сколько вещества содержится в образовавшемся растворе? 20 г + 30 г = 50 г 3. Чему равна масса образовавшегося раствора? 100 г + 300 г = 400 г 4. Какова процентная концентрация полученного раствора? (50/400)100 = 12, 5(%) Ответ: 12, 5%

Пример решения с помощью алгебраического метода 1. Пусть х - процентная концентрация полученного раствора. 2. В первом растворе содержится 0, 2 • 100(г) соли, а во втором 0, 1 • 300(г), а в полученном растворе х • (100 + 300)(г) соли. 3. Составим уравнение: 0, 2 • 100 + 0, 1 • 300 = х • (100 + 300); х = 0, 125 (12, 5%) Ответ: 12, 5%

Задача 3. Смешали 10%-ный и 25%-ный растворы соли и получили 3 кг 20%-ного раствора. Какое количество каждого раствора в килограммах было использовано? Примеры решения с помощью следующих методов: 1. Алгебраический метод 2. Графический метод 3. “Правило смешения” 4. “Правило креста”

Пример решения с помощью алгебраического метода а) C помощью уравнения: Пусть х (кг) - масса 1 -го раствора, тогда 3 -х (кг) -масса 2 -го раствора. 0, 1 • х (кг) содержится соли в 1 -ом растворе, 0, 25 • (3 -х) (кг) содержится соли в 2 -ом растворе, 0, 2 • 3 (кг) содержится соли в смеси. Учитывая, что масса соли в 1 -ом и 2 -ом растворах равна массе соли в смеси, составим и решим уравнение: 0, 1 • х + 0, 25 • (3 -х) = 0, 2 • 3; 0, 15 х = 0, 15; х = 1, 1 кг-масса 1 -го раствора 3 - х = 3 - 1 =2 (кг) - масса 2 -го раствора. Ответ: 1 кг, 2 кг. б) С помощью системы уравнений Пусть х (кг) - количество первого раствора, у (кг) - количество второго раствора. Система уравнений имеет вид: Ответ: 1 кг, 2 кг.
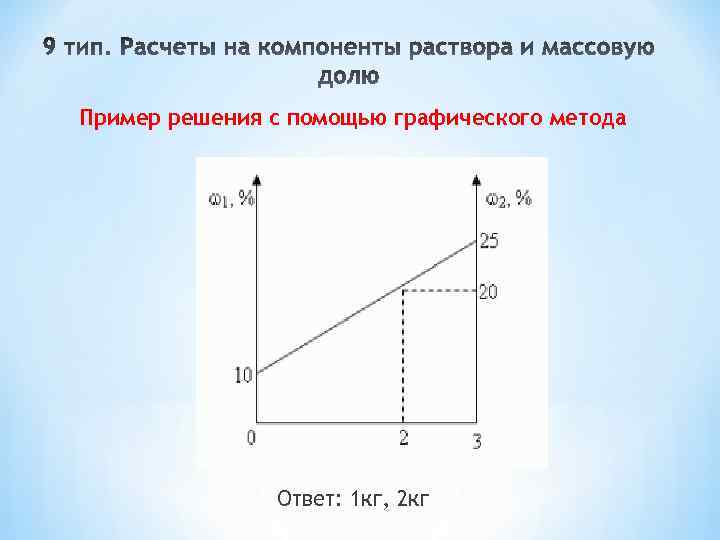
Пример решения с помощью графического метода Ответ: 1 кг, 2 кг

Пример решения с помощью «правила смешения» Ответ: 1 кг, 2 кг

Пример решения с помощью «правила креста» Ответ: 1 кг, 2 кг

Задача 4. Сосуд емкостью 5 л содержит 2 л р %-ного (по объёму) раствора соли. Сколько литров 20%-ного раствора такой же соли надо налить в сосуд, чтобы процентное содержание соли в сосуде стало наибольшим? Пример решения с помощью графического метода

Заметим, что по условию, объём второго раствора не превышает трёх литров. 1) Если р < 20, то для того, чтобы получить максимальную массовую долю вещества в растворе, необходимо добавить 3 л 20% ного раствора соли; 2) Если р = 20, то при добавлении 2 -го раствора, процентное содержание соли в растворе не изменится, следовательно, можно прилить от 0 л до 3 л 20% - ного раствора соли; 3) Если р > 20, то при добавлении 2 -го раствора, процентное содержание соли будет уменьшаться, т. е. прилить нужно 0 л. Ответ: 3 л, если 0 < р < 20, [0, 3], если р = 20, 0 л, если 20 < р 100.

Задача 5. В двух сосудах по 5 л каждый содержится раствор соли. Первый сосуд содержит 3 л р% - ного раствора, а второй - 4 л 2 р% - ного раствора одной и той же соли. Сколько литров надо перелить из второго сосуда в первый, чтобы получить в нем 10% - ный раствор соли? При каких значениях р задача имеет решение?

Пример решения с помощью алгебраического метода

Найдем, при каких значениях р задача имеет решение. По условию задачи 5 -ти литровый сосуд содержит 3 л первого раствора, следовательно, к нему можно прилить от 0 до 2 л второго раствора. Имеем, Решая неравенство, получаем Ответ:

Типы расчетных задач, их решение.ppt