химия. сигареты.pptx
- Количество слайдов: 51

Презентация по химии Ученицы 11 «Б» класса Игнатовой Аллы.

СИГАРЕТЫ

НЕМНОГО О… Сигаре та (от французского cigarette — маленькая сигара) — бумажный цилиндр, внутри которого находится измельчённый табак для курения. Большинство сигарет фабричного производства имеют размер 84 мм в длину и 7 -8 мм в диаметре, а также специальный фильтр, частично снижающий концентрацию ядовитых веществ во вдыхаемом курильщиком дыме. Бо льшая часть бумаги, используемой для производства сигарет, сделана из льна или льняного волокна. Она содержит 20— 30 % карбоната кальция, обладающего отбеливающим эффектом.


ДЛЯ УСКОРЕНИЯ СГОРАНИЯ ТАБАКА В СИГАРЕТЫ ЧАСТО ДОБАВЛЯЮТ СПЕЦИАЛЬНЫЕ ВЕЩЕСТВА. БЕЗ ДОБАВОК ТАБАК ГОРИТ ДОСТАТОЧНО ПЛОХО, ОСОБЕННО В ОТСУТСТВИЕ ПРИНУДИТЕЛЬНОЙ ТЯГИ (ЗАТЯЖЕК КУРЯЩЕГО). ПАЧКА СИГАРЕТ — ПЛОТНАЯ БУМАЖНАЯ УПАКОВКА, ОБЫЧНО СОДЕРЖАЩАЯ 20 СИГАРЕТЕСТЬ СПЕЦИАЛЬНЫЕ ПАЧКИ СИГАРЕТ, . СОДЕРЖАЩИЕ 10— 25 И ДРУГОЕ ИХ КОЛИЧЕСТВО, НО ЭТО СКОРЕЕ ИСКЛЮЧЕНИЕ, НЕЖЕЛИ ПРАВИЛО. СООТВЕТСТВИИ С ДЕЙСТВУЮЩИМ В ЗАКОНОМ РФ НА КАЖДОЙ ПАЧКЕ ДОЛЖНА НАХОДИТЬСЯ НАДПИСЬ, ПРЕДУПРЕЖДАЮЩАЯ О ВРЕДЕ КУРЕНИЯ, ДОЛЖНА БЫТЬ НАКЛЕЕНА СПЕЦИАЛЬНАЯ АКЦИЗНАЯ МАРКА И ПРИВЕДЕНА ЦЕНА, ВЫШЕ КОТОРОЙ РАСПРОСТРАНЕНИЕ ЗАПРЕЩЕНО. ПОСТОЯННОЕ КУРЕНИЕ СИГАРЕТ, КАК И ДРУГИЕ СПОСОБЫ КУРЕНИЯ ТАБАКА, ВЫЗЫВАЕТ СИЛЬНУЮ ЗАВИСИМОСТЬ И ОКАЗЫВАЕТ УСТОЙЧИВОЕ НЕГАТИВНОЕ ВОЗДЕЙСТВИЕ НА ЗДОРОВЬЕ КУРЯЩЕГО. ТРАДАЕТ ТАКЖЕ С ЗДОРОВЬЕ НЕКУРЯЩИХ ЛЮДЕЙ, КОТОРЫЕ НАХОДЯТСЯ РЯДОМ С КУРИЛЬЩИКОМ И ЧАСТО ПОДВЕРГАЮТСЯ ДЕЙСТВИЮ ТАБАЧНОГО ДЫМА. ФЕДЕРАЛЬНОЕ ЗАКОНОДАТЕЛЬСТВО РФ ЗАПРЕЩАЕТ ПРОДАЖУ ТАБАЧНЫХ ИЗДЕЛИЙ НЕСОВЕРШЕННОЛЕТНИМ.
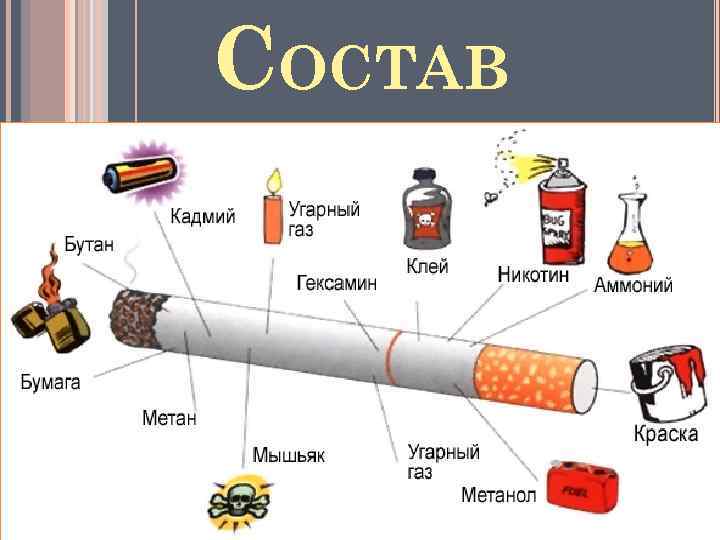
СОСТАВ
БУТАН

БУТА Н (C 4 H 10) — ОРГАНИЧЕСКОЕ СОЕДИНЕНИЕ КЛАССА АЛКАНОВ. В ХИМИИ НАЗВАНИЕ ИСПОЛЬЗУЕТСЯ В ОСНОВНОМ ДЛЯ ОБОЗНАЧЕНИЯ Н- БУТАНА. ТАКОЕ ЖЕ НАЗВАНИЕ ИМЕЕТ СМЕСЬ Н-БУТАНА И ЕГО ИЗОМЕРА ИЗОБУТАНА CH(CH 3)3. НАЗВАНИЕ ПРОИСХОДИТ ОТ КОРНЯ «БУТ-» (АНГЛИЙСКОЕ НАЗВАНИЕ МАСЛЯНОЙ КИСЛОТЫ — BUTYRIC ACID) И СУФФИКСА «-АН» (ПРИНАДЛЕЖНОСТЬ К АЛКАНАМ). БОЛЬШИХ В КОНЦЕНТРАЦИЯХ ЯДОВИТ, ВДЫХАНИЕ БУТАНА ВЫЗЫВАЕТ ДИСФУНКЦИЮ ЛЁГОЧНО-ДЫХАТЕЛЬНОГО АППАРАТА. СОДЕРЖИТСЯ В ПРИРОДНОМ ГАЗЕ, ОБРАЗУЕТСЯ ПРИ КРЕКИНГЕ НЕФТЕПРОДУКТОВ, ПРИ РАЗДЕЛЕНИИ ПОПУТНОГО НЕФТЯНОГО ГАЗА, "ЖИРНОГО" ПРИРОДНОГО ГАЗА. АК К ПРЕДСТАВИТЕЛЬ УГЛЕВОДОРОДНЫХ ГАЗОВ ПОЖАРО- И ВЗРЫВООПАСЕН, МАЛОТОКСИЧЕН, ИМЕЕТ СПЕЦИФИЧЕСКИЙ ХАРАКТЕРНЫЙ ЗАПАХ, ОБЛАДАЕТ НАРКОТИЧЕСКИМИ СВОЙСТВАМИ. ПО СТЕПЕНИ ВОЗДЕЙСТВИЯ НА ОРГАНИЗМ ГАЗ ОТНОСИТСЯ К ВЕЩЕСТВАМ 4 -ГО КЛАССА ОПАСНОСТИ (МАЛООПАСНЫЕ) ПО ГОСТ 12. 1. 007 -76. ВРЕДНО ВОЗДЕЙСТВУЕТ НА НЕРВНУЮ СИСТЕМУ.
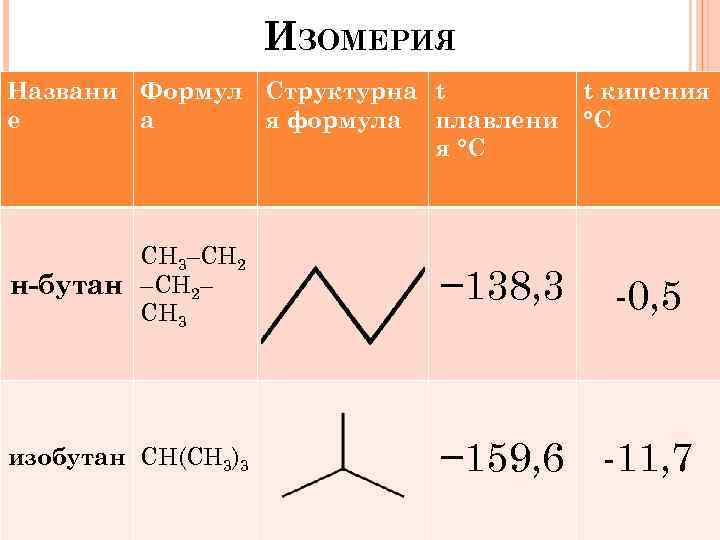
ИЗОМЕРИЯ Названи Формул Структурна t е а я формула плавлени я °С t кипения °С CH 3–CH 2 н-бутан –CH 2– CH 3 − 138, 3 изобутан CH(CH 3)3 − 159, 6 -11, 7 -0, 5

ФИЗИЧЕСКИЕ СВОЙСТВА БУТАН — БЕСЦВЕТНЫЙ ГОРЮЧИЙ ГАЗ, СО СПЕЦИФИЧЕСКИМ ЗАПАХОМ, ЛЕГКО СЖИЖАЕМЫЙ (НИЖЕ 0 °C И НОРМАЛЬНОМ ДАВЛЕНИИ ИЛИ ПРИ ПОВЫШЕННОМ ДАВЛЕНИИ И ОБЫЧНОЙ ТЕМПЕРАТУРЕ — ЛЕГКОЛЕТУЧАЯ ЖИДКОСТЬ). ТОЧКА ЗАМЕРЗАНИЯ -138°С (ПРИ НОРМАЛЬНОМ ДАВЛЕНИИ). РАСТВОРИМОСТЬ В ВОДЕ — МГ В 100 М Л ВОДЫ (ДЛЯ Н-БУТАНА, ПРИ 6, 1 20 °C, ЗНАЧИТЕЛЬНО ЛУЧШЕ РАСТВОРЯЕТСЯ В ОРГАНИЧЕСКИХ РАСТВОРИТЕЛЯХ ). МОЖЕТ ОБРАЗОВЫВАТЬ АЗЕОТРОПНУЮ СМЕСЬ С ВОДОЙ ПРИ ТЕМПЕРАТУРЕ ОКОЛО 100 °C И ДАВЛЕНИИ 10 АТМ. НАХОЖДЕНИЕ И ПОЛУЧЕНИЕ СОДЕРЖИТСЯ В ГАЗОВОМ КОНДЕНСАТЕ И НЕФТЯНОМ ГАЗЕДО 12 % ( ). ЯВЛЯЕТСЯ ПРОДУКТОМ КАТАЛИТИЧЕСКОГО И ГИДРОКАТАЛИТИЧЕСКОГО КРЕКИНГА НЕФТЯНЫХ ФРАКЦИЙ. В ЛАБОРАТОРИИ МОЖЕТ БЫТЬ ПОЛУЧЕН ПО РЕАКЦИИ ВЮРЦА. 2 C 2 H 5 BR + 2 A →CH 3 -CH 2 -CH 3 + N 2 NABR
МЕТАН

МЕТА Н (ЛАТ. METHANUM) — ПРОСТЕЙШИЙ УГЛЕВОДОРОД, БЕСЦВЕТНЫЙ ГАЗ (В НОРМАЛЬНЫХ УСЛОВИЯХ) БЕЗ ЗАПАХА, ХИМИЧЕСКАЯ ФОРМУЛА — CH 4. МАЛОРАСТВОРИМ В ВОДЕ, ЛЕГЧЕ ВОЗДУХА. ПРИ ИСПОЛЬЗОВАНИИ В БЫТУ, ПРОМЫШЛЕННОСТИ В МЕТАН ОБЫЧНО ДОБАВЛЯЮТ ОДОРАНТЫ (ОБЫЧНО МЕРКАПТАНЫ) СО СПЕЦИФИЧЕСКИМ «ЗАПАХОМ ГАЗА» . ЕТАН НЕТОКСИЧЕН И НЕОПАСЕН М ДЛЯ ЗДОРОВЬЯ ЧЕЛОВЕКА. ОДНАКО ИМЕЮТСЯ ДАННЫЕ, ЧТО МЕТАН ОТНОСИТСЯ К ТОКСИЧЕСКИМ ВЕЩЕСТВАМ, ДЕЙСТВУЮЩИМ НА ЦЕНТРАЛЬНУЮ НЕРВНУЮ СИСТЕМУ. НАКАПЛИВАЯСЬ В ЗАКРЫТОМ ПОМЕЩЕНИИ, МЕТАН ВЗРЫВООПАСЕН. БОГАЩЕНИЕ ОДОРАНТАМИ О ДЕЛАЕТСЯ ДЛЯ ТОГО, ЧТОБЫ ЧЕЛОВЕК ВОВРЕМЯ ЗАМЕТИЛ УТЕЧКУ ГАЗА. НА ПРОМЫШЛЕННЫХ ПРОИЗВОДСТВАХ ЭТУ РОЛЬ ВЫПОЛНЯЮТ ДАТЧИКИ И ВО МНОГИХ СЛУЧАЯХ МЕТАН ДЛЯ ЛАБОРАТОРИЙ И ПРОМЫШЛЕННЫХ ПРОИЗВОДСТВ ОСТАЕТСЯ БЕЗ ЗАПАХА.

ПОЛУЧЕНИЕ В ЛАБОРАТОРИИ ПОЛУЧАЮТ НАГРЕВАНИЕМ НАТРОННОЙ ИЗВЕСТИ (СМЕСЬ ГИДРОКСИДОВ НАТРИЯ И КАЛЬЦИЯ) ИЛИ БЕЗВОДНОГО ГИДРОКСИДА НАТРИЯ С ЛЕДЯНОЙ УКСУСНОЙ КИСЛОТОЙ. 2 NAOH+CH 3 COOH→(T)NA 2 CO 3+CH 4↑+H 2 O ДЛЯ ЭТОЙ РЕАКЦИИ ВАЖНО ОТСУТСТВИЕ ВОДЫ, ПОЭТОМУ И ИСПОЛЬЗУЕТСЯ ГИДРОКСИД НАТРИЯ, ТАК КАК ОН МЕНЕЕ ГИГРОСКОПИЧЕН. ВОЗМОЖНО ПОЛУЧЕНИЕ МЕТАНА СПЛАВЛЕНИЕМ АЦЕТАТА НАТРИЯ С ГИДРОКСИДОМ НАТРИЯ: CH 3 COONA +NAOH → CH 4↑ + NA 2 CO 3 ТАКЖЕ ДЛЯ ЛАБОРАТОРНОГО ПОЛУЧЕНИЯ МЕТАНА ИСПОЛЬЗУЮТ ГИДРОЛИЗ КАРБИДА АЛЮМИНИЯ ИЛИ НЕКОТОРЫХ МЕТАЛЛОРГАНИЧЕСКИХ СОЕДИНЕНИЙ (НАПР. , МЕТИЛМАГНИЙБРОМИДА).

ХИМИЧЕСКИЕ СВОЙСТВА ГОРИТ В ВОЗДУХЕ ГОЛУБОВАТЫМ ПЛАМЕНЕМ, ПРИ ЭТОМ ВЫДЕЛЯЕТСЯ ЭНЕРГИЯ ОКОЛО 39 МДЖ НА 1 М³. С ВОЗДУХОМ ОБРАЗУЕТ ВЗРЫВООПАСНЫЕ СМЕСИ ПРИ ОБЪЁМНЫХ КОНЦЕНТРАЦИЯХ ОТ 5 ДО 15 ПРОЦЕНТОВ. ТОЧКА ЗАМЕРЗАНИЯ − 184 С (ПРИ НОРМАЛЬНОМ ДАВЛЕНИИ) ВСТУПАЕТ С ГАЛОГЕНАМИ В РЕАКЦИИ ЗАМЕЩЕНИЯ (НАПРИМЕР, 4 + 3 CL 2= CH CHCL 3+ 3 HCL), КОТОРЫЕ ПРОХОДЯТ ПО СВОБОДНО РАДИКАЛЬНОМУ МЕХАНИЗМУ: CH 4 + CL 2 = CH 3 CL (ХЛОРМЕТАН)+ L HC CH 3 CL + ½ L 2 = CH 2 CL 2 (ДИХЛОРМЕТАН) C CH 2 CL 2 + ½CL 2 = CHCL 3 (ТРИХЛОРМЕТАН) CHCL 3 + ½CL 2 = CCL 4 (ТЕТРАХЛОРМЕТАН) ВЫШЕ 1400 °C РАЗЛАГАЕТСЯ ПО РЕАКЦИИ: 2 CH 4 = C 2 H 2 + 3 H 2 ОКИСЛЯЕТСЯ ДО МУРАВЬИНОЙ КИСЛОТЫ ПРИ 150— 200 °C И ДАВЛЕНИИ 30— 90 АТМ ПО ЦЕПНОМУ РАДИКАЛЬНОМУ МЕХАНИЗМУ: CH 4 + 3[O] = HCOOH + H 2 O

КАДМИЙ

КА ДМИЙ — ЭЛЕМЕНТ ПОБОЧНОЙ ПОДГРУППЫ ВТОРОЙ ГРУППЫ, ПЯТОГО ПЕРИОДА ПЕРИОДИЧЕСКОЙ СИСТЕМЫ ХИМИЧЕСКИХ ЭЛЕМЕНТОВ Д. И. МЕНДЕЛЕЕВА, С АТОМНЫМ НОМЕРОМ 48. ОБОЗНАЧАЕТСЯ СИМВОЛОМ CD (ЛАТ. CADMIUM). ПРОСТОЕ ВЕЩЕСТВО КАДМИЙ (CASНОМЕР: 7440 -43 -9) ПРИ НОРМАЛЬНЫХ УСЛОВИЯХ — МЯГКИЙ КОВКИЙ ТЯГУЧИЙ ПЕРЕХОДНЫЙ МЕТАЛЛ СЕРЕБРИСТО-БЕЛОГО ЦВЕТА. УСТОЙЧИВ В СУХОМ ВОЗДУХЕ, ВО ВЛАЖНОМ НА ЕГО ПОВЕРХНОСТИ ОБРАЗУЕТСЯ ПЛЁНКА ОКСИДА, ПРЕПЯТСТВУЮЩАЯ ДАЛЬНЕЙШЕМУ ОКИСЛЕНИЮ МЕТАЛЛА.

ФИЗИЧЕСКИЕ СВОЙСТВА КАДМИЙ — СЕРЕБРИСТО-БЕЛЫЙ МЯГКИЙ МЕТАЛЛ С ГЕКСАГОНАЛЬНОЙ РЕШЁТКОЙ. ЕСЛИ КАДМИЕВУЮ ПАЛОЧКУ ИЗГИБАТЬ, ТО МОЖНО УСЛЫШАТЬ СЛАБЫЙ ТРЕСК — ЭТО ТРУТСЯ ДРУГ О ДРУГА МИКРОКРИСТАЛЛЫ МЕТАЛЛА (ТАК ЖЕ ТРЕЩИТ И ПРУТОК ОЛОВА). ХИМИЧЕСКИЕ СВОЙСТВА КАДМИЙ РАСПОЛОЖЕН В ОДНОЙ ГРУППЕ ПЕРИОДИЧЕСКОЙ СИСТЕМЫ С ЦИНКОМ И РТУТЬЮ, ЗАНИМАЯ ПРОМЕЖУТОЧНОЕ МЕСТО МЕЖДУ НИМИ, ПОЭТОМУ НЕКОТОРЫЕ ХИМИЧЕСКИЕ СВОЙСТВА ЭТИХ ЭЛЕМЕНТОВ СХОДНЫ. ТАК, СУЛЬФИДЫ И ОКСИДЫ ЭТИХ ЭЛЕМЕНТОВ ПРАКТИЧЕСКИ НЕРАСТВОРИМЫ В ВОДЕ. С УГЛЕРОДОМ КАДМИЙ НЕ ВЗАИМОДЕЙСТВУЕТ И КАРБИДОВ НЕ ОБРАЗУЕТ.

ФИЗИОЛОГИЧЕСКОЕ ДЕЙСТВИЕ СОЕДИНЕНИЯ КАДМИЯ ЯДОВИТЫ. ОСОБЕННО ОПАСНЫМ СЛУЧАЕМ ЯВЛЯЕТСЯ ВДЫХАНИЕ ПАРОВ ЕГО ОКСИДА CDO). ВДЫХАНИЕ В ТЕЧЕНИЕ 1 МИНУТЫ ( ВОЗДУХА С СОДЕРЖАНИЕМ 2, 5 Г/М 3 ОКИСИ КАДМИЯ, ИЛИ 30 СЕКУНД ПРИ КОНЦЕНТРАЦИИ 5 Г/М 3 ЯВЛЯЕТСЯ СМЕРТЕЛЬНЫМ. КАДМИЙ ЯВЛЯЕТСЯ КАНЦЕРОГЕНОМ. В КАЧЕСТВЕ ПЕРВОЙ ПОМОЩИ ПРИ ОСТРОМ КАДМИЕВОМ ОТРАВЛЕНИИ РЕКОМЕНДУЕТСЯ СВЕЖИЙ ВОЗДУХ, ПОЛНЫЙ ПОКОЙ, ПРЕДОТВРАЩЕНИЕ ОХЛАЖДЕНИЯ. ПРИ РАЗДРАЖЕНИИ ДЫХАТЕЛЬНЫХ ПУТЕЙ — ТЁПЛОЕ МОЛОКО С СОДОЙ, ИНГАЛЯЦИИ 2 %-НЫМ РАСТВОРОМ NAHCO 3. ПРИ УПОРНОМ КАШЛЕ — КОДЕИН, ДИОНИН, ГОРЧИЧНИКИ НА ГРУДНУЮ КЛЕТКУ, НЕОБХОДИМА ВРАЧЕБНАЯ ПОМОЩЬ. ПРОТИВОЯДИЕМ ПРИ ОТРАВЛЕНИИ, ВЫЗВАННОМ ПРИЁМОМ ВНУТРЬ КАДМИЕВЫХ СОЛЕЙ, СЛУЖИТ АЛЬБУМИН С КАРБОНАТОМ НАТРИЯ.

ОСТРАЯ ТОКСИЧНОСТЬ ПАРЫ КАДМИЯ, ВСЕ ЕГО СОЕДИНЕНИЯ ТОКСИЧНЫ, ЧТО СВЯЗАНО, В ЧАСТНОСТИ, С ЕГО СПОСОБНОСТЬЮ СВЯЗЫВАТЬ СЕРОСОДЕРЖАЩИЕ ФЕРМЕНТЫ И АМИНОКИСЛОТЫ. СИМПТОМЫ ОСТРОГО ОТРАВЛЕНИЯ СОЛЯМИ КАДМИЯ — РВОТА И СУДОРОГИ. ХРОНИЧЕСКАЯ ТОКСИЧНОСТЬ КАДМИЙ — КУМУЛЯТИВНЫЙ ЯД (СПОСОБЕН НАКАПЛИВАТЬСЯ В ОРГАНИЗМЕ). САНИТАРНО-ЭКОЛОГИЧЕСКИЕ НОРМАТИВЫ В ПИТЬЕВОЙ ВОДЕ ПДК ДЛЯ КАДМИЯ 0, 001 МГ/ДМ³ (САНПИН 2. 1. 4. 1074 -01

МЫШЬЯК

МЫШЬЯ К — ХИМИЧЕСКИЙ ЭЛЕМЕНТ 15 -Й ГРУППЫ (ПО УСТАРЕВШЕЙ КЛАССИФИКАЦИИ — ГЛАВНОЙ ПОДГРУППЫ ПЯТОЙ ГРУППЫ) ЧЕТВЁРТОГО ПЕРИОДА ПЕРИОДИЧЕСКОЙ СИСТЕМЫ; ИМЕЕТ АТОМНЫЙ НОМЕР 33, ОБОЗНАЧАЕТСЯ СИМВОЛОМ AS. ПРОСТОЕ ВЕЩЕСТВО ПРЕДСТАВЛЯЕТ СОБОЙ ХРУПКИЙ ПОЛУМЕТАЛЛ СТАЛЬНОГО ЦВЕТА.

НАХОЖДЕНИЕ В ПРИРОДЕ МЫШЬЯК — РАССЕЯННЫЙ ЭЛЕМЕНТСОДЕРЖАНИЕ В ЗЕМНОЙ КОРЕ. 1, 7· 10− 4% ПО МАССЕ. В МОРСКОЙ ВОДЕ 0, 003 МГ/Л. ЭТО ВЕЩЕСТВО МОЖЕТ ВСТРЕЧАТЬСЯ В САМОРОДНОМ СОСТОЯНИИ, ИМЕЕТ ВИД МЕТАЛЛИЧЕСКИ БЛЕСТЯЩИХ СЕРЫХ СКОРЛУПОК ИЛИ ПЛОТНЫХ МАСС, СОСТОЯЩИХ ИЗ МАЛЕНЬКИХ ЗЕРНЫШЕК. ЗВЕСТНО ОКОЛО 200 И МЫШЬЯКСОДЕРЖАЩИХ МИНЕРАЛОВ. В НЕБОЛЬШИХ КОНЦЕНТРАЦИЯХ ЧАСТО СОДЕРЖИТСЯ В СВИНЦОВЫХ, МЕДНЫХ И СЕРЕБРЯНЫХ РУДАХ. ДОВОЛЬНО ЧАСТО ВСТРЕЧАЮТСЯ ДВА ПРИРОДНЫХ СОЕДИНЕНИЯ МЫШЬЯКА С СЕРОЙ: ОРАНЖЕВО-КРАСНЫЙ ПРОЗРАЧНЫЙ РЕАЛЬГАР SS И ЛИМОННОA ЖЕЛТЫЙ АУРИПИГМЕНТ AS 2 S 3. МИНЕРАЛ, ИМЕЮЩИЙ ПРОМЫШЛЕННОЕ ЗНАЧЕНИЕ — АРСЕНОПИРИТ (МЫШЬЯКОВЫЙ КОЛЧЕДАН) EASS ИЛИ F FES 2 • FEAS 2 (46 % AS), ТАКЖЕ ДОБЫВАЮТ МЫШЬЯКОВИСТЫЙ КОЛЧЕДАН — ЛЁЛЛИНГИТFEAS 2) (72, 8 % AS), СКОРОДИТ FEASO 4 ( (27 — 36 % AS). БОЛЬШАЯ ЧАСТЬ МЫШЬЯКА ДОБЫВАЕТСЯ ПОПУТНО ПРИ ПЕРЕРАБОТКЕ МЫШЬЯКСОДЕРЖАЩИХ ЗОЛОТЫХ, СВИНЦОВО-ЦИНКОВЫХ, МЕДНОКОЛЧЕДАННЫХ И ДРУГИХ РУД.
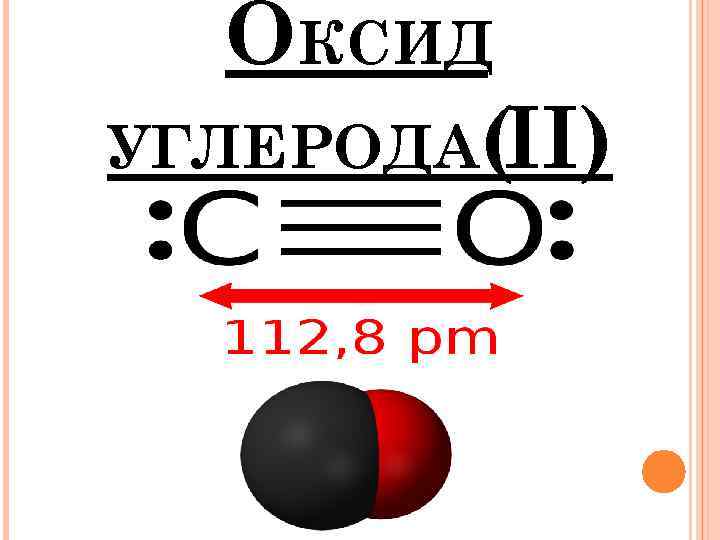
ОКСИД УГЛЕРОДА(II)

ОКСИД УГЛЕРОДА( (УГАРНЫЙ ГАЗ, ОКИСЬ УГЛЕРОДА, МОНООКСИД II) УГЛЕРОДА) — БЕСЦВЕТНЫЙ ЯДОВИТЫЙ ГАЗ (ПРИ НОРМАЛЬНЫХ УСЛОВИЯХ) БЕЗ ВКУСА И ЗАПАХА. ХИМИЧЕСКАЯ ФОРМУЛА — CO. НИЖНИЙ И ВЕРХНИЙ КОНЦЕНТРАЦИОННЫЕ ПРЕДЕЛЫ РАСПРОСТРАНЕНИЯ ПЛАМЕНИ: ОТ 12, 5 ДО 74 % (ПО ОБЪЁМУ) СТРОЕНИЕ МОЛЕКУЛЫ МОЛЕКУЛА CO ИМЕЕТ ТРОЙНУЮ СВЯЗЬ, КАК И МОЛЕКУЛА АЗОТА N 2. ТАК КАК ЭТИ МОЛЕКУЛЫ СХОДНЫ ПО СТРОЕНИЮ (ИЗОЭЛЕКТРОННЫ, ДВУХАТОМНЫ, ИМЕЮТ БЛИЗКУЮ МОЛЯРНУЮ МАССУ), ТО И СВОЙСТВА ИХ ТАКЖЕ СХОЖИ — ОЧЕНЬ НИЗКИЕ ТЕМПЕРАТУРЫ ПЛАВЛЕНИЯ И КИПЕНИЯ, БЛИЗКИЕ ЗНАЧЕНИЯ СТАНДАРТНЫХ ЭНТРОПИЙ И Т. П. В РАМКАХ МЕТОДА ВАЛЕНТНЫХ СВЯЗЕЙ СТРОЕНИЕ МОЛЕКУЛЫ CO МОЖНО ОПИСАТЬ ФОРМУЛОЙ : C=O: . СОГЛАСНО МЕТОДУ МОЛЕКУЛЯРНЫХ ОРБИТАЛЕЙ ЭЛЕКТРОННАЯ КОНФИГУРАЦИЯ НЕВОЗБУЖДЁННОЙ МОЛЕКУЛЫ CO Σ² OΣ²ZΠ 4 X, YΣ²C. ТРОЙНАЯ СВЯЗЬ ОБРАЗОВАНА Σ— СВЯЗЬЮ, ОБРАЗОВАННОЙ ЗА СЧЁТ Z ЭЛЕКТРОННОЙ ПАРЫ, А ЭЛЕКТРОНЫ ДВАЖДЫ Σ ВЫРОЖДЕННОГО УРОВНЯ ΠX, Y СООТВЕТСТВУЮТ ДВУМ Σ—СВЯЗЯМ. ЭЛЕКТРОНЫ НА НЕСВЯЗЫВАЮЩИХ ΣC—ОРБИТАЛИ И ΣO—ОРБИТАЛИ СООТВЕТСТВУЮТ ДВУМ ЭЛЕКТРОННЫМ ПАРАМ, ОДНА ИЗ КОТОРЫХ ЛОКАЛИЗОВАНА У АТОМА УГЛЕРОДА, ДРУГАЯ — У АТОМА КИСЛОРОДА.

СВОЙСТВА Стандартная энергия Гиббса образования ΔG − 137, 14 к. Дж/моль (г) (при 298 К) Стандартная энтропия образования S 197, 54 Дж/моль·K (г) (при 298 К) Стандартная мольная теплоёмкость Cp 29, 11 Дж/моль·K (г) (при 298 К) Энтальпия плавления ΔHпл 0, 838 к. Дж/моль Энтальпия кипения ΔHкип 6, 04 к. Дж/моль Критическая температура tкрит − 140, 23 °C Критическое давление Pкрит 3, 499 МПа Критическая плотность ρкрит 0, 301 г/см³

ГЕКСАМИН

ГЕКСАМЕТИЛЕНТЕТРАМИН ((CH 2)6 N 4, ИЛИ C 6 H 12 N 4), (УРОТРОПИН, ГЕКСАМИН, АНГЛ. : METHENAMINE (INN), 1, 3, 5, 7 -TETRAAZAADAMANTANE, HEXAMETHYLENETETRAMINE ИЛИ HEXAMETYLENETETRAMINE). ПРИМЕНЯЕТСЯ В МЕДИЦИНЕ ПОД МЕЖДУНАРОДНЫМ НЕПАТЕНТОВАННЫМ НАИМЕНОВАНИЕМ (МНН) МЕТЕНАМИН.

ПОЛУЧЕНИЕ И СВОЙСТВА ВПЕРВЫЕ ПОЛУЧЕН РУССКИМ ХИМИКОМА. М. БУТЛЕРОВЫМ В 1859 ГОДУ. ОБРАЗУЕТСЯ ПРИ ВЗАИМОДЕЙСТВИИ АММИАКА 4 МОЛЬ ) С ФОРМАЛЬДЕГИДОМ ( (6 МОЛЬ ). БЕЛОЕ КРИСТАЛЛИЧЕСКОЕ ВЕЩЕСТВО, СУБЛИМИРУЕТСЯ ПРИ 270 °C. ЛЕГКО РАСТВОРИМ В ВОДЕ, СПИРТЕ, РАСТВОРИМ В ХЛОРОФОРМЕ, МАЛО РАСТВОРИМ В ЭФИРЕ. ТЕПЛОТА СГОРАНИЯ 30, 045 МДЖ/КГ СТРУКТУРНО ПОДОБЕН АДАМАНТАНУ. КРУПНЕЙШИМ ПРОИЗВОДИТЕЛЕМ УРОТРОПИНА ВРОССИИ ЯВЛЯЕТСЯ ГУБАХИНСКИЙ ОАО «МЕТАФРАКС» .

КЛЕЙ
Клей — вещество или смесь, а также многокомпонентные композиции на основе органических или неорганических веществ, способные соединять (склеивать) различные материалы — в частности, древесину, кожу, бумагу, ткани, стекло, керамику, металлы, пластмассы, резину. Склеивание обусловлено образованием прочной адгезионной связи между прослойкой клея и материалами соединяемых поверхностей. На прочность клеевого шва влияет и когезия клея к поверхности.

КЛАССИФИКАЦИЯ ПО СОСТАВУ - неорганические (растворы, расплавы, а также припои, в частности — полимерные композиции типа «клей-припой» ) - органические (растворы, расплавы, полимеризующиеся) Основой органического клея служат главным образом синтетическое олигомеры и полимеры (например, фенолоформальдегидные, эпоксидные, полиэфирные смолы, полиамиды, полиимиды, полиуретаны, кремнийорганические полимеры, каучуки и др. ) образующие клеевую пленку в результате затвердевания при охлаждении (термопластичные клеи), отверждения (термореактивные клеи) или вулканизации (резиновые клеи); этим процессам иногда предшествует улетучивание растворителя. К неорганическим клеям относят алюмофосфатные, керамические (основа — оксиды магния, алюминия, кремния, щелочных металлов), силикатные (основа — калиевое или натриевое жидкое стекло), металлические (основа — жидкий металл, например ртуть). По физическому состоянию клеи могут быть жидкими (растворы, эмульсии, суспензии) или твёрдыми (пленки, прутки, гранулы, порошки); последние используются в виде расплава или наносят на нагретые поверхности.
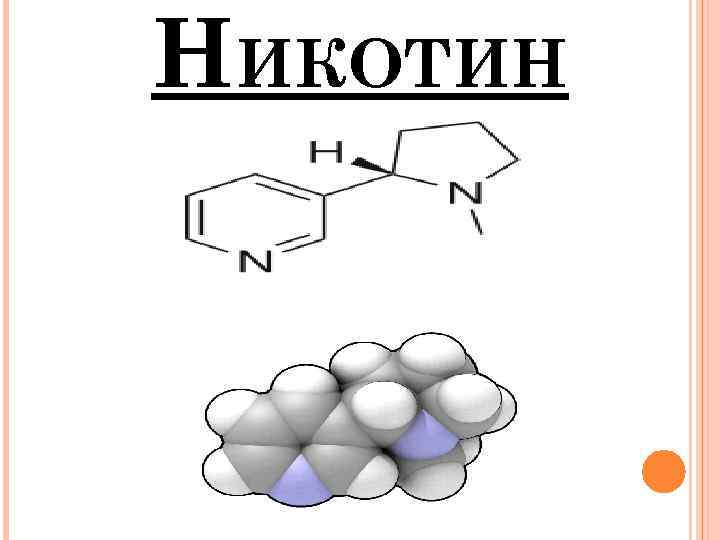
НИКОТИН

НИКОТИ Н — АЛКАЛОИД, СОДЕРЖАЩИЙСЯ В РАСТЕНИЯХ СЕМЕЙСТВА (SOLANACEAE), ПРЕИМУЩЕСТВЕННО В ТАБАКЕ И, В МЕНЬШИХ КОЛИЧЕСТВАХ, В ТОМАТАХ, КАРТОФЕЛЕ, БАКЛАЖАНАХ, ЗЕЛЁНОМ ПЕРЦЕ. НИКОТИНОВЫЕ АЛКАЛОИДЫ ТАКЖЕ ПРИСУТСТВУЮТ В ЛИСТЬЯХ КОКИ. НИКОТИН СОСТАВЛЯЕТ ОТ 0, 3 ДО 5 % ОТ МАССЫ ТАБАКА В СУХОМ ВИДЕ, БИОСИНТЕЗ НИКОТИНА ПРОИСХОДИТ В КОРНЯХ, НАКАПЛИВАНИЕ НИКОТИНА — В ЛИСТЬЯХ. ИКОТИН — Н СИЛЬНОДЕЙСТВУЮЩИЙ НЕЙРОТОКСИН И КАРДИОТОКСИН, ОСОБЕННО ДЕЙСТВУЮЩИЙ НА НАСЕКОМЫХ; ВСЛЕДСТВИЕ ЭТОГО НИКОТИН РАНЬШЕ ШИРОКО ИСПОЛЬЗОВАЛСЯ КАК ИНСЕКТИЦИД, А В НАСТОЯЩЕЕ ВРЕМЯ В ПАСЛЁНОВЫХ ТОМ ЖЕ КАЧЕСТВЕ ПРОДОЛЖАЮТ ИСПОЛЬЗОВАТЬСЯ ПРОИЗВОДНЫЕ НИКОТИНА — ТАКИЕ, КАК, НАПРИМЕР, ИМИДАКЛОПРИД.

НИКОТИН — ГИГРОСКОПИЧЕСКАЯ МАСЛЯНИСТАЯ ЖИДКОСТЬ С НЕПРИЯТНЫМ ЗАПАХОМ И ЖГУЧИМ ВКУСОМ, ЛЕГКО СМЕШИВАЮЩАЯСЯ С ВОДОЙ В ОСНОВНОЙ ФОРМЕ. КАК АМИН, НИКОТИН ОБРАЗУЕТ СОЛИ С КИСЛОТАМИ, КОТОРЫЕ ОБЫЧНО ТВЁРДЫЕ И ВОДОРАСТВОРИМЫЕ. ИКОТИН ЛЕГКО ПРОНИКАЕТ ЧЕРЕЗ Н КОЖУ. ОСНОВНОЙ НИКОТИН СГОРАЕТ ПРИ ТЕМПЕРАТУРЕ НИЖЕ ТОЧКИ КИПЕНИЯ, А ЕГО ПАРЫ ВОСПЛАМЕНЯЮТСЯ ПРИ 95 °C В ВОЗДУХЕ, НЕСМОТРЯ НА НИЗКОЕ ДАВЛЕНИЕ ПАРА. О ЭТОЙ ПРИЧИНЕ БО ЬШАЯ ЧАСТЬ НИКОТИНА П Л СГОРАЕТ ПРИ ВЫКУРИВАНИИ СИГАРЕТЫ, ОДНАКО, ВДЫХАЕМОЙ ЧАСТИ ДОСТАТОЧНО ДЛЯ ПОЛУЧЕНИЯ ТРЕБУЕМЫХ ЭФФЕКТОВ. НИКОТИН ЛЕГКО ОКИСЛЯЕТСЯ ДО НЕТОКСИЧНОЙ НИКОТИНОВОЙ КИСЛОТЫ (ВИТАМИН PP). ОДНАКО В ОРГАНИЗМЕ ЧЕЛОВЕКА ОТСУТСТВУЮТ ФЕРМЕНТЫ, НЕОБХОДИМЫЕ ДЛЯ ТАКОГО ОКИСЛЕНИЯ. ОЭТОМУ ДАЖЕ ХРОНИЧЕСКИЕ П КУРИЛЬЩИКИ МОГУТ СТРАДАТЬ ОТ НЕДОСТАТКА ЭТОГО ВИТАМИНА.
АММОНИЙ

АММО НИЙ (ЛАТ. AMMONIUM) — КОМПЛЕКСНЫЙ НЕОРГАНИЧЕСКИЙ КАТИОН, В СОЕДИНЕНИЯХ ИГРАЕТ РОЛЬ ОДНОВАЛЕНТНОГО МЕТАЛЛА. ХИМИЧЕСКАЯ ФОРМУЛА — 4+. ПРИ РАСТВОРЕНИИ АММИАКА В NH РАСТВОРАХ КИСЛОТ ПРОИСХОДИТ РЕАКЦИЯ: NH 3 + H+ = NH 4+ ИОН АММОНИЯ ЯВЛЯЕТСЯ ПРАВИЛЬНЫМ ТЕТРАЭДРОМ С АЗОТОМ В ЦЕНТРЕ И АТОМАМИ ВОДОРОДА В ВЕРШИНАХ ТЕТРАЭДРА. РАЗМЕР ИОНА — 1, 43 Å. СУЩЕСТВУЕТ ТАКЖЕ КОРОТКОЖИВУЩИЙ СВОБОДНЫЙ РАДИКАЛ АММОНИЯ С ФОРМУЛОЙ NH 4. ДИССОЦИАЦИЯ СОЛЕЙ АММОНИЯ ПРИ ДИССОЦИАЦИИ СОЕДИНЕНИЙ АММОНИЯ В ВОДНЫХ РАСТВОРАХ АММОНИЙ ПРИСУТСТВУЕТ В ВИДЕ КАТИОНА, НАПРИМЕР: NH 4 CI = NH 4+ + CL−.


СВОЙСТВА СОЛЕЙ АММОНИЯ БОЛЬШИНСТВО СОЛЕЙ ИОНА АММОНИЯ — БЕСЦВЕТНЫЕ КРИСТАЛЛИЧЕСКИЕ ВЕЩЕСТВА, ХОРОШО РАСТВОРИМЫЕ В ВОДЕ И ЛЕГКО РАЗЛАГАЮЩИЕСЯ ПРИ НАГРЕВАНИИ С ВЫДЕЛЕНИЕМ ГАЗОВ. ПРОЧНОСТЬ СОЛЕЙ АММОНИЯ СИЛЬНО РАЗЛИЧАЕТСЯ. СЛИ ЗАПИСАТЬ РЕАКЦИЮ Е АММИАКА С КИСЛОТАМИ СЛЕДУЮЩИМ ОБРАЗОМ: NH 3 + Н+X− → [NH 4]+X−, ТО ЧЕМ СИЛЬНЕЕ КИСЛОТНЫЙ ОСТАТОК Х− УДЕРЖИВАЕТ КАТИОН Н+, ТЕМ ТРУДНЕЕ ПРОИСХОДИТ ПРЯМОЙ ПРОЦЕСС И ЛЕГЧЕ — ОБРАТНЫЙ. ПОЭТОМУ, ЧЕМ МЕНЬШЕ КОНСТАНТА ДИССОЦИАЦИИ КИСЛОТЫ, ТЕМ МЕНЕЕ УСТОЙЧИВА ЕЁ АММОНИЙНАЯ СОЛЬ. АК, СОЛЬ СИЛЬНОЙ КИСЛОТЫ Т HCL ХЛОРИД АММОНИЯ NH 4 CL ВПОЛНЕ СТАБИЛЕН ПРИ КОМНАТНОЙ ТЕМПЕРАТУРЕ, А СОЛЬ СЛАБОЙ УГОЛЬНОЙ КИСЛОТЫ В ЭТИХ УСЛОВИЯХ ЗАМЕТНО РАЗЛАГАЕТСЯ. АММОНИЕВЫЕ СОЛИ ЛЕТУЧИХ КИСЛОТ ПРИ НАГРЕВАНИИ РАЗЛАГАЮТСЯ, ВЫДЕЛЯЯ ГАЗООБРАЗНЫЕ ПРОДУКТЫ, КОТОРЫЕ ПРИ ОХЛАЖДЕНИИ ВНОВЬ ОБРАЗУЮТ СОЛЬ: NH 4 CL →NH 3 + HCL ЕСЛИ СОЛЬ ОБРАЗОВАНА НЕЛЕТУЧЕЙ КИСЛОТОЙ, ТО НАГРЕВАНИЕМ МОЖНО УДАЛИТЬ NH 3: NH 4 H 2 PO 4 → Н 3 PO 4 + NH 3 ЕСЛИ АНИОН СОЛИ АММОНИЯ СОДЕРЖИТ АТОМОКИСЛИТЕЛЬ, ТО ПРИ ЕЁ НАГРЕВАНИИ ПРОИСХОДИТ РЕАКЦИЯ ВНУТРИМОЛЕКУЛЯРНОГО ОКИСЛЕНИЯ-ВОССТАНОВЛЕНИЯ, НАПРИМЕР: (NH 4)2 CR 2 O 7 → N 2 + CR 2 O 3 + 4 H 2 O NH 4 NO 3 → N 2 O + 2 H 2 O

РЕАКЦИЯ ДЛЯ ОБНАРУЖЕНИЯ АММОНИЯ — ВЫДЕЛЕНИЕ АММИАКА ПРИ ДЕЙСТВИИ ЕДКИХ ЩЕЛОЧЕЙ НА СОЛИ АММОНИЯ: NH 4 CI + NAOH = NH 3 + H 2 O + NACI ШИРОКО ИСПОЛЬЗУЕТСЯ ДЛЯ СПЕКТРОФОТОМЕТРИЧЕСКОГО КОЛИЧЕСТВЕННОГО АНАЛИЗА ТАКЖЕ РЕАКЦИЯ С РЕАКТИВОМ ЕССЛЕРА. Н
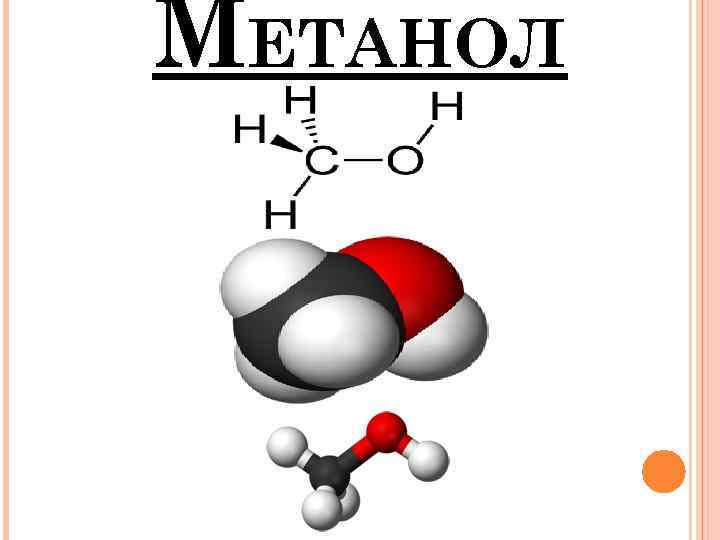
МЕТАНОЛ
Метано л (метиловый спирт, древесный спирт, карбинол, метилгидрат, гидроксид метила) — CH 3 OH, простейший одноатомный спирт, бесцветная ядовитая жидкость. Метанол — это первый представитель гомологического ряда одноатомных спиртов. С воздухом в объёмных концентрациях 6, 72 — 36, 5% образует взрывоопасные смеси (температура вспышки 15, 6 °C). Метанол смешивается в любых соотношениях с водой и большинством органических растворителей.

ПОЛУЧЕНИЕ ДО 1960 -Х ГОДОВ МЕТАНОЛ СИНТЕЗИРОВАЛИ ТОЛЬКО НА ЦИНКХРОМОВОМ КАТАЛИЗАТОРЕ ПРИ ТЕМПЕРАТУРЕ 300— 400 ° ДАВЛЕНИИ 25— 40 МПА (= 250 CИ — 400 БАР = 254, 9— 407, 9 КГСВПОСЛЕДСТВИИ РАСПРОСТРАНЕНИЕ ПОЛУЧИЛ /СМ²). СИНТЕЗ МЕТАНОЛА НА МЕДЬСОДЕРЖАЩИХ КАТАЛИЗАТОРАХ (МЕДЬЦИНКАЛЮМОХРОМОВОМ, МЕДЬ-ЦИНКАЛЮМИНИЕВОМ ИЛИ ДР. ) ПРИ 200— 300 °C И ДАВЛЕНИИ 4— 15 МПА (= 40— 150 = 40, 79— 153 КГС/СМ²). БАР СОВРЕМЕННЫЙ ПРОМЫШЛЕННЫЙ МЕТОД ПОЛУЧЕНИЯ — КАТАЛИТИЧЕСКИЙ СИНТЕЗ ИЗ ОКСИДА УГЛЕРОДА( I) (CO) И ВОДОРОДА ( 2 H 2) ПРИ СЛЕДУЮЩИХ УСЛОВИЯХ: I ТЕМПЕРАТУРА — 250 ° C, ДАВЛЕНИЕ — МПА (= 70 АР = 71, 38 КГС/СМ²), 7 Б КАТАЛИЗАТОР — СМЕСЬ NO (ОКСИД ЦИНКА) И CUO (ОКСИД МЕДИ(II)): Z ДО ПРОМЫШЛЕННОГО ОСВОЕНИЯ КАТАЛИТИЧЕСКОГО СПОСОБА ПОЛУЧЕНИЯ МЕТАНОЛ ПОЛУЧАЛИ ПРИ СУХОЙ ПЕРЕГОНКЕ ДЕРЕВА (ОТСЮДА ЕГО НАЗВАНИЕ «ДРЕВЕСНЫЙ СПИРТ» ). В ДАННОЕ ВРЕМЯ ЭТОТ СПОСОБ ИМЕЕТ ВТОРОСТЕПЕННОЕ ЗНАЧЕНИЕ. ТАКЖЕ ИЗВЕСТНЫ СХЕМЫ ИСПОЛЬЗОВАНИЯ С ЭТОЙ ЦЕЛЬЮ ОТХОДОВ НЕФТЕПЕРЕРАБОТКИ, КОКСУЮЩИХСЯ УГЛЕЙ. CO 2 + 3 H 2 <--> CH 3 OH + H 2 O + 49. 53 К ДЖ/МОЛЬ H 2 O + CO <--> CO 2 + H 2 + 41. 2 К ДЖ/МОЛЬ
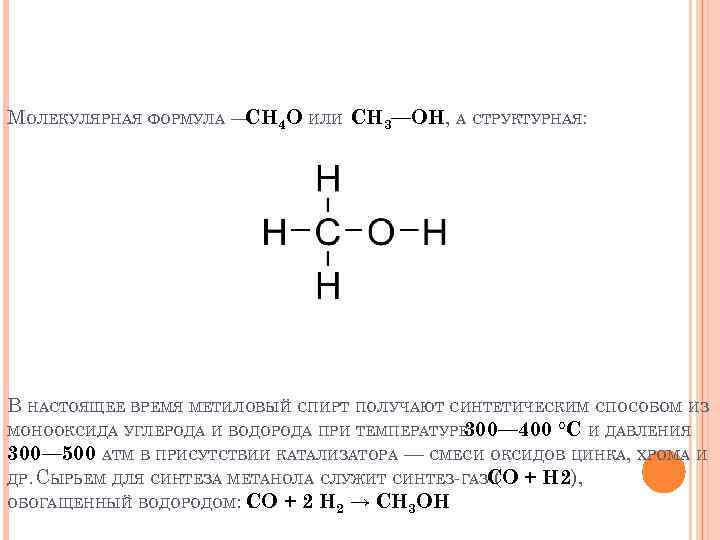
МОЛЕКУЛЯРНАЯ ФОРМУЛА — 4 O ИЛИ CH 3—OH, А СТРУКТУРНАЯ: CH В НАСТОЯЩЕЕ ВРЕМЯ МЕТИЛОВЫЙ СПИРТ ПОЛУЧАЮТ СИНТЕТИЧЕСКИМ СПОСОБОМ ИЗ МОНООКСИДА УГЛЕРОДА И ВОДОРОДА ПРИ ТЕМПЕРАТУРЕ 300— 400 °C И ДАВЛЕНИЯ 300— 500 АТМ В ПРИСУТСТВИИ КАТАЛИЗАТОРА — СМЕСИ ОКСИДОВ ЦИНКА, ХРОМА И ДР. СЫРЬЕМ ДЛЯ СИНТЕЗА МЕТАНОЛА СЛУЖИТ СИНТЕЗ-ГАЗCO + H 2), ( ОБОГАЩЕННЫЙ ВОДОРОДОМ: : O + 2 H 2 → CH 3 OH C
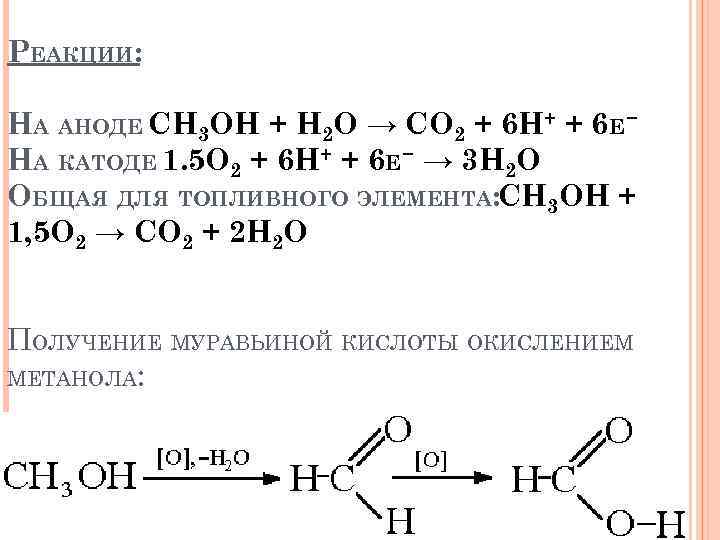
РЕАКЦИИ: НА АНОДЕ CH 3 OH + H 2 O → CO 2 + 6 H+ + 6 E − НА КАТОДЕ 1. 5 O 2 + 6 H+ + 6 E − → 3 H 2 O ОБЩАЯ ДЛЯ ТОПЛИВНОГО ЭЛЕМЕНТА: CH 3 OH + 1, 5 O 2 → CO 2 + 2 H 2 O ПОЛУЧЕНИЕ МУРАВЬИНОЙ КИСЛОТЫ ОКИСЛЕНИЕМ МЕТАНОЛА:
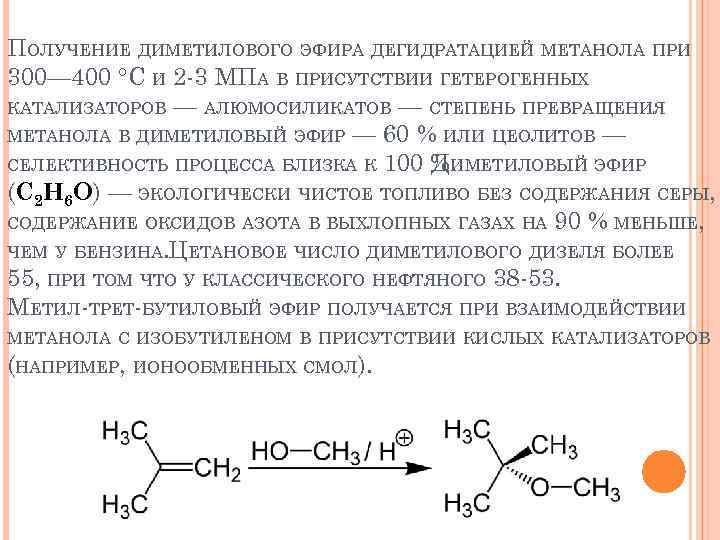
ПОЛУЧЕНИЕ ДИМЕТИЛОВОГО ЭФИРА ДЕГИДРАТАЦИЕЙ МЕТАНОЛА ПРИ 300— 400 °C И 2 -3 МПА В ПРИСУТСТВИИ ГЕТЕРОГЕННЫХ КАТАЛИЗАТОРОВ — АЛЮМОСИЛИКАТОВ — СТЕПЕНЬ ПРЕВРАЩЕНИЯ МЕТАНОЛА В ДИМЕТИЛОВЫЙ ЭФИР — 60 % ИЛИ ЦЕОЛИТОВ — СЕЛЕКТИВНОСТЬ ПРОЦЕССА БЛИЗКА К 100 %. ДИМЕТИЛОВЫЙ ЭФИР (C 2 H 6 O) — ЭКОЛОГИЧЕСКИ ЧИСТОЕ ТОПЛИВО БЕЗ СОДЕРЖАНИЯ СЕРЫ, СОДЕРЖАНИЕ ОКСИДОВ АЗОТА В ВЫХЛОПНЫХ ГАЗАХ НА 90 % МЕНЬШЕ, ЧЕМ У БЕНЗИНА. ЦЕТАНОВОЕ ЧИСЛО ДИМЕТИЛОВОГО ДИЗЕЛЯ БОЛЕЕ 55, ПРИ ТОМ ЧТО У КЛАССИЧЕСКОГО НЕФТЯНОГО 38 -53. МЕТИЛ-ТРЕТ-БУТИЛОВЫЙ ЭФИР ПОЛУЧАЕТСЯ ПРИ ВЗАИМОДЕЙСТВИИ МЕТАНОЛА С ИЗОБУТИЛЕНОМ В ПРИСУТСТВИИ КИСЛЫХ КАТАЛИЗАТОРОВ (НАПРИМЕР, ИОНООБМЕННЫХ СМОЛ).

КРАСКА

КРА СКИ — ОБЩЕЕ НАИМЕНОВАНИЕ ДЛЯ ГРУППЫ ЦВЕТНЫХ КРАСЯЩИХ ВЕЩЕСТВ, ПРЕДНАЗНАЧЕННЫХ ДЛЯ НЕПОСРЕДСТВЕННОГО ИСПОЛЬЗОВАНИЯ В ТОЙ ИЛИ ИНОЙ СФЕРЕ БЫТА. О ХИМИЧЕСКОМУ СОСТАВУ П ПИГМЕНТЫ И ИЗГОТОВЛЕННЫЕ ИЗ НИХ КРАСКИ РАЗДЕЛЯЮТСЯ НА МИНЕРАЛЬНЫЕ (НЕОРГАНИЧЕСКИЕ СОЛИ ИЛИ ОКСИДЫ МЕТАЛЛОВ) И ОРГАНИЧЕСКИЕ (СЛОЖНЫЕ СОЕДИНЕНИЯ, В ОСНОВНОМ РАСТИТЕЛЬНОГО ИЛИ ЖИВОТНОГО ПРОИСХОЖДЕНИЯ). И ТЕ И ДРУГИЕ МОГУТ БЫТЬ ЕСТЕСТВЕННЫМИ (ПРИРОДНЫМИ) И ИСКУССТВЕННЫМИ (СИНТЕТИЧЕСКИМИ). КРАСКИ ЧАЩЕ ВСЕГО ПОД СЛОВОМ «КРАСКИ» ПОДРАЗУМЕВАЮТ СУСПЕНЗИИ ПИГМЕНТОВ ИЛИ ИХ СМЕСИ С НАПОЛНИТЕЛЯМИ, В СВЯЗУЮЩЕМ — ОЛИФЕ, ПВА-ЭМУЛЬСИИ, ЛАТЕКСАХ ИЛИ ДРУГИХ ПЛЕНКООБРАЗУЮЩИХ ВЕЩЕСТВАХ. КРАСКИ НАНОСЯТ НЕПОСРЕДСТВЕННО НА ИМЕЮЩИЙСЯ МАТЕРИАЛ ИЛИ НА ГРУНТ (ЖИВОПИСЬ).


2011 -2012 Г.
химия. сигареты.pptx