Копия Презентация на тему соли.ppt
- Количество слайдов: 18
 Презентация по химии на тему: «Соли и их свойства» .
Презентация по химии на тему: «Соли и их свойства» .
 Определение l l l Соли - сложные вещества, при диссоциации (разложении) которых в одном растворе образуются катионы металлов и анионы кислотных остатков. Анионы - отрицательные электроны. Катионы - положительные электроны.
Определение l l l Соли - сложные вещества, при диссоциации (разложении) которых в одном растворе образуются катионы металлов и анионы кислотных остатков. Анионы - отрицательные электроны. Катионы - положительные электроны.
 Соли делят на: средние; l кислые; l основные. l
Соли делят на: средние; l кислые; l основные. l
 Средние соли При диссоциации средние соли дают только катионы металла (или NH+) и анионы 4 кислотного остатка. 2+ Mg. SO 4 Mg +SO 24 Средние соли – продукт полного замещения атомов водорода кислот на атомы металла.
Средние соли При диссоциации средние соли дают только катионы металла (или NH+) и анионы 4 кислотного остатка. 2+ Mg. SO 4 Mg +SO 24 Средние соли – продукт полного замещения атомов водорода кислот на атомы металла.
 Получение средних солей: l Реакции кислот с металлами , основными или амфотерными оксидами и основаниями. Mg+HSO=Mg. SO+H 2 4 2 l 4 Реакции оснований с кислотными и амфотерными оксидами. 2 2 KOH+SO=K 2 SO+H 2 O 2 3
Получение средних солей: l Реакции кислот с металлами , основными или амфотерными оксидами и основаниями. Mg+HSO=Mg. SO+H 2 4 2 l 4 Реакции оснований с кислотными и амфотерными оксидами. 2 2 KOH+SO=K 2 SO+H 2 O 2 3
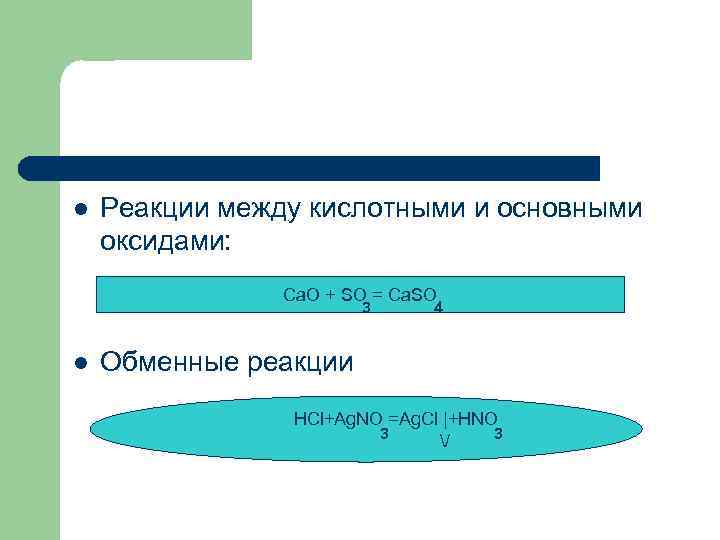 l Реакции между кислотными и основными оксидами: Ca. O + SO = Ca. SO 3 l 4 Обменные реакции HCl+Ag. NO =Ag. Cl |+HNO 3 3 /
l Реакции между кислотными и основными оксидами: Ca. O + SO = Ca. SO 3 l 4 Обменные реакции HCl+Ag. NO =Ag. Cl |+HNO 3 3 /
 Химические свойства l Термическое разложение: l 3 Сa. CO=Ca. O+CO 2 Гидролиз (взаимодействие ионов соли с водой с образованием малодиссоциирующих частиц): KS+H 2 O KHS+KOH 2 2
Химические свойства l Термическое разложение: l 3 Сa. CO=Ca. O+CO 2 Гидролиз (взаимодействие ионов соли с водой с образованием малодиссоциирующих частиц): KS+H 2 O KHS+KOH 2 2
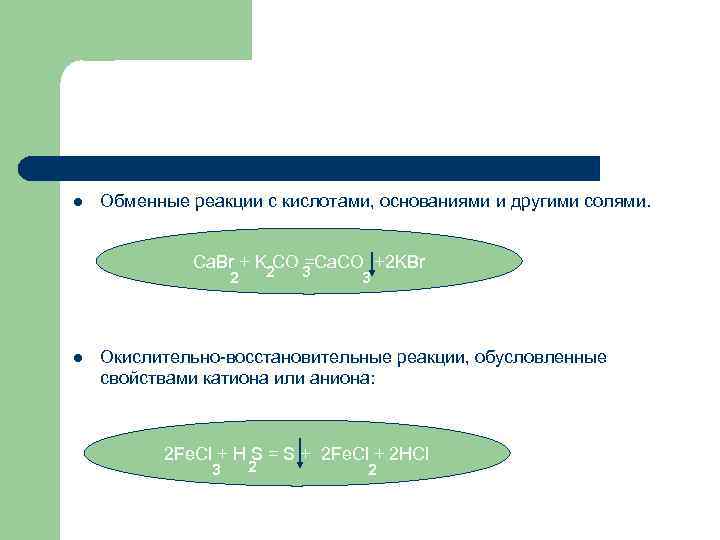 l Обменные реакции с кислотами, основаниями и другими солями. Сa. Br + K CO =Ca. CO +2 KBr 2 2 l 3 3 Окислительно-восстановительные реакции, обусловленные свойствами катиона или аниона: 2 Fe. Cl + H S = S + 2 Fe. Cl + 2 HCl 3 2 2
l Обменные реакции с кислотами, основаниями и другими солями. Сa. Br + K CO =Ca. CO +2 KBr 2 2 l 3 3 Окислительно-восстановительные реакции, обусловленные свойствами катиона или аниона: 2 Fe. Cl + H S = S + 2 Fe. Cl + 2 HCl 3 2 2
 Кислые соли при диссоциации дают катионы + металла (или NH 4 ), ионы водородов и 4 2 анионы кислотного остатка: 2 Na. HCO 3 Na+ + HCO + 3 - + Na + H + CO 23
Кислые соли при диссоциации дают катионы + металла (или NH 4 ), ионы водородов и 4 2 анионы кислотного остатка: 2 Na. HCO 3 Na+ + HCO + 3 - + Na + H + CO 23
 Кислые соли – продукт неполного замещения атомов водорода соответствующей кислоты на атомы металла.
Кислые соли – продукт неполного замещения атомов водорода соответствующей кислоты на атомы металла.
 Получение кислых солей: l кислота + основание (недостаток)= кислая соль: Na. ON + H SO = Na. HSO + H O. 2 l 4 4 2 2 2 4 основание + кислотный оксид (избыток)= кислая соль: Сa(OH) + 2 CO = Ca(HCO ). 2 l 2 3 2 2 средняя соль + кислота = кислая соль: 2 3 PO Сa(PO) 2+4 H PO = 3 Ca(H 2 )). . Сa(PO)+ 4 HPO 3 Ca(HPO 33 422 3 4 2 42 2
Получение кислых солей: l кислота + основание (недостаток)= кислая соль: Na. ON + H SO = Na. HSO + H O. 2 l 4 4 2 2 2 4 основание + кислотный оксид (избыток)= кислая соль: Сa(OH) + 2 CO = Ca(HCO ). 2 l 2 3 2 2 средняя соль + кислота = кислая соль: 2 3 PO Сa(PO) 2+4 H PO = 3 Ca(H 2 )). . Сa(PO)+ 4 HPO 3 Ca(HPO 33 422 3 4 2 42 2
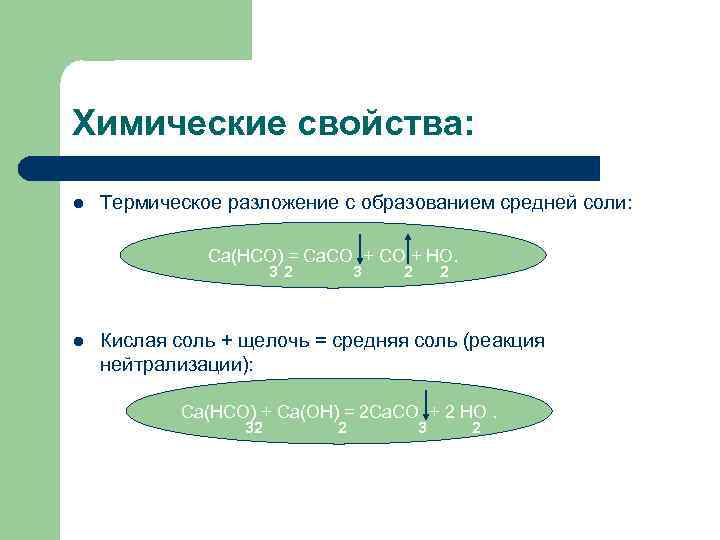 Химические свойства: l Термическое разложение с образованием средней соли: Ca(HCO) = Ca. CO + HO. 32 l 3 2 2 Кислая соль + щелочь = средняя соль (реакция нейтрализации): Сa(HCO) + Ca(OH) = 2 Ca. CO + 2 HO. 32 2 3 2
Химические свойства: l Термическое разложение с образованием средней соли: Ca(HCO) = Ca. CO + HO. 32 l 3 2 2 Кислая соль + щелочь = средняя соль (реакция нейтрализации): Сa(HCO) + Ca(OH) = 2 Ca. CO + 2 HO. 32 2 3 2
 Основные соли: l Основные соли при диссоциации дают катионы металла, анионы кислотного остатка и ионы OH - : 2 - Fe(OH)Cl l + Fe(OH) + Cl - Fe 2+ OH- + Cl -. + Основные соли – продукт неполного замещения групп ОН соответствующего основания на кислотные остатки.
Основные соли: l Основные соли при диссоциации дают катионы металла, анионы кислотного остатка и ионы OH - : 2 - Fe(OH)Cl l + Fe(OH) + Cl - Fe 2+ OH- + Cl -. + Основные соли – продукт неполного замещения групп ОН соответствующего основания на кислотные остатки.
 Получение основных солей: l Осторожное добавление небольших количеств щелочей к растворам средних солей металлов: Al. Cl + 2 Na. OH = Al(OH) Cl + 2 Na. Cl. 2 3 l Действие солей слабых кислот на средние соли: 2 Mg. Cl + 2 Na CO + H O = [Mg(OH)] CO + 2 Na. Cl. 2 2 3 2
Получение основных солей: l Осторожное добавление небольших количеств щелочей к растворам средних солей металлов: Al. Cl + 2 Na. OH = Al(OH) Cl + 2 Na. Cl. 2 3 l Действие солей слабых кислот на средние соли: 2 Mg. Cl + 2 Na CO + H O = [Mg(OH)] CO + 2 Na. Cl. 2 2 3 2
![Химические свойства: l Термическое разложение: [Cu(OH)] CO = 2 Cu. O + CO + Химические свойства: l Термическое разложение: [Cu(OH)] CO = 2 Cu. O + CO +](https://present5.com/presentation/164339003_94605630/image-15.jpg) Химические свойства: l Термическое разложение: [Cu(OH)] CO = 2 Cu. O + CO + H O. 2 l 3 2 2 Основная соль + кислота = средняя соль (реакция нейтрализации): Fe(OH)Cl + HCl Fe. Cl + H O. 2 2
Химические свойства: l Термическое разложение: [Cu(OH)] CO = 2 Cu. O + CO + H O. 2 l 3 2 2 Основная соль + кислота = средняя соль (реакция нейтрализации): Fe(OH)Cl + HCl Fe. Cl + H O. 2 2
 Двойные соли образованы двумя катионами и одним анионом: KAl(SO ) 42 K+ + Al 3+ 2 SO 2 -. + 4 Смешанные соли образованы одним катионами и двумя анионами: Ca. OCl 2 2+ - - Ca + Cl + OCl.
Двойные соли образованы двумя катионами и одним анионом: KAl(SO ) 42 K+ + Al 3+ 2 SO 2 -. + 4 Смешанные соли образованы одним катионами и двумя анионами: Ca. OCl 2 2+ - - Ca + Cl + OCl.
 Физические свойства l Соли представляют собой твердые вещества , часто характеризующиеся высокими температурами плвления.
Физические свойства l Соли представляют собой твердые вещества , часто характеризующиеся высокими температурами плвления.
 По растворимости в воде соли делят на : l l l 1)Легкорастворимые (Na. CL, KCL, Ca. CL 2); 2 2)Труднорастворимые 2 (Pb. Cl 2, Ca. SO 4 , Ag. SO 4 ); 3)Практически нерастворимые (Ba. SO 4 , Pb. SO 3 , Ca. CO ); 3
По растворимости в воде соли делят на : l l l 1)Легкорастворимые (Na. CL, KCL, Ca. CL 2); 2 2)Труднорастворимые 2 (Pb. Cl 2, Ca. SO 4 , Ag. SO 4 ); 3)Практически нерастворимые (Ba. SO 4 , Pb. SO 3 , Ca. CO ); 3


