Рафинирование металла при дуговой сварке.ppt
- Количество слайдов: 15
 Презентация по предмету «Теория сварочных процессов» на тему: Рафинирование металла при дуговой сварке Волгодонск 2013
Презентация по предмету «Теория сварочных процессов» на тему: Рафинирование металла при дуговой сварке Волгодонск 2013
 Содержание 1. Рафинирование сварочной ванны 2. Влияние серы на структуру и свойства шва 3. Механизм влияния примесей серы 4. Десульфурация сварочной ванны 5. Снижение содержания фосфора в металле шва 2
Содержание 1. Рафинирование сварочной ванны 2. Влияние серы на структуру и свойства шва 3. Механизм влияния примесей серы 4. Десульфурация сварочной ванны 5. Снижение содержания фосфора в металле шва 2
 Рафинирование сварочной ванны Важная металлургическая операция, протекающая в сварочной ванне одновременно с раскислением и легированием металла, - его рафинирование, т. е. очищение от вредных примесей - серы и фосфора. Полное удаление этих примесей при плавке и сварке стали невозможно. Однако для рафинирования металла шва по содержанию серы условия сварочного процесса в общем более благоприятны, чем в сталеплавильном производстве. Наиболее существенными из них являются следующие: 1) более высокая температура металла и шлака, особенно на стадии образования капель (Тк = 3000 К), что способствует диссоциации сернистых и фосфорных соединений, ослабляет их химические связи и тем самым облегчает удаление серы и фосфора из металла шва в шлак; 2) интенсивное перемешивание металла со шлаком в кипящих каплях и в сварочной ванне увеличивает относительную массу шлака в 100 -1000 раз по сравнению с относительной массой шлака при плавке стали; 3) использование специальных рафинирующих компонентов: кальция Са, церия Се, лантана La, иттрия I и других в электродных покрытиях или сварочных флюсах позволяет провести удаление или связывание вредных примесей. Таким образом, несмотря на кратковременность взаимодействия металла со шлаком, при сварке плавлением есть возможность получать металл шва с меньшим содержанием серы и фосфора, чем в основном металле. 3
Рафинирование сварочной ванны Важная металлургическая операция, протекающая в сварочной ванне одновременно с раскислением и легированием металла, - его рафинирование, т. е. очищение от вредных примесей - серы и фосфора. Полное удаление этих примесей при плавке и сварке стали невозможно. Однако для рафинирования металла шва по содержанию серы условия сварочного процесса в общем более благоприятны, чем в сталеплавильном производстве. Наиболее существенными из них являются следующие: 1) более высокая температура металла и шлака, особенно на стадии образования капель (Тк = 3000 К), что способствует диссоциации сернистых и фосфорных соединений, ослабляет их химические связи и тем самым облегчает удаление серы и фосфора из металла шва в шлак; 2) интенсивное перемешивание металла со шлаком в кипящих каплях и в сварочной ванне увеличивает относительную массу шлака в 100 -1000 раз по сравнению с относительной массой шлака при плавке стали; 3) использование специальных рафинирующих компонентов: кальция Са, церия Се, лантана La, иттрия I и других в электродных покрытиях или сварочных флюсах позволяет провести удаление или связывание вредных примесей. Таким образом, несмотря на кратковременность взаимодействия металла со шлаком, при сварке плавлением есть возможность получать металл шва с меньшим содержанием серы и фосфора, чем в основном металле. 3
 Влияние серы на структуру и свойства шва Источниками поступления серы и фосфора в зону сварки служат: флюсы и электродные покрытия, в состав которых входят содержащие примеси серы компоненты, например марганцевые руды, а также расплавленные основной и электродный металлы. Содержание серы в металле в количестве, превышающем допустимые нормы, резко снижает его механические свойства и является причиной красноломкости металла, а при сварке приводит к появлению в шве кристаллизационых трещин. еханизм влияния примесей серы на наплавленный металл состоит в следующем. В сталях сера образует с железом сульфид железа Fe. S, температура плавления которого составляет 1468 К, т. е. ниже температуры плавления стали на 300 К. Сульфид железа почти не растворяется в твердом железе. 4
Влияние серы на структуру и свойства шва Источниками поступления серы и фосфора в зону сварки служат: флюсы и электродные покрытия, в состав которых входят содержащие примеси серы компоненты, например марганцевые руды, а также расплавленные основной и электродный металлы. Содержание серы в металле в количестве, превышающем допустимые нормы, резко снижает его механические свойства и является причиной красноломкости металла, а при сварке приводит к появлению в шве кристаллизационых трещин. еханизм влияния примесей серы на наплавленный металл состоит в следующем. В сталях сера образует с железом сульфид железа Fe. S, температура плавления которого составляет 1468 К, т. е. ниже температуры плавления стали на 300 К. Сульфид железа почти не растворяется в твердом железе. 4
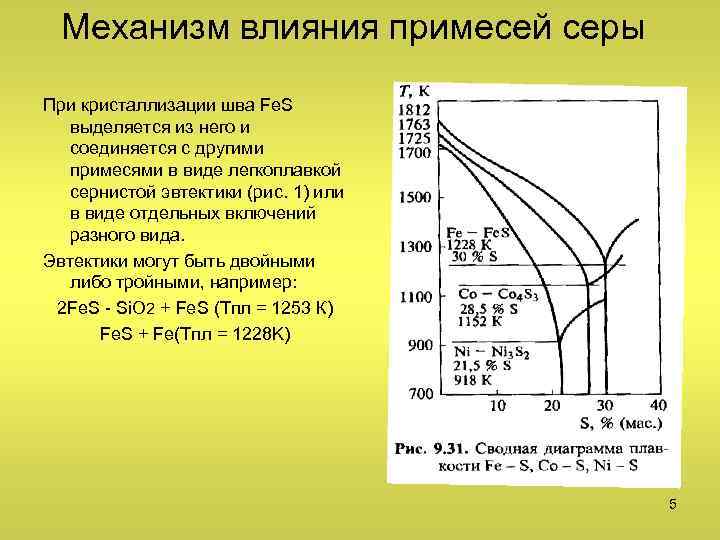 Механизм влияния примесей серы При кристаллизации шва Fe. S выделяется из него и соединяется с другими примесями в виде легкоплавкой сернистой эвтектики (рис. 1) или в виде отдельных включений разного вида. Эвтектики могут быть двойными либо тройными, например: 2 Fe. S - Si. O 2 + Fe. S (Тпл = 1253 К) Fe. S + Fe(Тпл = 1228 K) 5
Механизм влияния примесей серы При кристаллизации шва Fe. S выделяется из него и соединяется с другими примесями в виде легкоплавкой сернистой эвтектики (рис. 1) или в виде отдельных включений разного вида. Эвтектики могут быть двойными либо тройными, например: 2 Fe. S - Si. O 2 + Fe. S (Тпл = 1253 К) Fe. S + Fe(Тпл = 1228 K) 5
 В процессе направленной кристаллизации металла шва, протекающем в интервале температур ликвидус-солидус, эти легкоплавкие сернистые эвтектики оттесняются растущими кристаллитами металла шва к границам между кристаллитами и к месту их стыка (в центральной части сварочной ванны) и становятся частью так называемых межкристаллитных прослоек. К моменту окончания кристаллизации металла шва такие межкристаллитные прослойки могут быть еще в жидком состоянии (Тэ < Тс). Если возникнут растягивающие напряжения от усадки шва и временных сварочных деформаций в шве, то возможно появление на этих участках горячих трещин кристаллизационного типа. Одновременное присутствие в металле шва углерода и кремния увеличивает склонность шва к кристаллизационным трещинам в результате снижения температуры затвердевания ликватов и увеличения температурного интервала хрупкости. Участки швов с сернистыми ликватами, не разрушившиеся при кристаллизации, имеют пониженные механические свойства и потенциально склонны к разрушению как при высоких, так и при низких температурах. Особенно вредно влияет сера на свойства коррозионно-стойких сталей и сплавов никеля. 6
В процессе направленной кристаллизации металла шва, протекающем в интервале температур ликвидус-солидус, эти легкоплавкие сернистые эвтектики оттесняются растущими кристаллитами металла шва к границам между кристаллитами и к месту их стыка (в центральной части сварочной ванны) и становятся частью так называемых межкристаллитных прослоек. К моменту окончания кристаллизации металла шва такие межкристаллитные прослойки могут быть еще в жидком состоянии (Тэ < Тс). Если возникнут растягивающие напряжения от усадки шва и временных сварочных деформаций в шве, то возможно появление на этих участках горячих трещин кристаллизационного типа. Одновременное присутствие в металле шва углерода и кремния увеличивает склонность шва к кристаллизационным трещинам в результате снижения температуры затвердевания ликватов и увеличения температурного интервала хрупкости. Участки швов с сернистыми ликватами, не разрушившиеся при кристаллизации, имеют пониженные механические свойства и потенциально склонны к разрушению как при высоких, так и при низких температурах. Особенно вредно влияет сера на свойства коррозионно-стойких сталей и сплавов никеля. 6
 Десульфурация сварочной ванны Для снижения содержания серы в металле шва нужно вводить в сварочную ванну такие элементы, которые имели бы к сере большее сродство, чем железо. Кроме того, образующиеся сульфиды этих элементов должны удовлетворять следующим требованиям: обладать более высокой, чем у железа или никеля, температурой плавления и не создавать сульфидных легкоплавких эвтектик. По степени возрастания химической прочности образующихся сульфидов, т. е. их энтальпии, элементы, вводимые для десульфурации сварочной ванны, располагаются в следующей последовательности: Аl, Са, Na, Mn, Mg. Однако использование их для связывания серы сопряжено с трудностями, так как все эти элементы имеют и более высокое сродство к кислороду, т. е. связываются им в оксиды, практически не удаляющиеся из кристаллизующегося шва и образующие включения. Из числа перечисленных элементов наибольший интерес с этой точки зрения представляет марганец, поскольку: 1) он имеет сравнительно высокое сродство к сере; 2) как правило, он присутствует в свариваемых сталях в сравнительно больших количествах (0, 5. . . 0, 65 %); 3) Мп мало растворим в Fe и образует тугоплавкий и пластичный сульфид Mn. S шаровидной формы (Tпл= 1893 К), равномерно распределяющийся преимущественно в объемах зерен; 4) при концентрации марганца в стали более 0, 6 %, он способствует переходу серы из Fe. S в Mn. S, т. е. в шлак. 7
Десульфурация сварочной ванны Для снижения содержания серы в металле шва нужно вводить в сварочную ванну такие элементы, которые имели бы к сере большее сродство, чем железо. Кроме того, образующиеся сульфиды этих элементов должны удовлетворять следующим требованиям: обладать более высокой, чем у железа или никеля, температурой плавления и не создавать сульфидных легкоплавких эвтектик. По степени возрастания химической прочности образующихся сульфидов, т. е. их энтальпии, элементы, вводимые для десульфурации сварочной ванны, располагаются в следующей последовательности: Аl, Са, Na, Mn, Mg. Однако использование их для связывания серы сопряжено с трудностями, так как все эти элементы имеют и более высокое сродство к кислороду, т. е. связываются им в оксиды, практически не удаляющиеся из кристаллизующегося шва и образующие включения. Из числа перечисленных элементов наибольший интерес с этой точки зрения представляет марганец, поскольку: 1) он имеет сравнительно высокое сродство к сере; 2) как правило, он присутствует в свариваемых сталях в сравнительно больших количествах (0, 5. . . 0, 65 %); 3) Мп мало растворим в Fe и образует тугоплавкий и пластичный сульфид Mn. S шаровидной формы (Tпл= 1893 К), равномерно распределяющийся преимущественно в объемах зерен; 4) при концентрации марганца в стали более 0, 6 %, он способствует переходу серы из Fe. S в Mn. S, т. е. в шлак. 7
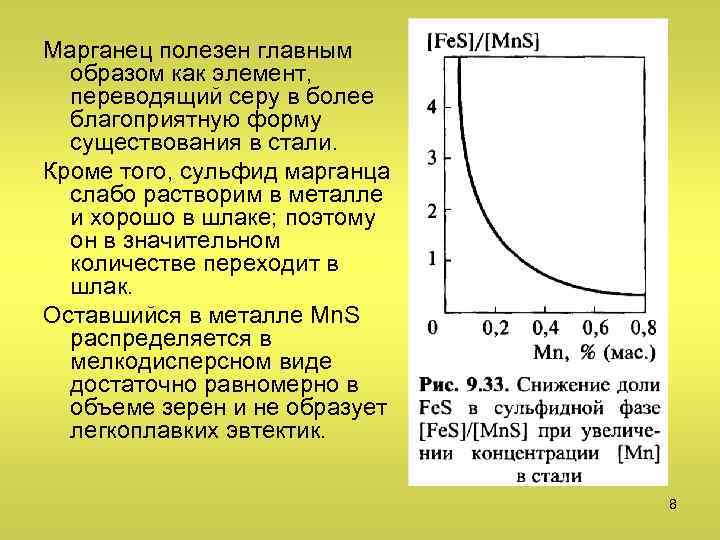 Марганец полезен главным образом как элемент, переводящий серу в более благоприятную форму существования в стали. Кроме того, сульфид марганца слабо растворим в металле и хорошо в шлаке; поэтому он в значительном количестве переходит в шлак. Оставшийся в металле Mn. S распределяется в мелкодисперсном виде достаточно равномерно в объеме зерен и не образует легкоплавких эвтектик. 8
Марганец полезен главным образом как элемент, переводящий серу в более благоприятную форму существования в стали. Кроме того, сульфид марганца слабо растворим в металле и хорошо в шлаке; поэтому он в значительном количестве переходит в шлак. Оставшийся в металле Mn. S распределяется в мелкодисперсном виде достаточно равномерно в объеме зерен и не образует легкоплавких эвтектик. 8
 В сварочной практике связывают и удаляют серу чаще всего двумя способами: с помощью Мn и Мn. О, а также Са. О. Рассмотрим первый из элементов-десульфураторов - марганец. Основная реакция связывания серы марганцем описывается уравнением [Fe. S] + [Mn] <=> (Mn. S) + [Fe] Чем больше марганца, тем меньше Fe. S в металле шва. При этом чистый Мn вводят в сварочную проволоку или в основной металл. Однако эффективность связывания серы в сульфид марганца по реакции мала, так как вправо реакция заметно развивается лишь при пониженных температурах, когда протекающие процессы замедляются. В итоге в металле шва оказывается значительное количество Fe. S. Поэтому реакция дополняется второй реакцией сульфида железа с дополнительно введенным оксидом марганца: [Fe. S] + (Mn. O)<=> (Mn. S) + [Fe. O]. Преимущество второй реакции состоит в том, что константа равновесия Кс растет с увеличением температуры, т. е. с ростом температуры реакция сдвигается в сторону большего выхода (Mn. S) и [Fe. O]. Рассматривая реакции совместно, можно отметить, что превращению Fe. S в Mn. S способствуют: лучшая раскисленность металла (т. е. уменьшение [Fe. O]); увеличение содержания марганца в металле; высокая концентрация (Мn. О) в шлаке. В углеродистых сталях обычно отношение [Mn]/[S] равно 20. . . 25, что позволяет избежать кристаллизационных трещин. В легированных сталях это соотношение должно быть существенно выше, чтобы получить швы без трещин. 9
В сварочной практике связывают и удаляют серу чаще всего двумя способами: с помощью Мn и Мn. О, а также Са. О. Рассмотрим первый из элементов-десульфураторов - марганец. Основная реакция связывания серы марганцем описывается уравнением [Fe. S] + [Mn] <=> (Mn. S) + [Fe] Чем больше марганца, тем меньше Fe. S в металле шва. При этом чистый Мn вводят в сварочную проволоку или в основной металл. Однако эффективность связывания серы в сульфид марганца по реакции мала, так как вправо реакция заметно развивается лишь при пониженных температурах, когда протекающие процессы замедляются. В итоге в металле шва оказывается значительное количество Fe. S. Поэтому реакция дополняется второй реакцией сульфида железа с дополнительно введенным оксидом марганца: [Fe. S] + (Mn. O)<=> (Mn. S) + [Fe. O]. Преимущество второй реакции состоит в том, что константа равновесия Кс растет с увеличением температуры, т. е. с ростом температуры реакция сдвигается в сторону большего выхода (Mn. S) и [Fe. O]. Рассматривая реакции совместно, можно отметить, что превращению Fe. S в Mn. S способствуют: лучшая раскисленность металла (т. е. уменьшение [Fe. O]); увеличение содержания марганца в металле; высокая концентрация (Мn. О) в шлаке. В углеродистых сталях обычно отношение [Mn]/[S] равно 20. . . 25, что позволяет избежать кристаллизационных трещин. В легированных сталях это соотношение должно быть существенно выше, чтобы получить швы без трещин. 9
 Вторым элементом-десульфуратором служит кальций. Ввод кальция дает следующие положительные результаты. Во-первых, газообразный кальций активно реагирует одновременно с серой и кислородом расплавленной стали, образуя свойственные только ему специфические соединения - оксисуль-фиды. Даже при весьма низкой концентрации в металле (не выше 0, 0001 %) кальций вследствие своей поверхностной активности оказывает заметное влияние на процесс рафинирования, особенно при совместном введении кальция и присадок редкоземельных элементов - церия и лантана. Во-вторых, при использовании кальция как элемента-десуль-фуратора возможно связывание серы известью Са. О. Эта реакция приводит к образованию весьма прочного и тугоплавкого сульфида кальция, практически не растворимого в металле. Процесс протекает в соответствии с реакцией [Fe. S] + (Са. О) <=> (Ca. S) + [Fe. O]. Константа равновесия реакции растет с увеличением температуры, при этом процесс интенсивнее развивается вправо -в сторону образования в шлаке Ca. S. Лучшее раскисление металла и введение в шлак окиси кальция будет способствовать уменьшению содержания Fe. S в металле. Увеличение содержания Са. О в шлаке приводит к росту константы распределения L = (S)/[S], что обеспечивает более полный переход серы из металла в шлак. Установлено, что наличие кремния и алюминия в металле значительно ускоряет процесс десульфурации сварочной ванны, причем сера удаляется одновременно с кислородом. Это является следствием как прямого испарения серы в виде соединений AI 2 S 3 (температура возгонки равна 1823 К) и Si. S (температура возгонки равна 1213 К), так и включения ее в состав образующихся шлаковых частиц. 10
Вторым элементом-десульфуратором служит кальций. Ввод кальция дает следующие положительные результаты. Во-первых, газообразный кальций активно реагирует одновременно с серой и кислородом расплавленной стали, образуя свойственные только ему специфические соединения - оксисуль-фиды. Даже при весьма низкой концентрации в металле (не выше 0, 0001 %) кальций вследствие своей поверхностной активности оказывает заметное влияние на процесс рафинирования, особенно при совместном введении кальция и присадок редкоземельных элементов - церия и лантана. Во-вторых, при использовании кальция как элемента-десуль-фуратора возможно связывание серы известью Са. О. Эта реакция приводит к образованию весьма прочного и тугоплавкого сульфида кальция, практически не растворимого в металле. Процесс протекает в соответствии с реакцией [Fe. S] + (Са. О) <=> (Ca. S) + [Fe. O]. Константа равновесия реакции растет с увеличением температуры, при этом процесс интенсивнее развивается вправо -в сторону образования в шлаке Ca. S. Лучшее раскисление металла и введение в шлак окиси кальция будет способствовать уменьшению содержания Fe. S в металле. Увеличение содержания Са. О в шлаке приводит к росту константы распределения L = (S)/[S], что обеспечивает более полный переход серы из металла в шлак. Установлено, что наличие кремния и алюминия в металле значительно ускоряет процесс десульфурации сварочной ванны, причем сера удаляется одновременно с кислородом. Это является следствием как прямого испарения серы в виде соединений AI 2 S 3 (температура возгонки равна 1823 К) и Si. S (температура возгонки равна 1213 К), так и включения ее в состав образующихся шлаковых частиц. 10
 Снижение содержания фосфора в металле шва Фосфор, как и сера, является вредной примесью, ухудшающей механические свойства стали, особенно при пониженной температуре, т. е. вызывающей ее хладноломкость. Это объясняется тем, что в сталях фосфор образует частично растворимые в феррите фосфиды Fе 3 Р (или Fe 2 P) по реакции 3 Fe + P<=>Fe 3 P (15, 63 % Р). Фосфор относится к числу сильно ликвирующих примесей, которые неравномерно распределяются в металле. Ликвацию фосфора усиливает углерод. При этом возможно образование легкоплавкой эвтектики тройного типа Fe + Р + С, еще более снижающей прочность и пластичность шва в температурном интервале хрупкости в сталях (Tпл=1173 К). Особенно низкой является температура плавления фосфидной эвтектики (Tпл=923 К) и соответственно низкой является ее стойкость против образования горячих трещин при сварке никелевых сплавов. Удаление фосфора из сварочной ванны основано на его окислении в составе фосфидов и последующем связывании фосфорного ангидрида Р 2 О 5 в прочное комплексное соединение, легко переходящее в шлак. Окисление фосфора развивается в сварочной ванне в соответствии со следующей реакцией: 2 Fe 3 P + 5 Fe. O<=> Р 2 О 5 + 11 Fe. 11
Снижение содержания фосфора в металле шва Фосфор, как и сера, является вредной примесью, ухудшающей механические свойства стали, особенно при пониженной температуре, т. е. вызывающей ее хладноломкость. Это объясняется тем, что в сталях фосфор образует частично растворимые в феррите фосфиды Fе 3 Р (или Fe 2 P) по реакции 3 Fe + P<=>Fe 3 P (15, 63 % Р). Фосфор относится к числу сильно ликвирующих примесей, которые неравномерно распределяются в металле. Ликвацию фосфора усиливает углерод. При этом возможно образование легкоплавкой эвтектики тройного типа Fe + Р + С, еще более снижающей прочность и пластичность шва в температурном интервале хрупкости в сталях (Tпл=1173 К). Особенно низкой является температура плавления фосфидной эвтектики (Tпл=923 К) и соответственно низкой является ее стойкость против образования горячих трещин при сварке никелевых сплавов. Удаление фосфора из сварочной ванны основано на его окислении в составе фосфидов и последующем связывании фосфорного ангидрида Р 2 О 5 в прочное комплексное соединение, легко переходящее в шлак. Окисление фосфора развивается в сварочной ванне в соответствии со следующей реакцией: 2 Fe 3 P + 5 Fe. O<=> Р 2 О 5 + 11 Fe. 11
 Затем идет процесс связывания шлаком фосфорного ангидрида. По возрастающей силе сродства к ангидриду Р 2 О 5 основные и амфотерные оксиды можно расположить в следующей последовательности: Fe 2 O 3 ->Аl 2 О 3 -> Fe. O -> Mn. O -> Mg. O -> Ca. O, т. е. наиболее активными по отношению к фосфорному ангидриду являются Ca. O, Mg. O и Мn. О. Запишем уравнения реакции связывания фосфорного ангидрида: - наиболее активный процесс: 4 Са. О + Р 2 О 5 <=> (Са. О)4 • Р 2 О 5; -менее активный процесс: 4 Мn. О + Р 2 О 5 <=> (Мn. О)4 • Р 2 О 5. Для процесса удаления фосфора из сварочной ванны, объединив уравнения получим: 2 Fe 3 P + 5 Fe. O + 4 Са. О <=> (Са. О)4 • Р 2 О 5 + 11 Fe. 12
Затем идет процесс связывания шлаком фосфорного ангидрида. По возрастающей силе сродства к ангидриду Р 2 О 5 основные и амфотерные оксиды можно расположить в следующей последовательности: Fe 2 O 3 ->Аl 2 О 3 -> Fe. O -> Mn. O -> Mg. O -> Ca. O, т. е. наиболее активными по отношению к фосфорному ангидриду являются Ca. O, Mg. O и Мn. О. Запишем уравнения реакции связывания фосфорного ангидрида: - наиболее активный процесс: 4 Са. О + Р 2 О 5 <=> (Са. О)4 • Р 2 О 5; -менее активный процесс: 4 Мn. О + Р 2 О 5 <=> (Мn. О)4 • Р 2 О 5. Для процесса удаления фосфора из сварочной ванны, объединив уравнения получим: 2 Fe 3 P + 5 Fe. O + 4 Са. О <=> (Са. О)4 • Р 2 О 5 + 11 Fe. 12
 Концентрации фосфора в сварочной ванне полнота его удаления в шлак будет зависеть от содержания в шлаке следующих соединений: 1) свободных оксидов Са. О и Fe. O, с увеличением содержания которых реакция сдвигается вправо, т. е. в направлении очищения металла от фосфора; 2) комплексного соединения, связывающего фосфор, например (Са. О)4*Р 2 О 5 Уменьшение содержания свободных оксидов и комплексных соединений в шлаке способствует очищению металла от фосфора. Этого достигают разбавлением шлаков соответствующими нейтральными добавками, например плавиковым шпатом, который одновременно разжижает шлак, а также повышает его общую реакционную способность. Таким образом, основные шлаки могут обеспечить необходимое очищение металла шва от фосфора. Кислые шлаки значительно хуже удаляют фосфор из металла. Имеющиеся в них основные оксиды Ca. O, Mn. O, Fe. O связаны в силикаты, и развитие реакции происходит влево. При этом увеличивается содержание фосфора в металле шва и тормозится его удаление в шлак. Константа равновесия реакции с ростом температуры уменьшается, что свидетельствует об интенсификации реакции перехода фосфора из шлака в металл. Поэтому при пониженных температурах следует ожидать более активного перехода фосфора в шлак. В этом отношении «короткие» шлаки эффективнее «длинных» . При сварке в среде защитных газов удаление фосфора из металла шва связано с большими трудностями. Главным фактором сохранения высоких значений механических свойств является предельное снижение фосфора в основном металле. 13
Концентрации фосфора в сварочной ванне полнота его удаления в шлак будет зависеть от содержания в шлаке следующих соединений: 1) свободных оксидов Са. О и Fe. O, с увеличением содержания которых реакция сдвигается вправо, т. е. в направлении очищения металла от фосфора; 2) комплексного соединения, связывающего фосфор, например (Са. О)4*Р 2 О 5 Уменьшение содержания свободных оксидов и комплексных соединений в шлаке способствует очищению металла от фосфора. Этого достигают разбавлением шлаков соответствующими нейтральными добавками, например плавиковым шпатом, который одновременно разжижает шлак, а также повышает его общую реакционную способность. Таким образом, основные шлаки могут обеспечить необходимое очищение металла шва от фосфора. Кислые шлаки значительно хуже удаляют фосфор из металла. Имеющиеся в них основные оксиды Ca. O, Mn. O, Fe. O связаны в силикаты, и развитие реакции происходит влево. При этом увеличивается содержание фосфора в металле шва и тормозится его удаление в шлак. Константа равновесия реакции с ростом температуры уменьшается, что свидетельствует об интенсификации реакции перехода фосфора из шлака в металл. Поэтому при пониженных температурах следует ожидать более активного перехода фосфора в шлак. В этом отношении «короткие» шлаки эффективнее «длинных» . При сварке в среде защитных газов удаление фосфора из металла шва связано с большими трудностями. Главным фактором сохранения высоких значений механических свойств является предельное снижение фосфора в основном металле. 13
 Список используемой литературы: 1. Коновалов А. В. , Неровный В. М. , Куркин А. С. , Теория сварочных процессов. Учебник для вузов. 2007 г. 2. Теория сварочных процессов: Учебник для вузов по специальности Оборудование и технология сварочного производства /В. Н. Волченко, В. М. Ямпольский, В. А. Винокуров и др. ; Под ред. В. В. Фролова. – М. : Высшая школа, 1988. 559 с 14
Список используемой литературы: 1. Коновалов А. В. , Неровный В. М. , Куркин А. С. , Теория сварочных процессов. Учебник для вузов. 2007 г. 2. Теория сварочных процессов: Учебник для вузов по специальности Оборудование и технология сварочного производства /В. Н. Волченко, В. М. Ямпольский, В. А. Винокуров и др. ; Под ред. В. В. Фролова. – М. : Высшая школа, 1988. 559 с 14
 Спасибо за внимание! 15
Спасибо за внимание! 15


