Презентация Параграф 11 schelochnye-metally
























- Размер: 2.9 Mегабайта
- Количество слайдов: 28
Описание презентации Презентация Параграф 11 schelochnye-metally по слайдам
 Отгадайте фамилию русского ученого, который сказал: «Металлом называется светлое тело, которое ковать можно» . 1. Самый тугоплавкий. 2. Самый распространенный на земле. 3. Самый легкий. 4. Самый электропроводный. 5. Самый твердый. 6. Самый пластичный. 7. Самый легкоплавкий. 8. Самый тяжелый. 9. Самый космический. Л О М О Н О С О ВAu Os Cr Hg Li W Fe Al Ag
Отгадайте фамилию русского ученого, который сказал: «Металлом называется светлое тело, которое ковать можно» . 1. Самый тугоплавкий. 2. Самый распространенный на земле. 3. Самый легкий. 4. Самый электропроводный. 5. Самый твердый. 6. Самый пластичный. 7. Самый легкоплавкий. 8. Самый тяжелый. 9. Самый космический. Л О М О Н О С О ВAu Os Cr Hg Li W Fe Al Ag

 Периодическая система химических элементов Д. И. Менделеева Группы элементов I IIIII VIIIIV V VI VII III VI VIV 21 3 4 5 6 7 10 Периоды Ряды Cu Медь29 63. 546 В Бор 5 10. 811 Ne Неон 10 20, 18 Be Вериллий 4 9, 012 Ca Кальций 20 40, 08 Ag Серебро 47 107. 868 Ra Радий 88 [226] La Лантан 57 138. 81 Al Алюминий 13 26, 9815 O Кислород 8 15. 996 N Азот 7 14. 0067 Ge Германий 32 72. 59 C Углерод 6 12, 011 F фтор 9 18. 9984 Br Бром 35 79. 904 H Водород 1 1. 00797 Se Селен 34 78. 96 I Иод 53 126. 904 Cl Хлор 17 35, 453 As Мышьяк 33 74. 9216 He Гелий 2 4, 003 Ar Аргон 18 39, 948 Xe Ксенон 54 131, 3 Kr Криптон 36 83, 8 Te Теллур 52 127. 60 Fe Железо 26 55. 847 Mg Магний 12 24, 312 S Сера 16 32, 064 P Фосфор 15 30, 9738 Si Кремний 14 28, 086 Ti Титан 22 47. 90 Mo Молибден 42 95. 94 Tс Технеций 43 99 V Ванадий 23 50. 942 Cr Хром 24 51. 996 Mn Марганец 25 54. 938 Sс Скандий 21 44. 956 Ga Галлий 31 69. 72 Re Рений 75 186. 2 Rh Родий 45 102. 905 Ir Иридий 77 192. 2 Ru Рутений 44 101. 07 Os Осмий 76 190. 2 Pt Платина 78 195. 09 Pd Палладий 46 106. 4 At Астат 85 210 Rn Радон 86 [222] Mt Мейтнерий 109 [266 ]Hs Хассий 108 [265 ]Ba Барий 56 137. 34 Sr Стронций 38 87. 62 Rb Рубидий 37 85. 47 In Индий 49 114. 82 98 Zn Цинк 30 65. 37 W Вольфрам 74 183. 85 Po Полоний 84 208. 982 Zr Цирконий 40 91. 224 Nb Ниобий 41 92. 906 Ta Тантал 73 180. 9479 Cd Кадмий 48 112. 41 Sb Сурьма 51 121. 75 Hf Гафний 72 178. 49 Sn Олово 50 118. 71 Pb Свинец 82 207. 2 Bi Висмут 83 208. 98 Co Кобальт 27 58. 933 Ni Никель28 58. 71 Y Иттрий 39 88. 9059 Au Золото 79 196. 966 Tl Таллий 81 204. 383 Hg Ртуть 80 200. 59 Ac Актиний 89 227. 028 Bh Борий 107 [262]Sg Сиборгий 106 [263]Db Дубний 105 [262]Rf Резерфордий 104 [261]Щелочные металлы
Периодическая система химических элементов Д. И. Менделеева Группы элементов I IIIII VIIIIV V VI VII III VI VIV 21 3 4 5 6 7 10 Периоды Ряды Cu Медь29 63. 546 В Бор 5 10. 811 Ne Неон 10 20, 18 Be Вериллий 4 9, 012 Ca Кальций 20 40, 08 Ag Серебро 47 107. 868 Ra Радий 88 [226] La Лантан 57 138. 81 Al Алюминий 13 26, 9815 O Кислород 8 15. 996 N Азот 7 14. 0067 Ge Германий 32 72. 59 C Углерод 6 12, 011 F фтор 9 18. 9984 Br Бром 35 79. 904 H Водород 1 1. 00797 Se Селен 34 78. 96 I Иод 53 126. 904 Cl Хлор 17 35, 453 As Мышьяк 33 74. 9216 He Гелий 2 4, 003 Ar Аргон 18 39, 948 Xe Ксенон 54 131, 3 Kr Криптон 36 83, 8 Te Теллур 52 127. 60 Fe Железо 26 55. 847 Mg Магний 12 24, 312 S Сера 16 32, 064 P Фосфор 15 30, 9738 Si Кремний 14 28, 086 Ti Титан 22 47. 90 Mo Молибден 42 95. 94 Tс Технеций 43 99 V Ванадий 23 50. 942 Cr Хром 24 51. 996 Mn Марганец 25 54. 938 Sс Скандий 21 44. 956 Ga Галлий 31 69. 72 Re Рений 75 186. 2 Rh Родий 45 102. 905 Ir Иридий 77 192. 2 Ru Рутений 44 101. 07 Os Осмий 76 190. 2 Pt Платина 78 195. 09 Pd Палладий 46 106. 4 At Астат 85 210 Rn Радон 86 [222] Mt Мейтнерий 109 [266 ]Hs Хассий 108 [265 ]Ba Барий 56 137. 34 Sr Стронций 38 87. 62 Rb Рубидий 37 85. 47 In Индий 49 114. 82 98 Zn Цинк 30 65. 37 W Вольфрам 74 183. 85 Po Полоний 84 208. 982 Zr Цирконий 40 91. 224 Nb Ниобий 41 92. 906 Ta Тантал 73 180. 9479 Cd Кадмий 48 112. 41 Sb Сурьма 51 121. 75 Hf Гафний 72 178. 49 Sn Олово 50 118. 71 Pb Свинец 82 207. 2 Bi Висмут 83 208. 98 Co Кобальт 27 58. 933 Ni Никель28 58. 71 Y Иттрий 39 88. 9059 Au Золото 79 196. 966 Tl Таллий 81 204. 383 Hg Ртуть 80 200. 59 Ac Актиний 89 227. 028 Bh Борий 107 [262]Sg Сиборгий 106 [263]Db Дубний 105 [262]Rf Резерфордий 104 [261]Щелочные металлы
 Происхождение названий щелочных металлов • Li (1817) лат. » литос» — камень • Na (1807) араб. «натрум» -сода • К (1807) араб. «алкали» — щелочь • Rb (1861) лат. «рубидус» — темно-красный • Cs (1860) лат. «цезиус» — небесно-голубой • Fr (1939) от названия страны Франция.
Происхождение названий щелочных металлов • Li (1817) лат. » литос» — камень • Na (1807) араб. «натрум» -сода • К (1807) араб. «алкали» — щелочь • Rb (1861) лат. «рубидус» — темно-красный • Cs (1860) лат. «цезиус» — небесно-голубой • Fr (1939) от названия страны Франция.
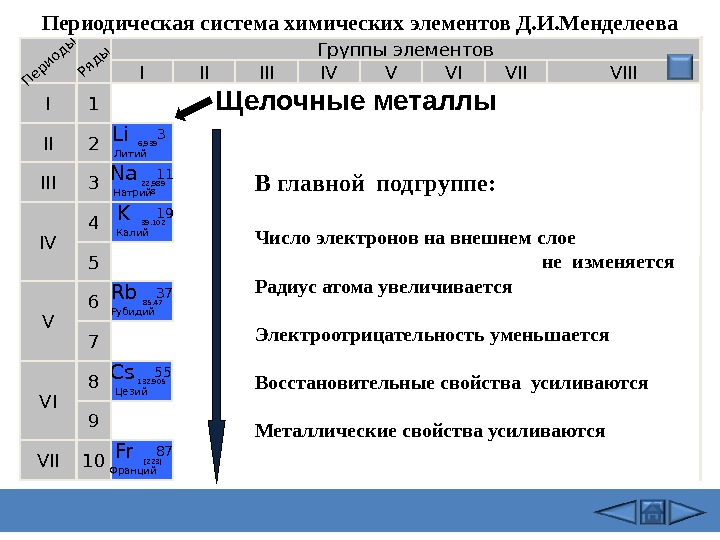
 Группы элементов I IIIII VIIIIV V VI VII III VI VIV 21 3 4 5 6 7 10 Li Литий 3 6, 939 Периоды Ряды K Калий 19 39. 102 Na Натрий 11 22, 989 8 Rb Рубидий 37 85. 47 Cs Цезий 55 132. 905 Fr Франций 87 [223]98 Щелочные металлы. Периодическая система химических элементов Д. И. Менделеева В главной подгруппе: Число электронов на внешнем слое не изменяется Радиус атома увеличивается Электроотрицательность уменьшается Восстановительные свойства усиливаются Металлические свойства усиливаются
Группы элементов I IIIII VIIIIV V VI VII III VI VIV 21 3 4 5 6 7 10 Li Литий 3 6, 939 Периоды Ряды K Калий 19 39. 102 Na Натрий 11 22, 989 8 Rb Рубидий 37 85. 47 Cs Цезий 55 132. 905 Fr Франций 87 [223]98 Щелочные металлы. Периодическая система химических элементов Д. И. Менделеева В главной подгруппе: Число электронов на внешнем слое не изменяется Радиус атома увеличивается Электроотрицательность уменьшается Восстановительные свойства усиливаются Металлические свойства усиливаются
![Li Na K Rb Cs Fr 7 23 39 85 133 [223] 2 s 1 3 Li Na K Rb Cs Fr 7 23 39 85 133 [223] 2 s 1 3](/docs//paragraf_11_schelochnye-metally_images/paragraf_11_schelochnye-metally_5.jpg) Li Na K Rb Cs Fr 7 23 39 85 133 [223] 2 s 1 3 s 1 4 s 1 5 s 1 6 s 1 7 s 1)) )))))) )))))))Элемент А r Валентные электроны. Число энергетически х уровней Металлические свойства Восстановительные свойства. R атома
Li Na K Rb Cs Fr 7 23 39 85 133 [223] 2 s 1 3 s 1 4 s 1 5 s 1 6 s 1 7 s 1)) )))))) )))))))Элемент А r Валентные электроны. Число энергетически х уровней Металлические свойства Восстановительные свойства. R атома
 Вещества серебристо-белого цвета Электропроводны и теплопроводны Легкоплавкие. пластичные. Li Na K Rb Cs t t плпл = 98 t t плпл = 181 t t плпл = 64 t t плпл = 28 t t плпл =
Вещества серебристо-белого цвета Электропроводны и теплопроводны Легкоплавкие. пластичные. Li Na K Rb Cs t t плпл = 98 t t плпл = 181 t t плпл = 64 t t плпл = 28 t t плпл =
 Периодическая система химических элементов Д. И. Менделеева Группы элементов I IIIII VIIIIV V VI VII III VI VIV 21 3 4 5 6 7 Периоды Ряды 98 10 Л тий / Lithium (Li) ии Внешний вид простого вещества Мягкий металл серебристо-белого цвета. Электронная коефигуранция [He] 2 s 1 ЭО (по Полингу) 0, 98 Степень окисления 1 Плотность 0, 534 г/см³ Температура плавления 453, 69 K Температура кипения 1613 KLi
Периодическая система химических элементов Д. И. Менделеева Группы элементов I IIIII VIIIIV V VI VII III VI VIV 21 3 4 5 6 7 Периоды Ряды 98 10 Л тий / Lithium (Li) ии Внешний вид простого вещества Мягкий металл серебристо-белого цвета. Электронная коефигуранция [He] 2 s 1 ЭО (по Полингу) 0, 98 Степень окисления 1 Плотность 0, 534 г/см³ Температура плавления 453, 69 K Температура кипения 1613 KLi
 Периодическая система химических элементов Д. И. Менделеева Группы элементов I IIIII VIIIIV V VI VII III VI VIV 21 3 4 5 6 7 Периоды Ряды 98 10 Натрий/Natrium (Na) Внешний вид простого вещества серебристо-белый мягкий металл Электронная коефигуранция [Ne] 3 s 1 ЭО (по Полингу) 0, 93 Степень окисления 1 Плотность 0, 971 г/см ³ Температура плавления 370, 96 К Температура кипения 1156, 1 К
Периодическая система химических элементов Д. И. Менделеева Группы элементов I IIIII VIIIIV V VI VII III VI VIV 21 3 4 5 6 7 Периоды Ряды 98 10 Натрий/Natrium (Na) Внешний вид простого вещества серебристо-белый мягкий металл Электронная коефигуранция [Ne] 3 s 1 ЭО (по Полингу) 0, 93 Степень окисления 1 Плотность 0, 971 г/см ³ Температура плавления 370, 96 К Температура кипения 1156, 1 К
 Периодическая система химических элементов Д. И. Менделеева Группы элементов I IIIII VIIIIV V VI VII III VI VIV 21 3 4 5 6 7 Периоды Ряды 98 10 Калий / Kalium (K) Внешний вид простого вещества Серебристо-белый мягкий металл Электронная конфигуранция [Ar] 3 d 10 4 s 1 ЭО (по Полингу) 0, 82 Степень окисления 1 Плотность 0, 856 г/см³ Температура плавления 336, 8 К Температура кипения 1047 К
Периодическая система химических элементов Д. И. Менделеева Группы элементов I IIIII VIIIIV V VI VII III VI VIV 21 3 4 5 6 7 Периоды Ряды 98 10 Калий / Kalium (K) Внешний вид простого вещества Серебристо-белый мягкий металл Электронная конфигуранция [Ar] 3 d 10 4 s 1 ЭО (по Полингу) 0, 82 Степень окисления 1 Плотность 0, 856 г/см³ Температура плавления 336, 8 К Температура кипения 1047 К
 Периодическая система химических элементов Д. И. Менделеева Группы элементов I IIIII VIIIIV V VI VII III VI VIV 21 3 4 5 6 7 Периоды Ряды 98 10 Руб дий / Rubidium (Rb) ии Внешний вид простого вещества Серебристо-белый мягкий металл Электронная конфигуранция [Kr] 5 s 1 ЭО (по Полингу) 0, 82 Степень окисления 1 Плотность 1, 532 г/см³ Температура плавления 312, 2 К Температура кипения 961 К
Периодическая система химических элементов Д. И. Менделеева Группы элементов I IIIII VIIIIV V VI VII III VI VIV 21 3 4 5 6 7 Периоды Ряды 98 10 Руб дий / Rubidium (Rb) ии Внешний вид простого вещества Серебристо-белый мягкий металл Электронная конфигуранция [Kr] 5 s 1 ЭО (по Полингу) 0, 82 Степень окисления 1 Плотность 1, 532 г/см³ Температура плавления 312, 2 К Температура кипения 961 К
 Периодическая система химических элементов Д. И. Менделеева Группы элементов I IIIII VIIIIV V VI VII III VI VIV 21 3 4 5 6 7 Периоды Ряды 98 10 Цезий / Caesium (Cs) Внешний вид простого вещества очень мягкий вязкий серебристо-жёлтый похожий на золото металл Электронная конфигуранция [Xe] 6 s 1 ЭО (по Полингу) 0, 79 Степень окисления 1 Плотность 1, 873 г/см Температура плавления 301, 6 К Температура кипения 951, 6 К
Периодическая система химических элементов Д. И. Менделеева Группы элементов I IIIII VIIIIV V VI VII III VI VIV 21 3 4 5 6 7 Периоды Ряды 98 10 Цезий / Caesium (Cs) Внешний вид простого вещества очень мягкий вязкий серебристо-жёлтый похожий на золото металл Электронная конфигуранция [Xe] 6 s 1 ЭО (по Полингу) 0, 79 Степень окисления 1 Плотность 1, 873 г/см Температура плавления 301, 6 К Температура кипения 951, 6 К
 Периодическая система химических элементов Д. И. Менделеева Группы элементов I IIIII VIIIIV V VI VII III VI VIV 21 3 4 5 6 7 Периоды Ряды 98 10 Франций / Francium (Fr) Внешний вид простого вещества радиоактивный щелочной металл Электронная конфигуранция [Rn] 7 s 1 ЭО (по Полингу) 2, 2 Степень окисления 1 Плотность 1, 87 г/см Температура плавления 300 К Температура кипения 950 К
Периодическая система химических элементов Д. И. Менделеева Группы элементов I IIIII VIIIIV V VI VII III VI VIV 21 3 4 5 6 7 Периоды Ряды 98 10 Франций / Francium (Fr) Внешний вид простого вещества радиоактивный щелочной металл Электронная конфигуранция [Rn] 7 s 1 ЭО (по Полингу) 2, 2 Степень окисления 1 Плотность 1, 87 г/см Температура плавления 300 К Температура кипения 950 К
![Фотография Описание минерала Химический состав Li. Al[Si 2 O 6 ] Цвет Бесцветный, Фотография Описание минерала Химический состав Li. Al[Si 2 O 6 ] Цвет Бесцветный,](/docs//paragraf_11_schelochnye-metally_images/paragraf_11_schelochnye-metally_13.jpg) Фотография Описание минерала Химический состав Li. Al[Si 2 O 6 ] Цвет Бесцветный, красный, желтый, зеленый Плотность 3, 1— 3, 2 г/см 3 Твердость 6, 5 Сподуменн
Фотография Описание минерала Химический состав Li. Al[Si 2 O 6 ] Цвет Бесцветный, красный, желтый, зеленый Плотность 3, 1— 3, 2 г/см 3 Твердость 6, 5 Сподуменн
 Фотография Описание минерала Химический состав Na С l Цвет Бесцветный, красный, желтый, синий Плотность 2, 2— 2, 3 г/см 3 Твердость 2, 5 Вкус Солёный Галит
Фотография Описание минерала Химический состав Na С l Цвет Бесцветный, красный, желтый, синий Плотность 2, 2— 2, 3 г/см 3 Твердость 2, 5 Вкус Солёный Галит
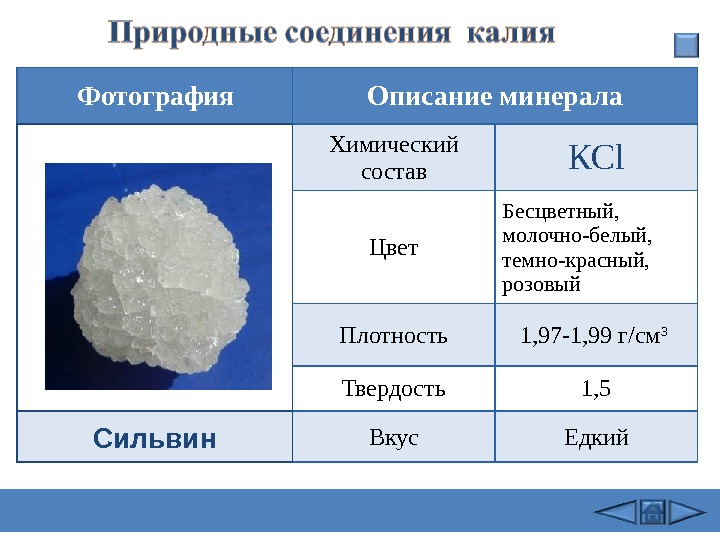
 Фотография Описание минерала Химический состав КС l Цвет Бесцветный, молочно-белый, темно-красный, розовый Плотность 1, 97 -1, 99 г/см 3 Твердость 1, 5 Вкус Едкий Сильвин
Фотография Описание минерала Химический состав КС l Цвет Бесцветный, молочно-белый, темно-красный, розовый Плотность 1, 97 -1, 99 г/см 3 Твердость 1, 5 Вкус Едкий Сильвин
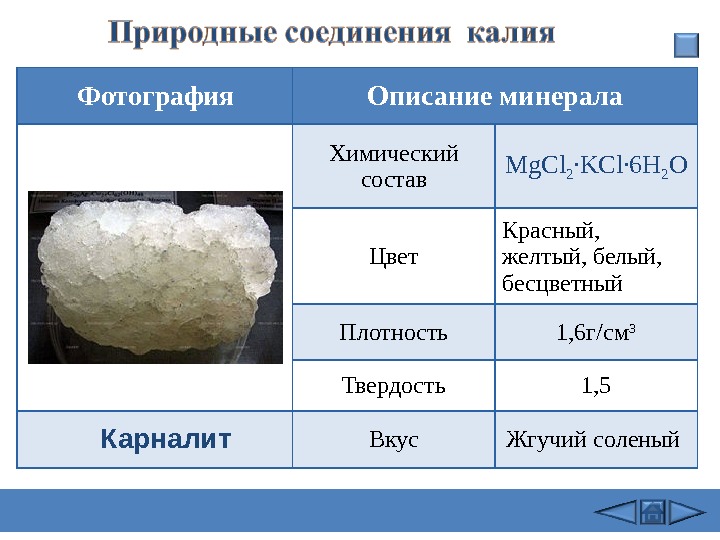
 Фотография Описание минерала Химический состав Mg. Cl 2 ·KCl· 6 H 2 O Цвет Красный, желтый, белый, бесцветный Плотность 1, 6 г/см 3 Твердость 1, 5 Вкус Жгучий соленый Карналит
Фотография Описание минерала Химический состав Mg. Cl 2 ·KCl· 6 H 2 O Цвет Красный, желтый, белый, бесцветный Плотность 1, 6 г/см 3 Твердость 1, 5 Вкус Жгучий соленый Карналит
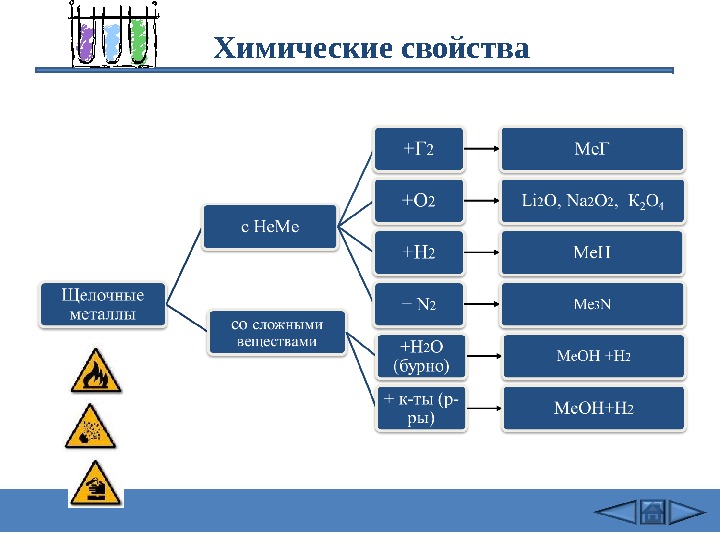
 Химические свойства
Химические свойства
 Химические свойства 1) 2 Na + Cl 2 = 2 Na. Cl ( в атмосфере F 2 и Cl 2 щелочные Me самовоспламеняются) 2) 4 Li + O 2 = 2 Li 2 O 2 Na + O 2 = Na 2 O 2 2 K + 2 O 2 = K 2 O 4 оксид Li пероксид Na надпероксид K 2 Na + Na 2 O 2 = 2 Na 2 O 6 K + K 2 O 4 = 4 K 2 O 3) 2 Na + Н 2 = 2 Na. Н (при нагревании 200 -400 o C) 4) 6 Li + N 2 = 2 Li 3 N ( Li — при комнатной T , остальные щелочные Me — при нагревании) 5 ) 2 Na + 2 Н 2 О = 2 Na. ОН + Н 2 ( Li — спокойно, Na — энергично, остальные – со взрывом – воспламеняется выделяющийся Н 2 Rb и Cs реагируют не только с жидкой Н 2 О , но и со льдом.
Химические свойства 1) 2 Na + Cl 2 = 2 Na. Cl ( в атмосфере F 2 и Cl 2 щелочные Me самовоспламеняются) 2) 4 Li + O 2 = 2 Li 2 O 2 Na + O 2 = Na 2 O 2 2 K + 2 O 2 = K 2 O 4 оксид Li пероксид Na надпероксид K 2 Na + Na 2 O 2 = 2 Na 2 O 6 K + K 2 O 4 = 4 K 2 O 3) 2 Na + Н 2 = 2 Na. Н (при нагревании 200 -400 o C) 4) 6 Li + N 2 = 2 Li 3 N ( Li — при комнатной T , остальные щелочные Me — при нагревании) 5 ) 2 Na + 2 Н 2 О = 2 Na. ОН + Н 2 ( Li — спокойно, Na — энергично, остальные – со взрывом – воспламеняется выделяющийся Н 2 Rb и Cs реагируют не только с жидкой Н 2 О , но и со льдом.
 Качественное определение щелочных металлов Li+ Na+ K+Для распознавания соединений щелочных металлов по окраске пламени исследуемое вещество вносится в пламя горелки на кончике железной проволоки. Li+ — карминово-красный K+ — фиолетовый Cs+ — фиолетово-синий Na+ — желтый Rb + — красный
Качественное определение щелочных металлов Li+ Na+ K+Для распознавания соединений щелочных металлов по окраске пламени исследуемое вещество вносится в пламя горелки на кончике железной проволоки. Li+ — карминово-красный K+ — фиолетовый Cs+ — фиолетово-синий Na+ — желтый Rb + — красный
 Сколько воды и хлорида натрия нужно взять для приготовления физиологического раствора массой 0, 5 кг? 4, 5 г соли 495, 5 г воды Смесь хлорида и гидрокарбоната натрия массой 15 г обработали уксусной кислотой, при этом выделилось 2, 8 л (н. у. ) газа. Определите массовые доли в процентах компонентов смеси. 70% Na. HCO 3 30% Na. Cl Хлорид калия — очень ценное минеральное удобрение. Рассчитайте массовую долю калия (%) в этом веществе. 52% Тривиальные названия солей: Поваренная сольответ. Раствор хлорида натрия (0, 9%) применяется в медицине. Такой раствор называется физиологическим ответ. Питьевая сода применяется в кулинарии, для выпечки кондитерских изделий. Хлорид натрия — как добавка к пище ответ. Калийные удобрения играю важную роль в жизни растений. Na. Cl Кристалли-ч еская сода. Na 2 CO 3 *10 H 2 O Питьевая сода Na. HCO 3 поташ. K 2 CO 3 Калийная селитра KNO 3 Глауберова соль Na 2 SO 4 *10 H 2 O
Сколько воды и хлорида натрия нужно взять для приготовления физиологического раствора массой 0, 5 кг? 4, 5 г соли 495, 5 г воды Смесь хлорида и гидрокарбоната натрия массой 15 г обработали уксусной кислотой, при этом выделилось 2, 8 л (н. у. ) газа. Определите массовые доли в процентах компонентов смеси. 70% Na. HCO 3 30% Na. Cl Хлорид калия — очень ценное минеральное удобрение. Рассчитайте массовую долю калия (%) в этом веществе. 52% Тривиальные названия солей: Поваренная сольответ. Раствор хлорида натрия (0, 9%) применяется в медицине. Такой раствор называется физиологическим ответ. Питьевая сода применяется в кулинарии, для выпечки кондитерских изделий. Хлорид натрия — как добавка к пище ответ. Калийные удобрения играю важную роль в жизни растений. Na. Cl Кристалли-ч еская сода. Na 2 CO 3 *10 H 2 O Питьевая сода Na. HCO 3 поташ. K 2 CO 3 Калийная селитра KNO 3 Глауберова соль Na 2 SO 4 *10 H 2 O
 1) Электролиз расплавов соединений щелочных металлов: 2 Ме. Cl = 2 Ме + Cl 2 4 Ме. OH = 4 Ме + 2 Н 2 О + О 2 2) Восстановление оксидов и гидроксидов щелочных металлов: 2 Li 2 O + Si = 4 Li + Si. O 2 KOH + Na = Nа. OH + K Получение щелочных металлов Ванна состоит из стального кожуха с шамотной футеровкой, графитовым анодом А и кольцевым железный катодом К, между которыми расположена сетчатая диафрагма. Электролитом служит более легкоплавкая смесь его с 25% Na. F и 12% КСl (что позволяет проводить процесс при 610– 650°С). Металлический натрий собирается в верхней части кольцевого катодного пространства, откуда и переходит в сборник. По мере хода электролиза в ванну добавляют Na. Cl. Схема электролизера для получения натрия. Получение щелочных металлов
1) Электролиз расплавов соединений щелочных металлов: 2 Ме. Cl = 2 Ме + Cl 2 4 Ме. OH = 4 Ме + 2 Н 2 О + О 2 2) Восстановление оксидов и гидроксидов щелочных металлов: 2 Li 2 O + Si = 4 Li + Si. O 2 KOH + Na = Nа. OH + K Получение щелочных металлов Ванна состоит из стального кожуха с шамотной футеровкой, графитовым анодом А и кольцевым железный катодом К, между которыми расположена сетчатая диафрагма. Электролитом служит более легкоплавкая смесь его с 25% Na. F и 12% КСl (что позволяет проводить процесс при 610– 650°С). Металлический натрий собирается в верхней части кольцевого катодного пространства, откуда и переходит в сборник. По мере хода электролиза в ванну добавляют Na. Cl. Схема электролизера для получения натрия. Получение щелочных металлов
 Соединения щелочных металлов 1. Гидроксиды: Na. OH – едкий натр, каустическая сода, каустик КОН – едкое кали 2. Соли: Na 2 CO 3 • 10 Н 2 О – кристаллическая сода Na. HCO 3 – пищевая сода К 2 СО 3 – поташ Na 2 SO 4 • 10 H 2 O – глауберова соль
Соединения щелочных металлов 1. Гидроксиды: Na. OH – едкий натр, каустическая сода, каустик КОН – едкое кали 2. Соли: Na 2 CO 3 • 10 Н 2 О – кристаллическая сода Na. HCO 3 – пищевая сода К 2 СО 3 – поташ Na 2 SO 4 • 10 H 2 O – глауберова соль
 Физические свойства щелочных металлов Щелочные металлы — серебристо–белые вещества, за исключением цезия — серебристо-желтого цвета, с металлическим блеском. Все щелочные металлы характеризуются малой плотностью, малой твердостью, низкими температурами плавления и кипения и хорошей электропроводностью. Благодаря малой плотности Li, Na и К всплывают на воде (Li–даже на керосине). Щелочные металлы легко режутся ножом. Несветящееся пламя газовой горелки щелочные металлы и их летучие соединения окрашивают в характерные цвета: Li – в карминово–красный, Na – в желтый, К – фиолетовый , Rb — красный и Cs – в фиолетово-синий. Заполни пропуски
Физические свойства щелочных металлов Щелочные металлы — серебристо–белые вещества, за исключением цезия — серебристо-желтого цвета, с металлическим блеском. Все щелочные металлы характеризуются малой плотностью, малой твердостью, низкими температурами плавления и кипения и хорошей электропроводностью. Благодаря малой плотности Li, Na и К всплывают на воде (Li–даже на керосине). Щелочные металлы легко режутся ножом. Несветящееся пламя газовой горелки щелочные металлы и их летучие соединения окрашивают в характерные цвета: Li – в карминово–красный, Na – в желтый, К – фиолетовый , Rb — красный и Cs – в фиолетово-синий. Заполни пропуски
 1. В ряду от лития к францию атомный радиус: уменьшается не изменяется увеличивается 2. Степень окисления щелочных металлов равна: +1 -1 +2 3. Цвет пламени, в который его окрашивают ионы натрия фиолетовый красный желтый 4. Соединение Na. OH называется. каустическая сода поташ кристаллическая сода проверить Тест «Щелочные металлы»
1. В ряду от лития к францию атомный радиус: уменьшается не изменяется увеличивается 2. Степень окисления щелочных металлов равна: +1 -1 +2 3. Цвет пламени, в который его окрашивают ионы натрия фиолетовый красный желтый 4. Соединение Na. OH называется. каустическая сода поташ кристаллическая сода проверить Тест «Щелочные металлы»
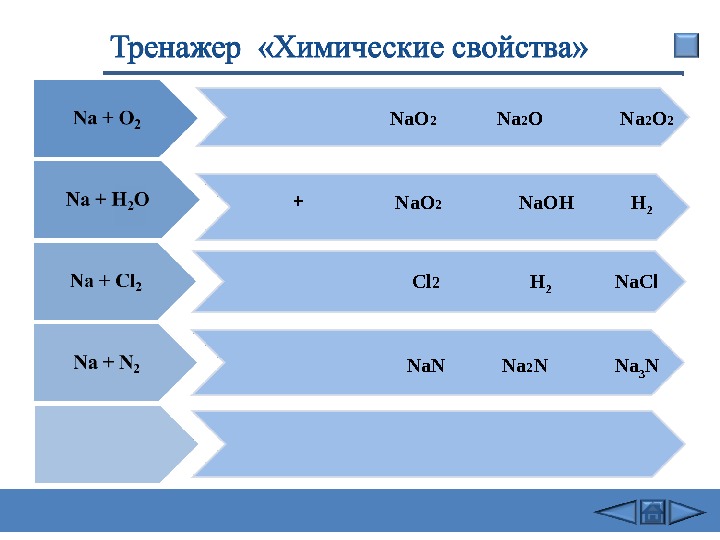
 + N а. О 2 N а 2 O 2 N а. ОН Na. C l Na 2 N Na 3 NN а. О 2 Cl 2 Na. N Na 2 O H
+ N а. О 2 N а 2 O 2 N а. ОН Na. C l Na 2 N Na 3 NN а. О 2 Cl 2 Na. N Na 2 O H
 Проверь себя: ☺☺ Вычеркните неверное суждение о щелочных металлах: 1. 1. Число электронов на внешнем энергетическом уровне щелочных металлов равно 1. 2. 2. В реакциях щелочные металлы являются окислителями и восстановителями. 3. 3. При взаимодействии натрия с кислородом образуется пероксид натрия 4. 4. Щелочные металлы – это металлы IA IA группы Периодической системы химических элементов. 5. 5. Щелочные металлы получают электролизом расплавов их солей. 6. 6. Щелочные металлы не взаимодействуют с водой. 7. 7. Качественной реакцией на ионы щелочных металлов является их взаимодействие с кислородом. 8. 8. При переходе от лития к калию уменьшается радиус атома
Проверь себя: ☺☺ Вычеркните неверное суждение о щелочных металлах: 1. 1. Число электронов на внешнем энергетическом уровне щелочных металлов равно 1. 2. 2. В реакциях щелочные металлы являются окислителями и восстановителями. 3. 3. При взаимодействии натрия с кислородом образуется пероксид натрия 4. 4. Щелочные металлы – это металлы IA IA группы Периодической системы химических элементов. 5. 5. Щелочные металлы получают электролизом расплавов их солей. 6. 6. Щелочные металлы не взаимодействуют с водой. 7. 7. Качественной реакцией на ионы щелочных металлов является их взаимодействие с кислородом. 8. 8. При переходе от лития к калию уменьшается радиус атома
 От лития к францию у атомов щелочных металлов увеличивается Более сильным восстановителем, чем К будет Активнее всех с водой будет взаимодействовать Na может реагировать со всеми веществами группы Щелочные металлы находятся в природе в виде… число валентных электронов восстановительные свойства Электроотрицательность окислительные свойства Rb Li Ca Na Rb Na Li Cs С a, H 2 O, Cl 2 N 2 , H 2 O CO 2 , H 2 , C Na. OH, O 2 , S оксидов сульфидов солей в свободном виде
От лития к францию у атомов щелочных металлов увеличивается Более сильным восстановителем, чем К будет Активнее всех с водой будет взаимодействовать Na может реагировать со всеми веществами группы Щелочные металлы находятся в природе в виде… число валентных электронов восстановительные свойства Электроотрицательность окислительные свойства Rb Li Ca Na Rb Na Li Cs С a, H 2 O, Cl 2 N 2 , H 2 O CO 2 , H 2 , C Na. OH, O 2 , S оксидов сульфидов солей в свободном виде

