Развитие периодического закона.pptx
- Количество слайдов: 10
 Презентация на тему: «Развитие периодического закона» Исполнитель: Кукарская Валерия
Презентация на тему: «Развитие периодического закона» Исполнитель: Кукарская Валерия
 Введение • Периодический закон Д. И. Менделеева — фундаментальный закон, устанавливающий периодическое изменение свойств химических элементов в зависимости от увеличения зарядов ядер их атомов. Открыт Д. И. Менделеевым в марте 1869 года при сопоставлении свойств всех известных в то время элементов и величин их атомных масс. Термин «периодический закон» Менделеев впервые употребил в ноябре 1870, а в октябре 1871 дал окончательную формулировку Периодического закона : «свойства простых тел, а также формы и свойства соединений элементов, а потому и свойства образуемых ими простых и сложных тел, стоят в периодической зависимости от их атомного веса» . Графическим (табличным) выражением периодического закона является разработанная Менделеевым периодическая система элементов.
Введение • Периодический закон Д. И. Менделеева — фундаментальный закон, устанавливающий периодическое изменение свойств химических элементов в зависимости от увеличения зарядов ядер их атомов. Открыт Д. И. Менделеевым в марте 1869 года при сопоставлении свойств всех известных в то время элементов и величин их атомных масс. Термин «периодический закон» Менделеев впервые употребил в ноябре 1870, а в октябре 1871 дал окончательную формулировку Периодического закона : «свойства простых тел, а также формы и свойства соединений элементов, а потому и свойства образуемых ими простых и сложных тел, стоят в периодической зависимости от их атомного веса» . Графическим (табличным) выражением периодического закона является разработанная Менделеевым периодическая система элементов.
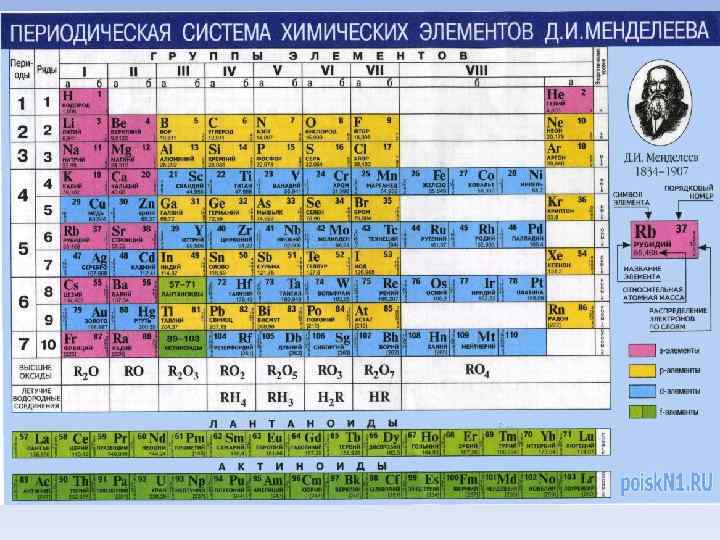
 Развитие: • Формулировка Менделеевым периодического закона и построение периодической таблицы означали лишь начало развития учения о периодичности свойств элементов. Предсказания Менделеева вначале были встречены с известным скепсисом; лишь после того, как были открыты предсказанные элементы, и обнаружено совпадение их реальных свойств с предсказанными, периодический закон был признан в качестве одного из фундаментальных законов химии. В развитии периодического закона принято выделять два этапа – химический и физический. • Химический этап развития периодического закона начался с открытия предсказанных элементов.
Развитие: • Формулировка Менделеевым периодического закона и построение периодической таблицы означали лишь начало развития учения о периодичности свойств элементов. Предсказания Менделеева вначале были встречены с известным скепсисом; лишь после того, как были открыты предсказанные элементы, и обнаружено совпадение их реальных свойств с предсказанными, периодический закон был признан в качестве одного из фундаментальных законов химии. В развитии периодического закона принято выделять два этапа – химический и физический. • Химический этап развития периодического закона начался с открытия предсказанных элементов.
 • В 1875 г. французский химик Поль Эмиль Лекок де Буабодран открыл новый элемент, который был назван галлием. Менделеев сразу же указал, что галлий представляет собой экаалюминий. Дальнейшие исследования полностью подтвердили это, причём оказалось, что Менделеев предсказал плотность галлия точнее, чем Лекок де Буабодран экспериментально определил её. • В 1879 г. шведский химик Ларс Фредерик Нильсон опубликовал сообщение об открытии скандия. Свойства скандия в точности соответствовали свойствам менделеевского экабора. • В 1886 г. немецкий химик Клеменс Александр Винклер открыл германий. Исследование свойств нового элемента показало, что он полностью идентичен с экасилицием Менделеева. • Полное подтверждение предсказаний Менделеева означало торжество периодического закона. С середины 1880 -х годов учение о периодичности было окончательно признано в качестве одной из основ теоретической химии.
• В 1875 г. французский химик Поль Эмиль Лекок де Буабодран открыл новый элемент, который был назван галлием. Менделеев сразу же указал, что галлий представляет собой экаалюминий. Дальнейшие исследования полностью подтвердили это, причём оказалось, что Менделеев предсказал плотность галлия точнее, чем Лекок де Буабодран экспериментально определил её. • В 1879 г. шведский химик Ларс Фредерик Нильсон опубликовал сообщение об открытии скандия. Свойства скандия в точности соответствовали свойствам менделеевского экабора. • В 1886 г. немецкий химик Клеменс Александр Винклер открыл германий. Исследование свойств нового элемента показало, что он полностью идентичен с экасилицием Менделеева. • Полное подтверждение предсказаний Менделеева означало торжество периодического закона. С середины 1880 -х годов учение о периодичности было окончательно признано в качестве одной из основ теоретической химии.

 • Тем не менее, в периодическом законе оставались некоторые проблемы. Предстояло определиться с местом в периодической таблице для двух групп элементов – инертных газов, имеющих нулевую валентность, и тринадцати редкоземельных элементов. . В 1900 -1902 гг. Д. И. Менделеев, Уильям Рамзай, первооткрыватель инертных газов, и Богуслав Браунер произвели модернизацию периодической таблицы. Менделеев и Рамзай пришли к выводу о необходимости образования в таблице нулевой группы элементов, в которую вошли инертные газы. Нулевая группа прекрасно вписалась в периодическую таблицу; инертный газ явился элементом, переходным между галогенами и щелочными металлами. Браунер предложил решение проблемы размещения в таблице редкоземельных элементов. Таким образом, все эти элементы, очень подобные один другому, стали бы на том месте в 4 группе восьмого ряда, которое до сих пор занимал церий. . . Элементы редких земель создали бы особую интерпериодическую группу, аналогичную до некоторой степени восьмой группе, поместившись в середине остальных групп периодической системы. . . " Шестой период таблицы, таким образом, должен быть длиннее, чем четвёртый и пятый, которые в свою очередь длиннее, чем второй и третий периоды. В коротком варианте периодической таблицы Браунер предложил поместить все РЗЭ в одну клетку четвёртой группы.
• Тем не менее, в периодическом законе оставались некоторые проблемы. Предстояло определиться с местом в периодической таблице для двух групп элементов – инертных газов, имеющих нулевую валентность, и тринадцати редкоземельных элементов. . В 1900 -1902 гг. Д. И. Менделеев, Уильям Рамзай, первооткрыватель инертных газов, и Богуслав Браунер произвели модернизацию периодической таблицы. Менделеев и Рамзай пришли к выводу о необходимости образования в таблице нулевой группы элементов, в которую вошли инертные газы. Нулевая группа прекрасно вписалась в периодическую таблицу; инертный газ явился элементом, переходным между галогенами и щелочными металлами. Браунер предложил решение проблемы размещения в таблице редкоземельных элементов. Таким образом, все эти элементы, очень подобные один другому, стали бы на том месте в 4 группе восьмого ряда, которое до сих пор занимал церий. . . Элементы редких земель создали бы особую интерпериодическую группу, аналогичную до некоторой степени восьмой группе, поместившись в середине остальных групп периодической системы. . . " Шестой период таблицы, таким образом, должен быть длиннее, чем четвёртый и пятый, которые в свою очередь длиннее, чем второй и третий периоды. В коротком варианте периодической таблицы Браунер предложил поместить все РЗЭ в одну клетку четвёртой группы.
 • Модернизация периодической системы в начале XX века завершила химический этап её развития. Химия в принципе не могла объяснить причину периодичности свойств элементов и их соединений. Дальнейшее развитие периодического закона в XX веке связано с блестящими успехами физики, приведшими к революционным изменениям в естествознании.
• Модернизация периодической системы в начале XX века завершила химический этап её развития. Химия в принципе не могла объяснить причину периодичности свойств элементов и их соединений. Дальнейшее развитие периодического закона в XX веке связано с блестящими успехами физики, приведшими к революционным изменениям в естествознании.
 Физический этап развития периодического закона можно в свою очередь разделить на несколько стадий: • 1. Установление делимости атома на основании открытия электрона и радиоактивности (1896 – 1897); • 2. Разработка моделей строения атома (1911 – 1913); • 3. Открытие и разработка системы изотопов (1913); • 4. Открытие закона Мозли (1913), позволяющего экспериментально определять заряд ядра и номер элемента в периодической системе; • 5. Разработка теории периодической системы на основании представлений о строении электронных оболочек атомов (1921 – 1925); • 6. Создание основ квантовой теории периодической системы (1926 – 1932).
Физический этап развития периодического закона можно в свою очередь разделить на несколько стадий: • 1. Установление делимости атома на основании открытия электрона и радиоактивности (1896 – 1897); • 2. Разработка моделей строения атома (1911 – 1913); • 3. Открытие и разработка системы изотопов (1913); • 4. Открытие закона Мозли (1913), позволяющего экспериментально определять заряд ядра и номер элемента в периодической системе; • 5. Разработка теории периодической системы на основании представлений о строении электронных оболочек атомов (1921 – 1925); • 6. Создание основ квантовой теории периодической системы (1926 – 1932).
 Рисунок. Первая таблица Д. И. Менделеева
Рисунок. Первая таблица Д. И. Менделеева


