растворы 1.ppt
- Количество слайдов: 40
 Презентация курса лекций Растворы и дисперсные системы к. т. н. Вострикова Н. М. 1
Презентация курса лекций Растворы и дисперсные системы к. т. н. Вострикова Н. М. 1
 Курс лекций Неорганическая химия План 1. 2. 3. 4. 5. 6. 7. 8. 9. 10. 11. 12. Понятие «раствор» Дисперность систем Классификация растворов Теории растворов: физическая и химическая Концентрация растворов Растворы неэлектролитов Растворы электролитов. Теория ЭД Аррениуса. Электролитическая диссоциация воды Ионно-обменные реакции Гетерогенные равновесные системы Гидролиз солей: по катиону; по аниону; по катиону и аниону 1. Гидролиз ковалентных соединений 2. Реакции обмена, сопровождающиеся гидролизом Протолитическая теория растворов 2
Курс лекций Неорганическая химия План 1. 2. 3. 4. 5. 6. 7. 8. 9. 10. 11. 12. Понятие «раствор» Дисперность систем Классификация растворов Теории растворов: физическая и химическая Концентрация растворов Растворы неэлектролитов Растворы электролитов. Теория ЭД Аррениуса. Электролитическая диссоциация воды Ионно-обменные реакции Гетерогенные равновесные системы Гидролиз солей: по катиону; по аниону; по катиону и аниону 1. Гидролиз ковалентных соединений 2. Реакции обмена, сопровождающиеся гидролизом Протолитическая теория растворов 2
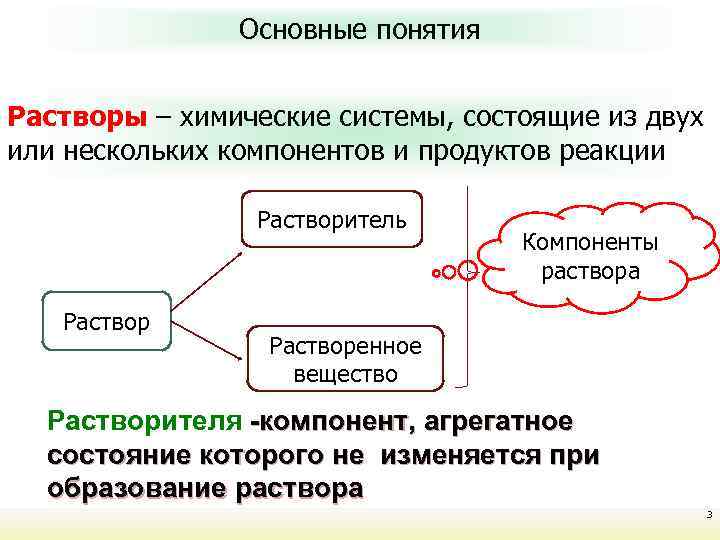 Курс лекций Неорганическая химия Основные понятия Растворы – химические системы, состоящие из двух Растворы – или нескольких компонентов и продуктов реакции Растворитель Раствор Компоненты раствора Растворенное вещество Растворителя -компонент, агрегатное состояние которого не изменяется при образование раствора 3
Курс лекций Неорганическая химия Основные понятия Растворы – химические системы, состоящие из двух Растворы – или нескольких компонентов и продуктов реакции Растворитель Раствор Компоненты раствора Растворенное вещество Растворителя -компонент, агрегатное состояние которого не изменяется при образование раствора 3
 Сходство • С механическими соединениями • С химическими соединениями • Имеют постоянный • Однородны состав • Могут быть легко разделены а составные части • Тепловые эффекты при растворении • Изменение обьема при растворении Растворы занимают промежуточноё положение между химическими соединениями и механическими смесями 2/7/2018 4
Сходство • С механическими соединениями • С химическими соединениями • Имеют постоянный • Однородны состав • Могут быть легко разделены а составные части • Тепловые эффекты при растворении • Изменение обьема при растворении Растворы занимают промежуточноё положение между химическими соединениями и механическими смесями 2/7/2018 4
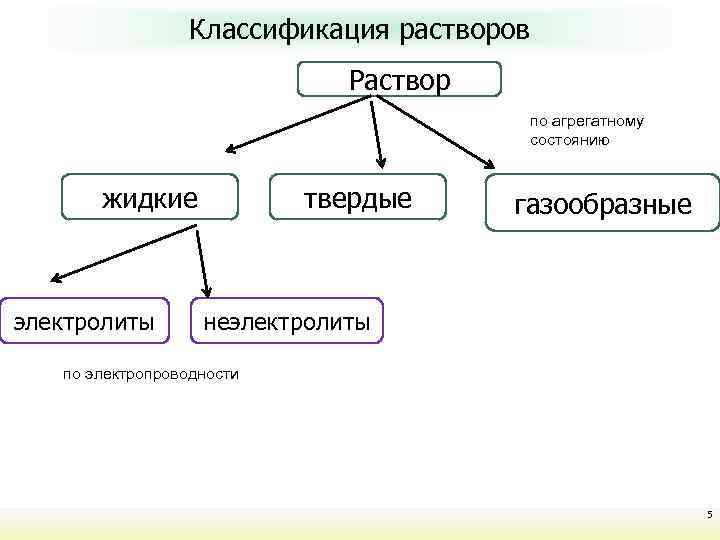 Растворы и дисперсные системы Курс лекций Неорганическая химия Классификация растворов Раствор по агрегатному состоянию жидкие электролиты твердые газообразные неэлектролиты по электропроводности 5
Растворы и дисперсные системы Курс лекций Неорганическая химия Классификация растворов Раствор по агрегатному состоянию жидкие электролиты твердые газообразные неэлектролиты по электропроводности 5
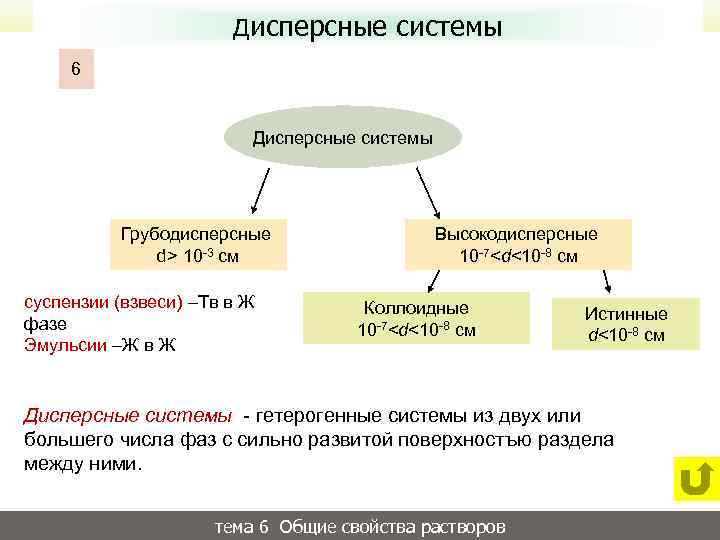 Курс лекций Неорганическая химия Дисперсные системы 6 Дисперсные системы Грубодисперсные d> 10 -3 см суспензии (взвеси) –Тв в Ж фазе Эмульсии –Ж в Ж Высокодисперсные 10 -7
Курс лекций Неорганическая химия Дисперсные системы 6 Дисперсные системы Грубодисперсные d> 10 -3 см суспензии (взвеси) –Тв в Ж фазе Эмульсии –Ж в Ж Высокодисперсные 10 -7
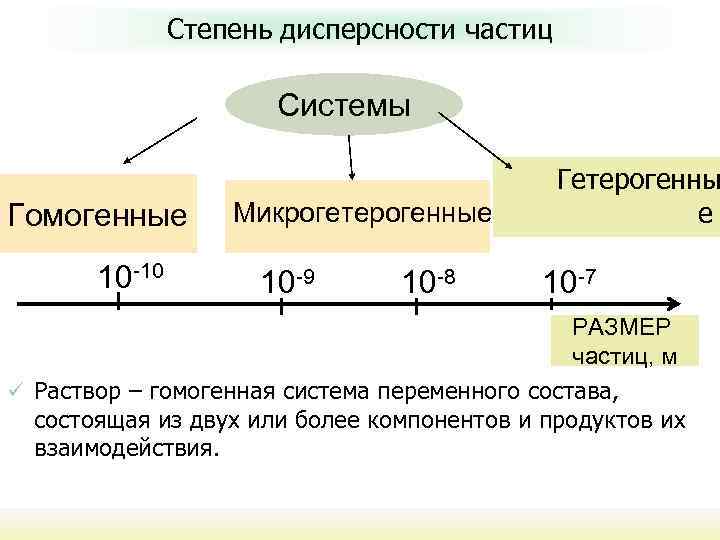 Курс лекций Неорганическая химия Степень дисперсности частиц Системы Гомогенные 10 -10 Микрогетерогенные 10 -9 10 -8 Гетерогенны е 10 -7 РАЗМЕР частиц, м ü Раствор – гомогенная система переменного состава, состоящая из двух или более компонентов и продуктов их взаимодействия.
Курс лекций Неорганическая химия Степень дисперсности частиц Системы Гомогенные 10 -10 Микрогетерогенные 10 -9 10 -8 Гетерогенны е 10 -7 РАЗМЕР частиц, м ü Раствор – гомогенная система переменного состава, состоящая из двух или более компонентов и продуктов их взаимодействия.
 Курс лекций Неорганическая химия Смеси раствор Fe. CI 3 +H 2 O Cu. SO 4 +H 2 O суспензия Известковое молоко ил в речной воде эмульсии Водоэмульсионная краска молоко 8
Курс лекций Неорганическая химия Смеси раствор Fe. CI 3 +H 2 O Cu. SO 4 +H 2 O суспензия Известковое молоко ил в речной воде эмульсии Водоэмульсионная краска молоко 8
 Курс лекций Неорганическая химия Теории растворов Физическая ТР Вант-Гофф, Оствальд : Растворы образуются за счет равномерного распределения молекул растворенного вещества среди молекул растворителя Химическая ТР Д. И. Менделеев Растворы как продукты химического взаимодействия молекул растворителя и растворенного вещества. Продукты взаимодействия гидраты (растворитель вода) или сольваты. Na. Cl(к) + n H 2 O(ж) Na+(H 2 O)х + Cl- (H 2 O)n-x, 9
Курс лекций Неорганическая химия Теории растворов Физическая ТР Вант-Гофф, Оствальд : Растворы образуются за счет равномерного распределения молекул растворенного вещества среди молекул растворителя Химическая ТР Д. И. Менделеев Растворы как продукты химического взаимодействия молекул растворителя и растворенного вещества. Продукты взаимодействия гидраты (растворитель вода) или сольваты. Na. Cl(к) + n H 2 O(ж) Na+(H 2 O)х + Cl- (H 2 O)n-x, 9
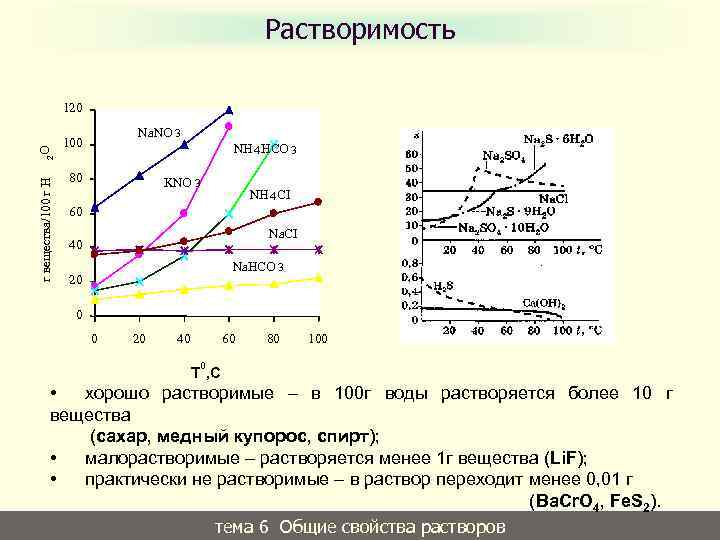 Растворимость г вещества/100 г Н 2 О 120 Na. NO 3 100 NH 4 HCO 3 80 KNO 3 NH 4 CI 60 Na. CI 40 Na. HCO 3 20 0 0 20 40 60 80 100 0 Т , С • хорошо растворимые – в 100 г воды растворяется более 10 г вещества (сахар, медный купорос, спирт); • малорастворимые – растворяется менее 1 г вещества (Li. F); • практически не растворимые – в раствор переходит менее 0, 01 г (Ba. Cr. O 4, Fe. S 2). тема 6 Общие свойства растворов 10
Растворимость г вещества/100 г Н 2 О 120 Na. NO 3 100 NH 4 HCO 3 80 KNO 3 NH 4 CI 60 Na. CI 40 Na. HCO 3 20 0 0 20 40 60 80 100 0 Т , С • хорошо растворимые – в 100 г воды растворяется более 10 г вещества (сахар, медный купорос, спирт); • малорастворимые – растворяется менее 1 г вещества (Li. F); • практически не растворимые – в раствор переходит менее 0, 01 г (Ba. Cr. O 4, Fe. S 2). тема 6 Общие свойства растворов 10
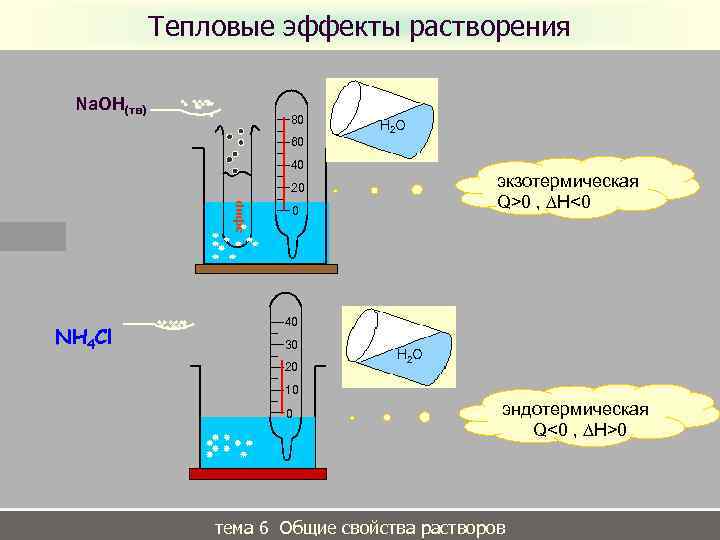 Тепловые эффекты растворения Na. OH(тв) 80 Н 2 О 60 40 экзотермическая Q>0 , ∆H<0 эфир 20 NH 4 Cl 0 40 30 20 Н 2 О 10 0 эндотермическая Q<0 , ∆H>0 Тема 1. элементы химическойрастворов тема 6 Общие свойства термодинамики 11
Тепловые эффекты растворения Na. OH(тв) 80 Н 2 О 60 40 экзотермическая Q>0 , ∆H<0 эфир 20 NH 4 Cl 0 40 30 20 Н 2 О 10 0 эндотермическая Q<0 , ∆H>0 Тема 1. элементы химическойрастворов тема 6 Общие свойства термодинамики 11
 Качественная характеристика растворов Растворимостью называется способность вещества растворяться в том или ином растворителе. üраствор, находящийся в равновесии с растворённым веществом насыщенные ü это раствор, содержащий при заданной температуре меньше растворенного вещества, чем должен содержать насыщенный раствор ненасыщенные üэто раствор, содержащий при заданной температуре больше растворенного вещества, чем должен содержать насыщенный раствор пересыщенные 12
Качественная характеристика растворов Растворимостью называется способность вещества растворяться в том или ином растворителе. üраствор, находящийся в равновесии с растворённым веществом насыщенные ü это раствор, содержащий при заданной температуре меньше растворенного вещества, чем должен содержать насыщенный раствор ненасыщенные üэто раствор, содержащий при заданной температуре больше растворенного вещества, чем должен содержать насыщенный раствор пересыщенные 12
 Концентрация растворов Массовая доля-отношение массы компонента раствора к общей массе раствора Объемная доля-отношение объема компонента раствора к общему объему раствора Молярная доля-отношение количества вещества компонента раствора к общему количеству веществ в растворе = тема 6 Общие свойства растворов 13
Концентрация растворов Массовая доля-отношение массы компонента раствора к общей массе раствора Объемная доля-отношение объема компонента раствора к общему объему раствора Молярная доля-отношение количества вещества компонента раствора к общему количеству веществ в растворе = тема 6 Общие свойства растворов 13
 Молярная концентрация растворов это отношение количества растворенного вещества к объему раствора Вычислить молярность раствора, если 23, 4 г Na 2 SO 4 растворено в 125 мл раствора. 1 М-молярный 0, 1 М- децимолярный 0, 01 М-сантимолярный 0, 001 М-миллимолярный тема 6 Общие свойства растворов 14
Молярная концентрация растворов это отношение количества растворенного вещества к объему раствора Вычислить молярность раствора, если 23, 4 г Na 2 SO 4 растворено в 125 мл раствора. 1 М-молярный 0, 1 М- децимолярный 0, 01 М-сантимолярный 0, 001 М-миллимолярный тема 6 Общие свойства растворов 14
 Молярная концентрация эквивалентов Количество эквивалентов вещества Х Молярная масса эквивалента вещества Х Эквивалентом (1/ZX ) называют условную частицу вещества Х, которая эквивалентна одному иону водорода в кислотно-основной реакции или одному электрону в окислительно-восстановительной реакции. Фактор эквивалентности (fэкв (Х) )– это число, показывающее, какая доля реальной частицы вещества Х эквивалентна одному иону водорода в кислотно-основной реакции или одному электрону в окислительно-восстановительной реакции. Mn. O 4 - + 8 H+ + 5ē = Mn 2+ + 4 H 2 O fэкв (KMn. O 4)=1|5 Na 2 CO 3 + 2 HCl = 2 Na. Cl + H 2 О+ CO 2 fэкв Na 2 CO 3)=1|2 15
Молярная концентрация эквивалентов Количество эквивалентов вещества Х Молярная масса эквивалента вещества Х Эквивалентом (1/ZX ) называют условную частицу вещества Х, которая эквивалентна одному иону водорода в кислотно-основной реакции или одному электрону в окислительно-восстановительной реакции. Фактор эквивалентности (fэкв (Х) )– это число, показывающее, какая доля реальной частицы вещества Х эквивалентна одному иону водорода в кислотно-основной реакции или одному электрону в окислительно-восстановительной реакции. Mn. O 4 - + 8 H+ + 5ē = Mn 2+ + 4 H 2 O fэкв (KMn. O 4)=1|5 Na 2 CO 3 + 2 HCl = 2 Na. Cl + H 2 О+ CO 2 fэкв Na 2 CO 3)=1|2 15
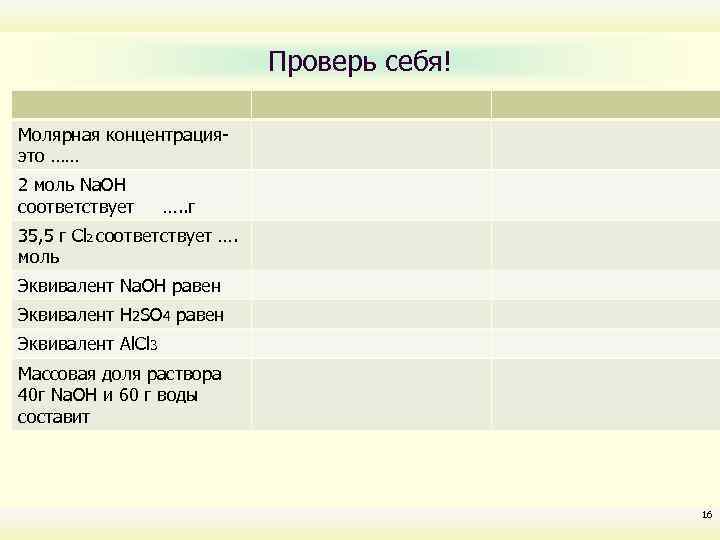 Проверь себя! Молярная концентрацияэто …… 2 моль Na. OH соответствует …. . г 35, 5 г Сl 2 соответствует …. моль Эквивалент Na. OH равен Эквивалент H 2 SO 4 равен Эквивалент Al. Cl 3 Массовая доля раствора 40 г Na. OH и 60 г воды составит 16
Проверь себя! Молярная концентрацияэто …… 2 моль Na. OH соответствует …. . г 35, 5 г Сl 2 соответствует …. моль Эквивалент Na. OH равен Эквивалент H 2 SO 4 равен Эквивалент Al. Cl 3 Массовая доля раствора 40 г Na. OH и 60 г воды составит 16
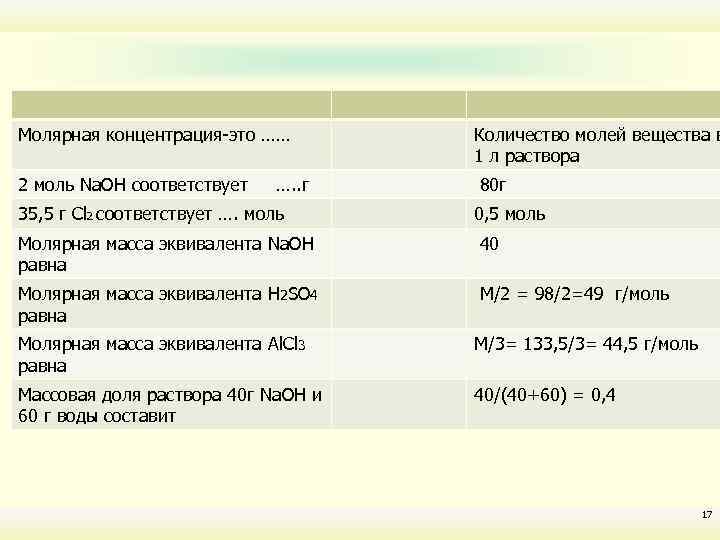 Молярная концентрация-это …… 2 моль Na. OH соответствует …. . г 35, 5 г Сl 2 соответствует …. моль Количество молей вещества в 1 л раствора 80 г 0, 5 моль Молярная масса эквивалента Na. OH равна 40 Молярная масса эквивалента H 2 SO 4 равна М/2 = 98/2=49 г/моль Молярная масса эквивалента Al. Cl 3 равна М/3= 133, 5/3= 44, 5 г/моль Массовая доля раствора 40 г Na. OH и 60 г воды составит 40/(40+60) = 0, 4 17
Молярная концентрация-это …… 2 моль Na. OH соответствует …. . г 35, 5 г Сl 2 соответствует …. моль Количество молей вещества в 1 л раствора 80 г 0, 5 моль Молярная масса эквивалента Na. OH равна 40 Молярная масса эквивалента H 2 SO 4 равна М/2 = 98/2=49 г/моль Молярная масса эквивалента Al. Cl 3 равна М/3= 133, 5/3= 44, 5 г/моль Массовая доля раствора 40 г Na. OH и 60 г воды составит 40/(40+60) = 0, 4 17
 Пример • Определить нормальность 1 М раствора серной кислоты. Фактор эквивалентности равен ½. 18
Пример • Определить нормальность 1 М раствора серной кислоты. Фактор эквивалентности равен ½. 18
 Моляльная концентрация растворов Моляльность раствора - число молей вещества в 1000 г растворителя: В 200 мл Н 2 О растворено 11, 1 г Са. С 12. Найти Сm=? моль/кг , m 2 - масса растворителя, m 1 - масса растворенного вещества. тема 6 Общие свойства растворов 19
Моляльная концентрация растворов Моляльность раствора - число молей вещества в 1000 г растворителя: В 200 мл Н 2 О растворено 11, 1 г Са. С 12. Найти Сm=? моль/кг , m 2 - масса растворителя, m 1 - масса растворенного вещества. тема 6 Общие свойства растворов 19
 Свойства растворов неэлектролитов • Свойства растворов, которые зависят от концентрации растворенных частиц, но не зависят от их составаколлигативные q. Понижение давления пара над раствором q Повышение температуры кипения q Понижение температуры кристаллизации растворов q Осмотическое давление К разбавленным растворам, характеризующих равновесие фазовых переходов р. г. р. т. 20
Свойства растворов неэлектролитов • Свойства растворов, которые зависят от концентрации растворенных частиц, но не зависят от их составаколлигативные q. Понижение давления пара над раствором q Повышение температуры кипения q Понижение температуры кристаллизации растворов q Осмотическое давление К разбавленным растворам, характеризующих равновесие фазовых переходов р. г. р. т. 20
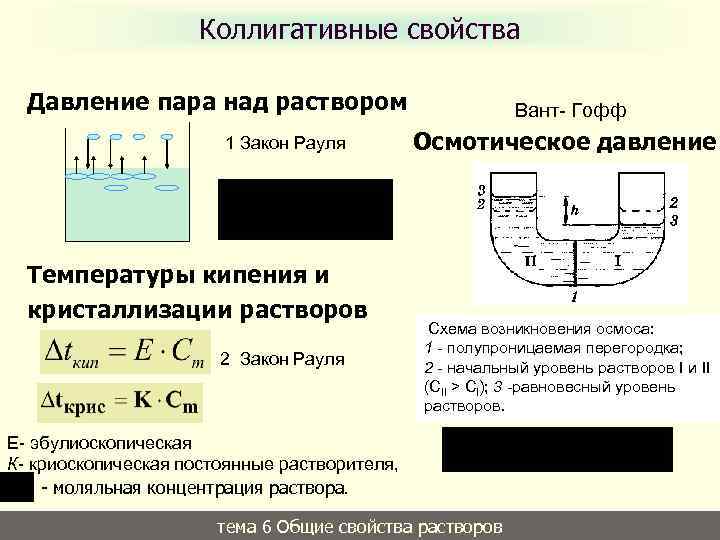 Коллигативные свойства Давление пара над раствором 1 Закон Рауля Температуры кипения и кристаллизации растворов 2 Закон Рауля Вант- Гофф Осмотическое давление Схема возникновения осмоса: 1 - полупроницаемая перегородка; 2 - начальный уровень растворов I и II (СII > CI); 3 -равновесный уровень растворов. Е- эбулиоскопическая К- криоскопическая постоянные растворителя, - моляльная концентрация раствора. тема 6 Общие свойства растворов 21
Коллигативные свойства Давление пара над раствором 1 Закон Рауля Температуры кипения и кристаллизации растворов 2 Закон Рауля Вант- Гофф Осмотическое давление Схема возникновения осмоса: 1 - полупроницаемая перегородка; 2 - начальный уровень растворов I и II (СII > CI); 3 -равновесный уровень растворов. Е- эбулиоскопическая К- криоскопическая постоянные растворителя, - моляльная концентрация раствора. тема 6 Общие свойства растворов 21
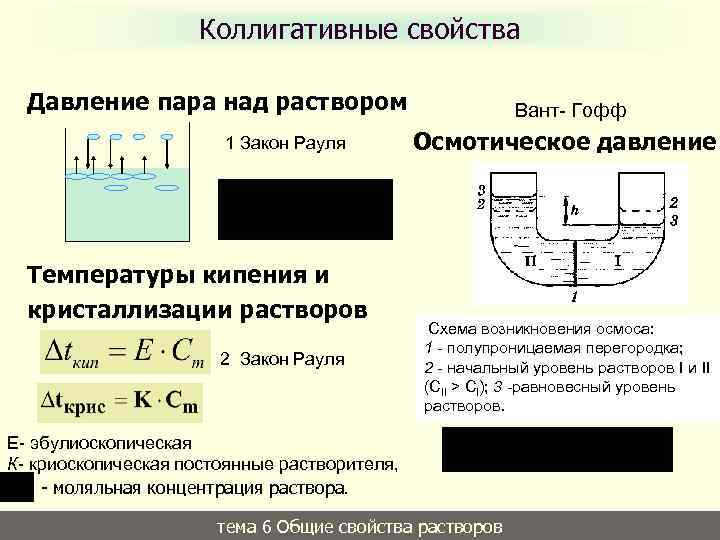 Коллигативные свойства Давление пара над раствором 1 Закон Рауля Температуры кипения и кристаллизации растворов 2 Закон Рауля Вант- Гофф Осмотическое давление Схема возникновения осмоса: 1 - полупроницаемая перегородка; 2 - начальный уровень растворов I и II (СII > CI); 3 -равновесный уровень растворов. Е- эбулиоскопическая К- криоскопическая постоянные растворителя, - моляльная концентрация раствора. тема 6 Общие свойства растворов 22
Коллигативные свойства Давление пара над раствором 1 Закон Рауля Температуры кипения и кристаллизации растворов 2 Закон Рауля Вант- Гофф Осмотическое давление Схема возникновения осмоса: 1 - полупроницаемая перегородка; 2 - начальный уровень растворов I и II (СII > CI); 3 -равновесный уровень растворов. Е- эбулиоскопическая К- криоскопическая постоянные растворителя, - моляльная концентрация раствора. тема 6 Общие свойства растворов 22
 Электролиты Это вещества, которые в растворенном или расплавленном состоянии проводят электрический ток. Это растворы - А + + анион - + - катион - + + _ К - щелочей, солей и неорганических кислот в воде, растворы ряда солей в органических растворителях _ _ _ 1859 г. Ионные равновесия в растворах электролитов 23
Электролиты Это вещества, которые в растворенном или расплавленном состоянии проводят электрический ток. Это растворы - А + + анион - + - катион - + + _ К - щелочей, солей и неорганических кислот в воде, растворы ряда солей в органических растворителях _ _ _ 1859 г. Ионные равновесия в растворах электролитов 23
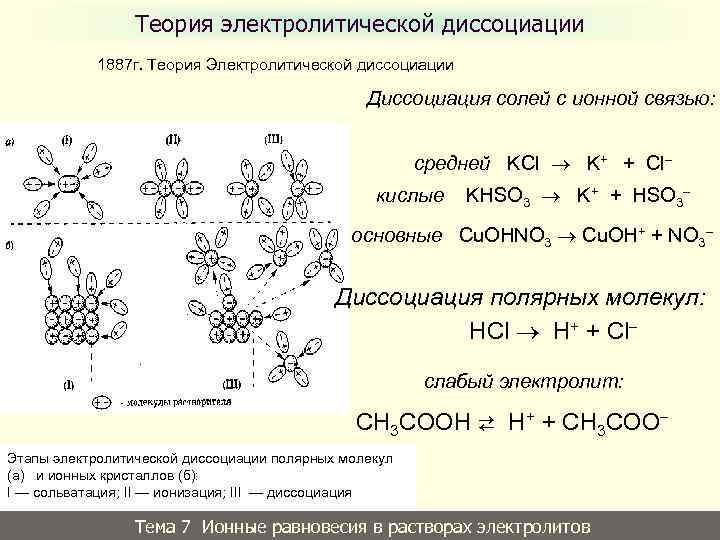 Теория электролитической диссоциации 1887 г. Теория Электролитической диссоциации Диссоциация солей с ионной связью: средней KCl K+ + Cl кислые KHSO 3 K+ + HSO 3 основные Cu. OHNO 3 Cu. OH+ + NO 3 Диссоциация полярных молекул: HCl H+ + Cl слабый электролит: СH 3 CОOН ⇄ H+ + СH 3 CОО Этапы электролитической диссоциации полярных молекул (а) и ионных кристаллов (б): I — сольватация; II — ионизация; III — диссоциация Тема 7 Ионные равновесия в растворах электролитов 24
Теория электролитической диссоциации 1887 г. Теория Электролитической диссоциации Диссоциация солей с ионной связью: средней KCl K+ + Cl кислые KHSO 3 K+ + HSO 3 основные Cu. OHNO 3 Cu. OH+ + NO 3 Диссоциация полярных молекул: HCl H+ + Cl слабый электролит: СH 3 CОOН ⇄ H+ + СH 3 CОО Этапы электролитической диссоциации полярных молекул (а) и ионных кристаллов (б): I — сольватация; II — ионизация; III — диссоциация Тема 7 Ионные равновесия в растворах электролитов 24
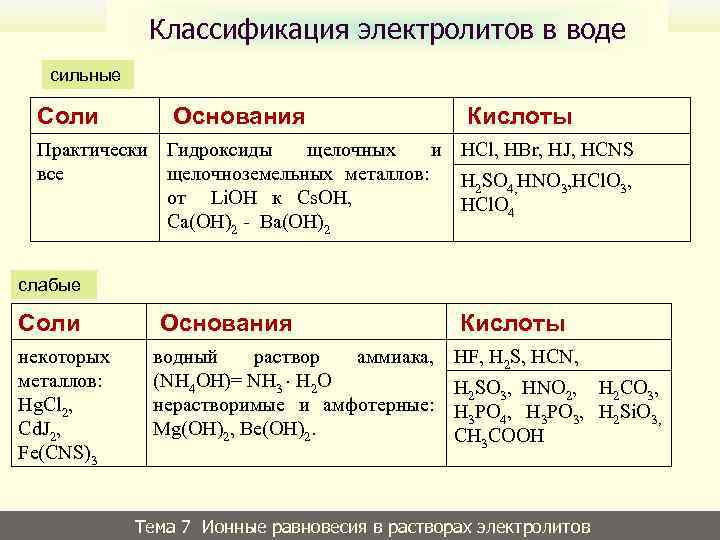 Классификация электролитов в воде сильные Соли Основания Кислоты Практически Гидроксиды щелочных и HCl, HBr, HJ, HCNS все щелочноземельных металлов: H 2 SO 4, HNO 3, HCl. О 3, от Li. ОН к Cs. ОН, НCl. O 4 Са(ОН)2 - Ba(ОН)2 слабые Соли некоторых металлов: Hg. Cl 2, Cd. J 2, Fe(CNS)3 Основания водный раствор аммиака, (NH 4 OH)= NH 3 H 2 O нерастворимые и амфотерные: Mg(OH)2, Be(OH)2. Кислоты HF, H 2 S, HCN, H 2 SO 3, HNO 2, H 2 CO 3, H 3 PO 4, H 3 PO 3, H 2 Si. O 3, CH 3 COOH Тема 7 Ионные равновесия в растворах электролитов 25
Классификация электролитов в воде сильные Соли Основания Кислоты Практически Гидроксиды щелочных и HCl, HBr, HJ, HCNS все щелочноземельных металлов: H 2 SO 4, HNO 3, HCl. О 3, от Li. ОН к Cs. ОН, НCl. O 4 Са(ОН)2 - Ba(ОН)2 слабые Соли некоторых металлов: Hg. Cl 2, Cd. J 2, Fe(CNS)3 Основания водный раствор аммиака, (NH 4 OH)= NH 3 H 2 O нерастворимые и амфотерные: Mg(OH)2, Be(OH)2. Кислоты HF, H 2 S, HCN, H 2 SO 3, HNO 2, H 2 CO 3, H 3 PO 4, H 3 PO 3, H 2 Si. O 3, CH 3 COOH Тема 7 Ионные равновесия в растворах электролитов 25
 Ионнообменные реакции Необратимые реакции образуется осадок (↓) выделяются газообразные вещества образуется слабый электролит образуются комплексне соединения Ba. Cl 2 + Na 2 SO 4 = Ba. SO 4 ↓ + 2 Na. Cl Na 2 S+ 2 HCl = H 2 S↑ + 2 Na. Cl 2 CH 3 COOK + H 2 SO 4 = 2 CH 3 COOH + K 2 SO 4 Hg(NO 3)2 + 4 KJ = K 2[Hg. J 4] +2 KNO 3 Тема 7: Ионные равновесия в растворах электролитов 26
Ионнообменные реакции Необратимые реакции образуется осадок (↓) выделяются газообразные вещества образуется слабый электролит образуются комплексне соединения Ba. Cl 2 + Na 2 SO 4 = Ba. SO 4 ↓ + 2 Na. Cl Na 2 S+ 2 HCl = H 2 S↑ + 2 Na. Cl 2 CH 3 COOK + H 2 SO 4 = 2 CH 3 COOH + K 2 SO 4 Hg(NO 3)2 + 4 KJ = K 2[Hg. J 4] +2 KNO 3 Тема 7: Ионные равновесия в растворах электролитов 26
 Курс лекций Неорганическая химия Растворы слабых электролитов Диссоциация: H 3 PO 4 ⇄ H 2 PO 4 К 1= 7, 1 10 – 3 = 27% H 2 PO 4 ⇄ HPO 4 К 2= 6. 2 10 – 8 = 0, 15% HPO 42 ⇄ PO 43 К 3 = 5. 0 10 – 13 = 0, 005% n Константа равновесия СН 3 СООН ⇄ Н+ + СН 3 СОО n Закон разбавления Оствальда Зависимости Кд некоторых слабых электролитов в водных растворах от температуры Тема 7 Ионные равновесия в растворах электролитов 27
Курс лекций Неорганическая химия Растворы слабых электролитов Диссоциация: H 3 PO 4 ⇄ H 2 PO 4 К 1= 7, 1 10 – 3 = 27% H 2 PO 4 ⇄ HPO 4 К 2= 6. 2 10 – 8 = 0, 15% HPO 42 ⇄ PO 43 К 3 = 5. 0 10 – 13 = 0, 005% n Константа равновесия СН 3 СООН ⇄ Н+ + СН 3 СОО n Закон разбавления Оствальда Зависимости Кд некоторых слабых электролитов в водных растворах от температуры Тема 7 Ионные равновесия в растворах электролитов 27
 Курс лекций Неорганическая химия Диссоциация воды Н 2 О ⇄ Н+ + ОН− K w =[Н+] [ОН−] = 10− 14 Ig[Н+]+lg[ОН−] = lg 10− 14 Ig[Н+]+lg[ОН−] = − 14 p. H = −Ig[Н+] p. OH= −lg[ОН−] p. H + p. OH = 14 28
Курс лекций Неорганическая химия Диссоциация воды Н 2 О ⇄ Н+ + ОН− K w =[Н+] [ОН−] = 10− 14 Ig[Н+]+lg[ОН−] = lg 10− 14 Ig[Н+]+lg[ОН−] = − 14 p. H = −Ig[Н+] p. OH= −lg[ОН−] p. H + p. OH = 14 28
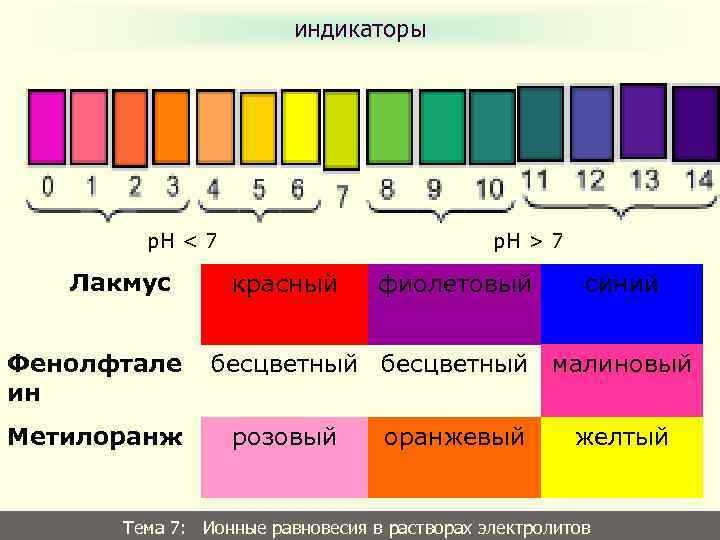 индикаторы р. Н < 7 Лакмус Фенолфтале ин Метилоранж р. Н > 7 красный фиолетовый синий бесцветный малиновый розовый оранжевый желтый Тема: Ионные равновесия в растворах электролитов Тема 7: Равновесия в растворах слабых электролитов 29
индикаторы р. Н < 7 Лакмус Фенолфтале ин Метилоранж р. Н > 7 красный фиолетовый синий бесцветный малиновый розовый оранжевый желтый Тема: Ионные равновесия в растворах электролитов Тема 7: Равновесия в растворах слабых электролитов 29
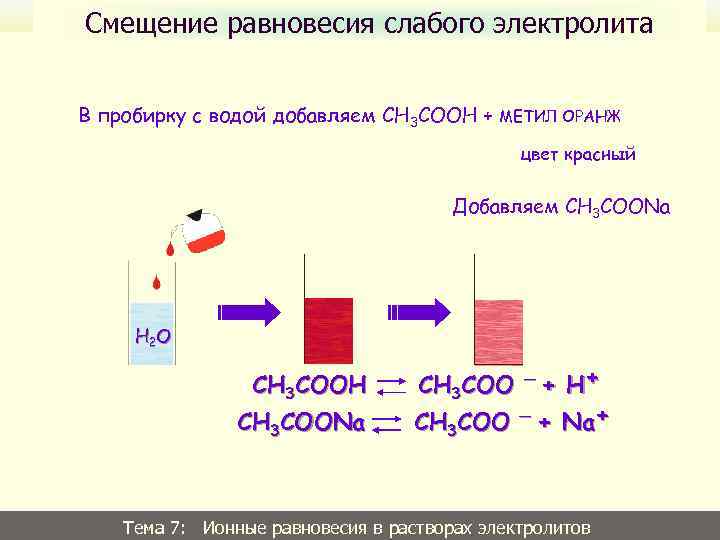 Смещение равновесия слабого электролита В пробирку с водой добавляем CH 3 COOH + МЕТИЛ ОРАНЖ цвет красный Добавляем CH 3 COONa H 2 O CH 3 COOH CH 3 COONa + H+ _ CH 3 COO + Na+ CH 3 COO _ Тема: Ионные равновесия в растворах электролитов Тема 7: Равновесия в растворах слабых электролитов 30
Смещение равновесия слабого электролита В пробирку с водой добавляем CH 3 COOH + МЕТИЛ ОРАНЖ цвет красный Добавляем CH 3 COONa H 2 O CH 3 COOH CH 3 COONa + H+ _ CH 3 COO + Na+ CH 3 COO _ Тема: Ионные равновесия в растворах электролитов Тема 7: Равновесия в растворах слабых электролитов 30
 Раздел 4. Растворы и дисперсные системы Протолитическая теория кислот и оснований - Протон Н+ Н+ основание кислота НСI(г. ) + H 2 О(ж. ) H 3 О+(водн. ) + СI (водн. ) кисл. 1 основ. 2 кисл. 2 основ. 2 Na. OH(т. ) + H 2 O(ж) Na+(вод. ) + OH (вод. ) OH (вод. ) + H 3 O+(водн. ) 2 H 2 O(ж) Кислота – донор катионов водорода: НСl ⇄ H+ + Сl NH 4+ H+ + NH 3 НCO 3 H+ + CO 32 Основание – акцептор катионов водорода: NH 3 + H+ NH 4+ , Аl. ОН 2+ + H+ Аl 3++ H 2 О PO 43 + H+ НPO 42 Тема: Ионные равновесия в растворах электролитов Тема 7: Равновесия в растворах слабых электролитов 31
Раздел 4. Растворы и дисперсные системы Протолитическая теория кислот и оснований - Протон Н+ Н+ основание кислота НСI(г. ) + H 2 О(ж. ) H 3 О+(водн. ) + СI (водн. ) кисл. 1 основ. 2 кисл. 2 основ. 2 Na. OH(т. ) + H 2 O(ж) Na+(вод. ) + OH (вод. ) OH (вод. ) + H 3 O+(водн. ) 2 H 2 O(ж) Кислота – донор катионов водорода: НСl ⇄ H+ + Сl NH 4+ H+ + NH 3 НCO 3 H+ + CO 32 Основание – акцептор катионов водорода: NH 3 + H+ NH 4+ , Аl. ОН 2+ + H+ Аl 3++ H 2 О PO 43 + H+ НPO 42 Тема: Ионные равновесия в растворах электролитов Тема 7: Равновесия в растворах слабых электролитов 31
 Растворы и дисперсные системы Курс лекций Неорганическая химия Гидролиз солей По катиону По аниону по катиону и по аниону совместный Тема 7: Ионные равновесия в растворах электролитов 32
Растворы и дисперсные системы Курс лекций Неорганическая химия Гидролиз солей По катиону По аниону по катиону и по аниону совместный Тема 7: Ионные равновесия в растворах электролитов 32
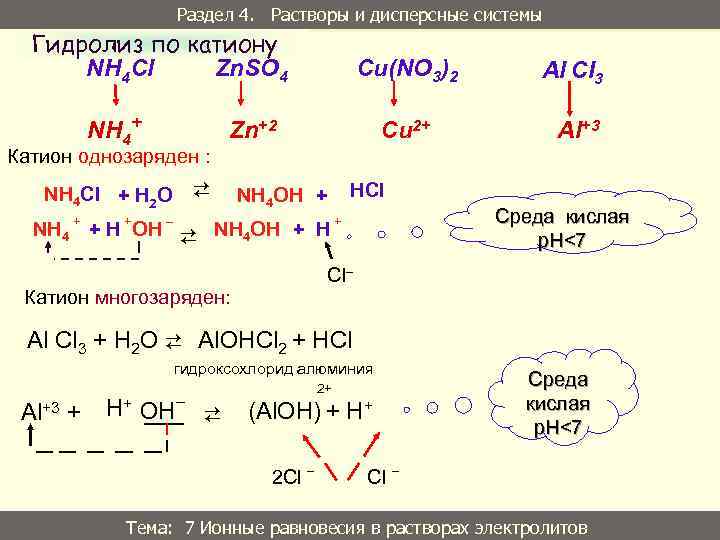 Раздел 4. Растворы и дисперсные системы Гидролиз по катиону NH 4 Cl Zn. SO 4 NH 4+ Cu(NO 3)2 Al CI 3 Cu 2+ Al+3 Zn+2 Катион однозаряден : ⇄ NН 4 Cl + Н 2 O NH 4 + + + H OH HCl NH 4 OH + ⇄ NH 4 OH + H Среда кислая p. H<7 + Cl Катион многозаряден: Al Cl 3 + H 2 O ⇄ Al. OHCl 2 + HCl гидроксохлорид алюминия Al+3 + H+ OH _ Среда кислая p. H<7 2+ ⇄ (Al. OH) + H+ 2 Cl _ Тема: Ионные равновесия в растворах электролитов Тема: 7 Ионные равновесия в растворах электролитов 33
Раздел 4. Растворы и дисперсные системы Гидролиз по катиону NH 4 Cl Zn. SO 4 NH 4+ Cu(NO 3)2 Al CI 3 Cu 2+ Al+3 Zn+2 Катион однозаряден : ⇄ NН 4 Cl + Н 2 O NH 4 + + + H OH HCl NH 4 OH + ⇄ NH 4 OH + H Среда кислая p. H<7 + Cl Катион многозаряден: Al Cl 3 + H 2 O ⇄ Al. OHCl 2 + HCl гидроксохлорид алюминия Al+3 + H+ OH _ Среда кислая p. H<7 2+ ⇄ (Al. OH) + H+ 2 Cl _ Тема: Ионные равновесия в растворах электролитов Тема: 7 Ионные равновесия в растворах электролитов 33
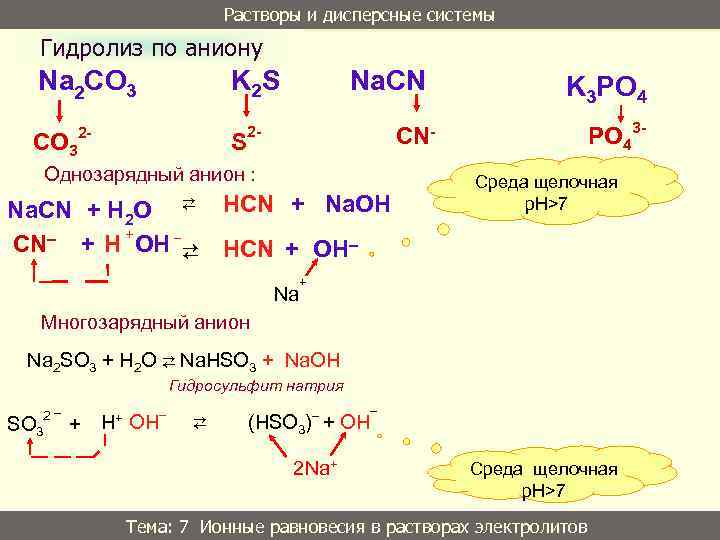 Растворы и дисперсные системы Гидролиз по аниону Na 2 CO 3 K 2 S 2 - 2 - CO 3 S + Н OН ⇄ CN– K 3 PO 43 - CN- Однозарядный анион : Na. СN + Н O ⇄ НСN 2 + Na. СN + Na. OH Среда щелочная p. H>7 НСN + OН Na + Многозарядный анион Na 2 SO 3 + H 2 O ⇄ Na. HSO 3 + Na. OH Гидросульфит натрия SO 3 2 _ + H+ OH ⇄ _ (HSO 3) + OH 2 Na+ _ Среда щелочная p. H>7 Тема: 7 Ионные равновесия в растворах электролитов 34
Растворы и дисперсные системы Гидролиз по аниону Na 2 CO 3 K 2 S 2 - 2 - CO 3 S + Н OН ⇄ CN– K 3 PO 43 - CN- Однозарядный анион : Na. СN + Н O ⇄ НСN 2 + Na. СN + Na. OH Среда щелочная p. H>7 НСN + OН Na + Многозарядный анион Na 2 SO 3 + H 2 O ⇄ Na. HSO 3 + Na. OH Гидросульфит натрия SO 3 2 _ + H+ OH ⇄ _ (HSO 3) + OH 2 Na+ _ Среда щелочная p. H>7 Тема: 7 Ионные равновесия в растворах электролитов 34
 Растворы и дисперсные системы Гидролиз по катиону и аниону Однозарядный катион и анион : NН 4 СN + Н 2 O ⇄ НСN + NН 4 OН CN– + NН 4+ + Н+OН ⇄ НСN + NН 4 OН Однозарядный катион и многозарядный анион : (NН 4)2 СО 3 + Н 2 О ⇄ NH 4 OH + NН 4 Н СО 3 NH 4+ + СО 32 + HОН ⇄ NH 4 OH + НСО 3 Многозарядный катион и однозарядный анион : Zn(NO 2) 2 + Н 2 О ⇄ Zn. ОНNO 2 + НNO 2 Zn 2+ + NO 2 + HОН ⇄ Zn. ОН+ + HNО 2 Тема: 7 Ионные равновесия в растворах электролитов 35
Растворы и дисперсные системы Гидролиз по катиону и аниону Однозарядный катион и анион : NН 4 СN + Н 2 O ⇄ НСN + NН 4 OН CN– + NН 4+ + Н+OН ⇄ НСN + NН 4 OН Однозарядный катион и многозарядный анион : (NН 4)2 СО 3 + Н 2 О ⇄ NH 4 OH + NН 4 Н СО 3 NH 4+ + СО 32 + HОН ⇄ NH 4 OH + НСО 3 Многозарядный катион и однозарядный анион : Zn(NO 2) 2 + Н 2 О ⇄ Zn. ОНNO 2 + НNO 2 Zn 2+ + NO 2 + HОН ⇄ Zn. ОН+ + HNО 2 Тема: 7 Ионные равновесия в растворах электролитов 35
 Гидролиз по катиону и аниону • Если продукты гидролиза покидают сферу реакции (выпадает осадок, выделяется газ), то гидролиз протекает необратимо: • Al 2 S 3 + 6 H 2 O • 2 Al(OH) 3 + 3 H 2 S Реакции обмена, сопровождающиеся гидролизом: Na 2 Al. Cl 3+3 2 CO 3 + 3 H 2 O 2 Al(OH)3↓ + CO 2 + 6 Na. Cl 3 2 Al 3+ + 6 Cl + 6 Na++ 3 CO 32 + 3 H 2 O 2 Al(OH)3↓ + 3 CO 2 + 6 Na+ + 6 Cl 2 Al 3+ + 3 CO 32 + 3 H 2 O 2 Al(OH)3↓ + 3 CO 2 2 Cu(NO 3)2 + 2 Na 2 CO 3 + H 2 O (Cu. OH)2 CO 3↓ + 4 Na. NO 3 + CO 2 36
Гидролиз по катиону и аниону • Если продукты гидролиза покидают сферу реакции (выпадает осадок, выделяется газ), то гидролиз протекает необратимо: • Al 2 S 3 + 6 H 2 O • 2 Al(OH) 3 + 3 H 2 S Реакции обмена, сопровождающиеся гидролизом: Na 2 Al. Cl 3+3 2 CO 3 + 3 H 2 O 2 Al(OH)3↓ + CO 2 + 6 Na. Cl 3 2 Al 3+ + 6 Cl + 6 Na++ 3 CO 32 + 3 H 2 O 2 Al(OH)3↓ + 3 CO 2 + 6 Na+ + 6 Cl 2 Al 3+ + 3 CO 32 + 3 H 2 O 2 Al(OH)3↓ + 3 CO 2 2 Cu(NO 3)2 + 2 Na 2 CO 3 + H 2 O (Cu. OH)2 CO 3↓ + 4 Na. NO 3 + CO 2 36
 Гидролиз ковалентных соединений q. PCl 3 + 3 H 2 O = H 3 PO 3 + 3 HCl q. P 2 S 5 + 8 H 2 O = 2 H 3 PO 4 + 5 H 2 S 37
Гидролиз ковалентных соединений q. PCl 3 + 3 H 2 O = H 3 PO 3 + 3 HCl q. P 2 S 5 + 8 H 2 O = 2 H 3 PO 4 + 5 H 2 S 37
 Произведение растворимости (ПР) ПР- численно равна произведению концентрации ионов в насыщенном растворе малорастворимого электролита ПР(Ba. SO 4 ) =1 10 10 ПР(Pb. SO 4) =2, 2 10 8 Сравним значения ПР солей: Чем больше ПР, тем больше растворимость Пример 38
Произведение растворимости (ПР) ПР- численно равна произведению концентрации ионов в насыщенном растворе малорастворимого электролита ПР(Ba. SO 4 ) =1 10 10 ПР(Pb. SO 4) =2, 2 10 8 Сравним значения ПР солей: Чем больше ПР, тем больше растворимость Пример 38
 Задача Рассчитать растворимость Pb. Cl 2 в воде, если ПР =1, 7 10 5 Между твердой фазой и ионами в растворе устанавливается равновесие: Pb. Cl 2 ⇄ Pb 2+ + 2 Cl 1 моль 1 моль если обозначить: Х Х Запишем выражение: 2 моль 2 Х ПР = Pb 2+ Cl 2 =1, 7 10 5 или: ПР = Х 2 Х 2 =1, 7 10 5 4 Х 3=1, 7 10 5 Х= 1, 3 10 2 = 0, 013 моль/л Pb 2+ = 1, 3 10 2 моль/л Cl =2, 6 10 2 моль/л 39
Задача Рассчитать растворимость Pb. Cl 2 в воде, если ПР =1, 7 10 5 Между твердой фазой и ионами в растворе устанавливается равновесие: Pb. Cl 2 ⇄ Pb 2+ + 2 Cl 1 моль 1 моль если обозначить: Х Х Запишем выражение: 2 моль 2 Х ПР = Pb 2+ Cl 2 =1, 7 10 5 или: ПР = Х 2 Х 2 =1, 7 10 5 4 Х 3=1, 7 10 5 Х= 1, 3 10 2 = 0, 013 моль/л Pb 2+ = 1, 3 10 2 моль/л Cl =2, 6 10 2 моль/л 39
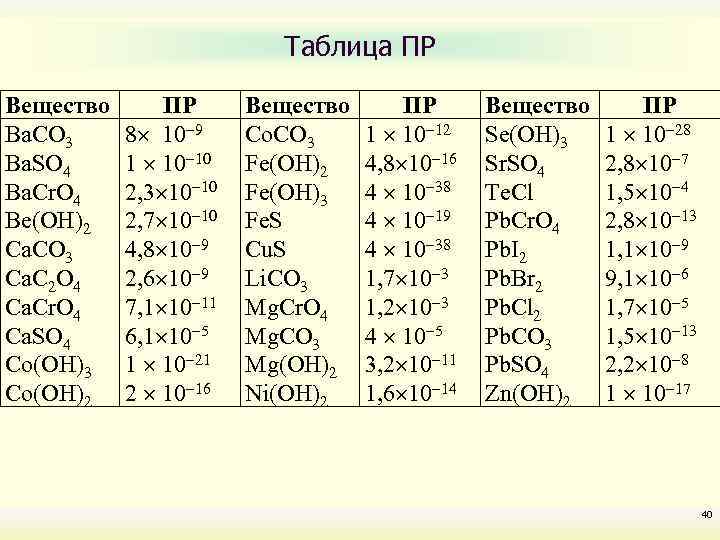 Таблица ПР Вещество Ba. CO 3 Ba. SO 4 Ba. Cr. O 4 Be(OH)2 Ca. CO 3 Ca. C 2 O 4 Ca. Cr. O 4 Ca. SO 4 Co(OH)3 Co(OH)2 ПР 8 10 9 1 10 10 2, 3 10 10 2, 7 10 10 4, 8 10 9 2, 6 10 9 7, 1 10 11 6, 1 10 5 1 10 21 2 10 16 Вещество Cо. CO 3 Fe(OH)2 Fe(OH)3 Fe. S Cu. S Li. CO 3 Мg. Cr. O 4 Mg. CO 3 Mg(OH)2 Ni(OH)2 ПР 1 10 12 4, 8 10 16 4 10 38 4 10 19 4 10 38 1, 7 10 3 1, 2 10 3 4 10 5 3, 2 10 11 1, 6 10 14 Вещество Se(OH)3 Sr. SO 4 Te. Cl Pb. Cr. O 4 Pb. I 2 Pb. Br 2 Pb. Cl 2 Pb. CO 3 Pb. SO 4 Zn(OH)2 ПР 1 10 28 2, 8 10 7 1, 5 10 4 2, 8 10 13 1, 1 10 9 9, 1 10 6 1, 7 10 5 1, 5 10 13 2, 2 10 8 1 10 17 40
Таблица ПР Вещество Ba. CO 3 Ba. SO 4 Ba. Cr. O 4 Be(OH)2 Ca. CO 3 Ca. C 2 O 4 Ca. Cr. O 4 Ca. SO 4 Co(OH)3 Co(OH)2 ПР 8 10 9 1 10 10 2, 3 10 10 2, 7 10 10 4, 8 10 9 2, 6 10 9 7, 1 10 11 6, 1 10 5 1 10 21 2 10 16 Вещество Cо. CO 3 Fe(OH)2 Fe(OH)3 Fe. S Cu. S Li. CO 3 Мg. Cr. O 4 Mg. CO 3 Mg(OH)2 Ni(OH)2 ПР 1 10 12 4, 8 10 16 4 10 38 4 10 19 4 10 38 1, 7 10 3 1, 2 10 3 4 10 5 3, 2 10 11 1, 6 10 14 Вещество Se(OH)3 Sr. SO 4 Te. Cl Pb. Cr. O 4 Pb. I 2 Pb. Br 2 Pb. Cl 2 Pb. CO 3 Pb. SO 4 Zn(OH)2 ПР 1 10 28 2, 8 10 7 1, 5 10 4 2, 8 10 13 1, 1 10 9 9, 1 10 6 1, 7 10 5 1, 5 10 13 2, 2 10 8 1 10 17 40


