d95d3d46d1debe76b1894f3ffa46ae8e.ppt
- Количество слайдов: 28
 Презентация к уроку химии на тему «Щелочные металлы» Жироухова Галина Викторовна ГБОУ СПО «Суражский педагогический колледж» преподаватель естественных дисциплин
Презентация к уроку химии на тему «Щелочные металлы» Жироухова Галина Викторовна ГБОУ СПО «Суражский педагогический колледж» преподаватель естественных дисциплин
 Щелочные металлы
Щелочные металлы
 Металлические свойства усиливаются Строение атома 1 +3 Li )) … 2 s … 2 ↑ Na ))) … 3 s 1 +11 … 3 ↑ K )))) … 4 s +19 … 4 ↑ Rb ))))) … 5 s 1 +37 … 5 ↑ +55 Cs )))))) … 6 s 1 … 6 ↑ Fr ))))))) … 7 s 1 +87 … 7 ↑ 1 1 1 1
Металлические свойства усиливаются Строение атома 1 +3 Li )) … 2 s … 2 ↑ Na ))) … 3 s 1 +11 … 3 ↑ K )))) … 4 s +19 … 4 ↑ Rb ))))) … 5 s 1 +37 … 5 ↑ +55 Cs )))))) … 6 s 1 … 6 ↑ Fr ))))))) … 7 s 1 +87 … 7 ↑ 1 1 1 1
 Li от лат. «литос» - камень Юхан Август Арфведсон
Li от лат. «литос» - камень Юхан Август Арфведсон
 К от араб. "алкали" - щелочь Гэмфри Дэви
К от араб. "алкали" - щелочь Гэмфри Дэви
 Na от араб. "натрум" - сода Йенс Якоб Берцелиус
Na от араб. "натрум" - сода Йенс Якоб Берцелиус
 Rb от лат. "рубидус" - темно-красный Cs от лат. "цезиус" - небесно-голубой Густав Роберт Кирхгоф Роберт Вильгельм Бунзен
Rb от лат. "рубидус" - темно-красный Cs от лат. "цезиус" - небесно-голубой Густав Роберт Кирхгоф Роберт Вильгельм Бунзен
 Fr свое название получил от страны Франция. 87 Fr Francium (223)
Fr свое название получил от страны Франция. 87 Fr Francium (223)
 натрий цезий литий калий
натрий цезий литий калий
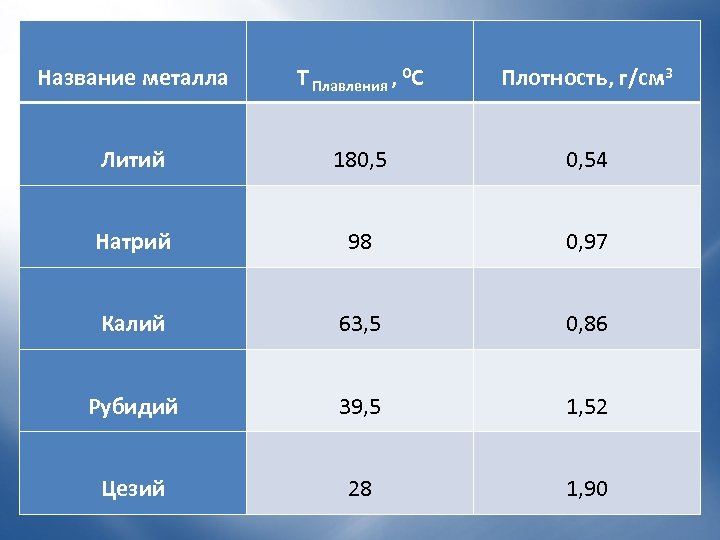 Название металла Т Плавления , 0 С Плотность, г/см 3 Литий 180, 54 Натрий 98 0, 97 Калий 63, 5 0, 86 Рубидий 39, 5 1, 52 Цезий 28 1, 90
Название металла Т Плавления , 0 С Плотность, г/см 3 Литий 180, 54 Натрий 98 0, 97 Калий 63, 5 0, 86 Рубидий 39, 5 1, 52 Цезий 28 1, 90
 Окраска пламени ионами щелочных металлов Li+ К+ Na+ Cs+ Rb+
Окраска пламени ионами щелочных металлов Li+ К+ Na+ Cs+ Rb+

 о t 2 Na+H 2 = 2 Na. H (гидрид) ? +? 2 Na+Cl 2 = 2 Na. Cl (хлорид) ? +? 2 Na+S = Na 2 S (сульфид) ? +? 6 Li+N 2 = 2 Li 3 N (нитрид) ? +?
о t 2 Na+H 2 = 2 Na. H (гидрид) ? +? 2 Na+Cl 2 = 2 Na. Cl (хлорид) ? +? 2 Na+S = Na 2 S (сульфид) ? +? 6 Li+N 2 = 2 Li 3 N (нитрид) ? +?
 Взаимодействие натрия с водой
Взаимодействие натрия с водой
 2 Li + 2 Н 2 О → 2 Li. ОН + Н 2 Li. ОН + HCl → Li. Cl + Н 2 О 2 Li + 2 HCl → 2 Li. Cl + Н 2
2 Li + 2 Н 2 О → 2 Li. ОН + Н 2 Li. ОН + HCl → Li. Cl + Н 2 О 2 Li + 2 HCl → 2 Li. Cl + Н 2
 Na. Cl → Na + Cl + + К (-) Na + 1 е → Na 0 -– 2 e → CI 0 ↑ A (+) 2 Cl 2 пэт 2 Na. Cl → 2 Na + CI 2↑ 1 2 2 1
Na. Cl → Na + Cl + + К (-) Na + 1 е → Na 0 -– 2 e → CI 0 ↑ A (+) 2 Cl 2 пэт 2 Na. Cl → 2 Na + CI 2↑ 1 2 2 1
 Химические свойства оксидов щелочных металлов: Химические свойства гидроксидов щелочных металлов: 1. С солью (р) 1. С водой 2. С кислотными оксидами 3. С кислотой 4. С амфотерными оксидами 3. С кислотой 5. С амфотерными гидроксидами
Химические свойства оксидов щелочных металлов: Химические свойства гидроксидов щелочных металлов: 1. С солью (р) 1. С водой 2. С кислотными оксидами 3. С кислотой 4. С амфотерными оксидами 3. С кислотой 5. С амфотерными гидроксидами
 К КОН К 2 SO 4 2 К + 2 Н 2 О → 2 КОН + Н 2↑ К 2 O К 2 О + Н 2 О → 2 КОН + Н 2 SO 4 → К 2 SO 4 + 2 Н 2 О или 2 КОН + Сu. SO 4 → Сu(ОН)2↓ + К 2 SO 4 К 2 О + Н 2 SO 4 → К 2 SO 4 + Н 2 О или К 2 О + SO 3→ К 2 SO 4
К КОН К 2 SO 4 2 К + 2 Н 2 О → 2 КОН + Н 2↑ К 2 O К 2 О + Н 2 О → 2 КОН + Н 2 SO 4 → К 2 SO 4 + 2 Н 2 О или 2 КОН + Сu. SO 4 → Сu(ОН)2↓ + К 2 SO 4 К 2 О + Н 2 SO 4 → К 2 SO 4 + Н 2 О или К 2 О + SO 3→ К 2 SO 4
 Соединения К KMn. O 4 K 2 CO 3 KCl. O 3 KNO 3
Соединения К KMn. O 4 K 2 CO 3 KCl. O 3 KNO 3
 Na. HCO 3 Na. NO 3 Na. OH Соединения Na Na 2 CO 3 Na. Cl
Na. HCO 3 Na. NO 3 Na. OH Соединения Na Na 2 CO 3 Na. Cl
 Атомы щелочных элементов имеют … а) по одному электрону на внешнем уровне в) полностью заполненный внешний уровень б) по два электрона на внешнем уровне
Атомы щелочных элементов имеют … а) по одному электрону на внешнем уровне в) полностью заполненный внешний уровень б) по два электрона на внешнем уровне
 Франций, завершающий I группу, является… а) очень твёрдым б) самым распространённым в земной коре в) радиоактивным
Франций, завершающий I группу, является… а) очень твёрдым б) самым распространённым в земной коре в) радиоактивным
 Щелочные металлы горят в атмосфере кислорода, образуя… а) пероксиды состава Ме 2 О 2 б) оксиды состава Ме 2 О в) пероксиды Ме 2 О 2 и оксиды Ме 2 О
Щелочные металлы горят в атмосфере кислорода, образуя… а) пероксиды состава Ме 2 О 2 б) оксиды состава Ме 2 О в) пероксиды Ме 2 О 2 и оксиды Ме 2 О
 При взаимодействии щелочных металлов с водой образуются… а) гидриды и кислород б) щёлочи и водород в) пероксиды и водород
При взаимодействии щелочных металлов с водой образуются… а) гидриды и кислород б) щёлочи и водород в) пероксиды и водород
 Натрий и калий в промышленности получают: а) электролизом расплавов б) пирометаллургическими методами в) гидрометаллургическими методами г) металлотермическими методами
Натрий и калий в промышленности получают: а) электролизом расплавов б) пирометаллургическими методами в) гидрометаллургическими методами г) металлотермическими методами
 Щелочные металлы в свободном виде в природе не встречаются, потому что: а) их в природе крайне мало б) эти металлы чрезвычайно химически активны в) эти металлы взаимодействуют с водой
Щелочные металлы в свободном виде в природе не встречаются, потому что: а) их в природе крайне мало б) эти металлы чрезвычайно химически активны в) эти металлы взаимодействуют с водой
 Список использованной литературы: 1. http: //img 1. liveinternet. ru/images/attach/c/0//53/703/53703839_Arfwedson_Jo han_A. jpg 2. http: //upload. wikimedia. org/wikipedia/commons/thumb/f/fe/Gustav_Robert_Ki rchhoff. jpg/300 px-Gustav_Robert_Kirchhoff. jpg 3. http: //www. elite-home. narod. ru/zum/sc 31 a. jpg 4. http: //upload. wikimedia. org/wikipedia/ru/thumb/2/2 a/Jons_Jacob_Berzelius. jpg /300 px-Jons_Jacob_Berzelius. jpg 5. http: //www. persons-info. com/userfiles/image/persons/0 -10000/40005000/4473/BUNZEN_Robert_Vilgelm_fon_2. jpg 6. http: //chemistry-chemists. com/Video/sodium. jpg 7. http: //www. periodictable. ru/003 Li/slides/Li 3. jpg 8. http: //chemistry-chemists. com/N 1_2012/S 1/image/Potassium. JPG 9. http: //chemistry-chemists. com/N 1_2012/U 5/Chemistry. And. Chemists_1_2012 U 5 -0_files/Cesium. jpg
Список использованной литературы: 1. http: //img 1. liveinternet. ru/images/attach/c/0//53/703/53703839_Arfwedson_Jo han_A. jpg 2. http: //upload. wikimedia. org/wikipedia/commons/thumb/f/fe/Gustav_Robert_Ki rchhoff. jpg/300 px-Gustav_Robert_Kirchhoff. jpg 3. http: //www. elite-home. narod. ru/zum/sc 31 a. jpg 4. http: //upload. wikimedia. org/wikipedia/ru/thumb/2/2 a/Jons_Jacob_Berzelius. jpg /300 px-Jons_Jacob_Berzelius. jpg 5. http: //www. persons-info. com/userfiles/image/persons/0 -10000/40005000/4473/BUNZEN_Robert_Vilgelm_fon_2. jpg 6. http: //chemistry-chemists. com/Video/sodium. jpg 7. http: //www. periodictable. ru/003 Li/slides/Li 3. jpg 8. http: //chemistry-chemists. com/N 1_2012/S 1/image/Potassium. JPG 9. http: //chemistry-chemists. com/N 1_2012/U 5/Chemistry. And. Chemists_1_2012 U 5 -0_files/Cesium. jpg
 10. http: //www. wallpampers. ru/pictures/1709/1600_Windows%207. jpg 11. http: //atik. in. ua/uploads/katalog/soda/IMG_1717. png 12. http: //naz 4. com/uploads/posts/2011 -11/1320538253_udobrenie_4. jpg 13. http: //www. krasota. uz/userfiles/images/640_1776300127. jpg 14. http: //img 1. liveinternet. ru/images/attach/c/1/61/147/61147650_276 s. jpg 15. http: //images. tiu. ru/527894_w 640_h 640_soda_kausticheskaya. jpg 16. http: //www. barbysbronich. ru/image_all/vetapteka/margancovka. png 17. http: //utstd. com. ua/images/selitra_kalievaja_upakovka. jpeg 18. http: //lifecity. com. ua/knowledge/1212277330_i-303. jpg
10. http: //www. wallpampers. ru/pictures/1709/1600_Windows%207. jpg 11. http: //atik. in. ua/uploads/katalog/soda/IMG_1717. png 12. http: //naz 4. com/uploads/posts/2011 -11/1320538253_udobrenie_4. jpg 13. http: //www. krasota. uz/userfiles/images/640_1776300127. jpg 14. http: //img 1. liveinternet. ru/images/attach/c/1/61/147/61147650_276 s. jpg 15. http: //images. tiu. ru/527894_w 640_h 640_soda_kausticheskaya. jpg 16. http: //www. barbysbronich. ru/image_all/vetapteka/margancovka. png 17. http: //utstd. com. ua/images/selitra_kalievaja_upakovka. jpeg 18. http: //lifecity. com. ua/knowledge/1212277330_i-303. jpg


