Презентация Microsoft PowerPoint.pptx
- Количество слайдов: 16

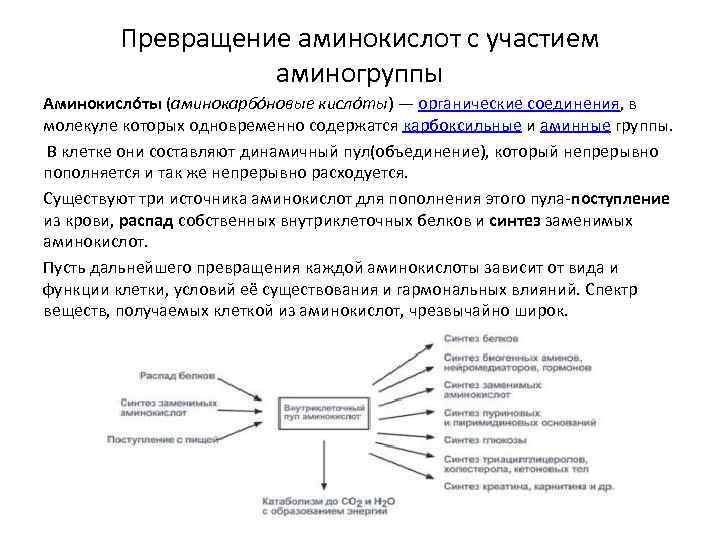
Превращение аминокислот с участием аминогруппы Аминокисло ты (аминокарбо новые кисло ты) — органические соединения, в молекуле которых одновременно содержатся карбоксильные и аминные группы. В клетке они составляют динамичный пул(объединение), который непрерывно пополняется и так же непрерывно расходуется. Существуют три источника аминокислот для пополнения этого пула-поступление из крови, распад собственных внутриклеточных белков и синтез заменимых аминокислот. Пусть дальнейшего превращения каждой аминокислоты зависит от вида и функции клетки, условий её существования и гармональных влияний. Спектр веществ, получаемых клеткой из аминокислот, чрезвычайно широк.
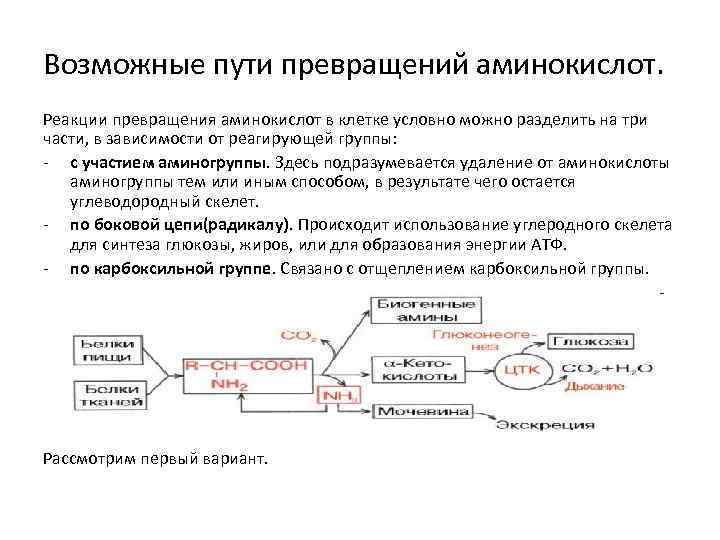
Возможные пути превращений аминокислот. Реакции превращения аминокислот в клетке условно можно разделить на три части, в зависимости от реагирующей группы: - с участием аминогруппы. Здесь подразумевается удаление от аминокислоты аминогруппы тем или иным способом, в результате чего остается углеводородный скелет. - по боковой цепи(радикалу). Происходит использование углеродного скелета для синтеза глюкозы, жиров, или для образования энергии АТФ. - по карбоксильной группе. Связано с отщеплением карбоксильной группы. Рассмотрим первый вариант.

Дезаминирование, отщепление (элиминирование) аминогруппы (NH 2) из органических соединений. Д. сопровождается замещением аминогруппы какой-либо др. группой (например, Н, ОН, OR, Hal) или образованием двойной связи. В отличии от трансаминирования при дезаминировании общее количество аминокислот уменьшается. Аминогруппа, которая удаляется от аминокислот в ходе дезаминирования, превращается далее в аммиак. В организме человека дезаминирование в основном происходит в печени, Аммиак является токсичным для человека, поэтому существуют ферменты, превращающие аммиак в мочевину или мочевую кислоту.

Превращение продуктов реакции дезаминирования АК

Дезаминирование бывает прямым и непрямым. Прямое дезаминирование - это дезаминирование, которое происходит в 1 стадию с участием одного фермента. Прямому дезаминированию повергаются глу, гис, сер, тре, цис. Существует 5 видов прямого дезаминирования АК: • окислительное; • неокислительное; • внутримолекулярное; • восстановительное; • гидролитическое. Окислительное дезаминирование - самый активный вид прямого дезаминирования АК. Непрямое дезаминирование(трансдезаминирование) - это дезаминирование, которое происходит в 2 стадий с участием нескольких ферментов. Оно характерно для большинства аминокислот, так как они не способны к прямому дезаминированию (нет ферментов).
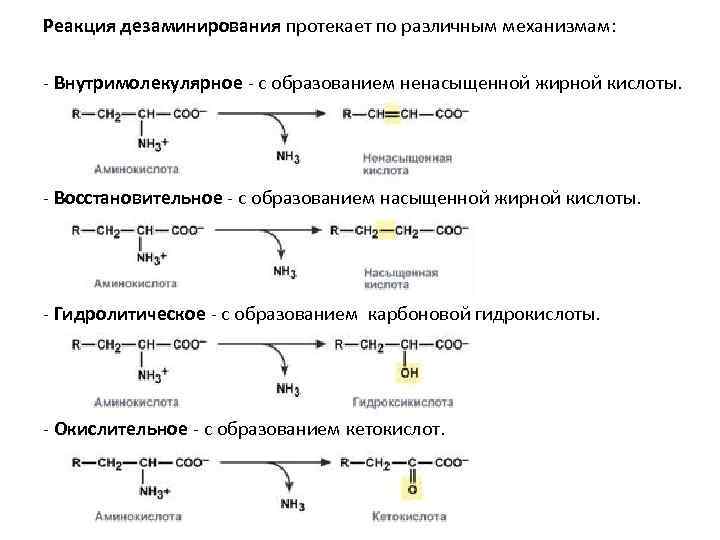
Реакция дезаминирования протекает по различным механизмам: - Внутримолекулярное - с образованием ненасыщенной жирной кислоты. - Восстановительное - с образованием насыщенной жирной кислоты. - Гидролитическое - с образованием карбоновой гидрокислоты. - Окислительное - с образованием кетокислот.
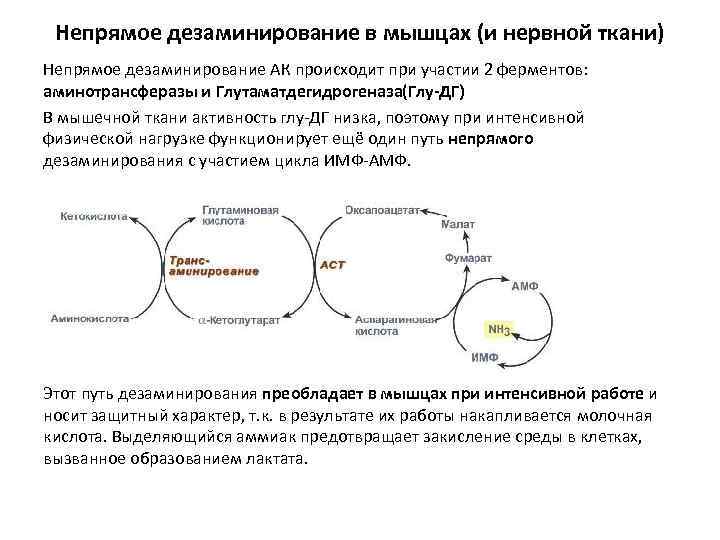
Непрямое дезаминирование в мышцах (и нервной ткани) Непрямое дезаминирование АК происходит при участии 2 ферментов: аминотрансферазы и Глутаматдегидрогеназа(Глу-ДГ) В мышечной ткани активность глу-ДГ низка, поэтому при интенсивной физической нагрузке функционирует ещё один путь непрямого дезаминирования с участием цикла ИМФ-АМФ. Этот путь дезаминирования преобладает в мышцах при интенсивной работе и носит защитный характер, т. к. в результате их работы накапливается молочная кислота. Выделяющийся аммиак предотвращает закисление среды в клетках, вызванное образованием лактата.

Трансаминирование аминокислот Трансаминирование (переаминирование) – межмолекулярный перенос аминогруппы с a-аминокислоты на a-кетокислоту без промежуточного образования аммиака. Главные особенности реакции трансаминирования: 1. 2. 3. Это циклический процесс, все стадии которого катализируются одним и тем же ферментом - трансаминазой данной пары кислот. В этот цикл вступает одна аминокислота и кетокислота Все стадии этого процесса обратимы. Поэтому весь цикл в целом может протекать как в прямом, так и в обратном направлении. Направление этого цикла зависит от соотношения концентраций участников реакции - всех четырех кислот Каждая трансаминаза обычно специфична для одной пары субстратов и соответствующей ей пары продуктов и все стадии реакции катализируются только одним ферментом.
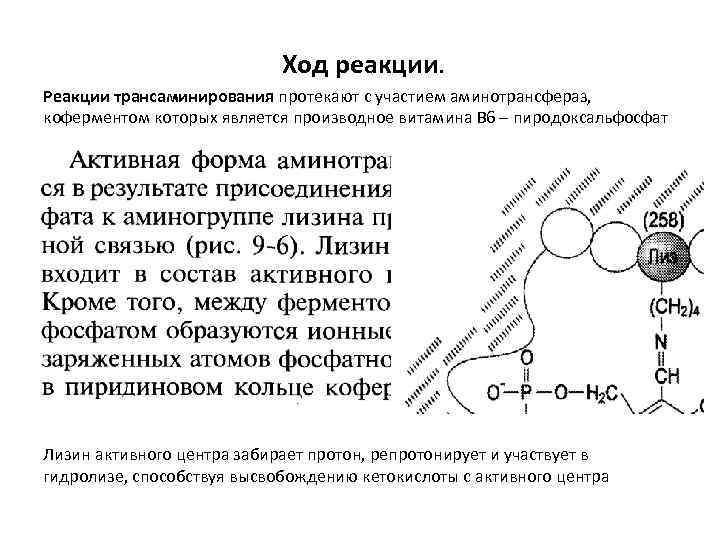
Ход реакции. Реакции трансаминирования протекают с участием аминотрансфераз, коферментом которых является производное витамина В 6 – пиродоксальфосфат Лизин активного центра забирает протон, репротонирует и участвует в гидролизе, способствуя высвобождению кетокислоты с активного центра

Энзимодиагностика • Энзимодиагностика заключается в постановке диагноза заболевания (или синдрома) на основе определения активности ферментов в биологических жидкостях человека. Энзимодиагностика -развивается по двум путям. Один путь-использование ферментов в качестве избирательных реагентов для открытия и количественного определения нормальных или аномальных химических веществ в сыворотке крови, моче, желудочном соке и др. (например, выявление при помощи ферментов глюкозы, белка или других веществ в моче, в норме не обнаруживаемых). Другой путь-открытие и количественное определение самих ферментов в биологических жидкостях при патологии. Наиболее активными в клетках являются те трансаминазы, для которых хотя бы один из субстратов является дикарбоновой альфа-кетокислотой - это Ал. Т - аланинаминотрансфераза (ГПТ) и Ас. Т - аспартатаминотрансфераза (ГЩТ). АЛТ и АСТ (аминотрансферазы) - это выявляемые при биохимическом анализе крови ферменты. Показатель уровня этих ферментов свидетельствует о поражении внутренних органов (печень, поджелудочная железа, сердце). Различное соотношение ферментов АЛТ и АСТ, а так же их абсолютные цифры могут помочь выявить пораженный орган, степень поражения и динамику процесса.

Активность Ал. Ат повышается при заболеваниях печени, особенно при инфекционном гепатите (в инкубационном периоде). Активность Ас. АТ в 2 -20 раз повышается при инфаркте миокарда, и этот показатель имеет прогностическое значение: если на 4 -й день болезни активность Ас. АТ не снижается, то это плохой прогностический признак. При стенокардии активность Ас. АТ не изменяется. При инфаркте миокарда может быть одновременное повышение активности Ал. АТ. Диагностически ценным является определение активности Ал. АТ и Ас. АТ одновременно и расчет коэффициента де Ритиса - Ас. АТ/Ал. АТ. В норме этот коэффициент равен 1, 3. При инфекционном гепатите он ниже, при инфаркте миокарда выше. В оценке ферментных тестов для диагностических целей особое значение имеет знание периода полужизни (полураспада) в плазме крови каждого из диагностических ферментов, что делает важным выбор точного времени для ферментного анализа крови. Весьма существенным является также знание особенностей распределения (топографии) ферментов в индивидуальных органах и тканях, а также их внутриклеточной локализации.

Роль трансаминирования и трансдезаминирования Реакции Трансаминирования: - Активируются в печени, мышцах и других органах при поступлении в клетку избыточного количества тех или иных аминокислот - с целью оптимизации их соотношения. - Обеспечивают синтез заменимых аминокислот в клетке при наличии их углеродного скелета. - Начинаются при прекращении использования аминокислот на синтез азотсодержащих соединений – с целью дальнейшего катаболизма их безазотистого остатка и выработки энергии. - Необходимы при внутриклеточном голодании, например при гипоглекимиях различного генеза. Процесс трансдезаминирования идет в организме непрерывно потому что: - Сопряженные реакции трансаминирования и дезаминировния создают поток лишнего аминного азота из периферических клеток в печень для синтеза мочевины и в почки для синтеза аммоннийных солей.

Обмен и роль Креатина Креатин (метилгуанидоацетатная кислота) — азотсодержащая карбоновая кислота, которая встречается в организме позвоночных. Участвует в энергетическом обмене в мышечных и нервных клетках. Креатин необходим для образования в мышцах и в клетках мозга высокоэнергетического соединения - кре-атинфосфата. Эта реакция легко обратима и катализируется ферментом креатинкиназой. Креа-тинфосфат играет важную роль в обеспечении энергией работающей мышцы в начальный период.
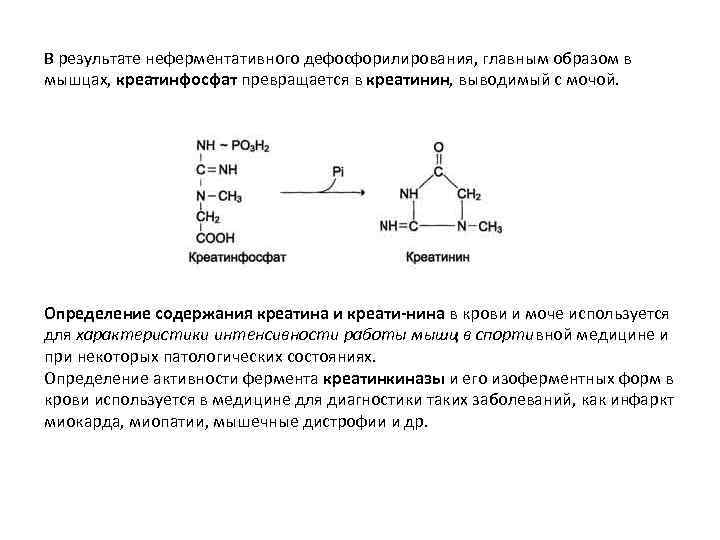
В результате неферментативного дефосфорилирования, главным образом в мышцах, креатинфосфат превращается в креатинин, выводимый с мочой. Определение содержания креатина и креати-нина в крови и моче используется для характеристики интенсивности работы мышц в спортивной медицине и при некоторых патологических состояниях. Определение активности фермента креатинкиназы и его изоферментных форм в крови используется в медицине для диагностики таких заболеваний, как инфаркт миокарда, миопатии, мышечные дистрофии и др.

Роль креатина • Креатин принимает участие в ресинтезе АТФ. • фосфат креатина нейтрализует кислоты, которые образуются во время выполнения упражнения и снижают p. H крови, что вызывает усталость мышц. • креатин активирует гликолиз. • При хронических и острых воспалениях оказывает антивоспалительное действие; • Снижение холестерина и укрепление сердечно-сосудистой системы; • Оказывает защитный эффект на ЦНС при ишемии и в гипоксических условиях. • способность дополнительно активизировать производство анаболических гормонов, которые представлены тестостероном и соматотропином. • креатин используется при лечении болезней, вызывающих атрофию мышц
Презентация Microsoft PowerPoint.pptx