9 Альдегиды. Углеводы.pptx
- Количество слайдов: 35
 Препараты альдегидов и их производных. Углеводы σ O R –C σ+ H
Препараты альдегидов и их производных. Углеводы σ O R –C σ+ H
 реакции окисления. ФС, ГФ Х реакция «серебряного зеркала» реакция с реактивом Несслера R-COH + K 2[Hg. I 4] +3 KOH → R-COOK + 4 KI + Hg↓ + 2 H 2 O
реакции окисления. ФС, ГФ Х реакция «серебряного зеркала» реакция с реактивом Несслера R-COH + K 2[Hg. I 4] +3 KOH → R-COOK + 4 KI + Hg↓ + 2 H 2 O
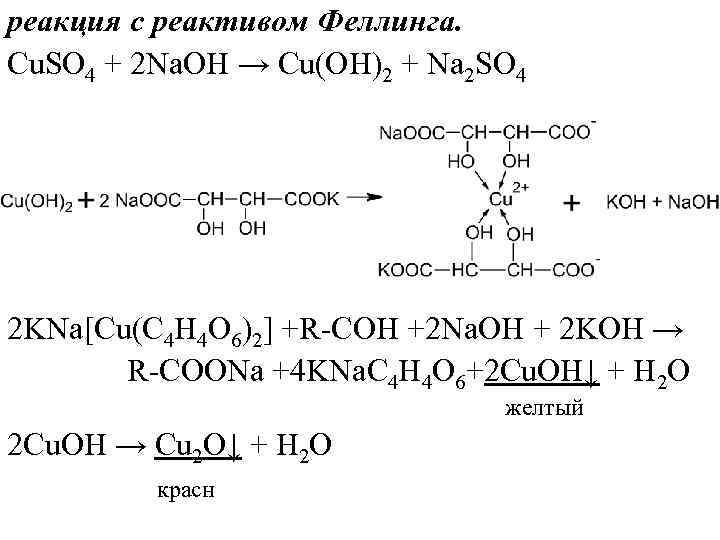 реакция с реактивом Феллинга. Cu. SO 4 + 2 Na. OH → Cu(OH)2 + Na 2 SO 4 2 KNa[Cu(C 4 H 4 O 6)2] +R-COH +2 Na. OH + 2 KOH → R-COONa +4 KNa. C 4 H 4 O 6+2 Cu. OH↓ + H 2 O желтый 2 Cu. OH → Cu 2 O↓ + H 2 O красн
реакция с реактивом Феллинга. Cu. SO 4 + 2 Na. OH → Cu(OH)2 + Na 2 SO 4 2 KNa[Cu(C 4 H 4 O 6)2] +R-COH +2 Na. OH + 2 KOH → R-COONa +4 KNa. C 4 H 4 O 6+2 Cu. OH↓ + H 2 O желтый 2 Cu. OH → Cu 2 O↓ + H 2 O красн
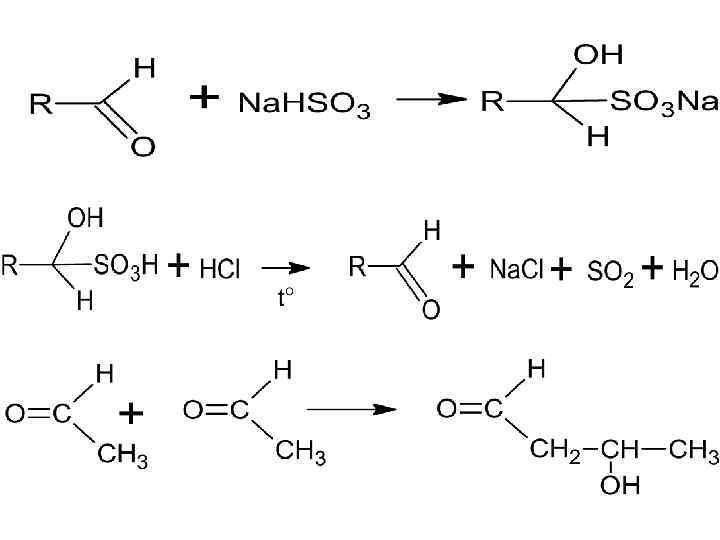
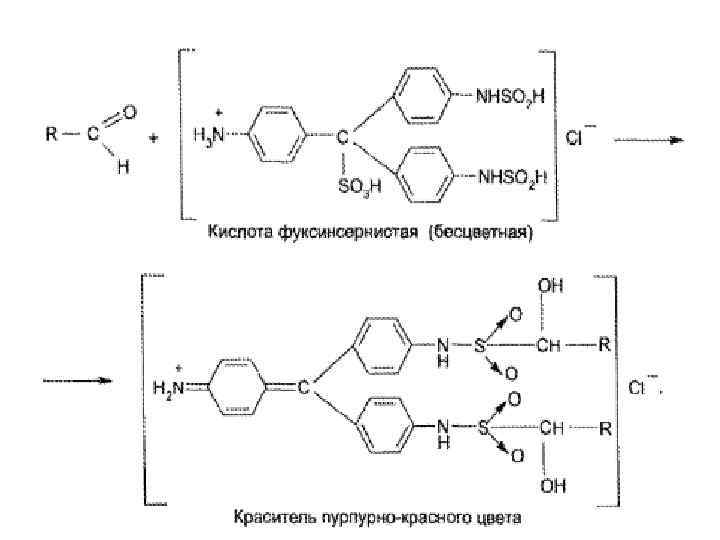
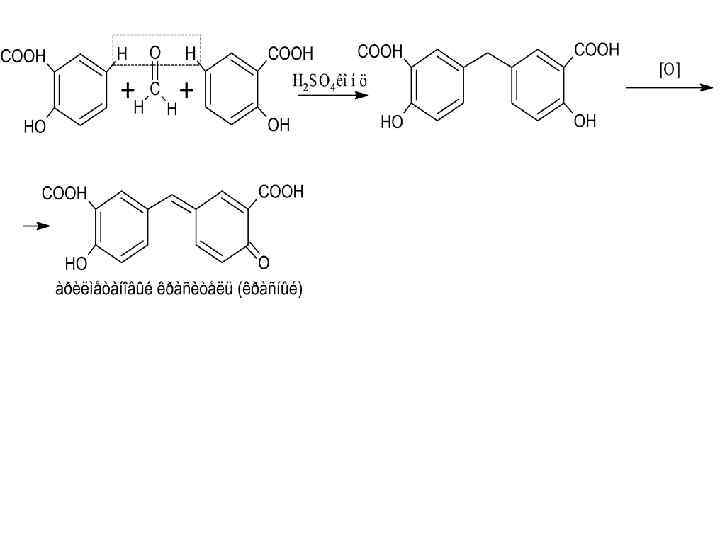
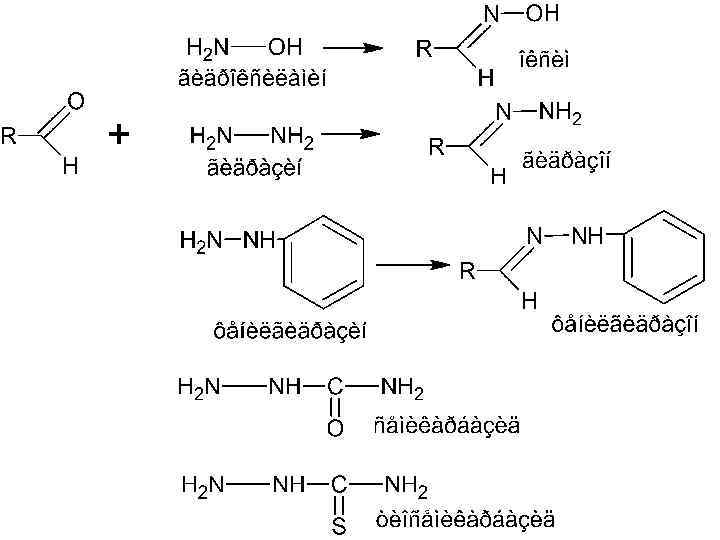
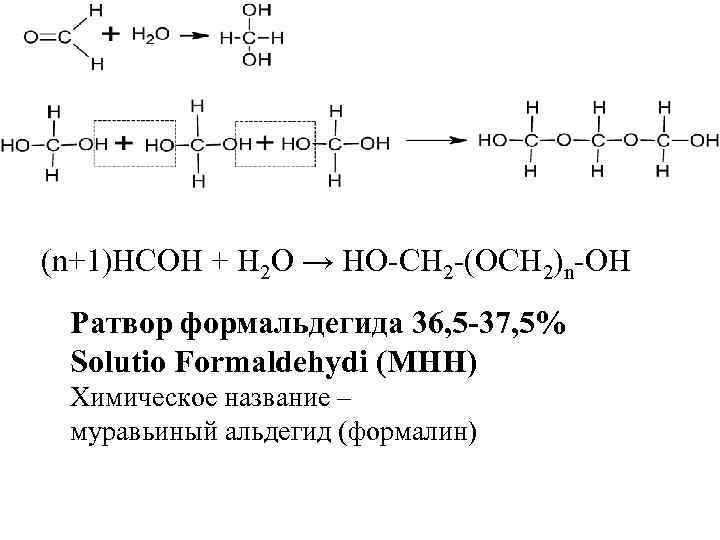 (n+1)HCOH + H 2 O → HO-CH 2 -(OCH 2)n-OH Ратвор формальдегида 36, 5 -37, 5% Solutio Formaldehydi (МНН) Химическое название – муравьиный альдегид (формалин)
(n+1)HCOH + H 2 O → HO-CH 2 -(OCH 2)n-OH Ратвор формальдегида 36, 5 -37, 5% Solutio Formaldehydi (МНН) Химическое название – муравьиный альдегид (формалин)
 Получение СН 3 ОН+ O 2 → НСОН + 2 H 2 O Чистота Специфическая примесь – муравьиная кислота алкаметрическим методом – не более 0, 2% (титруют 0, 1 н гидроксидом натрия по ф/фт). НСООН + Na. ОН → НСООNa + Н 2 О
Получение СН 3 ОН+ O 2 → НСОН + 2 H 2 O Чистота Специфическая примесь – муравьиная кислота алкаметрическим методом – не более 0, 2% (титруют 0, 1 н гидроксидом натрия по ф/фт). НСООН + Na. ОН → НСООNa + Н 2 О
 Количественное определение ФС. Йодометрический метод обратного титрования I 2 + HCOH ↔ HCOOH + HI I 2 + 2 Na. OH → Na. I + Na. IO + H 2 O HCOH + Na. IO + Na. OH → HCOONa + Na. I + H 2 O Суммарно: HCOH + I 2 + 3 Na. OH → HCOONa + 2 Na. I + 2 H 2 O Na. IO + Na. I + H 2 SO 4 → I 2 + Na 2 SO 4 + H 2 O I 2 + 2 Na 2 S 2 O 3 → 2 Na. I + Na 2 S 4 O 6 Кстех = 1/1 fэкв = 1· 1/2 = ½ М. э = ½ · М. м Т = М. э · Ст-та/1000 С% = (VI 2 – VNa 2 S 2 O 3) · K· T · 100 Vпр
Количественное определение ФС. Йодометрический метод обратного титрования I 2 + HCOH ↔ HCOOH + HI I 2 + 2 Na. OH → Na. I + Na. IO + H 2 O HCOH + Na. IO + Na. OH → HCOONa + Na. I + H 2 O Суммарно: HCOH + I 2 + 3 Na. OH → HCOONa + 2 Na. I + 2 H 2 O Na. IO + Na. I + H 2 SO 4 → I 2 + Na 2 SO 4 + H 2 O I 2 + 2 Na 2 S 2 O 3 → 2 Na. I + Na 2 S 4 O 6 Кстех = 1/1 fэкв = 1· 1/2 = ½ М. э = ½ · М. м Т = М. э · Ст-та/1000 С% = (VI 2 – VNa 2 S 2 O 3) · K· T · 100 Vпр
![косвенное йодометрическое титрование: HCOH + K 2[Hg. I 4] + 3 KOH → HCOOK косвенное йодометрическое титрование: HCOH + K 2[Hg. I 4] + 3 KOH → HCOOK](https://present5.com/presentation/55362899_24501156/image-11.jpg) косвенное йодометрическое титрование: HCOH + K 2[Hg. I 4] + 3 KOH → HCOOK + Hg↓ + 4 KI + 2 H 2 O Hg + I 2 → Hg. I 2 + 2 KI → K 2[Hg. I 4] I 2 + 2 Na 2 S 2 O 3 → 2 Na. I + Na 2 S 4 O 6 Хранение Т° не ниже 9 о. С параформ [CH 2 O]n выпадает в виде белого осадка
косвенное йодометрическое титрование: HCOH + K 2[Hg. I 4] + 3 KOH → HCOOK + Hg↓ + 4 KI + 2 H 2 O Hg + I 2 → Hg. I 2 + 2 KI → K 2[Hg. I 4] I 2 + 2 Na 2 S 2 O 3 → 2 Na. I + Na 2 S 4 O 6 Хранение Т° не ниже 9 о. С параформ [CH 2 O]n выпадает в виде белого осадка
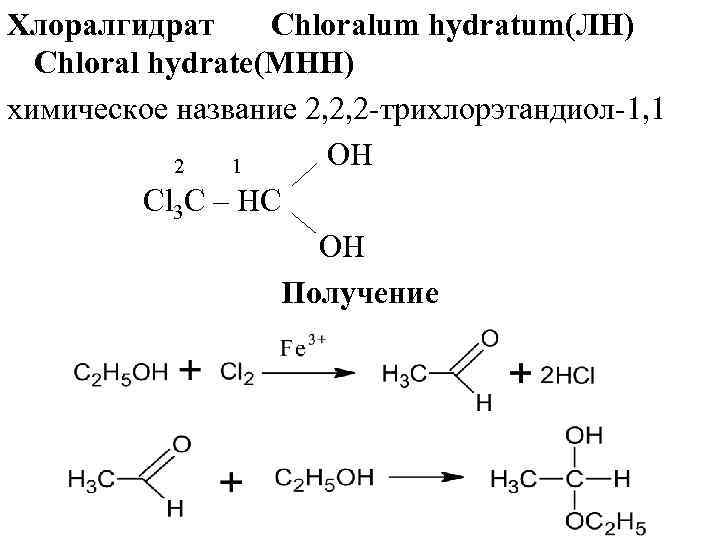 Хлоралгидрат Chloralum hydratum(ЛН) Chloral hydrate(МНН) химическое название 2, 2, 2 -трихлорэтандиол-1, 1 OH 2 1 Cl 3 C – HC OH Получение
Хлоралгидрат Chloralum hydratum(ЛН) Chloral hydrate(МНН) химическое название 2, 2, 2 -трихлорэтандиол-1, 1 OH 2 1 Cl 3 C – HC OH Получение
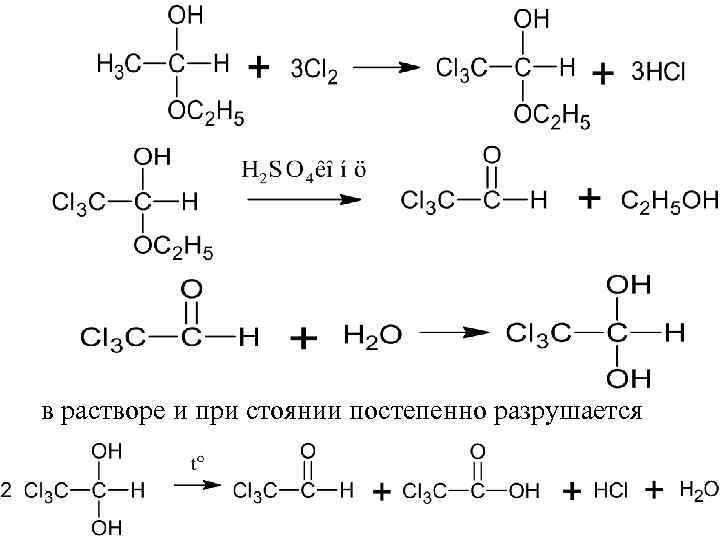 в растворе и при стоянии постепенно разрушается
в растворе и при стоянии постепенно разрушается
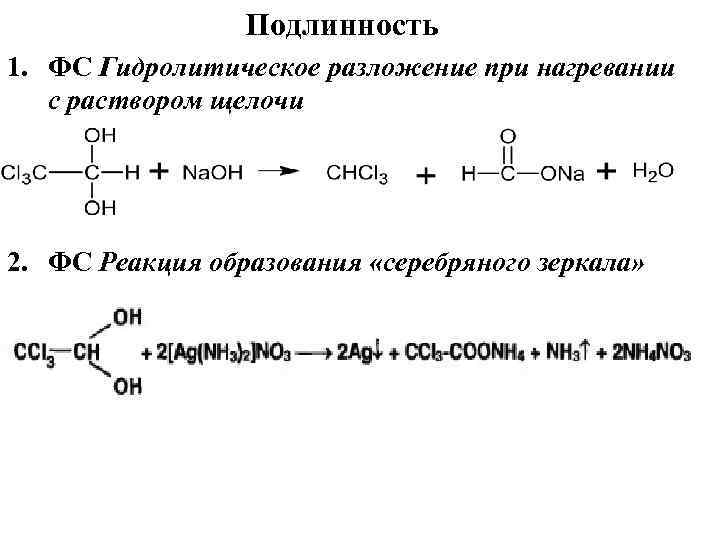 Подлинность 1. ФС Гидролитическое разложение при нагревании с раствором щелочи 2. ФС Реакция образования «серебряного зеркала»
Подлинность 1. ФС Гидролитическое разложение при нагревании с раствором щелочи 2. ФС Реакция образования «серебряного зеркала»
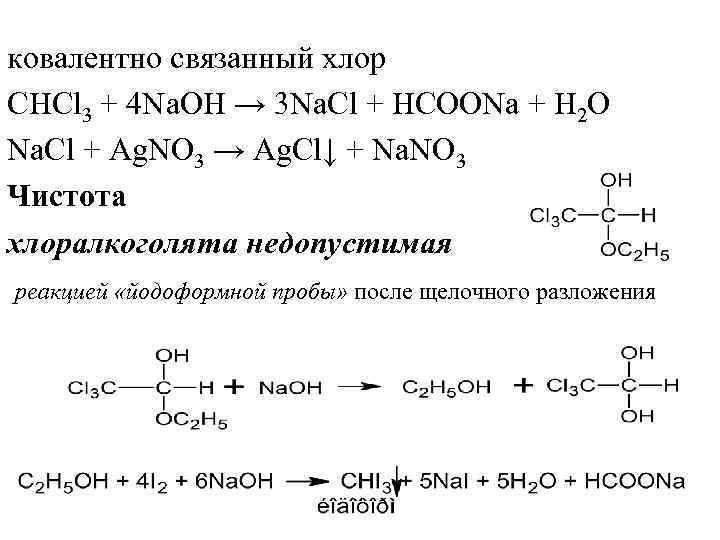 ковалентно связанный хлор CHCl 3 + 4 Na. OH → 3 Na. Cl + HCOONa + H 2 O Na. Cl + Ag. NO 3 → Ag. Cl↓ + Na. NO 3 Чистота хлоралкоголята недопустимая реакцией «йодоформной пробы» после щелочного разложения
ковалентно связанный хлор CHCl 3 + 4 Na. OH → 3 Na. Cl + HCOONa + H 2 O Na. Cl + Ag. NO 3 → Ag. Cl↓ + Na. NO 3 Чистота хлоралкоголята недопустимая реакцией «йодоформной пробы» после щелочного разложения
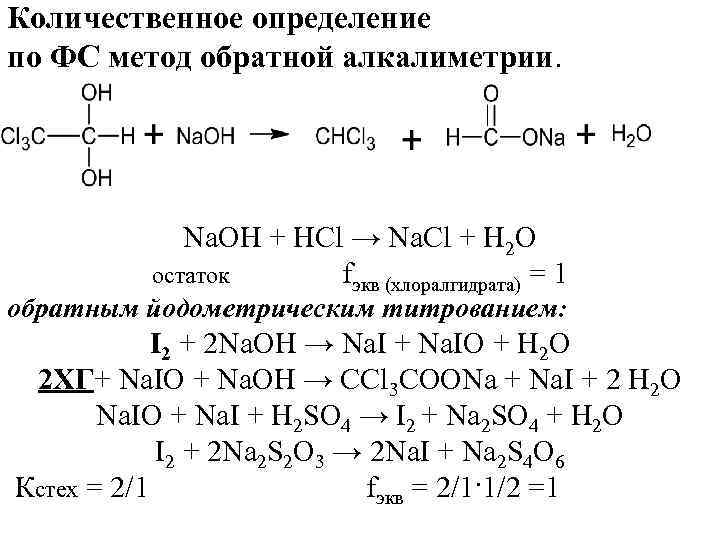 Количественное определение по ФС метод обратной алкалиметрии. Na. OH + HCl → Na. Cl + H 2 O остаток fэкв (хлоралгидрата) = 1 обратным йодометрическим титрованием: I 2 + 2 Na. OH → Na. I + Na. IO + H 2 O 2 ХГ+ Na. IO + Na. OH → CCl 3 COONa + Na. I + 2 H 2 O Na. IO + Na. I + H 2 SO 4 → I 2 + Na 2 SO 4 + H 2 O I 2 + 2 Na 2 S 2 O 3 → 2 Na. I + Na 2 S 4 O 6 Кстех = 2/1 fэкв = 2/1·1/2 =1
Количественное определение по ФС метод обратной алкалиметрии. Na. OH + HCl → Na. Cl + H 2 O остаток fэкв (хлоралгидрата) = 1 обратным йодометрическим титрованием: I 2 + 2 Na. OH → Na. I + Na. IO + H 2 O 2 ХГ+ Na. IO + Na. OH → CCl 3 COONa + Na. I + 2 H 2 O Na. IO + Na. I + H 2 SO 4 → I 2 + Na 2 SO 4 + H 2 O I 2 + 2 Na 2 S 2 O 3 → 2 Na. I + Na 2 S 4 O 6 Кстех = 2/1 fэкв = 2/1·1/2 =1
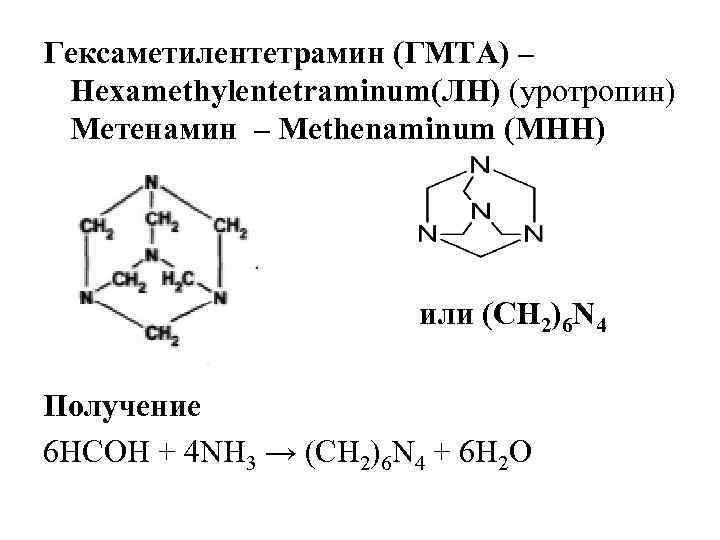 Гексаметилентетрамин (ГМТА) – Hexamethylentetraminum(ЛН) (уротропин) Метенамин – Methenaminum (МНН) или (СН 2)6 N 4 Получение 6 НСОН + 4 NH 3 → (CH 2)6 N 4 + 6 H 2 O
Гексаметилентетрамин (ГМТА) – Hexamethylentetraminum(ЛН) (уротропин) Метенамин – Methenaminum (МНН) или (СН 2)6 N 4 Получение 6 НСОН + 4 NH 3 → (CH 2)6 N 4 + 6 H 2 O
 Подлинность 1. ИК- спектр 2. Реакция кислотного гидролиза (CH 2)6 N 4 + 2 H 2 SO 4 + 6 H 2 O → 6 HCOH + 2(NH 4)2 SO 4 + 2 Na. OH → Na 2 SO 4 + 2 NH 3↑ + H 2 O 1. Реакции с общеалкалоидными осадительными реактивами (на третичный амин). с растворами: 1) пикриновой кислоты – желтый осадок пикратов 2) йода в калия йодиде – красно-бурый осадок тетрайодида (CH 2)6 N 4·I 4 3) бромной водой – оранжево-желтый осадок 4) йодмонохлорида– (CH 2)6 N 4 ∙ 2 ICl↓ (колич. ) 5) серебра нитрата (CH 2)6 N 4 ∙ 3 Ag. NO 3↓ (колич. )
Подлинность 1. ИК- спектр 2. Реакция кислотного гидролиза (CH 2)6 N 4 + 2 H 2 SO 4 + 6 H 2 O → 6 HCOH + 2(NH 4)2 SO 4 + 2 Na. OH → Na 2 SO 4 + 2 NH 3↑ + H 2 O 1. Реакции с общеалкалоидными осадительными реактивами (на третичный амин). с растворами: 1) пикриновой кислоты – желтый осадок пикратов 2) йода в калия йодиде – красно-бурый осадок тетрайодида (CH 2)6 N 4·I 4 3) бромной водой – оранжево-желтый осадок 4) йодмонохлорида– (CH 2)6 N 4 ∙ 2 ICl↓ (колич. ) 5) серебра нитрата (CH 2)6 N 4 ∙ 3 Ag. NO 3↓ (колич. )
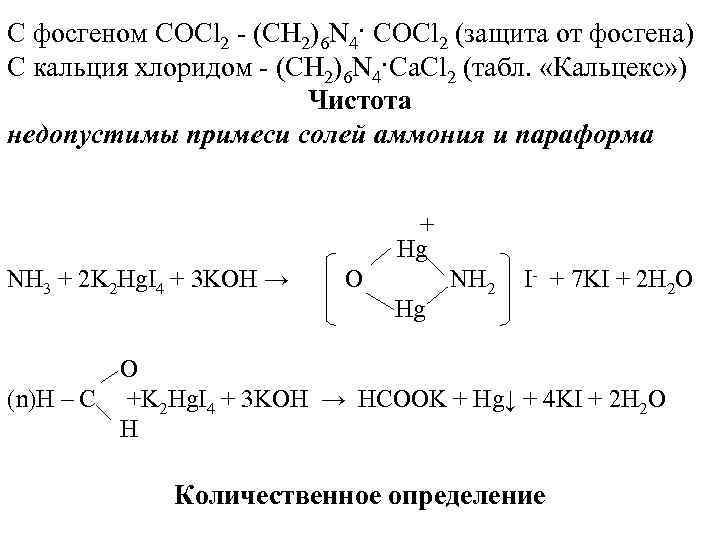 С фосгеном COCl 2 - (CH 2)6 N 4· COCl 2 (защита от фосгена) С кальция хлоридом - (CH 2)6 N 4·Са. Cl 2 (табл. «Кальцекс» ) Чистота недопустимы примеси солей аммония и параформа + Hg NH 3 + 2 K 2 Hg. I 4 + 3 KOH → O NH 2 I- + 7 KI + 2 H 2 O Hg O (n)H – C +K 2 Hg. I 4 + 3 KOH → HCOOK + Hg↓ + 4 KI + 2 H 2 O H Количественное определение
С фосгеном COCl 2 - (CH 2)6 N 4· COCl 2 (защита от фосгена) С кальция хлоридом - (CH 2)6 N 4·Са. Cl 2 (табл. «Кальцекс» ) Чистота недопустимы примеси солей аммония и параформа + Hg NH 3 + 2 K 2 Hg. I 4 + 3 KOH → O NH 2 I- + 7 KI + 2 H 2 O Hg O (n)H – C +K 2 Hg. I 4 + 3 KOH → HCOOK + Hg↓ + 4 KI + 2 H 2 O H Количественное определение
 1. ГФ Х обратное ацидиметрическое титрование. t o. C (CH 2)6 N 4 + 2 H 2 SO 4 + 6 H 2 O → 6 HCOH + 2(NH 4)2 SO 4 H 2 SO 4 (остаок) + 2 Na. OH → Na 2 SO 4 + H 2 O Кстех = ½; fэкв = ½· ½ = ¼; М. э = ¼ · М. м 1. Ацидиметрия в водной среде. (CH 2)6 N 4 + HCl → (CH 2)6 N 4· HCl fэкв = 1
1. ГФ Х обратное ацидиметрическое титрование. t o. C (CH 2)6 N 4 + 2 H 2 SO 4 + 6 H 2 O → 6 HCOH + 2(NH 4)2 SO 4 H 2 SO 4 (остаок) + 2 Na. OH → Na 2 SO 4 + H 2 O Кстех = ½; fэкв = ½· ½ = ¼; М. э = ¼ · М. м 1. Ацидиметрия в водной среде. (CH 2)6 N 4 + HCl → (CH 2)6 N 4· HCl fэкв = 1
 3. Кислотно – основное титрование в неводной среде (CH 2)6 N 4 + HCl. O 4 → (CH 2)6 N 4 ∙ HCl. O 4 Аргентометрия (вариант Фольгарда) 2(CH 2)6 N 4 +3 Ag. NO 3(избыаок) → 2(CH 2)6 N 4· 3 Ag. NO 3↓ Ag. NO 3(остаок) +NH 4 SCN →Ag. SCN↓ +NH 4 NO 3 NH 4 SCN +NH 4 Fe(SO 4)2· 12 H 2 O → Fe(SCN)3 +(NH 4)2 SO 4 + 12 H 2 O красное окр. йодометрическое титрование титрант–йод (CH 2)6 N 4 ∙ 2 I 2↓ йодхлорметрическое титрант–йодмонохлорид (CH 2)6 N 4 ∙ 2 ICl↓
3. Кислотно – основное титрование в неводной среде (CH 2)6 N 4 + HCl. O 4 → (CH 2)6 N 4 ∙ HCl. O 4 Аргентометрия (вариант Фольгарда) 2(CH 2)6 N 4 +3 Ag. NO 3(избыаок) → 2(CH 2)6 N 4· 3 Ag. NO 3↓ Ag. NO 3(остаок) +NH 4 SCN →Ag. SCN↓ +NH 4 NO 3 NH 4 SCN +NH 4 Fe(SO 4)2· 12 H 2 O → Fe(SCN)3 +(NH 4)2 SO 4 + 12 H 2 O красное окр. йодометрическое титрование титрант–йод (CH 2)6 N 4 ∙ 2 I 2↓ йодхлорметрическое титрант–йодмонохлорид (CH 2)6 N 4 ∙ 2 ICl↓
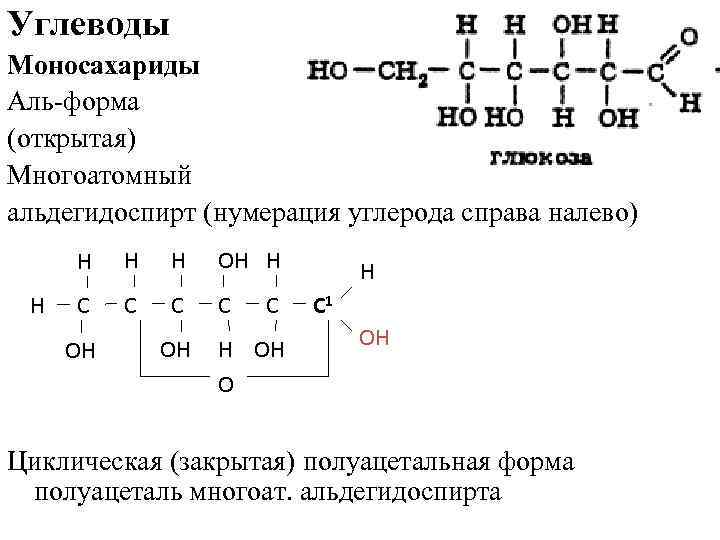 Углеводы Моносахариды Аль-форма (открытая) Многоатомный альдегидоспирт (нумерация углерода справа налево) Н Н ОН Н С С ОН ОН С Н ОН О Н С 1 ОН Циклическая (закрытая) полуацетальная форма полуацеталь многоат. альдегидоспирта
Углеводы Моносахариды Аль-форма (открытая) Многоатомный альдегидоспирт (нумерация углерода справа налево) Н Н ОН Н С С ОН ОН С Н ОН О Н С 1 ОН Циклическая (закрытая) полуацетальная форма полуацеталь многоат. альдегидоспирта
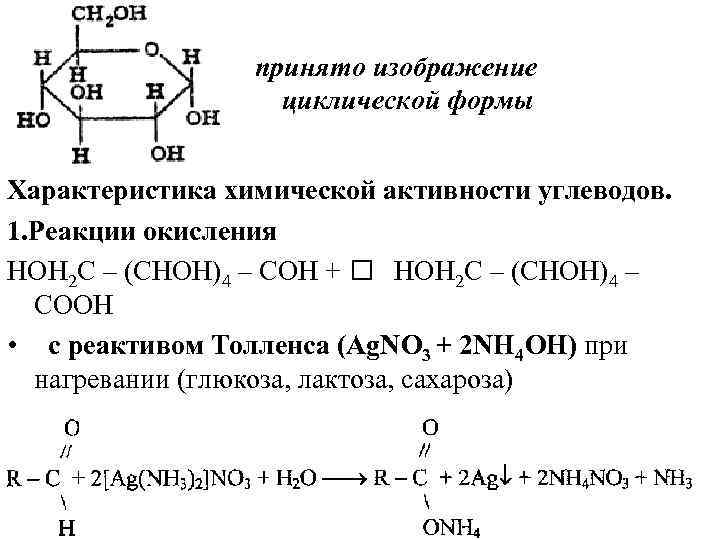 принято изображение циклической формы Характеристика химической активности углеводов. 1. Реакции окисления НОН 2 С – (СНОН)4 – СOH + НОН 2 С – (СНОН)4 – СOOН • с реактивом Толленса (Ag. NO 3 + 2 NH 4 OH) при нагревании (глюкоза, лактоза, сахароза)
принято изображение циклической формы Характеристика химической активности углеводов. 1. Реакции окисления НОН 2 С – (СНОН)4 – СOH + НОН 2 С – (СНОН)4 – СOOН • с реактивом Толленса (Ag. NO 3 + 2 NH 4 OH) при нагревании (глюкоза, лактоза, сахароза)
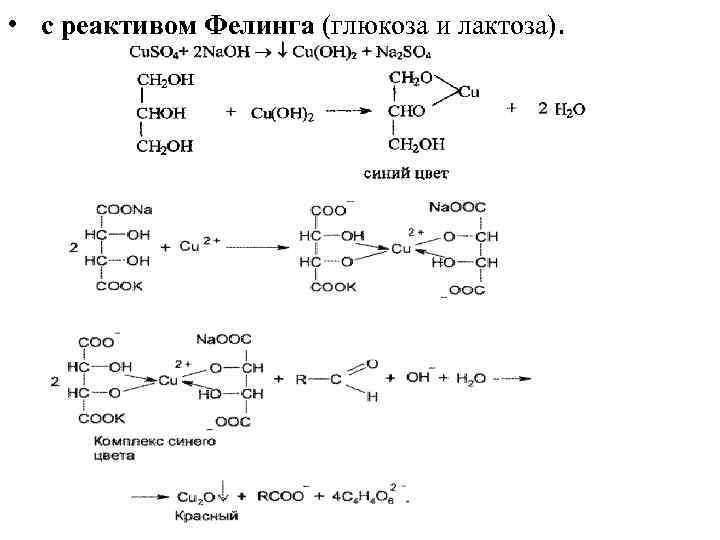 • с реактивом Фелинга (глюкоза и лактоза).
• с реактивом Фелинга (глюкоза и лактоза).
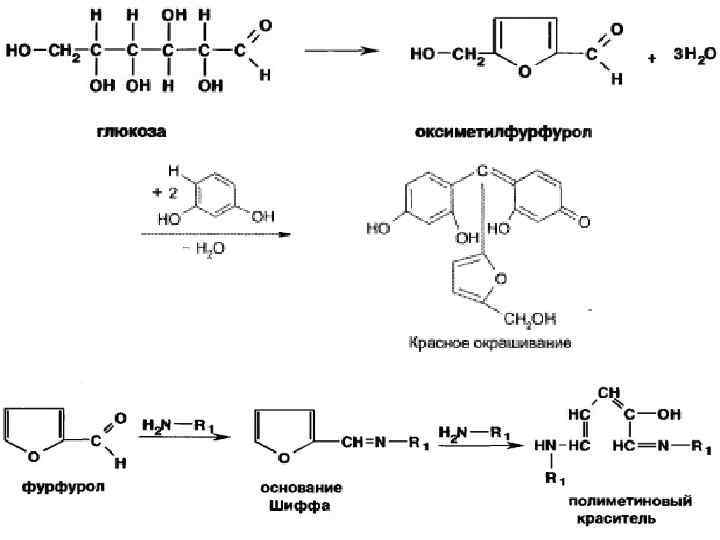
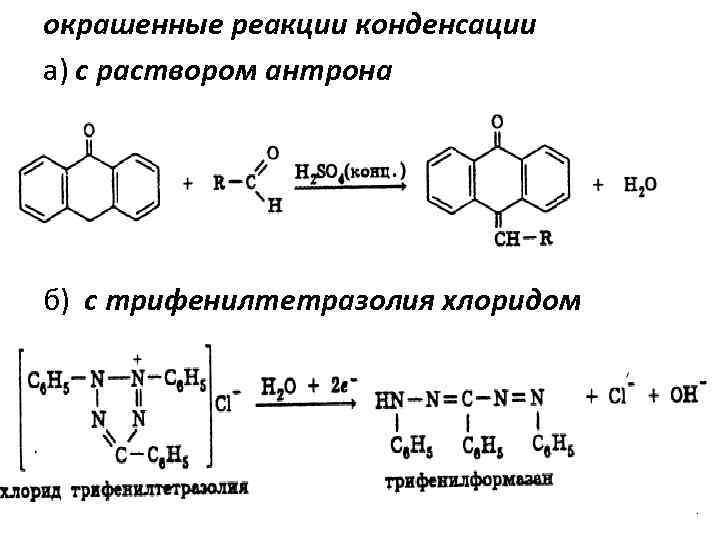 окрашенные реакции конденсации а) с раствором антрона б) с трифенилтетразолия хлоридом
окрашенные реакции конденсации а) с раствором антрона б) с трифенилтетразолия хлоридом
 в) с фенилгидразином – реакция образования озазонов. Озазоны – кристаллические вещества с четкой Т°пл. 6. реакциям этерификации
в) с фенилгидразином – реакция образования озазонов. Озазоны – кристаллические вещества с четкой Т°пл. 6. реакциям этерификации
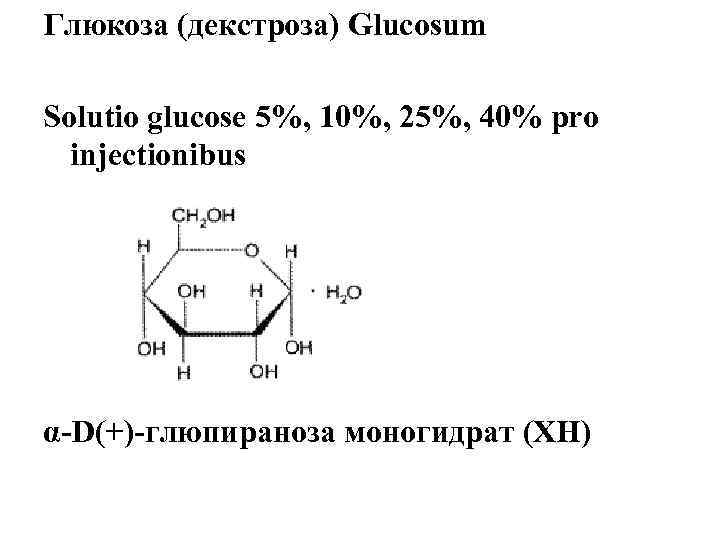 Глюкоза (декстроза) Glucosum Solutio glucose 5%, 10%, 25%, 40% pro injectionibus α-D(+)-глюпираноза моногидрат (ХН)
Глюкоза (декстроза) Glucosum Solutio glucose 5%, 10%, 25%, 40% pro injectionibus α-D(+)-глюпираноза моногидрат (ХН)
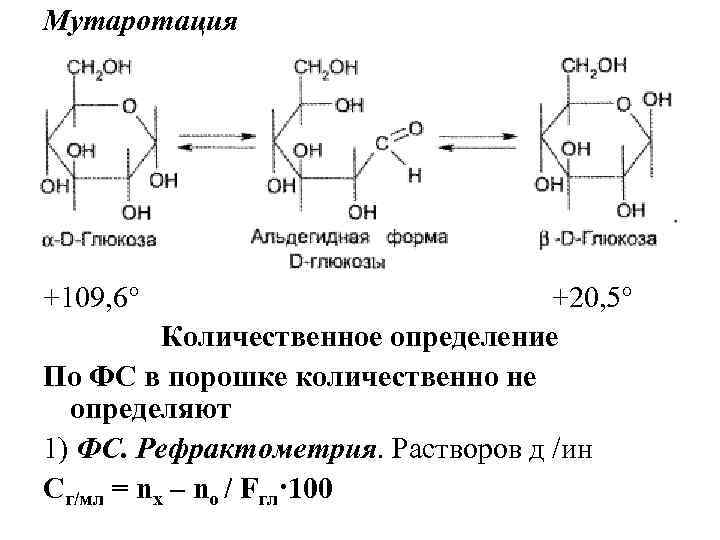 Мутаротация +109, 6° +20, 5° Количественное определение По ФС в порошке количественно не определяют 1) ФС. Рефрактометрия. Растворов д /ин Cг/мл = nx – no / Fгл·100
Мутаротация +109, 6° +20, 5° Количественное определение По ФС в порошке количественно не определяют 1) ФС. Рефрактометрия. Растворов д /ин Cг/мл = nx – no / Fгл·100
 Поляриметрия. ГЖХ Обратный йодометрический метод I 2 + 2 Na. OH Na. I + Na. OI + H 2 O НОН 2 С – (СНОН)4 – СOH + Na. OI + Na. OH НОН 2 С – (СНОН)4 – СOONa + Na. I+ H 2 O Na. I + Na. OI + H 2 SO 4 I 2 + Na 2 SO 4 + H 2 O I 2 + 2 Na 2 S 2 O 3 2 Na I + Na 2 S 4 O 6
Поляриметрия. ГЖХ Обратный йодометрический метод I 2 + 2 Na. OH Na. I + Na. OI + H 2 O НОН 2 С – (СНОН)4 – СOH + Na. OI + Na. OH НОН 2 С – (СНОН)4 – СOONa + Na. I+ H 2 O Na. I + Na. OI + H 2 SO 4 I 2 + Na 2 SO 4 + H 2 O I 2 + 2 Na 2 S 2 O 3 2 Na I + Na 2 S 4 O 6
 Кстех. =1/1, титрант ( УЧ ½ I 2) fэкв. = 1·½ = ½ М. э=½ М. м С= (VI 2· К - VNa 2 S 2 O 3 · К) ·Т а обратный куприметрический метод. Растворы глюкозы для инъекций стабилизатор Вейбеля – состоящий из раствора HCI 0, 1 н – добавляют до р. Н = 3, 0 – 4, 0 и натрия хлорида – 0, 26 г на 1 литр
Кстех. =1/1, титрант ( УЧ ½ I 2) fэкв. = 1·½ = ½ М. э=½ М. м С= (VI 2· К - VNa 2 S 2 O 3 · К) ·Т а обратный куприметрический метод. Растворы глюкозы для инъекций стабилизатор Вейбеля – состоящий из раствора HCI 0, 1 н – добавляют до р. Н = 3, 0 – 4, 0 и натрия хлорида – 0, 26 г на 1 литр
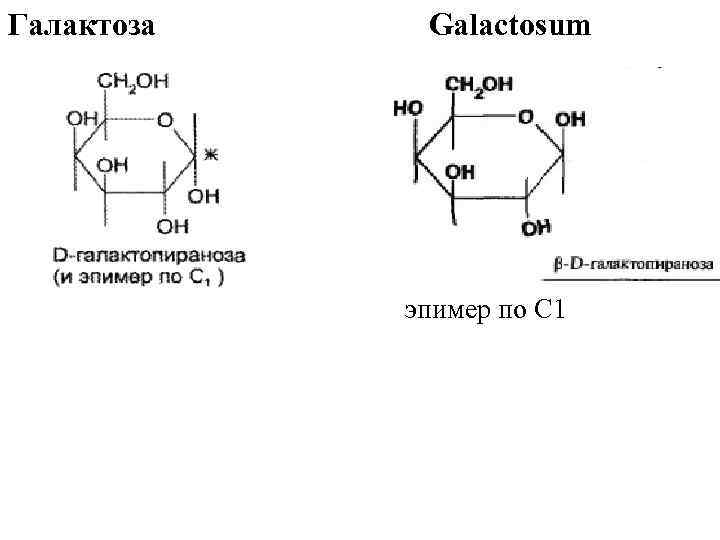 Галактоза Galactosum эпимер по С 1
Галактоза Galactosum эпимер по С 1
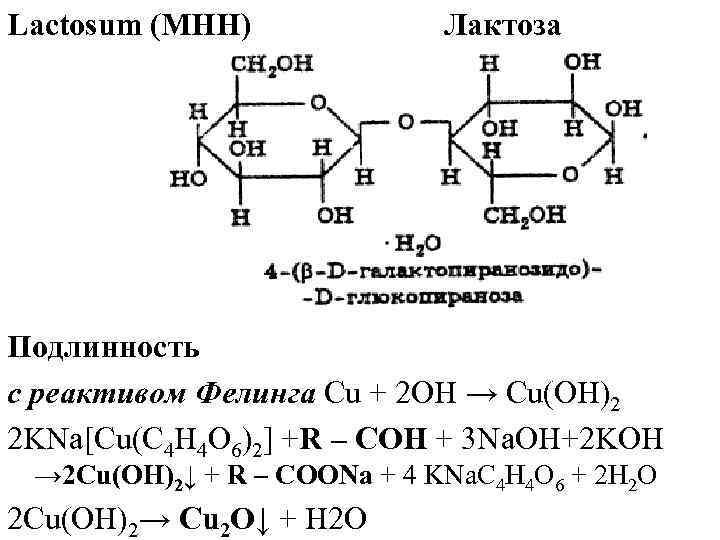 Lactosum (МНН) Лактоза Подлинность с реактивом Фелинга Cu + 2 OH → Cu(ОН)2 2 KNa[Cu(C 4 H 4 O 6)2] +R – CОН + 3 Na. OH+2 KOH → 2 Cu(OH)2↓ + R – COONa + 4 KNa. C 4 H 4 O 6 + 2 H 2 O 2 Cu(OH)2→ Cu 2 O↓ + H 2 O
Lactosum (МНН) Лактоза Подлинность с реактивом Фелинга Cu + 2 OH → Cu(ОН)2 2 KNa[Cu(C 4 H 4 O 6)2] +R – CОН + 3 Na. OH+2 KOH → 2 Cu(OH)2↓ + R – COONa + 4 KNa. C 4 H 4 O 6 + 2 H 2 O 2 Cu(OH)2→ Cu 2 O↓ + H 2 O
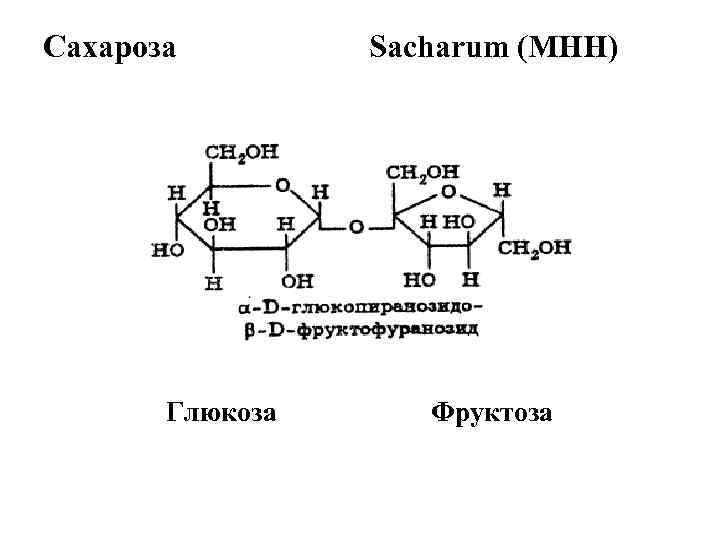 Сахароза Sacharum (МНН) Глюкоза Фруктоза
Сахароза Sacharum (МНН) Глюкоза Фруктоза
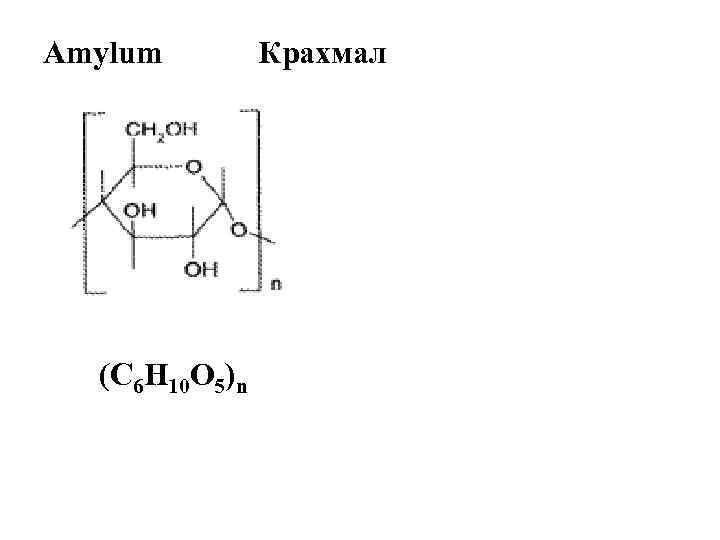 Amylum Крахмал (С 6 Н 10 О 5)n
Amylum Крахмал (С 6 Н 10 О 5)n


