Молекулярная физика.pptx
- Количество слайдов: 11
 Предмет и методы молекулярной физики. Физические основы молекулярнокинетической теории (МКТ). Идеальный газ как модельная термодинамическая система. Уравнение состояния. Основное уравнение МКТ идеального газа.
Предмет и методы молекулярной физики. Физические основы молекулярнокинетической теории (МКТ). Идеальный газ как модельная термодинамическая система. Уравнение состояния. Основное уравнение МКТ идеального газа.
 • Молекулярная физика – раздел курса общей физики, в котором изучаются макроскопические свойства вещества, обусловленные его молекулярным строением, характером движения молекул и силами, действующими между ними. • Задачи молекулярной физики решаются методами статистической механики, термодинамики и физической кинетики, они связаны с изучением движения и взаимодействия частиц (атомов, молекул, ионов), составляющих физические тела. • Молекулярная физика и термодинамика изучают поведение макросистем. Макросистемой называется система, состоящая из очень большого числа частиц. • Область физики, в которой изучаются физические свойства тел в различных агрегатных состояниях на основе рассмотрения их микроскопического (молекулярного) строения, называется молекулярной физикой; рассматриваются строение и свойства тел, фазовые превращения, явления переноса и др.
• Молекулярная физика – раздел курса общей физики, в котором изучаются макроскопические свойства вещества, обусловленные его молекулярным строением, характером движения молекул и силами, действующими между ними. • Задачи молекулярной физики решаются методами статистической механики, термодинамики и физической кинетики, они связаны с изучением движения и взаимодействия частиц (атомов, молекул, ионов), составляющих физические тела. • Молекулярная физика и термодинамика изучают поведение макросистем. Макросистемой называется система, состоящая из очень большого числа частиц. • Область физики, в которой изучаются физические свойства тел в различных агрегатных состояниях на основе рассмотрения их микроскопического (молекулярного) строения, называется молекулярной физикой; рассматриваются строение и свойства тел, фазовые превращения, явления переноса и др.
 Два метода молекулярной физики: Статистический Термодинамический В статистическом методе микроскопические величины, характеризующие движение молекулы, являются случайными. Для построения теории : гипотетическая модель механизма молекулярного движения и строения вещества-> разрабатываются методы нахождения плотности вероятностей величин -> вычисляют средние значения этих величин. Позволяет установить связь поведения системы в целом с поведением и свойствами отдельных частиц. В термодинамическом методе исследования вещества, в отличие от статистического, ставится своей задачей установление зависимости между наблюдаемыми макроскопическими (измеряемыми в опыте) величинами, (давление, температура, объем, концентрация, напряженность электр. или маг. поля и т. п. ) Позволяет изучать явления без знания внутренних их внутренних механизмов (и моделей).
Два метода молекулярной физики: Статистический Термодинамический В статистическом методе микроскопические величины, характеризующие движение молекулы, являются случайными. Для построения теории : гипотетическая модель механизма молекулярного движения и строения вещества-> разрабатываются методы нахождения плотности вероятностей величин -> вычисляют средние значения этих величин. Позволяет установить связь поведения системы в целом с поведением и свойствами отдельных частиц. В термодинамическом методе исследования вещества, в отличие от статистического, ставится своей задачей установление зависимости между наблюдаемыми макроскопическими (измеряемыми в опыте) величинами, (давление, температура, объем, концентрация, напряженность электр. или маг. поля и т. п. ) Позволяет изучать явления без знания внутренних их внутренних механизмов (и моделей).
 • Основой молекулярной физики является молекулярнокинетическая теория (МКТ), родоначальником которой был М. В. Ломносов. • Физические основы молекулярно-кинетической теории: 1. Все вещества в природе - жидкие, твердые, газообразные - состоят из мельчайших частиц (атомов и молекул). Молекулы химического вещества могут быть простыми и сложными, т. е. состоять из одного или нескольких атомов. Атом- наименьшая частица. Молекулы и атомы представляют собой электрически нейтральные частицы. При определенных условиях молекулы и атомы могут превращаться в положительные или отрицательные ионы. 2. Атомы и молекулы находятся в непрерывном хаотическом движении, которое называется тепловым движением 3. Частицы вещества взаимодействуют друг с другом: существуют силы притяжения или отталкивания, зависящие от расстояния между частицами. Силы имеют электрическую природу, так как гравитационная сила пренебрежимо мала.
• Основой молекулярной физики является молекулярнокинетическая теория (МКТ), родоначальником которой был М. В. Ломносов. • Физические основы молекулярно-кинетической теории: 1. Все вещества в природе - жидкие, твердые, газообразные - состоят из мельчайших частиц (атомов и молекул). Молекулы химического вещества могут быть простыми и сложными, т. е. состоять из одного или нескольких атомов. Атом- наименьшая частица. Молекулы и атомы представляют собой электрически нейтральные частицы. При определенных условиях молекулы и атомы могут превращаться в положительные или отрицательные ионы. 2. Атомы и молекулы находятся в непрерывном хаотическом движении, которое называется тепловым движением 3. Частицы вещества взаимодействуют друг с другом: существуют силы притяжения или отталкивания, зависящие от расстояния между частицами. Силы имеют электрическую природу, так как гравитационная сила пренебрежимо мала.
 • Экспериментальное подтверждение МКТ: • Существует множество молекул и известно 113 разных атомов- химических элементов. Атомы химических элементов, комбинируясь друг с другом создают миллионы существующих молекул. • Броуновское движение – тепловое движение мельчайших микроскопических частиц, взвешенных в газе или жидкости, под влиянием беспорядочных ударов молекул. Скорость беспорядочно меняется по модулю и амплитуде- траектория зигзагообразная кривая. • Диффузия- самопроизвольное проникновение и перемешивание частиц двух или более соприкасающихся веществ - проявление хаотического теплового движения.
• Экспериментальное подтверждение МКТ: • Существует множество молекул и известно 113 разных атомов- химических элементов. Атомы химических элементов, комбинируясь друг с другом создают миллионы существующих молекул. • Броуновское движение – тепловое движение мельчайших микроскопических частиц, взвешенных в газе или жидкости, под влиянием беспорядочных ударов молекул. Скорость беспорядочно меняется по модулю и амплитуде- траектория зигзагообразная кривая. • Диффузия- самопроизвольное проникновение и перемешивание частиц двух или более соприкасающихся веществ - проявление хаотического теплового движения.
 • Температура – физическая величина, характеризующая состояние термодинамического равновесия макроскопической системы. • Термодинамическая температура T и температура по Международной шкале t связаны соотношением: T=273. 16+t • Температура T=0 называется абсолютным нулем; 0 К недостижим, хотя приближение к нему сколь угодно близко возможно. • Атомный вес (атомная масса) A химического эелемнта — отношение массы атома этого элемента к 1/12 массы атома углерода С 12. Атомный вес С 12 равен 12. За единицу массы атомов и молекул принимается 1/12 массы атома изотопа углерода 12 C (с массовым числом 12). Она называется атомной единицей массы (а. е. м. ): 1 а. е. м. = 1, 66· 10– 27 кг. • Моль – это количество вещества, содержащее столько же частиц (молекул), сколько содержится атомов в 0, 012 кг углерода 12 C. Молекула углерода состоит из одного атома. • Таким образом, в одном моле любого вещества содержится одно и то же число частиц (молекул). Это число называется постоянной Авогадро NA = 6, 02· 1023 моль– 1.
• Температура – физическая величина, характеризующая состояние термодинамического равновесия макроскопической системы. • Термодинамическая температура T и температура по Международной шкале t связаны соотношением: T=273. 16+t • Температура T=0 называется абсолютным нулем; 0 К недостижим, хотя приближение к нему сколь угодно близко возможно. • Атомный вес (атомная масса) A химического эелемнта — отношение массы атома этого элемента к 1/12 массы атома углерода С 12. Атомный вес С 12 равен 12. За единицу массы атомов и молекул принимается 1/12 массы атома изотопа углерода 12 C (с массовым числом 12). Она называется атомной единицей массы (а. е. м. ): 1 а. е. м. = 1, 66· 10– 27 кг. • Моль – это количество вещества, содержащее столько же частиц (молекул), сколько содержится атомов в 0, 012 кг углерода 12 C. Молекула углерода состоит из одного атома. • Таким образом, в одном моле любого вещества содержится одно и то же число частиц (молекул). Это число называется постоянной Авогадро NA = 6, 02· 1023 моль– 1.
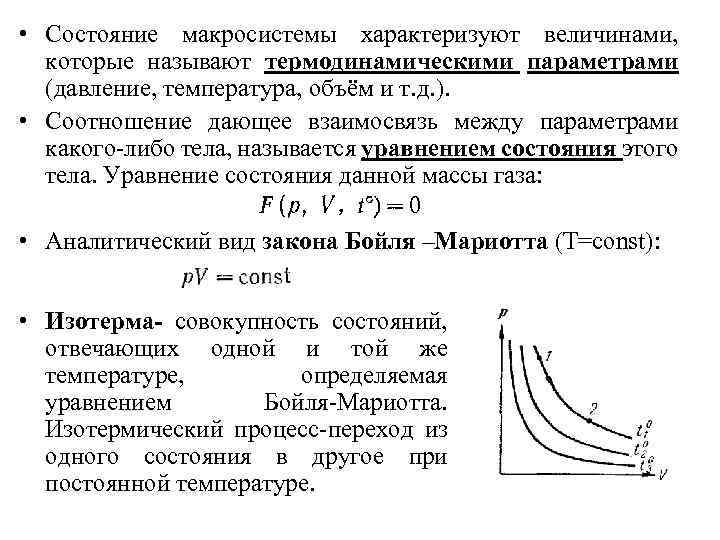 • Состояние макросистемы характеризуют величинами, которые называют термодинамическими параметрами (давление, температура, объём и т. д. ). • Соотношение дающее взаимосвязь между параметрами какого-либо тела, называется уравнением состояния этого тела. Уравнение состояния данной массы газа: • Аналитический вид закона Бойля –Мариотта (T=const): • Изотерма- совокупность состояний, отвечающих одной и той же температуре, определяемая уравнением Бойля-Мариотта. Изотермический процесс-переход из одного состояния в другое при постоянной температуре.
• Состояние макросистемы характеризуют величинами, которые называют термодинамическими параметрами (давление, температура, объём и т. д. ). • Соотношение дающее взаимосвязь между параметрами какого-либо тела, называется уравнением состояния этого тела. Уравнение состояния данной массы газа: • Аналитический вид закона Бойля –Мариотта (T=const): • Изотерма- совокупность состояний, отвечающих одной и той же температуре, определяемая уравнением Бойля-Мариотта. Изотермический процесс-переход из одного состояния в другое при постоянной температуре.
 • Закон Гей-Люссака-при неизменном давлении объём данной массы газа меняется линейно с температурой: • При постоянном объеме: • t° - температура по шкале Цельсия, V 0 -объем при 0° С, p 0 - давление при 0° С, α- коэффициент равный 1/273 1/град. • Процесс, протекающий при постоянном давлении, называется изобарическим. • Процесс, протекающий при неизменном объеме, называется изохорическим. Изобара Изохора
• Закон Гей-Люссака-при неизменном давлении объём данной массы газа меняется линейно с температурой: • При постоянном объеме: • t° - температура по шкале Цельсия, V 0 -объем при 0° С, p 0 - давление при 0° С, α- коэффициент равный 1/273 1/град. • Процесс, протекающий при постоянном давлении, называется изобарическим. • Процесс, протекающий при неизменном объеме, называется изохорическим. Изобара Изохора
 • Идеальный газ- математическая модель газа, для которой: • потенциальной энергией взаимодействия молекул можно пренебречь по сравнению с их кинетической энергией; • соударения частиц между собой и со стенками сосуда абсолютно упруги; • время взаимодействия между молекулами пренебрежимо мало по сравнению со средним временем между столкновениями. • На основе МКТ и свойства ид. газа приняты следующие допущения: • Диаметр молекулы << среднего расстояния между молекулами. • Импульс передается только при соударениях (силы притяжения между молекулами- отсутствуют, а силы отталкивания- возникают только при соударениях) • Суммарная энергия частиц газа постоянна (при A=0, нет теплопередачи) • Частицы газа движутся независимо друг от друга, давление газа на стенку равно полному импульсу, переданному при столкновении частиц со стенкой в единицу времени.
• Идеальный газ- математическая модель газа, для которой: • потенциальной энергией взаимодействия молекул можно пренебречь по сравнению с их кинетической энергией; • соударения частиц между собой и со стенками сосуда абсолютно упруги; • время взаимодействия между молекулами пренебрежимо мало по сравнению со средним временем между столкновениями. • На основе МКТ и свойства ид. газа приняты следующие допущения: • Диаметр молекулы << среднего расстояния между молекулами. • Импульс передается только при соударениях (силы притяжения между молекулами- отсутствуют, а силы отталкивания- возникают только при соударениях) • Суммарная энергия частиц газа постоянна (при A=0, нет теплопередачи) • Частицы газа движутся независимо друг от друга, давление газа на стенку равно полному импульсу, переданному при столкновении частиц со стенкой в единицу времени.
 • Воздух, азот, кислород, при комнатной температуре и атмосферном давлении близки к идеальному газу. • Объединим уравнения Бойля-Мариотта и Гей-Люссака. • Рассмотрим два состояния с параметрами: P 1, V 1, T 1 и P 2, V 2, T 2. • Из 1 в 1’- изотерма, • из 1’ в 2 -изохора. • Тогда: • Так как состояния 1 и 2 были взяты совершенно произвольно, то можно утверждать, что для любого состояния: • где В – постоянная данной массы газа.
• Воздух, азот, кислород, при комнатной температуре и атмосферном давлении близки к идеальному газу. • Объединим уравнения Бойля-Мариотта и Гей-Люссака. • Рассмотрим два состояния с параметрами: P 1, V 1, T 1 и P 2, V 2, T 2. • Из 1 в 1’- изотерма, • из 1’ в 2 -изохора. • Тогда: • Так как состояния 1 и 2 были взяты совершенно произвольно, то можно утверждать, что для любого состояния: • где В – постоянная данной массы газа.
 • В соответствии с законом Авогадро: килограмм- молекулы всех газов занимают при одинаковых условиях (т. е. при одинаковых температуре и давлении) одинаковый объём. Если количество газа равно одному киломолю, величина В будет одинакова для всех газов. • Обозначим соответствующую киломолю величину В буквой R, а объём V км, тогда: • -Уравнение Клапейрона: связывает параметры киломоля идеального газа и является уравнением состояния идеального газа, величина R-универсальная газовая постоянная: • Уравнение Клапейрона для любой массы газа m, учитывая V=Vкм*m/μ, μ- масса киломоля:
• В соответствии с законом Авогадро: килограмм- молекулы всех газов занимают при одинаковых условиях (т. е. при одинаковых температуре и давлении) одинаковый объём. Если количество газа равно одному киломолю, величина В будет одинакова для всех газов. • Обозначим соответствующую киломолю величину В буквой R, а объём V км, тогда: • -Уравнение Клапейрона: связывает параметры киломоля идеального газа и является уравнением состояния идеального газа, величина R-универсальная газовая постоянная: • Уравнение Клапейрона для любой массы газа m, учитывая V=Vкм*m/μ, μ- масса киломоля:


