2 алканы.ppt
- Количество слайдов: 34
 Предельные (насыщенные) углеводороды Углеводородами называются органические соединения, состоящие только из углерода и водорода. Углеводороды Предельные Ациклические (алканы) Непредельные Ароматические Циклические (циклоалканы) Предельными (насыщенными) называются углеводороды, в молекулах которых все углеродные атомы связаны друг с другом простой (одинарной) -связью. В молекулах насыщенных углеводородов атомы углерода находятся в первом гибридном состоянии (sp 3). Эти вещества не способны вступать в реакции присоединения, что и явилось причиной такого их названия. Простейший представитель – метан (СН 4). Гомологическая разница – СН 2. Гомологический ряд – Cn. H 2 n+2.
Предельные (насыщенные) углеводороды Углеводородами называются органические соединения, состоящие только из углерода и водорода. Углеводороды Предельные Ациклические (алканы) Непредельные Ароматические Циклические (циклоалканы) Предельными (насыщенными) называются углеводороды, в молекулах которых все углеродные атомы связаны друг с другом простой (одинарной) -связью. В молекулах насыщенных углеводородов атомы углерода находятся в первом гибридном состоянии (sp 3). Эти вещества не способны вступать в реакции присоединения, что и явилось причиной такого их названия. Простейший представитель – метан (СН 4). Гомологическая разница – СН 2. Гомологический ряд – Cn. H 2 n+2.
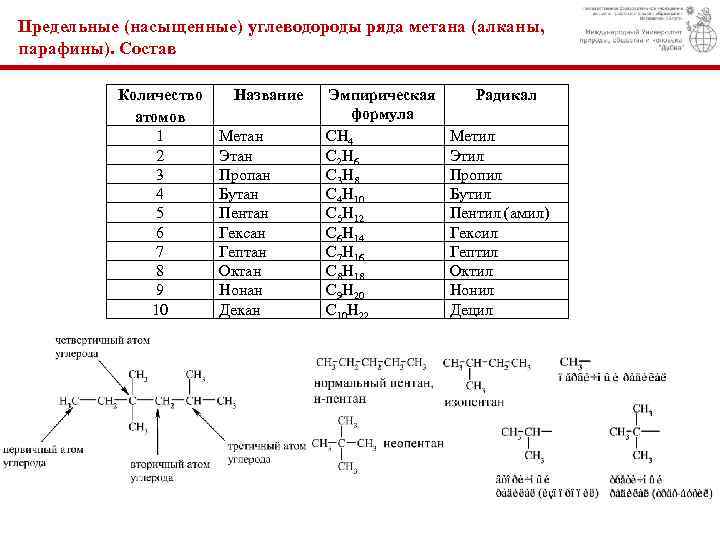 Предельные (насыщенные) углеводороды ряда метана (алканы, парафины). Состав Количество атомов 1 2 3 4 5 6 7 8 9 10 Название Метан Этан Пропан Бутан Пентан Гексан Гептан Октан Нонан Декан Эмпирическая формула CH 4 C 2 H 6 C 3 H 8 C 4 H 10 C 5 H 12 C 6 H 14 C 7 H 16 C 8 H 18 C 9 H 20 C 10 H 22 Радикал Метил Этил Пропил Бутил Пентил (амил) Гексил Гептил Октил Нонил Децил
Предельные (насыщенные) углеводороды ряда метана (алканы, парафины). Состав Количество атомов 1 2 3 4 5 6 7 8 9 10 Название Метан Этан Пропан Бутан Пентан Гексан Гептан Октан Нонан Декан Эмпирическая формула CH 4 C 2 H 6 C 3 H 8 C 4 H 10 C 5 H 12 C 6 H 14 C 7 H 16 C 8 H 18 C 9 H 20 C 10 H 22 Радикал Метил Этил Пропил Бутил Пентил (амил) Гексил Гептил Октил Нонил Децил
 Предельные (насыщенные) углеводороды ряда метана (алканы, парафины). Строение Все валентные углы в молекуле метана равны и составляют 109º 28. В молекуле любого гомолога метана цепочка углеродных атомов образует последовательность тетраэдров, соединенных друг с другом простыми связями С—С длиной 0, 154 нм. Энергия связи С—С составляет 355, 3 к. Дж/моль. Молекула октана. Стереохимия — часть химии, посвященная изучению пространственного строения молекул и влияния этого строения на физические и химические свойства веществ, на направление и скорость их реакций. Объектами изучения в стереохимии являются, главным образом, органические вещества, а из неорганических — в основном, комплексные и внутрикомплексные (хелатные) соединения.
Предельные (насыщенные) углеводороды ряда метана (алканы, парафины). Строение Все валентные углы в молекуле метана равны и составляют 109º 28. В молекуле любого гомолога метана цепочка углеродных атомов образует последовательность тетраэдров, соединенных друг с другом простыми связями С—С длиной 0, 154 нм. Энергия связи С—С составляет 355, 3 к. Дж/моль. Молекула октана. Стереохимия — часть химии, посвященная изучению пространственного строения молекул и влияния этого строения на физические и химические свойства веществ, на направление и скорость их реакций. Объектами изучения в стереохимии являются, главным образом, органические вещества, а из неорганических — в основном, комплексные и внутрикомплексные (хелатные) соединения.
 Предельные (насыщенные) углеводороды ряда метана (алканы, парафины). Строение Можно представить множество форм молекулы этана, отличающихся друг от друга взаимным поворотом углеродных тетраэдров вокруг соединяющей их связи углерод – углерод. Мерой поворота является торсионный (диэдральный) угол φ. Молекула этана. Торсионный угол. Такие различные формы молекул называются «конформациями» . Конформациями называют неидентичные расположения атомов в молекуле, полученные при вращении вокруг одной или нескольких простых связей без их разрыва. Конформерами, или поворотными изомерами, называют молекулы, находящиеся в наиболее устойчивых конформациях, при незначительном отклонении от которых атомы самопроизвольно возвращаются в первоначальное положение.
Предельные (насыщенные) углеводороды ряда метана (алканы, парафины). Строение Можно представить множество форм молекулы этана, отличающихся друг от друга взаимным поворотом углеродных тетраэдров вокруг соединяющей их связи углерод – углерод. Мерой поворота является торсионный (диэдральный) угол φ. Молекула этана. Торсионный угол. Такие различные формы молекул называются «конформациями» . Конформациями называют неидентичные расположения атомов в молекуле, полученные при вращении вокруг одной или нескольких простых связей без их разрыва. Конформерами, или поворотными изомерами, называют молекулы, находящиеся в наиболее устойчивых конформациях, при незначительном отклонении от которых атомы самопроизвольно возвращаются в первоначальное положение.
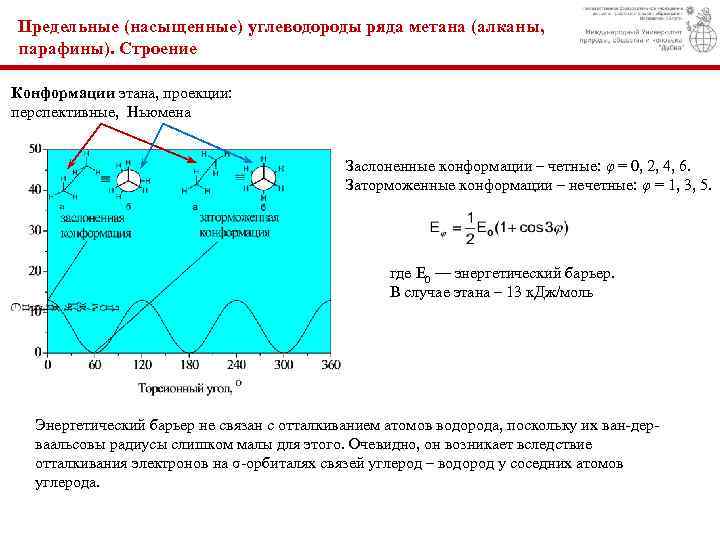 Предельные (насыщенные) углеводороды ряда метана (алканы, парафины). Строение Конформации этана, проекции: перспективные, Ньюмена Заслоненные конформации – четные: φ = 0, 2, 4, 6. Заторможенные конформации – нечетные: φ = 1, 3, 5. где E 0 — энергетический барьер. В случае этана – 13 к. Дж/моль Энергетический барьер не связан с отталкиванием атомов водорода, поскольку их ван-дерваальсовы радиусы слишком малы для этого. Очевидно, он возникает вследствие отталкивания электронов на σ-орбиталях связей углерод – водород у соседних атомов углерода.
Предельные (насыщенные) углеводороды ряда метана (алканы, парафины). Строение Конформации этана, проекции: перспективные, Ньюмена Заслоненные конформации – четные: φ = 0, 2, 4, 6. Заторможенные конформации – нечетные: φ = 1, 3, 5. где E 0 — энергетический барьер. В случае этана – 13 к. Дж/моль Энергетический барьер не связан с отталкиванием атомов водорода, поскольку их ван-дерваальсовы радиусы слишком малы для этого. Очевидно, он возникает вследствие отталкивания электронов на σ-орбиталях связей углерод – водород у соседних атомов углерода.
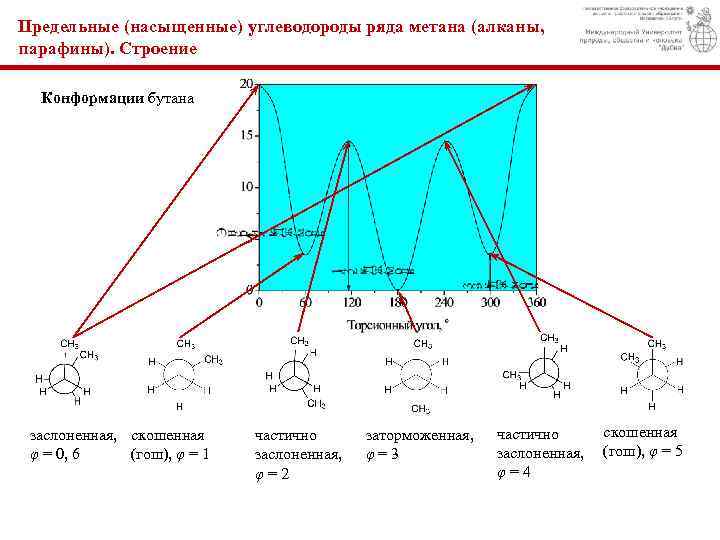 Предельные (насыщенные) углеводороды ряда метана (алканы, парафины). Строение Конформации бутана заслоненная, скошенная φ = 0, 6 (гош), φ = 1 частично заслоненная, φ = 2 заторможенная, φ = 3 скошенная частично заслоненная, (гош), φ = 5 φ = 4
Предельные (насыщенные) углеводороды ряда метана (алканы, парафины). Строение Конформации бутана заслоненная, скошенная φ = 0, 6 (гош), φ = 1 частично заслоненная, φ = 2 заторможенная, φ = 3 скошенная частично заслоненная, (гош), φ = 5 φ = 4
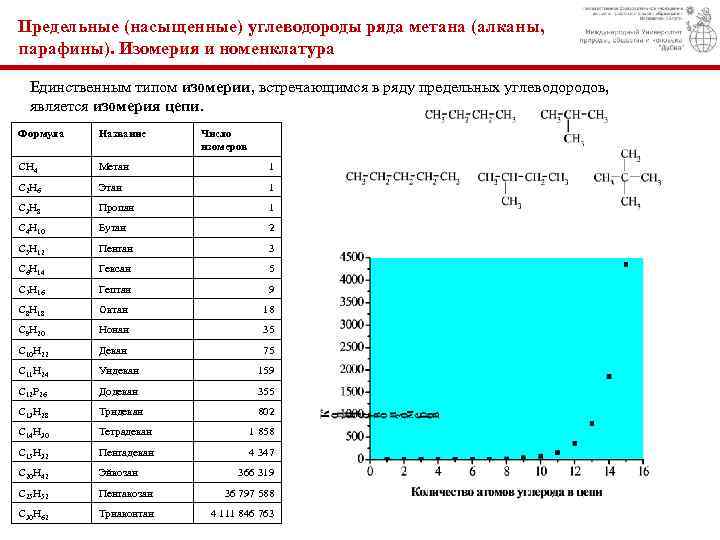 Предельные (насыщенные) углеводороды ряда метана (алканы, парафины). Изомерия и номенклатура Единственным типом изомерии, встречающимся в ряду предельных углеводородов, является изомерия цепи. Формула Название Число изомеров СН 4 Метан 1 С 2 Н 6 Этан 1 С 3 Н 8 Пропан 1 С 4 Н 10 Бутан 2 С 5 Н 12 Пентан 3 С 6 Н 14 Гексан 5 С 7 Н 16 Гептан 9 С 8 Н 18 Октан 18 С 9 Н 20 Нонан 35 С 10 Н 22 Декан 75 С 11 Н 24 Ундекан 159 С 12 Р 26 Додекан 355 С 13 Н 28 Тридекан 802 С 14 Н 30 Тетрадекан 1 858 С 15 Н 32 Пентадекан 4 347 С 20 Н 42 Эйкозан С 25 Н 52 Пентакозан 36 797 588 С 30 Н 62 Триаконтан 4 111 846 763 366 319
Предельные (насыщенные) углеводороды ряда метана (алканы, парафины). Изомерия и номенклатура Единственным типом изомерии, встречающимся в ряду предельных углеводородов, является изомерия цепи. Формула Название Число изомеров СН 4 Метан 1 С 2 Н 6 Этан 1 С 3 Н 8 Пропан 1 С 4 Н 10 Бутан 2 С 5 Н 12 Пентан 3 С 6 Н 14 Гексан 5 С 7 Н 16 Гептан 9 С 8 Н 18 Октан 18 С 9 Н 20 Нонан 35 С 10 Н 22 Декан 75 С 11 Н 24 Ундекан 159 С 12 Р 26 Додекан 355 С 13 Н 28 Тридекан 802 С 14 Н 30 Тетрадекан 1 858 С 15 Н 32 Пентадекан 4 347 С 20 Н 42 Эйкозан С 25 Н 52 Пентакозан 36 797 588 С 30 Н 62 Триаконтан 4 111 846 763 366 319
 Предельные (насыщенные) углеводороды ряда метана (алканы, парафины). Изомерия и номенклатура Номенклатура Одновалентные остатки – алкилы (метан – метил, изопропан – изопропил). Двухвалентные (обе валентности у одного С-атома): -ан на -илиден (этан – этилиден, исключение: метан – метилен). Трехвалентные: -ан на -идин (метан – метин, этан – этилидин). 1. Выбирают наиболее длинную (главную) неразветвленную цепь углеродных атомов: 2. Нумеруют С-атомы главной цепи. Атому, связанному с заместителем, присваивают наименьшее значение. В случае нескольких заместителей, направление нумерации выбирают таким образом, чтобы сумма номеров положений заместителей была минимальна: 3. Указывают положение и название заместителя. В случае нескольких заместителей, указывают положение и название каждого из них в алфавитном порядке. Количество одинаковых заместителей обозначают греческими числительными (ди-, три-, тетра- и т. д. ). 4. Называют углеводород, соответствующий главной цепи:
Предельные (насыщенные) углеводороды ряда метана (алканы, парафины). Изомерия и номенклатура Номенклатура Одновалентные остатки – алкилы (метан – метил, изопропан – изопропил). Двухвалентные (обе валентности у одного С-атома): -ан на -илиден (этан – этилиден, исключение: метан – метилен). Трехвалентные: -ан на -идин (метан – метин, этан – этилидин). 1. Выбирают наиболее длинную (главную) неразветвленную цепь углеродных атомов: 2. Нумеруют С-атомы главной цепи. Атому, связанному с заместителем, присваивают наименьшее значение. В случае нескольких заместителей, направление нумерации выбирают таким образом, чтобы сумма номеров положений заместителей была минимальна: 3. Указывают положение и название заместителя. В случае нескольких заместителей, указывают положение и название каждого из них в алфавитном порядке. Количество одинаковых заместителей обозначают греческими числительными (ди-, три-, тетра- и т. д. ). 4. Называют углеводород, соответствующий главной цепи:
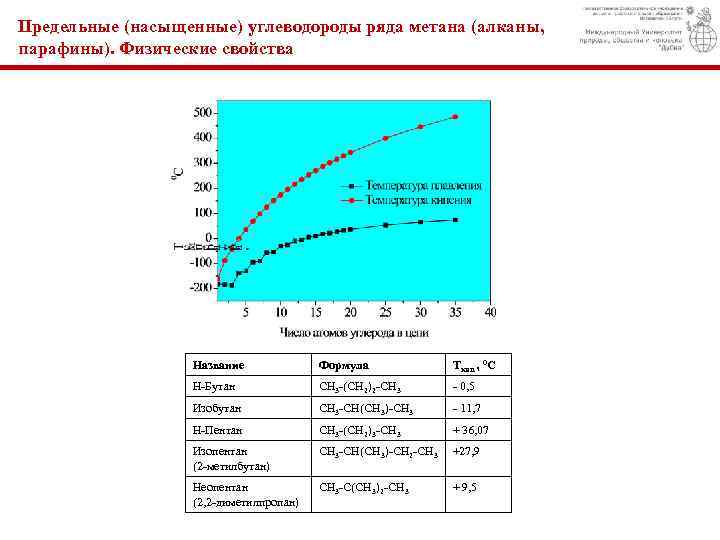 Предельные (насыщенные) углеводороды ряда метана (алканы, парафины). Физические свойства Название Формула Ткип. , 0 С Н-Бутан СН 3 -(СН 2)2 -СН 3 - 0, 5 Изобутан СН 3 -СН(СН 3)-СН 3 - 11, 7 Н-Пентан СН 3 -(СН 2)3 -СН 3 + 36, 07 Изопентан (2 -метилбутан) СН 3 -СН(СН 3)-СН 2 -СН 3 +27, 9 Неопентан (2, 2 -диметилпропан) СН 3 -С(СН 3)2 -СН 3 + 9, 5
Предельные (насыщенные) углеводороды ряда метана (алканы, парафины). Физические свойства Название Формула Ткип. , 0 С Н-Бутан СН 3 -(СН 2)2 -СН 3 - 0, 5 Изобутан СН 3 -СН(СН 3)-СН 3 - 11, 7 Н-Пентан СН 3 -(СН 2)3 -СН 3 + 36, 07 Изопентан (2 -метилбутан) СН 3 -СН(СН 3)-СН 2 -СН 3 +27, 9 Неопентан (2, 2 -диметилпропан) СН 3 -С(СН 3)2 -СН 3 + 9, 5
 Предельные (насыщенные) углеводороды ряда метана (алканы, парафины). Нахождение в природе и способы получения Природные источники: нефть, природные и попутные газы, нефти, угли, горный воск (озокерит). Анаэробное разложение растительных остатков приводит к образованию метана: Промышленные способы: 1. Переработка нефти, природных и попутных газов (см. термические превращения); 2. Взаимодействие оксида углерода (II) с водородом (синтез-газ), метод Фишера-Тропша: 3. Каталитическая гидрогенизация каменного угля: Способы направленного получения алканов. 1. Синтез метана 1. 1. Гидролиз карбида алюминия: 1. 2. Синтез метана из сероуглерода по Бертло:
Предельные (насыщенные) углеводороды ряда метана (алканы, парафины). Нахождение в природе и способы получения Природные источники: нефть, природные и попутные газы, нефти, угли, горный воск (озокерит). Анаэробное разложение растительных остатков приводит к образованию метана: Промышленные способы: 1. Переработка нефти, природных и попутных газов (см. термические превращения); 2. Взаимодействие оксида углерода (II) с водородом (синтез-газ), метод Фишера-Тропша: 3. Каталитическая гидрогенизация каменного угля: Способы направленного получения алканов. 1. Синтез метана 1. 1. Гидролиз карбида алюминия: 1. 2. Синтез метана из сероуглерода по Бертло:
 Предельные (насыщенные) углеводороды ряда метана (алканы, парафины). Нахождение в природе и способы получения 2. Общие способы получения 2. 1. Сплавление солей монокарбоновых кислот с едкими щелочами: 2. 2. Синтез Кольбе – электролиз солей монокарбоновых кислот. Метод применим для получения алканов с четным числом углеродных атомов: 2. 3. Гидролиз металлоорганических соединений Li, Na, Mg, Zn: 2. 4. Каталитическое гидрирование непредельных углеводородов:
Предельные (насыщенные) углеводороды ряда метана (алканы, парафины). Нахождение в природе и способы получения 2. Общие способы получения 2. 1. Сплавление солей монокарбоновых кислот с едкими щелочами: 2. 2. Синтез Кольбе – электролиз солей монокарбоновых кислот. Метод применим для получения алканов с четным числом углеродных атомов: 2. 3. Гидролиз металлоорганических соединений Li, Na, Mg, Zn: 2. 4. Каталитическое гидрирование непредельных углеводородов:
 Предельные (насыщенные) углеводороды ряда метана (алканы, парафины). Нахождение в природе и способы получения 2. 5. Восстановление производных алканов иодистоводородной кислотой: 2. 6. Синтез Вюрца: Побочные продукты 2. 7. Реакция галогеналканов с диалкилкупратами лития:
Предельные (насыщенные) углеводороды ряда метана (алканы, парафины). Нахождение в природе и способы получения 2. 5. Восстановление производных алканов иодистоводородной кислотой: 2. 6. Синтез Вюрца: Побочные продукты 2. 7. Реакция галогеналканов с диалкилкупратами лития:
 Предельные (насыщенные) углеводороды ряда метана (алканы, парафины). Химические свойства Алканы – чрезвычайно устойчивые соединения Классификация реакций и реагентов по способу разрыва и образования химической связи. Гетеролитический (ионный) механизм – разрыв связи – образование связи Гомолитический (свободнорадикальный) механизм – разрыв связи – образование связи Частицы с неспаренными электронами – свободные радикалы. Разрыв связи С - С Разрыв связи С - Н
Предельные (насыщенные) углеводороды ряда метана (алканы, парафины). Химические свойства Алканы – чрезвычайно устойчивые соединения Классификация реакций и реагентов по способу разрыва и образования химической связи. Гетеролитический (ионный) механизм – разрыв связи – образование связи Гомолитический (свободнорадикальный) механизм – разрыв связи – образование связи Частицы с неспаренными электронами – свободные радикалы. Разрыв связи С - С Разрыв связи С - Н
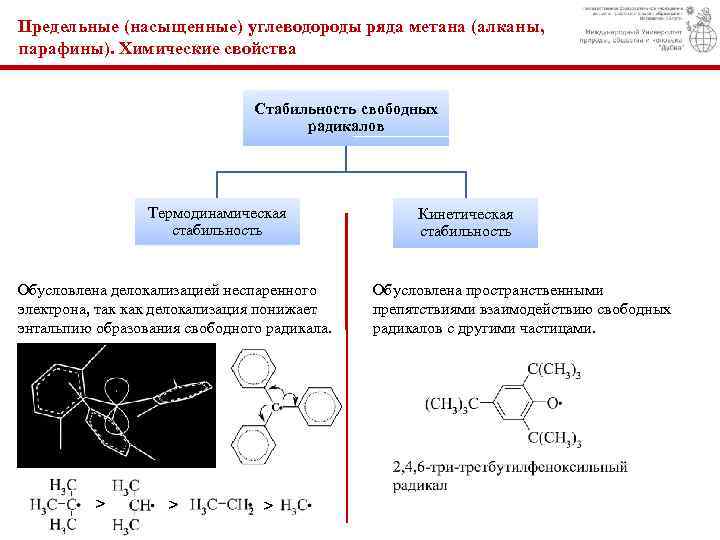 Предельные (насыщенные) углеводороды ряда метана (алканы, парафины). Химические свойства Стабильность свободных радикалов Термодинамическая стабильность Обусловлена делокализацией неспаренного электрона, так как делокализация понижает энтальпию образования свободного радикала. ˃ ˃ ˃ Кинетическая стабильность Обусловлена пространственными препятствиями взаимодействию свободных радикалов с другими частицами.
Предельные (насыщенные) углеводороды ряда метана (алканы, парафины). Химические свойства Стабильность свободных радикалов Термодинамическая стабильность Обусловлена делокализацией неспаренного электрона, так как делокализация понижает энтальпию образования свободного радикала. ˃ ˃ ˃ Кинетическая стабильность Обусловлена пространственными препятствиями взаимодействию свободных радикалов с другими частицами.
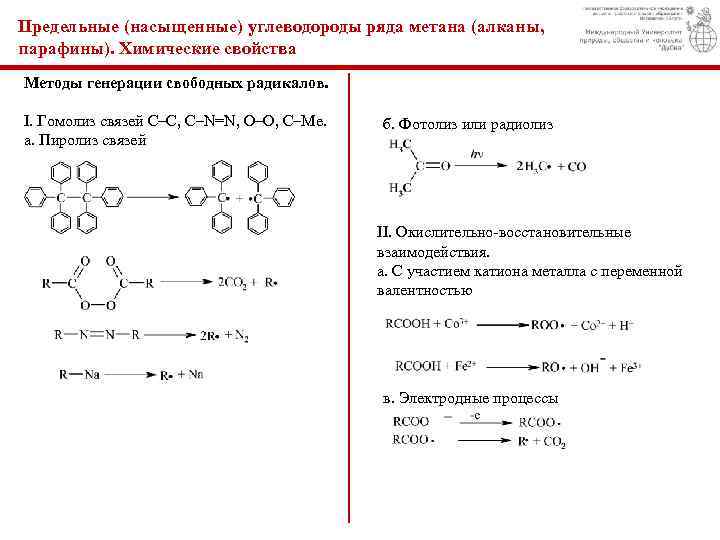 Предельные (насыщенные) углеводороды ряда метана (алканы, парафины). Химические свойства Методы генерации свободных радикалов. I. Гомолиз связей C–C, C–N=N, O–O, C–Me. а. Пиролиз связей б. Фотолиз или радиолиз II. Окислительно-восстановительные взаимодействия. а. С участием катиона металла с переменной валентностью в. Электродные процессы
Предельные (насыщенные) углеводороды ряда метана (алканы, парафины). Химические свойства Методы генерации свободных радикалов. I. Гомолиз связей C–C, C–N=N, O–O, C–Me. а. Пиролиз связей б. Фотолиз или радиолиз II. Окислительно-восстановительные взаимодействия. а. С участием катиона металла с переменной валентностью в. Электродные процессы
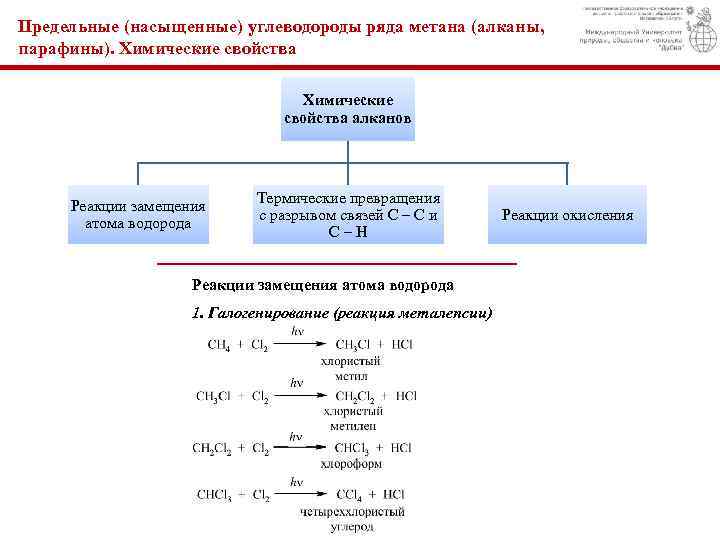 Предельные (насыщенные) углеводороды ряда метана (алканы, парафины). Химические свойства алканов Реакции замещения атома водорода Термические превращения с разрывом связей С – С и С – Н Реакции замещения атома водорода 1. Галогенирование (реакция металепсии) Реакции окисления
Предельные (насыщенные) углеводороды ряда метана (алканы, парафины). Химические свойства алканов Реакции замещения атома водорода Термические превращения с разрывом связей С – С и С – Н Реакции замещения атома водорода 1. Галогенирование (реакция металепсии) Реакции окисления
 Предельные (насыщенные) углеводороды ряда метана (алканы, парафины). Химические свойства Механизм радикального замещения (SR) Зарождение цепи k. Cтрет. ˃k. Cвтор. ˃k. Cперв. Устойчивость алкильных радикалов ˃ Развитие (рост) цепи Обрыв цепи ˃
Предельные (насыщенные) углеводороды ряда метана (алканы, парафины). Химические свойства Механизм радикального замещения (SR) Зарождение цепи k. Cтрет. ˃k. Cвтор. ˃k. Cперв. Устойчивость алкильных радикалов ˃ Развитие (рост) цепи Обрыв цепи ˃
 Предельные (насыщенные) углеводороды ряда метана (алканы, парафины). Химические свойства 2. Нитрование – это введение нитрогруппы (–NO 2). HNO 3 (HO–NO 2). Реакция Коновалова: k. Cтрет. ˃k. Cвтор. ˃k. Cперв. 3. Сульфирование – это введение сульфогруппы (–SO 3 H). H 2 SO 4 (HO–SO 3 H). 4. Сульфохлорирование – это введение сульфохлоридной группы (–SO 2 Cl). Протекает при облучении реакционной массы ультрафиолетом или в присутствии инициаторов свободных радикалов.
Предельные (насыщенные) углеводороды ряда метана (алканы, парафины). Химические свойства 2. Нитрование – это введение нитрогруппы (–NO 2). HNO 3 (HO–NO 2). Реакция Коновалова: k. Cтрет. ˃k. Cвтор. ˃k. Cперв. 3. Сульфирование – это введение сульфогруппы (–SO 3 H). H 2 SO 4 (HO–SO 3 H). 4. Сульфохлорирование – это введение сульфохлоридной группы (–SO 2 Cl). Протекает при облучении реакционной массы ультрафиолетом или в присутствии инициаторов свободных радикалов.
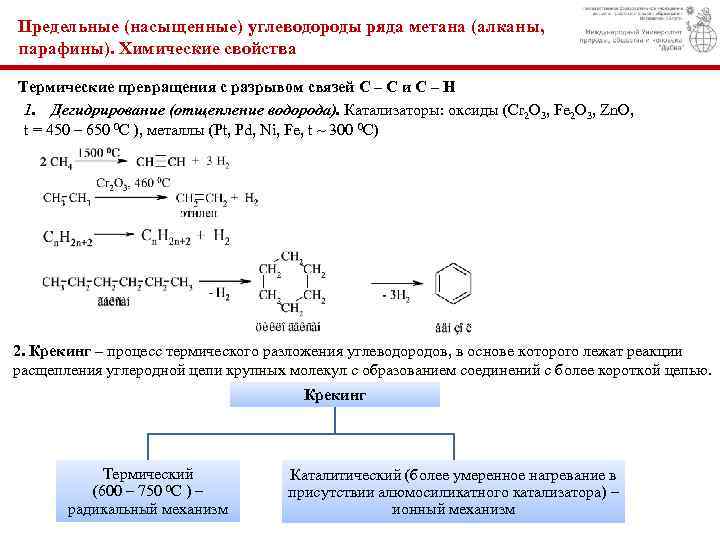 Предельные (насыщенные) углеводороды ряда метана (алканы, парафины). Химические свойства Термические превращения с разрывом связей С – С и С – Н 1. Дегидрирование (отщепление водорода). Катализаторы: оксиды (Cr 2 O 3, Fe 2 O 3, Zn. O, t = 450 – 650 0 C ), металлы (Pt, Pd, Ni, Fe, t ~ 300 0 C) 2. Крекинг – процесс термического разложения углеводородов, в основе которого лежат реакции расщепления углеродной цепи крупных молекул с образованием соединений с более короткой цепью. Крекинг Термический Каталитический (более умеренное нагревание в (600 – 750 0 C ) – присутствии алюмосиликатного катализатора) – радикальный механизм ионный механизм
Предельные (насыщенные) углеводороды ряда метана (алканы, парафины). Химические свойства Термические превращения с разрывом связей С – С и С – Н 1. Дегидрирование (отщепление водорода). Катализаторы: оксиды (Cr 2 O 3, Fe 2 O 3, Zn. O, t = 450 – 650 0 C ), металлы (Pt, Pd, Ni, Fe, t ~ 300 0 C) 2. Крекинг – процесс термического разложения углеводородов, в основе которого лежат реакции расщепления углеродной цепи крупных молекул с образованием соединений с более короткой цепью. Крекинг Термический Каталитический (более умеренное нагревание в (600 – 750 0 C ) – присутствии алюмосиликатного катализатора) – радикальный механизм ионный механизм
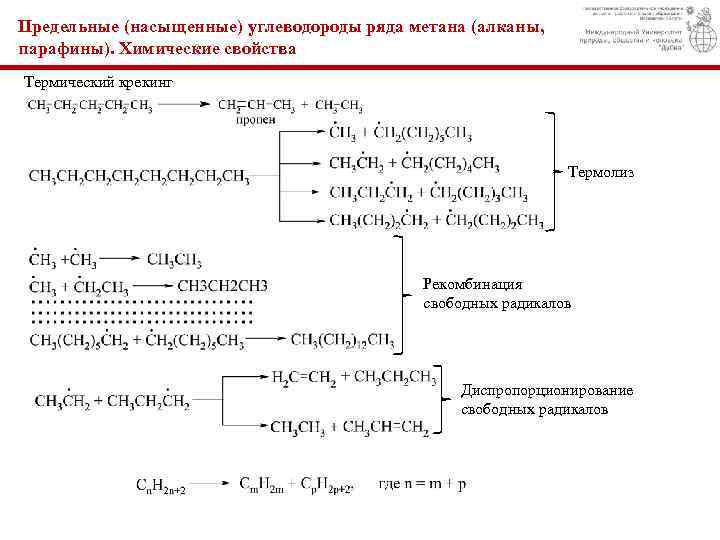 Предельные (насыщенные) углеводороды ряда метана (алканы, парафины). Химические свойства Термический крекинг Термолиз Рекомбинация свободных радикалов Диспропорционирование свободных радикалов
Предельные (насыщенные) углеводороды ряда метана (алканы, парафины). Химические свойства Термический крекинг Термолиз Рекомбинация свободных радикалов Диспропорционирование свободных радикалов
 Предельные (насыщенные) углеводороды ряда метана (алканы, парафины). Химические свойства 3. Изомеризация, основа каталитического риформинга бензиновых фракций нефти, происходит при нагревании с кислотами Льюиса (Al. Cl 3, Al. Br 3) в присутствии каталитических количеств алкенов и воды).
Предельные (насыщенные) углеводороды ряда метана (алканы, парафины). Химические свойства 3. Изомеризация, основа каталитического риформинга бензиновых фракций нефти, происходит при нагревании с кислотами Льюиса (Al. Cl 3, Al. Br 3) в присутствии каталитических количеств алкенов и воды).
 Предельные (насыщенные) углеводороды ряда метана (алканы, парафины). Химические свойства и применение Окисление 1. Горение 2. Неполное окисление Алкан [O] Спирт [O] Кетон [O] Карбоновая кислота
Предельные (насыщенные) углеводороды ряда метана (алканы, парафины). Химические свойства и применение Окисление 1. Горение 2. Неполное окисление Алкан [O] Спирт [O] Кетон [O] Карбоновая кислота
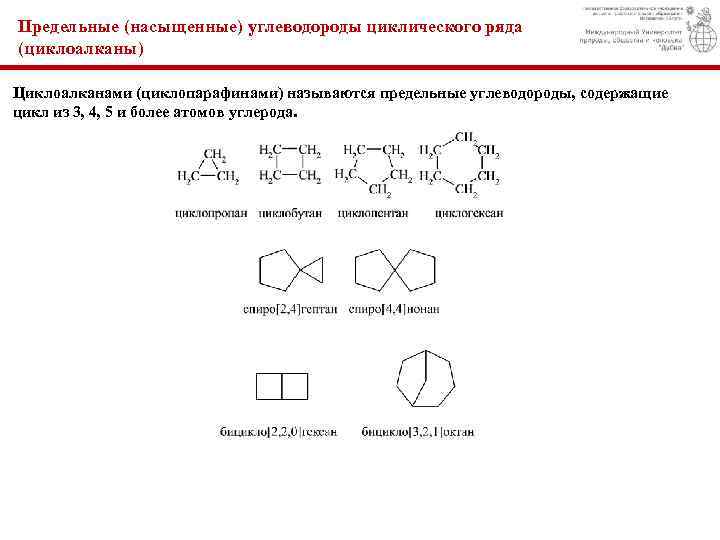 Предельные (насыщенные) углеводороды циклического ряда (циклоалканы) Циклоалканами (циклопарафинами) называются предельные углеводороды, содержащие цикл из 3, 4, 5 и более атомов углерода.
Предельные (насыщенные) углеводороды циклического ряда (циклоалканы) Циклоалканами (циклопарафинами) называются предельные углеводороды, содержащие цикл из 3, 4, 5 и более атомов углерода.
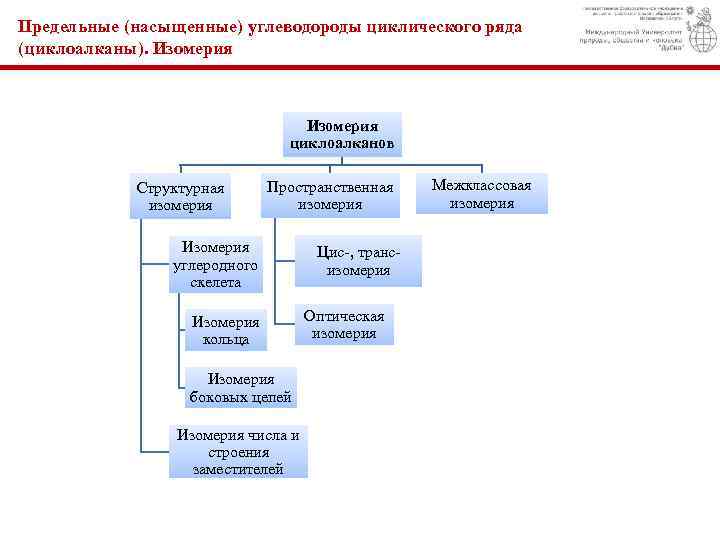 Предельные (насыщенные) углеводороды циклического ряда (циклоалканы). Изомерия циклоалканов Структурная изомерия Пространственная изомерия Изомерия углеродного скелета Изомерия кольца Изомерия боковых цепей Изомерия числа и строения заместителей Цис-, трансизомерия Оптическая изомерия Межклассовая изомерия
Предельные (насыщенные) углеводороды циклического ряда (циклоалканы). Изомерия циклоалканов Структурная изомерия Пространственная изомерия Изомерия углеродного скелета Изомерия кольца Изомерия боковых цепей Изомерия числа и строения заместителей Цис-, трансизомерия Оптическая изомерия Межклассовая изомерия
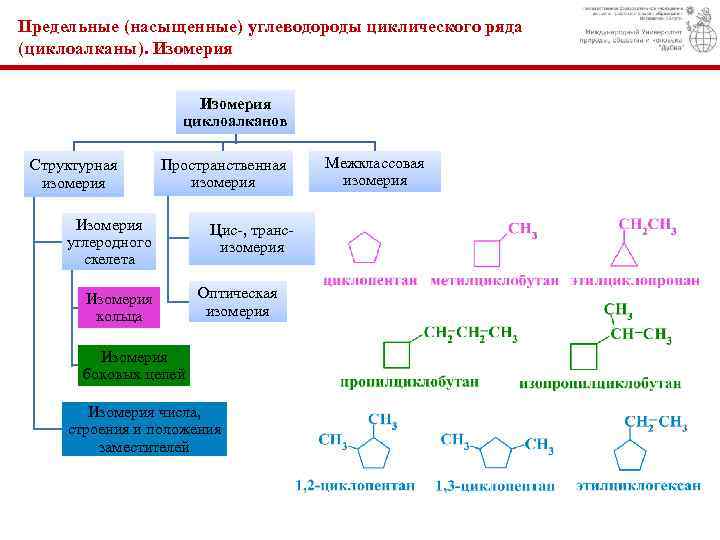 Предельные (насыщенные) углеводороды циклического ряда (циклоалканы). Изомерия циклоалканов Структурная изомерия Пространственная изомерия Изомерия углеродного скелета Изомерия кольца Цис-, трансизомерия Оптическая изомерия Изомерия боковых цепей Изомерия числа, строения и положения заместителей Межклассовая изомерия
Предельные (насыщенные) углеводороды циклического ряда (циклоалканы). Изомерия циклоалканов Структурная изомерия Пространственная изомерия Изомерия углеродного скелета Изомерия кольца Цис-, трансизомерия Оптическая изомерия Изомерия боковых цепей Изомерия числа, строения и положения заместителей Межклассовая изомерия
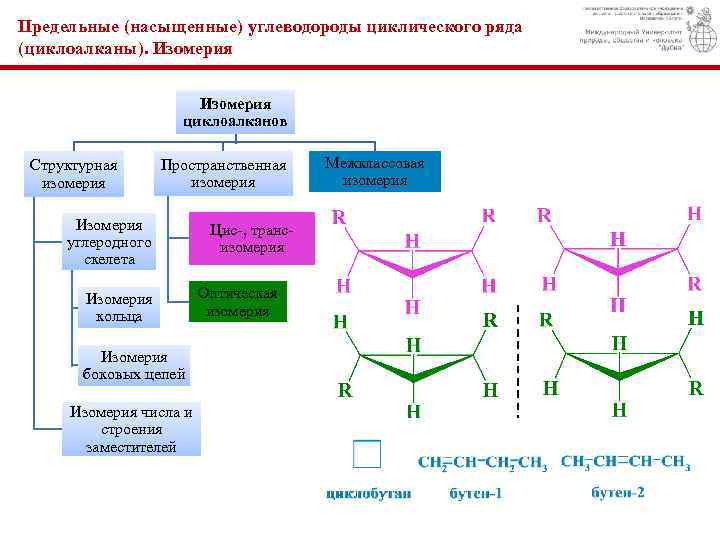 Предельные (насыщенные) углеводороды циклического ряда (циклоалканы). Изомерия циклоалканов Структурная изомерия Пространственная изомерия Изомерия углеродного скелета Изомерия кольца Изомерия боковых цепей Изомерия числа и строения заместителей Цис-, трансизомерия Оптическая изомерия Межклассовая изомерия
Предельные (насыщенные) углеводороды циклического ряда (циклоалканы). Изомерия циклоалканов Структурная изомерия Пространственная изомерия Изомерия углеродного скелета Изомерия кольца Изомерия боковых цепей Изомерия числа и строения заместителей Цис-, трансизомерия Оптическая изомерия Межклассовая изомерия
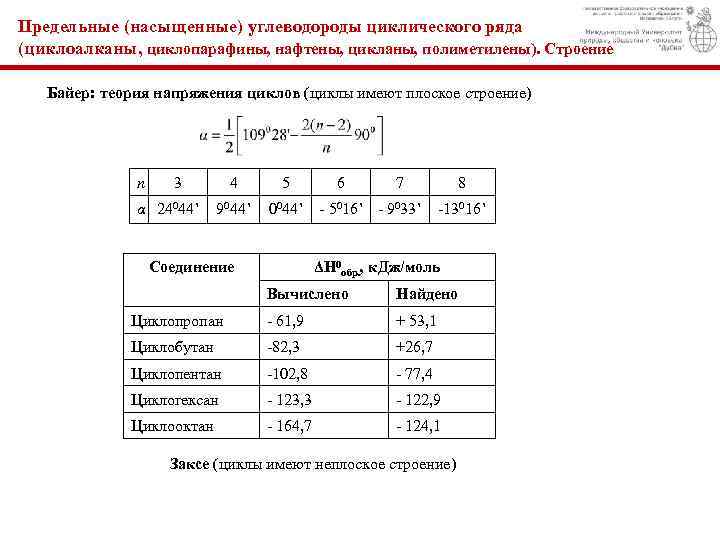 Предельные (насыщенные) углеводороды циклического ряда (циклоалканы, циклопаpафины, нафтены, цикланы, полиметилены). Строение Байер: теория напряжения циклов (циклы имеют плоское строение) n 3 α 24044’ 4 5 9044’ 0044’ Соединение 6 7 - 5016’ - 9033’ 8 -13016’ ΔН 0 обр. , к. Дж/моль Вычислено Найдено Циклопропан - 61, 9 + 53, 1 Циклобутан -82, 3 +26, 7 Циклопентан -102, 8 - 77, 4 Циклогексан - 123, 3 - 122, 9 Циклооктан - 164, 7 - 124, 1 Заксе (циклы имеют неплоское строение)
Предельные (насыщенные) углеводороды циклического ряда (циклоалканы, циклопаpафины, нафтены, цикланы, полиметилены). Строение Байер: теория напряжения циклов (циклы имеют плоское строение) n 3 α 24044’ 4 5 9044’ 0044’ Соединение 6 7 - 5016’ - 9033’ 8 -13016’ ΔН 0 обр. , к. Дж/моль Вычислено Найдено Циклопропан - 61, 9 + 53, 1 Циклобутан -82, 3 +26, 7 Циклопентан -102, 8 - 77, 4 Циклогексан - 123, 3 - 122, 9 Циклооктан - 164, 7 - 124, 1 Заксе (циклы имеют неплоское строение)
 Предельные (насыщенные) углеводороды циклического ряда (циклоалканы, циклопаpафины, нафтены, цикланы, полиметилены). Строение Факторы, влияющие на внутреннюю энергию циклических молекул Угловое напряжение (напряжение Байера) – изменение валентных углов. E 1=kθα 2 kθ~0, 0840 Напряжение заслонения (напряжение Питцера, напряжение заслонения) – вынужденное отклонение от наиболее выгодной нечетной конформации. φ E 2=5, 87(1 – cos 3φ) Трансаннулярное напряжение (напряжение Прелога) – взаимное отталкивание сближенных атомов и других фрагментов). В случае атомов водорода: E 3=4, 19(104 -2 r – 49, 2 r – 6) Напряжение связей – изменение межатомных расстояний. E 4 = kdx, x » 1.
Предельные (насыщенные) углеводороды циклического ряда (циклоалканы, циклопаpафины, нафтены, цикланы, полиметилены). Строение Факторы, влияющие на внутреннюю энергию циклических молекул Угловое напряжение (напряжение Байера) – изменение валентных углов. E 1=kθα 2 kθ~0, 0840 Напряжение заслонения (напряжение Питцера, напряжение заслонения) – вынужденное отклонение от наиболее выгодной нечетной конформации. φ E 2=5, 87(1 – cos 3φ) Трансаннулярное напряжение (напряжение Прелога) – взаимное отталкивание сближенных атомов и других фрагментов). В случае атомов водорода: E 3=4, 19(104 -2 r – 49, 2 r – 6) Напряжение связей – изменение межатомных расстояний. E 4 = kdx, x » 1.
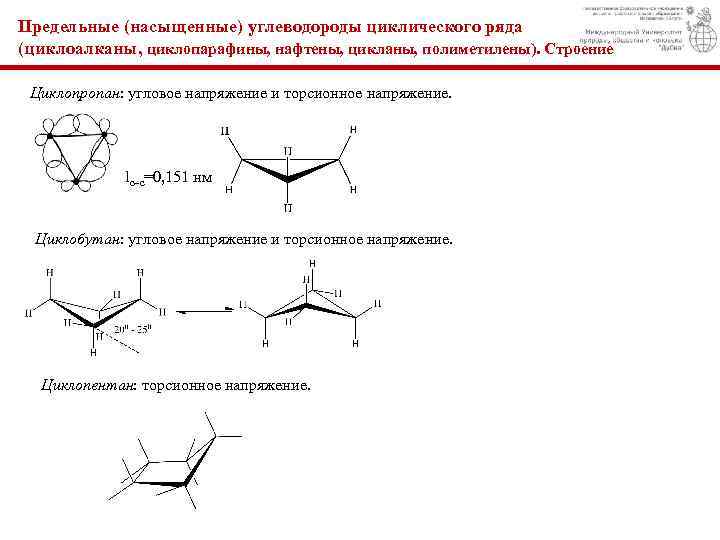 Предельные (насыщенные) углеводороды циклического ряда (циклоалканы, циклопаpафины, нафтены, цикланы, полиметилены). Строение Циклопропан: угловое напряжение и торсионное напряжение. lc–c=0, 151 нм Циклобутан: угловое напряжение и торсионное напряжение. Циклопентан: торсионное напряжение.
Предельные (насыщенные) углеводороды циклического ряда (циклоалканы, циклопаpафины, нафтены, цикланы, полиметилены). Строение Циклопропан: угловое напряжение и торсионное напряжение. lc–c=0, 151 нм Циклобутан: угловое напряжение и торсионное напряжение. Циклопентан: торсионное напряжение.
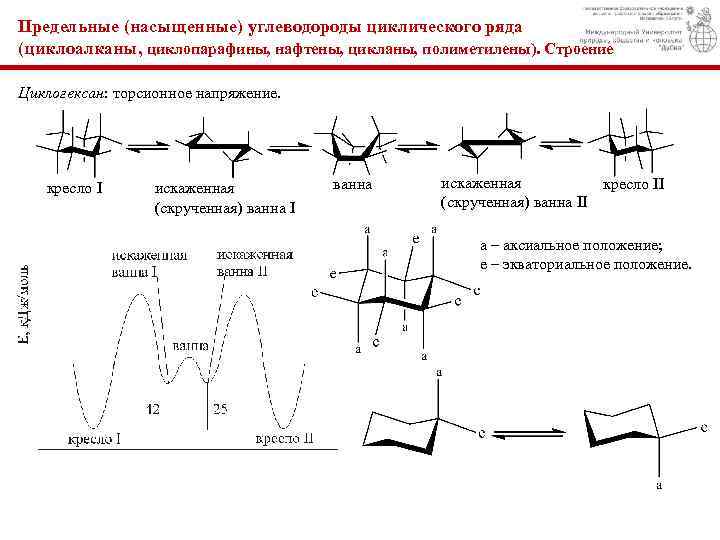 Предельные (насыщенные) углеводороды циклического ряда (циклоалканы, циклопаpафины, нафтены, цикланы, полиметилены). Строение Циклогексан: торсионное напряжение. кресло I искаженная (скрученная) ванна I ванна искаженная (скрученная) ванна II кресло II а – аксиальное положение; е – экваториальное положение.
Предельные (насыщенные) углеводороды циклического ряда (циклоалканы, циклопаpафины, нафтены, цикланы, полиметилены). Строение Циклогексан: торсионное напряжение. кресло I искаженная (скрученная) ванна I ванна искаженная (скрученная) ванна II кресло II а – аксиальное положение; е – экваториальное положение.
 Предельные (насыщенные) углеводороды циклического ряда (циклоалканы, циклопаpафины, нафтены, цикланы, полиметилены). Получение 1. Нахождение в природе: некоторые виды нефти. 2. Синтетические способы. 2. 1. Гидрирование ароматических и циклических ненасыщенных соединений. 2. 2. Взаимодействие дигалогенпроизводных предельных углеводородов с металлами
Предельные (насыщенные) углеводороды циклического ряда (циклоалканы, циклопаpафины, нафтены, цикланы, полиметилены). Получение 1. Нахождение в природе: некоторые виды нефти. 2. Синтетические способы. 2. 1. Гидрирование ароматических и циклических ненасыщенных соединений. 2. 2. Взаимодействие дигалогенпроизводных предельных углеводородов с металлами
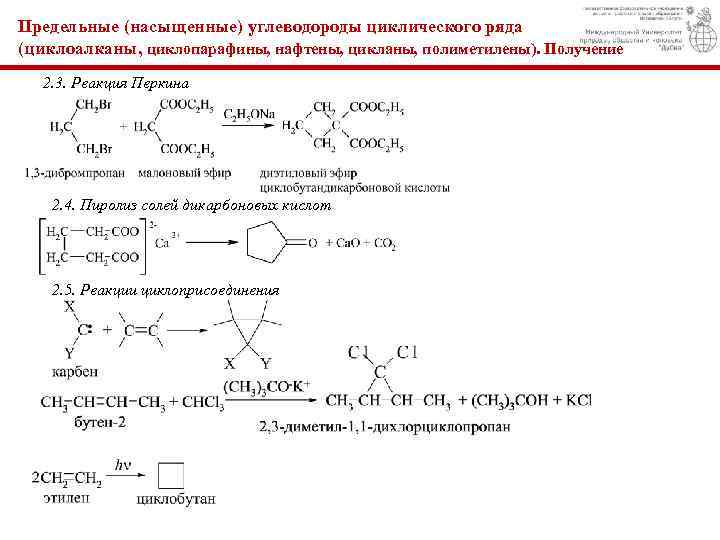 Предельные (насыщенные) углеводороды циклического ряда (циклоалканы, циклопаpафины, нафтены, цикланы, полиметилены). Получение 2. 3. Реакция Перкина 2. 4. Пиролиз солей дикарбоновых кислот 2. 5. Реакции циклоприсоединения
Предельные (насыщенные) углеводороды циклического ряда (циклоалканы, циклопаpафины, нафтены, цикланы, полиметилены). Получение 2. 3. Реакция Перкина 2. 4. Пиролиз солей дикарбоновых кислот 2. 5. Реакции циклоприсоединения
 Предельные (насыщенные) углеводороды циклического ряда (циклоалканы, циклопаpафины, нафтены, цикланы, полиметилены). Свойства Особенности химических свойств циклов различного размера: • малые циклы вступают в реакции присоединения; • средние циклы похожи на алканы. 1. Гидрирование. 2. Гидрогалогенирование (циклопропан, циклобутан и их гомологи). - по правилу Марковникова
Предельные (насыщенные) углеводороды циклического ряда (циклоалканы, циклопаpафины, нафтены, цикланы, полиметилены). Свойства Особенности химических свойств циклов различного размера: • малые циклы вступают в реакции присоединения; • средние циклы похожи на алканы. 1. Гидрирование. 2. Гидрогалогенирование (циклопропан, циклобутан и их гомологи). - по правилу Марковникова
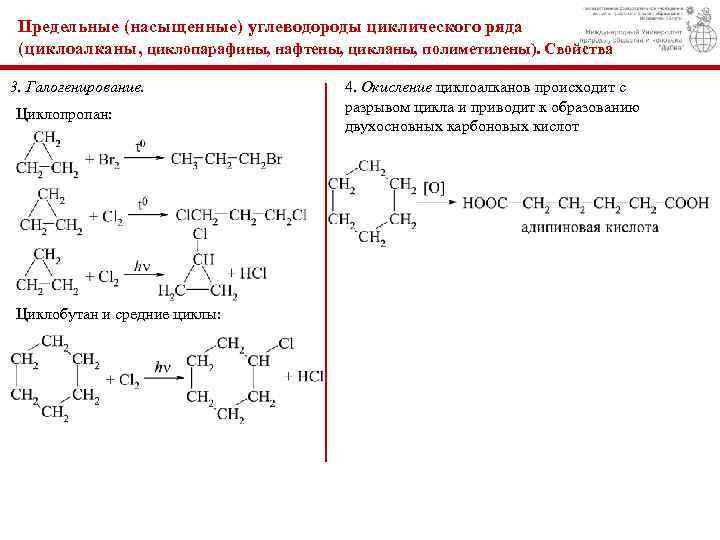 Предельные (насыщенные) углеводороды циклического ряда (циклоалканы, циклопаpафины, нафтены, цикланы, полиметилены). Свойства 3. Галогенирование. Циклопропан: Циклобутан и средние циклы: 4. Окисление циклоалканов происходит с разрывом цикла и приводит к образованию двухосновных карбоновых кислот
Предельные (насыщенные) углеводороды циклического ряда (циклоалканы, циклопаpафины, нафтены, цикланы, полиметилены). Свойства 3. Галогенирование. Циклопропан: Циклобутан и средние циклы: 4. Окисление циклоалканов происходит с разрывом цикла и приводит к образованию двухосновных карбоновых кислот


