Поздравляет Вас с началом нового (2016-2017) учебного года


Поздравляет Вас с началом нового (2016-2017) учебного года Желаем больших успехов в учебе и личной жизни Кафедра биохимии


Борис Иванович Ильин-Какуев – первый заведующий кафедрой биохимии

Профессор П.А.Верболович Второй зав. Кафедрой

Профессор Полосухина Татьяна Яковлевна

Третьим заведующим кафедрой стала профессор Светлана Михайловна Плешкова. Выпускница нашего университета, в те времена института


На сегодняшний день заведующим кафедрой стал профессор Шарипов Камалидин Орынбаевич


Лектор – доцент Ерджанова Сара Саид-Алиевна

Тема: Введение в биохимию. Понятие о строении и функциях белков. Классификация белков. Сложные белки: ГП, ХП, НП Лекция № 1

Ознакомить студентов с наукой биохимией значением ее для врачей. Дать понятие о строении белков и их функциях. Рассмотреть строение и роль сложных белков: гликопротеинов, хромопротеинов и нуклеопротеинов Цель:

1. Введение в биохимию 2. Понятие о строении и функциях белков 3. Сложные белки: гликопротеины, хромопротеины, нуклеопротеины – строение, роль, представители План лекции

Что такое биохимия? Итак, существует множество определений этого термина: Введение в биохимию

Википедии это: – наука о химическом составе живых клеток и организмов и о химических процессах, лежащих в основе их жизнедеятельности. Биохимия по энциклопедии Кольера это: – наука, которая описывает на языке химии строение и функции живых организмов. Биохимия по энциклопедии Брокгауза и Ефрона это: – греч., учение о химических процессах в живых существах. Биохимия (биол. химия) по XuMuK.ru: – изучает хим. состав и структуру в-в, содержащихся в живых организмах, пути и способы регуляции их метаболизма, а также энергетич. обеспечение процессов, происходящих в клетке и организме. Биохимия (биологическая, или физиологическая химия) по

Однако все эти определения не дают ответ на вечный вопрос моих студентов: Зачем врачу нужна биологическая химия?

Отступая от прямого ответа на поставленный вопрос, обращу внимание читателя на ту лавину знаний, которая обрушивается на студента-медика в первые три года пребывания в медицинском университете. Часть этих знаний как бы не имеет отношения к медицине – латинский язык, химия, физика, гуманитарные дисциплины, но их задача – сформировать представление о целостности нашего мира, о его единстве и неразрывности явлений.

Еще одна группа наук – медицинские науки, это анатомия, гистология, физиология и биохимия человека, патоанатомия и патофизиология, фармакология. Их значение можно сравнить с древним представлением об устройстве мира. Анатомия, гистология, цитология – океан, без которого все остальное не имеет значения. Биохимия, физиология и патофизиология – три кита в этом океане. Они сообщают будущему врачу о принципах функционирования организма, о химических процессах в живой материи. Их задача – проложить мосты в клинические дисциплины, дать врачу возможность понять суть процесса, вызывающего болезнь.

Все клинические дисциплины базируются на этих трех китах – биохимии, физиологии и патофизиологии. Убираем китов – и остаются только больное место и ничем необоснованные гадания о типе болезни, ее причинах и способах лечения.

Биохимия – это наука, изучающая химический состав живых организмов и химические процессы, которым подвергаются внутренние метаболиты. Открытия в области энзимологии, молекулярной генетики, биоэнергетики выдвинули биохимию в ряд фундаментальных дисциплин и сделали мощным оружием в решении многих проблем биологии, медицины, животноводства и растениеводства. Введение в биохимию
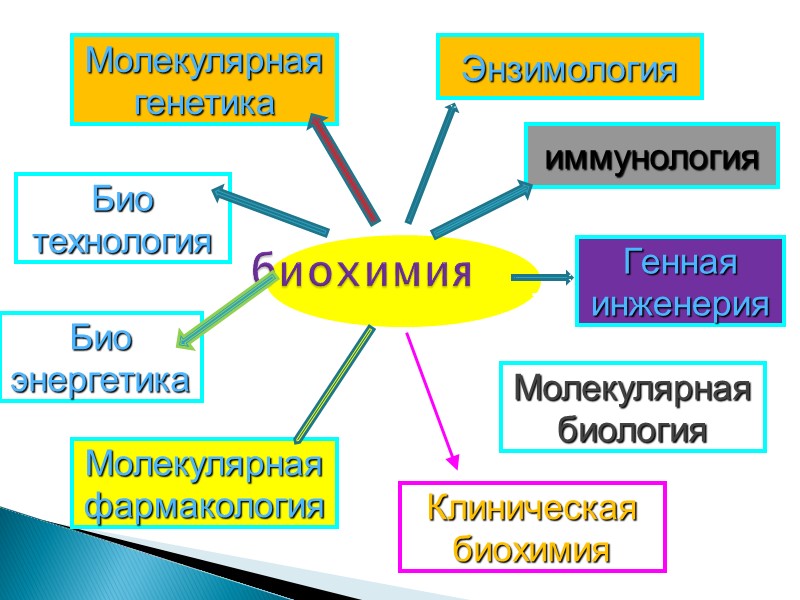
биохимия Молекулярная биология Био технология Био энергетика Молекулярная генетика иммунология Энзимология Молекулярная фармакология Генная инженерия Клиническая биохимия

Биохимия дает врачу сведения, благодаря которым можно разбираться в химизме процессов, протекающих в больном и здоровом организме, использовать показатели метаболитов и ферментов для диагностики и контроля. Она позволяет управлять этими процессами, рационально использовать терапию.

Белки (протеины) – высокомолекулярные биополимеры, состоящие из остатков α-аминокислот БЕЛКИ
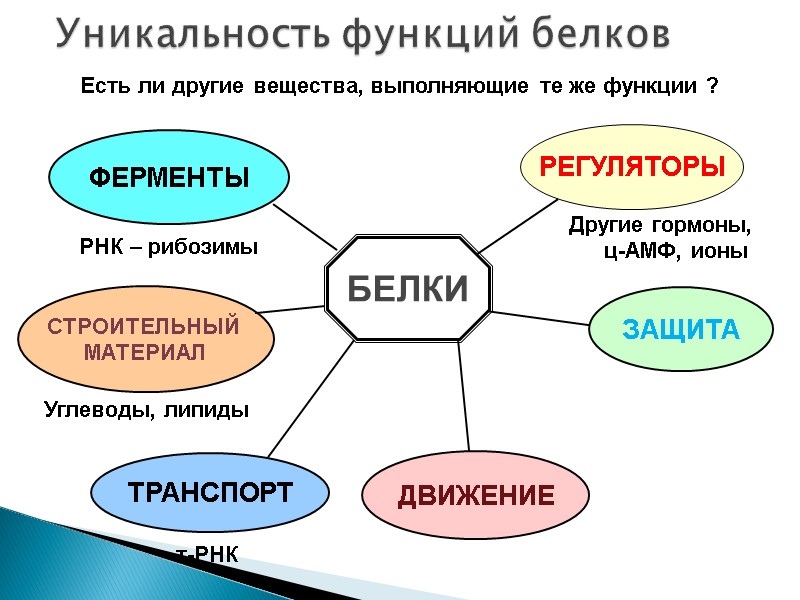
БЕЛКИ РЕГУЛЯТОРЫ ФЕРМЕНТЫ СТРОИТЕЛЬНЫЙ МАТЕРИАЛ ТРАНСПОРТ ДВИЖЕНИЕ ЗАЩИТА Уникальность функций белков Углеводы, липиды РНК – рибозимы Другие гормоны, ц-АМФ, ионы т-РНК Есть ли другие вещества, выполняющие те же функции ?

Белки выполняют все функции, кроме одной – ИНФОРМАЦИОННОЙ не способны к самовоспроизведению

Название происходит от греческого слова protos – первый, важнейший. В природе имеется около 1010- 1012 различных белков, обеспечивающих существование 106 живых существ.. Строение и функции белков

Многообразие белков

С белками связаны все признаки, отличающие живое от неживого: воспроизводимость себе подобных, сократимость, обмен веществ, высокий уровень структурной организации, способность преобразовывать и использовать энергию, ускорять химические реакции.

Белки

Белки состоят из 20 базовых аминокислот
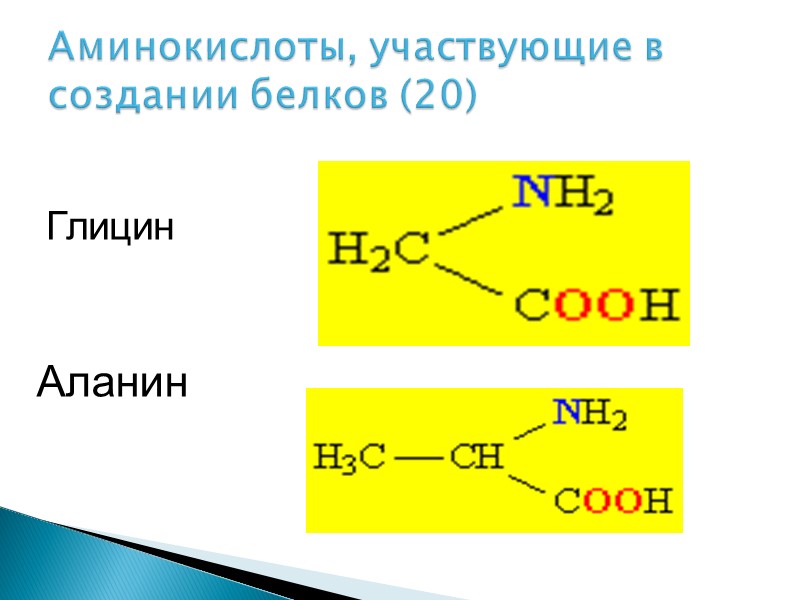
Аминокислоты, участвующие в создании белков (20) Глицин Аланин
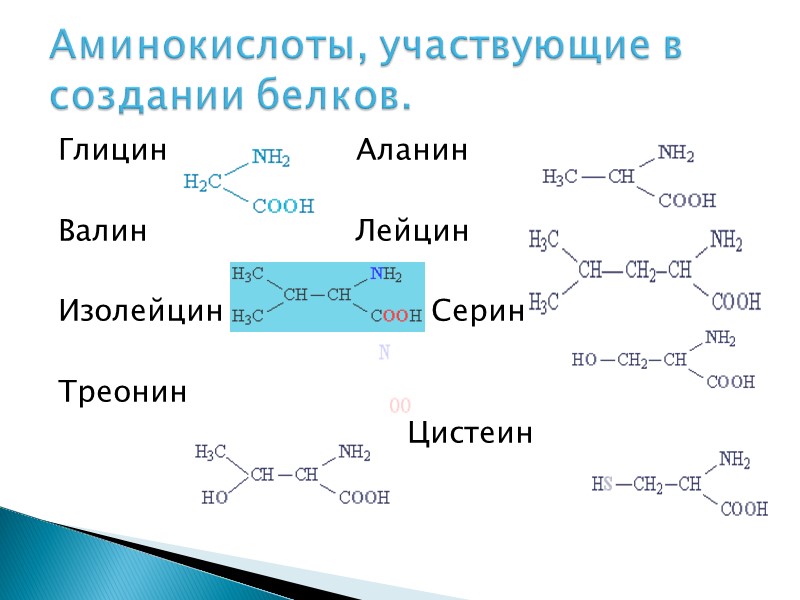
Глицин Аланин Валин Лейцин Изолейцин Серин Треонин Цистеин Аминокислоты, участвующие в создании белков.

МЕТИОНИН ЛИЗИН АРГИНИН АСПАРАГИН АСПАРАГИНОВАЯ КИСЛОТА ГЛУТАМИНОВАЯ КИСЛОТА

Функции белков

белки определяют структуру тела растений, микроорганизмов, животных, входят в состав клеточных и субклеточных мембран. Широко известны такие структурные белки как коллаген и эластин соединительной ткани, оссеин костей, кератин волос и ногтей, обеспечивающие прочность и структуру тканей. Структурная (опорная, пластическая)

Каталитическая – белки обладают свойствами биокатализаторов (ферментов), ускоряя течение химических процессов в организме.

Транспортная – белки переносят с кровью и другими биологическими жидкостями транспорту через мембраны

Защитная – обеспечивают иммунологические реакции. А) защита организма при ранении путем свертывания крови. Б) связывание токсических эндогенных и экзогенных веществ В) антитела. Г) интерфероны – блокируют синтез вирусных белков

Регуляторная –гормоны, ферменты, БАВ, пептиды -являются белками.

Сократительная – способность к передвижению в пространстве, работа сердца, дыхание, перистальтика кишечника, сужение и расширение сосудов обеспечиваются благодаря сократительным белкам мышечной ткани. Сократительная функция присуща и белкам цитоскелета, благодаря которым обеспечиваются важнейшие процессы жизнедеятельности клеток.

Электротрансформирующая функция заключается в превращении электрической и осмотической энергии в энергию макроэргов. 10-20% энергопотребления у человека, обеспечивается за счет окисления аминокислот

Белки участвуют в процессе передачи генетической информации.

Классификация белков

БЕЛКИ простые Сложные Простые белки - протеины, молекула которых состоит только из аминокислотных остатков Сложные белки -, состоят из простого белка и добавочной небелковой группы, называемой простетической.
БЕЛКИ Простые белки - протеины, молекула которых состоит только из аминокислотных остатков Сложные белки состоят из простого белка и добавочной небелковой группы, называемой простетической.
простые белки по растворимости и физико-химическим свойствам подразделяются на глобулярные и фибриллярные.

Глобулярные имеют шарообразную форму молекулы. Фибриллярные белки характеризуются волокнистой структурой, делятся на растворимые и нерастворимые. К первой подгруппе относятся миозин, актин, фибриноген, ко второй – склеропротеины (протеиноиды – кератины, эластины, коллагены).

1.Протеины Альбумины Глобулины Протамины Гистоны Склеропротеины Простые белка

протеиды, состоящие из простого белка и добавочной небелковой группы, называемой простетической. Сложные белки

Фосфопротеины Металлопротеины Липопротеины Хромопротеины Гликопротеины Нуклеопротеины Сложные белки

ФП это сложные белки, обособленной простетической группы не имеют. Ее роль выполняют остатки фосфорной кислоты, связанные сложноэфирными связями с гидроксильными группами оксиаминокислот: сер, тре, тир. К одному остатку аминокислоты может присоединиться несколько фрагментов фосфорной кислоты фосфопротеины
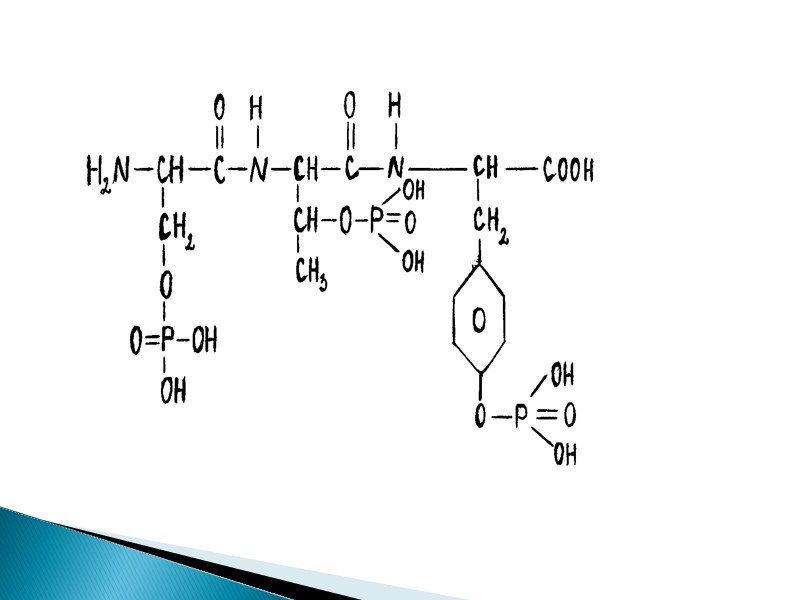

ФП – это полноценные белки с большой молекулярной массой при нагревании не свертываются (термостабильны), в воде не растворимы, но хорошо растворимы в разбавленных растворах солей и щелочей. Имеют кислый характер (ИЭТ ~ 4,7) из-за остатков фосфорной кислоты, поэтому осаждаются кислотами.

они служат пластическим материалом (источники незаменимых аминокислот и фосфора), играют важную роль в росте организма, поэтому особенно нужны детям. Значение ФП

казеин молока (Р ~ 1%), вителлин и фосвитин – ФП яичного желтка (Р ~ 10%), ихтуллин – в икре рыб (фосфора более 10%). Казеин (от лат caseus – сыр) – основной белок молока, составляет около 80% от белков коровьего молока. Энамелины, фосвитины, обнаруживаются в эмали зуба Представители

это сложные белки, содержащие в молекуле металлы, но в отличие от ХП здесь металлы свободны и выполняют роль простетической группы. Связь между белком и ионами металлов может быть прочной и непрочной у различных МП., Металлопротеины

) ферритин, содержат 20% трехвалентного (окисленного) железа и выполняют роль депо железа в организме. Белок откладывается в печени и селезенке; Представители

б) трансферрин, содержит около 0,13% железа и выполняет роль переносчика железа (главным образом в составе бета-глобулинов), которое в молекуле связано непрочно с ОН-группой тирозина; Представители МП

В)гемосидерин Роль этого белка изучена не достаточно. Это водонерастворимый комплекс, содержащий также УГВ и нуклеотиды. Содержится в РЭС печени и селезенки; Представители МП

г). Роль этого белка в транспорте меди, также обладает ферментативной активностью. церулоплазмин иначе называется феррооксидазой. В составе находится 6-8 атомов двухвалентной меди. церулоплазмин

глутатионпероксидаза содержит селен; митохондриальная супероксиддисмутаза содержит марганец, а цитозольная форма этого фермента содержит медь или цинк

железосерные белки выполняют роль дополнительных компонентов в процессе окисления;

б)металлотионеины находятся в печени, почках и кишечнике. Выполняют роль антитоксическую (обезвреживание тяжелых металлов).

К МП относят ряд ферментов, Например, карбоангидраза и карбоксипептидаза содержат цинк; купрум-фермент и цитохромоксидаза содержат медь

К МП относят также ряд ферментов, для которых металл является «мостиком» между белковой и небелковой частями, или непосредственно участвует в выполнении каталитической функции.

карбоангидраза содержит цинк, для активности фосфотрансфераз и киназ необходимы ионы магния и марганца, тирозиназа и ЦХО содержат медь.

это сложные комплексы, включающие в себя большие количества непрочно связанных между собой молекул различных представителей липидов (ФЛ, ХСН, ТАГ, СЖК, СФЛ). Липопротеины (ЛП)
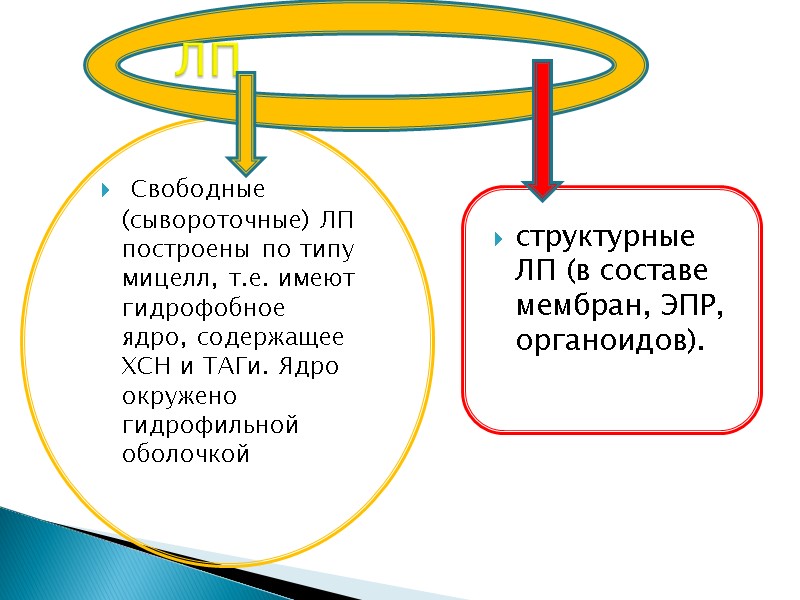
Свободные (сывороточные) ЛП построены по типу мицелл, т.е. имеют гидрофобное ядро, содержащее ХСН и ТАГи. Ядро окружено гидрофильной оболочкой структурные ЛП (в составе мембран, ЭПР, органоидов). ЛП

Ядро окружено гидрофильной оболочкой из белков и ФЛ. Хиломикроны (ХМ) Различают ЛПОНП пребета-ЛП ЛПНП , бета-ЛП ЛПВП, альфа-ЛП которые отличаются разным содержанием липидов и белка. ЛП – это транспортная форма липидов. Свободные ЛП
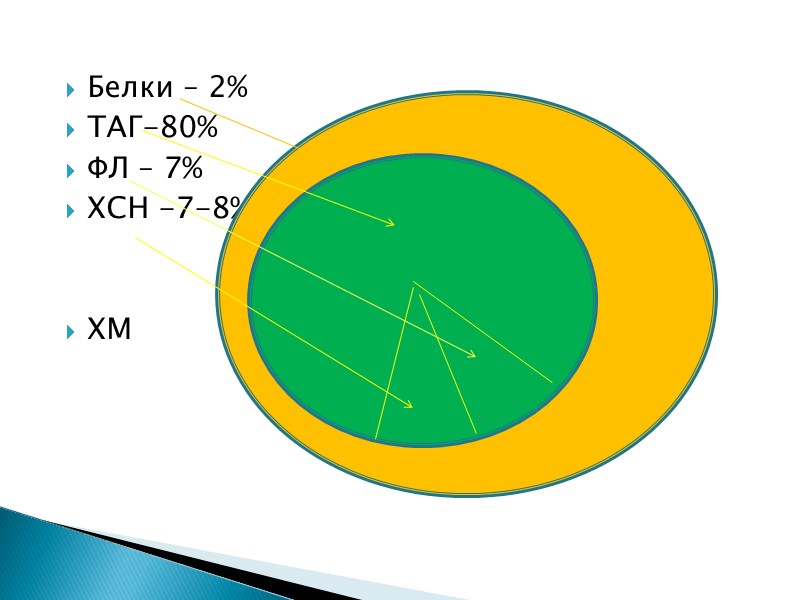
Белки – 2% ТАГ-80% ФЛ – 7% ХСН -7-8% ХМ

Гликопротеиды получили название от слова «glucos» - сладкий, т. к. было установлено, что они содержат углеводы. Простетическая группа представлена различными углеводами и их производными, связь ее с белком ковалентная, углеводпептидная. Гликопротеиды (ГП)

Все гликопротеиды обладают высокой молекулярной массой (до нескольких млн. Д), Обладают кислыми свойствами, растворимы в воде, слабых растворах нейтральных солей и щелочей, осаждаются кислотами и обладают высокой вязкостью.

ГП термостабильны, т. к. углеводы, входящие в их состав, значительно повышают устойчивость молекул к различным химическим веществам и нагреванию, защищают их от действия протеаз, определяя тем самым биологическую роль гликопротеидов. Углеводы придают белкам большую специфичность, за счет этих групп макромолекулы гликопротеида могут распознавать другие структуры.

Гликопротеиды в большом количестве содержатся в межклеточном веществе соединительной ткани, плазме крови, слюне и других секретах, в составе цитоплазматических и различных внутриклеточных мембран, в цитозоле.

Они транспортируют гидрофобные вещества и ионы металлов; входя в состав рецепторов мембран, обеспечивают специфичность контактов клетки, влияют на дифференцировку тканей, участвуют в иммунологических реакциях, выполняют защитную роль, покрывая слизистые оболочки. Значение ГП
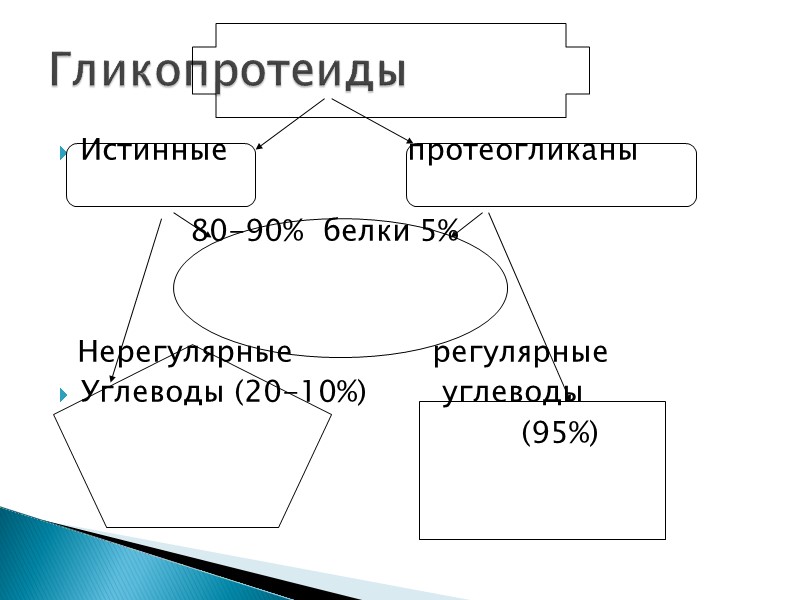
Истинные протеогликаны 80-90% белки 5% Нерегулярные регулярные Углеводы (20-10%) углеводы (95%) Гликопротеиды

В состав простетической группы истинных гликопротеидов входят различные моносахариды и их аминопроизводные, нейраминовые или сиаловые кислоты в различных сочетаниях и соотношениях, т.е. простетическая часть истинных гликопротеидов не имеет регулярного строения

иммуноглобулины, муцины, сиалопротеиды, гормоны тиреотропин, фолликулостимулирующий гормон, лютеинизирующий гормон; белки, обуславливающие групповую специфичность крови; протромбин, холинэстераза, транскортин, церулоплазмин, гаптоглобин и т.п. Представители истинных ГП

Протеогликаны содержат небольшую (2-5%) белковую часть и простетическую группу, представленную гликозамингликанами (ГАГами). ГАГи имеют регулярное строение, т. е. состоят из чередующихся дисахаридов, в состав которых включены уроновые кислоты и ацетилгексозамины протеогликаны

Различают 6 видов ГАГов - гиалуроновая кислота, хондроитинсульфаты А, В, С, кератансульфаты и гепарин, отличающиеся друг от друга природой уроновых кислот, гексозаминов, степенью сульфатирования, типом химической связи, соединяющей между собой мономеры, молекулярной массой, свойствами.
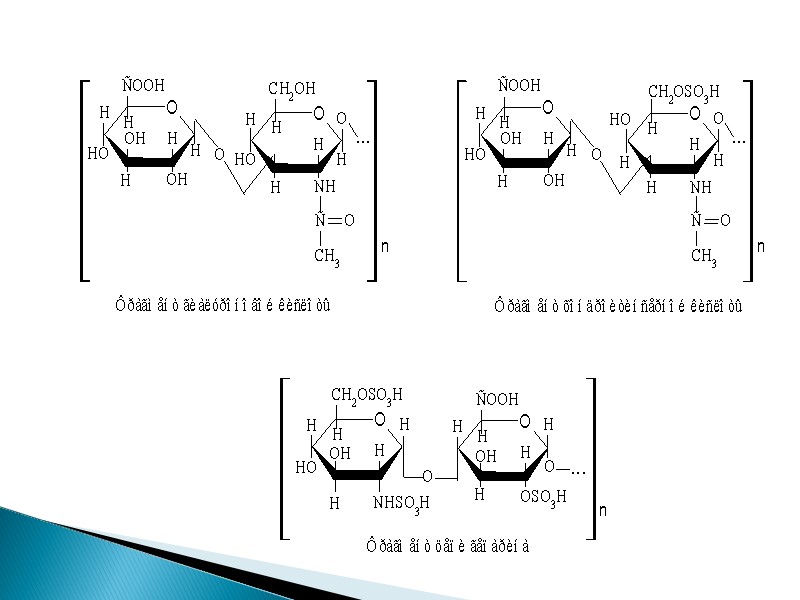

гиалуроновая кислота (глюкуроновая + ацетилглюкозамин) хондроитинсульфат (глюкуроновая к-та + ацетилгалактозамин) Гепарин (глюкуроновая к-та +глюкозаминсульфат) Химический состав ГАГов
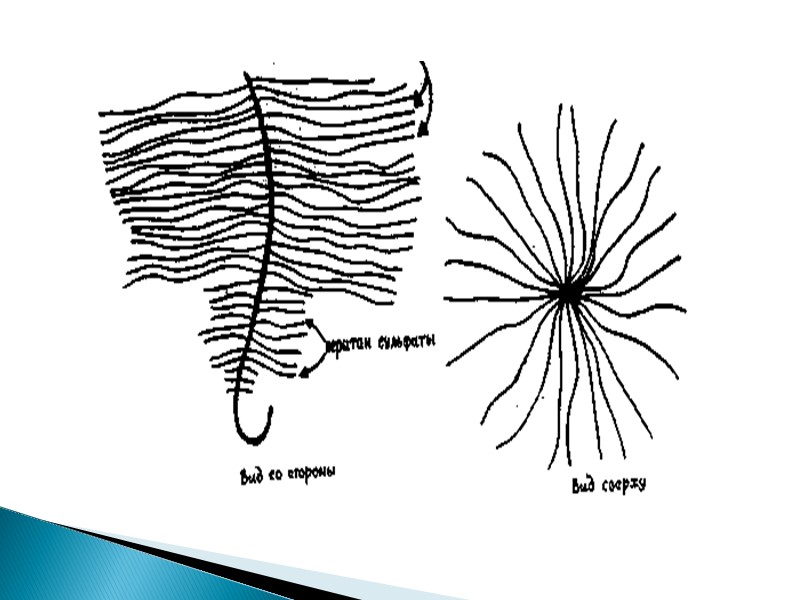

Основная роль в связывании воды. Активирует митоз Участвует в регуляции проницаемости тканей, являясь главным веществом рыхлой соединительной ткани. обладает цементирующим свойством, соединяя между собой эндотелиальные клетки. обнаружена в стекловидном теле. Содержится в большом количестве в пупочном канатике, препятствуя распространению патогенного агента в суставной жидкости, выполняет роль смазки, уменьшая трение между суставными поверхностями. Гиалуроновая кислота

Гепарин вырабатывается тучными клетками - обязательными компонентами соединительной ткани. В отличие от других гликозамингликанов, которые являются исключительно внеклеточными соединениями, гепарин является внутриклеточным соединением в составе тучных клеток артерий, печени, легких и кожи. гепарин

(антикоагулянт) активатор липазы и липопротеидлипазы, тем самым оказывая просветляющее и антиатерогенное действие. Гепарин уменьшает метаболизм клеток, благодаря изменению электрического потенциала клеточной поверхности, что ведет к торможению роста и блокаде фагоцитоза. На этом основано антитоксическое действие гепарина. Значение гепарина

Гепарин инактивирует ряд ферментов, в т.ч. активность лизосомальных ферментов; обладает антигиалуронидазным эффектом, снижает проницаемость основного вещества капилляров, освобождает ткани от излишков гистамина. Все это в совокупности обуславливает его противовоспалительное действие. Ингибирует митоз

Участвует в фибриллогенезе и оссификации Является наиболее распространенным ГАГом в организме человека. Ингибирует митоз Хондроитинсерная кислота

Обнаруживается в хрящах, костях, сердечных клапанах. Обуславливает прочность и упругость соединительной ткани Образует агрегаты протеогликанов. Хондроитинсерная кислота

ХП – это сложные белки, у которых небелковой частью являются окрашенные соединения,(металлы или витамины) принадлежащие к различным классам органических веществ (chroma-краска) Железо придает красную окраску Медь – голубовато-зеленую Магний – зеленую хромопротеины
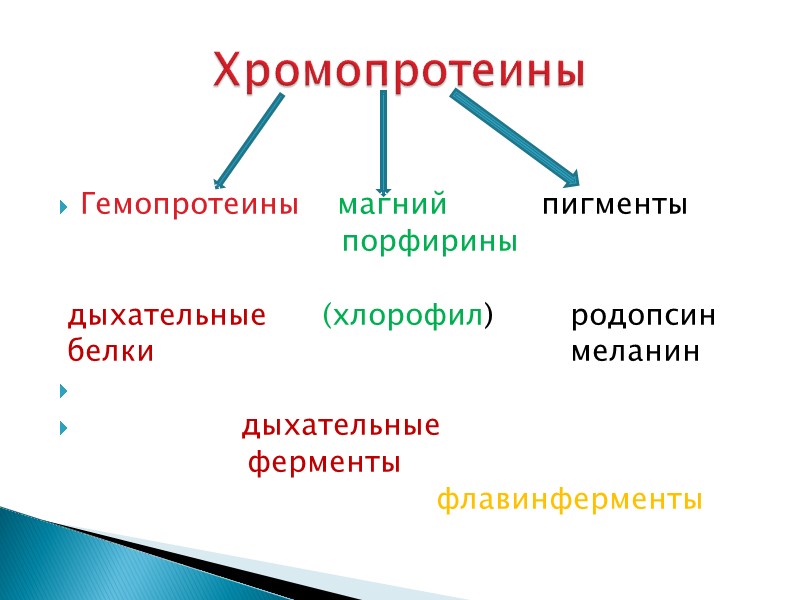
Гемопротеины магний пигменты порфирины дыхательные (хлорофил) родопсин белки меланин дыхательные ферменты флавинферменты Хромопротеины
гемоглобин (Нb) – красный пигмент крови миоглобин (Мgb) – красный пигмент мышц Дыхательные белки

Дыхательный белок, красный пигмент крови, содержится в эритроцитах. Состоит из простого белка типа гистонов – глобина и 4-х гемов. гемоглобин

Состоит из 4-х полипептидных цепей Двух альфа-цепей (141 остаток АК) Двух бета-цепей (146 остатков АК Молекулярная масса 70 000 Д Обладает видовой специфичностью Гемы гемоглобинов всех животных одинаковы глобин

1,3,5,8-тетраметил- 2,4-дивинил, 6,7- дипропионовокислый железопорфин Гем гемоглобина
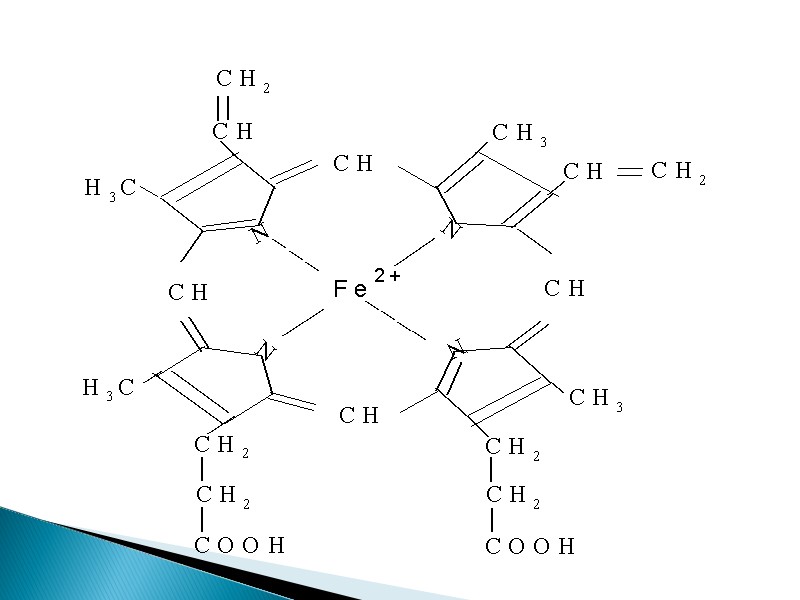
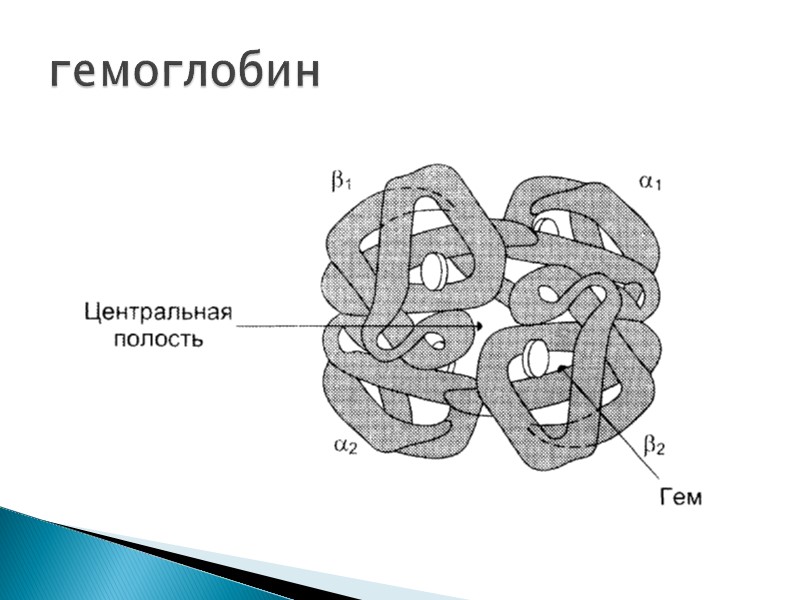
гемоглобин
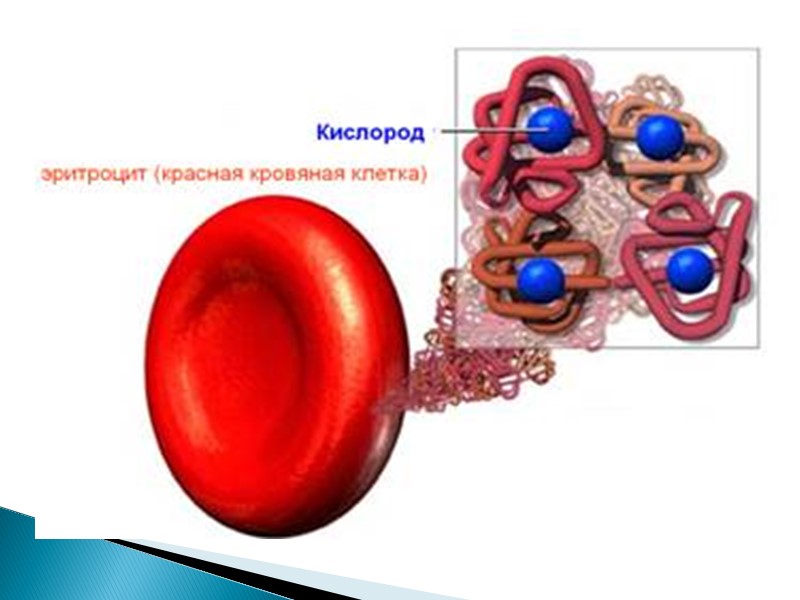

В 1957 году биохимики Д.Кендрью и М.Перутц получили Нобелевскую премию за расшифровку строения молекулы гемоглобина.

Значение гемоглобина 1.перенос кислорода от легких к тканям 2. перенос углекислого газа от тканей к легким

Нуклеопротеины – это сложные белки

Белки Альбумины, Глобулины, гистоны, протамины Простетическая группа – нуклеиновые кислот ДНК и РНК Нуклеопротеины


Белки выполняют все функции, кроме одной – ИНФОРМАЦИОННОЙ не способны к самовоспроизведению

Эту функцию выполняет ДНК главная и единственная ее функция

ДНК – самая большая молекула в клетке. Она намного больше белков и РНК Каждая хромосома = одна молекула ДНК 23 хромосомы человека = 23 молекулы ДНК ≈ 1 метр Самые длинные из них ≈ 8 см ДНК – это молекула-текст. В последова-тельности ее нуклеотидов записана вся наследственная программа организма

клетка хромосомы в ядре ДНК хромосома 1 молекула ДНК

1953 Фрэнсис Крик Джеймс Уотсон Открыта структура ДНК Дата рождения молекулярной биологии

Francis Harry Compton Crick James Dewey Watson Нобелевская премия 1962


Розалинд Франклин Рентгеноструктурный портрет ДНК – знаменитое фото 51 1920 - 1958

Молекулы ДНК и РНК можно увидеть в электронный микроскоп ДНК бактериальных плазмид
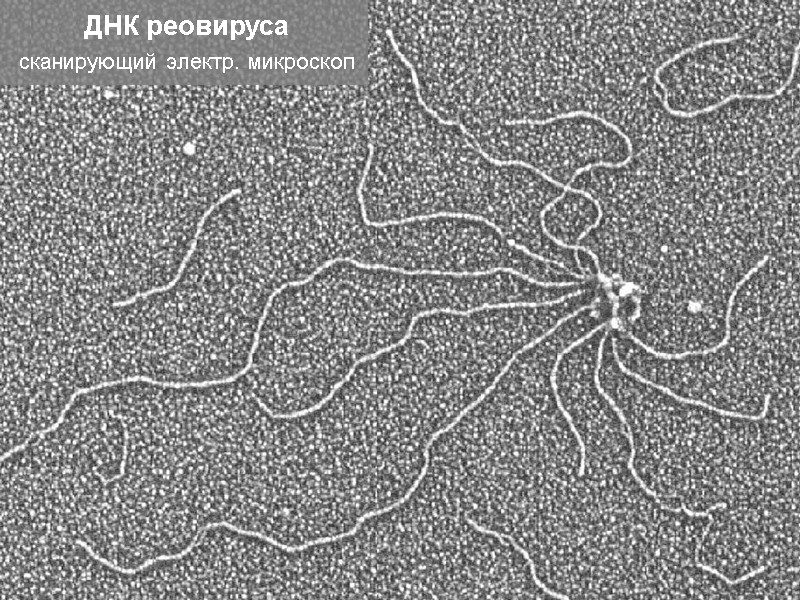
ДНК реовируса сканирующий электр. микроскоп
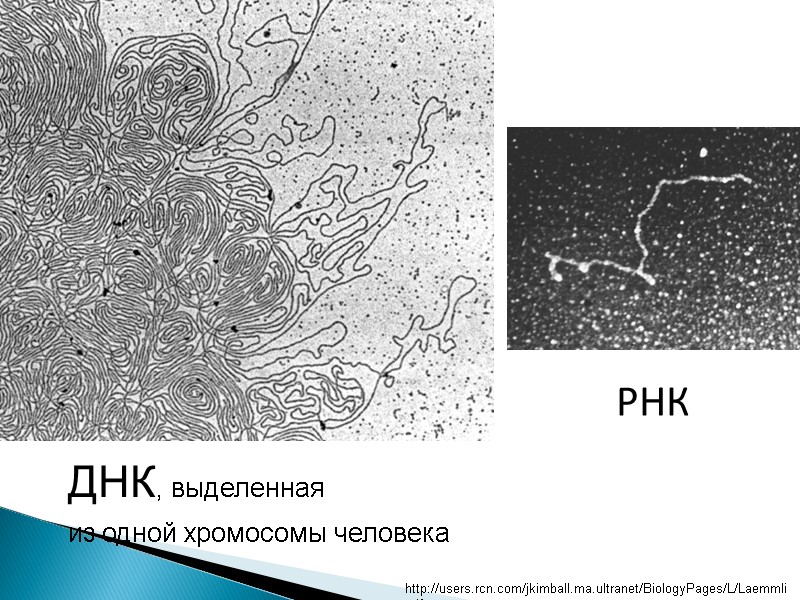
ДНК, выделенная из одной хромосомы человека РНК http://users.rcn.com/jkimball.ma.ultranet/BiologyPages/L/Laemmli.gif
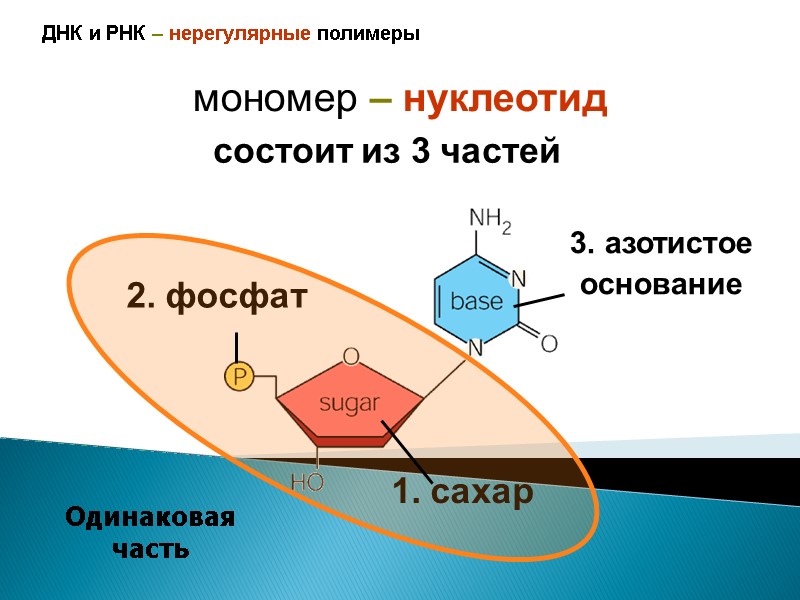
ДНК и РНК – нерегулярные полимеры мономер – нуклеотид 2. фосфат 1. сахар 3. азотистое основание Одинаковая часть состоит из 3 частей
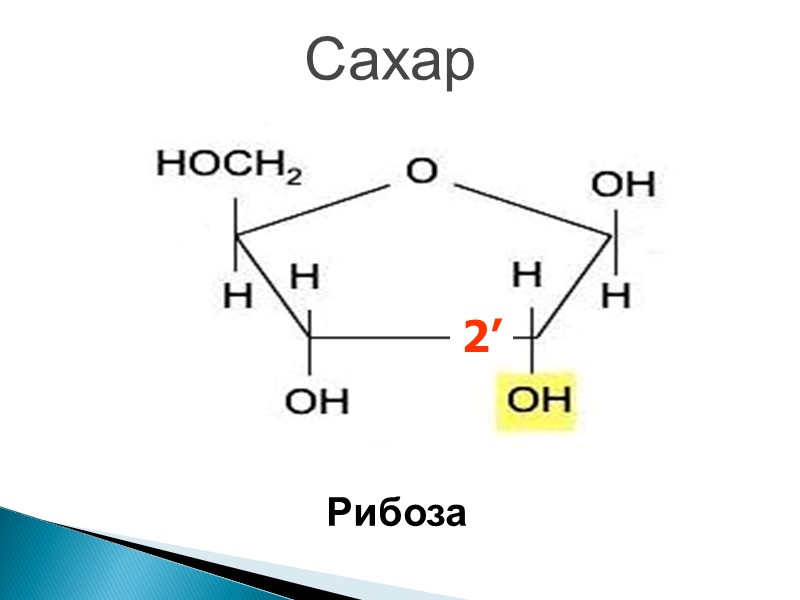
Сахар Рибоза 2’
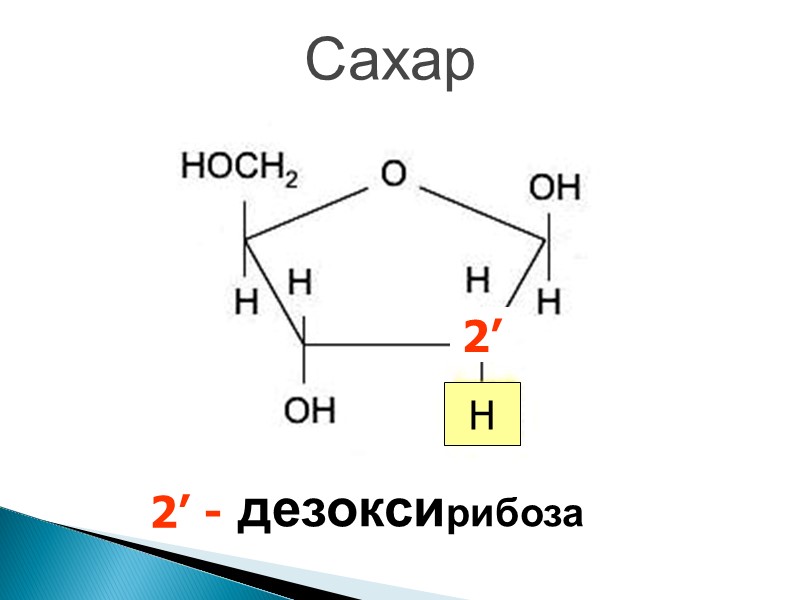
Сахар дезоксирибоза 2’ H 2’ -
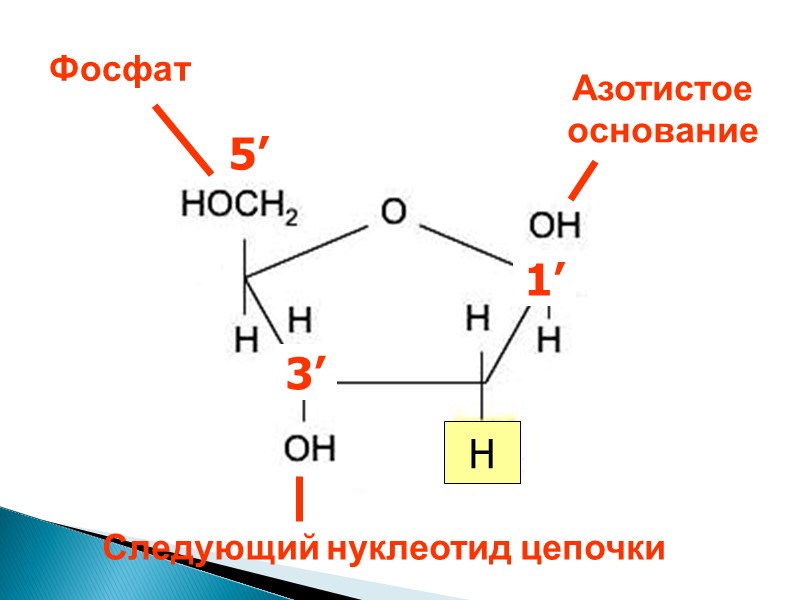
3’ H 1’ 5’ 3’
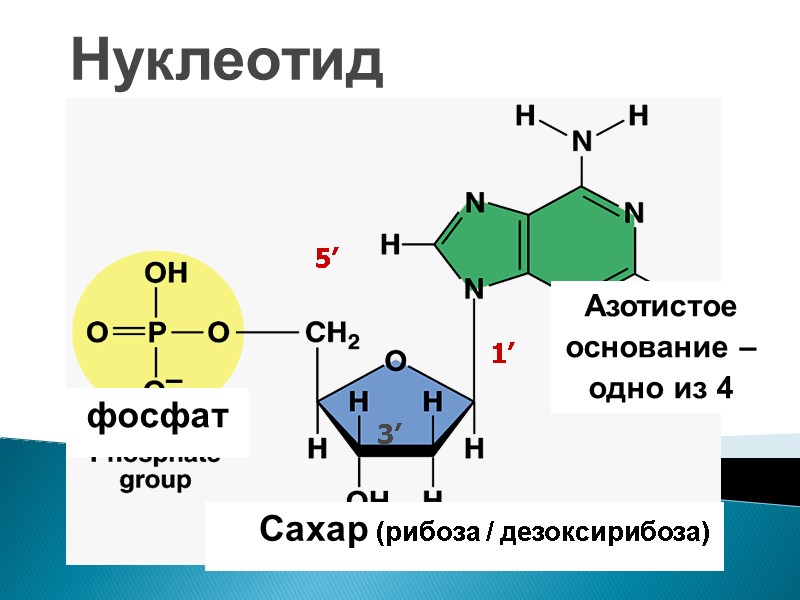
Нуклеотид фосфат Сахар (рибоза / дезоксирибоза) Азотистое основание – одно из 4 1’ 3’ 5’

Тимин, Т Цитозин, Ц Аденин, А Гуанин, Г ДНК

Тимин, Т Цитозин, Ц Аденин, А Гуанин, Г ДНК РНК Урацил, У Убрали метильную группу
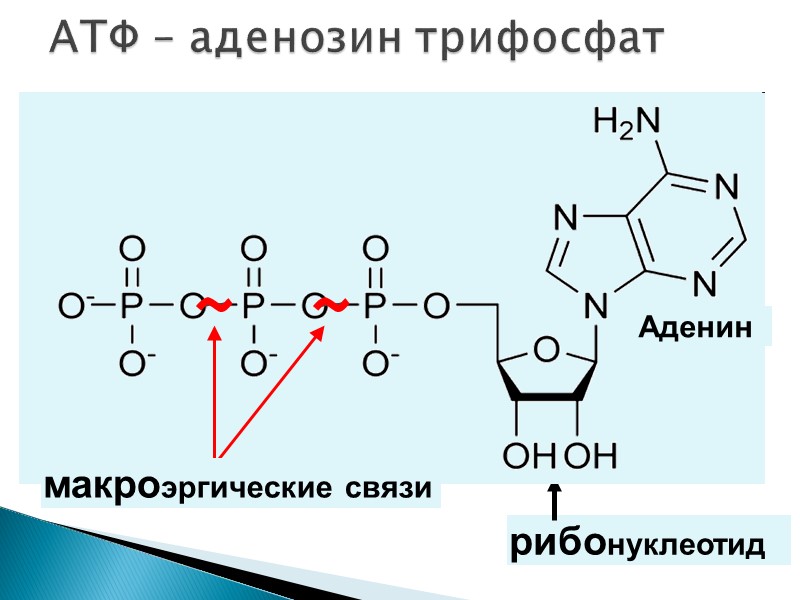
АТФ – аденозин трифосфат
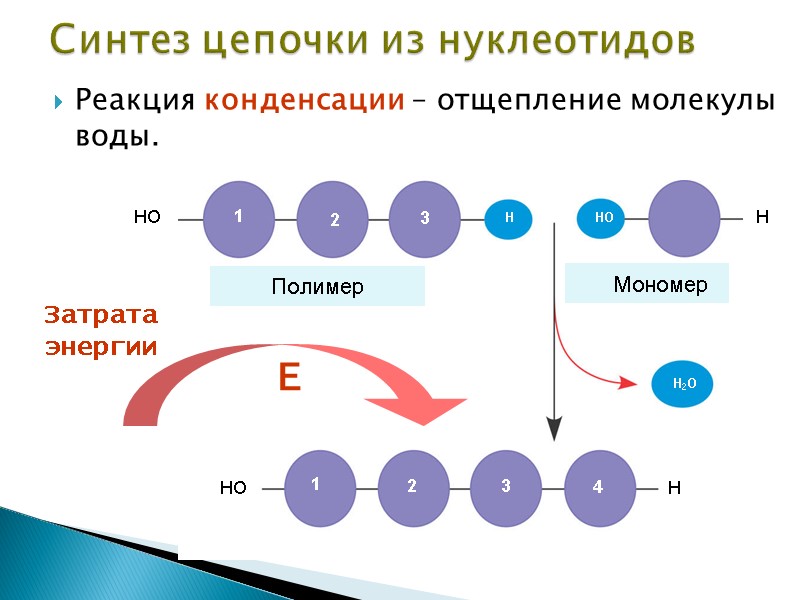
Реакция конденсации – отщепление молекулы воды. Синтез цепочки из нуклеотидов Затрата энергии Е
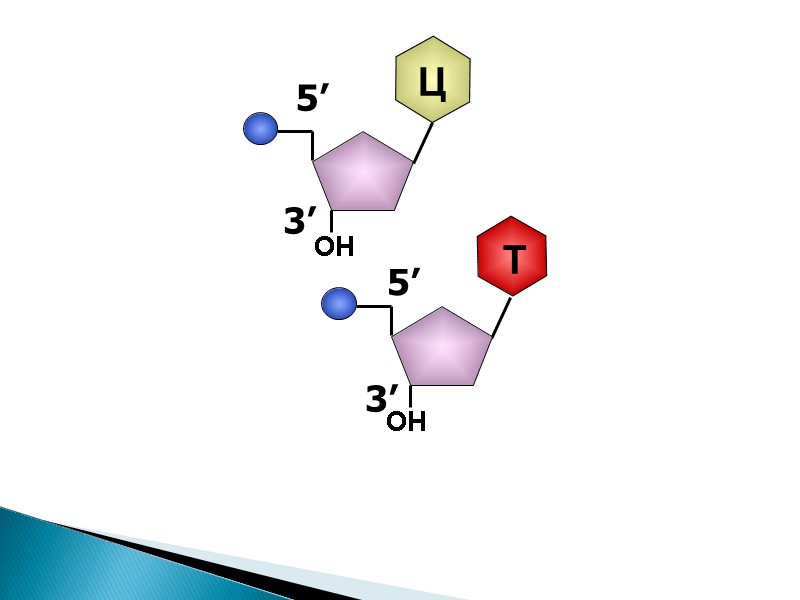
3’ 5’ Ц ОН

5’ Ц Фосфодиэфирная связь 5' конец цепи 3' конец цепи Фосфодиэфирная связь Направление роста

Растущий конец – всегда 3´ для всех нуклеиновых кислот – ДНК и РНК

Строение ДНК

1950 Правила Чаргаффа Эрвин Чаргафф
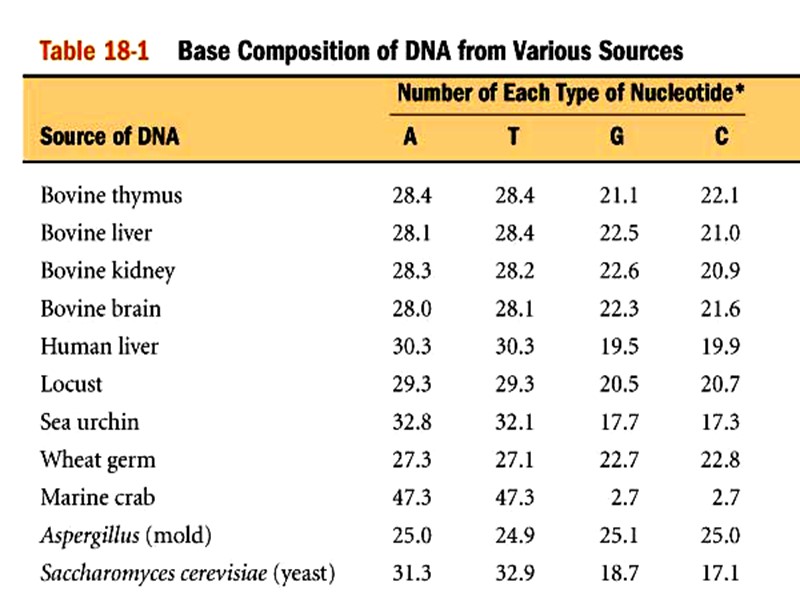
![Правила Чаргаффа [ А ] + [ Г ] = Правила Чаргаффа [ А ] + [ Г ] =](https://present5.com/presentacii-2/20171213\34898-lektsia__1_vvedenie_v_biokhimiyu_belki_16-17.ppt\34898-lektsia__1_vvedenie_v_biokhimiyu_belki_16-17_131.jpg)
Правила Чаргаффа [ А ] + [ Г ] = [ Т ] + [ Ц ] = 50%

Объяснение правилам Чаргаффа дали Уотсон и Крик ДНК – это 2 цепочки, соединенные по принципу комплементарности
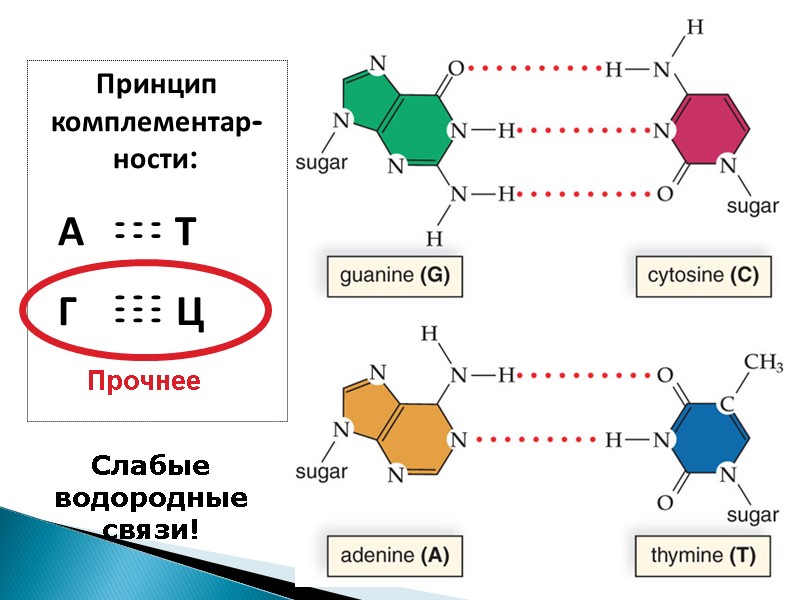
Принцип комплементар-ности: А Т Г Ц - - - - - - - - - - - - Слабые водородные связи!
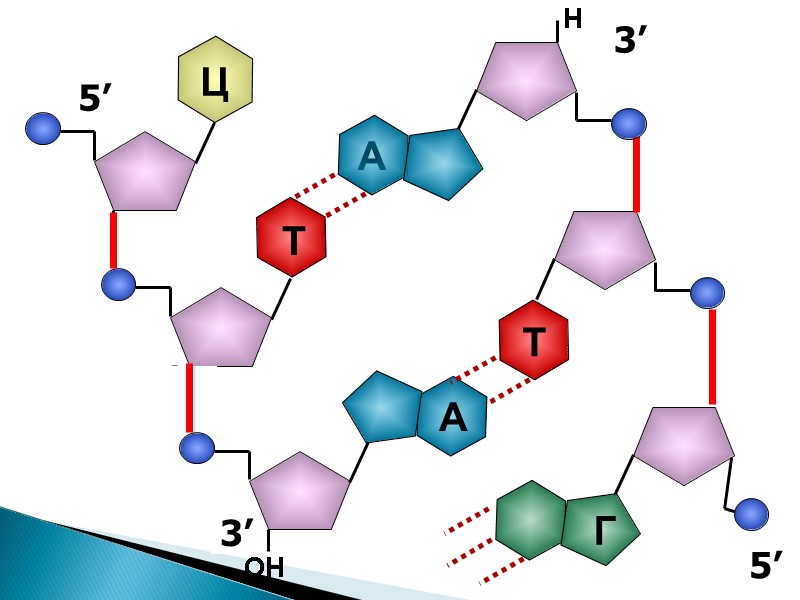
5’ Ц 3’ 5’
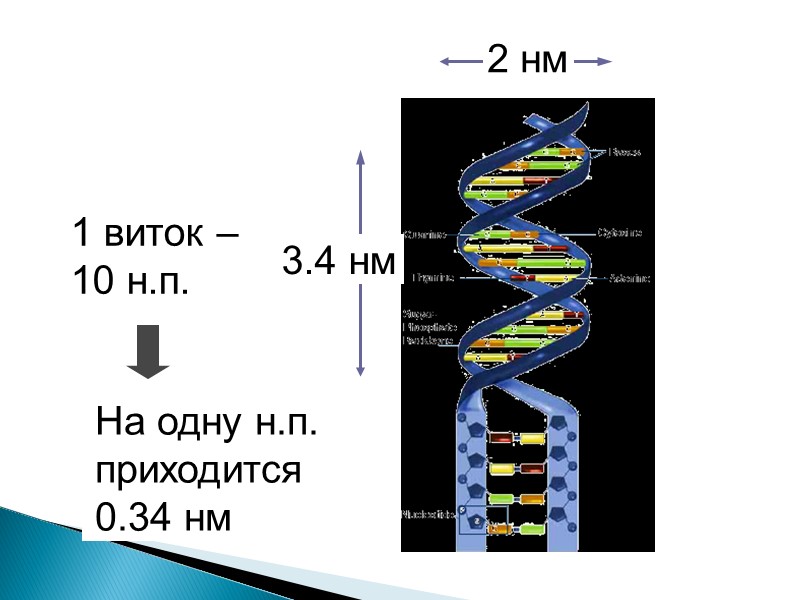
1 виток – 10 н.п. На одну н.п. приходится 0.34 нм
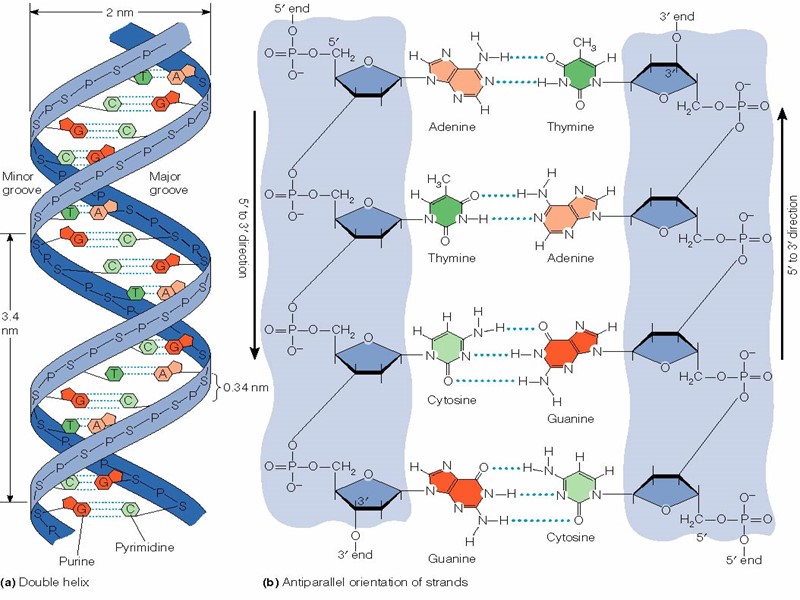
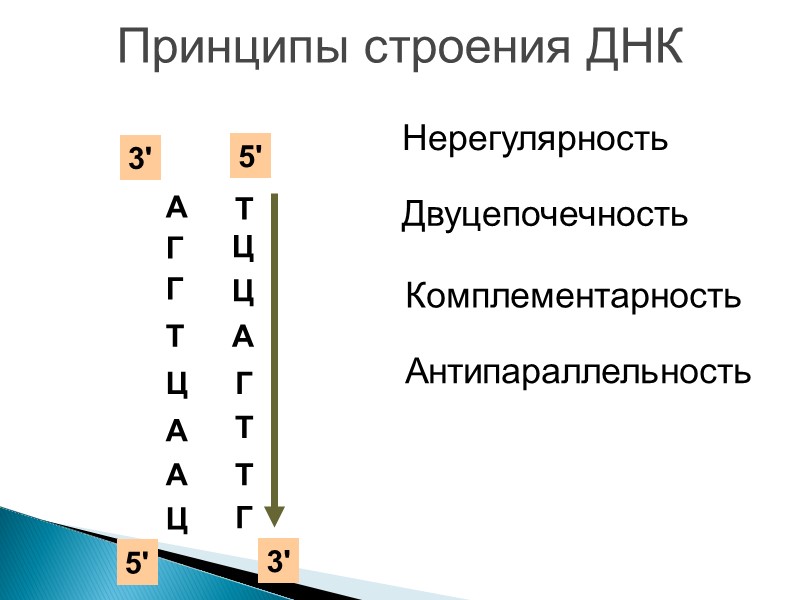
Принципы строения ДНК А Г Г Т Ц А А Ц Нерегулярность Двуцепочечность Ц Ц Комплементарность А Г Т Т Г Антипараллельность 3' 5' 5' 3' Т

Строение РНК

Одноцепочечные молекулы Сахар – рибоза вместо дезоксирибозы У вместо Т Намного меньше – сравнимы по размеру с белками. Отличия РНК от ДНК

и-РНК = м-РНК информационная, матричная до 10 тысяч нуклеотидов т- РНК транспортная около 100 нуклеотидов р-РНК рибосомальная 2-3 тысячи нуклеотидов Виды РНК как и белки, имеют 3-мерную конформацию линейная
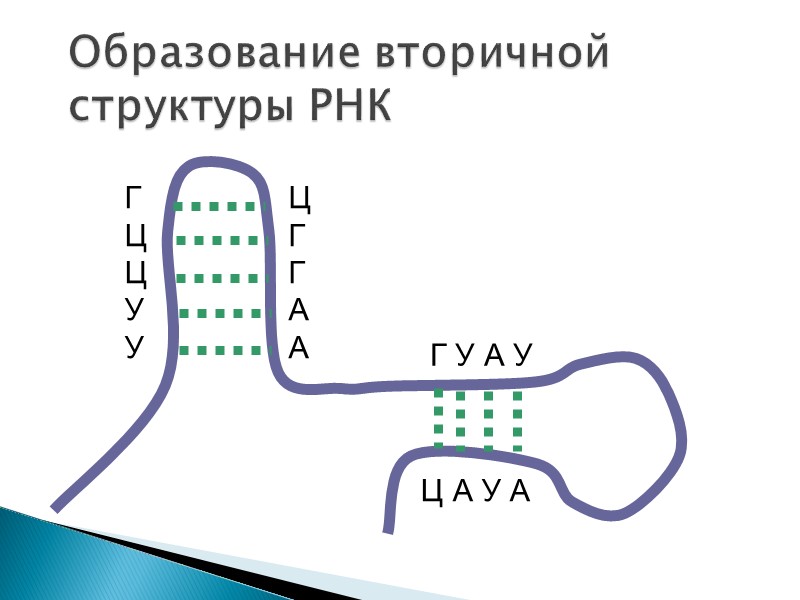
Образование вторичной структуры РНК Г Ц Ц У У Ц Г Г А А Г У А У Ц А У А

Схема образования петель в РНК за счет комплементарных участков
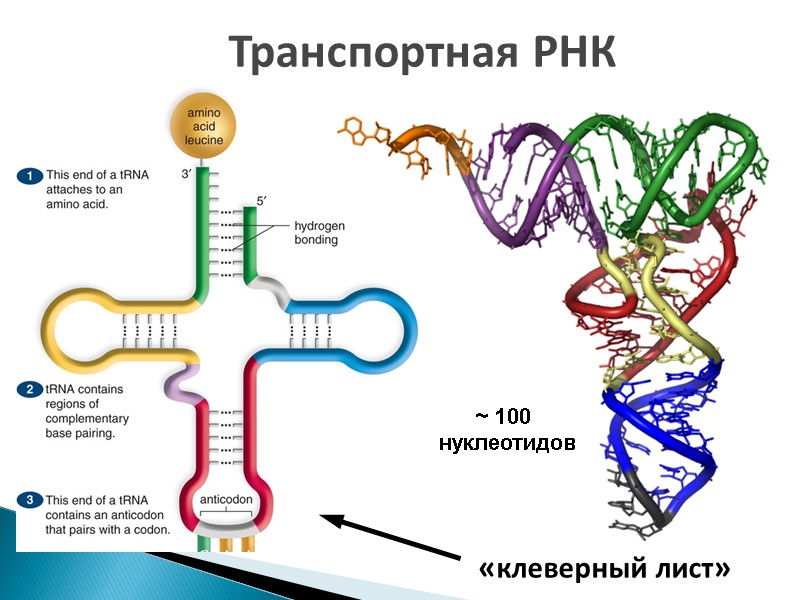
«клеверный лист» Транспортная РНК ~ 100 нуклеотидов
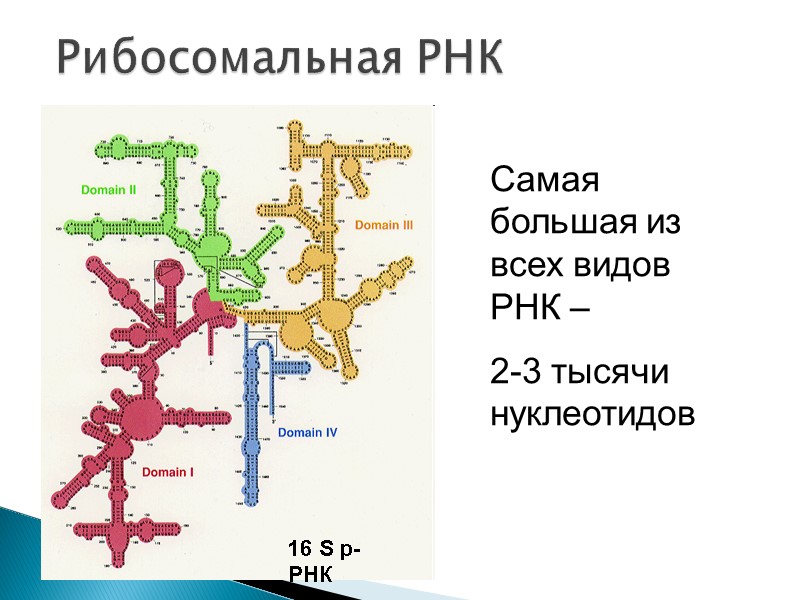
Рибосомальная РНК 16 S р-РНК Самая большая из всех видов РНК – 2-3 тысячи нуклеотидов

3’ 5’ Ц ОН Н Фосфодиэфирная связь
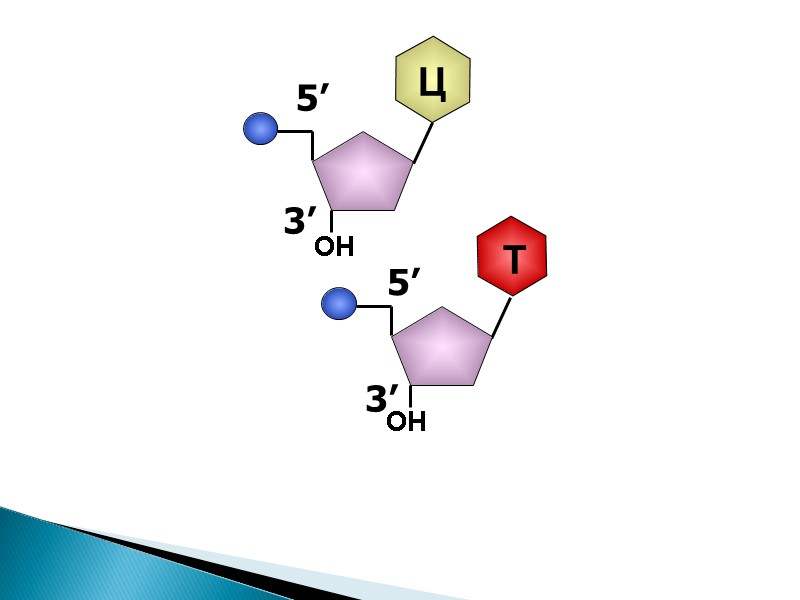
3’ 5’ Ц ОН

Информационная: реализация информации Все виды РНК – посредники в передаче информации от ДНК к белку Функции РНК в порядке их открытия Место встречи всех трех РНК – ? рибосома 1950-e

Информационная: хранение информации (у части вирусов) Примерно 80% вирусов человека и животных использует для записи информации РНК У них она выполняет ту же роль, что ДНК у всех остальных организмов Функции РНК в порядке их открытия

Каталитическая 1982 Рибозимы – РНК-ферменты Не все РНК, а лишь некоторые: Функции РНК в порядке их открытия р-РНК рибосом, РНК некоторых вирусов РНК в составе сплайсосомы

Регуляторная 1990-е Малые РНК регулируют работу генов в ядре и синтез белка в цитоплазме Аналогична функции ДНК-связывающих белков Функции РНК в порядке их открытия

ДНК – принцип комплементарности, позволяющий матричное копирование молекулы Белков – трехмерную структуру, позволяющую выполнять самые разные функции (катализ, регуляцию, транспорт) РНК сочетает свойства
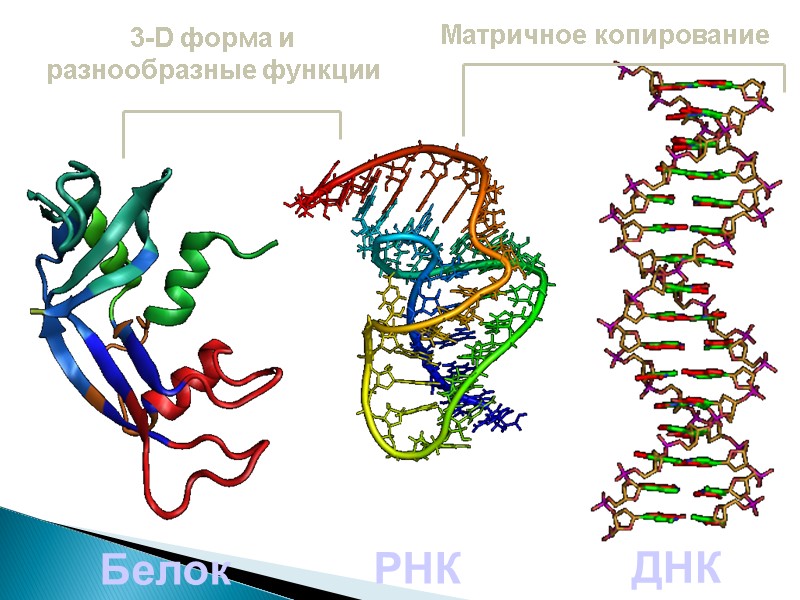
РНК ДНК Белок 3-D форма и разнообразные функции Матричное копирование

ИЛЛЮСТРАТИВНЫЙ МАТЕРИАЛ: Презентация (слайды) - связь биохимии с другими науками; - классификация белков; - классификация сложных белков;

Основная: 1. Северин Е.С. «Биохимия», М ГЭОТАР-МЕДИА, 2013 2. Сеитов З.С. «Биохимия», Алматы, 2012 3, Harper’s Illusstated Biochemistry, 29e, 2012 дополнительная : 1. Николаев А.Я. «Биологическая химия», М., 2007 2. Т.Т.Березов, Б.Ф.Коровкин «Биологическая химия», 2002 г. 3. Плешкова С.М. и др. «Учебное пособие для самостоятельного изучения биохимии» Часть 1 !Белки, ферменты, энергетический обмен, витамины!, Алматы, 2009 г 4. Марри., Греннер Д., Мейес П., Родуэлл В «Биохимия человека» В 2-х томах перевод с англ.: М.: Мир, 1993 – 384 с литература

1. Дайте определение биохимии как науки 2. Понятие о сложных белках 3. Назовите представителей истинных гликопротеинов 4. Перечислите гликозамингликаны 5. Назовите дыхательные белки 6. Из чего состоят мононуклеотиды? КОНТРОЛЬНЫЕ ВОПРОСЫ
34898-lektsia__1_vvedenie_v_biokhimiyu_belki_16-17.ppt
- Количество слайдов: 155

