 Повторение по теме: « Химическая связь. Строение вещества» . Цель урока: повторить n n n Виды химических связей Типы кристаллических решеток Степень окисления Окислительно-восстановительные реакции Расстановка коэффициентов методом электронного баланса
Повторение по теме: « Химическая связь. Строение вещества» . Цель урока: повторить n n n Виды химических связей Типы кристаллических решеток Степень окисления Окислительно-восстановительные реакции Расстановка коэффициентов методом электронного баланса
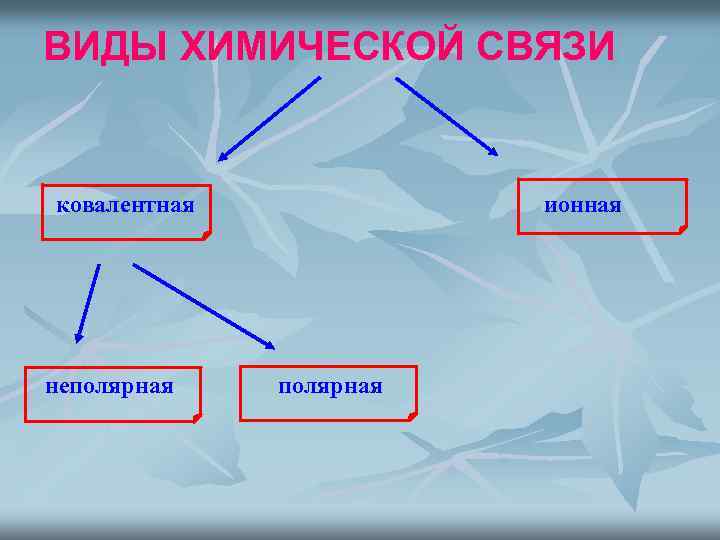 ВИДЫ ХИМИЧЕСКОЙ СВЯЗИ ковалентная неполярная ионная полярная
ВИДЫ ХИМИЧЕСКОЙ СВЯЗИ ковалентная неполярная ионная полярная
 Охарактеризуйте виды химических связей n n n К. Н. С. - это … К. П. С. - это … И. С. - это …
Охарактеризуйте виды химических связей n n n К. Н. С. - это … К. П. С. - это … И. С. - это …
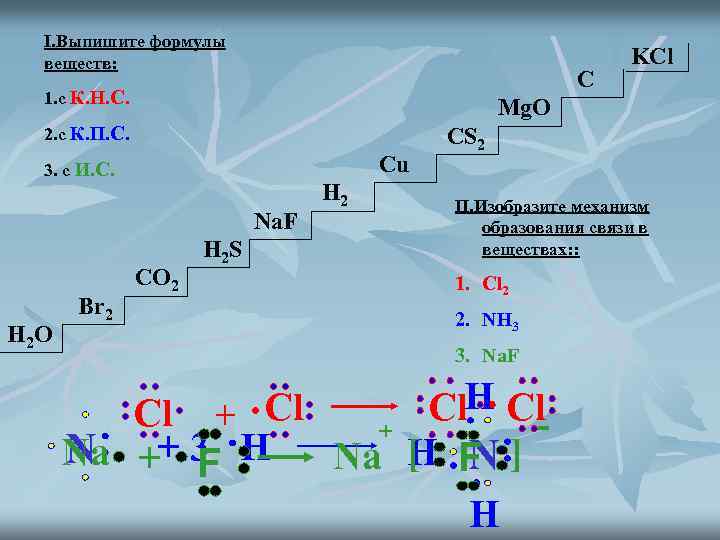 I. Выпишите формулы веществ: C 1. с К. Н. С. Mg. O 2. с К. П. С. Cu 3. с И. С. Na. F H 2 O Br 2 KCl CO 2 H 2 S H 2 CS 2 II. Изобразите механизм образования связи в веществах: : 1. Cl 2 2. NH 3 3. Na. F Сl Cl. H Cl Сl + + N [ N Na ++ 3 H Na H F ] F H
I. Выпишите формулы веществ: C 1. с К. Н. С. Mg. O 2. с К. П. С. Cu 3. с И. С. Na. F H 2 O Br 2 KCl CO 2 H 2 S H 2 CS 2 II. Изобразите механизм образования связи в веществах: : 1. Cl 2 2. NH 3 3. Na. F Сl Cl. H Cl Сl + + N [ N Na ++ 3 H Na H F ] F H
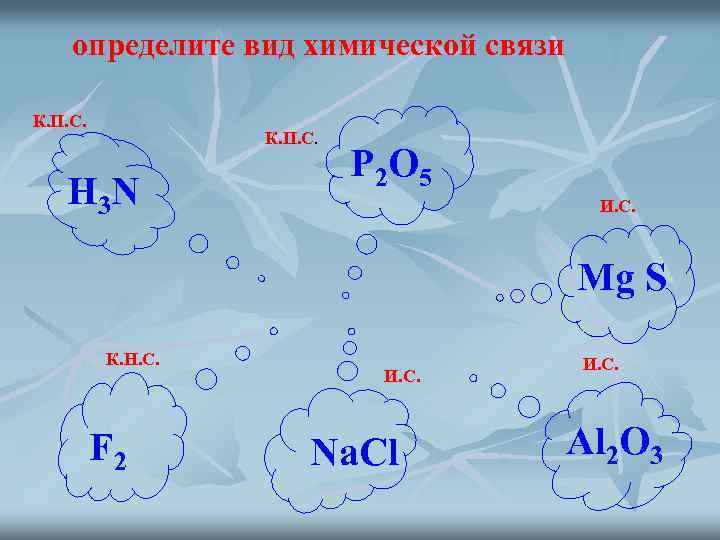 определите вид химической связи К. П. С. H 3 N P 2 O 5 И. С. Mg S К. Н. С. F 2 И. С. Na. Cl И. С. Al 2 O 3
определите вид химической связи К. П. С. H 3 N P 2 O 5 И. С. Mg S К. Н. С. F 2 И. С. Na. Cl И. С. Al 2 O 3
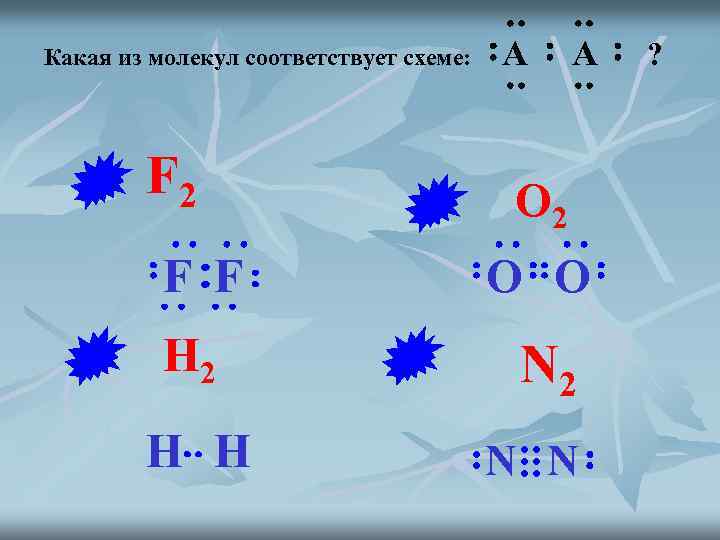 Какая из молекул соответствует схеме: F 2 A A O 2 F F O O H 2 N 2 H H N N ?
Какая из молекул соответствует схеме: F 2 A A O 2 F F O O H 2 N 2 H H N N ?
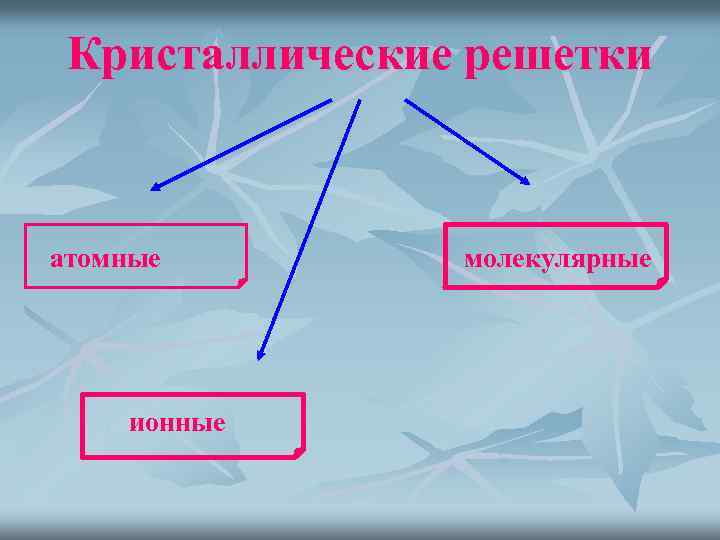 Кристаллические решетки атомные ионные молекулярные
Кристаллические решетки атомные ионные молекулярные
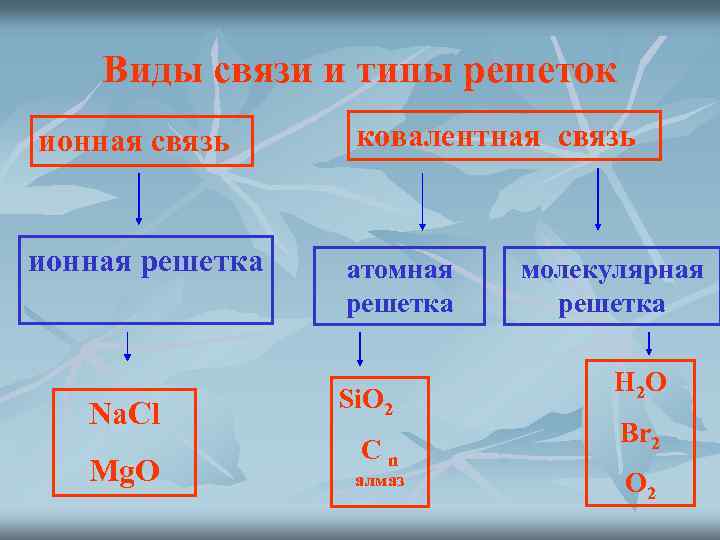 Виды связи и типы решеток ионная связь ионная решетка Na. Cl Mg. O ковалентная связь атомная решетка Si. O 2 Cn алмаз молекулярная решетка H 2 O Br 2 O 2
Виды связи и типы решеток ионная связь ионная решетка Na. Cl Mg. O ковалентная связь атомная решетка Si. O 2 Cn алмаз молекулярная решетка H 2 O Br 2 O 2
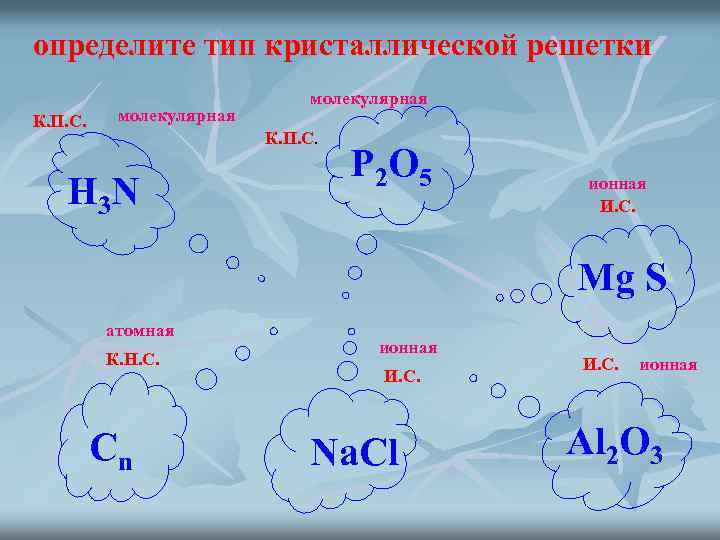 определите тип кристаллической решетки К. П. С. молекулярная К. П. С. H 3 N P 2 O 5 ионная И. С. Mg S атомная К. Н. С. Сn ионная И. С. Na. Cl И. С. ионная Al 2 O 3
определите тип кристаллической решетки К. П. С. молекулярная К. П. С. H 3 N P 2 O 5 ионная И. С. Mg S атомная К. Н. С. Сn ионная И. С. Na. Cl И. С. ионная Al 2 O 3
 степень окисления n n n Дайте определение степени окисления Окислительно-восстановительная реакция Окисление Восстановление Окислитель Восстановитель
степень окисления n n n Дайте определение степени окисления Окислительно-восстановительная реакция Окисление Восстановление Окислитель Восстановитель
 какая реакция является окислительно-восстановительной? +1 +6 -2 НЕТ +1 -2 +1 +6 -2 H 2 SO 4 +Na 2 O +6 -2 Na 2 SO 4 + H 2 O +1 -2 +1 +6 -2 SO 3 + H 2 O +4 -2 H 2 SO 4 0 +6 -2 2 SO 2 +1 -2 0 Н 2 S + O 2 +1 -2 2 SO 3 +1 -2 H 2 O 0 + S
какая реакция является окислительно-восстановительной? +1 +6 -2 НЕТ +1 -2 +1 +6 -2 H 2 SO 4 +Na 2 O +6 -2 Na 2 SO 4 + H 2 O +1 -2 +1 +6 -2 SO 3 + H 2 O +4 -2 H 2 SO 4 0 +6 -2 2 SO 2 +1 -2 0 Н 2 S + O 2 +1 -2 2 SO 3 +1 -2 H 2 O 0 + S
 Определите в каком веществе степень окисления серы равна +4 +1 НЕТ -2 Н 2 S +1 +6 -2 НЕТ H 2 SO 4 +6 -2 SO 3 +4 -2 SO 2 +1 +4 -2 H 2 SO 3
Определите в каком веществе степень окисления серы равна +4 +1 НЕТ -2 Н 2 S +1 +6 -2 НЕТ H 2 SO 4 +6 -2 SO 3 +4 -2 SO 2 +1 +4 -2 H 2 SO 3
 Какой коэффициент перед формулой окислителя? 0 0 4 Al + 3 O 2 восстановитель +3 -2 2 Al 2 O 3 окислитель нет нет ok
Какой коэффициент перед формулой окислителя? 0 0 4 Al + 3 O 2 восстановитель +3 -2 2 Al 2 O 3 окислитель нет нет ok
 Какой коэффициент перед формулой восстановителя? 0 0 2 P + 3 Cl 2 восстановитель +3 -1 2 PCl 3 окислитель ok нет нет
Какой коэффициент перед формулой восстановителя? 0 0 2 P + 3 Cl 2 восстановитель +3 -1 2 PCl 3 окислитель ok нет нет
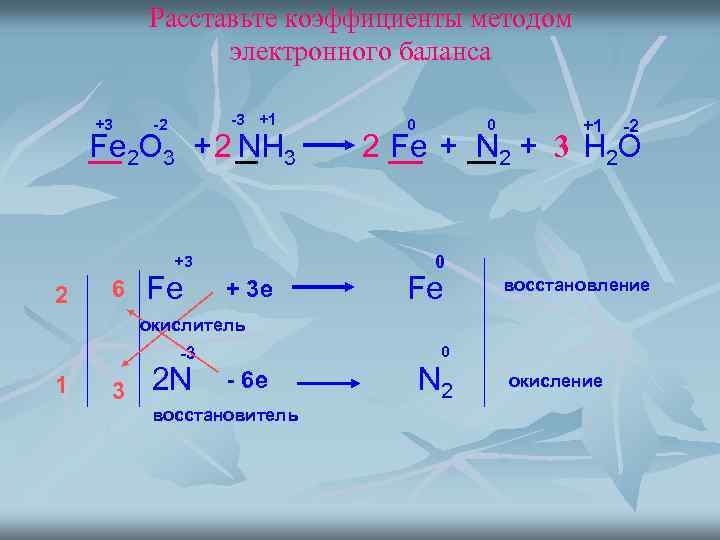 Расставьте коэффициенты методом электронного баланса +3 -3 +1 -2 Fe 2 O 3 + 2 NH 3 +3 2 6 Fe 0 0 +1 2 Fe + N 2 + 3 H 2 O 0 + 3 е Fe восстановление окислитель 0 -3 1 3 2 N -2 - 6 е восстановитель N 2 окисление
Расставьте коэффициенты методом электронного баланса +3 -3 +1 -2 Fe 2 O 3 + 2 NH 3 +3 2 6 Fe 0 0 +1 2 Fe + N 2 + 3 H 2 O 0 + 3 е Fe восстановление окислитель 0 -3 1 3 2 N -2 - 6 е восстановитель N 2 окисление
 итог n Что для вас оказалось самым сложным? n Что понравилось ? n Что не понравилось?
итог n Что для вас оказалось самым сложным? n Что понравилось ? n Что не понравилось?