3.Строение белков.ppt
- Количество слайдов: 25
 Повторение – мать учения…
Повторение – мать учения…
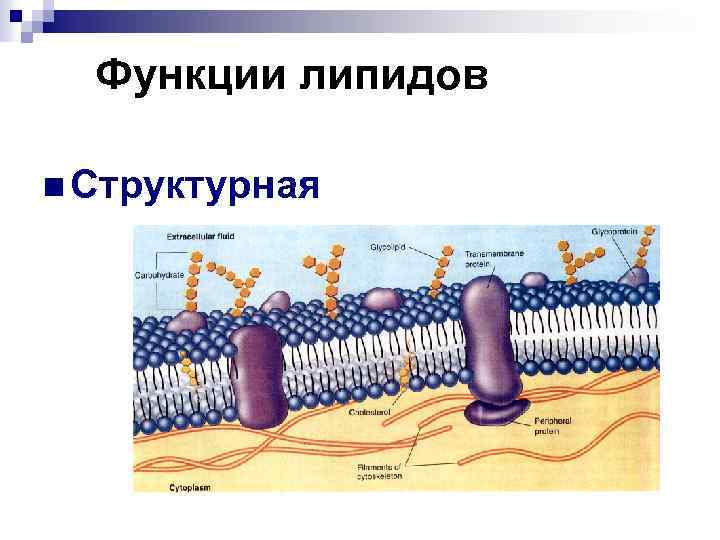 Функции липидов n Структурная
Функции липидов n Структурная
 Функции липидов n Защитная (аммортизация) n Запасающая n Энергетическая 1 г жира 38, 9 к. Дж Е
Функции липидов n Защитная (аммортизация) n Запасающая n Энергетическая 1 г жира 38, 9 к. Дж Е
 Функции липидов n Теплоизоляция n Источник метаболической воды 1 г жира 1, 1 г Н 2 О n Регуляторная n Специфические ff витаминов, восков, терпенов…
Функции липидов n Теплоизоляция n Источник метаболической воды 1 г жира 1, 1 г Н 2 О n Регуляторная n Специфические ff витаминов, восков, терпенов…
 Тест на гениальность… 1. n n n Самые умные, попробуйте ответить на вопросы: Как можно использовать липосомы? Почему у верблюда запасы жира не распределены равномерно под кожей, а сосредоточены в одном или двух горбах? Как при впадении в спячку у млекопитающих изменяется состав жирных кислот в фосфолипидах мембран?
Тест на гениальность… 1. n n n Самые умные, попробуйте ответить на вопросы: Как можно использовать липосомы? Почему у верблюда запасы жира не распределены равномерно под кожей, а сосредоточены в одном или двух горбах? Как при впадении в спячку у млекопитающих изменяется состав жирных кислот в фосфолипидах мембран?
 Гиганты в мире молекул понятие о мономерах, структурных звеньях, полимерах…
Гиганты в мире молекул понятие о мономерах, структурных звеньях, полимерах…
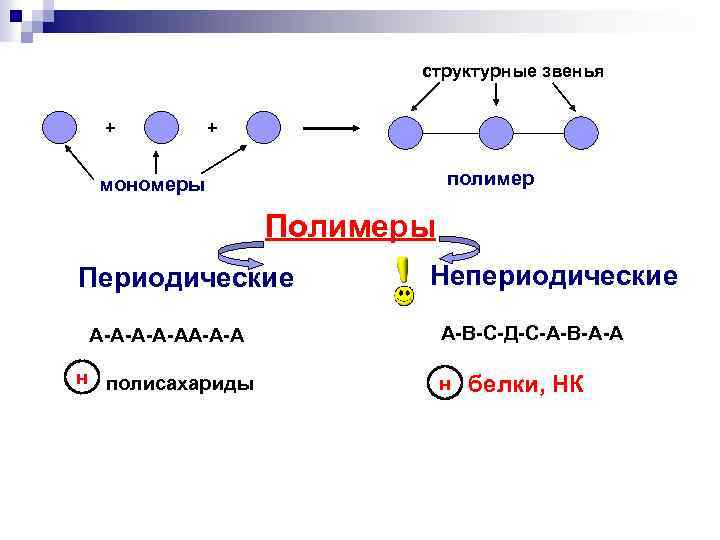 структурные звенья + + полимер мономеры Полимеры Периодические А-А-АА-А-А н полисахариды Непериодические А-В-С-Д-С-А-В-А-А н белки, НК
структурные звенья + + полимер мономеры Полимеры Периодические А-А-АА-А-А н полисахариды Непериодические А-В-С-Д-С-А-В-А-А н белки, НК
 Белки
Белки
 Белки n Непериодические полимеры, мономером которых является аминокислота
Белки n Непериодические полимеры, мономером которых является аминокислота
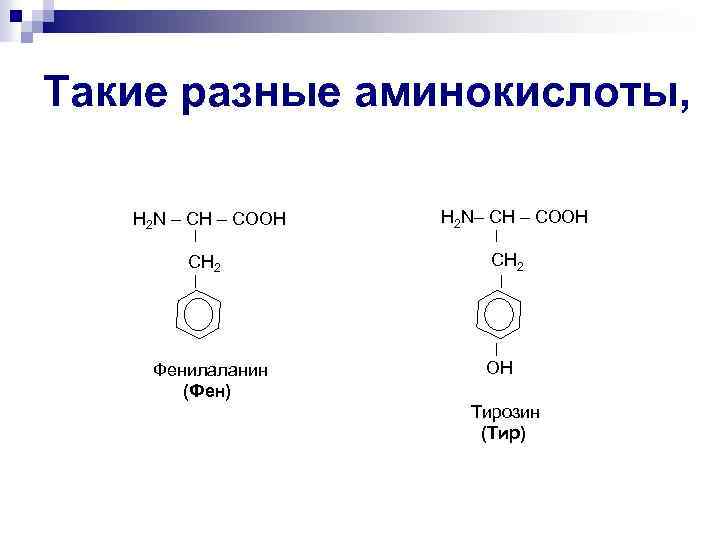 Такие разные аминокислоты, Н 2 N – CH – COOH СН 2 Фенилаланин (Фен) Н 2 N– CH – COOH СН 2 ОН Тирозин (Тир)
Такие разные аминокислоты, Н 2 N – CH – COOH СН 2 Фенилаланин (Фен) Н 2 N– CH – COOH СН 2 ОН Тирозин (Тир)
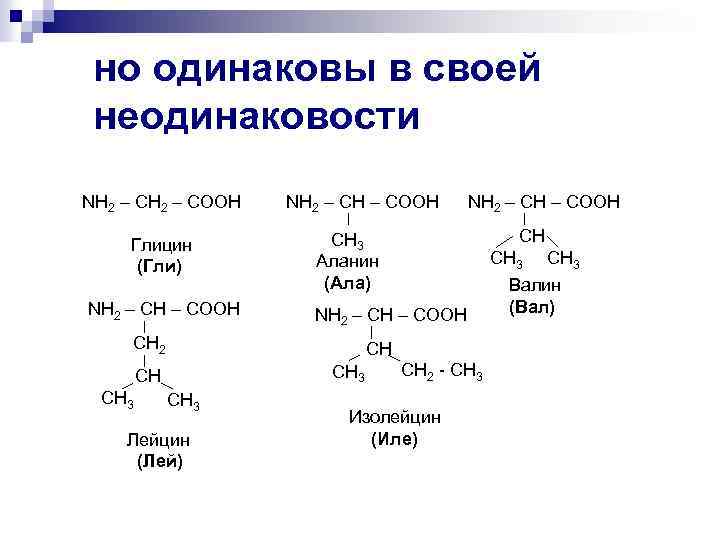 но одинаковы в своей неодинаковости NH 2 – COOH Глицин (Гли) NH 2 – CH – COOH СН СН 3 Аланин (Ала) NH 2 – CH – COOH СН 2 СН СН 3 NH 2 – CH – COOH СН 3 Лейцин (Лей) СН 2 - СН 3 Изолейцин (Иле) СН 3 Валин (Вал)
но одинаковы в своей неодинаковости NH 2 – COOH Глицин (Гли) NH 2 – CH – COOH СН СН 3 Аланин (Ала) NH 2 – CH – COOH СН 2 СН СН 3 NH 2 – CH – COOH СН 3 Лейцин (Лей) СН 2 - СН 3 Изолейцин (Иле) СН 3 Валин (Вал)
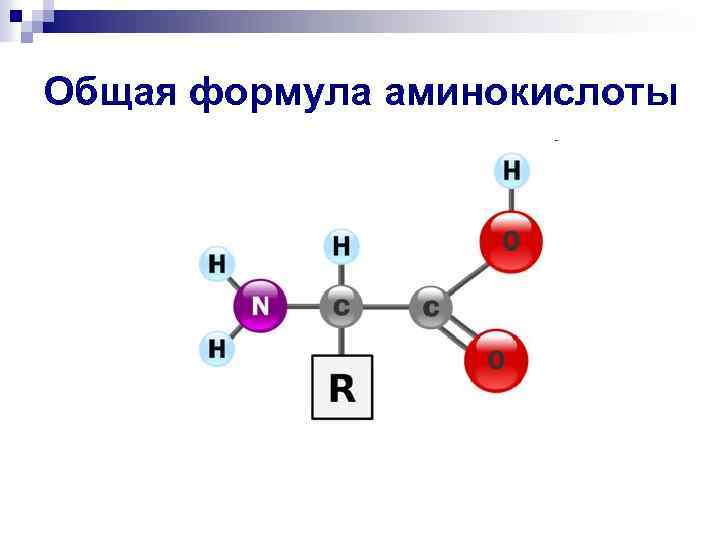 Общая формула аминокислоты
Общая формула аминокислоты
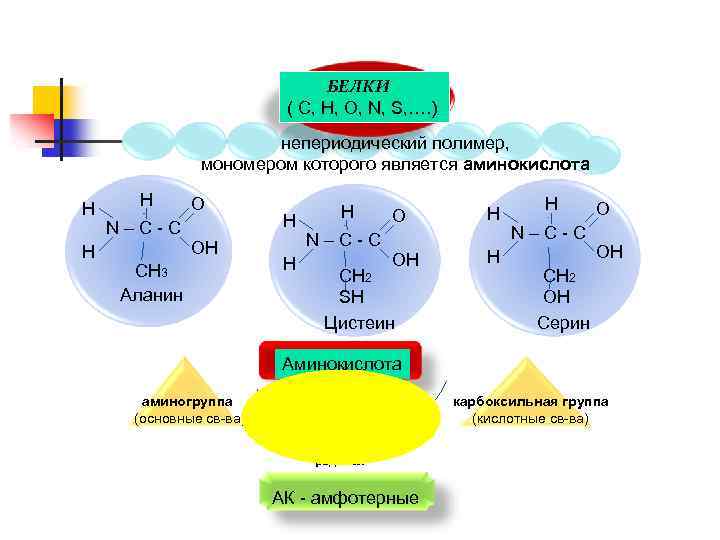 БЕЛКИ ( С, Н, О, N, S, …. ) непериодический полимер, мономером которого является аминокислота Н Н Н N–С-С О ОН СН 3 Аланин Н Н Н N–С-С О Н ОН Н СН 2 SН Цистеин Н N–С-С О ОН СН 2 ОН Серин Аминокислота аминогруппа (основные св-ва) Н 2 N – СН – СООН R радикал АК - амфотерные карбоксильная группа (кислотные св-ва)
БЕЛКИ ( С, Н, О, N, S, …. ) непериодический полимер, мономером которого является аминокислота Н Н Н N–С-С О ОН СН 3 Аланин Н Н Н N–С-С О Н ОН Н СН 2 SН Цистеин Н N–С-С О ОН СН 2 ОН Серин Аминокислота аминогруппа (основные св-ва) Н 2 N – СН – СООН R радикал АК - амфотерные карбоксильная группа (кислотные св-ва)
 Главное – система… n n n АК (по R): Неполярные Полярные + Заряженные -- АК (по отношению к Н 2 О) n Гидрофильные? n Гидрофобные?
Главное – система… n n n АК (по R): Неполярные Полярные + Заряженные -- АК (по отношению к Н 2 О) n Гидрофильные? n Гидрофобные?
 Невозможно забыть… АК (по способностити синтезироватьсяся в организме) Незаменимые: Вал, Лей, Иле, Лиз, Мет, Три, Тре, Фен Заменимые
Невозможно забыть… АК (по способностити синтезироватьсяся в организме) Незаменимые: Вал, Лей, Иле, Лиз, Мет, Три, Тре, Фен Заменимые
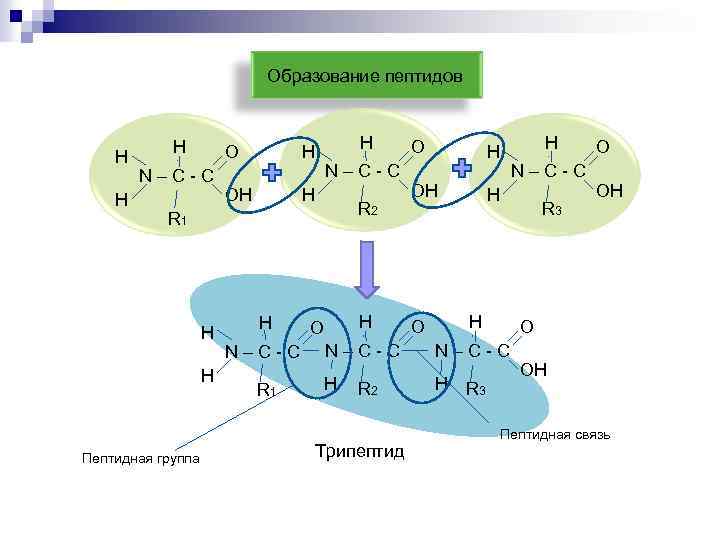 Образование пептидов Н Н Н О N–С-С ОН Н N–С-С R 2 R 1 Н Н Пептидная группа Н N–С-С R 1 Н О О Н Н ОН N–С-С Н R 3 Н О N–С-С Н Н Трипептид R 3 ОН О N–С-С R 2 О ОН Пептидная связь
Образование пептидов Н Н Н О N–С-С ОН Н N–С-С R 2 R 1 Н Н Пептидная группа Н N–С-С R 1 Н О О Н Н ОН N–С-С Н R 3 Н О N–С-С Н Н Трипептид R 3 ОН О N–С-С R 2 О ОН Пептидная связь
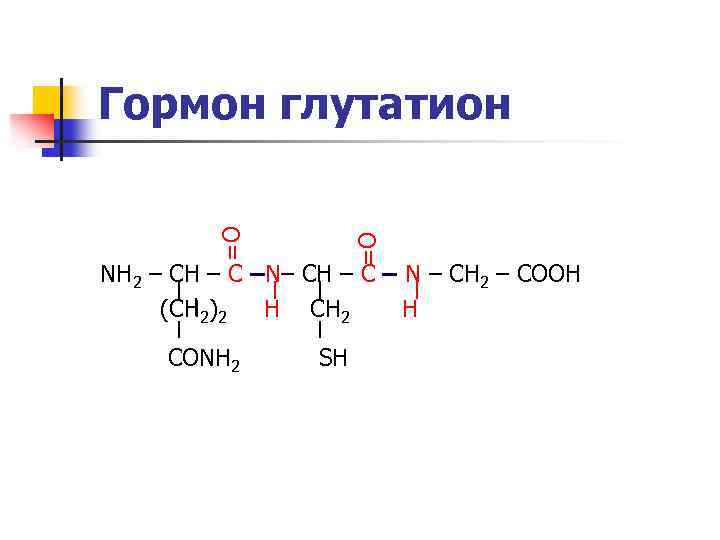 =O =O Гормон глутатион NH 2 – CH – С –N– CH – C – N – CH 2 – COOH (CH 2)2 H СН 2 H CONH 2 SH
=O =O Гормон глутатион NH 2 – CH – С –N– CH – C – N – CH 2 – COOH (CH 2)2 H СН 2 H CONH 2 SH
 Великое берет начало с малого Сир Публий, I в. до. н. э.
Великое берет начало с малого Сир Публий, I в. до. н. э.
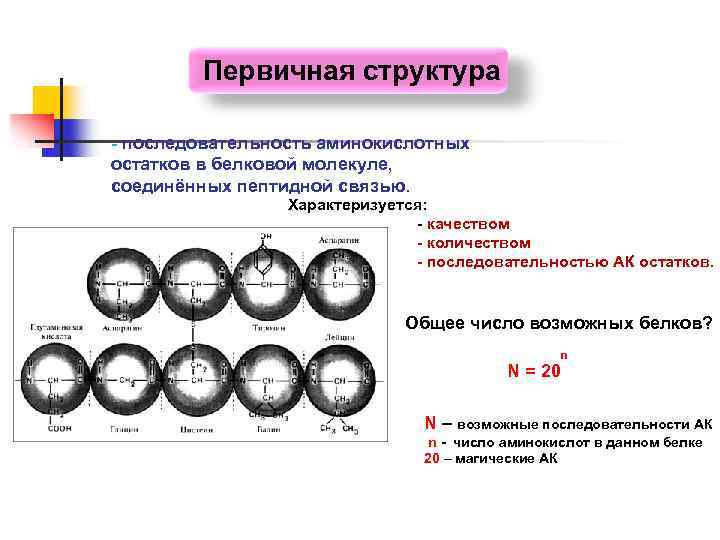 Первичная структура - последовательность аминокислотных остатков в белковой молекуле, соединённых пептидной связью. Характеризуется: - качеством - количеством - последовательностью АК остатков. Общее число возможных белков? n N = 20 N – возможные последовательности АК n - число аминокислот в данном белке 20 – магические АК
Первичная структура - последовательность аминокислотных остатков в белковой молекуле, соединённых пептидной связью. Характеризуется: - качеством - количеством - последовательностью АК остатков. Общее число возможных белков? n N = 20 N – возможные последовательности АК n - число аминокислот в данном белке 20 – магические АК
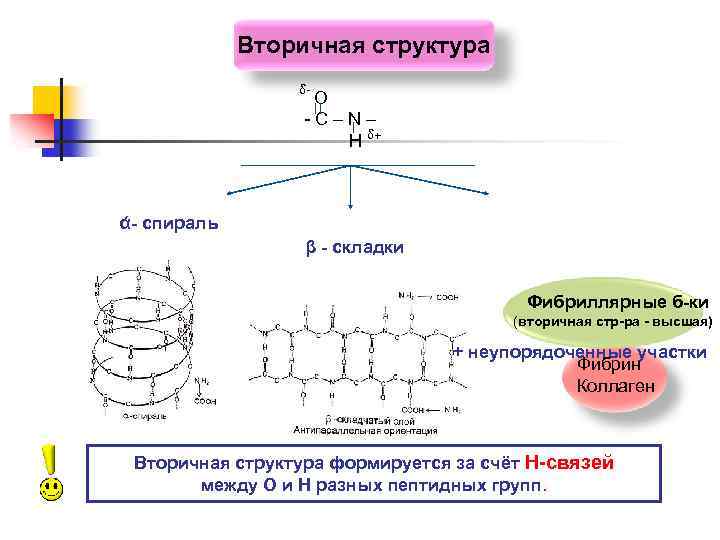 Вторичная структура δ- О -С–N– Н δ+ ά- спираль β - складки Фибриллярные б-ки (вторичная стр-ра - высшая) + неупорядоченные участки Фибрин Коллаген Вторичная структура формируется за счёт Н-связей между О и Н разных пептидных групп.
Вторичная структура δ- О -С–N– Н δ+ ά- спираль β - складки Фибриллярные б-ки (вторичная стр-ра - высшая) + неупорядоченные участки Фибрин Коллаген Вторичная структура формируется за счёт Н-связей между О и Н разных пептидных групп.
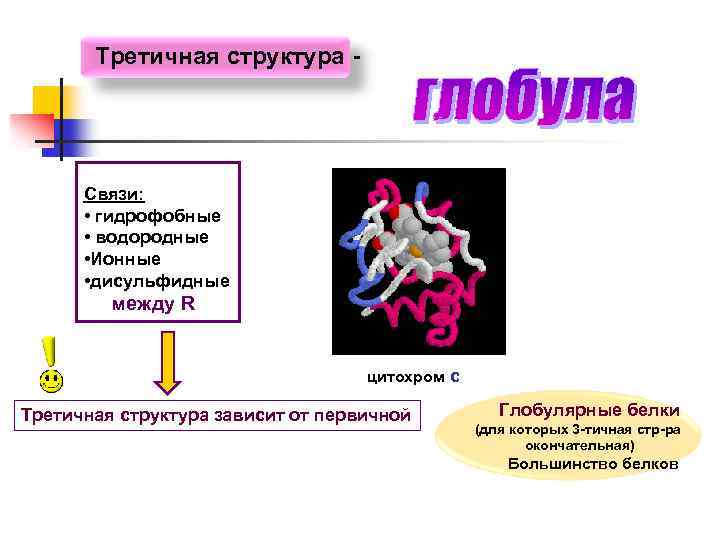 Третичная структура - Связи: • гидрофобные • водородные • Ионные • дисульфидные между R цитохром с Третичная структура зависит от первичной Глобулярные белки (для которых 3 -тичная стр-ра окончательная) Большинство белков
Третичная структура - Связи: • гидрофобные • водородные • Ионные • дисульфидные между R цитохром с Третичная структура зависит от первичной Глобулярные белки (для которых 3 -тичная стр-ра окончательная) Большинство белков
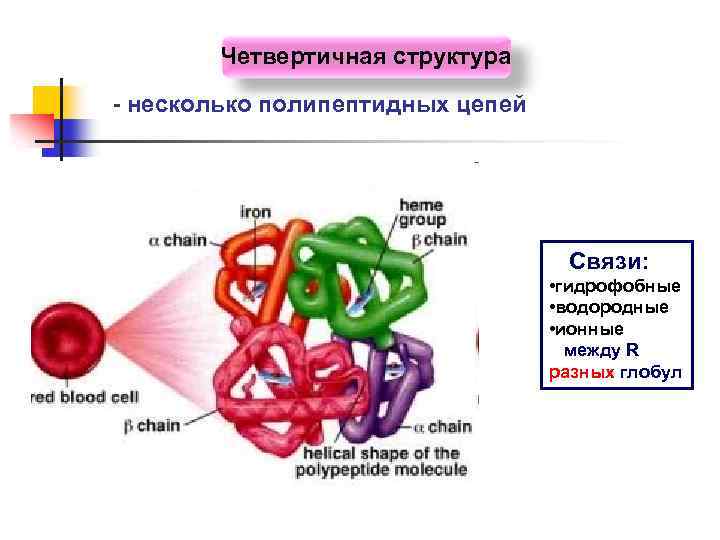 Четвертичная структура - несколько полипептидных цепей Связи: • гидрофобные • водородные • ионные между R разных глобул
Четвертичная структура - несколько полипептидных цепей Связи: • гидрофобные • водородные • ионные между R разных глобул
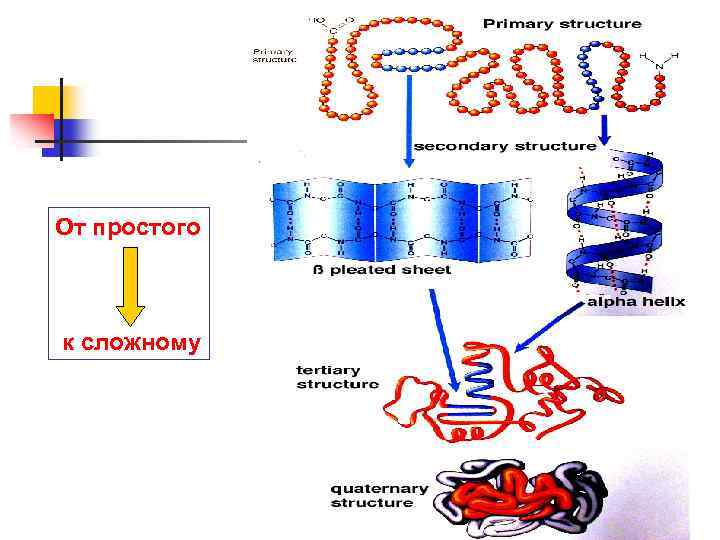 От простого к сложному
От простого к сложному
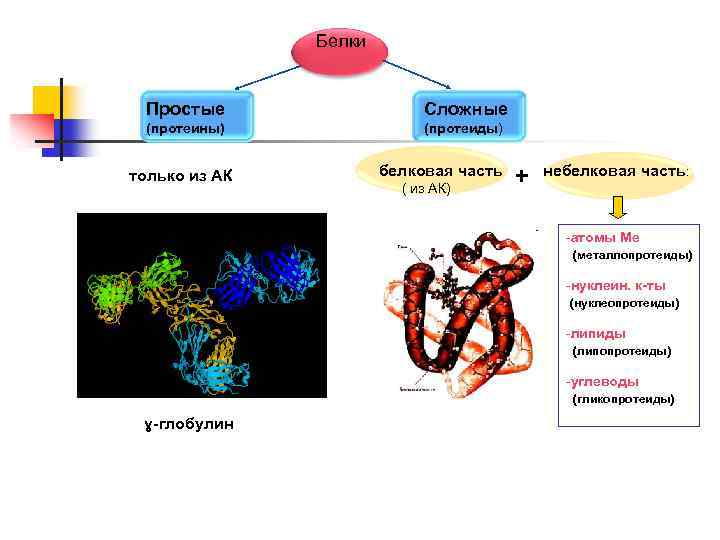 Белки Простые Сложные (протеины) (протеиды) только из АК белковая часть ( из АК) + небелковая часть: -атомы Ме (металлопротеиды) -нуклеин. к-ты (нуклеопротеиды) -липиды (липопротеиды) -углеводы (гликопротеиды) ɣ-глобулин
Белки Простые Сложные (протеины) (протеиды) только из АК белковая часть ( из АК) + небелковая часть: -атомы Ме (металлопротеиды) -нуклеин. к-ты (нуклеопротеиды) -липиды (липопротеиды) -углеводы (гликопротеиды) ɣ-глобулин
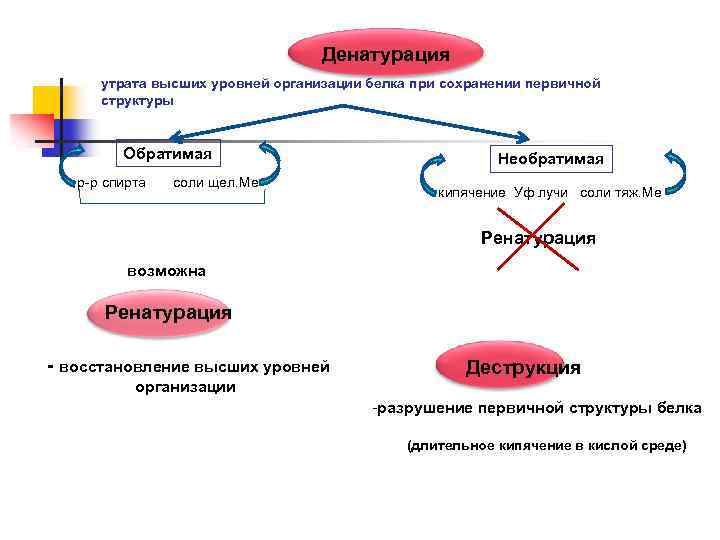 Денатурация утрата высших уровней организации белка при сохранении первичной структуры Обратимая р-р спирта соли щел. Ме Необратимая кипячение Уф лучи соли тяж. Ме Ренатурация возможна Ренатурация - восстановление высших уровней организации Деструкция -разрушение первичной структуры белка (длительное кипячение в кислой среде)
Денатурация утрата высших уровней организации белка при сохранении первичной структуры Обратимая р-р спирта соли щел. Ме Необратимая кипячение Уф лучи соли тяж. Ме Ренатурация возможна Ренатурация - восстановление высших уровней организации Деструкция -разрушение первичной структуры белка (длительное кипячение в кислой среде)


