 Повторение изученного в 8 классе
Повторение изученного в 8 классе
 Основные классы неорганических веществ l l l Эх. Оу Нх. Ас Ме(ОН)х Мех. Асу Классифицируйте следующие соединения: NO 2 Ca. SO 3 (Ca. ОН)2 СO 3 Na. Cl CO КOH Ca. O H 2 S Fe(OH)2 HNO 3 Cr. НРO 4 Al 2 O 3 Назовите вещества.
Основные классы неорганических веществ l l l Эх. Оу Нх. Ас Ме(ОН)х Мех. Асу Классифицируйте следующие соединения: NO 2 Ca. SO 3 (Ca. ОН)2 СO 3 Na. Cl CO КOH Ca. O H 2 S Fe(OH)2 HNO 3 Cr. НРO 4 Al 2 O 3 Назовите вещества.
 Алгоритм составления формул по валентности l Записать знаки химических элементов: первое место – Ме или не. Ме с меньшей ЭО второе место – не. Ме с большей ЭО l Над знаками элементов подписать валентность: первое место – № группы или указана в задании второе место – (8 – № группы) l Определить число атомов элементов (индекс) путем деления НОК (наименьшее общее кратное валентностей) на валентность
Алгоритм составления формул по валентности l Записать знаки химических элементов: первое место – Ме или не. Ме с меньшей ЭО второе место – не. Ме с большей ЭО l Над знаками элементов подписать валентность: первое место – № группы или указана в задании второе место – (8 – № группы) l Определить число атомов элементов (индекс) путем деления НОК (наименьшее общее кратное валентностей) на валентность
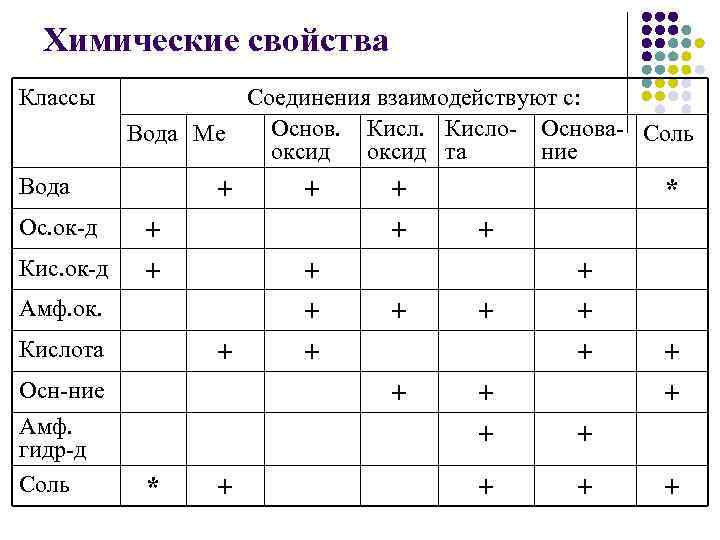 Химические свойства Классы Соединения взаимодействуют с: Основ. Кисло- Основа- Соль Вода Ме оксид та ние Вода Ос. ок-д Кис. ок-д + + + Амф. ок. Кислота + Осн-ние Амф. гидр-д Соль + + + + * + + + +
Химические свойства Классы Соединения взаимодействуют с: Основ. Кисло- Основа- Соль Вода Ме оксид та ние Вода Ос. ок-д Кис. ок-д + + + Амф. ок. Кислота + Осн-ние Амф. гидр-д Соль + + + + * + + + +
 Алгоритм составления уравнения реакции l l l Составить формулы всех вступающих в реакцию веществ, разделив их знаком (+). Поставить стрелку и составить формулы всех продуктов реакции, разделив их знаком (+). Уравнять количество атомов каждого элемента, используя коэффициенты и «правило чётности» .
Алгоритм составления уравнения реакции l l l Составить формулы всех вступающих в реакцию веществ, разделив их знаком (+). Поставить стрелку и составить формулы всех продуктов реакции, разделив их знаком (+). Уравнять количество атомов каждого элемента, используя коэффициенты и «правило чётности» .
 Окислительно-восстановительные реакции l Степень окисления Mn 2 O 3 + Si → Si. O 2 + Mn Cl 2 + KOH → KCl + KCl. O + H 2 O Zn + H 2 SO 4 → Zn. SO 4 + H 2 S + H 2 O l l Определить степень окисления элементов. Установить окислитель и восстановитель. Составить электронный баланс. Расставить коэффициенты.
Окислительно-восстановительные реакции l Степень окисления Mn 2 O 3 + Si → Si. O 2 + Mn Cl 2 + KOH → KCl + KCl. O + H 2 O Zn + H 2 SO 4 → Zn. SO 4 + H 2 S + H 2 O l l Определить степень окисления элементов. Установить окислитель и восстановитель. Составить электронный баланс. Расставить коэффициенты.
 Решение задач l l l Внимательно прочитать задачу, записать, что дано. Составить уравнение реакции. Найти количество вещества, которое дано по условию. Составить пропорцию, найти количество вещества, которое нужно найти. Найти массу или объем вещества. Какой объем водорода (н. у. ) выделится при действии на цинк раствора соляной кислоты, содержащей 10, 95 г хлороводорода?
Решение задач l l l Внимательно прочитать задачу, записать, что дано. Составить уравнение реакции. Найти количество вещества, которое дано по условию. Составить пропорцию, найти количество вещества, которое нужно найти. Найти массу или объем вещества. Какой объем водорода (н. у. ) выделится при действии на цинк раствора соляной кислоты, содержащей 10, 95 г хлороводорода?
 Домашнее задание l l l § 1 – 3 (Габриелян) упр. 2, 10 стр. 8 – 9, упр. 5 – 7, стр. 20. Дайте характеристику элементу № 19 исходя из положения элемента в Периодической системе (состав ядра, строение электронной оболочки, вид связи в простом веществе и тип кристаллической решетки, число валентных электронов, состав высшего оксида и гидроксида, их характер, состав летучего водородного соединения (для неметалла)). Закончите уравнения реакций, расставьте коэффициенты и назовите участвующие в них вещества: Na + … → Na. OH + H 2 Na. OH + … → Na 2 SO 3 Ba. Cl 2 + … → Ba. SO 4 + HCl. Вычислите массу осадка, образовавшегося при взаимодействии 27, 6 г карбоната калия с раствором хлорида магния. Расставьте коэффициенты методом электронного баланса, укажите окислитель и восстановитель: H 2 O + Fe → Fe 2 O 3 + H 2.
Домашнее задание l l l § 1 – 3 (Габриелян) упр. 2, 10 стр. 8 – 9, упр. 5 – 7, стр. 20. Дайте характеристику элементу № 19 исходя из положения элемента в Периодической системе (состав ядра, строение электронной оболочки, вид связи в простом веществе и тип кристаллической решетки, число валентных электронов, состав высшего оксида и гидроксида, их характер, состав летучего водородного соединения (для неметалла)). Закончите уравнения реакций, расставьте коэффициенты и назовите участвующие в них вещества: Na + … → Na. OH + H 2 Na. OH + … → Na 2 SO 3 Ba. Cl 2 + … → Ba. SO 4 + HCl. Вычислите массу осадка, образовавшегося при взаимодействии 27, 6 г карбоната калия с раствором хлорида магния. Расставьте коэффициенты методом электронного баланса, укажите окислитель и восстановитель: H 2 O + Fe → Fe 2 O 3 + H 2.