Лекция 3 - Неорганические вещества (1).ppt
- Количество слайдов: 10
 Поволжский государственный университет сервиса (ПВГУС) Кафедра «Современное естествознание» СЛАЙД-ЛЕКЦИИ по дисциплине «Химия» для СПО Составитель: асс. Беляева Ю. В. Тольятти, 2013
Поволжский государственный университет сервиса (ПВГУС) Кафедра «Современное естествознание» СЛАЙД-ЛЕКЦИИ по дисциплине «Химия» для СПО Составитель: асс. Беляева Ю. В. Тольятти, 2013
 ЧАСТЬ II – НЕОРГАНИЧЕСКАЯ ХИМИЯ Глава 6. Важнейшие классы неорганических соединений 6. 1. Классификация и номенклатура простых и сложных веществ 6. 2. Оксиды, их классификация и свойства 6. 3. Основания (гидроксиды металлов), их классификация и свойства 6. 4. Кислоты, их классификация и свойства 6. 5. Соли, их классификация и свойства
ЧАСТЬ II – НЕОРГАНИЧЕСКАЯ ХИМИЯ Глава 6. Важнейшие классы неорганических соединений 6. 1. Классификация и номенклатура простых и сложных веществ 6. 2. Оксиды, их классификация и свойства 6. 3. Основания (гидроксиды металлов), их классификация и свойства 6. 4. Кислоты, их классификация и свойства 6. 5. Соли, их классификация и свойства
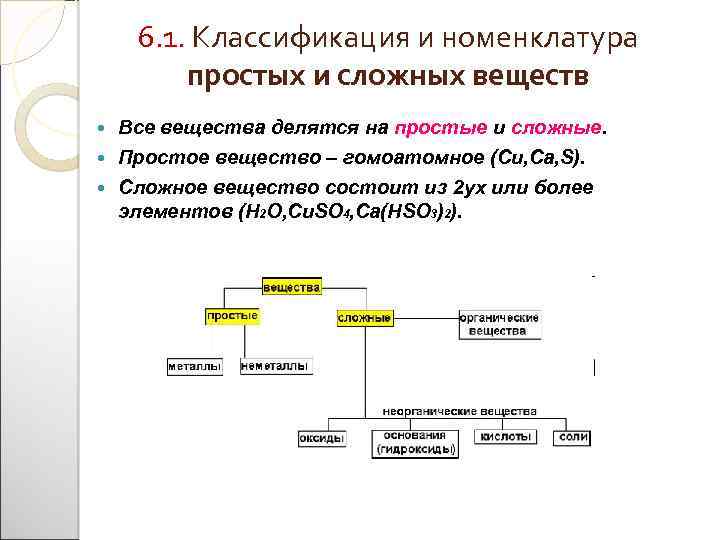 6. 1. Классификация и номенклатура простых и сложных веществ Все вещества делятся на простые и сложные. Простое вещество – гомоатомное (Cu, Ca, S). Сложное вещество состоит из 2 ух или более элементов (H 2 O, Cu. SO 4, Ca(HSO 3)2).
6. 1. Классификация и номенклатура простых и сложных веществ Все вещества делятся на простые и сложные. Простое вещество – гомоатомное (Cu, Ca, S). Сложное вещество состоит из 2 ух или более элементов (H 2 O, Cu. SO 4, Ca(HSO 3)2).
 6. 2. ОКСИДЫ, их классификация и свойства Оксиды – это сложные вещества, которые состоят из 2 ух элементов, одним из которых является кислород О. Например, Mg. O-оксид магния; Al 2 o 3 -оксид алюминия; Fe. O -оксид железа; Zr. O 2 -диоксид циркония или оксид циркония (IV) и т. д.
6. 2. ОКСИДЫ, их классификация и свойства Оксиды – это сложные вещества, которые состоят из 2 ух элементов, одним из которых является кислород О. Например, Mg. O-оксид магния; Al 2 o 3 -оксид алюминия; Fe. O -оксид железа; Zr. O 2 -диоксид циркония или оксид циркония (IV) и т. д.
 Куприт - Cu 2 O Физические свойства основных оксидов: 1. твердые вещества, 2. чаще нерастворимые в воде, 3. окрашенные в различные цвета, например Cu 2 O –красного цвета, Mg. O – белого. Физические свойства кислотных оксидов: 1. твердые, жидкие и газообразные: Р 2 О 5 – твердый, Si. O 2 – твердый, СО 2 – газообразный, . SO 3 – жидкий. Оксид серы VI - SO 3 2. к воде относятся по-разному (Р 2 О 5 – растворимый, Si. O 2 – нерастворимый). Кремний - Si. O 2 Физические свойства амфотерных оксидов: 1. твердые вещества, 2. мало или нерастворимые в воде. (Al 2 O 3 – нерастворим в Н 2 О), 3. некоторые из них имеют характерную окраску (Fe 2 О 3 – бурый). углекислый газ
Куприт - Cu 2 O Физические свойства основных оксидов: 1. твердые вещества, 2. чаще нерастворимые в воде, 3. окрашенные в различные цвета, например Cu 2 O –красного цвета, Mg. O – белого. Физические свойства кислотных оксидов: 1. твердые, жидкие и газообразные: Р 2 О 5 – твердый, Si. O 2 – твердый, СО 2 – газообразный, . SO 3 – жидкий. Оксид серы VI - SO 3 2. к воде относятся по-разному (Р 2 О 5 – растворимый, Si. O 2 – нерастворимый). Кремний - Si. O 2 Физические свойства амфотерных оксидов: 1. твердые вещества, 2. мало или нерастворимые в воде. (Al 2 O 3 – нерастворим в Н 2 О), 3. некоторые из них имеют характерную окраску (Fe 2 О 3 – бурый). углекислый газ
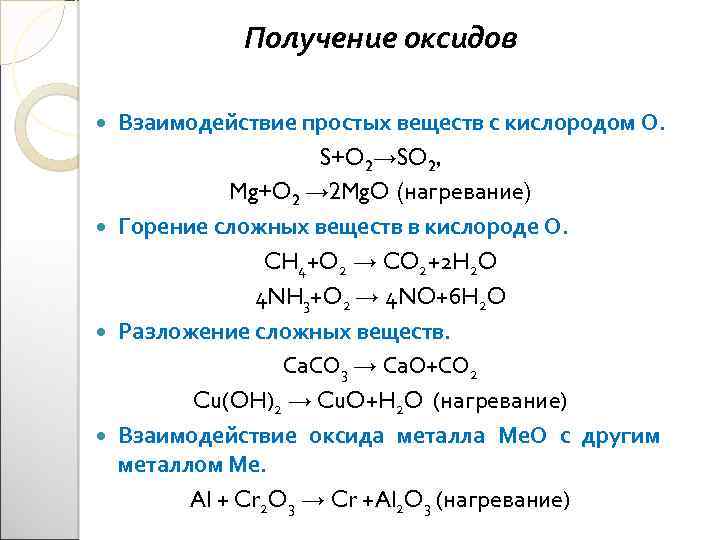 Получение оксидов Взаимодействие простых веществ с кислородом О. S+O 2→SO 2, Mg+O 2 → 2 Mg. O (нагревание) Горение сложных веществ в кислороде О. CH 4+O 2 → CO 2+2 H 2 O 4 NH 3+O 2 → 4 NO+6 H 2 O Разложение сложных веществ. Са. СО 3 → Са. О+СО 2 Cu(OH)2 → Cu. O+H 2 O (нагревание) Взаимодействие оксида металла Ме. О с другим металлом Ме. Al + Cr 2 O 3 → Cr +Al 2 O 3 (нагревание)
Получение оксидов Взаимодействие простых веществ с кислородом О. S+O 2→SO 2, Mg+O 2 → 2 Mg. O (нагревание) Горение сложных веществ в кислороде О. CH 4+O 2 → CO 2+2 H 2 O 4 NH 3+O 2 → 4 NO+6 H 2 O Разложение сложных веществ. Са. СО 3 → Са. О+СО 2 Cu(OH)2 → Cu. O+H 2 O (нагревание) Взаимодействие оксида металла Ме. О с другим металлом Ме. Al + Cr 2 O 3 → Cr +Al 2 O 3 (нагревание)
 Основные оксиды – это оксиды типичных металлов, которым соответствуют основания (гидроксиды). Химические свойства основных оксидов: 1. Оксид + вода = основание (щелочь) K 2 O + H 2 O→ 2 KOH Са. О + Н 2 О → Са(ОН)2 2. Оксид + кислота = соль + вода Zn. O + H 2 SO 4 → Zn. SO 4 + H 2 O Cu. O + H 2 SO 4 → Cu. SO 4 + H 2 O 3. Основный оксид + кислотный оксид = соль Ba. O + Si. O 2 → Ba 2 Si. O 3 Mg. O + CO 2 → Mg. CO 3
Основные оксиды – это оксиды типичных металлов, которым соответствуют основания (гидроксиды). Химические свойства основных оксидов: 1. Оксид + вода = основание (щелочь) K 2 O + H 2 O→ 2 KOH Са. О + Н 2 О → Са(ОН)2 2. Оксид + кислота = соль + вода Zn. O + H 2 SO 4 → Zn. SO 4 + H 2 O Cu. O + H 2 SO 4 → Cu. SO 4 + H 2 O 3. Основный оксид + кислотный оксид = соль Ba. O + Si. O 2 → Ba 2 Si. O 3 Mg. O + CO 2 → Mg. CO 3
 Кислотные оксиды – это оксиды неметаллов или переходных металлов в высоких степенях окисления, которым соответствуют кислоты. Химические свойства кислотных оксидов: 1. Кислотный оксид + вода = кислота SO 3 + H 2 O → H 2 SO 4 CO 2 + H 2 O → H 2 CO 3 2. Кислотный оксид + основание(щелочь) = соль + вода CO 2 + Ca(OH)2 → Ca. CO 3↓ + H 2 O SO 2 + 2 Na. OH → Na 2 SO 3 + H 2 O 3. Основный оксид + кислотный оксид = соль K 2 O + Si. O 3 → K 2 SO 4 Mg. O + CO 2 → Mg. CO 3
Кислотные оксиды – это оксиды неметаллов или переходных металлов в высоких степенях окисления, которым соответствуют кислоты. Химические свойства кислотных оксидов: 1. Кислотный оксид + вода = кислота SO 3 + H 2 O → H 2 SO 4 CO 2 + H 2 O → H 2 CO 3 2. Кислотный оксид + основание(щелочь) = соль + вода CO 2 + Ca(OH)2 → Ca. CO 3↓ + H 2 O SO 2 + 2 Na. OH → Na 2 SO 3 + H 2 O 3. Основный оксид + кислотный оксид = соль K 2 O + Si. O 3 → K 2 SO 4 Mg. O + CO 2 → Mg. CO 3
 Амфотерные оксиды – это оксиды металлов, которые в зависимости от условий могут проявлять свойства либо кислотных, либо основных оксидов. Например, Ве. О, Zn. O, Pb. O, Sn. O, Al 2 O 3, Cr 2 O 3, Pb. O 2, Sn. O 2 Химические свойства амфотерных оксидов: 1. Амфотерный оксид + щелочь = соль + вода Al 2 O 3 + Na. OH(тв. ) → Na. Al. O 2 + H 2 O 2. Амфотерный оксид + кислота = соль + вода Al 2 O 3 + 6 HCl → 2 Al. Cl 3 + 3 H 2 O 3. Амфотерный оксид + кислотный оксид = соль Zn. O + SO 3 → Zn. SO 4 4. Амфотерный оксид + основный оксид = соль Be. O + K 2 O → K 2 Be. O 2
Амфотерные оксиды – это оксиды металлов, которые в зависимости от условий могут проявлять свойства либо кислотных, либо основных оксидов. Например, Ве. О, Zn. O, Pb. O, Sn. O, Al 2 O 3, Cr 2 O 3, Pb. O 2, Sn. O 2 Химические свойства амфотерных оксидов: 1. Амфотерный оксид + щелочь = соль + вода Al 2 O 3 + Na. OH(тв. ) → Na. Al. O 2 + H 2 O 2. Амфотерный оксид + кислота = соль + вода Al 2 O 3 + 6 HCl → 2 Al. Cl 3 + 3 H 2 O 3. Амфотерный оксид + кислотный оксид = соль Zn. O + SO 3 → Zn. SO 4 4. Амфотерный оксид + основный оксид = соль Be. O + K 2 O → K 2 Be. O 2
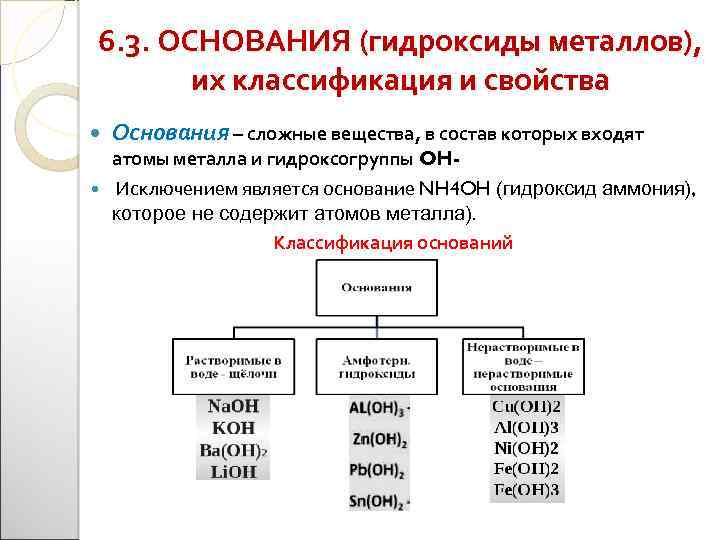 6. 3. ОСНОВАНИЯ (гидроксиды металлов), их классификация и свойства Основания – сложные вещества, в состав которых входят атомы металла и гидроксогруппы OH Исключением является основание NH 4 OH (гидроксид аммония), которое не содержит атомов металла). Классификация оснований
6. 3. ОСНОВАНИЯ (гидроксиды металлов), их классификация и свойства Основания – сложные вещества, в состав которых входят атомы металла и гидроксогруппы OH Исключением является основание NH 4 OH (гидроксид аммония), которое не содержит атомов металла). Классификация оснований


