Поверхностные явления — Внутри жидкости силы уравновешиваются










Копия Поверхностные явления.ppt
- Количество слайдов: 14
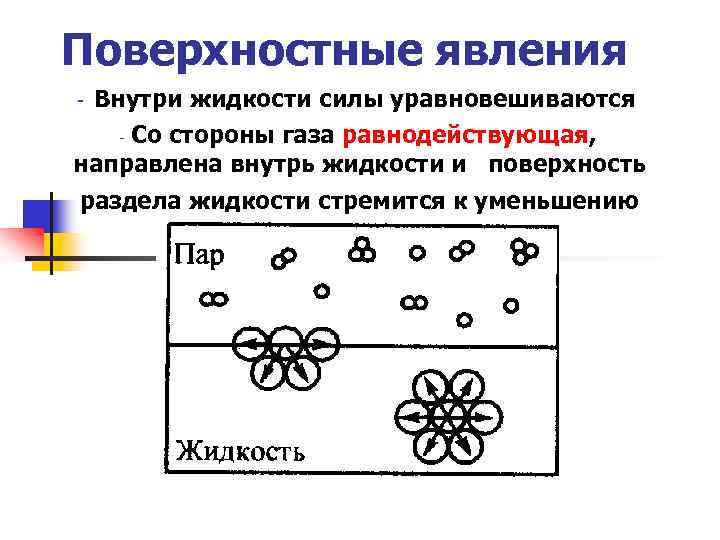
 Поверхностные явления - Внутри жидкости силы уравновешиваются Со стороны газа равнодействующая, - направлена внутрь жидкости и поверхность раздела жидкости стремится к уменьшению
Поверхностные явления - Внутри жидкости силы уравновешиваются Со стороны газа равнодействующая, - направлена внутрь жидкости и поверхность раздела жидкости стремится к уменьшению
 l Поверхностное натяжение — это работа, необходимая для создания 1 м 2 поверхности [ ]= Дж/м 2 l Поверхностное натяжение — это избыточная энергия, отнесённая к единице площади поверхности раздела фаз = Е/ S l Методы измерения l 1. Капиллярный метод
l Поверхностное натяжение — это работа, необходимая для создания 1 м 2 поверхности [ ]= Дж/м 2 l Поверхностное натяжение — это избыточная энергия, отнесённая к единице площади поверхности раздела фаз = Е/ S l Методы измерения l 1. Капиллярный метод
 l 2. Метод отрыва кольца. l 3. Сталагмометрический метод Траубе или метод счёта капель l 4. прибор Ребиндера l = К Р, l где К — константа капилляра
l 2. Метод отрыва кольца. l 3. Сталагмометрический метод Траубе или метод счёта капель l 4. прибор Ребиндера l = К Р, l где К — константа капилляра
 l зависит: l от природы вещества l Вода — 72, 7 эрг/см 2 l Ртуть — 430 l Спирт — 22 l Эфир — 17 l Сыворотка крови — 46… 47 l От температуры: - обратно пропорционально
l зависит: l от природы вещества l Вода — 72, 7 эрг/см 2 l Ртуть — 430 l Спирт — 22 l Эфир — 17 l Сыворотка крови — 46… 47 l От температуры: - обратно пропорционально
 l Поверхностная энергия Е = S l зависит от площади и от состава растворов: l ПАВ-поверностно активные вещества (мыла, спирты, жирные кислоты) l ПИВ –поверхностно инактивные (неорг-е кислоты, щелочи, соли) l ПАВ ¡ Ионогенные и неиногенные (не диссоциируют) ¡ Эндогенные (образуются в организме: белки, фосфолипиды, ЖК и их соли, гормоны) и экзогенные (раздражают и деструктивные в-ва) ¡ слюны – смачивают пищевые комков, антимикробное д. ) ¡ Печени – в желчи ЖК • Эмульгируют жиры • Активируют фермент липазу • Образуют водораствоимые комплексы с Ж ¡ легких- • повышают адсорбцию О 2 • Препятятвуют слипанию альвеол
l Поверхностная энергия Е = S l зависит от площади и от состава растворов: l ПАВ-поверностно активные вещества (мыла, спирты, жирные кислоты) l ПИВ –поверхностно инактивные (неорг-е кислоты, щелочи, соли) l ПАВ ¡ Ионогенные и неиногенные (не диссоциируют) ¡ Эндогенные (образуются в организме: белки, фосфолипиды, ЖК и их соли, гормоны) и экзогенные (раздражают и деструктивные в-ва) ¡ слюны – смачивают пищевые комков, антимикробное д. ) ¡ Печени – в желчи ЖК • Эмульгируют жиры • Активируют фермент липазу • Образуют водораствоимые комплексы с Ж ¡ легких- • повышают адсорбцию О 2 • Препятятвуют слипанию альвеол
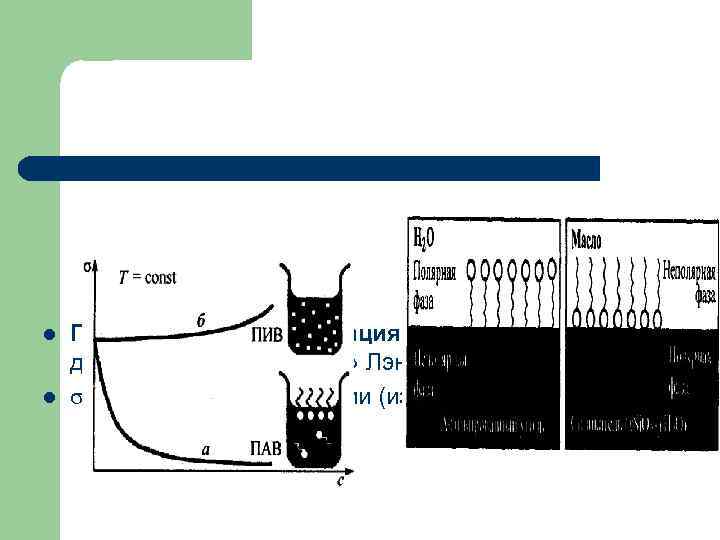
 l Поверхностная ориентация молекул ПАВ- дифильность : «частокол» Лэнгмюра l зависит от концентрации (изотерма или адсорбции)
l Поверхностная ориентация молекул ПАВ- дифильность : «частокол» Лэнгмюра l зависит от концентрации (изотерма или адсорбции)
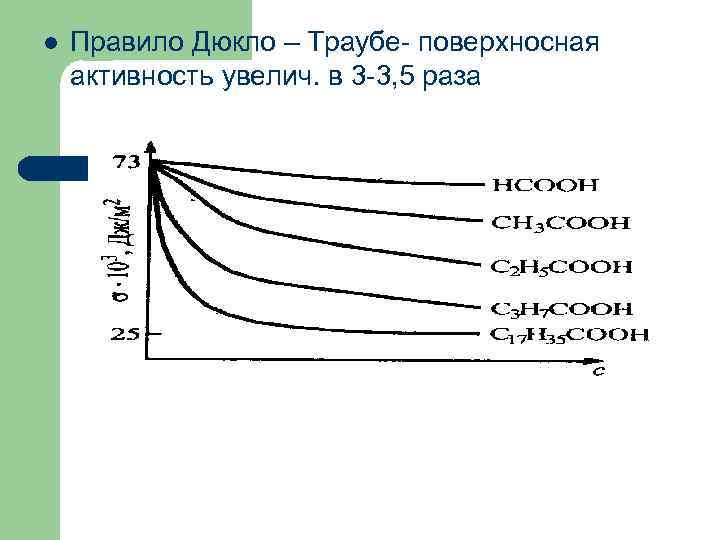
 l Правило Дюкло – Траубе- поверхносная активность увелич. в 3 -3, 5 раза
l Правило Дюкло – Траубе- поверхносная активность увелич. в 3 -3, 5 раза
 § Адсорбция - явление накопления одного вещества на поверхности другого. § Накопление одного вещества внутри другого называется абсорбцией. § Вещество, которое адсорбируется, называется адсорбтивом; на котором - адсорбентом. § Процесс, обратный адсорбции, называется десорбцией. § Удаление адсорбированных веществ с адсорбента при помощи растворителей носит название элюирования. § Адсорбция с химическим взаимодействием - хемосорбция. . § Адсорбция, абсорбция и хемосорбция - сорбция. §. Адсорбция зависит: § 1. От физической и химической природы адсорбтива и адсорбента. § 3. От температуры [с повышением температуры физическая адсорбция уменьшается, а химическая — увеличивается]. § 4. От концентрации адсорбируемого вещества. § 5. От степени раздробленности вещества
§ Адсорбция - явление накопления одного вещества на поверхности другого. § Накопление одного вещества внутри другого называется абсорбцией. § Вещество, которое адсорбируется, называется адсорбтивом; на котором - адсорбентом. § Процесс, обратный адсорбции, называется десорбцией. § Удаление адсорбированных веществ с адсорбента при помощи растворителей носит название элюирования. § Адсорбция с химическим взаимодействием - хемосорбция. . § Адсорбция, абсорбция и хемосорбция - сорбция. §. Адсорбция зависит: § 1. От физической и химической природы адсорбтива и адсорбента. § 3. От температуры [с повышением температуры физическая адсорбция уменьшается, а химическая — увеличивается]. § 4. От концентрации адсорбируемого вещества. § 5. От степени раздробленности вещества
 • Адсорбция на границе раздела жидкость-газ • Величину адсорбции на поверхности раствора можно выразить уравнением Гиббса: • , где
• Адсорбция на границе раздела жидкость-газ • Величину адсорбции на поверхности раствора можно выразить уравнением Гиббса: • , где
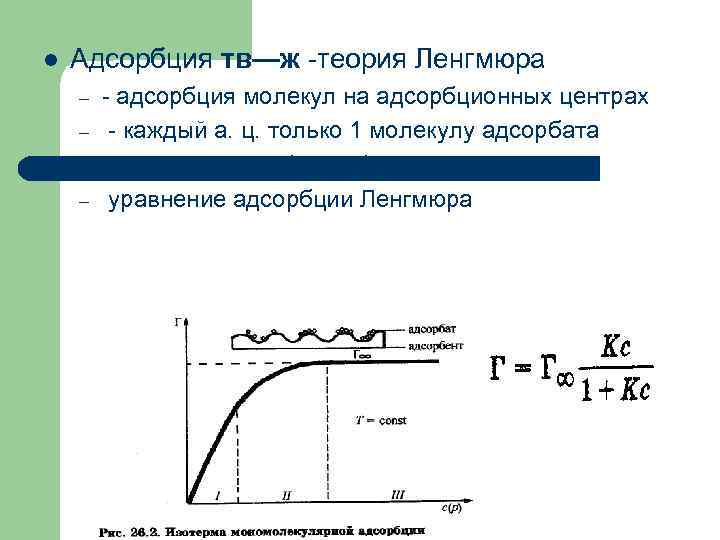
 l Адсорбция тв—ж -теория Ленгмюра – - адсорбция молекул на адсорбционных центрах – - каждый а. ц. только 1 молекулу адсорбата – - процесс адсорбции обратим – уравнение адсорбции Ленгмюра
l Адсорбция тв—ж -теория Ленгмюра – - адсорбция молекул на адсорбционных центрах – - каждый а. ц. только 1 молекулу адсорбата – - процесс адсорбции обратим – уравнение адсорбции Ленгмюра
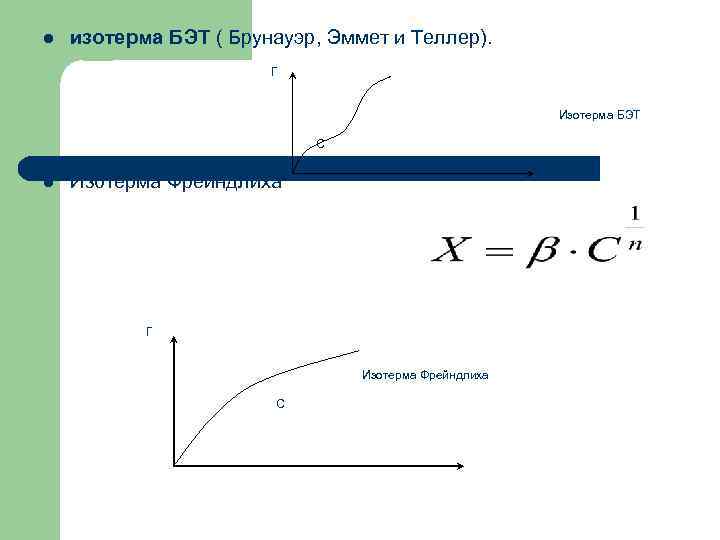
 l изотерма БЭТ ( Брунауэр, Эммет и Теллер). Г Изотерма БЭТ С l Изотерма Фрейндлиха Г Изотерма Фрейндлиха С
l изотерма БЭТ ( Брунауэр, Эммет и Теллер). Г Изотерма БЭТ С l Изотерма Фрейндлиха Г Изотерма Фрейндлиха С
 l Свойства адсорбции на твёрдых адсорбентах l 1. Адсорбция обратима. l 2. Повышение температуры понижает физадсорбцию, но увеличивает химадсорбцию. l 3 Повышение давления газов увеличивает адсорбции. l 4. При малых концентрациях преобладает адсорбция растворённого вещества, при больших концентрациях — адсорбция растворителя. l 5. На адсорбцию влияет природа адсорбента и адсорбтива l 6. Адсорбция на твёрдых адсорбентах носит избирательный характер.
l Свойства адсорбции на твёрдых адсорбентах l 1. Адсорбция обратима. l 2. Повышение температуры понижает физадсорбцию, но увеличивает химадсорбцию. l 3 Повышение давления газов увеличивает адсорбции. l 4. При малых концентрациях преобладает адсорбция растворённого вещества, при больших концентрациях — адсорбция растворителя. l 5. На адсорбцию влияет природа адсорбента и адсорбтива l 6. Адсорбция на твёрдых адсорбентах носит избирательный характер.
 l Избирательная адсорбция l 1. Правило Панета-Фаянса: l на твёрдом адсорбенте преимущественно адсорбируются ионы, входящие в состав адсорбента, или имеющие с адсорбентом общую группу. l 2. избирательный характер, зависит от заряда адсорбента и адсорбтива: (+ ) на (-) l 3. Многовалентные ионы адсорбируются сильнее одновалентных. l 4. Ионы одинакового заряда - в лиотропном ряду. Чем больше гидратирован ион, тем меньше адсорбируется. l В организме человека избирательно – токсины столбняка поражают клетки центральной нервной системы, а токсины дизентерии — вегетативную нервную систему. – Цианистые соединения блокируют железосодержащие дыхательные ферменты. ; – холерный токсин действует на клеточную мембрану.
l Избирательная адсорбция l 1. Правило Панета-Фаянса: l на твёрдом адсорбенте преимущественно адсорбируются ионы, входящие в состав адсорбента, или имеющие с адсорбентом общую группу. l 2. избирательный характер, зависит от заряда адсорбента и адсорбтива: (+ ) на (-) l 3. Многовалентные ионы адсорбируются сильнее одновалентных. l 4. Ионы одинакового заряда - в лиотропном ряду. Чем больше гидратирован ион, тем меньше адсорбируется. l В организме человека избирательно – токсины столбняка поражают клетки центральной нервной системы, а токсины дизентерии — вегетативную нервную систему. – Цианистые соединения блокируют железосодержащие дыхательные ферменты. ; – холерный токсин действует на клеточную мембрану.
 l Ионная адсорбция – Эквивалентная (редко) – Ионно-обменная (обмен одноименно заряженных ионов, – Функц. группами анионитов обычно являются группы ОН– и СН 3 СОО–. (ОН– обменивается на Cl-) – Функц. группами катионитов являются –СООН, –SO 3 H и –SH- группы. (Н+ на Са+) – Избирательная адсорбция
l Ионная адсорбция – Эквивалентная (редко) – Ионно-обменная (обмен одноименно заряженных ионов, – Функц. группами анионитов обычно являются группы ОН– и СН 3 СОО–. (ОН– обменивается на Cl-) – Функц. группами катионитов являются –СООН, –SO 3 H и –SH- группы. (Н+ на Са+) – Избирательная адсорбция

