Дисперсные системы.ppt
- Количество слайдов: 61

• Поверхностные явления лежат в основе адсорбционной терапии – удаление из желудочно-кишечного тракта при отравлениях токсинов токсикантов (яды вирусного, бактериального, грибкового и растительного происхождения) (прямые и побочные продукты антропогенной деятельности) • В медицинской практике широко применяются катионообменные смолы для декалцинирования крови с целю ее консервирования 10% водный раствор натрия цитрат при р. Н 77, 5 предохраняет кровь от свертывания

• Материал протезов, в том числе при протезировании полости рта, должен обладать биосовместимостью с биожидкостями и тканями. В противном случае на протезе будут адсорбироваться слоя белков и других поверхностно-активных веществ (ПАВ), что • ухудшает эксплуатационные характеристики протеза • вызывает воспалительные процессы • аллергические реакции в полости рта.
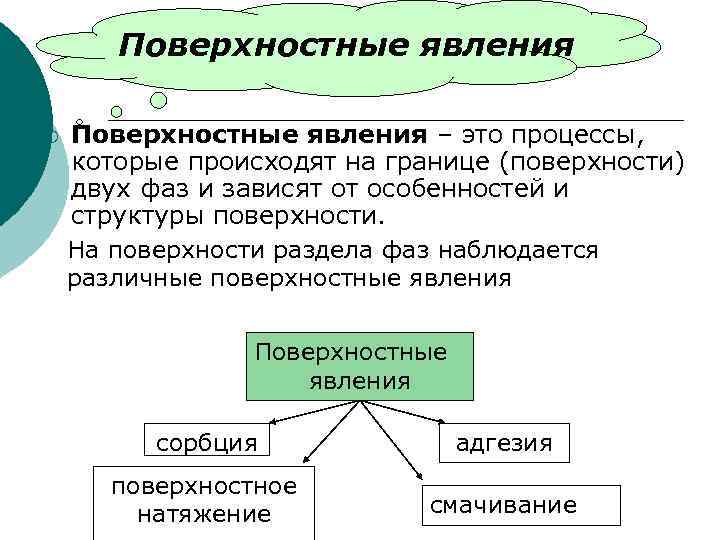
Поверхностные явления ¡ Поверхностные явления – это процессы, которые происходят на границе (поверхности) двух фаз и зависят от особенностей и структуры поверхности. На поверхности раздела фаз наблюдается различные поверхностные явления Поверхностные явления сорбция адгезия поверхностное натяжение смачивание
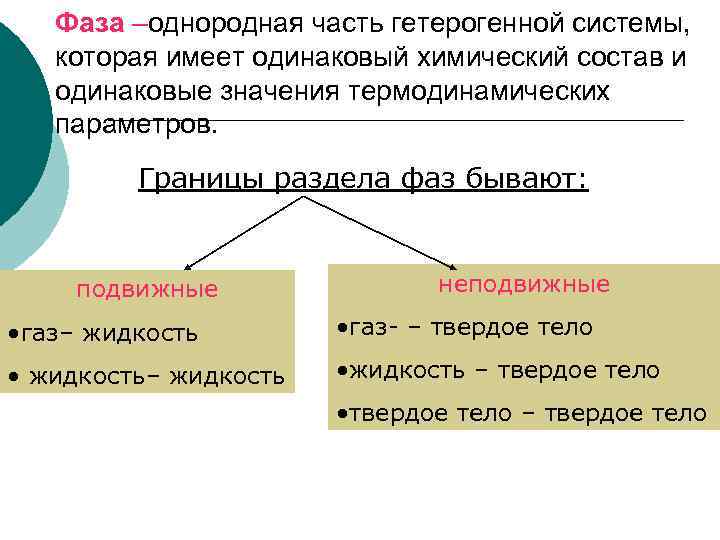
Фаза –однородная часть гетерогенной системы, которая имеет одинаковый химический состав и одинаковые значения термодинамических параметров. Границы раздела фаз бывают: подвижные неподвижные • газ– жидкость • газ- – твердое тело • жидкость– жидкость • жидкость – твердое тело • твердое тело – твердое тело

Свободная поверхностная энергия, поверхностное натяжение ¡ Свободной поверхностной энергией (Gs) называется термодинамическая функция, характеризующая энергию межмолекулярного взаимодействия частиц на поверхности раздела фаз с частицами каждой из контактирующих фаз. σ – удельная свободная поверхностная энергия (или коэффициент поверхностного натяжения [Дж/м 2 или Н/м]), S – площадь поверхности раздела фаз, м 2. Поверхностное натяжение (σ) – это величина, определяемая энергией, необходимой для увеличения поверхности жидкости на единиц площади.
![Рассмотрим в качестве примера жидкость , находящуюся в равновесии с паром [жидкость — пар] Рассмотрим в качестве примера жидкость , находящуюся в равновесии с паром [жидкость — пар]](https://present5.com/presentation/3/22386376_134679197.pdf-img/22386376_134679197.pdf-7.jpg)
Рассмотрим в качестве примера жидкость , находящуюся в равновесии с паром [жидкость — пар] Силы, действующие на молекулы (а) в объеме жидкой фазы, одинаковы и равнодействующая этих сил равна нулю (f= 0). Силы межмолекулярного взаимодействия молекул (б) нескомпенсированы, их равнодействующая сила не равна нулю и направлена в сторону жидкости. q. Рис. действие межмолекулярных сил на поверхности раздела и внутри жидкости

¡ При выходе молекулы из объема на поверхность совершается работа Ws против этих сил. В результате возникает поверхностный слой молекул с избыточной поверхностной энергией Гиббса. ¡ Таким образом, в поверхностном слое накапливается некоторый избыток энергии – поверхностная энергия Гиббса Gs. Поверхностное натяжение (σ) зависит от: 1. Природы жидкости; 2. Температуры - σ↓, при Т↑; 3. Давления - σ↓ при р↑; 4. Природы и концентрации растворенных веществ – могут ↓, ↑ и не влиять.
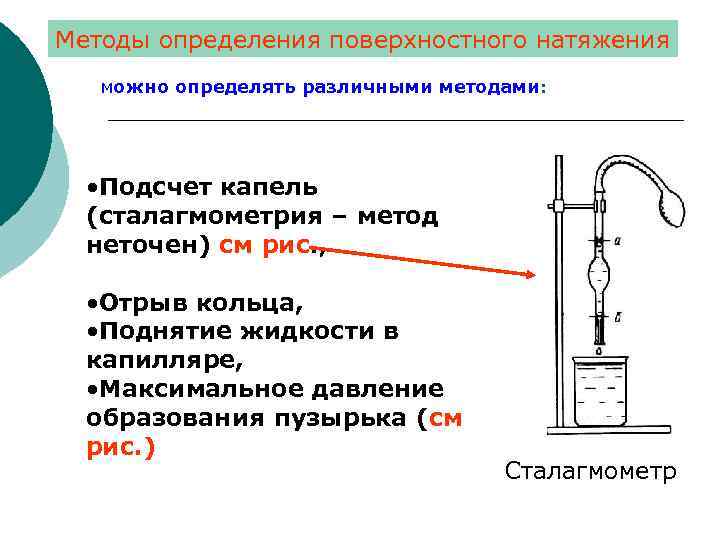
Методы определения поверхностного натяжения можно определять различными методами: • Подсчет капель (сталагмометрия – метод неточен) см рис. , • Отрыв кольца, • Поднятие жидкости в капилляре, • Максимальное давление образования пузырька (см рис. ) Сталагмометр
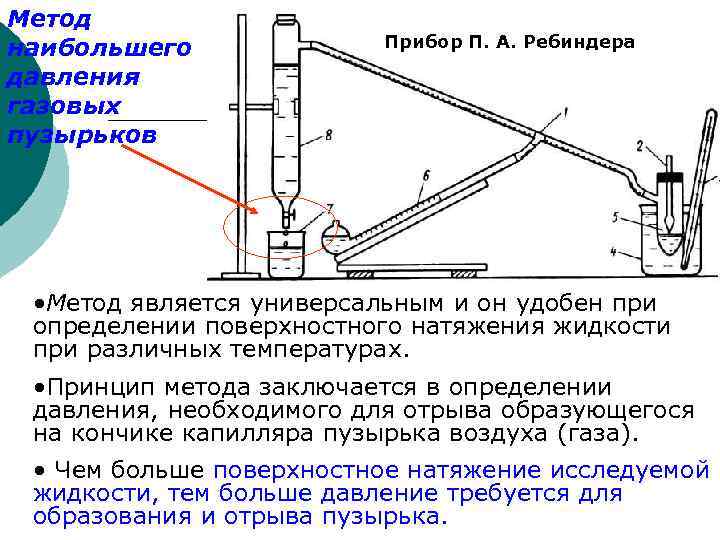
Метод наибольшего давления газовых пузырьков Прибор П. А. Ребиндера • Метод является универсальным и он удобен при определении поверхностного натяжения жидкости при различных температурах. • Принцип метода заключается в определении давления, необходимого для отрыва образующегося на кончике капилляра пузырька воздуха (газа). • Чем больше поверхностное натяжение исследуемой жидкости, тем больше давление требуется для образования и отрыва пузырька.

Из уравнения следует, что самопроизвольные поверхностные явления с уменьшением поверхностной энергии Гиббса (ΔG<0) возможны: 1)за счет уменьшения площади поверхности раздела фаз (ΔS< 0), что происходит при коалесценции (например, слиянии капелек жира на поверхности воды) и коагуляции (объединение более мелких частиц в агрегаты); 2) за счет уменьшения поверхностного натяжения (Δσ < 0), что наблюдается при сорбции (адсорбции) и ее последствия: смачивание , эмульгирование и др.

Сорбция и ее виды ¡ Сорбция (от латин. «sorbeo» поглощаю, втягиваю)– гетерогенный процесс самопроизвольного поглощения твердым телом или жидкостью (сорбентом) веществ (сорбтива) из окружающей среды. В зависимости от степени прочности связывания сорбтива сорбентом сорбция может быть обратимой и необратимой.

¡ Если она является обратимой (что бывает чаще), то в системе устанавливается равновесие, которое характеризуется константой сорбционного равновесия (Кс). Благодаря десорбции в воздухе над водной поверхностью всегда находятся летучие вещества, содержащиеся в данной водной системе, обуславливающие запах питьевой или сточной воды, пищевых продуктов, т. е. органолептические показатели их качества.
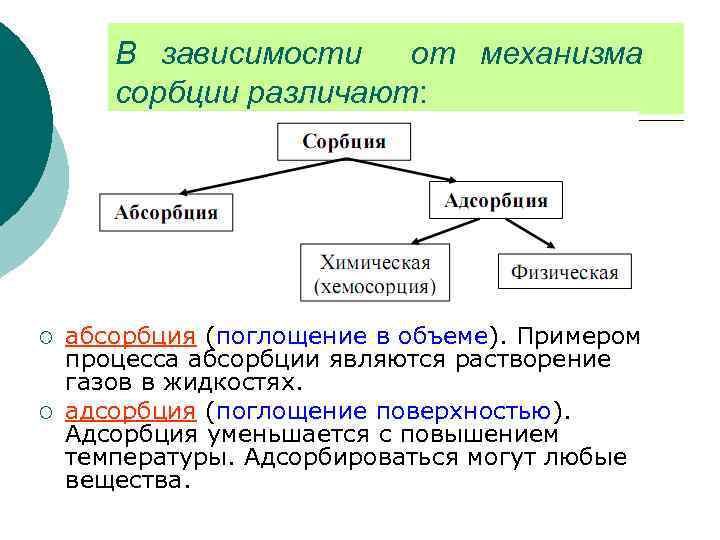
В зависимости от механизма сорбции различают: ¡ ¡ абсорбция (поглощение в объеме). Примером процесса абсорбции являются растворение газов в жидкостях. адсорбция (поглощение поверхностью). Адсорбция уменьшается с повышением температуры. Адсорбироваться могут любые вещества.
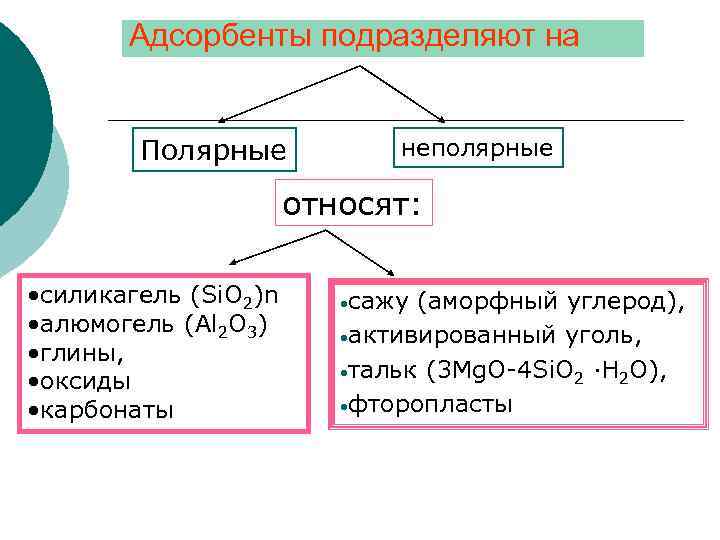
Адсорбенты подразделяют на Полярные неполярные относят: • силикагель (Si. O 2)n • алюмогель (Аl 2 О 3) • глины, • оксиды • карбонаты • сажу (аморфный углерод), • активированный уголь, • тальк (3 Mg. O-4 Si. O 2 ·H 2 O), • фторопласты
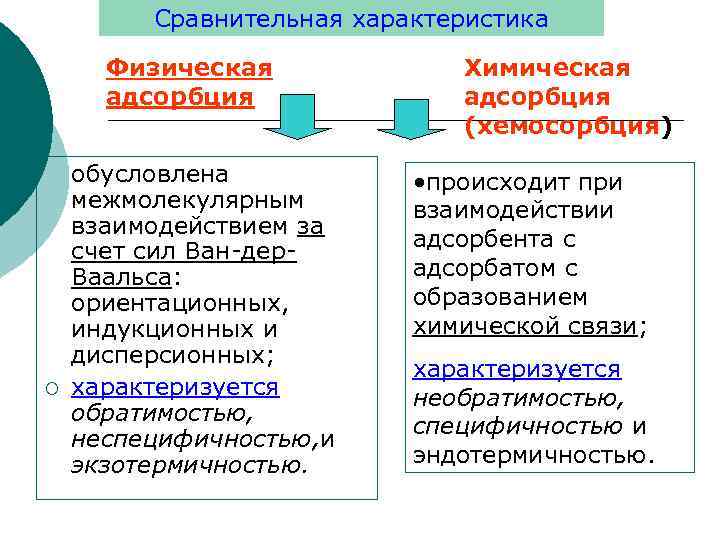
Сравнительная характеристика Физическая адсорбция ¡ обусловлена межмолекулярным взаимодействием за счет сил Ван-дер. Ваальса: ориентационных, индукционных и дисперсионных; характеризуется обратимостью, неспецифичностью, и экзотермичностью. Химическая адсорбция (хемосорбция) • происходит при взаимодействии адсорбента с адсорбатом с образованием химической связи; характеризуется необратимостью, специфичностью и эндотермичностью.

В соответствии с принципом Ле Шателье физической адсорбции способствуют: *снижение температуры, увеличение концентрации поглощаемого вещества или *повышение давления в системе при адсорбции газа или пара. q Химической адсорбции способствуют повышение температуры (приводит обычно к большему связыванию адсорбата). q

Мерой адсорбции на подвижной границе раздела фаз служит величина адсорбции Г (гамма), которая выражается количеством растворенного вещества, приходящегося на единицу площади поверхности (моль/м 2). ¡ Связь между величиной адсорбции и коэффициентом поверхностного натяжения устанавливает уравнение Гиббса: ¡

где Сср. -средняя концентрация адсорбата в данном интервале концентраций; ¡ R — универсальная газовая постоянная, равная 8, 31 Н·м/(моль·К); Т — температура, К. ¡ Отношение -dσ/d. С принято называть поверхностной активностью (g). ¡ Поверхностная активность — это способность вещества изменять поверхностное натяжение. ¡

ПАВ – поверхностно-активные вещества ¡ ¡ – это вещества, понижающие поверхностное натяжение воды или согласно уравнению Гиббса, обладающие положительной адсорбцией. Их молекулы дифильны, т. е. содержат одновременно полярную группу (-ОН, СООН, -NH 2, -SO 3 H и др. ) и неполярную углеводородную цепь.
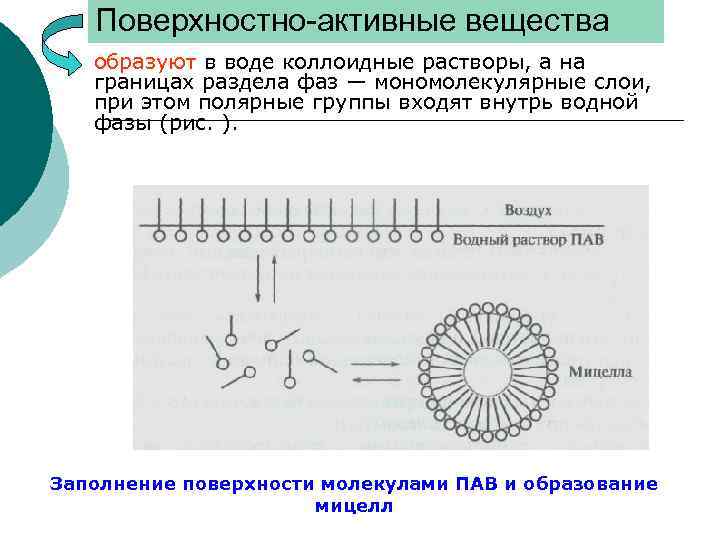
Поверхностно-активные вещества ¡ образуют в воде коллоидные растворы, а на границах раздела фаз — мономолекулярные слои, при этом полярные группы входят внутрь водной фазы (рис. ). Заполнение поверхности молекулами ПАВ и образование мицелл

Рис. Ориентация молекул ПАВ на границе масло—вода: ¡ ¡ ¡ а — ПАВ с преобладанием гидрофильных свойств и высокой поверхностной активностью; б — ПАВ с одинаково выраженными гидрофильно-гидрофобными свойствами; в — ПАВ с преобладанием гидрофобных свойств и низкой поверхностной активностью.

К биологически активным ПАВ относятся, в частности, растворимые в воде органические кислоты и их соли, сложные эфиры, белки, фосфолипиды и др. ¡ С помощью этих веществ поддерживается гидрофильнолипофильный гомеостаз организма, в частности осуществляется транспорт жиров. ¡
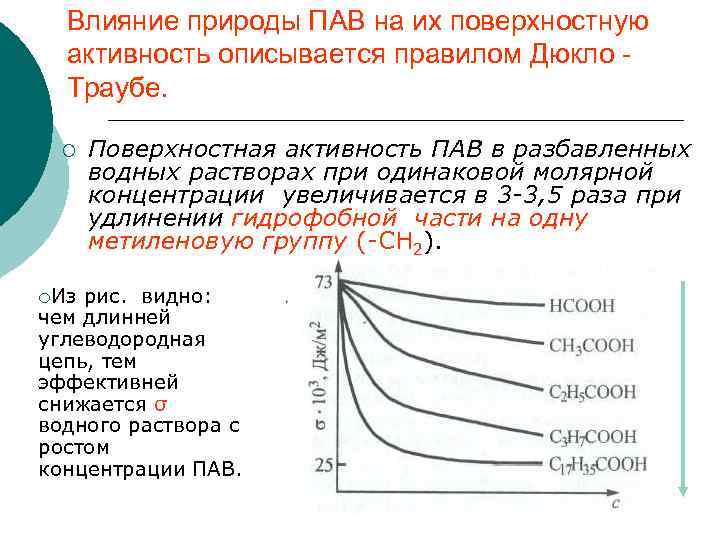
Влияние природы ПАВ на их поверхностную активность описывается правилом Дюкло Траубе. ¡ ¡Из Поверхностная активность ПАВ в разбавленных водных растворах при одинаковой молярной концентрации увеличивается в 3 -3, 5 раза при удлинении гидрофобной части на одну метиленовую группу (-СН 2). рис. видно: чем длинней углеводородная цепь, тем эффективней снижается σ водного раствора с ростом концентрации ПАВ.

¡ С удлинением углеводородной цепи усиливаются гидрофобные свойства молекул и понижается растворимость вещества в воде, при этом молекулы вытесняются на поверхность, снижая поверхностное натяжение.

Предельная адсорбция ¡ С увеличением концентрации ПАВ величина адсорбции возрастает сначала резко, а затем дальнейшее увеличение концентрации ПАВ вызывает незначительное увеличение адсорбции и, в конце концов, величина адсороции перестает зависеть от концентрации ПАВ. Величину Гmах называют предельной адсорбцией, она соответствует образованию на поверхности насыщенного мономолекулярного адсорбционного слоя.

¡ По значению Гmах можно найти площадь поперечного сечения молекулы (S) и ее осевую длину (δ), равную толщине насыщенного адсорбционного слоя: где NA — постоянная Авогадро; М — молярная масса ПАВ; ρ — плотность раствора ПАВ

Адсорбция на неподвижной границе раздела фаз Неэлектролиты и слабые электролиты на поверхности адсорбента адсорбируются из растворов в виде молекул и такой процесс называют молекулярной адсорбцией.

Для системы адсороат—адсороент влияние природы растворителя на адсорбцию может быть также сформулировано в виде правила: чем лучше в данном растворителе растворяется данный адсорбат, тем он хуже адсорбируется; чем хуже растворяется — тем лучше из него адсорбируется.

Величину адсорбции из растворов экспериментально определяют по изменению концентрации вещества после завершения адсорбции

Адсорбция сильных электролитов Ионная адсорбция

Адсорбируемость ионов определяется величиной их заряда, радиуса и степенью сольватации. ¡ ¡ При равенстве заряда лучше адсорбируются ионы с большим радиусом, так как они менее сольватированы.
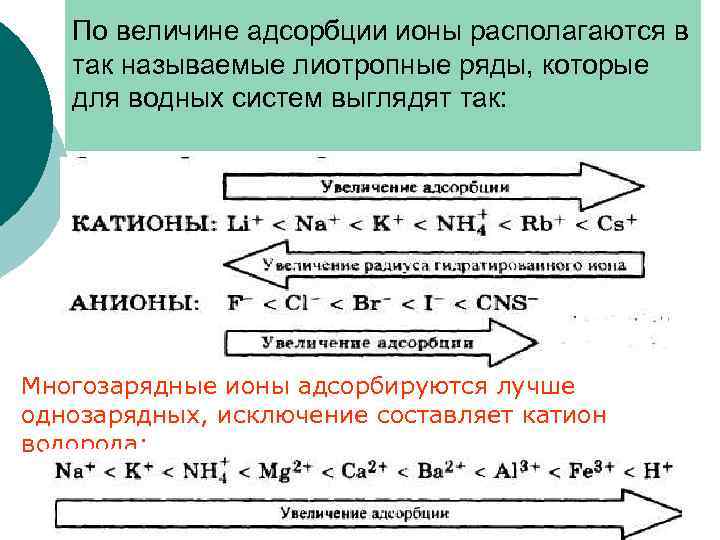
По величине адсорбции ионы располагаются в так называемые лиотропные ряды, которые для водных систем выглядят так: Многозарядные ионы адсорбируются лучше однозарядных, исключение составляет катион водорода:

При эквивалентной адсорбции ¡ ¡ катионы и анионы адсорбируются в таких количествах, которые соответствуют нулевому суммарному заряду (т. е. поверхность осадка не заряжена). Эквивалентную адсорбцию формально можно рассматривать как адсорбцию неэлектролита, так как при этом не возникают отрицательно или положительно заряженные поверхности.

Избирательная адсорбция • При избирательной адсорбции на поверхности адсорбента накапливаются либо катионы, либо анионы. • Ионы противоположного заряда сохраняют при этом относительную подвижность в растворе. • Таким образом, в результате избирательной адсорбции возникают заряженные поверхности. В соответствии с правилом Панета— Фаянса: из раствора преимущественно адсорбируются ионы, которые входят в состав кристаллической решетки адсорбента или им изоморфные (сходные по строению).
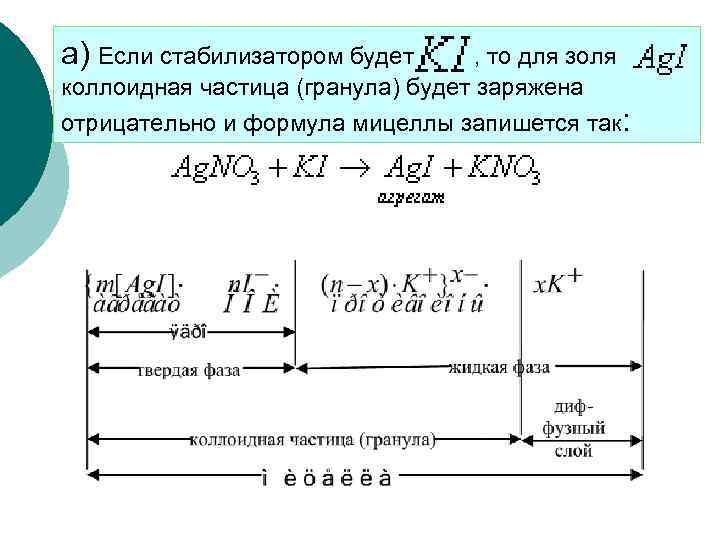
а) Если стабилизатором будет , то для золя коллоидная частица (гранула) будет заряжена отрицательно и формула мицеллы запишется так:
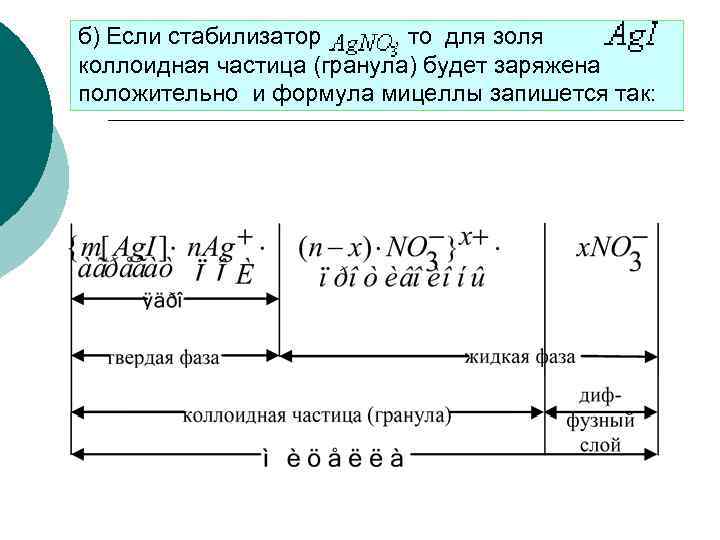
б) Если стабилизатор , то для золя коллоидная частица (гранула) будет заряжена положительно и формула мицеллы запишется так:

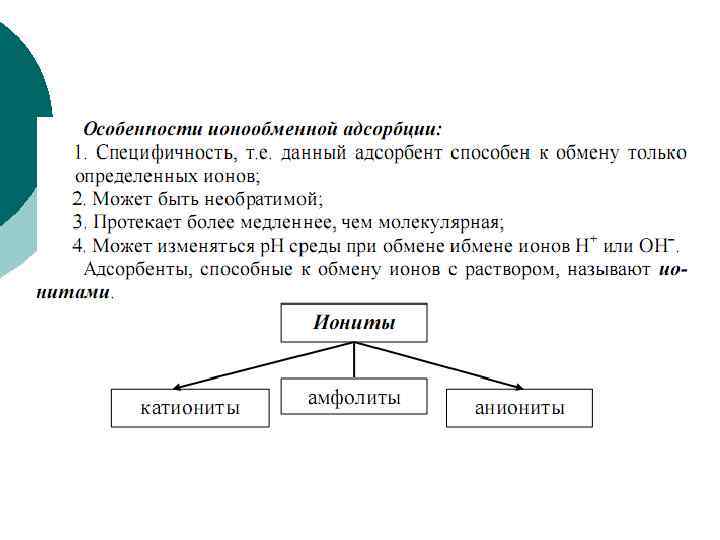

Ионнобменные реакции выражается уравнениями:

Активность ионитов- это ¡ поглощающая способность, характеризующаяся обменной ёмкостью, -количеством ионов (моль), связанных 1 г сухого ионита из раствора в равновесных условиях. Регенерация ионита Методика работы с ионообменными сорбентами для количественного анализа состоит из следующих операций: 1)подготовка ионита и заполнение колонки; 2)хроматографирование и определение содержания анализируемого вещества; 3) регенерация ионита.

¡ ¡ ¡ Особенностью ионитов является их способность к многократной регенерации (т. к. ионный обмен – обратимый процесс), после которой восстанавливается их ионообменная способность. Использованный ионит вновь регенерируют, пропуская через катионит 4% (или 2 М) раствор соляной кислоты, а через анионит — 5% раствор щелочи. Затем ионит промывают водой до нейтральной реакции (р. Н=7). Одну и ту же колонку можно использовать 10— 12 раз без регенерации

Хроматография ¡ ¡ Явление адсорбции лежит в основе такого важного метода анализа, как адсорбционная хроматография. Хроматография — физико-химический метод исследования, основанный на многократно повторяющихся процессах сорбции и десорбции между двумя фазами — подвижной и неподвижной. Основоположником данного метода является русский ботаник М. С. Цвет
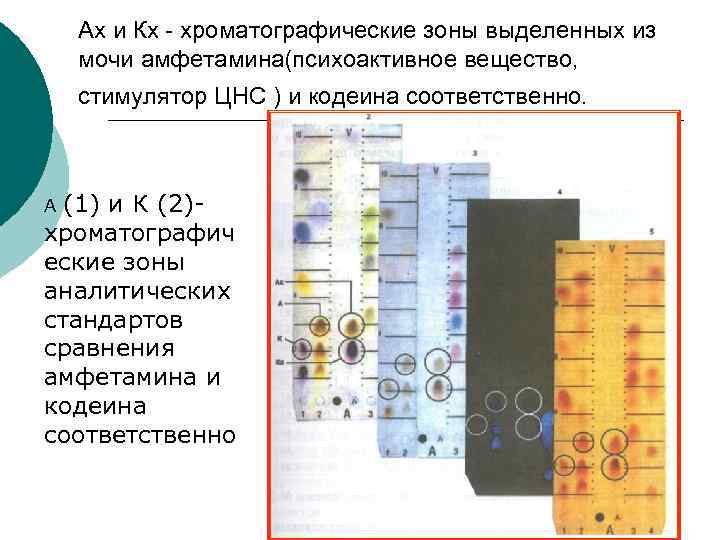
Ах и Кх - хроматографические зоны выделенных из мочи амфетамина(психоактивное вещество, стимулятор ЦНС ) и кодеина соответственно. (1) и К (2)хроматографич еские зоны аналитических стандартов сравнения амфетамина и кодеина соответственно А

Она является одним из чувствительных методов исследования, удовлетворяющим современным требованиям анализа. ¡ Хроматография является методом разделения сложных смесей на составные компоненты, которые не меняют своих первоначальных свойств. ¡

Методы хроматографии классифицируются: ¡ ¡ ¡ 1) по агрегатному состоянию смеси, в которой проводят разделение на компоненты (газовая, жидкостная и газожидкостная); 2) по механизму разделения (адсорбционная, распределительная, ионообменная, осадочная и др. ); 3) по форме проведения хроматографического процесса (колоночная, капиллярная, плоскостная, т. е. бумажная и тонкослойная).

ФИЗИКОХИМИЯ ДИСПЕРСНЫХ СИСТЕМ. РАСТВОРЫ ВМС Окружающий мир – растительные и животные организмы, ¡ объекты неживой природы (почва, горные породы, спрессованные порошки и др. ), ¡ продукты питания и т. д. – это дисперсионные системы разной степени организации. ¡

¡ Дисперсными системами (ДС) называют гетерогенные системы, в которых одна фаза является непрерывной (дисперсионная среда), а другая представляет собой совокупность частиц (дисперсная фаза), размеры которых превосходят молекулярные

Классификация ДС. 1. 2. 3. по агрегатному состоянию дисперсной фазы и дисперсионной среды по размеру частиц (дисперсности) по отсутствию или наличию взаимодействия между частицами дисперсной фазы
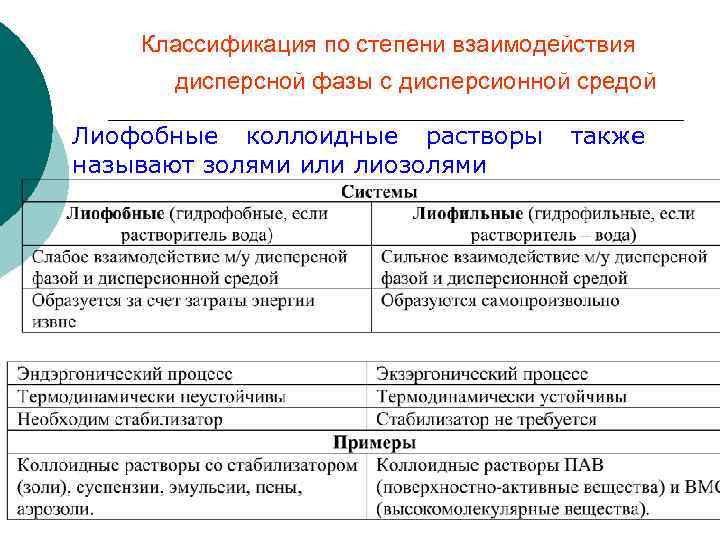
Классификация по степени взаимодействия дисперсной фазы с дисперсионной средой Лиофобные коллоидные растворы называют золями или лиозолями также

Условия образования и существования лиофобных коллоидных растворов ¡ ¡ Любое вещество может быть получено в коллоидном состоянии, но только необходимо создать следующие соответствующие условия: малая растворимость дисперсной фазы, то есть плохое сродство ее к дисперсионной среде; определенный размер частиц ( м); присутствие стабилизатора электролита.

Мицелла – это структурная коллоидная единица, т. е. частица дисперсной фазы, окруженная двойным электрическим слоем. ¡ ¡ ¡ Необходимыми условиями образования мицеллы являются: 1) Образование в результате реакции труднорастворимого вещества, m молекул которого образуют агрегат коллоидной частицы. 2) Наличие стабилизатора – электролита, предоставляющего ионы, адсорбируемые поверхностью труднорастворимого соединения. Согласно правилу Панетта– Фаянса, лучше всего адсорбируется тот ион, который входит в состав кристаллической решетки адсорбента.

¡ ¡ Абсорбируемые ионы, достраивающие кристаллическую решетку труднорастроримого соединения, называют потенциалопределяющими ионами (ПОИ) коллоидной частицы, поскольку заряд частицы совпадает по знаку с зарядом этих ионов. Адсорбция потенциалопределяющих ионов происходит самопроизвольно, сопровождаясь уменьшением свободной энергии поверхности ядра (∆Gs). Стабилизатором, как правило, является исходное вещество, взятое в избытке.

• Агрегат с потенциал определяющими ионами образуют ядро мицеллы. • Другие ионы стабилизатора (противоионы) образуют около твердой поверхности два слоя: адсорбционный (неподвижный), прочно связанный с ядром, и диффузионный (подвижный), расположенный на определенном расстоянии от ядра в дисперсионной среде. • Количества ПОИ и противоионов должны соответствовать их стехиометрии в молекуле стабилизатора.

¡ ¡ ¡ Ядро совместно с адсорбционным слоем противоионов называется коллоидной частицей (гранулой). Коллоидная частица (гранула), окруженная противоионами электролита, называется мицеллой. Мицелла – нейтральная частица, а коллоидная частица, как правило, имеет заряд, знак и величина которого определяются электрокинетическим потенциалом , возникающим на границе между адсорбционным и диффузным слоем.

¡ ¡ Коагуляция – процесс объединения коллоидных частиц с образованием более крупных агрегатов из-за потери коллоидным раствором агрегативной устойчивости. Согласно правилу Шульце – Гарди: коагулирующим действием обладает тот ион электролита, который имеет заряд, противоположный заряду гранулы. Коагулирующее действие ионов тем сильнее, чем выше заряд иона – коагулятора (правило значимости).

¡ ¡ Однако от правила Шульце – Гарди встречаются отклонения, поскольку на порог коагуляции кроме заряда иона- коагулянта влияет радиус этого иона и природа иона, сопутствующего иону-коагулянту. Поэтому влияние электролитов на коагуляцию коллоидных растворов необходимо учитывать при введении растворов солей в живые организмы. При этом важно помнить, что имеет значение не только концентрация электролита, но и заряд иона. Так, изотонический раствор нельзя заменить изотоническим раствором , так как двухзарядные ионы обладают более высоким коагулирующим действием, чем однозарядные.

¡ ¡ ¡ Коагуляция в ряде случаев зависит и от способа прибавления электролита–коагулятора. Экспериментально доказано, что если электролит добавлять к золю небольшими порциями, то в итоге коагуляция наступает при более высокой концентрации электролита, чем при внесении сразу большого его количества и такое явление называют привыканием золей. Причиной привыкание золей может быть образование петизатора или адсорбция ионов, заряженных одноименно с частицей, что приводит к повышению первоначального заряда частиц. В целом, принимая во внимание эти данные, следует заметить, что растворы электролитов необходимо водить внутривенно или внутримышечно очень медленно, чтобы не вызвать коагуляцию.

¡ Прозрачные, опалесцирующие при боковом освещении, дают конус Тиндаля (т. е. размер достаточен, чтобы рассеивать свет)


Дисперсные системы.ppt