PYaiDS_2010_L_8.ppt
- Количество слайдов: 21
 ПОВЕРХНОСТНЫЕ ЯВЛЕНИЯ И ДИСПЕРСНЫЕ СИСТЕМЫ ЛЕКЦИЯ 8
ПОВЕРХНОСТНЫЕ ЯВЛЕНИЯ И ДИСПЕРСНЫЕ СИСТЕМЫ ЛЕКЦИЯ 8
 Содержание лекции Получение и очистка дисперсных систем 1. Способы получения дисперсных систем. 2. Диспергационные методы получения дисперсных систем. 3. Конденсационные методы получения дисперсных систем. 4. Мембранные методы очистки дисперсных систем.
Содержание лекции Получение и очистка дисперсных систем 1. Способы получения дисперсных систем. 2. Диспергационные методы получения дисперсных систем. 3. Конденсационные методы получения дисперсных систем. 4. Мембранные методы очистки дисперсных систем.
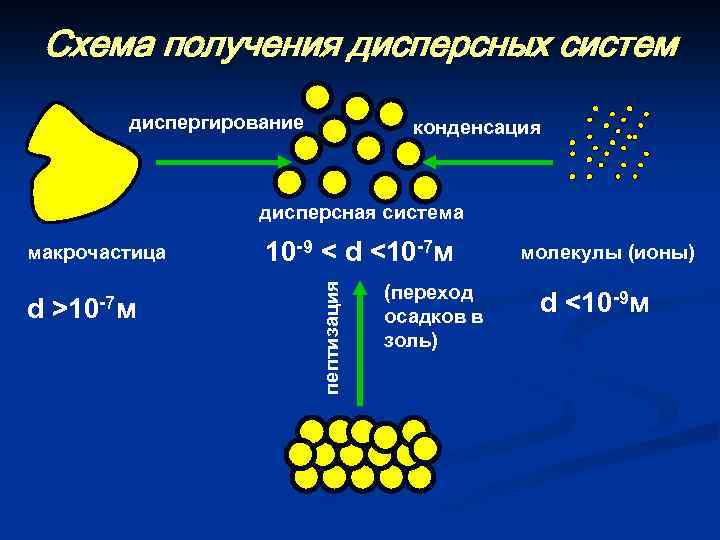 Схема получения дисперсных систем диспергирование конденсация дисперсная система d >10 -7 м 10 -9 < d <10 -7 м пептизация макрочастица (переход осадков в золь) молекулы (ионы) d <10 -9 м
Схема получения дисперсных систем диспергирование конденсация дисперсная система d >10 -7 м 10 -9 < d <10 -7 м пептизация макрочастица (переход осадков в золь) молекулы (ионы) d <10 -9 м
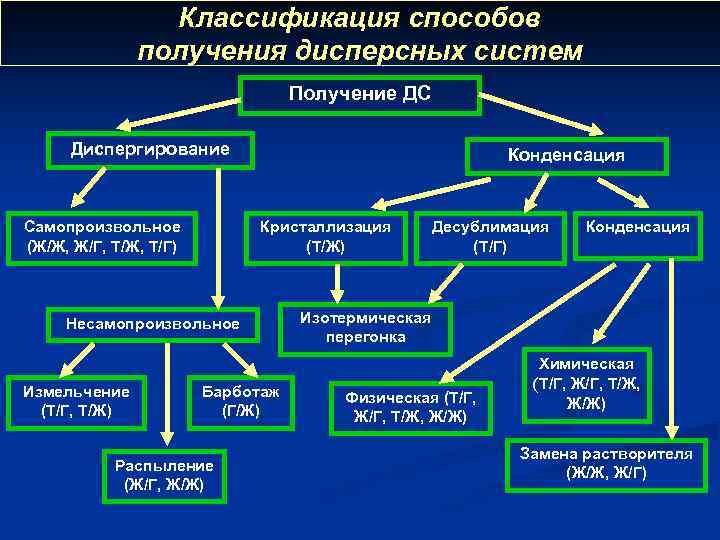 Классификация способов получения дисперсных систем Получение ДС Диспергирование Самопроизвольное (Ж/Ж, Ж/Г, Т/Ж, Т/Г) Конденсация Кристаллизация (Т/Ж) Несамопроизвольное Измельчение (Т/Г, Т/Ж) Барботаж (Г/Ж) Распыление (Ж/Г, Ж/Ж) Десублимация (Т/Г) Конденсация Изотермическая перегонка Физическая (Т/Г, Ж/Г, Т/Ж, Ж/Ж) Химическая (Т/Г, Ж/Г, Т/Ж, Ж/Ж) Замена растворителя (Ж/Ж, Ж/Г)
Классификация способов получения дисперсных систем Получение ДС Диспергирование Самопроизвольное (Ж/Ж, Ж/Г, Т/Ж, Т/Г) Конденсация Кристаллизация (Т/Ж) Несамопроизвольное Измельчение (Т/Г, Т/Ж) Барботаж (Г/Ж) Распыление (Ж/Г, Ж/Ж) Десублимация (Т/Г) Конденсация Изотермическая перегонка Физическая (Т/Г, Ж/Г, Т/Ж, Ж/Ж) Химическая (Т/Г, Ж/Г, Т/Ж, Ж/Ж) Замена растворителя (Ж/Ж, Ж/Г)
 Условия диспергирования n Самопроизвольное диспергирование (лиофильные системы) n Несамопроизвольное диспергирование (лиофобные системы) T∆Sэ > ∆H T∆Sэ < ∆H ∆H < 0 ∆H > 0 Wa > Wк Wa < Wк
Условия диспергирования n Самопроизвольное диспергирование (лиофильные системы) n Несамопроизвольное диспергирование (лиофобные системы) T∆Sэ > ∆H T∆Sэ < ∆H ∆H < 0 ∆H > 0 Wa > Wк Wa < Wк
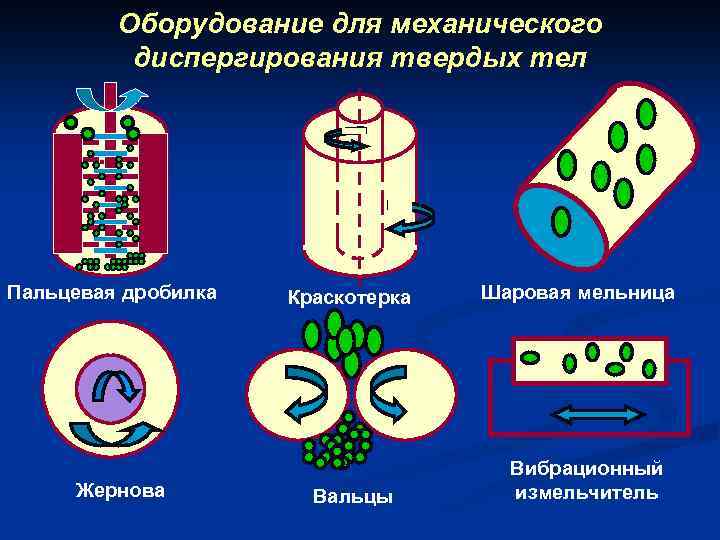 Оборудование для механического диспергирования твердых тел Пальцевая дробилка Жернова Краскотерка Вальцы Шаровая мельница Вибрационный измельчитель
Оборудование для механического диспергирования твердых тел Пальцевая дробилка Жернова Краскотерка Вальцы Шаровая мельница Вибрационный измельчитель
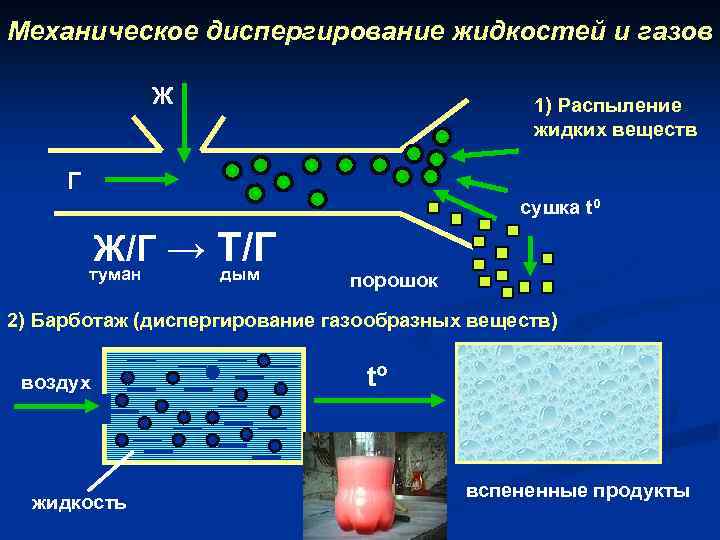 Механическое диспергирование жидкостей и газов Ж 1) Распыление жидких веществ Г сушка t 0 Ж/Г → Т/Г туман дым порошок 2) Барботаж (диспергирование газообразных веществ) воздух жидкость tº вспененные продукты
Механическое диспергирование жидкостей и газов Ж 1) Распыление жидких веществ Г сушка t 0 Ж/Г → Т/Г туман дым порошок 2) Барботаж (диспергирование газообразных веществ) воздух жидкость tº вспененные продукты
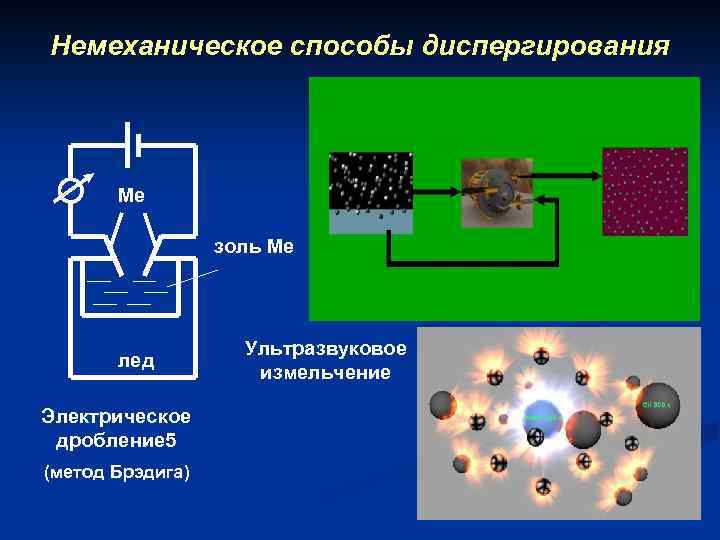 Немеханическое способы диспергирования Ме золь Ме лед Электрическое дробление 5 (метод Брэдига) Ультразвуковое измельчение
Немеханическое способы диспергирования Ме золь Ме лед Электрическое дробление 5 (метод Брэдига) Ультразвуковое измельчение
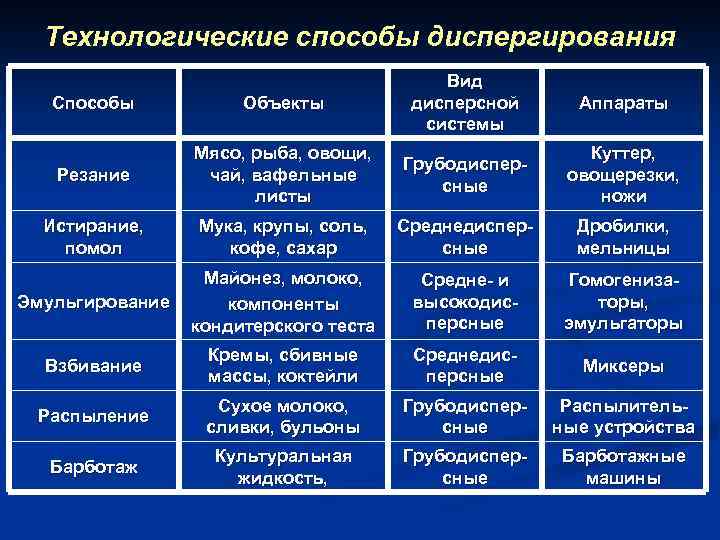 Технологические способы диспергирования Способы Объекты Вид дисперсной системы Резание Мясо, рыба, овощи, чай, вафельные листы Грубодисперсные Куттер, овощерезки, ножи Истирание, помол Мука, крупы, соль, кофе, сахар Среднедисперсные Дробилки, мельницы Эмульгирование Майонез, молоко, компоненты кондитерского теста Средне- и высокодисперсные Гомогенизаторы, эмульгаторы Взбивание Кремы, сбивные массы, коктейли Среднедисперсные Миксеры Распыление Сухое молоко, сливки, бульоны Грубодисперсные Распылительные устройства Барботаж Культуральная жидкость, Грубодисперсные Барботажные машины Аппараты
Технологические способы диспергирования Способы Объекты Вид дисперсной системы Резание Мясо, рыба, овощи, чай, вафельные листы Грубодисперсные Куттер, овощерезки, ножи Истирание, помол Мука, крупы, соль, кофе, сахар Среднедисперсные Дробилки, мельницы Эмульгирование Майонез, молоко, компоненты кондитерского теста Средне- и высокодисперсные Гомогенизаторы, эмульгаторы Взбивание Кремы, сбивные массы, коктейли Среднедисперсные Миксеры Распыление Сухое молоко, сливки, бульоны Грубодисперсные Распылительные устройства Барботаж Культуральная жидкость, Грубодисперсные Барботажные машины Аппараты
 Количественные характеристики диспергирования Е=b ln(L 1/L 2) Е – энергия, необходимая для измельчения вещества закон Кика b – const 1=d. H/d. K 2=SH/SK L 1 и L 2 – начальные и конечные размеры вещества степень диспергирования d. H, d. K– диаметр частиц SН, SК – площадь поверхности VH и VK – объем частиц 3 =VH/VK W=WS+ WD= S+k. V работа диспергирования – величина пропорциональная или равная поверхностному натяжению на границе раздела между дисперсной фазой и дисперсионной средой; S – увеличение площади поверхности раздела фаз в результате диспергирования; V – объем исходного тела до диспергирования; k – коэффициент, эквивалентный работе деформирования единицы объема тела
Количественные характеристики диспергирования Е=b ln(L 1/L 2) Е – энергия, необходимая для измельчения вещества закон Кика b – const 1=d. H/d. K 2=SH/SK L 1 и L 2 – начальные и конечные размеры вещества степень диспергирования d. H, d. K– диаметр частиц SН, SК – площадь поверхности VH и VK – объем частиц 3 =VH/VK W=WS+ WD= S+k. V работа диспергирования – величина пропорциональная или равная поверхностному натяжению на границе раздела между дисперсной фазой и дисперсионной средой; S – увеличение площади поверхности раздела фаз в результате диспергирования; V – объем исходного тела до диспергирования; k – коэффициент, эквивалентный работе деформирования единицы объема тела
 Влияние физико-механических свойств на энергозатраты в производстве муки Работа, затрачиваемая на измельчение: А = А 1+А 2+А 3 где А 1, А 2, А 3 – работа, затрачиваемая на упругие и пластические деформации частиц, на образование новых поверхностей раздела, на деформацию и изнашивание рабочих органов. где К – работа на образование единицы поверхности раздела, F = FK – F – площадь образовавшейся поверхности, n – коэффициент, зависящий от конструктивных и технологических особенностей. Энергетический коэффициент :
Влияние физико-механических свойств на энергозатраты в производстве муки Работа, затрачиваемая на измельчение: А = А 1+А 2+А 3 где А 1, А 2, А 3 – работа, затрачиваемая на упругие и пластические деформации частиц, на образование новых поверхностей раздела, на деформацию и изнашивание рабочих органов. где К – работа на образование единицы поверхности раздела, F = FK – F – площадь образовавшейся поверхности, n – коэффициент, зависящий от конструктивных и технологических особенностей. Энергетический коэффициент :
 Гидротермическая обработка зерна n n ГТО заключается в искусственном воздействии на зерно воды и тепла с использованием фактора времени с учетом энтальпии и относительной влажности окружающей среды. В результате ГТО изменяются структурномеханические свойства оболочек и эндосперма, а также ослабевают связи между оболочкой и эндоспермом. Режим ГТО и степень изменения первоначальных свойств зависит от сорта и типа зерна, цели переработки (в муку или крупу). Цель ГТО при переработке зерна в муку – снижение прочности эндосперма, в крупу – снижение прочности оболочек.
Гидротермическая обработка зерна n n ГТО заключается в искусственном воздействии на зерно воды и тепла с использованием фактора времени с учетом энтальпии и относительной влажности окружающей среды. В результате ГТО изменяются структурномеханические свойства оболочек и эндосперма, а также ослабевают связи между оболочкой и эндоспермом. Режим ГТО и степень изменения первоначальных свойств зависит от сорта и типа зерна, цели переработки (в муку или крупу). Цель ГТО при переработке зерна в муку – снижение прочности эндосперма, в крупу – снижение прочности оболочек.
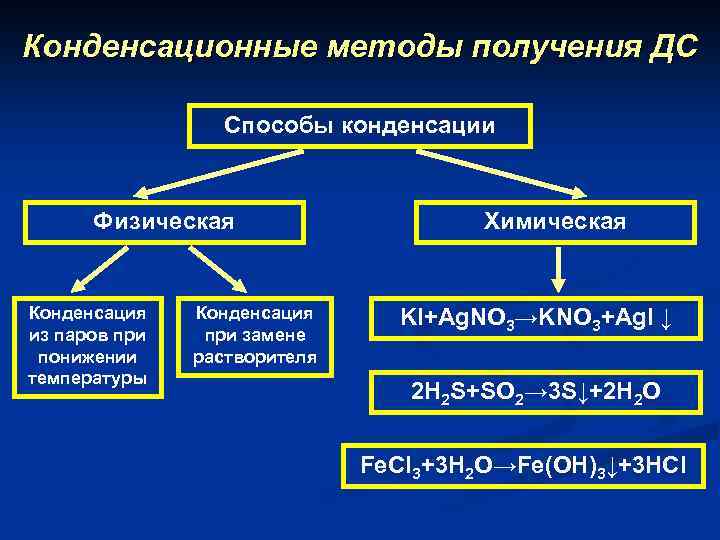 Конденсационные методы получения ДС Cпособы конденсации Физическая Конденсация из паров при понижении температуры Конденсация при замене растворителя Химическая KI+Ag. NO 3→KNO 3+Agl ↓ 2 H 2 S+SO 2→ 3 S↓+2 H 2 O Fe. Cl 3+3 H 2 O→Fe(OH)3↓+3 HCl
Конденсационные методы получения ДС Cпособы конденсации Физическая Конденсация из паров при понижении температуры Конденсация при замене растворителя Химическая KI+Ag. NO 3→KNO 3+Agl ↓ 2 H 2 S+SO 2→ 3 S↓+2 H 2 O Fe. Cl 3+3 H 2 O→Fe(OH)3↓+3 HCl
 Количественные характеристики конденсации Ж=CП/CS П= p П/ p S ln кр= – степень пересыщения для раствора и пара; p. П, СП – давление пересыщенного пара и концентрация вещества в пересыщенном растворе p. S – равновесное давление насыщенного пара над плоской поверхностью; СS – равновесная концентрация вещества в растворе 2 V М rкр. RT – поверхностное натяжение; VМ – молярный объем; rкр – критический радиус зародыша; R – универсальная газовая постоянная; T – температура, К Основной закон дисперсологии Д=К/СТ rкр= 2 V М RT ln(CП/СS) С – концентрация дисперсной фазы К – константа (К=4, 65 105) T – температура, К
Количественные характеристики конденсации Ж=CП/CS П= p П/ p S ln кр= – степень пересыщения для раствора и пара; p. П, СП – давление пересыщенного пара и концентрация вещества в пересыщенном растворе p. S – равновесное давление насыщенного пара над плоской поверхностью; СS – равновесная концентрация вещества в растворе 2 V М rкр. RT – поверхностное натяжение; VМ – молярный объем; rкр – критический радиус зародыша; R – универсальная газовая постоянная; T – температура, К Основной закон дисперсологии Д=К/СТ rкр= 2 V М RT ln(CП/СS) С – концентрация дисперсной фазы К – константа (К=4, 65 105) T – температура, К
 Основы термодинамики и кинетики конденсации А=- Gкргом =1/3σ∆SКР Для сферической частицы Gкр=4/3 rкр2 Gкргет=0, 25(1 - rкр= 2 V M ln кр. RT Gкргом= соs )2(2+cos ) Gкргом Скорость зарождения центров конденсации I 1=A 1 exp[- G/RT] 16 3 VM 2 3 ln 2 кр. R 2 T 2 rкргом=rкргет Gкргет< Gкргом Скорость транспортировки вещества I 2=A 2 exp[-Е /RT] V=I 1 I 2= I 0 exp[-Gкр/КT]
Основы термодинамики и кинетики конденсации А=- Gкргом =1/3σ∆SКР Для сферической частицы Gкр=4/3 rкр2 Gкргет=0, 25(1 - rкр= 2 V M ln кр. RT Gкргом= соs )2(2+cos ) Gкргом Скорость зарождения центров конденсации I 1=A 1 exp[- G/RT] 16 3 VM 2 3 ln 2 кр. R 2 T 2 rкргом=rкргет Gкргет< Gкргом Скорость транспортировки вещества I 2=A 2 exp[-Е /RT] V=I 1 I 2= I 0 exp[-Gкр/КT]
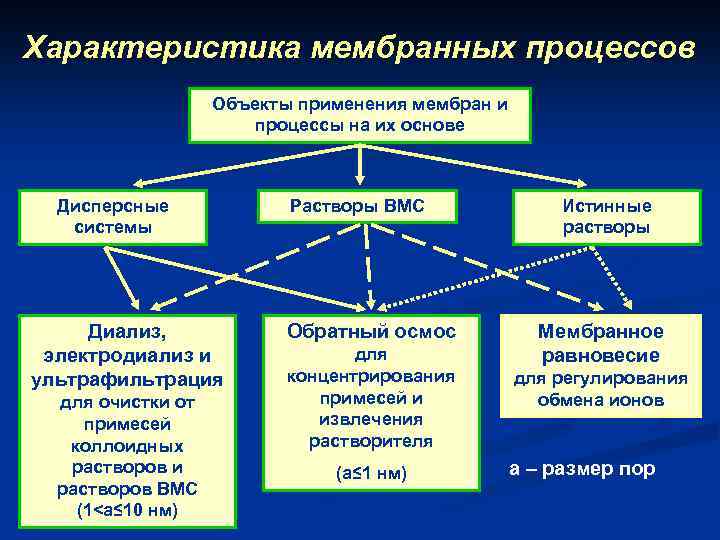 Характеристика мембранных процессов Объекты применения мембран и процессы на их основе Дисперсные системы Диализ, электродиализ и ультрафильтрация для очистки от примесей коллоидных растворов и растворов ВМС (1
Характеристика мембранных процессов Объекты применения мембран и процессы на их основе Дисперсные системы Диализ, электродиализ и ультрафильтрация для очистки от примесей коллоидных растворов и растворов ВМС (1
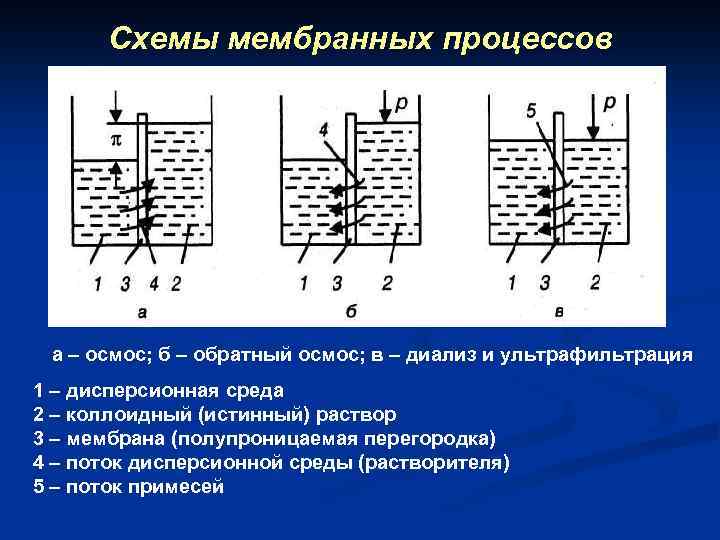 Схемы мембранных процессов а – осмос; б – обратный осмос; в – диализ и ультрафильтрация 1 – дисперсионная среда 2 – коллоидный (истинный) раствор 3 – мембрана (полупроницаемая перегородка) 4 – поток дисперсионной среды (растворителя) 5 – поток примесей
Схемы мембранных процессов а – осмос; б – обратный осмос; в – диализ и ультрафильтрация 1 – дисперсионная среда 2 – коллоидный (истинный) раствор 3 – мембрана (полупроницаемая перегородка) 4 – поток дисперсионной среды (растворителя) 5 – поток примесей
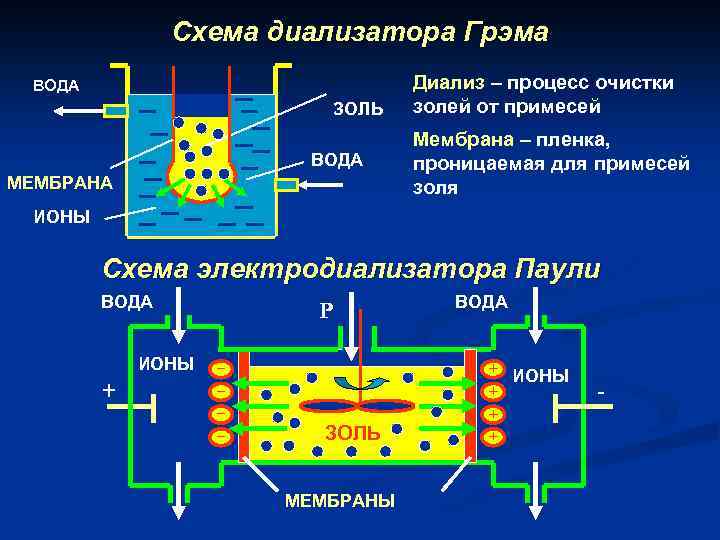 Схема диализатора Грэма ВОДА ЗОЛЬ ВОДА МЕМБРАНА Диализ – процесс очистки золей от примесей Мембрана – пленка, проницаемая для примесей золя ИОНЫ Схема электродиализатора Паули ВОДА ИОНЫ + Р _ _ ЗОЛЬ МЕМБРАНЫ ВОДА + ИОНЫ + + + -
Схема диализатора Грэма ВОДА ЗОЛЬ ВОДА МЕМБРАНА Диализ – процесс очистки золей от примесей Мембрана – пленка, проницаемая для примесей золя ИОНЫ Схема электродиализатора Паули ВОДА ИОНЫ + Р _ _ ЗОЛЬ МЕМБРАНЫ ВОДА + ИОНЫ + + + -
 Количественные характеристики мембранных процессов W=-d. C/d =SDдиф. (С 1 -С 1)/V Уравнение скорости диализа i=Dдиф. (С 1 -С 1)K /L Уравнение диффузии примесей через мембрану d. V/d =K PS/ L Уравнение фильтрации G=V/(S P) Уравнение проницаемости мембраны =(C 1 -C 2/C 1) 100% Уравнение селективности мембраны S – площадь мембраны V – объем фильтруемой системы С 1 и С 2 – начальная и конечная концентрация системы Dдиф. – коэффициент диффузии i – диффузионный поток вещества K – адсорбционная константа взаимодействия диффундирующего вещества с мембраной L – толщина мембраны Р – дополнительное давление – вязкость системы – время фильтрации
Количественные характеристики мембранных процессов W=-d. C/d =SDдиф. (С 1 -С 1)/V Уравнение скорости диализа i=Dдиф. (С 1 -С 1)K /L Уравнение диффузии примесей через мембрану d. V/d =K PS/ L Уравнение фильтрации G=V/(S P) Уравнение проницаемости мембраны =(C 1 -C 2/C 1) 100% Уравнение селективности мембраны S – площадь мембраны V – объем фильтруемой системы С 1 и С 2 – начальная и конечная концентрация системы Dдиф. – коэффициент диффузии i – диффузионный поток вещества K – адсорбционная константа взаимодействия диффундирующего вещества с мембраной L – толщина мембраны Р – дополнительное давление – вязкость системы – время фильтрации
![Схема мембранного равновесия Доннана [Kат Z+]=C 1 [Na+]=C Na+ 2 [Kат. Z+]=C 1 [Na+]=X Схема мембранного равновесия Доннана [Kат Z+]=C 1 [Na+]=C Na+ 2 [Kат. Z+]=C 1 [Na+]=X](https://present5.com/presentation/102472334_194529794/image-20.jpg) Схема мембранного равновесия Доннана [Kат Z+]=C 1 [Na+]=C Na+ 2 [Kат. Z+]=C 1 [Na+]=X Cl- [Cl-]=ZC 1 [Cl-]=C 2 [Cl-]=ZC 1+X Na+ Cl- Начальное состояние [Na+]=C 2 -X Cl- [Cl-]=C 2 -X Na+ Равновесное состояние
Схема мембранного равновесия Доннана [Kат Z+]=C 1 [Na+]=C Na+ 2 [Kат. Z+]=C 1 [Na+]=X Cl- [Cl-]=ZC 1 [Cl-]=C 2 [Cl-]=ZC 1+X Na+ Cl- Начальное состояние [Na+]=C 2 -X Cl- [Cl-]=C 2 -X Na+ Равновесное состояние
 Вопросы к лекции 8 1. 2. 3. 4. 5. 6. 7. 8. 9. 10. Какими методами получают дисперсные системы? Перечислите наиболее распространенные технологические приемы диспергирования. Какими количественными характеристиками описывают процесс диспергирования? Какими способами можно получить дисперсные системы из гомогенных систем? Чем отличаются процессы гомогенной и гетерогенной конденсации? Какие методы используют для очистки дисперсных систем? Дайте определения процессам осмоса, обратного осмоса, диализа, электродиализа. Какими количественными показателями характеризуются мембранные процессы? От каких факторов зависит интенсивность мембранных процессов? Приведите примеры мембранных процессов в биотехнологии.
Вопросы к лекции 8 1. 2. 3. 4. 5. 6. 7. 8. 9. 10. Какими методами получают дисперсные системы? Перечислите наиболее распространенные технологические приемы диспергирования. Какими количественными характеристиками описывают процесс диспергирования? Какими способами можно получить дисперсные системы из гомогенных систем? Чем отличаются процессы гомогенной и гетерогенной конденсации? Какие методы используют для очистки дисперсных систем? Дайте определения процессам осмоса, обратного осмоса, диализа, электродиализа. Какими количественными показателями характеризуются мембранные процессы? От каких факторов зависит интенсивность мембранных процессов? Приведите примеры мембранных процессов в биотехнологии.


