PYaiDS_2010_L_6.ppt
- Количество слайдов: 15
 ПОВЕРХНОСТНЫЕ ЯВЛЕНИЯ И ДИСПЕРСНЫЕ СИСТЕМЫ ЛЕКЦИЯ 6
ПОВЕРХНОСТНЫЕ ЯВЛЕНИЯ И ДИСПЕРСНЫЕ СИСТЕМЫ ЛЕКЦИЯ 6
 Содержание лекции 1. Молекулярная адсорбция из растворов. 2. Хроматография. 3. Адсорбция электролитов (ионная адсорбция). 4. Ионообменная адсорбция.
Содержание лекции 1. Молекулярная адсорбция из растворов. 2. Хроматография. 3. Адсорбция электролитов (ионная адсорбция). 4. Ионообменная адсорбция.
 Закономерности процесса молекулярной адсорбции из растворов n n n n Молекулярная адсорбция описывается 5 типами изотерм: Ленгмюра, БЭТ, совместной адсорбции растворенного вещества и растворителя, адсорбции и абсорбции. Процесс является более продолжительным, чем в случае адсорбции газов, так как замедлена стадия диффузии (особенно для крупных молекул на микропористых адсорбентах). Процесс идет интенсивнее при низких температурах в связи с уменьшением десорбции. На полярном адсорбенте лучше адсорбируется полярный адсорбтив, а на неполярном – неполярный. Адсорбция растворенного вещества происходит интенсивнее, если растворитель имеет большую величину поверхностного натяжения. Чем лучше растворимость адсорбтива, тем хуже он адсорбируется. Адсорбция ПАВ всегда идет в сторону выравнивания полярностей фаз адсорбента и жидкой среды и тем сильнее, чем больше первоначальная разность полярностей.
Закономерности процесса молекулярной адсорбции из растворов n n n n Молекулярная адсорбция описывается 5 типами изотерм: Ленгмюра, БЭТ, совместной адсорбции растворенного вещества и растворителя, адсорбции и абсорбции. Процесс является более продолжительным, чем в случае адсорбции газов, так как замедлена стадия диффузии (особенно для крупных молекул на микропористых адсорбентах). Процесс идет интенсивнее при низких температурах в связи с уменьшением десорбции. На полярном адсорбенте лучше адсорбируется полярный адсорбтив, а на неполярном – неполярный. Адсорбция растворенного вещества происходит интенсивнее, если растворитель имеет большую величину поверхностного натяжения. Чем лучше растворимость адсорбтива, тем хуже он адсорбируется. Адсорбция ПАВ всегда идет в сторону выравнивания полярностей фаз адсорбента и жидкой среды и тем сильнее, чем больше первоначальная разность полярностей.
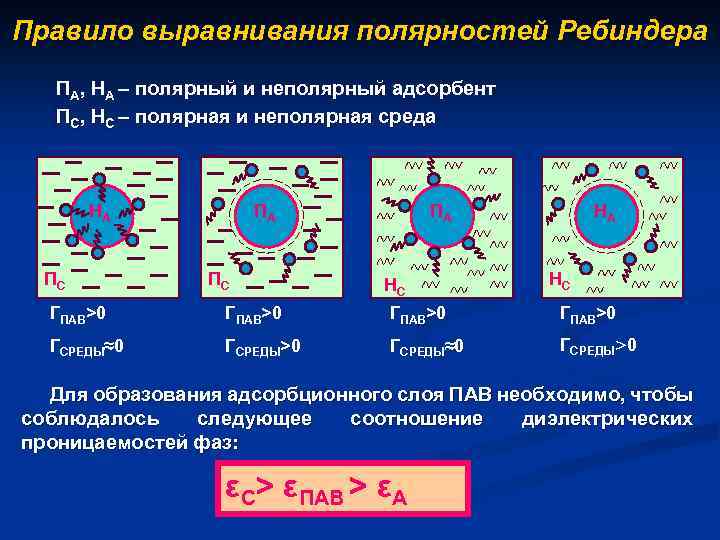 Правило выравнивания полярностей Ребиндера ПА, НА – полярный и неполярный адсорбент ПС, НС – полярная и неполярная среда НА ПС ПА НС НА НС ГПАВ>0 ГСРЕДЫ≈0 ГСРЕДЫ>0 Для образования адсорбционного слоя ПАВ необходимо, чтобы соблюдалось следующее соотношение диэлектрических проницаемостей фаз: εС> εПАВ > εА
Правило выравнивания полярностей Ребиндера ПА, НА – полярный и неполярный адсорбент ПС, НС – полярная и неполярная среда НА ПС ПА НС НА НС ГПАВ>0 ГСРЕДЫ≈0 ГСРЕДЫ>0 Для образования адсорбционного слоя ПАВ необходимо, чтобы соблюдалось следующее соотношение диэлектрических проницаемостей фаз: εС> εПАВ > εА
 Частные случаи (правила) молекулярной адсорбции n n Непредельные органические соединения адсорбируются лучше, чем предельные. Ароматические соединения адсорбируются лучше, чем алифитические. Для ферментов адсорбционная способность возрастает с увеличением молекулярной массы. Для гомологического ряда органических кислот адсорбционная способность возрастает в 3 -3. 5 раза при увеличении длины углеводородной цепи на СН 2 группу.
Частные случаи (правила) молекулярной адсорбции n n Непредельные органические соединения адсорбируются лучше, чем предельные. Ароматические соединения адсорбируются лучше, чем алифитические. Для ферментов адсорбционная способность возрастает с увеличением молекулярной массы. Для гомологического ряда органических кислот адсорбционная способность возрастает в 3 -3. 5 раза при увеличении длины углеводородной цепи на СН 2 группу.
 Хроматография n n Хроматография – метод разделения и анализа многокомпонентных смесей, основанный на их различной адсорбционной способности (М. С. Цвет 1903 г. ) Чем больше концентрация компонента в смеси, тем в большем количестве он будет адсорбироваться. Чем выше адсорбционная способность компонента, тем в большем количестве он будет адсорбироваться. Если вещество в чистом виде обладает низкой адсорбционной способностью по отношению к выбранному адсорбенту, то оно будет плохо адсорбироваться и из многокомпонентной смеси.
Хроматография n n Хроматография – метод разделения и анализа многокомпонентных смесей, основанный на их различной адсорбционной способности (М. С. Цвет 1903 г. ) Чем больше концентрация компонента в смеси, тем в большем количестве он будет адсорбироваться. Чем выше адсорбционная способность компонента, тем в большем количестве он будет адсорбироваться. Если вещество в чистом виде обладает низкой адсорбционной способностью по отношению к выбранному адсорбенту, то оно будет плохо адсорбироваться и из многокомпонентной смеси.
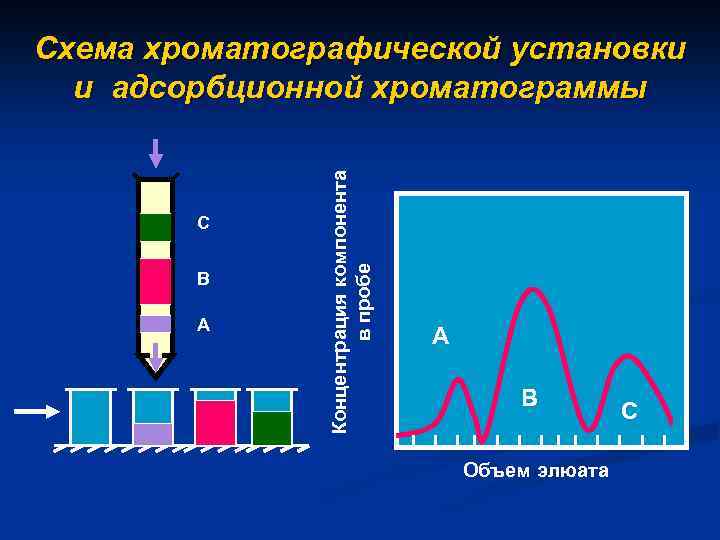 С В А Концентрация компонента в пробе Схема хроматографической установки и адсорбционной хроматограммы А В Объем элюата С
С В А Концентрация компонента в пробе Схема хроматографической установки и адсорбционной хроматограммы А В Объем элюата С
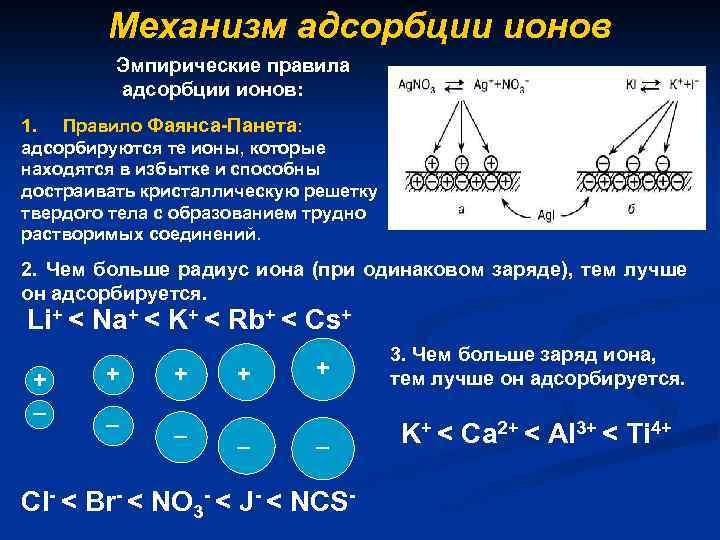 Механизм адсорбции ионов Эмпирические правила адсорбции ионов: 1. Правило Фаянса-Панета: адсорбируются те ионы, которые находятся в избытке и способны достраивать кристаллическую решетку твердого тела с образованием трудно растворимых соединений. 2. Чем больше радиус иона (при одинаковом заряде), тем лучше он адсорбируется. Li+ < Na+ < K+ < Rb+ < Cs+ + _ + + 3. Чем больше заряд иона, тем лучше он адсорбируется. _ _ K+ < Ca 2+ < Al 3+ < Ti 4+ Cl- < Br- < NO 3 - < J- < NCS-
Механизм адсорбции ионов Эмпирические правила адсорбции ионов: 1. Правило Фаянса-Панета: адсорбируются те ионы, которые находятся в избытке и способны достраивать кристаллическую решетку твердого тела с образованием трудно растворимых соединений. 2. Чем больше радиус иона (при одинаковом заряде), тем лучше он адсорбируется. Li+ < Na+ < K+ < Rb+ < Cs+ + _ + + 3. Чем больше заряд иона, тем лучше он адсорбируется. _ _ K+ < Ca 2+ < Al 3+ < Ti 4+ Cl- < Br- < NO 3 - < J- < NCS-
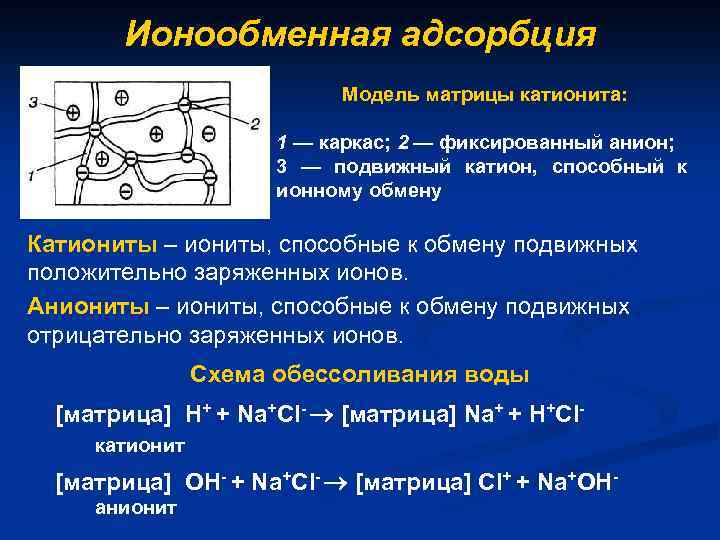 Ионообменная адсорбция Модель матрицы катионита: 1 — каркас; 2 — фиксированный анион; 3 — подвижный катион, способный к ионному обмену Катиониты – иониты, способные к обмену подвижных положительно заряженных ионов. Аниониты – иониты, способные к обмену подвижных отрицательно заряженных ионов. Схема обессоливания воды [матрица] Н+ + Na+Cl- [матрица] Na+ + H+Clкатионит [матрица] OН- + Na+Cl- [матрица] Cl+ + Na+OHанионит
Ионообменная адсорбция Модель матрицы катионита: 1 — каркас; 2 — фиксированный анион; 3 — подвижный катион, способный к ионному обмену Катиониты – иониты, способные к обмену подвижных положительно заряженных ионов. Аниониты – иониты, способные к обмену подвижных отрицательно заряженных ионов. Схема обессоливания воды [матрица] Н+ + Na+Cl- [матрица] Na+ + H+Clкатионит [матрица] OН- + Na+Cl- [матрица] Cl+ + Na+OHанионит
 Кинетика ионообменной адсорбции 1. 2. 3. 4. 5. Диффузия адсорбирующихся ионов из раствора к поверхности ионита Диффузия ионов адсорбата внутри гранул ионита Обмен ионов на границе раздела фаз Диффузия замещенных ионов внутри гранул ионита Диффузия противоионов в объем раствора. Коэффициент внешней диффузии 10 -9 м 2/с Коэффициент внутренней диффузии 10 -15 -10 -10 м 2/с
Кинетика ионообменной адсорбции 1. 2. 3. 4. 5. Диффузия адсорбирующихся ионов из раствора к поверхности ионита Диффузия ионов адсорбата внутри гранул ионита Обмен ионов на границе раздела фаз Диффузия замещенных ионов внутри гранул ионита Диффузия противоионов в объем раствора. Коэффициент внешней диффузии 10 -9 м 2/с Коэффициент внутренней диффузии 10 -15 -10 -10 м 2/с
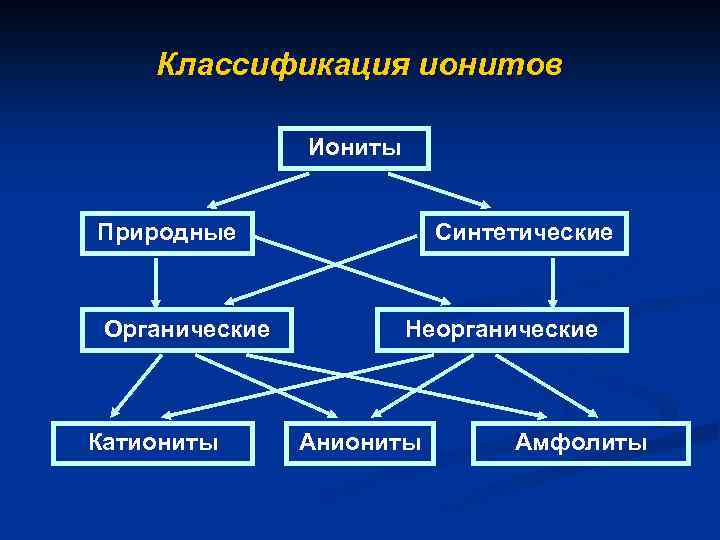 Классификация ионитов Иониты Природные Органические Катиониты Синтетические Неорганические Аниониты Амфолиты
Классификация ионитов Иониты Природные Органические Катиониты Синтетические Неорганические Аниониты Амфолиты
 Свойства ионитов Ионообменная емкость характеризует способность ионита обменивать противоионы. Статическая емкость – общее количество ионогенных групп, приходящихся на единицу массы ионита. Динамическая емкость – количество ионогенных групп, участвующих в реакциях ионного обмена при определенных условиях. n Кислотно-основные свойства определяют способность к обмену ионов разного знака. Выделяют 5 групп: сильнокислотные катиониты (-SO 3 H), слабокислотные катиониты (-ОН; -СООН; -Si. OH), слабоосновные аниониты (-NH 2; =NH), сильноосновные аниониты ([-N(CH 3)3]+Cl-; -PO(OH)3), полифункциональные иониты (амфолиты). n Селективность – сродство ионита к ионам адсорбтива. Определяется их зарядом, степенью гидратированности и адсорбционной активностью. n Набухаемость – способность ионита поглощать воду. Определяется как отношение разностей объемов (масс) набухшего и воздушно-сухого ионита к объему (массе) воздушно-сухого ионита. n Химическая стойкость оценивается по изменению обменной емкости после обработки ионита тем или иным реагентом. Практическое значение имеет стойкость ионита к щелочам, кислотам, окислителям (моющие и дезинфицирующие средства). n Механическая прочность оценивается по изменению гранулометрического состава ионита после определенного числа циклов обработки. n
Свойства ионитов Ионообменная емкость характеризует способность ионита обменивать противоионы. Статическая емкость – общее количество ионогенных групп, приходящихся на единицу массы ионита. Динамическая емкость – количество ионогенных групп, участвующих в реакциях ионного обмена при определенных условиях. n Кислотно-основные свойства определяют способность к обмену ионов разного знака. Выделяют 5 групп: сильнокислотные катиониты (-SO 3 H), слабокислотные катиониты (-ОН; -СООН; -Si. OH), слабоосновные аниониты (-NH 2; =NH), сильноосновные аниониты ([-N(CH 3)3]+Cl-; -PO(OH)3), полифункциональные иониты (амфолиты). n Селективность – сродство ионита к ионам адсорбтива. Определяется их зарядом, степенью гидратированности и адсорбционной активностью. n Набухаемость – способность ионита поглощать воду. Определяется как отношение разностей объемов (масс) набухшего и воздушно-сухого ионита к объему (массе) воздушно-сухого ионита. n Химическая стойкость оценивается по изменению обменной емкости после обработки ионита тем или иным реагентом. Практическое значение имеет стойкость ионита к щелочам, кислотам, окислителям (моющие и дезинфицирующие средства). n Механическая прочность оценивается по изменению гранулометрического состава ионита после определенного числа циклов обработки. n
 Количественные характеристики ионообменной адсорбции К 1, 2 = С 11/Z 1 • C 21/Z 2 С 21/Z 2 • C 11/Z 1 ПОЕ = n m Сi – количество поглощенных ионов Сi – концентрация ионов в растворе Z – заряд ионов n – число грамм–эквивалентов поглощенных ионов m – масса ионита Вещество Торф Значение ПОЕ, г-экв. /кг 0, 6 - 1 Чернозем 0, 6 – 0, 8 Подзол, суглинок 0, 05 - 0, 2
Количественные характеристики ионообменной адсорбции К 1, 2 = С 11/Z 1 • C 21/Z 2 С 21/Z 2 • C 11/Z 1 ПОЕ = n m Сi – количество поглощенных ионов Сi – концентрация ионов в растворе Z – заряд ионов n – число грамм–эквивалентов поглощенных ионов m – масса ионита Вещество Торф Значение ПОЕ, г-экв. /кг 0, 6 - 1 Чернозем 0, 6 – 0, 8 Подзол, суглинок 0, 05 - 0, 2
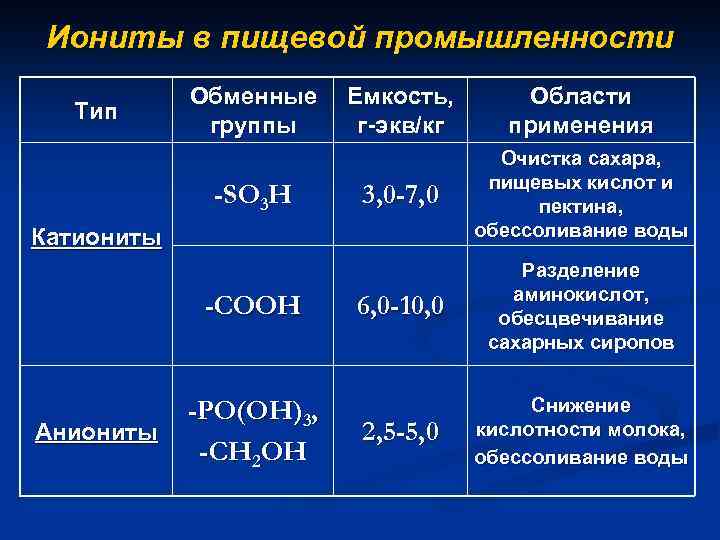 Иониты в пищевой промышленности Тип Обменные Емкость, группы г-экв/кг -SO 3 H 3, 0 -7, 0 Очистка сахара, пищевых кислот и пектина, обессоливание воды 6, 0 -10, 0 Разделение аминокислот, обесцвечивание сахарных сиропов 2, 5 -5, 0 Снижение кислотности молока, обессоливание воды Катиониты -COOH Аниониты -PO(OH)3, -CH 2 OH Области применения
Иониты в пищевой промышленности Тип Обменные Емкость, группы г-экв/кг -SO 3 H 3, 0 -7, 0 Очистка сахара, пищевых кислот и пектина, обессоливание воды 6, 0 -10, 0 Разделение аминокислот, обесцвечивание сахарных сиропов 2, 5 -5, 0 Снижение кислотности молока, обессоливание воды Катиониты -COOH Аниониты -PO(OH)3, -CH 2 OH Области применения
 Вопросы к лекции 6 1. 2. 3. 4. 5. 6. 7. 8. 9. 10. Что общего и чем отличаются различные виды адсорбции на границе раствора с твердым адсорбентом? В каком случае ПАВ адсорбируются на межфазной границе жидкость - твердое тело? Почему при некоторых пищевых отравлениях рекомендуют принимать таблетки активированного угля? На каком принципе основан хроматографический метод анализа? От каких факторов зависит процесс адсорбции электролитов? В чем заключается особенность ионообменной адсорбции? Что представляют собой катиониты и аниониты? Напишите формулу для определения ПОЕ ионита. Каким образом можно определить константу ионного обмена? Приведите примеры использования ионообменной адсорбции в пищевой промышленности?
Вопросы к лекции 6 1. 2. 3. 4. 5. 6. 7. 8. 9. 10. Что общего и чем отличаются различные виды адсорбции на границе раствора с твердым адсорбентом? В каком случае ПАВ адсорбируются на межфазной границе жидкость - твердое тело? Почему при некоторых пищевых отравлениях рекомендуют принимать таблетки активированного угля? На каком принципе основан хроматографический метод анализа? От каких факторов зависит процесс адсорбции электролитов? В чем заключается особенность ионообменной адсорбции? Что представляют собой катиониты и аниониты? Напишите формулу для определения ПОЕ ионита. Каким образом можно определить константу ионного обмена? Приведите примеры использования ионообменной адсорбции в пищевой промышленности?


