PYaiDS_2010_L_4.ppt
- Количество слайдов: 15
 ПОВЕРХНОСТНЫЕ ЯВЛЕНИЯ И ДИСПЕРСНЫЕ СИСТЕМЫ ЛЕКЦИЯ 4
ПОВЕРХНОСТНЫЕ ЯВЛЕНИЯ И ДИСПЕРСНЫЕ СИСТЕМЫ ЛЕКЦИЯ 4
 Содержание лекции 1. Адсорбция как поверхностное явление. 2. Виды адсорбции. 3. Количественные характеристики адсорбции. Причины адсорбции. 4. Теория мономолекулярной адсорбции. 5. Теория полимолекулярной адсорбции. 6. Обобщенная теория адсорбции БЭТ.
Содержание лекции 1. Адсорбция как поверхностное явление. 2. Виды адсорбции. 3. Количественные характеристики адсорбции. Причины адсорбции. 4. Теория мономолекулярной адсорбции. 5. Теория полимолекулярной адсорбции. 6. Обобщенная теория адсорбции БЭТ.
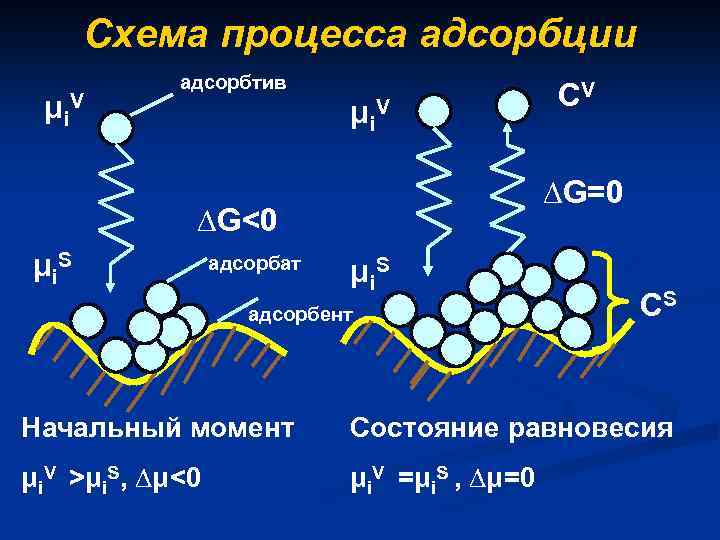 Схема процесса адсорбции μ i. V адсорбтив μ i. V ∆G=0 ∆G<0 μ i. S адсорбат CV μ i. S адсорбент CS Начальный момент Состояние равновесия μi. V >μi. S, ∆μ<0 μi. V =μi. S , ∆μ=0
Схема процесса адсорбции μ i. V адсорбтив μ i. V ∆G=0 ∆G<0 μ i. S адсорбат CV μ i. S адсорбент CS Начальный момент Состояние равновесия μi. V >μi. S, ∆μ<0 μi. V =μi. S , ∆μ=0
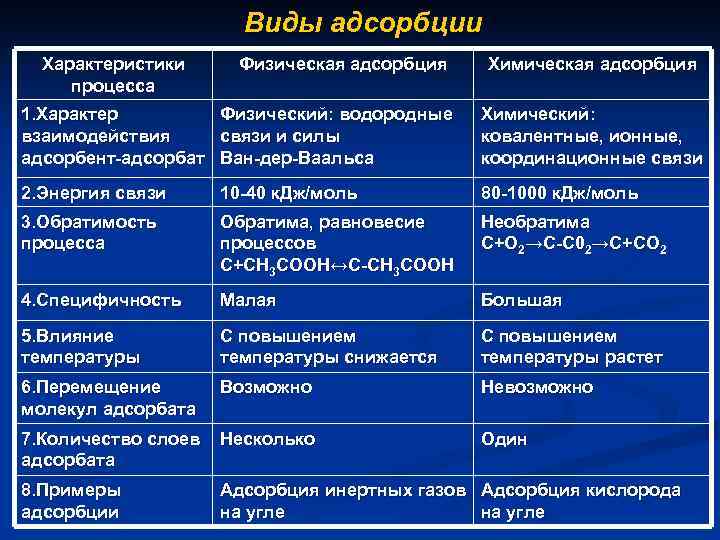 Виды адсорбции Характеристики процесса Физическая адсорбция Химическая адсорбция 1. Характер взаимодействия адсорбент-адсорбат Физический: водородные связи и силы Ван-дер-Ваальса Химический: ковалентные, ионные, координационные связи 2. Энергия связи 10 -40 к. Дж/моль 80 -1000 к. Дж/моль 3. Обратимость процесса Обратима, равновесие процессов С+СН 3 СООН↔С-СН 3 СООН Необратима С+О 2→С-С 02→С+СО 2 4. Специфичность Малая Большая 5. Влияние температуры С повышением температуры снижается С повышением температуры растет 6. Перемещение молекул адсорбата Возможно Невозможно 7. Количество слоев Несколько адсорбата 8. Примеры адсорбции Один Адсорбция инертных газов Адсорбция кислорода на угле
Виды адсорбции Характеристики процесса Физическая адсорбция Химическая адсорбция 1. Характер взаимодействия адсорбент-адсорбат Физический: водородные связи и силы Ван-дер-Ваальса Химический: ковалентные, ионные, координационные связи 2. Энергия связи 10 -40 к. Дж/моль 80 -1000 к. Дж/моль 3. Обратимость процесса Обратима, равновесие процессов С+СН 3 СООН↔С-СН 3 СООН Необратима С+О 2→С-С 02→С+СО 2 4. Специфичность Малая Большая 5. Влияние температуры С повышением температуры снижается С повышением температуры растет 6. Перемещение молекул адсорбата Возможно Невозможно 7. Количество слоев Несколько адсорбата 8. Примеры адсорбции Один Адсорбция инертных газов Адсорбция кислорода на угле
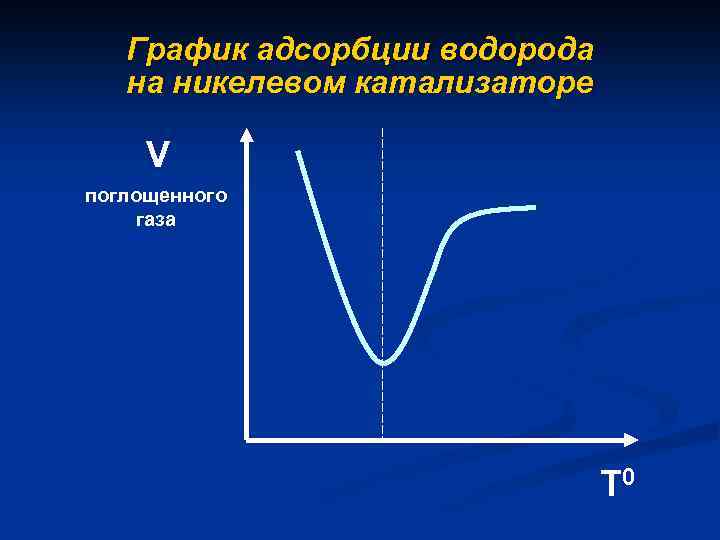 График адсорбции водорода на никелевом катализаторе V поглощенного газа Т 0
График адсорбции водорода на никелевом катализаторе V поглощенного газа Т 0
 Количественные характеристики адсорбции Абсолютная адсорбция А=с. Sh, где С – концентрация адсорбата в Гиббсовская адсорбция Г=А-с·h, С – равновесная концентрация Удельная адсорбция S поверхностном слое, h – толщина слоя адсорбтива, , h – толщина слоя Гi=ni/S или Гi=ni/m , n – избыточное i число молей адсорбата i– го компонента, S - площадь поверхности раздела фаз, m – масса адсорбента Уравнение адсорбции Изотерма адсорбции Г=f(с, Т) или Г=f(р, Т) Г=f(с) или Г=f(р), при Т=const
Количественные характеристики адсорбции Абсолютная адсорбция А=с. Sh, где С – концентрация адсорбата в Гиббсовская адсорбция Г=А-с·h, С – равновесная концентрация Удельная адсорбция S поверхностном слое, h – толщина слоя адсорбтива, , h – толщина слоя Гi=ni/S или Гi=ni/m , n – избыточное i число молей адсорбата i– го компонента, S - площадь поверхности раздела фаз, m – масса адсорбента Уравнение адсорбции Изотерма адсорбции Г=f(с, Т) или Г=f(р, Т) Г=f(с) или Г=f(р), при Т=const
 Фундаментальное уравнение адсорбции Гиббса В условиях равновесия при d. T=0, dp=0, dq=0 n n d. G<∑∆µidni i=1 ∑µidni+σd. S=0 i=1 При неизменных значениях n и S, подставив вместо nS=Г , получим: n n ∑Гi=-dσ/∑dµi i=1 фундаментальное уравнение адсорбции Гиббса Для адсорбции одного компонента: Г=-(с/RT)dσ/dc
Фундаментальное уравнение адсорбции Гиббса В условиях равновесия при d. T=0, dp=0, dq=0 n n d. G<∑∆µidni i=1 ∑µidni+σd. S=0 i=1 При неизменных значениях n и S, подставив вместо nS=Г , получим: n n ∑Гi=-dσ/∑dµi i=1 фундаментальное уравнение адсорбции Гиббса Для адсорбции одного компонента: Г=-(с/RT)dσ/dc
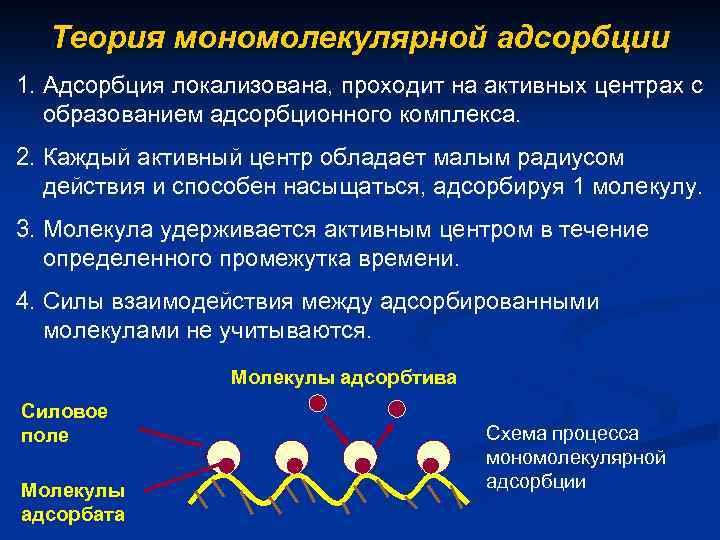 Теория мономолекулярной адсорбции 1. Адсорбция локализована, проходит на активных центрах с образованием адсорбционного комплекса. 2. Каждый активный центр обладает малым радиусом действия и способен насыщаться, адсорбируя 1 молекулу. 3. Молекула удерживается активным центром в течение определенного промежутка времени. 4. Силы взаимодействия между адсорбированными молекулами не учитываются. Молекулы адсорбтива Силовое поле Молекулы адсорбата Схема процесса мономолекулярной адсорбции
Теория мономолекулярной адсорбции 1. Адсорбция локализована, проходит на активных центрах с образованием адсорбционного комплекса. 2. Каждый активный центр обладает малым радиусом действия и способен насыщаться, адсорбируя 1 молекулу. 3. Молекула удерживается активным центром в течение определенного промежутка времени. 4. Силы взаимодействия между адсорбированными молекулами не учитываются. Молекулы адсорбтива Силовое поле Молекулы адсорбата Схема процесса мономолекулярной адсорбции
 Уравнение изотермы адсорбции Пусть поверхность имеет площадь равную 1. Θ – занятая доля поверхности, (1 - Θ) – свободная доля поверхности Скорость адсорбции Скорость десорбции Va=dΘ/dt=k 1 c(1 -Θ) Так как С - концентрация адсорбтива Vд=-dΘ/dt=k 2Θ При равновесии: Vа=Vд Θ=Г/Гmax Θ=k 1 с/(k 2+k 1 c) заполнении поверхности или Г=Гmax(c/(c+a)) Гmax – максимальная адсорбция при полном k 1, k 2 – константы скорости Θ=с/(а+с) а=k 1/k 2 - уравнение изотермы адсорбции Ленгмюра
Уравнение изотермы адсорбции Пусть поверхность имеет площадь равную 1. Θ – занятая доля поверхности, (1 - Θ) – свободная доля поверхности Скорость адсорбции Скорость десорбции Va=dΘ/dt=k 1 c(1 -Θ) Так как С - концентрация адсорбтива Vд=-dΘ/dt=k 2Θ При равновесии: Vа=Vд Θ=Г/Гmax Θ=k 1 с/(k 2+k 1 c) заполнении поверхности или Г=Гmax(c/(c+a)) Гmax – максимальная адсорбция при полном k 1, k 2 – константы скорости Θ=с/(а+с) а=k 1/k 2 - уравнение изотермы адсорбции Ленгмюра
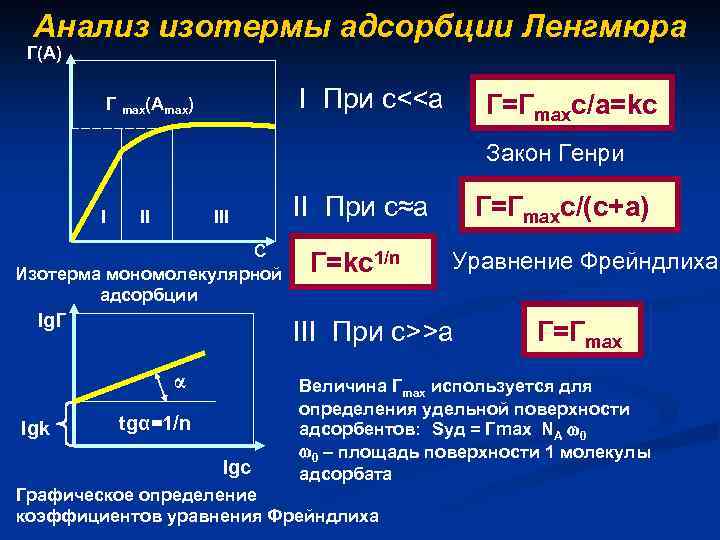 Анализ изотермы адсорбции Ленгмюра Г(А) I При с<>a α lgk Г=kc 1/n Г=Гmaxc/(c+a) tgα=1/n lgc Г=Гmax Величина Гmax используется для определения удельной поверхности адсорбентов: Sуд = Гmax NA 0 0 – площадь поверхности 1 молекулы адсорбата Графическое определение коэффициентов уравнения Фрейндлиха
Анализ изотермы адсорбции Ленгмюра Г(А) I При с<>a α lgk Г=kc 1/n Г=Гmaxc/(c+a) tgα=1/n lgc Г=Гmax Величина Гmax используется для определения удельной поверхности адсорбентов: Sуд = Гmax NA 0 0 – площадь поверхности 1 молекулы адсорбата Графическое определение коэффициентов уравнения Фрейндлиха
 Теория полимолекулярной адсорбции 1. Адсорбция не локализована и обусловлена физическими силами 2. На поверхности нет активных центров, а действует непрерывное силовое поле, распространяющееся на значительное расстояние 3. Адсорбционный слой полимолекулярен, его плотность убывает по нормали от поверхности 4. Адсорбционные силы не зависят от температуры
Теория полимолекулярной адсорбции 1. Адсорбция не локализована и обусловлена физическими силами 2. На поверхности нет активных центров, а действует непрерывное силовое поле, распространяющееся на значительное расстояние 3. Адсорбционный слой полимолекулярен, его плотность убывает по нормали от поверхности 4. Адсорбционные силы не зависят от температуры
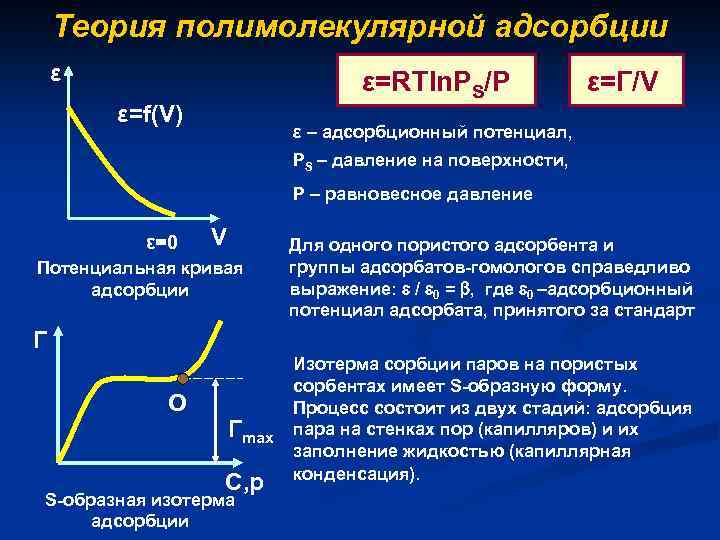 Теория полимолекулярной адсорбции ε ε=RTln. PS/P ε=f(V) ε=Г/V ε – адсорбционный потенциал, PS – давление на поверхности, Р – равновесное давление ε=0 V Потенциальная кривая адсорбции Для одного пористого адсорбента и группы адсорбатов-гомологов справедливо выражение: / 0 = , где 0 –адсорбционный потенциал адсорбата, принятого за стандарт Г О Гmax С, р S-образная изотерма адсорбции Изотерма сорбции паров на пористых сорбентах имеет S-образную форму. Процесс состоит из двух стадий: адсорбция пара на стенках пор (капилляров) и их заполнение жидкостью (капиллярная конденсация).
Теория полимолекулярной адсорбции ε ε=RTln. PS/P ε=f(V) ε=Г/V ε – адсорбционный потенциал, PS – давление на поверхности, Р – равновесное давление ε=0 V Потенциальная кривая адсорбции Для одного пористого адсорбента и группы адсорбатов-гомологов справедливо выражение: / 0 = , где 0 –адсорбционный потенциал адсорбата, принятого за стандарт Г О Гmax С, р S-образная изотерма адсорбции Изотерма сорбции паров на пористых сорбентах имеет S-образную форму. Процесс состоит из двух стадий: адсорбция пара на стенках пор (капилляров) и их заполнение жидкостью (капиллярная конденсация).
 Обобщенная теория адсорбции БЭТ (Брунауэра, Эммета, Теллера) 1. 2. 3. 4. На поверхности адсорбента имеется определенное число равных в энергетическом отношении активных центров. Каждая молекула первого слоя представляет активный центр для молекул второго, что приводит к образованию второго, третьего и т. д. слоев. Построение последующих слоев возможно при незаполненном первом. Взаимодействием соседних адсорбированных молекул в рамках одного слоя пренебрегают.
Обобщенная теория адсорбции БЭТ (Брунауэра, Эммета, Теллера) 1. 2. 3. 4. На поверхности адсорбента имеется определенное число равных в энергетическом отношении активных центров. Каждая молекула первого слоя представляет активный центр для молекул второго, что приводит к образованию второго, третьего и т. д. слоев. Построение последующих слоев возможно при незаполненном первом. Взаимодействием соседних адсорбированных молекул в рамках одного слоя пренебрегают.
![Уравнение теории БЭТ Г=Гmax C(р/р. S) (1 -(р/р. S))[1+(c-1)(р/р. S)] р (р. S) – Уравнение теории БЭТ Г=Гmax C(р/р. S) (1 -(р/р. S))[1+(c-1)(р/р. S)] р (р. S) –](https://present5.com/presentation/102472334_194529362/image-14.jpg) Уравнение теории БЭТ Г=Гmax C(р/р. S) (1 -(р/р. S))[1+(c-1)(р/р. S)] р (р. S) – давление пара адсорбтива в объеме (в поверхностном слое) при данной температуре С=kp/k. L kp=ka/kд – равновесная константа адсорбции k. L=1/p 0 – константа конденсации пара
Уравнение теории БЭТ Г=Гmax C(р/р. S) (1 -(р/р. S))[1+(c-1)(р/р. S)] р (р. S) – давление пара адсорбтива в объеме (в поверхностном слое) при данной температуре С=kp/k. L kp=ka/kд – равновесная константа адсорбции k. L=1/p 0 – константа конденсации пара
 Вопросы к лекции 4 1. Дайте определение процессам адсорбции и десорбции. Какие виды адсорбции Вы знаете? 2. Приведите примеры адсорбционных процессов. 3. Что называют адсорбатом, адсорбтивом, адсорбентом? 4. Назовите количественные характеристики процесса адсорбции. 5. Что такое изотерма адсорбции? 6. Какие величины связывает между собой фундаментальное уравнение адсорбции Гиббса? 7. Какие положения лежат в основе мономолекулярной теории адсорбции Ленгмюра? 8. Проанализируйте уравнение Ленгмюра и покажите его взаимосвязь с уравнением Фрейндлиха. 9. Какие положения лежат в основе полимолекулярной теории адсорбции Поляни? 10. Назовите область применения теории полимолекулярной адсорбции. 11. Какие положения лежат в основе теории полимолекулярной адсорбции БЭТ? 12. Что такое капиллярная конденсация? 13. Как можно определить удельную поверхность адсорбентов на основании теории БЭТ?
Вопросы к лекции 4 1. Дайте определение процессам адсорбции и десорбции. Какие виды адсорбции Вы знаете? 2. Приведите примеры адсорбционных процессов. 3. Что называют адсорбатом, адсорбтивом, адсорбентом? 4. Назовите количественные характеристики процесса адсорбции. 5. Что такое изотерма адсорбции? 6. Какие величины связывает между собой фундаментальное уравнение адсорбции Гиббса? 7. Какие положения лежат в основе мономолекулярной теории адсорбции Ленгмюра? 8. Проанализируйте уравнение Ленгмюра и покажите его взаимосвязь с уравнением Фрейндлиха. 9. Какие положения лежат в основе полимолекулярной теории адсорбции Поляни? 10. Назовите область применения теории полимолекулярной адсорбции. 11. Какие положения лежат в основе теории полимолекулярной адсорбции БЭТ? 12. Что такое капиллярная конденсация? 13. Как можно определить удельную поверхность адсорбентов на основании теории БЭТ?


