PYaiDS_2010_L_2.ppt
- Количество слайдов: 13
 ПОВЕРХНОСТНЫЕ ЯВЛЕНИЯ И ДИСПЕРСНЫЕ СИСТЕМЫ ЛЕКЦИЯ 2
ПОВЕРХНОСТНЫЕ ЯВЛЕНИЯ И ДИСПЕРСНЫЕ СИСТЕМЫ ЛЕКЦИЯ 2
 Содержание лекции 1. Термодинамические основы 2. 3. 4. 5. поверхностных явлений. Поверхностный слой и его формирование. Энергетический и силовой аспекты поверхностного натяжения. Методы определения поверхностного натяжения. Особенности искривленной поверхности фаз.
Содержание лекции 1. Термодинамические основы 2. 3. 4. 5. поверхностных явлений. Поверхностный слой и его формирование. Энергетический и силовой аспекты поверхностного натяжения. Методы определения поверхностного натяжения. Особенности искривленной поверхности фаз.
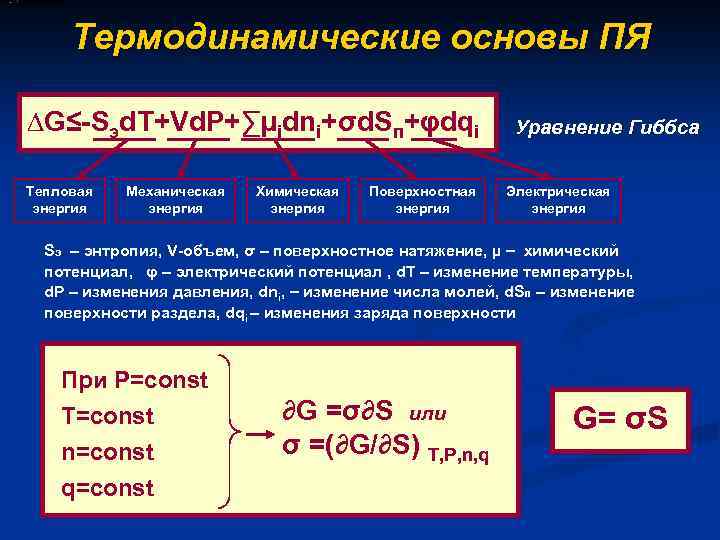 Термодинамические основы ПЯ ∆G≤-Sэd. Т+Vd. Р+∑µidni+σd. Sп+φdqi Тепловая энергия Механическая энергия Химическая энергия Поверхностная энергия Уравнение Гиббса Электрическая энергия Sэ – энтропия, V-объем, σ – поверхностное натяжение, µ – химический потенциал, φ – электрический потенциал , d. T – изменение температуры, d. P – изменения давления, dni, – изменение числа молей, d. Sп – изменение поверхности раздела, dqi – изменения заряда поверхности При Р=const Т=const n=const q=const ∂G =σ∂S или σ =(∂G/∂S) Т, Р, n, q G= σS
Термодинамические основы ПЯ ∆G≤-Sэd. Т+Vd. Р+∑µidni+σd. Sп+φdqi Тепловая энергия Механическая энергия Химическая энергия Поверхностная энергия Уравнение Гиббса Электрическая энергия Sэ – энтропия, V-объем, σ – поверхностное натяжение, µ – химический потенциал, φ – электрический потенциал , d. T – изменение температуры, d. P – изменения давления, dni, – изменение числа молей, d. Sп – изменение поверхности раздела, dqi – изменения заряда поверхности При Р=const Т=const n=const q=const ∂G =σ∂S или σ =(∂G/∂S) Т, Р, n, q G= σS
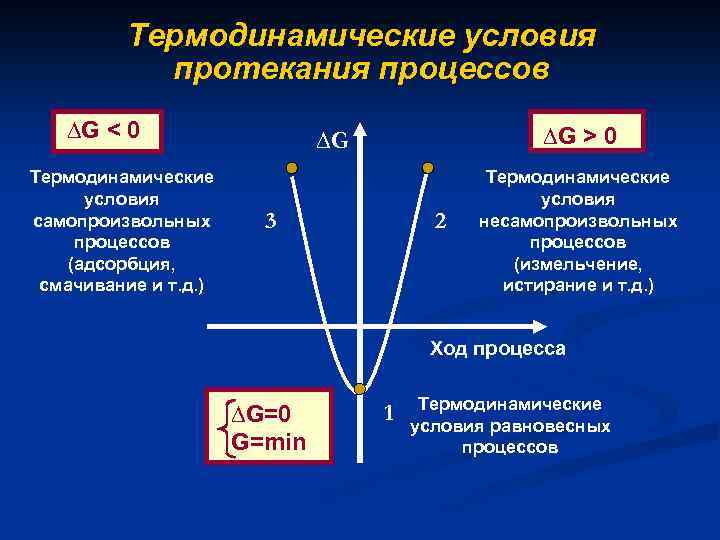 Термодинамические условия протекания процессов ∆G < 0 Термодинамические условия самопроизвольных процессов (адсорбция, смачивание и т. д. ) ∆G > 0 ∆G 3 2 Термодинамические условия несамопроизвольных процессов (измельчение, истирание и т. д. ) Ход процесса ∆G=0 G=min 1 Термодинамические условия равновесных процессов
Термодинамические условия протекания процессов ∆G < 0 Термодинамические условия самопроизвольных процессов (адсорбция, смачивание и т. д. ) ∆G > 0 ∆G 3 2 Термодинамические условия несамопроизвольных процессов (измельчение, истирание и т. д. ) Ход процесса ∆G=0 G=min 1 Термодинамические условия равновесных процессов
 Поверхностный слой и его формирование Свойства поверхности жидкости твердого тела • подвижность атомов • неподвижность • обновление поверхности • неизменность • эквипотенциальность • неэквипотенциальность • малая величина ∆G • большая величина ∆G • малая толщина • большая толщина поверхностного слоя
Поверхностный слой и его формирование Свойства поверхности жидкости твердого тела • подвижность атомов • неподвижность • обновление поверхности • неизменность • эквипотенциальность • неэквипотенциальность • малая величина ∆G • большая величина ∆G • малая толщина • большая толщина поверхностного слоя
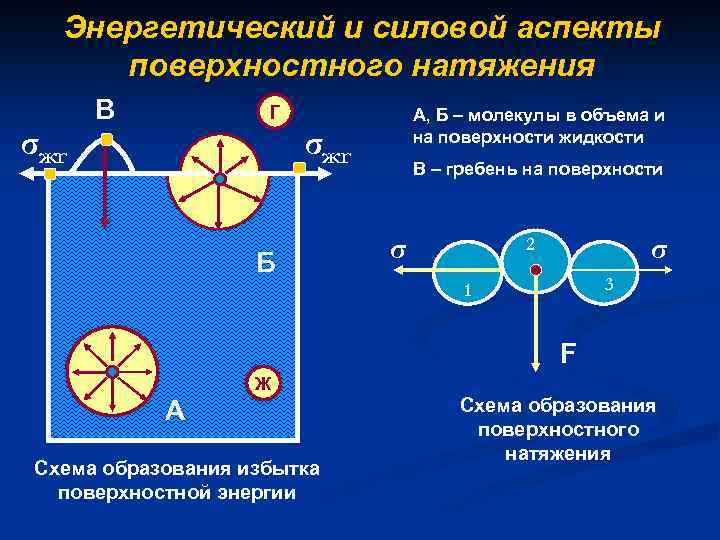 Энергетический и силовой аспекты поверхностного натяжения σжг В Г А, Б – молекулы в объема и на поверхности жидкости σжг Б В – гребень на поверхности σ σ 2 3 1 F Ж А Схема образования избытка поверхностной энергии Схема образования поверхностного натяжения
Энергетический и силовой аспекты поверхностного натяжения σжг В Г А, Б – молекулы в объема и на поверхности жидкости σжг Б В – гребень на поверхности σ σ 2 3 1 F Ж А Схема образования избытка поверхностной энергии Схема образования поверхностного натяжения
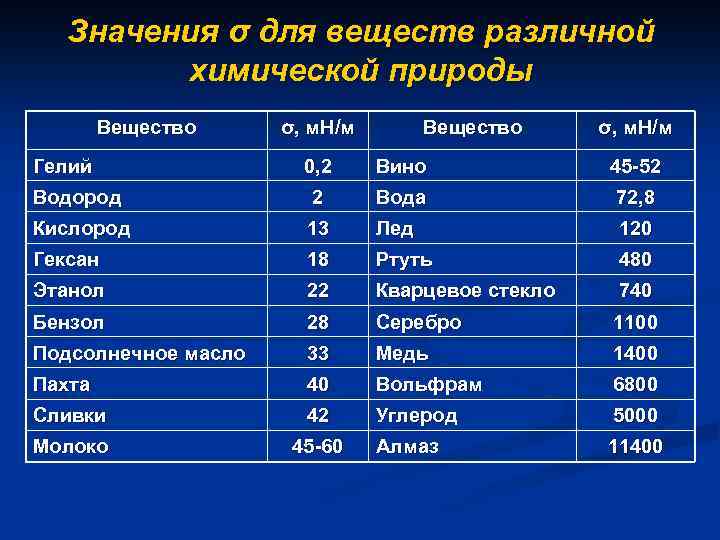 Значения σ для веществ различной химической природы Вещество Гелий σ, м. Н/м Вещество σ, м. Н/м 0, 2 Вино 45 -52 Водород 2 Вода 72, 8 Кислород 13 Лед 120 Гексан 18 Ртуть 480 Этанол 22 Кварцевое стекло 740 Бензол 28 Серебро 1100 Подсолнечное масло 33 Медь 1400 Пахта 40 Вольфрам 6800 Сливки 42 Углерод 5000 Молоко 45 -60 Алмаз 11400
Значения σ для веществ различной химической природы Вещество Гелий σ, м. Н/м Вещество σ, м. Н/м 0, 2 Вино 45 -52 Водород 2 Вода 72, 8 Кислород 13 Лед 120 Гексан 18 Ртуть 480 Этанол 22 Кварцевое стекло 740 Бензол 28 Серебро 1100 Подсолнечное масло 33 Медь 1400 Пахта 40 Вольфрам 6800 Сливки 42 Углерод 5000 Молоко 45 -60 Алмаз 11400
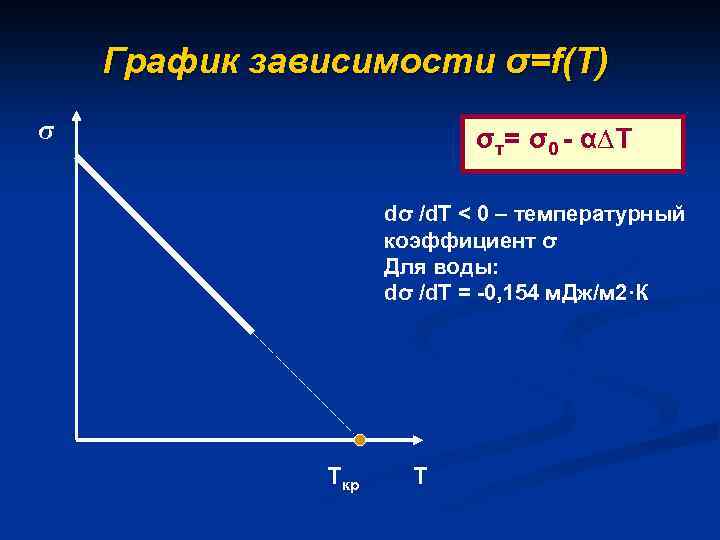 График зависимости σ=f(Т) σ σт= σ0 - α∆Т dσ /d. T < 0 – температурный коэффициент σ Для воды: dσ /d. T = -0, 154 м. Дж/м 2·К Ткр Т
График зависимости σ=f(Т) σ σт= σ0 - α∆Т dσ /d. T < 0 – температурный коэффициент σ Для воды: dσ /d. T = -0, 154 м. Дж/м 2·К Ткр Т
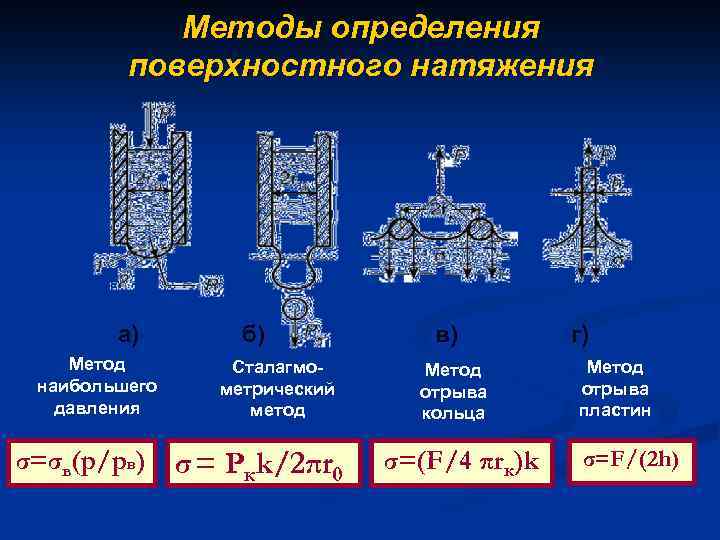 Методы определения поверхностного натяжения а) Метод наибольшего давления σ=σв(р/рв) б) Сталагмометрический метод σ = Ркk/2πr 0 в) Метод отрыва кольца σ=(F/4 πrк)k г) Метод отрыва пластин σ=F/(2 h)
Методы определения поверхностного натяжения а) Метод наибольшего давления σ=σв(р/рв) б) Сталагмометрический метод σ = Ркk/2πr 0 в) Метод отрыва кольца σ=(F/4 πrк)k г) Метод отрыва пластин σ=F/(2 h)
 Схема образования избыточного внутреннего давления P 0 σ σ r ∆P=Рr-P 0 V=4/3πr 3 Работа по изменению поверхностной энергии Работа по изменению объема тела Pr S=4πr 2 А=σd. S А=∆Рd. V ∆p=σ d. S/d. V d. S=8πrdr d. V=4πr 2 dr ∆p= ±σ(1/r 1 +1/r 2) Уравнение Лапласа p=± 2σ/r Для поверхности неправильной формы Для сферической поверхности
Схема образования избыточного внутреннего давления P 0 σ σ r ∆P=Рr-P 0 V=4/3πr 3 Работа по изменению поверхностной энергии Работа по изменению объема тела Pr S=4πr 2 А=σd. S А=∆Рd. V ∆p=σ d. S/d. V d. S=8πrdr d. V=4πr 2 dr ∆p= ±σ(1/r 1 +1/r 2) Уравнение Лапласа p=± 2σ/r Для поверхности неправильной формы Для сферической поверхности
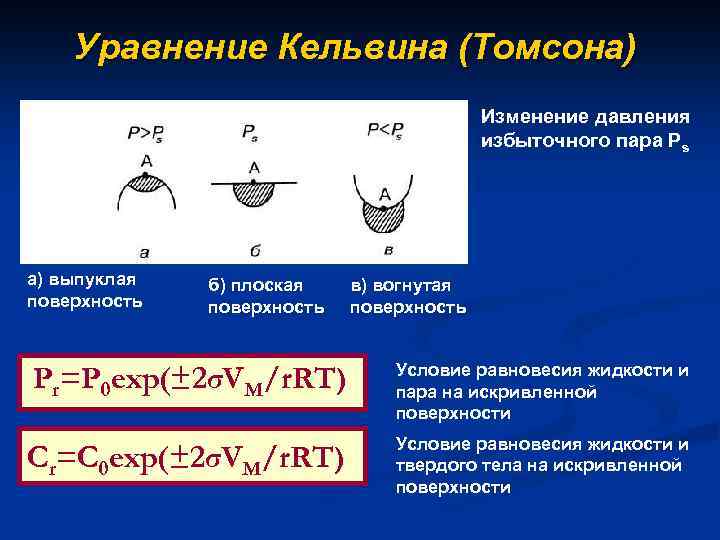 Уравнение Кельвина (Томсона) Изменение давления избыточного пара Рs a) выпуклая поверхность б) плоская поверхность в) вогнутая поверхность Pr=Р 0 exp(± 2σVМ/r. RT) Условие равновесия жидкости и пара на искривленной поверхности Cr=C 0 exp(± 2σVМ/r. RT) Условие равновесия жидкости и твердого тела на искривленной поверхности
Уравнение Кельвина (Томсона) Изменение давления избыточного пара Рs a) выпуклая поверхность б) плоская поверхность в) вогнутая поверхность Pr=Р 0 exp(± 2σVМ/r. RT) Условие равновесия жидкости и пара на искривленной поверхности Cr=C 0 exp(± 2σVМ/r. RT) Условие равновесия жидкости и твердого тела на искривленной поверхности
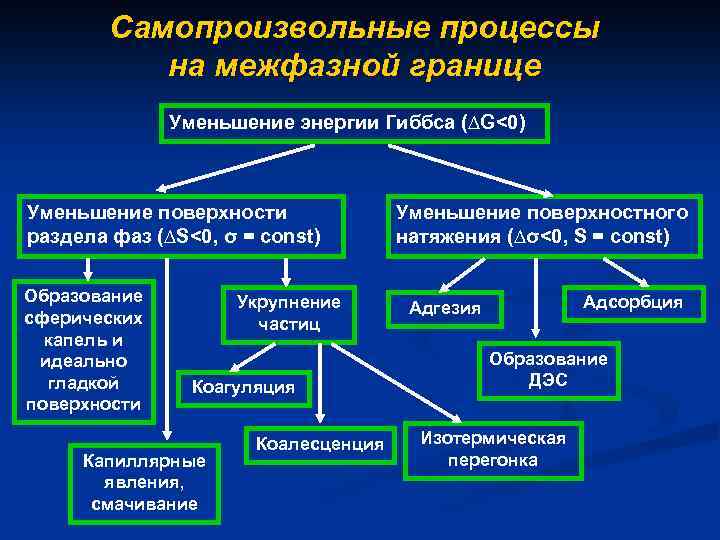 Самопроизвольные процессы на межфазной границе Уменьшение энергии Гиббса (∆G<0) Уменьшение поверхности раздела фаз (∆S<0, σ = const) Образование сферических капель и идеально гладкой поверхности Укрупнение частиц Коагуляция Капиллярные явления, смачивание Коалесценция Уменьшение поверхностного натяжения (∆σ<0, S = const) Адсорбция Адгезия Образование ДЭС Изотермическая перегонка
Самопроизвольные процессы на межфазной границе Уменьшение энергии Гиббса (∆G<0) Уменьшение поверхности раздела фаз (∆S<0, σ = const) Образование сферических капель и идеально гладкой поверхности Укрупнение частиц Коагуляция Капиллярные явления, смачивание Коалесценция Уменьшение поверхностного натяжения (∆σ<0, S = const) Адсорбция Адгезия Образование ДЭС Изотермическая перегонка
 Вопросы к лекции 2 1. Почему на поверхности раздела фаз возникает избыток поверхностной энергии? 2. Что представляет собой энергия Гиббса? Приведите примеры процессов, в результате которых энергия Гиббса возрастает (уменьшается). 3. Чем отличаются свойства поверхностей жидкости и твердого тела на границе с газовой фазой? 4. В чем заключаются энергетический и силовой аспекты поверхностного натяжения? 5. От каких факторов зависит величина поверхностного натяжения? 6. Назовите методы определения поверхностного натяжения. 7. Взаимосвязь каких физических величин показывает уравнение Лапласа? 8. Над какой поверхностью давление насыщенного пара больше – над выпуклой, вогнутой или плоской? 9. Как влияет радиус кривизны поверхности на величину избыточного давления? 10. На какие две группы делятся самопроизвольные процессы, протекающие на межфазных границах?
Вопросы к лекции 2 1. Почему на поверхности раздела фаз возникает избыток поверхностной энергии? 2. Что представляет собой энергия Гиббса? Приведите примеры процессов, в результате которых энергия Гиббса возрастает (уменьшается). 3. Чем отличаются свойства поверхностей жидкости и твердого тела на границе с газовой фазой? 4. В чем заключаются энергетический и силовой аспекты поверхностного натяжения? 5. От каких факторов зависит величина поверхностного натяжения? 6. Назовите методы определения поверхностного натяжения. 7. Взаимосвязь каких физических величин показывает уравнение Лапласа? 8. Над какой поверхностью давление насыщенного пара больше – над выпуклой, вогнутой или плоской? 9. Как влияет радиус кривизны поверхности на величину избыточного давления? 10. На какие две группы делятся самопроизвольные процессы, протекающие на межфазных границах?


