лекция 7 ФКХ рус.ppt
- Количество слайдов: 24

Поверхностные явления. Адсорбция на границе раздела фаз

• ФАЗА – однородная по составу и одинаковая по физическим и химическим свойствам часть физико-химической системы, отделенная от других ее частей поверхностями раздела; • гомогенная система; • гетерогенная система.

• Коллоидная химия изучает свойства систем, в которых одна из фаз находится в высокодисперсном состоянии. Дисперсные системы гетерогенны и обладают сильно развитой поверхностью, поэтому в таких системах большое значение приобретают поверхностные явления. Степень раздробленности вещества характеризуется величиной удельной поверхности s, которая равно отношению поверхности частиц S к объему V вещества, подвергнутого дроблению: s = S/V

Удельная поверхность – это суммарная поверхность всех частиц вещества, общий объем которых составляет 1 см 3. Если принять форму частицы в виде куба с ребром 1 см, то удельная поверхность: Для частиц шарообразной формы

• Поверхностные явления — это процессы, происходящие на границах раздела фаз, составляющих физико-химические системы, и обусловленные особенностями состава и строения поверхностного слоя (адсорбция, смачивание, растекание, адгезия и др. ) • Поверхность раздела фаз характеризуется • • • определенным видом энергии — поверхностной энергией Гиббса Gs. Удельная поверхностная энергия называется поверхностным натяжением σ =Gs/S (энергия Гиббса, приходящаяся на единицу площади поверхностного слоя). Энергия поверхности Gs = σ ⋅ S. Чем больше площадь поверхности раздела, тем больше в системе свободная поверхностная энергия. Площадь поверхности раздела при данной массе возрастает с уменьшением размера частей, на которые разделяется система (дисперсности).

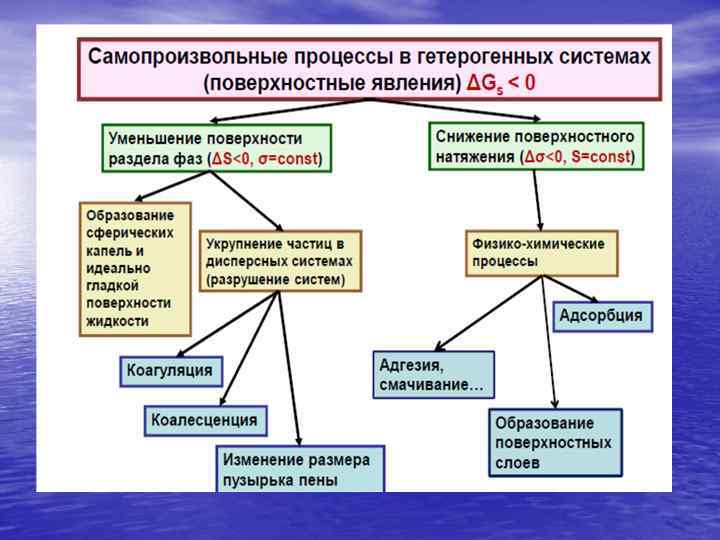
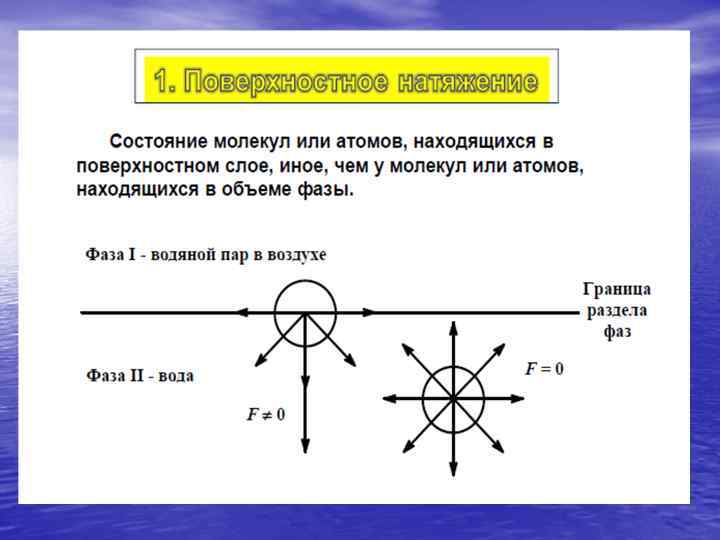

Поверхностное натяжение зависит от природы и агрегатного состояния контактирующих фаз.




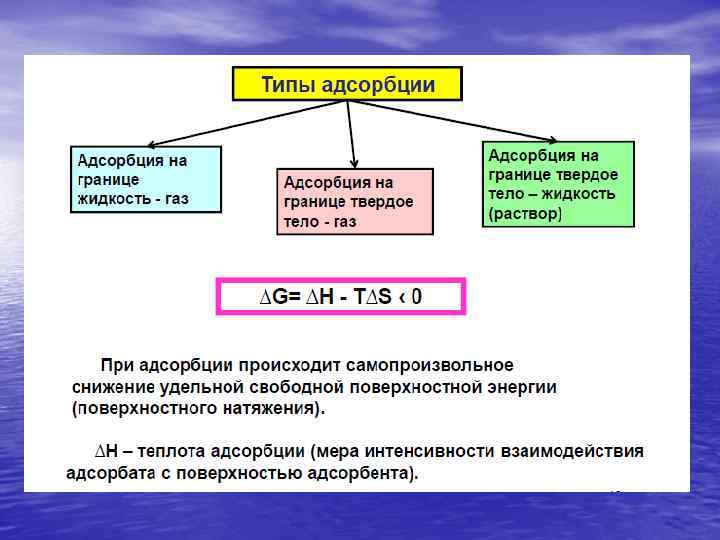



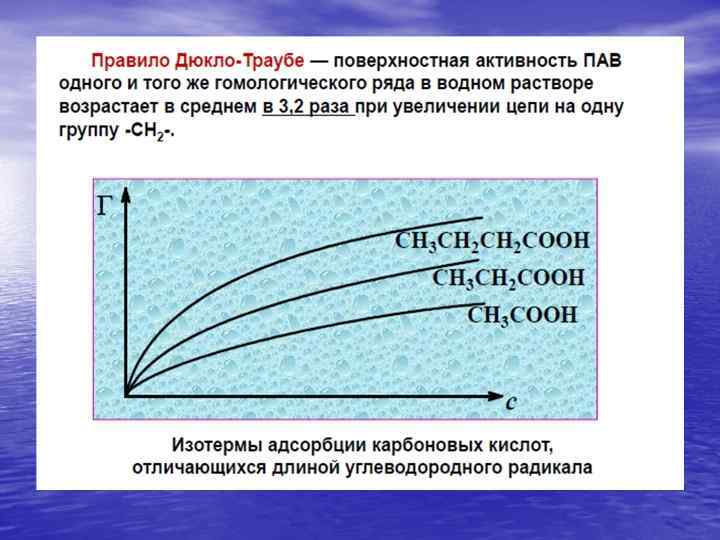





Теории адсорбции 1. Теория мономолекулярной адсорбции Ленгмюра 2. Теория полимолекулярной адсорбции Поляни Теоретические представления, развитые Ленгмюром и Поляни, в значительной степени идеализируют и упрощают истинную картину адсорбции. На самом деле поверхность адсорбента неоднородна, между адсорбированными частицами имеет место взаимодействие, активные центры не являются полностью независимыми друг от друга и т. д. Все это усложняет вид уравнения изотермы. Г. Фрейндлих показал, что при постоянной температуре число молей адсорбированного газа или растворенного вещества, приходящееся на единицу массы адсорбента (т. н. удельная адсорбция x/m), пропорционально равновесному давлению (для газа) или равновесной концентрации (для веществ, адсорбируемых из раствора) адсорбента, возведенным в некоторую степень, которая всегда меньше единицы:

лекция 7 ФКХ рус.ppt