Lection 9.ppt
- Количество слайдов: 17
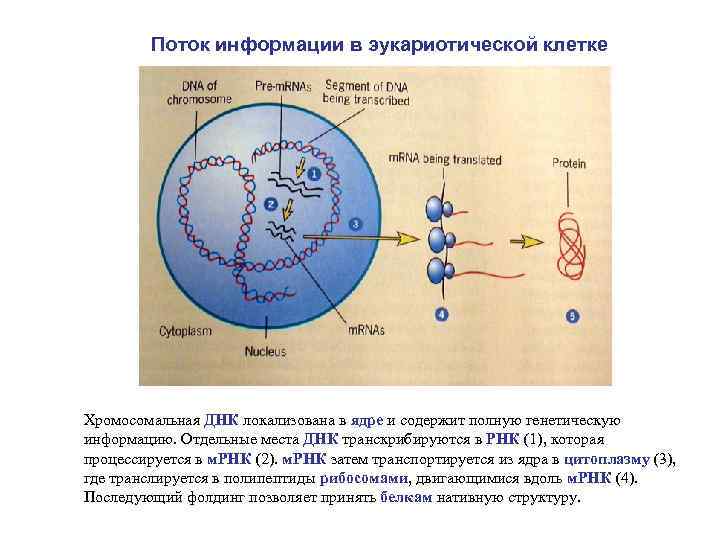 Поток информации в эукариотической клетке Хромосомальная ДНК локализована в ядре и содержит полную генетическую информацию. Отдельные места ДНК транскрибируются в РНК (1), которая процессируется в м. РНК (2). м. РНК затем транспортируется из ядра в цитоплазму (3), где транслируется в полипептиды рибосомами, двигающимися вдоль м. РНК (4). Последующий фолдинг позволяет принять белкам нативную структуру.
Поток информации в эукариотической клетке Хромосомальная ДНК локализована в ядре и содержит полную генетическую информацию. Отдельные места ДНК транскрибируются в РНК (1), которая процессируется в м. РНК (2). м. РНК затем транспортируется из ядра в цитоплазму (3), где транслируется в полипептиды рибосомами, двигающимися вдоль м. РНК (4). Последующий фолдинг позволяет принять белкам нативную структуру.
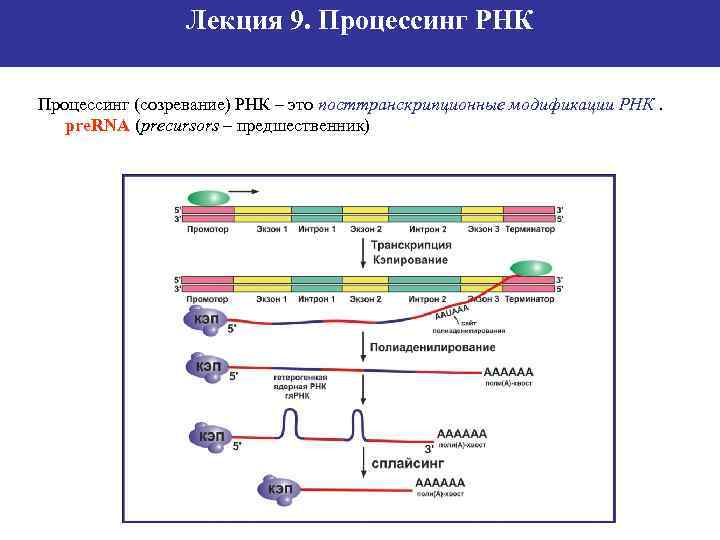 Лекция 9. Процессинг РНК Процессинг (созревание) РНК – это посттранскрипционные модификации РНК. pre. RNA (precursors – предшественник)
Лекция 9. Процессинг РНК Процессинг (созревание) РНК – это посттранскрипционные модификации РНК. pre. RNA (precursors – предшественник)
 Процессинг РНК у бактерий Процессинг для бактерий не характерен. - Первичные транскрипты большинства бактериальных кодирующих белок генов являются функционально активными м. РНК. - Бактериальные т. РНК и р. РНК сначала транскрибируются в виде пре-РНК, а затем процессируются. Существуют исключения: - Транскрипционный оперон, кодирующий Rs белки (L 1, L 7/12) и субъединицы РНКполимеразы (β и β’); - Существенная часть м. РНК подвергается полиаденилированию, однако хвосты короткие (14 -60 АК), дестабилизируют структуру ряда м. РНК; Таким образом, созревание РНК у бактерий включает разрезание, полиаденилирование РНК и модифицирование оснований.
Процессинг РНК у бактерий Процессинг для бактерий не характерен. - Первичные транскрипты большинства бактериальных кодирующих белок генов являются функционально активными м. РНК. - Бактериальные т. РНК и р. РНК сначала транскрибируются в виде пре-РНК, а затем процессируются. Существуют исключения: - Транскрипционный оперон, кодирующий Rs белки (L 1, L 7/12) и субъединицы РНКполимеразы (β и β’); - Существенная часть м. РНК подвергается полиаденилированию, однако хвосты короткие (14 -60 АК), дестабилизируют структуру ряда м. РНК; Таким образом, созревание РНК у бактерий включает разрезание, полиаденилирование РНК и модифицирование оснований.
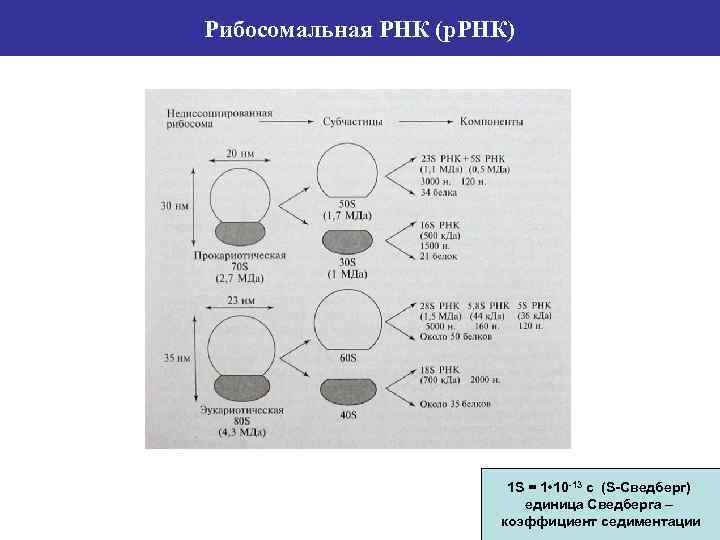 Рибосомальная РНК (р. РНК) 1 S = 1 • 10 -13 c (S-Сведберг) единица Сведберга – коэффициент седиментации
Рибосомальная РНК (р. РНК) 1 S = 1 • 10 -13 c (S-Сведберг) единица Сведберга – коэффициент седиментации
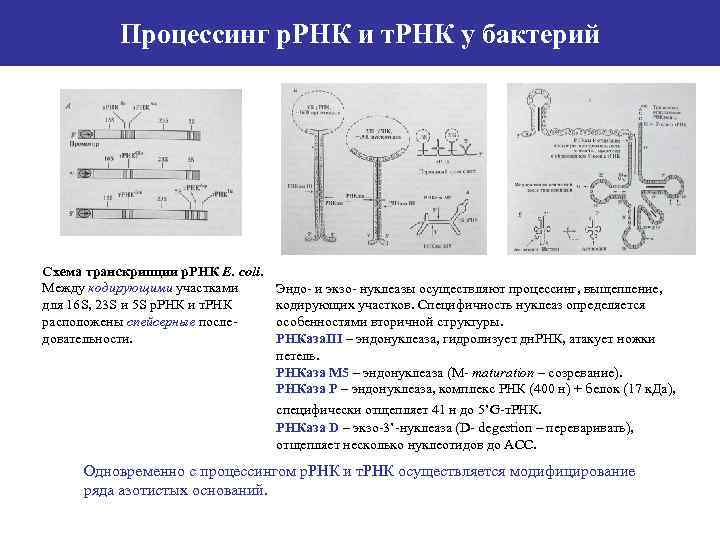 Процессинг р. РНК и т. РНК у бактерий Схема транскрипции р. РНК E. coli. Между кодирующими участками для 16 S, 23 S и 5 S р. РНК и т. РНК расположены спейсерные последовательности. Эндо- и экзо- нуклеазы осуществляют процессинг, выщепление, кодирующих участков. Специфичность нуклеаз определяется особенностями вторичной структуры. РНКаза. III – эндонуклеаза, гидролизует дн. РНК, атакует ножки петель. РНКаза М 5 – эндонуклеаза (М- maturation – созревание). РНКаза Р – эндонуклеаза, комплекс РНК (400 н) + белок (17 к. Да), специфически отщепляет 41 н до 5’G-т. РНКаза D – экзо-3’-нуклеаза (D- degestion – переваривать), отщепляет несколько нуклеотидов до АСС. Одновременно с процессингом р. РНК и т. РНК осуществляется модифицирование ряда азотистых оснований.
Процессинг р. РНК и т. РНК у бактерий Схема транскрипции р. РНК E. coli. Между кодирующими участками для 16 S, 23 S и 5 S р. РНК и т. РНК расположены спейсерные последовательности. Эндо- и экзо- нуклеазы осуществляют процессинг, выщепление, кодирующих участков. Специфичность нуклеаз определяется особенностями вторичной структуры. РНКаза. III – эндонуклеаза, гидролизует дн. РНК, атакует ножки петель. РНКаза М 5 – эндонуклеаза (М- maturation – созревание). РНКаза Р – эндонуклеаза, комплекс РНК (400 н) + белок (17 к. Да), специфически отщепляет 41 н до 5’G-т. РНКаза D – экзо-3’-нуклеаза (D- degestion – переваривать), отщепляет несколько нуклеотидов до АСС. Одновременно с процессингом р. РНК и т. РНК осуществляется модифицирование ряда азотистых оснований.
 Расщепление пре-р. РНК у E. coli Три гена р. РНК (5 S, 16 S, 23 S) сцеплены в единую единицу транскрипции (у E. coli 7 копий). Единый предшественник разрезается рибонуклеазами III, P и F в позициях, предписанных двунитевыми областями, образованными спариванием оснований между различными частями пре-р. РНК. Края разрезов впоследствии обрезаются за счет экзонуклеазного действия рибонуклеаз М 16, М 23 и М 5 и в конечном счете получаются зрелые р. РНК. Между генами р. РНК располагаются гены т. РНК. Их процессинг осуществляется по другой схеме.
Расщепление пре-р. РНК у E. coli Три гена р. РНК (5 S, 16 S, 23 S) сцеплены в единую единицу транскрипции (у E. coli 7 копий). Единый предшественник разрезается рибонуклеазами III, P и F в позициях, предписанных двунитевыми областями, образованными спариванием оснований между различными частями пре-р. РНК. Края разрезов впоследствии обрезаются за счет экзонуклеазного действия рибонуклеаз М 16, М 23 и М 5 и в конечном счете получаются зрелые р. РНК. Между генами р. РНК располагаются гены т. РНК. Их процессинг осуществляется по другой схеме.
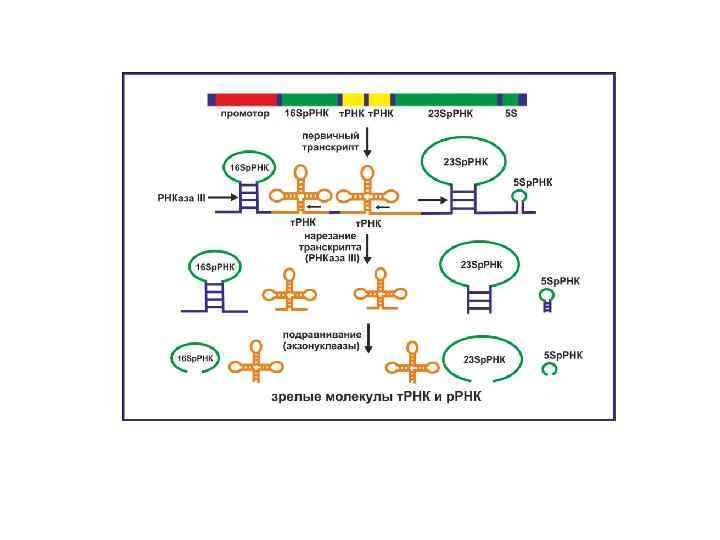
 Созревание пре-т. РНК E. coli Гены т. РНК распределены по геному некоторые сами по себе, а некоторые в виде тандемных множеств в мульти-т. РНКовых единицах транскрипции. По одному два гена т. РНК находится в единицах транскрипции р. РНК. Расщепляются они по-разному, но схожим образом. Пре-т. РНК принимает характерную спаренную структуру клеверного листа, образуются две дополнительные шпильки. Вначале пре-т. РНК разрезают рибонуклеазы Е или F, образующие новый 3’-конец непосредственно выше одной из шпилек. Рибонуклеаза D (экзонуклеаза), обрезает 7 нуклеотидов с этого нового 3’-конца и затем берет паузу, в то время как рибонуклеаза Р делает разрез в начале клеверного листа, образуя 5’-конец зрелой т. РНК. Затем рибонуклеаза D удаляет еще 2 нуклеотида, создавая 3’-конец зрелой молекулы. Все зрелые т. РНК должны оканчиваться тринуклеотидом 5’-CCA-3’. В случае т. РНКTyr конечный тринуклеотид присутствует. В других случаях рибонуклеаза Z делает разрез, а тринуклеотид добавляется специальными т. РНК-нуклеотидилтрансферазами.
Созревание пре-т. РНК E. coli Гены т. РНК распределены по геному некоторые сами по себе, а некоторые в виде тандемных множеств в мульти-т. РНКовых единицах транскрипции. По одному два гена т. РНК находится в единицах транскрипции р. РНК. Расщепляются они по-разному, но схожим образом. Пре-т. РНК принимает характерную спаренную структуру клеверного листа, образуются две дополнительные шпильки. Вначале пре-т. РНК разрезают рибонуклеазы Е или F, образующие новый 3’-конец непосредственно выше одной из шпилек. Рибонуклеаза D (экзонуклеаза), обрезает 7 нуклеотидов с этого нового 3’-конца и затем берет паузу, в то время как рибонуклеаза Р делает разрез в начале клеверного листа, образуя 5’-конец зрелой т. РНК. Затем рибонуклеаза D удаляет еще 2 нуклеотида, создавая 3’-конец зрелой молекулы. Все зрелые т. РНК должны оканчиваться тринуклеотидом 5’-CCA-3’. В случае т. РНКTyr конечный тринуклеотид присутствует. В других случаях рибонуклеаза Z делает разрез, а тринуклеотид добавляется специальными т. РНК-нуклеотидилтрансферазами.
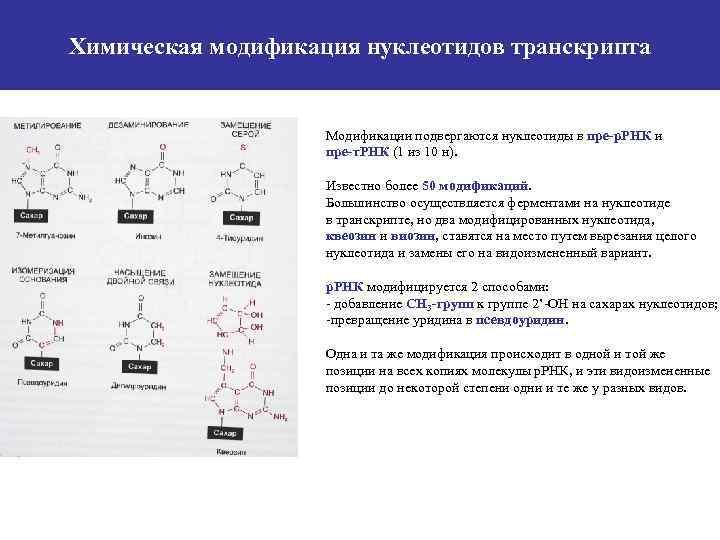 Химическая модификация нуклеотидов транскрипта Модификации подвергаются нуклеотиды в пре-р. РНК и пре-т. РНК (1 из 10 н). Известно более 50 модификаций. Большинство осуществляется ферментами на нуклеотиде в транскрипте, но два модифицированных нуклеотида, квеозин и виозин, ставятся на место путем вырезания целого нуклеотида и замены его на видоизмененный вариант. р. РНК модифицируется 2 способами: - добавление CН 3 -групп к группе 2’-ОН на сахарах нуклеотидов; -превращение уридина в псевдоуридин. Одна и та же модификация происходит в одной и той же позиции на всех копиях молекулы р. РНК, и эти видоизмененные позиции до некоторой степени одни и те же у разных видов.
Химическая модификация нуклеотидов транскрипта Модификации подвергаются нуклеотиды в пре-р. РНК и пре-т. РНК (1 из 10 н). Известно более 50 модификаций. Большинство осуществляется ферментами на нуклеотиде в транскрипте, но два модифицированных нуклеотида, квеозин и виозин, ставятся на место путем вырезания целого нуклеотида и замены его на видоизмененный вариант. р. РНК модифицируется 2 способами: - добавление CН 3 -групп к группе 2’-ОН на сахарах нуклеотидов; -превращение уридина в псевдоуридин. Одна и та же модификация происходит в одной и той же позиции на всех копиях молекулы р. РНК, и эти видоизмененные позиции до некоторой степени одни и те же у разных видов.
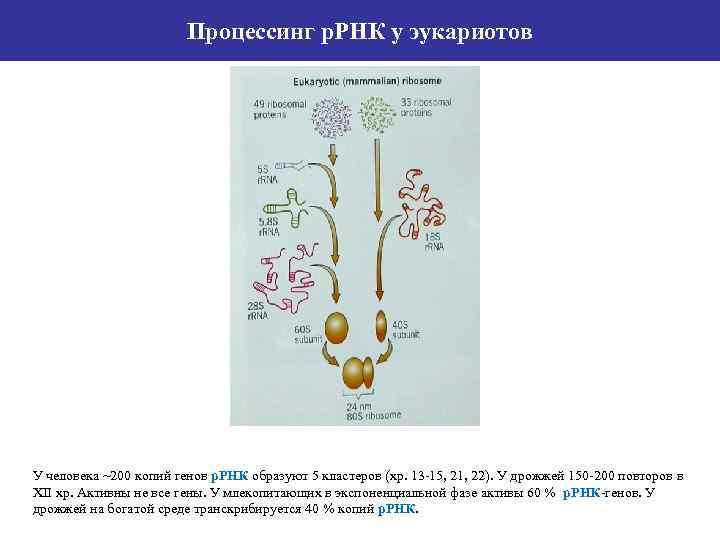 Процессинг р. РНК у эукариотов У человека ~200 копий генов р. РНК образуют 5 кластеров (хр. 13 -15, 21, 22). У дрожжей 150 -200 повторов в XII хр. Активны не все гены. У млекопитающих в экспоненциальной фазе активы 60 % р. РНК-генов. У дрожжей на богатой среде транскрибируется 40 % копий р. РНК.
Процессинг р. РНК у эукариотов У человека ~200 копий генов р. РНК образуют 5 кластеров (хр. 13 -15, 21, 22). У дрожжей 150 -200 повторов в XII хр. Активны не все гены. У млекопитающих в экспоненциальной фазе активы 60 % р. РНК-генов. У дрожжей на богатой среде транскрибируется 40 % копий р. РНК.
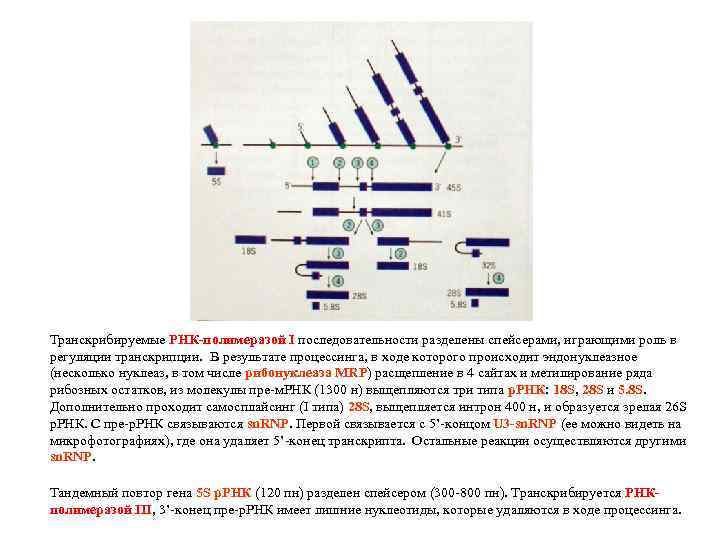 Транскрибируемые РНК-полимеразой I последовательности разделены спейсерами, играющими роль в регуляции транскрипции. В результате процессинга, в ходе которого происходит эндонуклеазное (несколько нуклеаз, в том числе рибонуклеаза MRP) расщепление в 4 сайтах и метилирование ряда рибозных остатков, из молекулы пре-м. РНК (1300 н) выщепляются три типа р. РНК: 18 S, 28 S и 5. 8 S. Дополнительно проходит самосплайсинг (I типа) 28 S, выщепляется интрон 400 н, и образуется зрелая 26 S р. РНК. С пре-р. РНК связываются sn. RNP. Первой связывается с 5’-концом U 3 -sn. RNP (ее можно видеть на микрофотографиях), где она удаляет 5’-конец транскрипта. Остальные реакции осуществляются другими sn. RNP. Тандемный повтор гена 5 S р. РНК (120 пн) разделен спейсером (300 -800 пн). Транскрибируется РНКполимеразой III, 3’-конец пре-р. РНК имеет лишние нуклеотиды, которые удаляются в ходе процессинга.
Транскрибируемые РНК-полимеразой I последовательности разделены спейсерами, играющими роль в регуляции транскрипции. В результате процессинга, в ходе которого происходит эндонуклеазное (несколько нуклеаз, в том числе рибонуклеаза MRP) расщепление в 4 сайтах и метилирование ряда рибозных остатков, из молекулы пре-м. РНК (1300 н) выщепляются три типа р. РНК: 18 S, 28 S и 5. 8 S. Дополнительно проходит самосплайсинг (I типа) 28 S, выщепляется интрон 400 н, и образуется зрелая 26 S р. РНК. С пре-р. РНК связываются sn. RNP. Первой связывается с 5’-концом U 3 -sn. RNP (ее можно видеть на микрофотографиях), где она удаляет 5’-конец транскрипта. Остальные реакции осуществляются другими sn. RNP. Тандемный повтор гена 5 S р. РНК (120 пн) разделен спейсером (300 -800 пн). Транскрибируется РНКполимеразой III, 3’-конец пре-р. РНК имеет лишние нуклеотиды, которые удаляются в ходе процессинга.
 Процессинг т. РНК у эукариотов ~40 -60 видов т. РНК в виде кластеров разбросаны по геному (дрожжи – 275 генов т. РНК, человек – 1300 генов т. РНК). Подавляющую часть кластера составляют спейсеры. Процессинг осуществляется: - эндонуклеазой, называемой рибонуклеазой Р, состоящей из РНК и белков. РНК- катализирует расщепление субстрата пре-т. РНК (у дрожжей – 250 н, у человека – 100 н); - на 3’-конце имеется триплет ССА, который добавляется с помощью фермента после процесинга т. РНК (и необходим для синтеза белков) в результате последовательных нуклеотидилтрансферазных реакций. ССА-ОН необходим для взаимодействия с аминоацил-т. РНК-синтетазой при образовании аминоацил-т. РНК; - удаление интрона из пре-т. РНК у эукариот осуществляет полифункциональный фермент, обладающий киназной, лигазной и фосфодиэстеразной активностью.
Процессинг т. РНК у эукариотов ~40 -60 видов т. РНК в виде кластеров разбросаны по геному (дрожжи – 275 генов т. РНК, человек – 1300 генов т. РНК). Подавляющую часть кластера составляют спейсеры. Процессинг осуществляется: - эндонуклеазой, называемой рибонуклеазой Р, состоящей из РНК и белков. РНК- катализирует расщепление субстрата пре-т. РНК (у дрожжей – 250 н, у человека – 100 н); - на 3’-конце имеется триплет ССА, который добавляется с помощью фермента после процесинга т. РНК (и необходим для синтеза белков) в результате последовательных нуклеотидилтрансферазных реакций. ССА-ОН необходим для взаимодействия с аминоацил-т. РНК-синтетазой при образовании аминоацил-т. РНК; - удаление интрона из пре-т. РНК у эукариот осуществляет полифункциональный фермент, обладающий киназной, лигазной и фосфодиэстеразной активностью.
 Сплайсинг пре-т. РНКТир у S. cerevisiae Интроны присутствуют только в 6 % всех генов т. РНК человека. длина интрона – 14 -60 н, располагается в антикодоновой петле. Два сайта сплайсинга разрезаются эндонуклеазой, состоящей из 4 субъединиц. Одна из которых использует структуру спаренного основаниями интрона в качестве направляющей, с тем чтобы опознать правильные позиции, в которых РНК должна быть разрезана. Затем двумя другими субъединицами фермента производятся выше- и ниже расположенные разрезы. На 3’-конце экзона образуется циклический фосфат, а на 5’- гидроксильная группа. Циклический фосфат превращается в 3’-ОН-конец посредством фосфодиэстеразы, а 5’-конец превращается в 5’-Р-конец действием киназы. Эти два конца удерживаются в тесной близости за счет естественной структуры спаренных оснований, принадлежащей т. РНК, и лигируются РНК-лигазой. Действия фосфодиэстеразы, киназы и лигазы обуславливаются одним белком.
Сплайсинг пре-т. РНКТир у S. cerevisiae Интроны присутствуют только в 6 % всех генов т. РНК человека. длина интрона – 14 -60 н, располагается в антикодоновой петле. Два сайта сплайсинга разрезаются эндонуклеазой, состоящей из 4 субъединиц. Одна из которых использует структуру спаренного основаниями интрона в качестве направляющей, с тем чтобы опознать правильные позиции, в которых РНК должна быть разрезана. Затем двумя другими субъединицами фермента производятся выше- и ниже расположенные разрезы. На 3’-конце экзона образуется циклический фосфат, а на 5’- гидроксильная группа. Циклический фосфат превращается в 3’-ОН-конец посредством фосфодиэстеразы, а 5’-конец превращается в 5’-Р-конец действием киназы. Эти два конца удерживаются в тесной близости за счет естественной структуры спаренных оснований, принадлежащей т. РНК, и лигируются РНК-лигазой. Действия фосфодиэстеразы, киназы и лигазы обуславливаются одним белком.
 Процессинг м. РНК у эукариотов Гетерогенная ядерная РНК (гя. РНК) – смесь транскриптов многих ядерных генов, локализована в ядре. Некоторые из них являются первичными транскриптами и имеют такую же длину, как и гены, с которых они были скопированы, другие – частично процессированы и утратили часть последовательности. Открыта в 1960 г. О. П. Самариной и Г. П. Георгиевым. Свойства м. РНК: 1. 2. 3. 4. 5. Содержит непрерывную кодирующую последовательность; Обнаруживается в цитоплазме; В процессе трансляции к ним присоединяются рибосомы; На 5’- и 3’-концах имеются нетранслируемые области (НТО), играющие регуляторную роль; Имеются специальные модификации на концах. На 5’-конце -метилгуанозин (cap), а на 3’-конце – poly(A) – хвост.
Процессинг м. РНК у эукариотов Гетерогенная ядерная РНК (гя. РНК) – смесь транскриптов многих ядерных генов, локализована в ядре. Некоторые из них являются первичными транскриптами и имеют такую же длину, как и гены, с которых они были скопированы, другие – частично процессированы и утратили часть последовательности. Открыта в 1960 г. О. П. Самариной и Г. П. Георгиевым. Свойства м. РНК: 1. 2. 3. 4. 5. Содержит непрерывную кодирующую последовательность; Обнаруживается в цитоплазме; В процессе трансляции к ним присоединяются рибосомы; На 5’- и 3’-концах имеются нетранслируемые области (НТО), играющие регуляторную роль; Имеются специальные модификации на концах. На 5’-конце -метилгуанозин (cap), а на 3’-конце – poly(A) – хвост.
 Процессинг 5’- и 3’-концов м. РНК А Б А. 5’-конец м. РНК кэпируется (cap - кепка), т. е. достраивается с образованием особой структуры метилгуанозина, ответственного за последующее связывание молекулы м. РНК с Rs. Кэпирование происходит почти сразу после синтеза первых 30 нуклеотидов. 1) Фосфогидролаза удаляет концевую фосфатную группу. 5’-концевого нуклеозидтрифосфата (трифосфат→дифосфат) 2) Гуанилтрансфераза добавляет гуанинмонофосфат в обратной ориентации, образуется 5’-5’-трифосфатный мостик. 3) Различные метилтрансферазы добавляют метильные группы к концевому G в положении 7’ и последнему нуклеотиду м. РНК в положении 2’-рибоза. Б. 3’-конец образуется в результате эндонуклеазного расщепления перед последовательностью AAUAAA (за 10 -30 н до сайта расщепления) и образования нового 3’-конца. рoly(А)-полимераза добавляет 200 -250 остатков А, матрица ДНК не участвует в этом процессе. РНК-полимераза продолжает транскрипцию пока не встретит сайт терминации. Остаток РНК не имеет 5’-кэпа и 3’-poly(A) и быстро распадается. С растущим poly(A)-хвостом связывается белок PABII, который стимулирует продолжение добавления А. Poly(A)-хвост необходим для переноса м. РНК из ядра в цитоплазму, для трансляции и определяет время жизни м. РНК. В 3’-НТО располагаются специфические последовательности (элементы нестабильности м. РНК), которые узнаются специфическими белками, связанными с ними и стабилизирующими м. РНК, сигналы полиаденилирования и сигналы внутриклеточной локализации. Poly(A) отсутствуют в гистоновых м. РНК.
Процессинг 5’- и 3’-концов м. РНК А Б А. 5’-конец м. РНК кэпируется (cap - кепка), т. е. достраивается с образованием особой структуры метилгуанозина, ответственного за последующее связывание молекулы м. РНК с Rs. Кэпирование происходит почти сразу после синтеза первых 30 нуклеотидов. 1) Фосфогидролаза удаляет концевую фосфатную группу. 5’-концевого нуклеозидтрифосфата (трифосфат→дифосфат) 2) Гуанилтрансфераза добавляет гуанинмонофосфат в обратной ориентации, образуется 5’-5’-трифосфатный мостик. 3) Различные метилтрансферазы добавляют метильные группы к концевому G в положении 7’ и последнему нуклеотиду м. РНК в положении 2’-рибоза. Б. 3’-конец образуется в результате эндонуклеазного расщепления перед последовательностью AAUAAA (за 10 -30 н до сайта расщепления) и образования нового 3’-конца. рoly(А)-полимераза добавляет 200 -250 остатков А, матрица ДНК не участвует в этом процессе. РНК-полимераза продолжает транскрипцию пока не встретит сайт терминации. Остаток РНК не имеет 5’-кэпа и 3’-poly(A) и быстро распадается. С растущим poly(A)-хвостом связывается белок PABII, который стимулирует продолжение добавления А. Poly(A)-хвост необходим для переноса м. РНК из ядра в цитоплазму, для трансляции и определяет время жизни м. РНК. В 3’-НТО располагаются специфические последовательности (элементы нестабильности м. РНК), которые узнаются специфическими белками, связанными с ними и стабилизирующими м. РНК, сигналы полиаденилирования и сигналы внутриклеточной локализации. Poly(A) отсутствуют в гистоновых м. РНК.
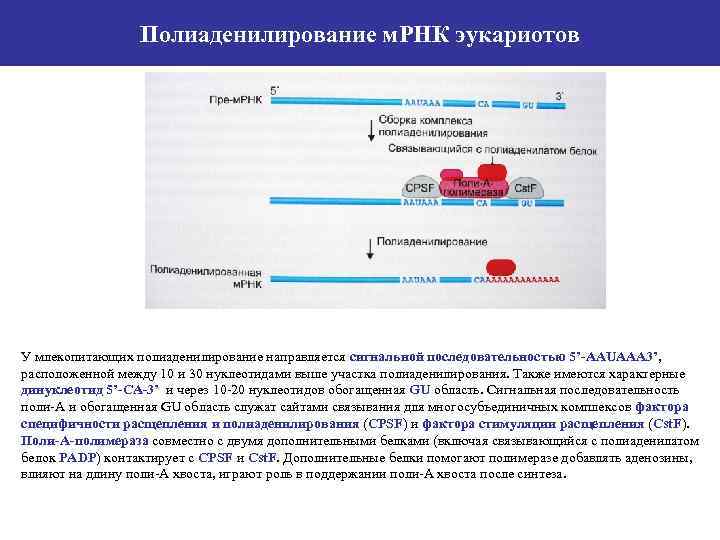 Полиаденилирование м. РНК эукариотов У млекопитающих полиаденилирование направляется сигнальной последовательностью 5’-AAUAAA 3’, расположенной между 10 и 30 нуклеотидами выше участка полиаденилирования. Также имеются характерные динуклеотид 5’-CA-3’ и через 10 -20 нуклеотидов обогащенная GU область. Сигнальная последовательность поли-А и обогащенная GU область служат сайтами связывания для многосубъединичных комплексов фактора специфичности расщепления и полиаденилирования (CPSF) и фактора стимуляции расщепления (Cst. F). Поли-А-полимераза совместно с двумя дополнительными белками (включая связывающийся с полиаденилатом белок PADP) контактирует с CPSF и Cst. F. Дополнительные белки помогают полимеразе добавлять аденозины, влияют на длину поли-А хвоста, играют роль в поддержании поли-А хвоста после синтеза.
Полиаденилирование м. РНК эукариотов У млекопитающих полиаденилирование направляется сигнальной последовательностью 5’-AAUAAA 3’, расположенной между 10 и 30 нуклеотидами выше участка полиаденилирования. Также имеются характерные динуклеотид 5’-CA-3’ и через 10 -20 нуклеотидов обогащенная GU область. Сигнальная последовательность поли-А и обогащенная GU область служат сайтами связывания для многосубъединичных комплексов фактора специфичности расщепления и полиаденилирования (CPSF) и фактора стимуляции расщепления (Cst. F). Поли-А-полимераза совместно с двумя дополнительными белками (включая связывающийся с полиаденилатом белок PADP) контактирует с CPSF и Cst. F. Дополнительные белки помогают полимеразе добавлять аденозины, влияют на длину поли-А хвоста, играют роль в поддержании поли-А хвоста после синтеза.
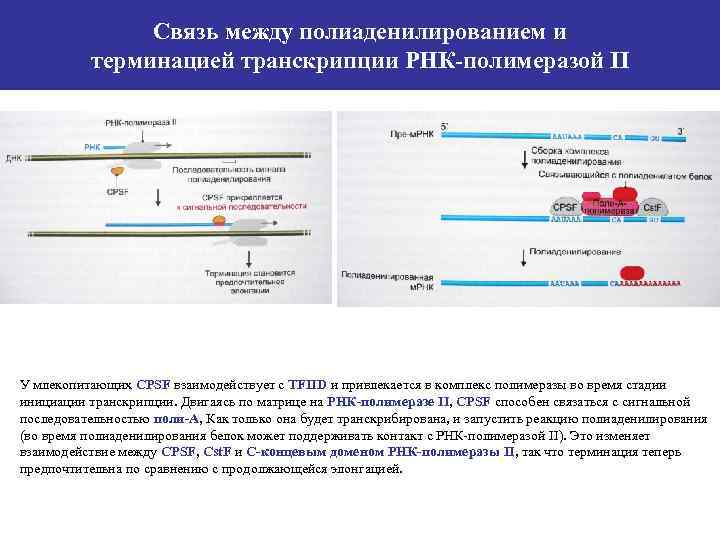 Связь между полиаденилированием и терминацией транскрипции РНК-полимеразой II У млекопитающих CPSF взаимодействует с TFIID и привлекается в комплекс полимеразы во время стадии инициации транскрипции. Двигаясь по матрице на РНК-полимеразе II, CPSF способен связаться с сигнальной последовательностью поли-А, Как только она будет транскрибирована, и запустить реакцию полиаденилирования (во время полиаденилирования белок может поддерживать контакт с РНК-полимеразой II). Это изменяет взаимодействие между CPSF, Cst. F и С-концевым доменом РНК-полимеразы II, так что терминация теперь предпочтительна по сравнению с продолжающейся элонгацией.
Связь между полиаденилированием и терминацией транскрипции РНК-полимеразой II У млекопитающих CPSF взаимодействует с TFIID и привлекается в комплекс полимеразы во время стадии инициации транскрипции. Двигаясь по матрице на РНК-полимеразе II, CPSF способен связаться с сигнальной последовательностью поли-А, Как только она будет транскрибирована, и запустить реакцию полиаденилирования (во время полиаденилирования белок может поддерживать контакт с РНК-полимеразой II). Это изменяет взаимодействие между CPSF, Cst. F и С-концевым доменом РНК-полимеразы II, так что терминация теперь предпочтительна по сравнению с продолжающейся элонгацией.


