Antibiotiki_2012_lektsia_dlya_studentov.ppt
- Количество слайдов: 39

Потенциометрические сенсоры для определения антибиотиков Снесарев Сергей Владимирович аспирант 2 -го года обучения кафедра аналитической химии и химической экологии Научный руководитель: профессор, доктор химических наук Кулапина Елена Григорьевна

Антибиотики как лекарственные средства являются одними из представителей химиотерапевтических лекарственных средств. Химиотерапия – лечение инфекционных заболеваний и злокачественных новообразований с помощью лекарственных средств, обладающих специфическим действием. Химиотерапевтические средства действуют не на макроорганизм, а на микроорганизм – возбудитель соответствующего заболевания (либо на клетки злокачественных опухолей). 2

В зависимости от источника и способа получения химиотерапевтические лекарственные средства можно разделить на 2 группы: • антибиотики – вещества природного происхождения либо вещества полученные путём модификации природных вещества; • синтетические химиотерапевтические средства (сульфаниламиды, нитрофураны, хинолоны, нитроимидазолы и т. д. ) 3

• Определение антибиотиков, как одной из групп лекарственных соединений, получивших широкое распространение, но в то же время, обладающих потенциальной опасностью для здоровья человека, является одной из актуальных проблем современной 4 аналитической химии.

Антибиотики вещества, синтезируемые микроорганизмами и продукты модификации этих веществ, избирательно подавляющие рост патогенных микроорганизмов, низших грибов, а также некоторых вирусов и клеток злокачественных новообразований. Антибиотики растительного происхождения называют фитонцидами. 5
Основные группы антибиотиков ТЕТРАЦИКЛИНЫ АМИНОГЛИКОЗИДЫ НИТРОФУРАНЫ МАКРОЛИДЫ ФТОРХИНОЛОНЫ ГЛИКОПЕПТИДЫ БЕТАЛАКТАМЫ ЛИНКОЗАМИДЫ АНТИБИОТИКИ РИФАМИЦИНЫ
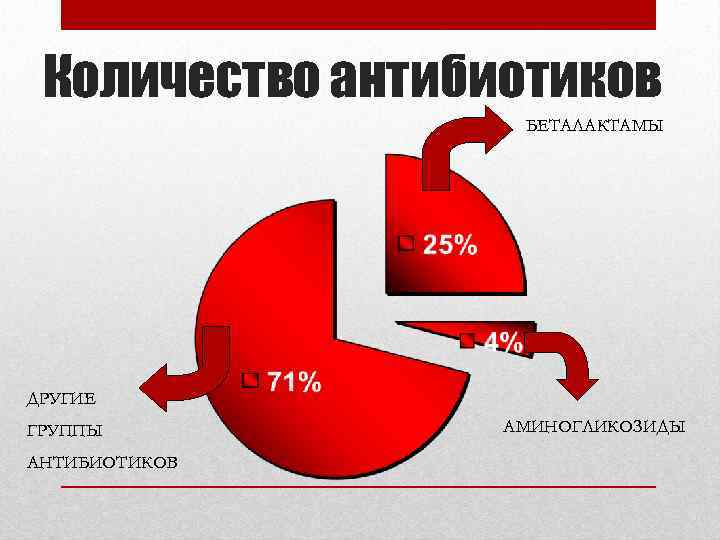
Количество антибиотиков БЕТАЛАКТАМЫ ДРУГИЕ ГРУППЫ АНТИБИОТИКОВ АМИНОГЛИКОЗИДЫ
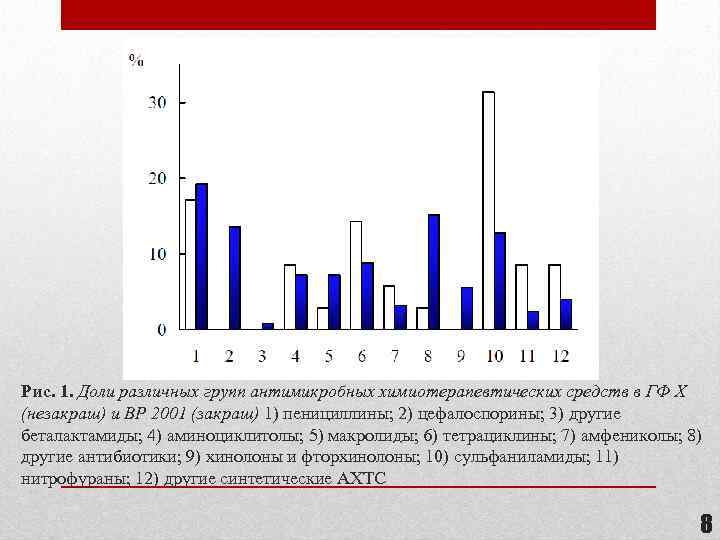
Рис. 1. Доли различных групп антимикробных химиотерапевтических средств в ГФ X (незакраш) и BP 2001 (закраш) 1) пенициллины; 2) цефалоспорины; 3) другие беталактамиды; 4) аминоциклитолы; 5) макролиды; 6) тетрациклины; 7) амфениколы; 8) другие антибиотики; 9) хинолоны и фторхинолоны; 10) сульфаниламиды; 11) нитрофураны; 12) другие синтетические АХТС 8
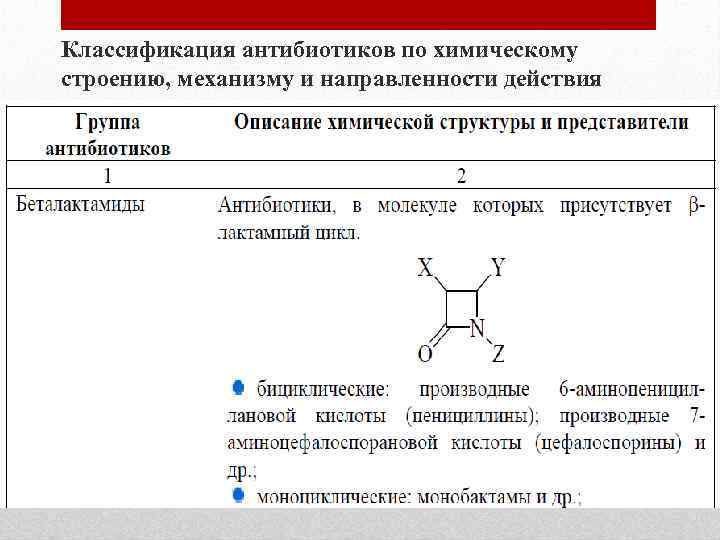
Классификация антибиотиков по химическому строению, механизму и направленности действия 9
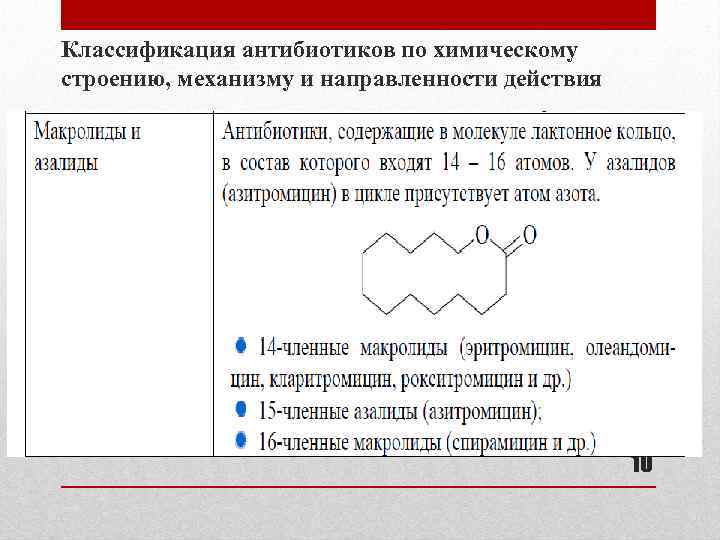
Классификация антибиотиков по химическому строению, механизму и направленности действия 10
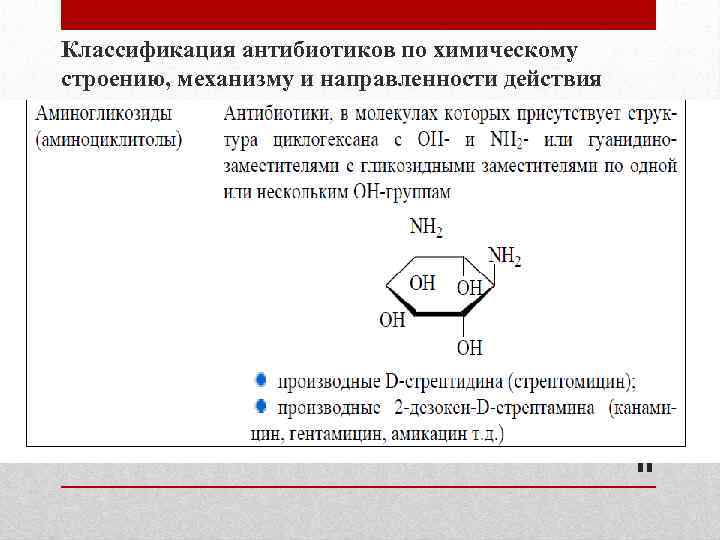
Классификация антибиотиков по химическому строению, механизму и направленности действия 11
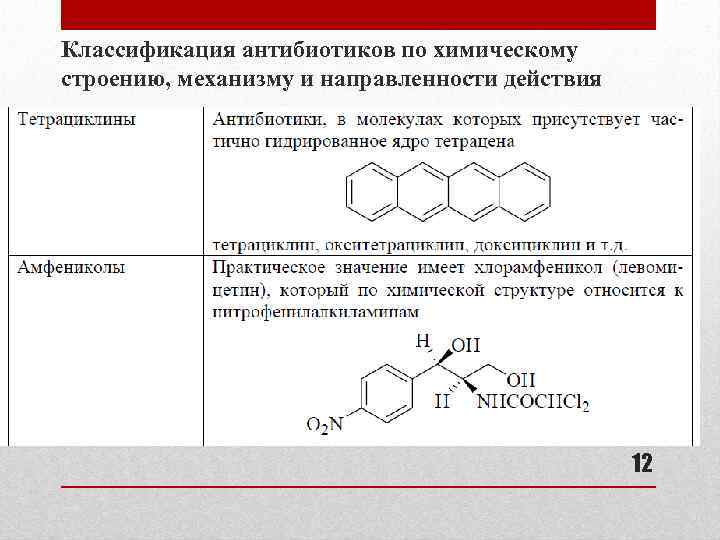
Классификация антибиотиков по химическому строению, механизму и направленности действия 12
БЕТАЛАКТАМЫ ПЕНИЦИЛЛИНЫ ЦЕФАЛОСПОРИНЫ КАРБОПЕНЕМЫ МОНОБАКТАМЫ
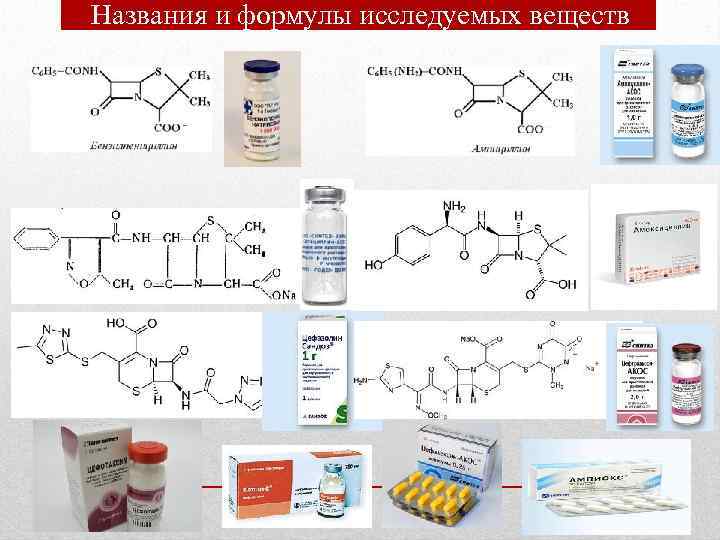
Названия и формулы исследуемых веществ 14
Существуют различные методы определения антибиотиков: вэжх, хм-спектромметрия, микробиологические и др. методы анализа. 15
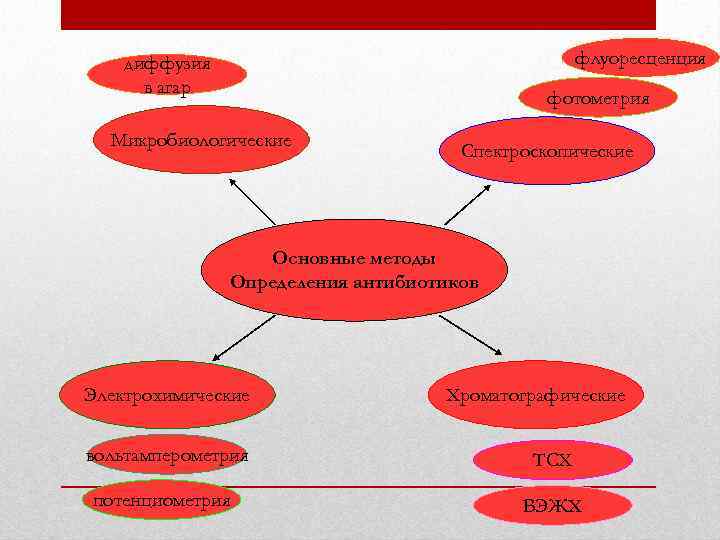
флуоресценция диффузия в агар фотометрия Микробиологические Спектроскопические Основные методы Определения антибиотиков Электрохимические Хроматографические вольтамперометрия ТСХ потенциометрия ВЭЖХ
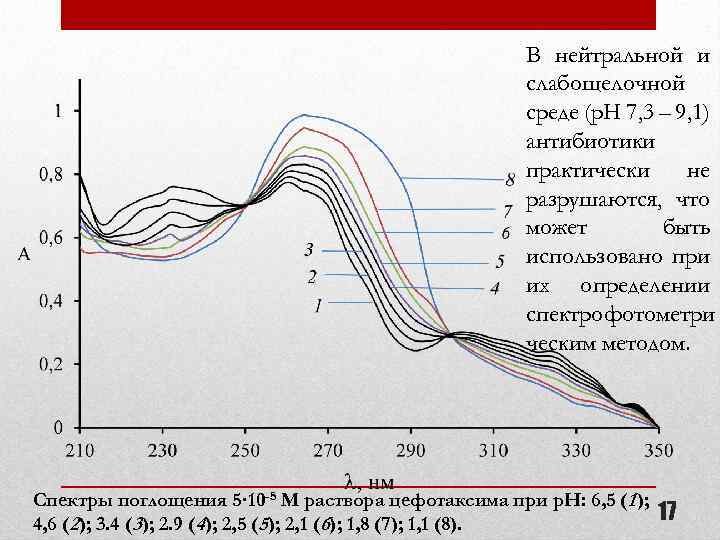
В нейтральной и слабощелочной среде (p. H 7, 3 – 9, 1) антибиотики практически не разрушаются, что может быть использовано при их определении спектрофотометри ческим методом. Спектры поглощения 5· 10 -5 М раствора цефотаксима при р. Н: 6, 5 (1 ); 4, 6 (2); 3. 4 (3); 2. 9 (4); 2, 5 (5); 2, 1 (6); 1, 8 (7); 1, 1 (8). 17

Потенциометрия с ионоселективными электродами является перспективным, экспрессным, простым, доступным и дешевым методом определения пенициллиновых антибиотиков. Потенциометрические β-лактамные сенсоры позволяют детектировать как индивидуальные антибиотики так и их суммарное содержание в различных объектах. 18
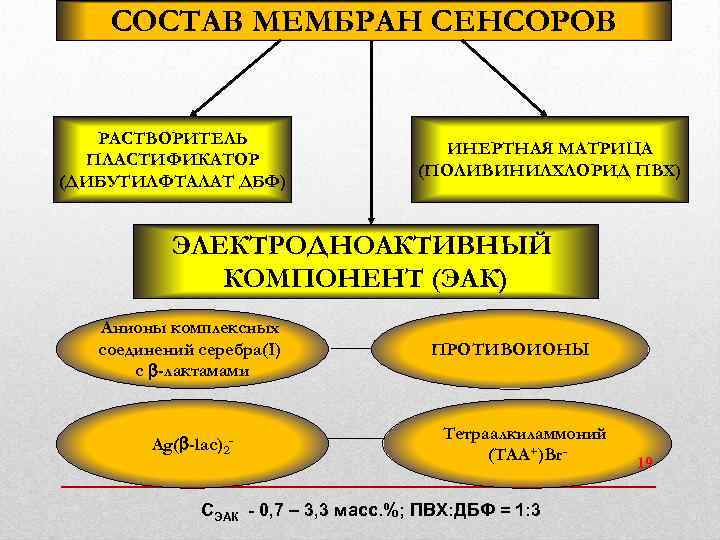
СОСТАВ МЕМБРАН СЕНСОРОВ РАСТВОРИТЕЛЬ ПЛАСТИФИКАТОР (ДИБУТИЛФТАЛАТ ДБФ) ИНЕРТНАЯ МАТРИЦА (ПОЛИВИНИЛХЛОРИД ПВХ) ЭЛЕКТРОДНОАКТИВНЫЙ КОМПОНЕНТ (ЭАК) Анионы комплексных соединений серебра(I) с -лактамами Ag( -lac)2 - ПРОТИВОИОНЫ Тетраалкиламмоний (ТАА+)Br- СЭАК - 0, 7 – 3, 3 масс. %; ПВХ: ДБФ = 1: 3 19
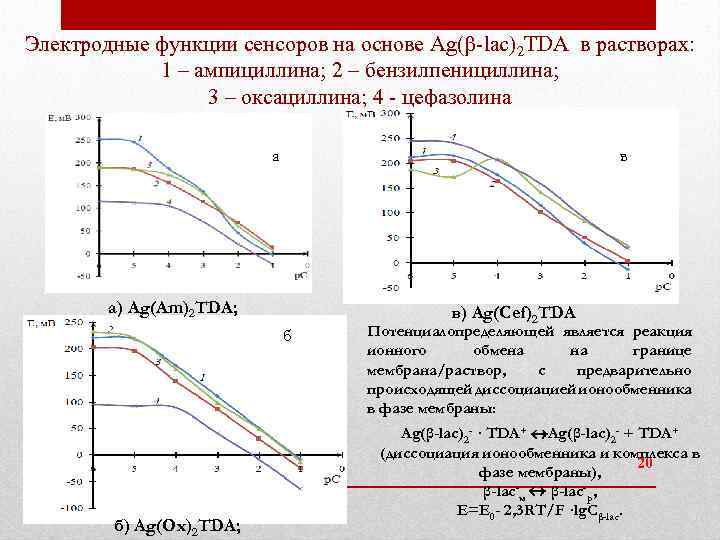
Электродные функции сенсоров на основе Ag( -lac)2 TDA в растворах: 1 – ампициллина; 2 – бензилпенициллина; 3 – оксациллина; 4 - цефазолина а в а) Ag(Am)2 TDA; б б) Ag(Ox)2 TDA; в) Ag(Cef)2 TDA Потенциалопределяющей является реакция ионного обмена на границе мембрана/раствор, с предварительно происходящей диссоциацией ионообменника в фазе мембраны: Ag(β-lac)2 - · TDA+ Ag(β-lac)2 - + TDA+ (диссоциация ионообменника и комплекса в 20 фазе мембраны), β-lac-м β-lac-р, Е=Е 0 - 2, 3 RT/F ·lg. Cβ-lac.
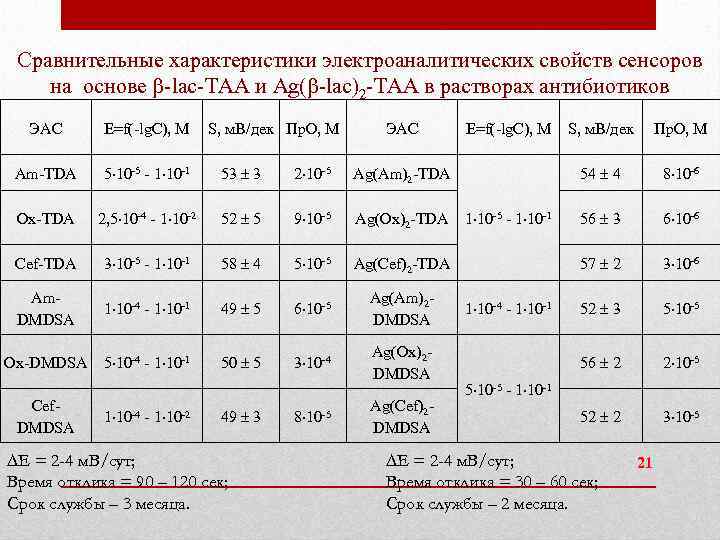
Сравнительные характеристики электроаналитических свойств сенсоров на основе -lac-TAA и Ag( -lac)2 -TAA в растворах антибиотиков ЭАС E=f(-lg. C), M Am-TDA 5 10 -5 - 1 10 -1 53 3 2 10 -5 Ag(Am)2 -TDA Ox-TDA 2, 5 10 -4 - 1 10 -2 52 5 9 10 -5 Ag(Ox)2 -TDA Cef-TDA 3 10 -5 - 1 10 -1 58 4 5 10 -5 Ag(Cef)2 -TDA Am. DMDSA 1 10 -4 - 1 10 -1 49 5 6 10 -5 Ag(Am)2 DMDSA Ox-DMDSA 5 10 -4 - 1 10 -1 50 5 3 10 -4 Ag(Ox)2 DMDSA Cef. DMDSA 1 10 -4 - 1 10 -2 S, м. В/дек Пр. О, М 49 3 E = 2 -4 м. В/сут; Время отклика = 90 – 120 сек; Срок службы – 3 месяца. 8 10 -5 ЭАС Ag(Cef)2 DMDSA E=f(-lg. C), M 8 10 -6 56 3 6 10 -6 57 2 3 10 -6 52 3 5 10 -5 56 2 1 10 -4 - 1 10 -1 Пр. О, М 54 4 1 10 -5 - 1 10 -1 S, м. В/дек 2 10 -5 52 2 3 10 -5 5 10 -5 - 1 10 -1 E = 2 -4 м. В/сут; Время отклика = 30 – 60 сек; Срок службы – 2 месяца. 21

Экспрессное и точное количественное определение β-лактамных антибиотиков в биологических жидкостях организма необходимо для оценки физиологических и биохимических процессов, протекающих в результате их метаболизмов в организме, для корректировки и оптимизации курса лечения. 22

Нами разработаны методики потенциометрического определения β-лактамных антибиотиков в лекарственных и биологических средах, а также общая методология раздельного определения βлактамных антибиотиков в фармацевтических препаратах и модельных растворах с использованием массивов слабоселективных сенсоров и метода искусственных нейронных сетей. 23
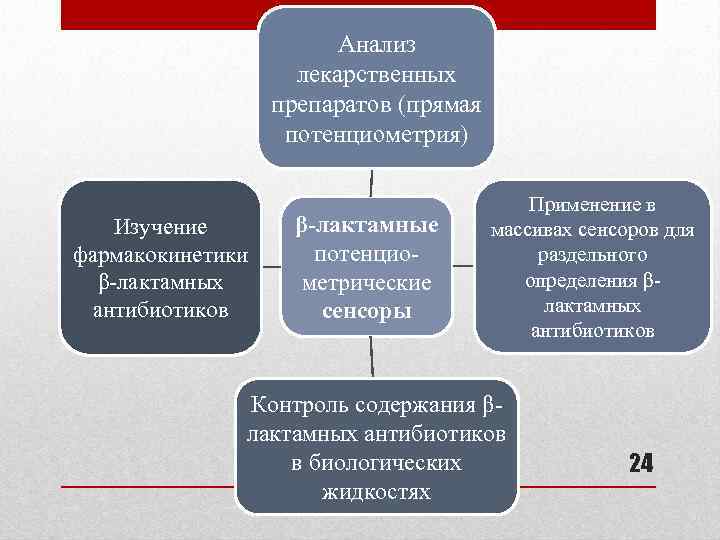
Анализ лекарственных препаратов (прямая потенциометрия) Изучение фармакокинетики β-лактамных антибиотиков β-лактамные потенциометрические сенсоры Применение в массивах сенсоров для раздельного определения βлактамных антибиотиков Контроль содержания βлактамных антибиотиков в биологических жидкостях 24
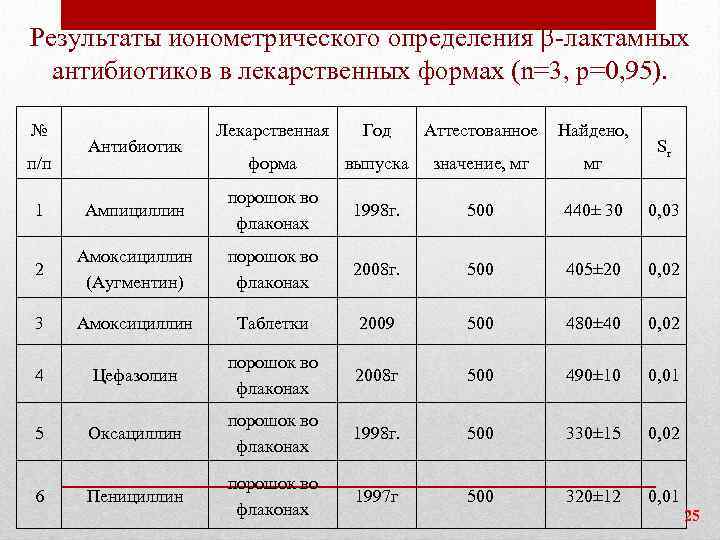
Результаты ионометрического определения -лактамных антибиотиков в лекарственных формах (n=3, р=0, 95). № п/п Антибиотик Лекарственная Год Аттестованное Найдено, форма выпуска значение, мг мг Sr 1 Ампициллин порошок во флаконах 1998 г. 500 440± 30 0, 03 2 Амоксициллин (Аугментин) порошок во флаконах 2008 г. 500 405± 20 0, 02 3 Амоксициллин Таблетки 2009 500 480± 40 0, 02 4 Цефазолин порошок во флаконах 2008 г 500 490± 10 0, 01 5 Оксациллин порошок во флаконах 1998 г. 500 330± 15 0, 02 6 Пенициллин порошок во флаконах 1997 г 500 320± 12 0, 01 25
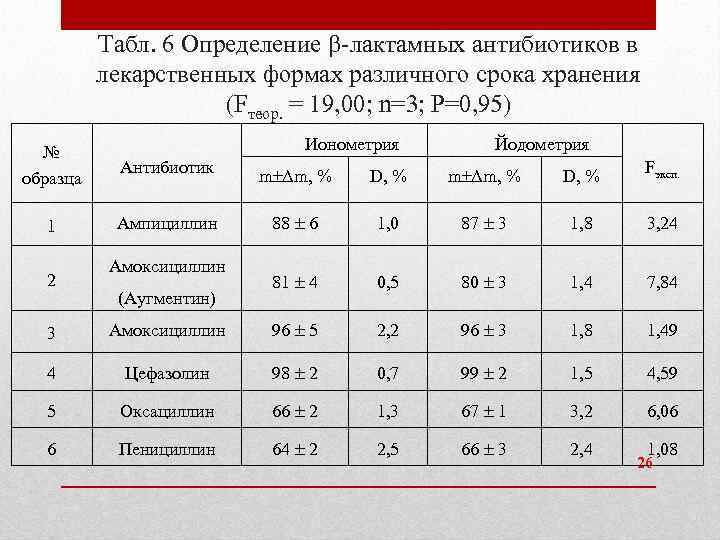
Табл. 6 Определение -лактамных антибиотиков в лекарственных формах различного срока хранения (Fтеор. = 19, 00; n=3; P=0, 95) Ионометрия № образца Антибиотик 1 Ампициллин 2 Амоксициллин (Аугментин) Йодометрия m Δm, % D, % Fэксп. 88 6 1, 0 87 3 1, 8 3, 24 81 4 0, 5 80 3 1, 4 7, 84 3 Амоксициллин 96 5 2, 2 96 3 1, 8 1, 49 4 Цефазолин 98 2 0, 7 99 2 1, 5 4, 59 5 Оксациллин 66 2 1, 3 67 1 3, 2 6, 06 6 Пенициллин 64 2 2, 5 66 3 2, 4 1, 08 26

Компонентами жидкости ротовой полости являются хлориды, карбонаты, фосфаты и другие соли натрия, кальция и магния. Концентрация электроли тов неодинакова. Жидкость ротовой полости содержит органические вещест ва, которых в 2 -3 раза больше, чем минеральных солей В составе жидкости ротовой полости выделяются различные белки, свободные аминокислоты, некоторые углеводы, мочевина, аммиак и другие вещества. ЖРП достаточно богата ферментами, она обладает способностью ак тивно расщеплять углеводы 27

Методика пробоподготовки ЖРП. Сбор ЖРП производится не ранее, чем через 15 мин. после еды, перед сбором рекомендуется прополоскать ро товую полость. В чистые полиэтиленовые пробирки собирают ЖРП, центрифугируют ее в течение 10 мин. при скорости 3500 об/мин для осаждения твердых остатков пищи. Для удаления остаточных белков проводят их осаждение. В супернатант V = 7, 5 мл вводят 0, 5 мл 0, 12 M Na. OH, 2 мл 0, 03 М Zn. SO 4 и вносят стандартные растворы антибиотика, центрифугируют еще 5 минут. Разведение составляет ¼. Надосадочную жидкость отбирают в ячейку (3 -5 мл), погружают электрод и при перемешивании измеряют величину ЭДС. Предварительно электрод кондиционируют в ЖРП без антибиотика. Электрод сравнения – хлоридсеребряный.
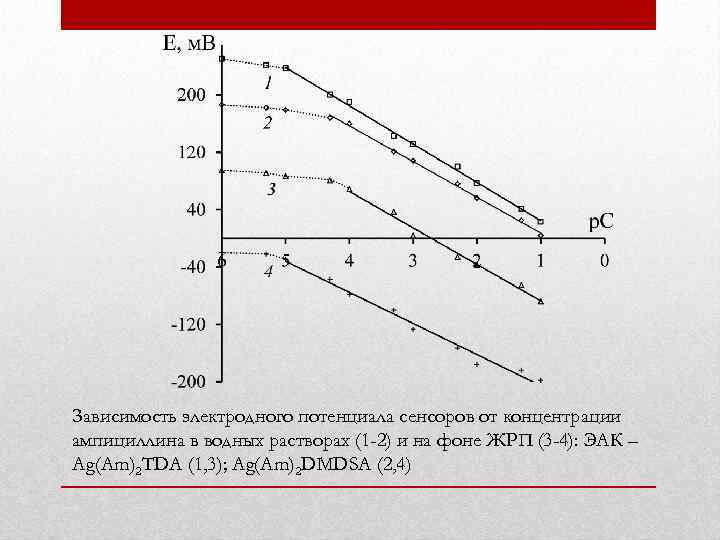
Зависимость электродного потенциала сенсоров от концентрации ампициллина в водных растворах (1 -2) и на фоне ЖРП (3 -4): ЭАК – Ag(Am)2 TDA (1, 3); Ag(Am)2 DMDSA (2, 4)
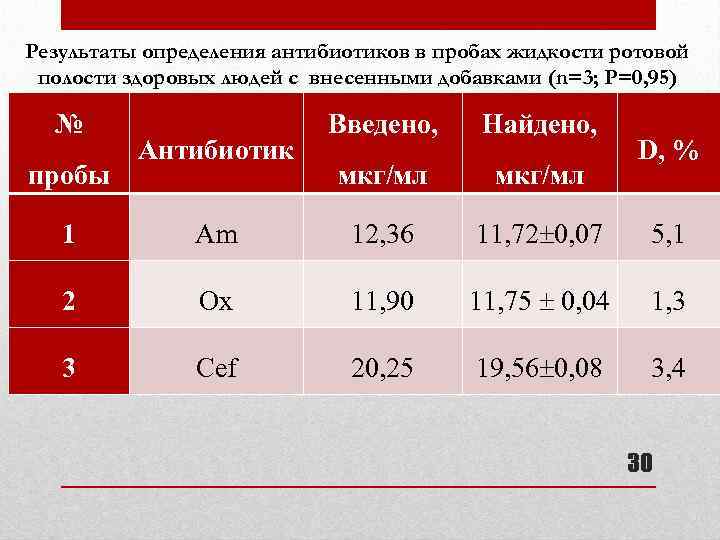
Результаты определения антибиотиков в пробах жидкости ротовой полости здоровых людей с внесенными добавками (n=3; P=0, 95) № пробы Антибиотик Введено, Найдено, мкг/мл D, % 1 Am 12, 36 11, 72 0, 07 5, 1 2 Ox 11, 90 11, 75 0, 04 1, 3 3 Cef 20, 25 19, 56 0, 08 3, 4 30
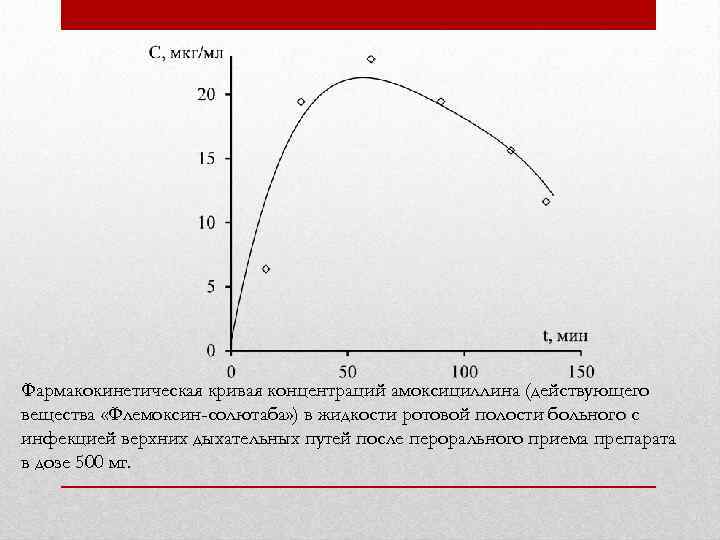
Фармакокинетическая кривая концентраций амоксициллина (действующего вещества «Флемоксин-солютаба» ) в жидкости ротовой полости больного с инфекцией верхних дыхательных путей после перорального приема препарата в дозе 500 мг.
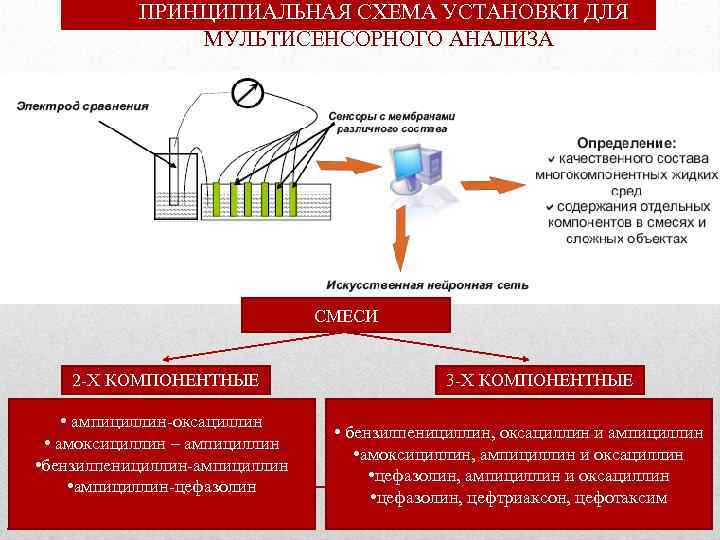
ПРИНЦИПИАЛЬНАЯ СХЕМА УСТАНОВКИ ДЛЯ МУЛЬТИСЕНСОРНОГО АНАЛИЗА CМЕСИ 2 -Х КОМПОНЕНТНЫЕ • ампициллин-оксациллин • амоксициллин – ампициллин • бензилпенициллин-ампициллин • ампициллин-цефазолин 3 -Х КОМПОНЕНТНЫЕ • бензилпенициллин, оксациллин и ампициллин • амоксициллин, ампициллин и оксациллин 32 • цефазолин, ампициллин и оксациллин • цефазолин, цефтриаксон, цефотаксим
33
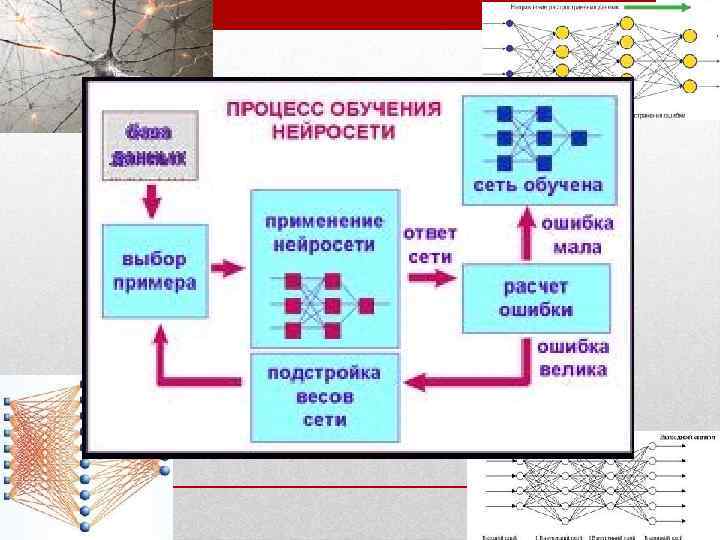

• Для обработки аналитических сигналов от массива сенсоров использовали метод искусственных нейронных сетей (ИНС). • Применялась ИНС с обратным распространением ошибок, состоящая из: ü 10 нейронов в первом слое; ü 6 нейронов во втором слое; ü 3 нейронов в третьем слое. • активационная функция – сигмоида, скорость обучения 0, 1; момент 0, 9; число эпох 20000. • Число калибровочных растворов, используемых для обучения нейронной сети, составляло 15 -40. 35
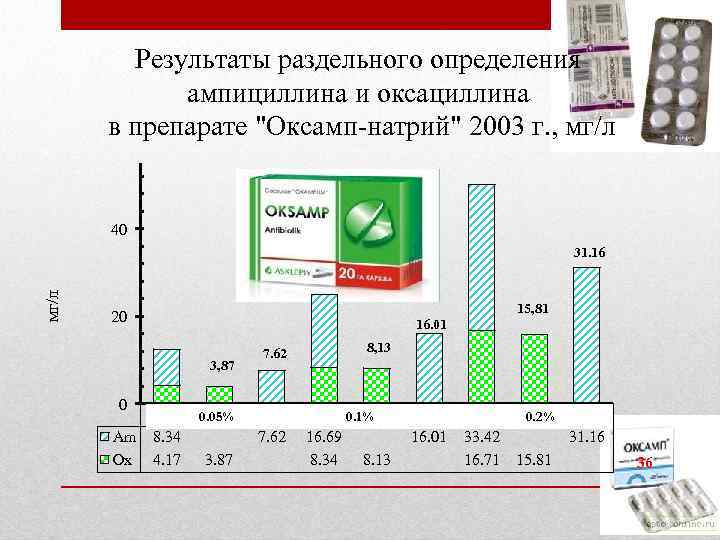
Результаты раздельного определения ампициллина и оксациллина в препарате "Оксамп-натрий" 2003 г. , мг/л 40 мг/л 31. 16 20 16. 01 3, 87 0 Am Ox 15, 81 1 8. 34 4. 17 2 0. 05% 3. 87 7. 62 8, 13 3 7. 62 4 0. 1%5 16. 69 8. 34 8. 13 6 16. 01 7 33. 42 16. 71 8 0. 2% 15. 81 9 31. 16 36
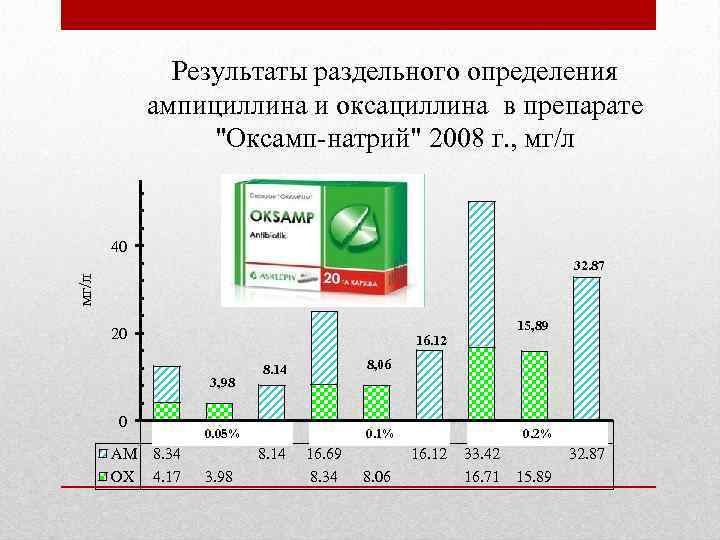
Результаты раздельного определения ампициллина и оксациллина в препарате "Оксамп-натрий" 2008 г. , мг/л 40 мг/л 32. 87 20 16. 12 3, 98 0 1 AM 8. 34 ОX 4. 17 15, 89 2 0. 05% 3. 98 8, 06 8. 14 3 8. 14 4 16. 69 8. 34 5 0. 1% 8. 06 6 16. 12 7 33. 42 16. 71 8 0. 2% 15. 89 9 32. 87

Антибиотики применяются в медицине, ветеринарии, пищевой промышленности при консервировании, для обработки пищевых продуктов при их транспортировке. В связи с этим требуется контроль за содержанием антибиотиков в лекарственных веществах, биологических жидкостях организма человека и животных, продуктах питания, сточных водах фармацевтических предприятий и других объектах.

Для количественного определения антибиотиков применяются микробиологические, различные варианты хроматографических методов (ВЭЖХ, ионообменная, хромато-массспектрометрия), спектрофотометрические, кинетические, флуориметрические, хемилюминесцентные, инверсионная вольтамперометрия, электрокаталитическое определение с модифицированными электродами, потенциометрия с ионоселективными электродами и импринтированными материалами. Каждый метод имеет свои преимущества и недостатки. Выбор метода зависит от доступности оборудования, наличия персонала, знающего данное оборудование, от количества анализов и их частоты, степени точности и других обстоятельств.
Antibiotiki_2012_lektsia_dlya_studentov.ppt