Positiivsed RNA viirused (loeng 3).ppt
- Количество слайдов: 56
 Positiivsed RNA viirused 2 Togaviridae, Coronaviridae ja Flaviviridae
Positiivsed RNA viirused 2 Togaviridae, Coronaviridae ja Flaviviridae
 Sugukonnas on kaks perekonda: - Alphavirus (28 liiki), esindajad Sindbis viirus (SIN), Semliki Forest viirus (SFV), Chikungunya viirus (CHIKV). Alphaviirused (v. a. kalade alphaviirused) on putuklevikuga viirused ning nakatavad ka oma lülijalgseid vektoreid (moskiitod, lestad ja puugid). Lülijalgsetele vektoritele on alphaviiruste infektsioon asümptomaatiline. - Rubivirus, ainus tuntud esindaja on rubella viirus (RUB, punetiste viirus). Ei oma putukvektorit, inimene on ainus peremees. Virion. Togaviridae sugukonda kuuluvaid viiruseid iseloomustavad membraaniga sfäärilised virionid (sugukonna nimetus tuleneb ladina keelsest sõnast toga). Virionide diameeter on ca 70 nm ja temas paiknev kapsiid (ca 40 nm) koosneb 240 -st kapsiidivalgu molekulist (T=4). Alphaviiruste membraan pärineb raku plasmamembraanist ja selles asuvad glükoproteiinidest koosnevad ”ogad” (alphaviirustel E 1 ja E 2 valgud, 80 x 3 koopiat kummastki). Sugukond Togaviridae.
Sugukonnas on kaks perekonda: - Alphavirus (28 liiki), esindajad Sindbis viirus (SIN), Semliki Forest viirus (SFV), Chikungunya viirus (CHIKV). Alphaviirused (v. a. kalade alphaviirused) on putuklevikuga viirused ning nakatavad ka oma lülijalgseid vektoreid (moskiitod, lestad ja puugid). Lülijalgsetele vektoritele on alphaviiruste infektsioon asümptomaatiline. - Rubivirus, ainus tuntud esindaja on rubella viirus (RUB, punetiste viirus). Ei oma putukvektorit, inimene on ainus peremees. Virion. Togaviridae sugukonda kuuluvaid viiruseid iseloomustavad membraaniga sfäärilised virionid (sugukonna nimetus tuleneb ladina keelsest sõnast toga). Virionide diameeter on ca 70 nm ja temas paiknev kapsiid (ca 40 nm) koosneb 240 -st kapsiidivalgu molekulist (T=4). Alphaviiruste membraan pärineb raku plasmamembraanist ja selles asuvad glükoproteiinidest koosnevad ”ogad” (alphaviirustel E 1 ja E 2 valgud, 80 x 3 koopiat kummastki). Sugukond Togaviridae.
 Alphaviiruseid leidub kõikjal maailmas, v. a. Anterktikas. Erinevad alphaviirused nakatavad imetajaid, linde ja kalu; peale selle nakatatakse ka oma selgrootuid vektoreid. Alphaviirused põhjustavad palavikku, löövet ja artriiti, kuid mitmetel alphaviirustel on võime põhjustada ka letaalset entsefaliiti (VEEV). Seepärast on looduslikud alphaviirused olulised patogeenid (VEEV on näiteks BSL 4 taseme patogeen; CHIKV BSL 3 taseme patogeen). SIN ja SFV laboratoorsed tüved on apatogeensed ja on tähtsad nii mudelobjektidena (viroloogia ja rakubioloogia) kui ka geenitehnoloogia (vaktsiinid, vähiteraapia) süsteemidena Alphaviiruste levik, peremehed SIN levikuala
Alphaviiruseid leidub kõikjal maailmas, v. a. Anterktikas. Erinevad alphaviirused nakatavad imetajaid, linde ja kalu; peale selle nakatatakse ka oma selgrootuid vektoreid. Alphaviirused põhjustavad palavikku, löövet ja artriiti, kuid mitmetel alphaviirustel on võime põhjustada ka letaalset entsefaliiti (VEEV). Seepärast on looduslikud alphaviirused olulised patogeenid (VEEV on näiteks BSL 4 taseme patogeen; CHIKV BSL 3 taseme patogeen). SIN ja SFV laboratoorsed tüved on apatogeensed ja on tähtsad nii mudelobjektidena (viroloogia ja rakubioloogia) kui ka geenitehnoloogia (vaktsiinid, vähiteraapia) süsteemidena Alphaviiruste levik, peremehed SIN levikuala
 Alphaviiruse zoonootiline tsükkel Viiruseid, mis looduses tsirkuleerivad lülijalgsete vektorite ja selgroogsete peremeeste vahel, nimetatakse arboviirusteks (arthropode borne virus). Arboviirused ei ole süstemaatiline ühik, kuid kajastab nende viiruste bioloogia olulist bioloogilist aspekti. Alphaviirused on tüüpilised arboviirused. Neid iseloomustab: -Infektsioonide hooajalisus (suvine aega) ja tsüklilisus (SIN epideemia kordub 7 -aastase perioodilisusega) -Infektsioon vektoris on asümptomaatiline -Levik ülekandevektori kaudu on ainus looduses esinev ülekandevorm -Levik inimesele on juhuslik (tupikperemees) ja on seotud muutustega moskiitode populatsioonis.
Alphaviiruse zoonootiline tsükkel Viiruseid, mis looduses tsirkuleerivad lülijalgsete vektorite ja selgroogsete peremeeste vahel, nimetatakse arboviirusteks (arthropode borne virus). Arboviirused ei ole süstemaatiline ühik, kuid kajastab nende viiruste bioloogia olulist bioloogilist aspekti. Alphaviirused on tüüpilised arboviirused. Neid iseloomustab: -Infektsioonide hooajalisus (suvine aega) ja tsüklilisus (SIN epideemia kordub 7 -aastase perioodilisusega) -Infektsioon vektoris on asümptomaatiline -Levik ülekandevektori kaudu on ainus looduses esinev ülekandevorm -Levik inimesele on juhuslik (tupikperemees) ja on seotud muutustega moskiitode populatsioonis.
 Alphaviiruste genoom. Alphaviiruste genoomne RNA on ca 12 kb pikkune. Teda iseloomustab: - Genoomi 5’-otsas asub cap 0 -struktuur; - Genoomi 3’-otsas asub polü(A) (umbes 70 jääki) järjestus. Alphaviiruste genoomid koosnevad kahest moodulist: - 5’-terminaalne 2/3 genoomi kodeerib mittestruktuurseid valke (NSP, ekspresseeruvad otse genoomilt). - 3’-poolne 1/3 genoomi kodeerib struktuurseid valke (SP) ja ekspresseerub sg. RNA kaudu. Sg RNA sünteesitakse infektsiooni käigus (virionides seda ei ole) subgenoomselt promooterilt viiruse Rd. Rp poolt. Togaviiruste sg. RNA on capeeritud ja polüadenüleeritud.
Alphaviiruste genoom. Alphaviiruste genoomne RNA on ca 12 kb pikkune. Teda iseloomustab: - Genoomi 5’-otsas asub cap 0 -struktuur; - Genoomi 3’-otsas asub polü(A) (umbes 70 jääki) järjestus. Alphaviiruste genoomid koosnevad kahest moodulist: - 5’-terminaalne 2/3 genoomi kodeerib mittestruktuurseid valke (NSP, ekspresseeruvad otse genoomilt). - 3’-poolne 1/3 genoomi kodeerib struktuurseid valke (SP) ja ekspresseerub sg. RNA kaudu. Sg RNA sünteesitakse infektsiooni käigus (virionides seda ei ole) subgenoomselt promooterilt viiruse Rd. Rp poolt. Togaviiruste sg. RNA on capeeritud ja polüadenüleeritud.
 Seondumine rakule ja sisenemine rakku Alphaviiruste infektsioonitsükkel on suhteliselt kiire (ca 6 tundi imetajate ja 1520 tundi putukate rakkudes) ja neile on iseloomulik lai peremeestering. See on võimalik, kuna rakkudesse sisenemiseks kasutatakse alternatiivseid retseptoreid. Näidatud on, et SIN retseptoriteks on 67 k. Da laminin-retseptor, hepariin-sulfaat, 63 k. Da valk (linnu rakud), 74 ja 110 k. Da valgud (neuronid). Mingid retseptorid peavad olema ka lülijalgsete vektorite rakkudel. 2011 aastal näidati et nii putuka- kui imatajarakkudes kasutab SIN retseptoriks natural resistance-associated macrophage protein (NRAMP) valku. Alphaviiruse antiretseptoriks on E 2 glükoproteiin. Retseptor-antiretseptor interaktsioon indutseerib virionis konformatsioonilised muutused, mis on olulised partikli edasisel lahtipakkimisel. Rakku sisenemine toimub retseptor-vahendatud endotsütoosi teel, viiruse membraani liitumine vesikulide membraaniga on p. H-ist sõltuv protsess: happelistes tingimustes (p. H 5 -6) E 1: E 2 dimeerid dissotsieeruvad ja moodustuvad E 1 trimeerid, mis on aktiivseks fusion-valguks. Membraanide liitumise tulemusena vabaneb viiruse kapsiid tsütoplasmasse. Tsütoplasmas toimub nukleokapsiidi lahtiharutamine raku ribosoomide poolt. Selle tulemusena vabaneb viiruse genoomne RNA raku tsütoplasmasse. Nakatanud rakud on superinfektsiooni suhtes resistentsed (alates 0. 5 -1 tundi peale primaarset infektsiooni).
Seondumine rakule ja sisenemine rakku Alphaviiruste infektsioonitsükkel on suhteliselt kiire (ca 6 tundi imetajate ja 1520 tundi putukate rakkudes) ja neile on iseloomulik lai peremeestering. See on võimalik, kuna rakkudesse sisenemiseks kasutatakse alternatiivseid retseptoreid. Näidatud on, et SIN retseptoriteks on 67 k. Da laminin-retseptor, hepariin-sulfaat, 63 k. Da valk (linnu rakud), 74 ja 110 k. Da valgud (neuronid). Mingid retseptorid peavad olema ka lülijalgsete vektorite rakkudel. 2011 aastal näidati et nii putuka- kui imatajarakkudes kasutab SIN retseptoriks natural resistance-associated macrophage protein (NRAMP) valku. Alphaviiruse antiretseptoriks on E 2 glükoproteiin. Retseptor-antiretseptor interaktsioon indutseerib virionis konformatsioonilised muutused, mis on olulised partikli edasisel lahtipakkimisel. Rakku sisenemine toimub retseptor-vahendatud endotsütoosi teel, viiruse membraani liitumine vesikulide membraaniga on p. H-ist sõltuv protsess: happelistes tingimustes (p. H 5 -6) E 1: E 2 dimeerid dissotsieeruvad ja moodustuvad E 1 trimeerid, mis on aktiivseks fusion-valguks. Membraanide liitumise tulemusena vabaneb viiruse kapsiid tsütoplasmasse. Tsütoplasmas toimub nukleokapsiidi lahtiharutamine raku ribosoomide poolt. Selle tulemusena vabaneb viiruse genoomne RNA raku tsütoplasmasse. Nakatanud rakud on superinfektsiooni suhtes resistentsed (alates 0. 5 -1 tundi peale primaarset infektsiooni).
 Alphaviiruste replikaas – mittestruktuursed valgud. Alphaviiruste replikaasi valgud transleeritakse genoomselt RNA-lt ühtse polüproteiin kujul. Polüproteiin protsessitakse valmis ns-valkudeks viiruse proteaasi poolt (täpselt reguleeritud protsess). Alphaviiruste NS-valgud on polüfunktsionaalsed valgud: NSP 1 on metüül- ja guanülüültransferaas, mis teostab viirus-spetsiifilist cap- sünteesi. Peale selle osaleb ns. P 1 negatiivse polaarsusega RNA sünteesi initsieerimisel ja seondab alphaviiruse replikatsioonikompleksi rakumembraanidele. . NSP 2 on NTPase, RNA helikaas, RNA-trifosfotaas ja tsüsteiin-proteaas. Ns. P 2 reguleerib viiruse replikatsiooni (negatiivsete ahelate ja sg. RNA sünteesi) ning osaleb nakatatud rakkudes raku-spetsiifilise transkriptsiooni ja translatsiooni mahasurumises. NSP 3 on osaleb viiruse replikaasi komplekside (CPV-de ja sfäärulite) moodustamises ning NS polüproteiini protsessingu reguleerimises. NSP 4 on alphaviiruste Rd. Rp, sisaldab polümeraaset motiivi GDD. Rakus on NSP 4 suhteliselt ebastabiilne ja suur osa temast lagundatakse ubiquitiin-proteosoom mehhanismi vahendusel (see võib olla viirusele vajalik NSP 4 taseme vähendamiseks). Vähemalt osa kõigist NS-valkudest moodustab nakatatud rakkudes membraanseoselise mittekovalentse kompleksi, mis on alphaviiruse hiliseks replikaasiks (varajases replikaasis on olulised ka NS-polüproteiini protsessingu vahevormid).
Alphaviiruste replikaas – mittestruktuursed valgud. Alphaviiruste replikaasi valgud transleeritakse genoomselt RNA-lt ühtse polüproteiin kujul. Polüproteiin protsessitakse valmis ns-valkudeks viiruse proteaasi poolt (täpselt reguleeritud protsess). Alphaviiruste NS-valgud on polüfunktsionaalsed valgud: NSP 1 on metüül- ja guanülüültransferaas, mis teostab viirus-spetsiifilist cap- sünteesi. Peale selle osaleb ns. P 1 negatiivse polaarsusega RNA sünteesi initsieerimisel ja seondab alphaviiruse replikatsioonikompleksi rakumembraanidele. . NSP 2 on NTPase, RNA helikaas, RNA-trifosfotaas ja tsüsteiin-proteaas. Ns. P 2 reguleerib viiruse replikatsiooni (negatiivsete ahelate ja sg. RNA sünteesi) ning osaleb nakatatud rakkudes raku-spetsiifilise transkriptsiooni ja translatsiooni mahasurumises. NSP 3 on osaleb viiruse replikaasi komplekside (CPV-de ja sfäärulite) moodustamises ning NS polüproteiini protsessingu reguleerimises. NSP 4 on alphaviiruste Rd. Rp, sisaldab polümeraaset motiivi GDD. Rakus on NSP 4 suhteliselt ebastabiilne ja suur osa temast lagundatakse ubiquitiin-proteosoom mehhanismi vahendusel (see võib olla viirusele vajalik NSP 4 taseme vähendamiseks). Vähemalt osa kõigist NS-valkudest moodustab nakatatud rakkudes membraanseoselise mittekovalentse kompleksi, mis on alphaviiruse hiliseks replikaasiks (varajases replikaasis on olulised ka NS-polüproteiini protsessingu vahevormid).
 Alphaviiruste RNA replikatsioon Replikatsiooni cis-järjestusted (polümeraasi seondumise kohad) paiknevad genoomi otstes. Järjestus NS- ja S moodulite vahel on sg. RNA promooteriks (19 b üla- ja 5 b allpool sg. RNA initsiatsioonisaidist). Replikatsioonil osalevad viiruse ns-valgud ja polüproteiinid. Peremeesraku valgulistest faktoritest, mis osalevad alphviiruste replikatsioonis, on praeguseks ajaks väga vähe teada. On andmeid, et selgroogsete rakkudes osaleb alphaviiruste replikatsioonis (millisel moel ei ole teada) raku La valk, mis seondub tugevasti ja spetsiifiliselt genoomi 3’-otsaga). Geneetiline analüüs näitab et viiruse replikatsiooni mõjutab mitusada erinevat valku Alphaviiruste replikatsioon on reguleeritud NS polüproteiini protsessingu kaudu. Replikatsiooniga kaasneb spetsiifiliste tsütopaatiliste vakuoolide (modifitseeritud endo- ja lüsosoomid) moodustumine rakus. Need vakuoolid on viiruse RNA replikatsiooni kohtadeks. Elektronmikroskoopilised uuringud on näidanud, et vakuoolid sisaldavad membraanseid struktuure, mida nimetatakse sfäärulideks (diameeter ca 50 nm) ja milles lokaliseeruvad alphaviiruste NS valgud ning toimub viiruse RNA süntees.
Alphaviiruste RNA replikatsioon Replikatsiooni cis-järjestusted (polümeraasi seondumise kohad) paiknevad genoomi otstes. Järjestus NS- ja S moodulite vahel on sg. RNA promooteriks (19 b üla- ja 5 b allpool sg. RNA initsiatsioonisaidist). Replikatsioonil osalevad viiruse ns-valgud ja polüproteiinid. Peremeesraku valgulistest faktoritest, mis osalevad alphviiruste replikatsioonis, on praeguseks ajaks väga vähe teada. On andmeid, et selgroogsete rakkudes osaleb alphaviiruste replikatsioonis (millisel moel ei ole teada) raku La valk, mis seondub tugevasti ja spetsiifiliselt genoomi 3’-otsaga). Geneetiline analüüs näitab et viiruse replikatsiooni mõjutab mitusada erinevat valku Alphaviiruste replikatsioon on reguleeritud NS polüproteiini protsessingu kaudu. Replikatsiooniga kaasneb spetsiifiliste tsütopaatiliste vakuoolide (modifitseeritud endo- ja lüsosoomid) moodustumine rakus. Need vakuoolid on viiruse RNA replikatsiooni kohtadeks. Elektronmikroskoopilised uuringud on näidanud, et vakuoolid sisaldavad membraanseid struktuure, mida nimetatakse sfäärulideks (diameeter ca 50 nm) ja milles lokaliseeruvad alphaviiruste NS valgud ning toimub viiruse RNA süntees.
 Alfaviiruse genoom ja valguekspressioon
Alfaviiruse genoom ja valguekspressioon
 SFV replikatsioon toimub modifitseeritud lüsosoomidel ja endosoomidel ns. P 1 ns. P 3
SFV replikatsioon toimub modifitseeritud lüsosoomidel ja endosoomidel ns. P 1 ns. P 3
 Sfäärul: viirus-indutseeritud miniorganell Alfaviirused, nagu ka paljud muud positiivse polaarsusega RNA viirused indutseerivad raku membraanidel spetsiifiliste struktuuride – sfäärulite moodustamise. Sfäärulid on replikatsioonikompleksi (replikaasi valgud ja replikatiivsed RNA vormid) paiknemise kohaks ja on erinevatel viirustel sarnase välimusega (kas ka sarnaste funktsioonidega? ). Alphaviiruste puhul moodustuvad sfäärulid algselt raku plasmamembraanil ja sisenevad rakku endotsütoosi raja kaudu.
Sfäärul: viirus-indutseeritud miniorganell Alfaviirused, nagu ka paljud muud positiivse polaarsusega RNA viirused indutseerivad raku membraanidel spetsiifiliste struktuuride – sfäärulite moodustamise. Sfäärulid on replikatsioonikompleksi (replikaasi valgud ja replikatiivsed RNA vormid) paiknemise kohaks ja on erinevatel viirustel sarnase välimusega (kas ka sarnaste funktsioonidega? ). Alphaviiruste puhul moodustuvad sfäärulid algselt raku plasmamembraanil ja sisenevad rakku endotsütoosi raja kaudu.
 Sfääruli moodustamise mudel (SIN) Sfäärulid moodustuvad plasmamembraanil varajase replikatsiooni käigus. Sfääruli moodustamine vajab ensümaatiliselt aktiivset ns. P 4 ja P 123 valke Sfääruli moodustamine vajab replitseeritava maatritsi olemasolu (ainult valkudest ei piisa). Seega võib eeldada, et ds. RNA süntees on vajalik sfääruli moodustamise käivitamiseks Replikaasi valgud paiknevad ilmselt sfääruli kaelas, mitte üle kogu sisepinna (teistel viiruse rühmadel on see ilmelt teiseti) Sfäärulid sisenevad raku tsütoplasmasse endotsütoosi teel. See pole viirusele absoluutselt vajalik ja võib erineda eri alphaviiruste vahel
Sfääruli moodustamise mudel (SIN) Sfäärulid moodustuvad plasmamembraanil varajase replikatsiooni käigus. Sfääruli moodustamine vajab ensümaatiliselt aktiivset ns. P 4 ja P 123 valke Sfääruli moodustamine vajab replitseeritava maatritsi olemasolu (ainult valkudest ei piisa). Seega võib eeldada, et ds. RNA süntees on vajalik sfääruli moodustamise käivitamiseks Replikaasi valgud paiknevad ilmselt sfääruli kaelas, mitte üle kogu sisepinna (teistel viiruse rühmadel on see ilmelt teiseti) Sfäärulid sisenevad raku tsütoplasmasse endotsütoosi teel. See pole viirusele absoluutselt vajalik ja võib erineda eri alphaviiruste vahel
 Replikatsiooni regulatsioon Varajane replikatsioon (negatiivsete ahelate süntees) toimub 0. 5 -3. 5 tundi peale infektsiooni. Varajane replikatsioon on sõltuv pidevast valgusünteesist. Vaba proteaasi (ns. P 2) kontsentratsioon rakus on sellel ajal veel madal ja polüproteiin(id) on seepärast suhteliselt stabiilsed. Varajase replikaasina funktsioneerib lühikese pooleelueaga (ca 20 min, selle määrab ära P 123 auto-proteolüüsi kiirus) kompleks, mis koosneb polüproteiinist P 123 ja ns. P 4 valgust (võimalik ka raku faktorite osalemine). ds. RNA süntees on ka sfäärulite moodustamise eelduseks Hiline replikatsioon (3 -6 tundi peale infektsiooni) ei ole sõltuv pidevast valgusünteesist ja toimub juba valminud sfäärulites. Hiline replikaas moodustub varajase replikaasi edasise protsessingu tulemusena ja kujutab endast täielikult protsessitud ns. P 1, 2, 3 ja 4 stabiilset kompleksi ning sünteesib nii genoomseid kui ka subgenoomseid positiivseid RNA ahelaid. Kuna hilises infektsioonis on NSP 2 proteaasi kontsentratsioon nakatatud rakkudes kõrge, siis väheneb järsult de nova sünteesitud polüproteiinide stabiilsus ja uusi varajase (ega ka hilise) replikaasi komplekse juurde ei moodustata.
Replikatsiooni regulatsioon Varajane replikatsioon (negatiivsete ahelate süntees) toimub 0. 5 -3. 5 tundi peale infektsiooni. Varajane replikatsioon on sõltuv pidevast valgusünteesist. Vaba proteaasi (ns. P 2) kontsentratsioon rakus on sellel ajal veel madal ja polüproteiin(id) on seepärast suhteliselt stabiilsed. Varajase replikaasina funktsioneerib lühikese pooleelueaga (ca 20 min, selle määrab ära P 123 auto-proteolüüsi kiirus) kompleks, mis koosneb polüproteiinist P 123 ja ns. P 4 valgust (võimalik ka raku faktorite osalemine). ds. RNA süntees on ka sfäärulite moodustamise eelduseks Hiline replikatsioon (3 -6 tundi peale infektsiooni) ei ole sõltuv pidevast valgusünteesist ja toimub juba valminud sfäärulites. Hiline replikaas moodustub varajase replikaasi edasise protsessingu tulemusena ja kujutab endast täielikult protsessitud ns. P 1, 2, 3 ja 4 stabiilset kompleksi ning sünteesib nii genoomseid kui ka subgenoomseid positiivseid RNA ahelaid. Kuna hilises infektsioonis on NSP 2 proteaasi kontsentratsioon nakatatud rakkudes kõrge, siis väheneb järsult de nova sünteesitud polüproteiinide stabiilsus ja uusi varajase (ega ka hilise) replikaasi komplekse juurde ei moodustata.
 Struktuursete valkude ekspressioon algab ca 3 tundi p. i. ja toimub sg. RNA-lt (nn. 26 S RNA) polüproteiini sünteesi teel. Polüproteiini alguses (kattevalgu AUG koodonist 25 b allpool) paikneb tugev translatsiooniline enhanser, mis võimendab struktuurse polüproteiini translatsiooni ligi kümme korda. Enhanseri toime põhineb viirusindutseeritud translatsioonilise bloki kompenseerimises. C (kapsiidivalk) omab autoproteaaset aktiivsust (kapsiidivalgu C-terminus on kemotrüpsiin-tüüpi seriin-proteaas) ja lõikab ennast polüproteiinist lahti. Kapsiidivalgu translatsioon toimub vabade polüsoomide poolt. Ülejäänud struktuurne polüproteiin transleeritakse ER membraanidega seotud polüsoomide abil. Toimuvad sünteesitud valkude modifitseerimised ja polüproteiini lõikamine raku signaal-endopeptidaaside poolt: P 62 (PE 2, E 3+E 2) kujutab endast transmembraanset valku. 6 k. Da on membraanseoseline valk. E 1 on teine transmembraane glükoproteiid. Sünteesi järgi jääb E 1 metastabiilsesse konformatsiooni (seda soodustavad raku chaperonid ja interaktsioonid E 2 valguga), mis jääb püsima kuni uute rakkude nakatamiseni (alles happeline p. H raku endosoomides toob kaasa E 1 stabiilse, fusogeense konformatsiooni moodutsmise). P 62, 6 k. Da ja E 1 valgud liiguvad koos raku plasmamembraani (sellel etapil moodustavad P 62 ja E 1 heterodimeerid ning juba ER-is toimub nende heterodimeeride trimeriseerumine). Struktuursete valkude valmimise viimaseks etapiks on P 62 protsessing E 3 ja E 2 (raku furiin-tüüpi proteaas trans-Golgi vesikulites) valkudeks.
Struktuursete valkude ekspressioon algab ca 3 tundi p. i. ja toimub sg. RNA-lt (nn. 26 S RNA) polüproteiini sünteesi teel. Polüproteiini alguses (kattevalgu AUG koodonist 25 b allpool) paikneb tugev translatsiooniline enhanser, mis võimendab struktuurse polüproteiini translatsiooni ligi kümme korda. Enhanseri toime põhineb viirusindutseeritud translatsioonilise bloki kompenseerimises. C (kapsiidivalk) omab autoproteaaset aktiivsust (kapsiidivalgu C-terminus on kemotrüpsiin-tüüpi seriin-proteaas) ja lõikab ennast polüproteiinist lahti. Kapsiidivalgu translatsioon toimub vabade polüsoomide poolt. Ülejäänud struktuurne polüproteiin transleeritakse ER membraanidega seotud polüsoomide abil. Toimuvad sünteesitud valkude modifitseerimised ja polüproteiini lõikamine raku signaal-endopeptidaaside poolt: P 62 (PE 2, E 3+E 2) kujutab endast transmembraanset valku. 6 k. Da on membraanseoseline valk. E 1 on teine transmembraane glükoproteiid. Sünteesi järgi jääb E 1 metastabiilsesse konformatsiooni (seda soodustavad raku chaperonid ja interaktsioonid E 2 valguga), mis jääb püsima kuni uute rakkude nakatamiseni (alles happeline p. H raku endosoomides toob kaasa E 1 stabiilse, fusogeense konformatsiooni moodutsmise). P 62, 6 k. Da ja E 1 valgud liiguvad koos raku plasmamembraani (sellel etapil moodustavad P 62 ja E 1 heterodimeerid ning juba ER-is toimub nende heterodimeeride trimeriseerumine). Struktuursete valkude valmimise viimaseks etapiks on P 62 protsessing E 3 ja E 2 (raku furiin-tüüpi proteaas trans-Golgi vesikulites) valkudeks.
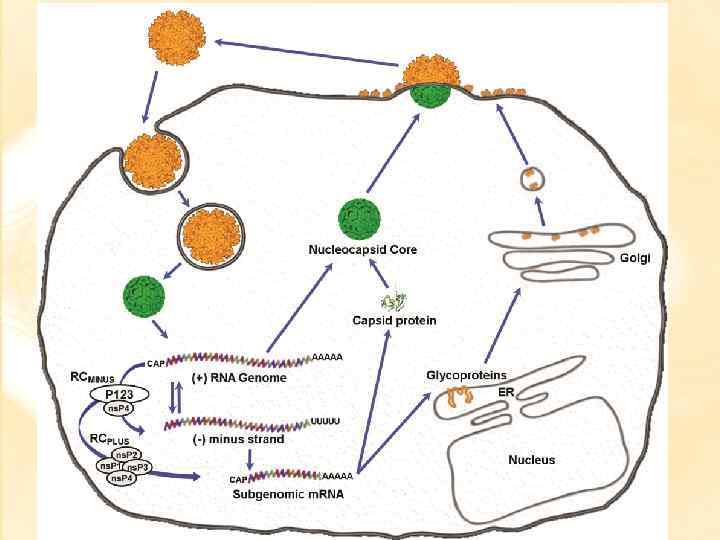
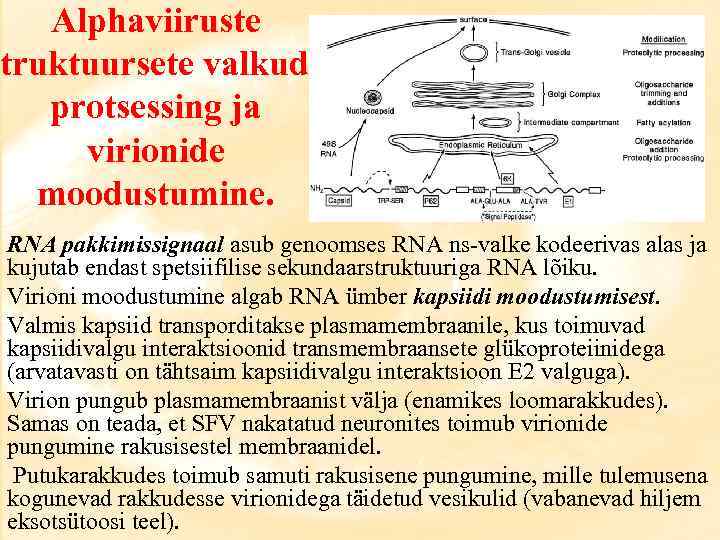 Alphaviiruste struktuursete valkude protsessing ja virionide moodustumine. RNA pakkimissignaal asub genoomses RNA ns-valke kodeerivas alas ja kujutab endast spetsiifilise sekundaarstruktuuriga RNA lõiku. Virioni moodustumine algab RNA ümber kapsiidi moodustumisest. Valmis kapsiid transporditakse plasmamembraanile, kus toimuvad kapsiidivalgu interaktsioonid transmembraansete glükoproteiinidega (arvatavasti on tähtsaim kapsiidivalgu interaktsioon E 2 valguga). Virion pungub plasmamembraanist välja (enamikes loomarakkudes). Samas on teada, et SFV nakatatud neuronites toimub virionide pungumine rakusisestel membraanidel. Putukarakkudes toimub samuti rakusisene pungumine, mille tulemusena kogunevad rakkudesse virionidega täidetud vesikulid (vabanevad hiljem eksotsütoosi teel).
Alphaviiruste struktuursete valkude protsessing ja virionide moodustumine. RNA pakkimissignaal asub genoomses RNA ns-valke kodeerivas alas ja kujutab endast spetsiifilise sekundaarstruktuuriga RNA lõiku. Virioni moodustumine algab RNA ümber kapsiidi moodustumisest. Valmis kapsiid transporditakse plasmamembraanile, kus toimuvad kapsiidivalgu interaktsioonid transmembraansete glükoproteiinidega (arvatavasti on tähtsaim kapsiidivalgu interaktsioon E 2 valguga). Virion pungub plasmamembraanist välja (enamikes loomarakkudes). Samas on teada, et SFV nakatatud neuronites toimub virionide pungumine rakusisestel membraanidel. Putukarakkudes toimub samuti rakusisene pungumine, mille tulemusena kogunevad rakkudesse virionidega täidetud vesikulid (vabanevad hiljem eksotsütoosi teel).
 Alphaviiruste mõju peremeesrakule Selgroogsete peremeeste rakkudes toob alphaviiruse infektsioon kaasa peremehe RNA ja valgu sünteesi inhibeerimise ning nakatatud raku surma. Peremehe valgusünteesi inhibeerimise mehhanismide kohta oletatakse, et see võib toimuda: - raku translatsioonifaktorite modifitseerimise; - viiruse m. RNA-de poolse konkureerimise (selleks on oluline ka ioonsete tingimuste muutumine nakatatud rakus) ja - viiruse kapsiidivalgu poolt teostatava raku translatsiooni otsese inhibeerimise teel Mitmed andmed näitavad, et peremehe transkriptsiooni ja translatsiooni mahasurumiseks on piisav viiruse mittestruktuursete valkude ekspressioon ning et struktuursed valgud (kapsiidi valk, E 2) võimendavad seda efekti. Peremeesrakkude surm leiab aset viirus-indutseeritud apoptoosi teel. Arvatakse, et oluliseks faktoriks, mis mõjutab rakkude apoptoosi, on alphaviiruste ns. P 2 valk (Vana Maailma alphaviirused) või kapsiidivalk (Uue Maailma alphaviirused; näidatud on et nende kapsiidivalk blokeerib tuuma ja tsütoplasma vahelist transporti). Selgrootute (vektorite) rakkudes läheb alphaviiruste replikatsioon reeglina kiiresti (umbes 24 tunni jooksul) üle persistentseks infektsiooniks. Sellega kaasneb viiruse replikatsiooni taseme järsk (mitu suurusjärku) vähenemine. Persistentse infektsiooni kujunemise molekulaarsed mehhanismid ei ole teada (oletatud on viirus-vastase faktori sünteesi rakkude poolt ja selle toimet viiruse replikatsioonile ja/või viiruse poolt nakatatud rakkudele). Putukarakkudes mõjutab alphaviiruse replikatsioon rakkude biosünteese ainult vähesel määral ja peremeesrakkude surm, kui see aset leiab, on reeglina nekrootiline (putukarakkudes alphaviirused apoptoosi ei indutseeri).
Alphaviiruste mõju peremeesrakule Selgroogsete peremeeste rakkudes toob alphaviiruse infektsioon kaasa peremehe RNA ja valgu sünteesi inhibeerimise ning nakatatud raku surma. Peremehe valgusünteesi inhibeerimise mehhanismide kohta oletatakse, et see võib toimuda: - raku translatsioonifaktorite modifitseerimise; - viiruse m. RNA-de poolse konkureerimise (selleks on oluline ka ioonsete tingimuste muutumine nakatatud rakus) ja - viiruse kapsiidivalgu poolt teostatava raku translatsiooni otsese inhibeerimise teel Mitmed andmed näitavad, et peremehe transkriptsiooni ja translatsiooni mahasurumiseks on piisav viiruse mittestruktuursete valkude ekspressioon ning et struktuursed valgud (kapsiidi valk, E 2) võimendavad seda efekti. Peremeesrakkude surm leiab aset viirus-indutseeritud apoptoosi teel. Arvatakse, et oluliseks faktoriks, mis mõjutab rakkude apoptoosi, on alphaviiruste ns. P 2 valk (Vana Maailma alphaviirused) või kapsiidivalk (Uue Maailma alphaviirused; näidatud on et nende kapsiidivalk blokeerib tuuma ja tsütoplasma vahelist transporti). Selgrootute (vektorite) rakkudes läheb alphaviiruste replikatsioon reeglina kiiresti (umbes 24 tunni jooksul) üle persistentseks infektsiooniks. Sellega kaasneb viiruse replikatsiooni taseme järsk (mitu suurusjärku) vähenemine. Persistentse infektsiooni kujunemise molekulaarsed mehhanismid ei ole teada (oletatud on viirus-vastase faktori sünteesi rakkude poolt ja selle toimet viiruse replikatsioonile ja/või viiruse poolt nakatatud rakkudele). Putukarakkudes mõjutab alphaviiruse replikatsioon rakkude biosünteese ainult vähesel määral ja peremeesrakkude surm, kui see aset leiab, on reeglina nekrootiline (putukarakkudes alphaviirused apoptoosi ei indutseeri).
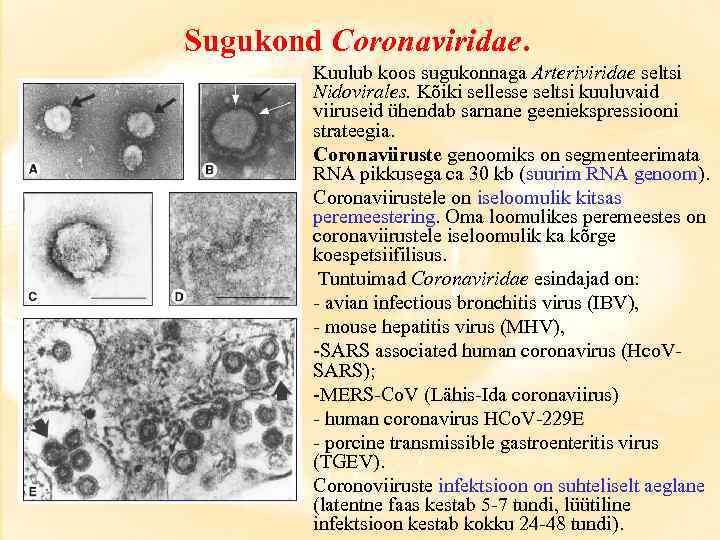 Sugukond Coronaviridae. Kuulub koos sugukonnaga Arteriviridae seltsi Nidovirales. Kõiki sellesse seltsi kuuluvaid viiruseid ühendab sarnane geeniekspressiooni strateegia. Coronaviiruste genoomiks on segmenteerimata RNA pikkusega ca 30 kb (suurim RNA genoom). Coronaviirustele on iseloomulik kitsas peremeestering. Oma loomulikes peremeestes on coronaviirustele iseloomulik ka kõrge koespetsiifilisus. Tuntuimad Coronaviridae esindajad on: - avian infectious bronchitis virus (IBV), - mouse hepatitis virus (MHV), -SARS associated human coronavirus (Hco. VSARS); -MERS-Co. V (Lähis-Ida coronaviirus) - human coronavirus HCo. V-229 E - porcine transmissible gastroenteritis virus (TGEV). Coronoviiruste infektsioon on suhteliselt aeglane (latentne faas kestab 5 -7 tundi, lüütiline infektsioon kestab kokku 24 -48 tundi).
Sugukond Coronaviridae. Kuulub koos sugukonnaga Arteriviridae seltsi Nidovirales. Kõiki sellesse seltsi kuuluvaid viiruseid ühendab sarnane geeniekspressiooni strateegia. Coronaviiruste genoomiks on segmenteerimata RNA pikkusega ca 30 kb (suurim RNA genoom). Coronaviirustele on iseloomulik kitsas peremeestering. Oma loomulikes peremeestes on coronaviirustele iseloomulik ka kõrge koespetsiifilisus. Tuntuimad Coronaviridae esindajad on: - avian infectious bronchitis virus (IBV), - mouse hepatitis virus (MHV), -SARS associated human coronavirus (Hco. VSARS); -MERS-Co. V (Lähis-Ida coronaviirus) - human coronavirus HCo. V-229 E - porcine transmissible gastroenteritis virus (TGEV). Coronoviiruste infektsioon on suhteliselt aeglane (latentne faas kestab 5 -7 tundi, lüütiline infektsioon kestab kokku 24 -48 tundi).
 Coronaviiruse virioni ehituse skeem. Virioni (diameeter ca 100 nm) kuulub: 1. RNA, mis on seotud nukleokapsiidivalguga (N valk) ja moodustab spiraalse paindliku nukleokapsiidi. 2. “Core” struktuur (65 nm) ümbritseb nukleokapsiidi ja mille moodustavad Mvalk ja N-valk. 3. Lipoproteiidne ümbris (pärineb rakusisestest membraanidest), milles paiknevad viiruse glükoproteiinid: - membraanvalk (M) on nii “core” valk kui ka ümbrise valk; -”ogavalk” (S). S-valk on coronaviiruse antiretseptor ja membraanide fusionvalk. - E-valk (envelope), minoorne glükoproteiin; - osadel coronaviirustel (nt. MHV) on membraanis veel ka hemoglutiniinesteraas (HE), mis võib osaleda viiruse seondumisel rakule ja/või viiruse vabanemisel nakatatud rakkudelt.
Coronaviiruse virioni ehituse skeem. Virioni (diameeter ca 100 nm) kuulub: 1. RNA, mis on seotud nukleokapsiidivalguga (N valk) ja moodustab spiraalse paindliku nukleokapsiidi. 2. “Core” struktuur (65 nm) ümbritseb nukleokapsiidi ja mille moodustavad Mvalk ja N-valk. 3. Lipoproteiidne ümbris (pärineb rakusisestest membraanidest), milles paiknevad viiruse glükoproteiinid: - membraanvalk (M) on nii “core” valk kui ka ümbrise valk; -”ogavalk” (S). S-valk on coronaviiruse antiretseptor ja membraanide fusionvalk. - E-valk (envelope), minoorne glükoproteiin; - osadel coronaviirustel (nt. MHV) on membraanis veel ka hemoglutiniinesteraas (HE), mis võib osaleda viiruse seondumisel rakule ja/või viiruse vabanemisel nakatatud rakkudelt.
 Coronaviiruste genoomne organisatsioon Coronaviiruste genoomne RNA on 27 -32 kb pikkune ja sisaldab 5’-cap ning 3’-polü(A) struktuure. Genoomses RNAs võib eraldada järgmiseid elemente: -RNA 5’-otsas asub 65 -98 b pikkune liiderjärjestus (asub ka kõigi sg. RNAde 5’-otstes); - liider-järjestusele järgneb 200 -400 b pikkune mittekodeeriv järjestus; - kodeeriv ala algab kahe suure, otsapidi kattuvat lugemisraamiga (ORF 1 a ja ORF 1 b, kokku ca 20 kb). Need lugemisraamid eksepresseeruvad ribosomaalse raaminihkega ja kodeerivad viiruse Rd. Rp-d, proteaasi ja seni tundmata mittestruktuurseid funktsiooniga valke (kokku on teada üle 10 proteolüütilise protsessingu produkti); - järgnevate lugemisraamide vahel paiknevad IS-järjestused (intergenic sequence, kasutakse ka nimetust TAS-järjestus); - genoomi 3’-osas asuvad konserveerunud lugemisraamid, mis kodeerivad S, E, M ja N valke. Muudu lugemisraamid (neid on erinevatel coronaviirustel 2 -4) on vähe konserveerunud ja kodeerivad muu hulgas HE-valku. - genoomi 3’-otsas (polü(A) järjestuse ees) asub 200 -500 b pikkune mittekodeeriv ala. • Nii 5’- kui ka 3’-NTR on vajalikud viiruse RNA transkriptsiooniks ja replikatsiooniks
Coronaviiruste genoomne organisatsioon Coronaviiruste genoomne RNA on 27 -32 kb pikkune ja sisaldab 5’-cap ning 3’-polü(A) struktuure. Genoomses RNAs võib eraldada järgmiseid elemente: -RNA 5’-otsas asub 65 -98 b pikkune liiderjärjestus (asub ka kõigi sg. RNAde 5’-otstes); - liider-järjestusele järgneb 200 -400 b pikkune mittekodeeriv järjestus; - kodeeriv ala algab kahe suure, otsapidi kattuvat lugemisraamiga (ORF 1 a ja ORF 1 b, kokku ca 20 kb). Need lugemisraamid eksepresseeruvad ribosomaalse raaminihkega ja kodeerivad viiruse Rd. Rp-d, proteaasi ja seni tundmata mittestruktuurseid funktsiooniga valke (kokku on teada üle 10 proteolüütilise protsessingu produkti); - järgnevate lugemisraamide vahel paiknevad IS-järjestused (intergenic sequence, kasutakse ka nimetust TAS-järjestus); - genoomi 3’-osas asuvad konserveerunud lugemisraamid, mis kodeerivad S, E, M ja N valke. Muudu lugemisraamid (neid on erinevatel coronaviirustel 2 -4) on vähe konserveerunud ja kodeerivad muu hulgas HE-valku. - genoomi 3’-otsas (polü(A) järjestuse ees) asub 200 -500 b pikkune mittekodeeriv ala. • Nii 5’- kui ka 3’-NTR on vajalikud viiruse RNA transkriptsiooniks ja replikatsiooniks
 Coronaviiruse infektsioonitsükli algus Coronoviiruste peamine antiretseptor on S-valk, mis seondab otseselt raku poolset retseptorit, mis on erinevatel coronaviirustel erinevad (see seletab ka, vähemalt osaliselt, miks on paljud coronaviirused kõrge koespetsiifilisusega): -MHV retseptor (MHVR) on BGP glükoproteiin (kartsinoembrüonaalseste glükoproteiinide sugukonnast). See retseptor on ekspresseeritud peamiselt MHC sihtmärk-rakkudel: maksa-, seedekulgla- ja B-rakkudel ning makrofaagidel. - TGEV ja HCo. V retseptoriks on aminopeptidaas N (APN), mis esineb paljude rakkude pinnal, k. a. hingamis- ja seedekulgla epiteeli rakud ning neuronid. Coronaviiruste sisenemisel rakku on teada kaks erinevat mehhanismi: - enamus coronaviiruseid (enamus MHV tüvesid, IBV) sisenevad rakku virioni ja raku plasmamembraani liitumise teel (p. H-sõltumatult); - mõned MHV tüved kasutavad sisenemiseks endotsütoosi ja membraanide liitumine on indutseeritud madala p. H poolt. Mõlemal juhul vabaneb nende protsesside tagajärjel raku tsütoplasmasse coronaviiruse nukleokapsiid. Järgnevalt toimub selle lahtipakkimine mille tulemusena viiruse genoom vabaneb ja aktiveerub.
Coronaviiruse infektsioonitsükli algus Coronoviiruste peamine antiretseptor on S-valk, mis seondab otseselt raku poolset retseptorit, mis on erinevatel coronaviirustel erinevad (see seletab ka, vähemalt osaliselt, miks on paljud coronaviirused kõrge koespetsiifilisusega): -MHV retseptor (MHVR) on BGP glükoproteiin (kartsinoembrüonaalseste glükoproteiinide sugukonnast). See retseptor on ekspresseeritud peamiselt MHC sihtmärk-rakkudel: maksa-, seedekulgla- ja B-rakkudel ning makrofaagidel. - TGEV ja HCo. V retseptoriks on aminopeptidaas N (APN), mis esineb paljude rakkude pinnal, k. a. hingamis- ja seedekulgla epiteeli rakud ning neuronid. Coronaviiruste sisenemisel rakku on teada kaks erinevat mehhanismi: - enamus coronaviiruseid (enamus MHV tüvesid, IBV) sisenevad rakku virioni ja raku plasmamembraani liitumise teel (p. H-sõltumatult); - mõned MHV tüved kasutavad sisenemiseks endotsütoosi ja membraanide liitumine on indutseeritud madala p. H poolt. Mõlemal juhul vabaneb nende protsesside tagajärjel raku tsütoplasmasse coronaviiruse nukleokapsiid. Järgnevalt toimub selle lahtipakkimine mille tulemusena viiruse genoom vabaneb ja aktiveerub.
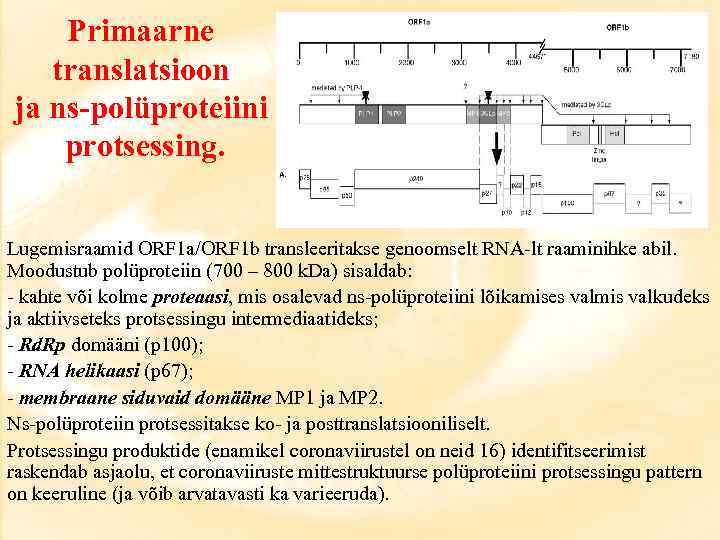 Primaarne translatsioon ja ns-polüproteiini protsessing. Lugemisraamid ORF 1 a/ORF 1 b transleeritakse genoomselt RNA-lt raaminihke abil. Moodustub polüproteiin (700 – 800 k. Da) sisaldab: - kahte või kolme proteaasi, mis osalevad ns-polüproteiini lõikamises valmis valkudeks ja aktiivseteks protsessingu intermediaatideks; - Rd. Rp domääni (p 100); - RNA helikaasi (p 67); - membraane siduvaid domääne MP 1 ja MP 2. Ns-polüproteiin protsessitakse ko- ja posttranslatsiooniliselt. Protsessingu produktide (enamikel coronaviirustel on neid 16) identifitseerimist raskendab asjaolu, et coronaviiruste mittestruktuurse polüproteiini protsessingu pattern on keeruline (ja võib arvatavasti ka varieeruda).
Primaarne translatsioon ja ns-polüproteiini protsessing. Lugemisraamid ORF 1 a/ORF 1 b transleeritakse genoomselt RNA-lt raaminihke abil. Moodustub polüproteiin (700 – 800 k. Da) sisaldab: - kahte või kolme proteaasi, mis osalevad ns-polüproteiini lõikamises valmis valkudeks ja aktiivseteks protsessingu intermediaatideks; - Rd. Rp domääni (p 100); - RNA helikaasi (p 67); - membraane siduvaid domääne MP 1 ja MP 2. Ns-polüproteiin protsessitakse ko- ja posttranslatsiooniliselt. Protsessingu produktide (enamikel coronaviirustel on neid 16) identifitseerimist raskendab asjaolu, et coronaviiruste mittestruktuurse polüproteiini protsessingu pattern on keeruline (ja võib arvatavasti ka varieeruda).
 Coronaviiruse replikatsioon ja transkriptsioon Replikatsiooniks nimetatakse coronaviirustel täispika antigenoomi ja genoomse RNA sünteesi Transkriptsiooniks nimetatakse sg. RNAde sünteesi genoomse (või antigenoomse) RNA maatritsil Coronaviiruste infektsiooni iseloomustab suure hulga 3 koterminaalsete sg. RNAde süntees. Need sg. RNAd on vajalikud 3’ORFide ekspressiooniks Erinevalt suurest enamikus “+” RNA genoomsete viiruste sg. RNAdest replitseeruvad coronaviiruse sg. RNAd nakatunud rakkudes (moodustuvad vastavad negatiivsed ahelad)
Coronaviiruse replikatsioon ja transkriptsioon Replikatsiooniks nimetatakse coronaviirustel täispika antigenoomi ja genoomse RNA sünteesi Transkriptsiooniks nimetatakse sg. RNAde sünteesi genoomse (või antigenoomse) RNA maatritsil Coronaviiruste infektsiooni iseloomustab suure hulga 3 koterminaalsete sg. RNAde süntees. Need sg. RNAd on vajalikud 3’ORFide ekspressiooniks Erinevalt suurest enamikus “+” RNA genoomsete viiruste sg. RNAdest replitseeruvad coronaviiruse sg. RNAd nakatunud rakkudes (moodustuvad vastavad negatiivsed ahelad)
 Transkriptsioon ja replikatsioon Ns-polüproteiini lõikamise produktid moodustavad (võimalik, et koos peremehe valkudega) funktsionaalse, membraanidega seotud (MP 1 ja MP 2 osalusel) replikatsioonikompleksi. Replikaasi kompleksi membraanid pärinevad (sõltuvalt nakatatud raku tüübist) kas ER, Golgi või endosoomide membraanidest. On võimalik, et eksisteerib mitut tüüpi Rd. Rp komplekse (sg. RNAde jaoks ja genoomse RNA jaoks). Esimeseks sünteesiks on RNA negatiivse ahela süntees. Coronaviiruste negatiivne RNA asub alati dupleksis positiivse ahelaga. Nakatatud rakkudes on negatiivseid ahelaid 10 -100 korda vähem kui positiivseid. Transkriptsiooni käigus sünteesitakse seeria sg. RNA-sid, millel kõigil on 5’-capstruktuur ja 3’-polü(A) järjestus. Kokku on erinevatel coronaviirustel leitud 5 -7 3’-koterminaalset sg. RNAd. Ehkki enamus sg. RNAdest on struktuurselt polütsistroonsed, on nad enamikus funktsionaalselt monotsistroonsed. Kõiki coronaviiruste sg. RNAsid iseloomustab: - 5’-otsas asuv 65 -95 b pikkune liiderjärjestus, mis on identne genoomi 5’-otsas asuvale liider-järjestusele. Genoomses RNAs geenide vahel liiderjärjestused puuduvad, selle asemel on vaid 7 -18 b lõigud (IS-saidid), mis on homoloogsed liiderjärjestuse 3’-otsaga; - rakkudes leidub sg. RNAdele vastavaid negatiivseid ahelaid, mis on transkriptsiooniliseks maatriksiks sg. RNAde sünteesil.
Transkriptsioon ja replikatsioon Ns-polüproteiini lõikamise produktid moodustavad (võimalik, et koos peremehe valkudega) funktsionaalse, membraanidega seotud (MP 1 ja MP 2 osalusel) replikatsioonikompleksi. Replikaasi kompleksi membraanid pärinevad (sõltuvalt nakatatud raku tüübist) kas ER, Golgi või endosoomide membraanidest. On võimalik, et eksisteerib mitut tüüpi Rd. Rp komplekse (sg. RNAde jaoks ja genoomse RNA jaoks). Esimeseks sünteesiks on RNA negatiivse ahela süntees. Coronaviiruste negatiivne RNA asub alati dupleksis positiivse ahelaga. Nakatatud rakkudes on negatiivseid ahelaid 10 -100 korda vähem kui positiivseid. Transkriptsiooni käigus sünteesitakse seeria sg. RNA-sid, millel kõigil on 5’-capstruktuur ja 3’-polü(A) järjestus. Kokku on erinevatel coronaviirustel leitud 5 -7 3’-koterminaalset sg. RNAd. Ehkki enamus sg. RNAdest on struktuurselt polütsistroonsed, on nad enamikus funktsionaalselt monotsistroonsed. Kõiki coronaviiruste sg. RNAsid iseloomustab: - 5’-otsas asuv 65 -95 b pikkune liiderjärjestus, mis on identne genoomi 5’-otsas asuvale liider-järjestusele. Genoomses RNAs geenide vahel liiderjärjestused puuduvad, selle asemel on vaid 7 -18 b lõigud (IS-saidid), mis on homoloogsed liiderjärjestuse 3’-otsaga; - rakkudes leidub sg. RNAdele vastavaid negatiivseid ahelaid, mis on transkriptsiooniliseks maatriksiks sg. RNAde sünteesil.
 Esimese põlvkonna sg. RNA-de ja nendes paikneva liiderjärjestuse päritolu ja seletamiseks eksisteerib kaks mudelit: Liider-praimeeritud transkriptsioon eeldab, et positiivse ahela transkriptsioon algab negatiivse ahela 3’-otsast ja katkeb peale liiderjärjestuse kopeerimist. 65 -98 b pikkune liider-RNA dissotsieerub sünteesikohalt ja seondub hiljem ühele IS-järjestustest negatiivses ahelas. Selle mudeli järgi kujutavad IS-elemendid endast transkriptsioonilisi promootereid. Negatiivse ahela sünteesi katkestus eeldab, et Rd. Rp teeb negatiivse ahela sünteesi käigus (genoomsel maatritsil) IS-elemendil pausi ja ”hüppab” seejärel üle genoomi otsale (liiderjärjestusele). Moodustub sg. RNA negatiivne ahel, millelt sünteesitakse positiivsed sg. RNAd. Seega kujutavad ISelemendid endast terminaatoreid. Coronaviiruse sg. RNA süntees
Esimese põlvkonna sg. RNA-de ja nendes paikneva liiderjärjestuse päritolu ja seletamiseks eksisteerib kaks mudelit: Liider-praimeeritud transkriptsioon eeldab, et positiivse ahela transkriptsioon algab negatiivse ahela 3’-otsast ja katkeb peale liiderjärjestuse kopeerimist. 65 -98 b pikkune liider-RNA dissotsieerub sünteesikohalt ja seondub hiljem ühele IS-järjestustest negatiivses ahelas. Selle mudeli järgi kujutavad IS-elemendid endast transkriptsioonilisi promootereid. Negatiivse ahela sünteesi katkestus eeldab, et Rd. Rp teeb negatiivse ahela sünteesi käigus (genoomsel maatritsil) IS-elemendil pausi ja ”hüppab” seejärel üle genoomi otsale (liiderjärjestusele). Moodustub sg. RNA negatiivne ahel, millelt sünteesitakse positiivsed sg. RNAd. Seega kujutavad ISelemendid endast terminaatoreid. Coronaviiruse sg. RNA süntees
 Coronaviiruse sg. RNA süntees Kuni coronaviiruste pöördgeneetika kasutuselevõtmiseni ei olnud võimalik eelistada kumbagi mudelit. Pöördgeneetika võimaldas aga otseselt kindlaks teha sg. RNAde ISjärjestuste päritolu. Katsed näitasid, et: - liider-järjestuse IS-elementi sisse viidud mutatsioonid ei esine kunagi sg. RNAdes; - sg. RNAde IS-järjestustesse sisse viidud mutatsioonid esinevad 100% vastaval sg. RNAdel. Seega on eksperimentaalselt kinnitust leidnud teine, negatiivse ahela sünteesi katkestuse mudel. Peale liider-järjestuse ja ISelementide reguleerivad coronaviiruse sg. RNAde sünteesi ka teised RNA elemendid.
Coronaviiruse sg. RNA süntees Kuni coronaviiruste pöördgeneetika kasutuselevõtmiseni ei olnud võimalik eelistada kumbagi mudelit. Pöördgeneetika võimaldas aga otseselt kindlaks teha sg. RNAde ISjärjestuste päritolu. Katsed näitasid, et: - liider-järjestuse IS-elementi sisse viidud mutatsioonid ei esine kunagi sg. RNAdes; - sg. RNAde IS-järjestustesse sisse viidud mutatsioonid esinevad 100% vastaval sg. RNAdel. Seega on eksperimentaalselt kinnitust leidnud teine, negatiivse ahela sünteesi katkestuse mudel. Peale liider-järjestuse ja ISelementide reguleerivad coronaviiruse sg. RNAde sünteesi ka teised RNA elemendid.
 Kuidas see töötab? Negatiivse ahela sünteesi katkestus põhineb ilmselt RNA struktuuril ja viiruse polümeraasi omadustel. Mõne geeni (N-geen) puhul reguleerivad seda protsessi täiendavad regulatsiooni elemendid
Kuidas see töötab? Negatiivse ahela sünteesi katkestus põhineb ilmselt RNA struktuuril ja viiruse polümeraasi omadustel. Mõne geeni (N-geen) puhul reguleerivad seda protsessi täiendavad regulatsiooni elemendid
 RNA replikatsioon ja rekombinatsioon. • Erinevalt sg. RNAde sünteesist peab RNA replikatsioonil toimuma kogu genoomi katkematu kopeerimine. Replikatsiooniks olulised cisjärjestused asuvad coronaviirustel genoomi 5’- ja 3’- otstes, kuid arvatakse, et on olemas ka sisemisi cis-järjestusi, mis on efektiivseks replitseerumiseks olulised. • Coronaviiruste infektsioonile on iseloomulik kõrge rekombinatsioonisagedus (ca 25%). Kõrge rekombinatsiooni tase on arvatavasti seotud replikatsiooni ja transkriptsiooni iseärasustega (polümeraasi ”hüpped” võivad arvatavasti toimuda ka ühelt RNAlt teise isolaadi RNA homoloogsele järjestusele). Arvatavasti on rekombinatsioonil olnud oluline roll coronaviiruste genoomide evolutsioonis. • Coronaviiruse replikatsioonil tekib palju mutantseid genoome. Samuti soodustab coronaviiruste replikatsiooni- ja transkriptsioonistrateegia DI genoomide teket.
RNA replikatsioon ja rekombinatsioon. • Erinevalt sg. RNAde sünteesist peab RNA replikatsioonil toimuma kogu genoomi katkematu kopeerimine. Replikatsiooniks olulised cisjärjestused asuvad coronaviirustel genoomi 5’- ja 3’- otstes, kuid arvatakse, et on olemas ka sisemisi cis-järjestusi, mis on efektiivseks replitseerumiseks olulised. • Coronaviiruste infektsioonile on iseloomulik kõrge rekombinatsioonisagedus (ca 25%). Kõrge rekombinatsiooni tase on arvatavasti seotud replikatsiooni ja transkriptsiooni iseärasustega (polümeraasi ”hüpped” võivad arvatavasti toimuda ka ühelt RNAlt teise isolaadi RNA homoloogsele järjestusele). Arvatavasti on rekombinatsioonil olnud oluline roll coronaviiruste genoomide evolutsioonis. • Coronaviiruse replikatsioonil tekib palju mutantseid genoome. Samuti soodustab coronaviiruste replikatsiooni- ja transkriptsioonistrateegia DI genoomide teket.
 Coronaviirused kasutavad praimaasi ja kontrollivad RNA sünteesi täpsust Coronaviiruste replikaasikompleksi kuulub 16 viiruse kodeeritud mittestruktuurset valku. Need moodustavad suurte polüproteiinide protsessingul ja täidavad erinevaid funktsioone: 1. ns. P 12 on viiruse Rd. Rp katalüütiline subühik. Tegemist on ebatavalise ensüümiga, mis ei suuda RNA sünteesi initsieerida, kuid suudab sünteesida RNAd ka DNA maatritsil. 2. ns. P 8 on coronaviiruse praimaas. See on samuti Rd. Rp, kuid sünteesib ca 6 b pikkuseid RNA praimeried (in vitro ka maatritsi siseregioonides) 3. Rd. Rp-l on olemas ka kvaliteedi-kontroll. Seda ei tee ensüüm ise vaid ns 14 – eksoribonukleaas. See ensüüm on vajalik replikatsiooniks, tema puudumisel teeb polümeraas palju enam vigu ja sünteesib defektseid RNAsid
Coronaviirused kasutavad praimaasi ja kontrollivad RNA sünteesi täpsust Coronaviiruste replikaasikompleksi kuulub 16 viiruse kodeeritud mittestruktuurset valku. Need moodustavad suurte polüproteiinide protsessingul ja täidavad erinevaid funktsioone: 1. ns. P 12 on viiruse Rd. Rp katalüütiline subühik. Tegemist on ebatavalise ensüümiga, mis ei suuda RNA sünteesi initsieerida, kuid suudab sünteesida RNAd ka DNA maatritsil. 2. ns. P 8 on coronaviiruse praimaas. See on samuti Rd. Rp, kuid sünteesib ca 6 b pikkuseid RNA praimeried (in vitro ka maatritsi siseregioonides) 3. Rd. Rp-l on olemas ka kvaliteedi-kontroll. Seda ei tee ensüüm ise vaid ns 14 – eksoribonukleaas. See ensüüm on vajalik replikatsiooniks, tema puudumisel teeb polümeraas palju enam vigu ja sünteesib defektseid RNAsid
 Coronaviiruse replikaasi kompleksid Coronaviiruste replikaasi kompleksid on ca 200 -300 nm diameetriga kahekordse membraaniga vesikulid, mis moodustuvad ER-st. Need vesiikulid moodustavad ühtse võrgustiku ja nendes toimub viiruse RNA süntees. Samas on viiruse replikaasi valke kõige enam näha mitte vesiikulites, vaid nende vahel asuvatel membraanidel. Vesiikulid on omavahel ühenduses kanalite võrgustiku abil, kuid ühendusi tsütosooliga pole EM tomograafi abil näha.
Coronaviiruse replikaasi kompleksid Coronaviiruste replikaasi kompleksid on ca 200 -300 nm diameetriga kahekordse membraaniga vesikulid, mis moodustuvad ER-st. Need vesiikulid moodustavad ühtse võrgustiku ja nendes toimub viiruse RNA süntees. Samas on viiruse replikaasi valke kõige enam näha mitte vesiikulites, vaid nende vahel asuvatel membraanidel. Vesiikulid on omavahel ühenduses kanalite võrgustiku abil, kuid ühendusi tsütosooliga pole EM tomograafi abil näha.
 Coronaviiruse virionide moodustamine Coronaviiruste struktuursed valgud modifitseeritakse raku ensüümide poolt: S-glükoproteiin sekreteeritakse ER vesikulitesse ja glükosüleeritakse. Sellele järgneb transport Golgi kompleksi, vähemal määral ka plasmamembraani. M-glükoproteiin sünteesitakse ER-il, kus ta seondub membraanidega ja modifitseeritakse. Valmis M-valk koguneb Golgi kompleksi. Erinevalt S-valgust ei transpordita M-valku plasmamembraani. N-fosfoproteiin transleeritakse vabadel polüsoomidel. E-valk paikneb E-valk perinukleaarses alas ja raku plasmamembraanidel. Coronaviiruste virionide moodustamine algab spiraalse nukleokapsiidi moodustamisest. N-valgu ja RNA interaktsioon on järjestuse-spetsiifiline: N-valgu eelistatud seondumise sait (pakkimissiganaal) asub genoomses RNAs ORF 1 geenist 3’-suunas. Moodustunud nukleokapsiidid interageeruvad Mvalguga. Seepärast toimubki coronaviiruste virionide pungumine rakusisestel membraanidel Pungumise käivitamiseks on oluline E- ja M-valkude interaktsioonide toimumine. S-valk aktiivselt pungumises ei osale ja tema paigutumine virionidesse toimub tänu interaktsioonidele M-valguga. Virionid väljuvad nakatunud rakust eksotsütoosi teel.
Coronaviiruse virionide moodustamine Coronaviiruste struktuursed valgud modifitseeritakse raku ensüümide poolt: S-glükoproteiin sekreteeritakse ER vesikulitesse ja glükosüleeritakse. Sellele järgneb transport Golgi kompleksi, vähemal määral ka plasmamembraani. M-glükoproteiin sünteesitakse ER-il, kus ta seondub membraanidega ja modifitseeritakse. Valmis M-valk koguneb Golgi kompleksi. Erinevalt S-valgust ei transpordita M-valku plasmamembraani. N-fosfoproteiin transleeritakse vabadel polüsoomidel. E-valk paikneb E-valk perinukleaarses alas ja raku plasmamembraanidel. Coronaviiruste virionide moodustamine algab spiraalse nukleokapsiidi moodustamisest. N-valgu ja RNA interaktsioon on järjestuse-spetsiifiline: N-valgu eelistatud seondumise sait (pakkimissiganaal) asub genoomses RNAs ORF 1 geenist 3’-suunas. Moodustunud nukleokapsiidid interageeruvad Mvalguga. Seepärast toimubki coronaviiruste virionide pungumine rakusisestel membraanidel Pungumise käivitamiseks on oluline E- ja M-valkude interaktsioonide toimumine. S-valk aktiivselt pungumises ei osale ja tema paigutumine virionidesse toimub tänu interaktsioonidele M-valguga. Virionid väljuvad nakatunud rakust eksotsütoosi teel.
 Coronaviiruste mõju peremehele Coronaviiruste põhjustatud tsütopaatilised efektid sõltuvad nii viirusest kui ka peremeesrakust. Paljude coronaviiruste (MHV, IBV jt) infektsiooni iseloomustub nakatatud rakkude fuseerumise indutseerimine. Samas on kõikidele coronaviiruste infektsioonidele iseloomulik ka nakatatud rakkude ümardumine ja rakkude lüüsimine. Andmeid raku metabolismi mõjutamise kohta on suhteliselt vähe. On teada, et: - mõned coronaviirused suruvad maha peremehe transkriptsiooni ja translatsiooni; - coronaviirused võivad indutseerida muutuseid nakatatud raku membraanides; - mõnede coronaviiruste E-valk võib põhjustada ka nakatunud rakkude apoptoosi. Paljudele coronaviirustele on iseloomulik persistentse infektsiooni tekitamine, see võib toimuda ka nakatunud rakukultuuri tasemel. Persistentselt nakatunud rakud sisaldavad sageli viiruse defektseid genoome. Persistentne infektsioon rakukultuuris võib olla seotud nii viirusele kui ka rakupopulatsioonile mõjuva evolutsioonilise survega: - defektsete genoomide tekkimise ja nende poolse interferentsiga; - infektsiooni suhtes resistentsete rakkude selektsiooniga. Organismi tasemel on coronaviiruste tekitatud infektsioon enamasti akuutne, kuid immunosupressiooni korral võib kujuneda ka persistentne infektsioon.
Coronaviiruste mõju peremehele Coronaviiruste põhjustatud tsütopaatilised efektid sõltuvad nii viirusest kui ka peremeesrakust. Paljude coronaviiruste (MHV, IBV jt) infektsiooni iseloomustub nakatatud rakkude fuseerumise indutseerimine. Samas on kõikidele coronaviiruste infektsioonidele iseloomulik ka nakatatud rakkude ümardumine ja rakkude lüüsimine. Andmeid raku metabolismi mõjutamise kohta on suhteliselt vähe. On teada, et: - mõned coronaviirused suruvad maha peremehe transkriptsiooni ja translatsiooni; - coronaviirused võivad indutseerida muutuseid nakatatud raku membraanides; - mõnede coronaviiruste E-valk võib põhjustada ka nakatunud rakkude apoptoosi. Paljudele coronaviirustele on iseloomulik persistentse infektsiooni tekitamine, see võib toimuda ka nakatunud rakukultuuri tasemel. Persistentselt nakatunud rakud sisaldavad sageli viiruse defektseid genoome. Persistentne infektsioon rakukultuuris võib olla seotud nii viirusele kui ka rakupopulatsioonile mõjuva evolutsioonilise survega: - defektsete genoomide tekkimise ja nende poolse interferentsiga; - infektsiooni suhtes resistentsete rakkude selektsiooniga. Organismi tasemel on coronaviiruste tekitatud infektsioon enamasti akuutne, kuid immunosupressiooni korral võib kujuneda ka persistentne infektsioon.
 Sugukond Flaviviridae Sugukonna nimi tuleneb sõnast flavus (kollane), kuna sugukonna tüüpesindaja on kollapalaviku viirus (yellow fever, YF). Sugukonda kuulub kolm perekonda viiruseid: Flaviviirused: ligi 80 erinevat viiruste liiki. Enamus flaviviiruseid kasutavad lülijalgseid vektoreid (moskiitod, puugid). Tuntumad esindajad on YF, Dengue viirus (DEN), jaapani entsefaliidi viirus (JE), West Nile viirus (WN) ja puukentsefaliidi viirus (TBE). Hepaciviirused. Hepatiidi viirus C (HCV) avastati 1989 aastal, maailmas on üle 170 miljoni viiruskandja maailmas. HCV on teada ainult inimestel, vektor puudub (levib vere kaudu). Pestiviirused. Siia perekonda kuuluvad põllumajanduslikult tähtsad viirused nagu bovine viral diarrhea virus (BVDV) ja classical swine fever virus (CSFV). Vektorit ei ole, ülekanne leiab aset otsesel kokkupuutel. Erinevatesse perekondadesse kuuluvate viiruste bioloogilised ja molekulaarsed omadused erinevad oluliselt, kuid neid kõiki ühendab: - Virionide sarnane morfoloogia. - Sarnane genoomne organisatsioon. - Sarnane RNA replikatsiooni strateegia.
Sugukond Flaviviridae Sugukonna nimi tuleneb sõnast flavus (kollane), kuna sugukonna tüüpesindaja on kollapalaviku viirus (yellow fever, YF). Sugukonda kuulub kolm perekonda viiruseid: Flaviviirused: ligi 80 erinevat viiruste liiki. Enamus flaviviiruseid kasutavad lülijalgseid vektoreid (moskiitod, puugid). Tuntumad esindajad on YF, Dengue viirus (DEN), jaapani entsefaliidi viirus (JE), West Nile viirus (WN) ja puukentsefaliidi viirus (TBE). Hepaciviirused. Hepatiidi viirus C (HCV) avastati 1989 aastal, maailmas on üle 170 miljoni viiruskandja maailmas. HCV on teada ainult inimestel, vektor puudub (levib vere kaudu). Pestiviirused. Siia perekonda kuuluvad põllumajanduslikult tähtsad viirused nagu bovine viral diarrhea virus (BVDV) ja classical swine fever virus (CSFV). Vektorit ei ole, ülekanne leiab aset otsesel kokkupuutel. Erinevatesse perekondadesse kuuluvate viiruste bioloogilised ja molekulaarsed omadused erinevad oluliselt, kuid neid kõiki ühendab: - Virionide sarnane morfoloogia. - Sarnane genoomne organisatsioon. - Sarnane RNA replikatsiooni strateegia.
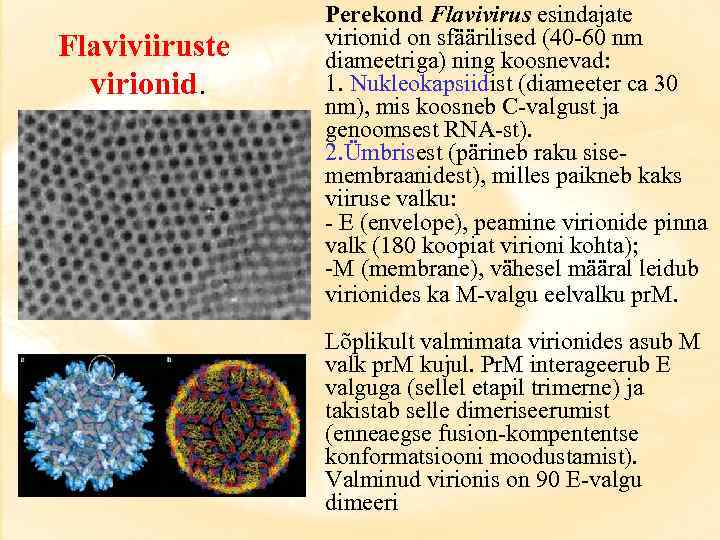 Flaviviiruste virionid. Perekond Flavivirus esindajate virionid on sfäärilised (40 -60 nm diameetriga) ning koosnevad: 1. Nukleokapsiidist (diameeter ca 30 nm), mis koosneb C-valgust ja genoomsest RNA-st). 2. Ümbrisest (pärineb raku sisemembraanidest), milles paikneb kaks viiruse valku: - E (envelope), peamine virionide pinna valk (180 koopiat virioni kohta); -M (membrane), vähesel määral leidub virionides ka M-valgu eelvalku pr. M. Lõplikult valmimata virionides asub M valk pr. M kujul. Pr. M interageerub E valguga (sellel etapil trimerne) ja takistab selle dimeriseerumist (enneaegse fusion-kompententse konformatsiooni moodustamist). Valminud virionis on 90 E-valgu dimeeri
Flaviviiruste virionid. Perekond Flavivirus esindajate virionid on sfäärilised (40 -60 nm diameetriga) ning koosnevad: 1. Nukleokapsiidist (diameeter ca 30 nm), mis koosneb C-valgust ja genoomsest RNA-st). 2. Ümbrisest (pärineb raku sisemembraanidest), milles paikneb kaks viiruse valku: - E (envelope), peamine virionide pinna valk (180 koopiat virioni kohta); -M (membrane), vähesel määral leidub virionides ka M-valgu eelvalku pr. M. Lõplikult valmimata virionides asub M valk pr. M kujul. Pr. M interageerub E valguga (sellel etapil trimerne) ja takistab selle dimeriseerumist (enneaegse fusion-kompententse konformatsiooni moodustamist). Valminud virionis on 90 E-valgu dimeeri
 Flaviviiruse genoomi struktuur Flaviviiruste genoom on positiivne RNA pikkusega ca 11 kb millel on: - 5’- cap 1 struktuur (m 7 Gppp. Amp); - sellele järgneb järjestus AG (need kaks nukleotiidi on kõigil flaviviirustel konserveerunud); - 5’-NTR (95 -132 b). NTR-id sisaldavad RNA struktuurelemente, mis on olulised viiruse RNA replikatsiooniks. 5’-NTR seondab replikatsiooniks vajalikke viiruse valke ja peremeesraku faktoreid (La); - üks lugemisraam (ca 10 kb), mis kodeerib viiruse polüproteiini. - 3’-NTR (114 -624 b), sisaldab pseudoknot struktuuri. See regioon erineb oluliselt moskiitode ja puukidega ülekanduvate viiruste vahel. 3’-NTR on negatiivsete ahelate sünteesi promooter ja seondab replikatsiooniks vajalikke viiruse ning peremeesraku (teada on e. EF-1 , seondamine) valke. On üheselt näidatud et flaviviiruste genoomi 5’ ja 3’ regioonid paarduvad omavahel ja et see on oluline viiruste replikatsiooniks (reguleerib translatsiooni/replikatsiooni vahekorda) Genoomi 3’-otsas asub stabiilne juuksenõela struktuur, mis on oluline interaktsiooniks kapsiidivalguga. Polü(A) järjestus reeglina puudub.
Flaviviiruse genoomi struktuur Flaviviiruste genoom on positiivne RNA pikkusega ca 11 kb millel on: - 5’- cap 1 struktuur (m 7 Gppp. Amp); - sellele järgneb järjestus AG (need kaks nukleotiidi on kõigil flaviviirustel konserveerunud); - 5’-NTR (95 -132 b). NTR-id sisaldavad RNA struktuurelemente, mis on olulised viiruse RNA replikatsiooniks. 5’-NTR seondab replikatsiooniks vajalikke viiruse valke ja peremeesraku faktoreid (La); - üks lugemisraam (ca 10 kb), mis kodeerib viiruse polüproteiini. - 3’-NTR (114 -624 b), sisaldab pseudoknot struktuuri. See regioon erineb oluliselt moskiitode ja puukidega ülekanduvate viiruste vahel. 3’-NTR on negatiivsete ahelate sünteesi promooter ja seondab replikatsiooniks vajalikke viiruse ning peremeesraku (teada on e. EF-1 , seondamine) valke. On üheselt näidatud et flaviviiruste genoomi 5’ ja 3’ regioonid paarduvad omavahel ja et see on oluline viiruste replikatsiooniks (reguleerib translatsiooni/replikatsiooni vahekorda) Genoomi 3’-otsas asub stabiilne juuksenõela struktuur, mis on oluline interaktsiooniks kapsiidivalguga. Polü(A) järjestus reeglina puudub.
 Flaviviiruse infektsioonitsükli algus Seondumine. Flaviviiruste antiretseptoriks on E-glükoproteiin. Täpsed rakkudele seondumise mehhanismid ja raku poolsed retseptorid pole üldjuhul teada (laboratoorsed tüved kasutavad retseptorina hepariin-sulfaati), DENV puhul on näidatud C-lektiini (DC-SIGN) kasutamine, muudel viirustel integriinide, GRP 78 ja CD 14 kasutamine. Teada on, et flaviviirused võivad seonduda rakkudele ka vironiga seondunud sub-neutraliseerivate antikehade vahendusel, seondudes antikehade kaudu raku Fc retseptoritele (nn. “antibody dependent enhancement”, ADE mehhanism). Sisenemine rakku toimub kas: -retseptor vahendatud endotsütoosi teel. Endosoomides toimub membraanide liitumine p. H-ist sõltuva mehhanismi abil (p. H langemine toob kaasa E-valgu konformatsioonilise muutuse – kõigepealt monomeride, siis homotrimeride moodustamise - mille käigus eksponeeritakse fusion-domeen). Core struktuur ei ole kompaktne ja RNA on kättesaadav ribosoomide jaoks. Translatsioon algab ORF-i esimesel AUG koodonil. Translatsiooni produktiks on polüproteiin, mis läbib keerulise ko- ja posttranslatsioonilise protsessingu. Protsessingus osalevad viiruse ja peremehe proteaasid.
Flaviviiruse infektsioonitsükli algus Seondumine. Flaviviiruste antiretseptoriks on E-glükoproteiin. Täpsed rakkudele seondumise mehhanismid ja raku poolsed retseptorid pole üldjuhul teada (laboratoorsed tüved kasutavad retseptorina hepariin-sulfaati), DENV puhul on näidatud C-lektiini (DC-SIGN) kasutamine, muudel viirustel integriinide, GRP 78 ja CD 14 kasutamine. Teada on, et flaviviirused võivad seonduda rakkudele ka vironiga seondunud sub-neutraliseerivate antikehade vahendusel, seondudes antikehade kaudu raku Fc retseptoritele (nn. “antibody dependent enhancement”, ADE mehhanism). Sisenemine rakku toimub kas: -retseptor vahendatud endotsütoosi teel. Endosoomides toimub membraanide liitumine p. H-ist sõltuva mehhanismi abil (p. H langemine toob kaasa E-valgu konformatsioonilise muutuse – kõigepealt monomeride, siis homotrimeride moodustamise - mille käigus eksponeeritakse fusion-domeen). Core struktuur ei ole kompaktne ja RNA on kättesaadav ribosoomide jaoks. Translatsioon algab ORF-i esimesel AUG koodonil. Translatsiooni produktiks on polüproteiin, mis läbib keerulise ko- ja posttranslatsioonilise protsessingu. Protsessingus osalevad viiruse ja peremehe proteaasid.
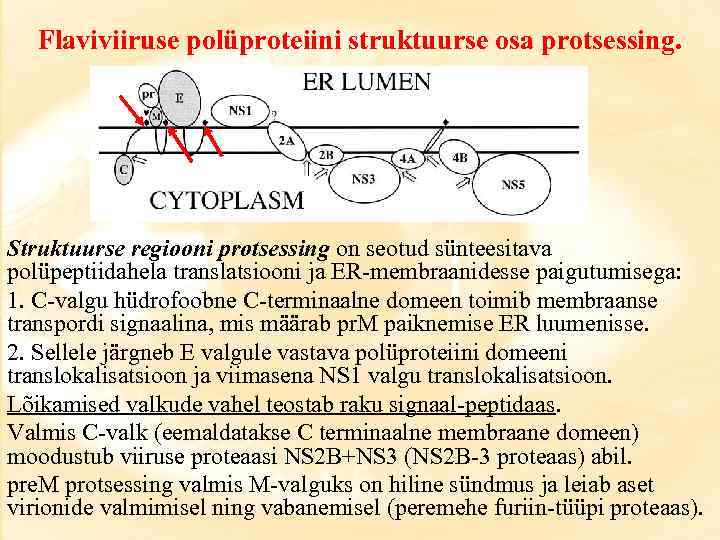 Flaviviiruse polüproteiini struktuurse osa protsessing. Struktuurse regiooni protsessing on seotud sünteesitava polüpeptiidahela translatsiooni ja ER-membraanidesse paigutumisega: 1. C-valgu hüdrofoobne C-terminaalne domeen toimib membraanse transpordi signaalina, mis määrab pr. M paiknemise ER luumenisse. 2. Sellele järgneb E valgule vastava polüproteiini domeeni translokalisatsioon ja viimasena NS 1 valgu translokalisatsioon. Lõikamised valkude vahel teostab raku signaal-peptidaas. Valmis C-valk (eemaldatakse C terminaalne membraane domeen) moodustub viiruse proteaasi NS 2 B+NS 3 (NS 2 B-3 proteaas) abil. pre. M protsessing valmis M-valguks on hiline sündmus ja leiab aset virionide valmimisel ning vabanemisel (peremehe furiin-tüüpi proteaas).
Flaviviiruse polüproteiini struktuurse osa protsessing. Struktuurse regiooni protsessing on seotud sünteesitava polüpeptiidahela translatsiooni ja ER-membraanidesse paigutumisega: 1. C-valgu hüdrofoobne C-terminaalne domeen toimib membraanse transpordi signaalina, mis määrab pr. M paiknemise ER luumenisse. 2. Sellele järgneb E valgule vastava polüproteiini domeeni translokalisatsioon ja viimasena NS 1 valgu translokalisatsioon. Lõikamised valkude vahel teostab raku signaal-peptidaas. Valmis C-valk (eemaldatakse C terminaalne membraane domeen) moodustub viiruse proteaasi NS 2 B+NS 3 (NS 2 B-3 proteaas) abil. pre. M protsessing valmis M-valguks on hiline sündmus ja leiab aset virionide valmimisel ning vabanemisel (peremehe furiin-tüüpi proteaas).
 Polüproteiini ns-osa protsessing. NS 1/2 A saidi protsessing leiab aset ER luumenis (proteaas teadmata), ülejäänud lõikamised toimuvad tsütoplasmas kas: - Viiruse NS 2 B-3 proteaasi poolt (NS 2 B, NS 3, NS 4 A ja NS 5 Nterminused) või - Raku signaal-peptidaasi poolt (NS 4 B N-terminus). Flaviviiruste polüproteiinide protsessingul puudub kindel ajaline järjestus ja tema tulemuseks on viirus-spetsiifilised valgud, mis asuva ER luumeni erinevatel külgedel: - C, NS 2 B-NS 5 paiknevad ER membraani tsütoplasmaatilisel küljel; - pre. M, E ja NS 1 paiknevad ER membraani luumeni poolel küljel ja - NS 2 A paikneb ER membraanis. Enamus flaviviiruste valke on membraanidega tugevasti seotud, vaid NS 3 ja NS 5 on membraanidega nõrgalt seotud
Polüproteiini ns-osa protsessing. NS 1/2 A saidi protsessing leiab aset ER luumenis (proteaas teadmata), ülejäänud lõikamised toimuvad tsütoplasmas kas: - Viiruse NS 2 B-3 proteaasi poolt (NS 2 B, NS 3, NS 4 A ja NS 5 Nterminused) või - Raku signaal-peptidaasi poolt (NS 4 B N-terminus). Flaviviiruste polüproteiinide protsessingul puudub kindel ajaline järjestus ja tema tulemuseks on viirus-spetsiifilised valgud, mis asuva ER luumeni erinevatel külgedel: - C, NS 2 B-NS 5 paiknevad ER membraani tsütoplasmaatilisel küljel; - pre. M, E ja NS 1 paiknevad ER membraani luumeni poolel küljel ja - NS 2 A paikneb ER membraanis. Enamus flaviviiruste valke on membraanidega tugevasti seotud, vaid NS 3 ja NS 5 on membraanidega nõrgalt seotud
 Flaviviiruste valgud C-valk (11 k. Da) on aluseline valk, mis seob RNAd ja moodustab nukleokapsiidi. Pre. M - ja M-valgud (vastavalt 26 ja 8 k. Da) on glükosüleeritud membraanvalgud. E-valk (53 -54 k. Da) on flaviviiruste peamine membraanvalk. E-valk on oluline virionide moodustumiseks, virionide seondumiseks rakkudele (antiretseptor) ning viiruse ja raku membraanide liitumiseks (fusion-valk). NS 1 -valk (35 k. Da) kujutab endast glükoproteiini, mis osaleb RNA replikatsioonis. NS 2 A-valk (24 k. Da) osaleb replikatsioonis teostades RNA maatritsi ja membraanseoselise replikaaskompleksi vahelisi interaktsioone. NS 2 B-valk (14 k. Da) on NS 3 proteaasi abifaktoriks (moodustab NS 3 -ga kompleksi). NS 3 -valk (68 -70 k. Da) omab kolme ensümaatilist aktiivsust. NS 3 on flaviviiruse: - trüpsiini tüüpi seriin-proteaas. - RNA helikaas-NTPaas - RNA-trifosfataas. NS 4 A-valk (16 k. Da) on transmembraane valk, mis osaleb replikatsioonis seondades teisi replikatsiooni kompleksi valke raku membraanile. NS 4 B-valgu (27 k. Da) on seotud replikatsiooni kompleksiga. NS 5 -valk (103 -104 k. Da) on enim konserveerunud flaviviiruste valk. NS 5: • N-terminaalne domeen kujutab endast viirus-spetsiifilist metüültransferaasi; • C-terminaalne domeen on flaviviiruse Rd. Rp.
Flaviviiruste valgud C-valk (11 k. Da) on aluseline valk, mis seob RNAd ja moodustab nukleokapsiidi. Pre. M - ja M-valgud (vastavalt 26 ja 8 k. Da) on glükosüleeritud membraanvalgud. E-valk (53 -54 k. Da) on flaviviiruste peamine membraanvalk. E-valk on oluline virionide moodustumiseks, virionide seondumiseks rakkudele (antiretseptor) ning viiruse ja raku membraanide liitumiseks (fusion-valk). NS 1 -valk (35 k. Da) kujutab endast glükoproteiini, mis osaleb RNA replikatsioonis. NS 2 A-valk (24 k. Da) osaleb replikatsioonis teostades RNA maatritsi ja membraanseoselise replikaaskompleksi vahelisi interaktsioone. NS 2 B-valk (14 k. Da) on NS 3 proteaasi abifaktoriks (moodustab NS 3 -ga kompleksi). NS 3 -valk (68 -70 k. Da) omab kolme ensümaatilist aktiivsust. NS 3 on flaviviiruse: - trüpsiini tüüpi seriin-proteaas. - RNA helikaas-NTPaas - RNA-trifosfataas. NS 4 A-valk (16 k. Da) on transmembraane valk, mis osaleb replikatsioonis seondades teisi replikatsiooni kompleksi valke raku membraanile. NS 4 B-valgu (27 k. Da) on seotud replikatsiooni kompleksiga. NS 5 -valk (103 -104 k. Da) on enim konserveerunud flaviviiruste valk. NS 5: • N-terminaalne domeen kujutab endast viirus-spetsiifilist metüültransferaasi; • C-terminaalne domeen on flaviviiruse Rd. Rp.
 Flaviviiruse RNA replikatsioon Replikatsioon on detekteeritav umbes 3 tundi p. i. Replikatsioon on seotud membraanidega ja leiab aset peamiselt perinukleaarsel ER-il (NB! mitte tuumas!). Flaviviiruse hilises infektsioonis on detekteeritavad replikatsiooni kompleksid, mis koosnevad 100 -200 nm läbimõõduga vesikulitest, milles paiknevad viiruse RNA ja replikatsiooni kompleksi valgud ning milles toimub viiruse RNA süntees. Replikatsioon algab negatiivsete ahelate sünteesiga, moodustub kaheahelaline replikatiivne intermediaat (vabasid negatiivseid RNA ahelaid ei moodustu). Uue põlvkonna positiivsete ahelate süntees toimub kaheahelalisel intermediaadil poolkonservatiivse mehhanismi abil. Süntees on suhteliselt aeglane ja täispika genoomi kopeerimine kestab ca 15 minutit (10 korda enam kui polioviirusel). Positiivseid ahelaid sünteesitakse vähemalt kümme korda enam kui negatiivseid. Erinevalt alphaviirustest toimub flaviviirustel negatiivsete ahelate süntees kogu infektsiooniaja jooksul. Sünteesitud positiivsed ahelad võivad toimida m. RNA-dena, maatritsidena uute negatiivsete ahelate sünteesil või minna moodustatavatesse virionidesse.
Flaviviiruse RNA replikatsioon Replikatsioon on detekteeritav umbes 3 tundi p. i. Replikatsioon on seotud membraanidega ja leiab aset peamiselt perinukleaarsel ER-il (NB! mitte tuumas!). Flaviviiruse hilises infektsioonis on detekteeritavad replikatsiooni kompleksid, mis koosnevad 100 -200 nm läbimõõduga vesikulitest, milles paiknevad viiruse RNA ja replikatsiooni kompleksi valgud ning milles toimub viiruse RNA süntees. Replikatsioon algab negatiivsete ahelate sünteesiga, moodustub kaheahelaline replikatiivne intermediaat (vabasid negatiivseid RNA ahelaid ei moodustu). Uue põlvkonna positiivsete ahelate süntees toimub kaheahelalisel intermediaadil poolkonservatiivse mehhanismi abil. Süntees on suhteliselt aeglane ja täispika genoomi kopeerimine kestab ca 15 minutit (10 korda enam kui polioviirusel). Positiivseid ahelaid sünteesitakse vähemalt kümme korda enam kui negatiivseid. Erinevalt alphaviirustest toimub flaviviirustel negatiivsete ahelate süntees kogu infektsiooniaja jooksul. Sünteesitud positiivsed ahelad võivad toimida m. RNA-dena, maatritsidena uute negatiivsete ahelate sünteesil või minna moodustatavatesse virionidesse.
 Flaviviiruste replikatsioonikompleks EM tomograafiga tehtud vaated DENV indutseeritud struktuuridele näitavad ühe katkematu võrgustiku, kuhu kuuluvad ERsist pärinevad membraanid, ja nendest moodustunud “sfäärulid” (milles paikneb ds. RNA) olemasolu nakatud rakus. Sfäärulitel on poorid, mille kaudu väljuvad sünteesitud RNA molekulid. Virionide moodustamine on otseselt seotud nende RNAde väljumisega sfäärulitest, st. toimub vahetult samas regioonis. Seega modifitseerivad flaviviirused ERmembraane ja saavutavad sellega viiruse valgusünteesi, viiruse valkude modifitseerimise, RNA replikatsiooni ja RNA-de pakkimise koordineerituse.
Flaviviiruste replikatsioonikompleks EM tomograafiga tehtud vaated DENV indutseeritud struktuuridele näitavad ühe katkematu võrgustiku, kuhu kuuluvad ERsist pärinevad membraanid, ja nendest moodustunud “sfäärulid” (milles paikneb ds. RNA) olemasolu nakatud rakus. Sfäärulitel on poorid, mille kaudu väljuvad sünteesitud RNA molekulid. Virionide moodustamine on otseselt seotud nende RNAde väljumisega sfäärulitest, st. toimub vahetult samas regioonis. Seega modifitseerivad flaviviirused ERmembraane ja saavutavad sellega viiruse valgusünteesi, viiruse valkude modifitseerimise, RNA replikatsiooni ja RNA-de pakkimise koordineerituse.
 Flaviviiruse virionide moodustumine ja vabanemine Virionide moodustumine leiab aset rakusisestel membraanidel: - C-valgu aluselised N- ja C-terminused interageeruvad genoomse RNAga. - Membraan omandatakse ER membraanist, pungumine toimub luumenisse, kus asuvad pre. M ja E valgud. Interaktsioon C-valguga toimub arvatavasti pre. M ja E-valkude tsütoplamaatiliste domeenide kaudu. Olulised on mitte ainult membraanid, vaid ka lipiid-tilgad - Vahetult enne vabanemist keskkonda leiab aset post-Golgi ensüümide poolt katalüüsitud pre. M protsessing (erinevatel viirustel erineval määral). See protsessing on vajalik virionide infektsioonilisuse tõstmiseks. Arvatavasti on pre. M funktsiooniks vältida E-valgu konformatsioonilist muutust, mis võiks aset leida transpordi käigus tema puudumisel (kui transport kulgeb läbi madala p. H-iga kompartmentite). - Virionid vabanevad raku pinnalt eksotsütoosi teel.
Flaviviiruse virionide moodustumine ja vabanemine Virionide moodustumine leiab aset rakusisestel membraanidel: - C-valgu aluselised N- ja C-terminused interageeruvad genoomse RNAga. - Membraan omandatakse ER membraanist, pungumine toimub luumenisse, kus asuvad pre. M ja E valgud. Interaktsioon C-valguga toimub arvatavasti pre. M ja E-valkude tsütoplamaatiliste domeenide kaudu. Olulised on mitte ainult membraanid, vaid ka lipiid-tilgad - Vahetult enne vabanemist keskkonda leiab aset post-Golgi ensüümide poolt katalüüsitud pre. M protsessing (erinevatel viirustel erineval määral). See protsessing on vajalik virionide infektsioonilisuse tõstmiseks. Arvatavasti on pre. M funktsiooniks vältida E-valgu konformatsioonilist muutust, mis võiks aset leida transpordi käigus tema puudumisel (kui transport kulgeb läbi madala p. H-iga kompartmentite). - Virionid vabanevad raku pinnalt eksotsütoosi teel.
 Flaviviiruse infektsiooni mõju peremeesrakule • Flaviviiruste infektsioon on erinevatele rakkudele erineva tsütopatogeensusega: • imetajate rakkudes põhjustab infektsioon enamasti tugevaid tsütopatoloogilisi efekte (vakuoliseerimine jne), samas ei inhibeeri flaviviirused peremehe makromolekulide sünteesi; • tsütopatoloogilised efektid lülijalgse vektori rakkudele kas on väiksemad (enamasti indutseeritakse rakkude liitumist) või on infektsioon mittetsütopaatiline: moskiitod jäävad viirusega persistentselt nakkunuks kogu elu jooksul ja toodavad oma süljenäärmeis väga suurel hulgal uusi virione.
Flaviviiruse infektsiooni mõju peremeesrakule • Flaviviiruste infektsioon on erinevatele rakkudele erineva tsütopatogeensusega: • imetajate rakkudes põhjustab infektsioon enamasti tugevaid tsütopatoloogilisi efekte (vakuoliseerimine jne), samas ei inhibeeri flaviviirused peremehe makromolekulide sünteesi; • tsütopatoloogilised efektid lülijalgse vektori rakkudele kas on väiksemad (enamasti indutseeritakse rakkude liitumist) või on infektsioon mittetsütopaatiline: moskiitod jäävad viirusega persistentselt nakkunuks kogu elu jooksul ja toodavad oma süljenäärmeis väga suurel hulgal uusi virione.
 Perekond Hepacivirus – hepatiidi C viirus (HCV) HCV on perekonna Hepacivirus ainus esindaja. Teada kuus peamist HCV subtüüpi, mis kõik kujutavad põhimõtteliselt endast iseseisvaid liike ja on erinevalt levinud erinevates maailma osades. Vaatamata laialdasele levikule ja ülisuurele meditsiinilisele tähtsusele avastati HCV alles 1989 aastal. Sellest ajast on seda viirust väga intensiivselt uuritud. HCV kujutab ühte kolmest kõige ohtlikumast inimese viiruslikust patogeenist: - HCV akuutne infektsioon esineb suhteliselt harva (umbes 25% nakkuse juhtudest); - HCV tekitab tavaliselt kroonilise infektsiooni (ca 70% infektsiooni juhtudest, k. a. täiskasvanutel), mis võib viia maksa tsirroosi või HCC tekkimisele; - HCV on seotud ka teiste haigustega, seal hulgas ka autoimmuunhaigustega; HCV vastu pole vaktsiini. Ajalooliselt kasutati raviks ribaviriini ja interferooni kombineeritud ravi, kuid selle ravi efektiivsus on mõnede HCV tüüpide (HCV-1 b) puhul alla 30%. Nüüd on kasutusel ka HCV proteaasi, NS 5 A valgu ja polümeraasi inhibiitorid. Intensiivsetele uuringutele vaatamata on andmeid HCV bioloogia kohta suhteliselt vähe, kuna HCV paljundamine rakukultuuris on väga keeruline (esmakordselt õnnestus see 2005 aastal). Ka on HCV peremeeste ring väga piiratud (inimesed ja šimpansid) ning erinevalt HBV-st puuduvad HCV-l odavad loommudelid. Selle tõttu pärineb enamus HCV-d puudutavaid andmeid kunstlikest süsteemidest. Ka on HCV poolt kodeeritud valke funktsionaalselt ja struktuurselt väga intensiivselt uuritud – enam kui pooltel HCV genoomi poolt kodeeritud valkudel on tehtud kristallstruktuur-analüüs.
Perekond Hepacivirus – hepatiidi C viirus (HCV) HCV on perekonna Hepacivirus ainus esindaja. Teada kuus peamist HCV subtüüpi, mis kõik kujutavad põhimõtteliselt endast iseseisvaid liike ja on erinevalt levinud erinevates maailma osades. Vaatamata laialdasele levikule ja ülisuurele meditsiinilisele tähtsusele avastati HCV alles 1989 aastal. Sellest ajast on seda viirust väga intensiivselt uuritud. HCV kujutab ühte kolmest kõige ohtlikumast inimese viiruslikust patogeenist: - HCV akuutne infektsioon esineb suhteliselt harva (umbes 25% nakkuse juhtudest); - HCV tekitab tavaliselt kroonilise infektsiooni (ca 70% infektsiooni juhtudest, k. a. täiskasvanutel), mis võib viia maksa tsirroosi või HCC tekkimisele; - HCV on seotud ka teiste haigustega, seal hulgas ka autoimmuunhaigustega; HCV vastu pole vaktsiini. Ajalooliselt kasutati raviks ribaviriini ja interferooni kombineeritud ravi, kuid selle ravi efektiivsus on mõnede HCV tüüpide (HCV-1 b) puhul alla 30%. Nüüd on kasutusel ka HCV proteaasi, NS 5 A valgu ja polümeraasi inhibiitorid. Intensiivsetele uuringutele vaatamata on andmeid HCV bioloogia kohta suhteliselt vähe, kuna HCV paljundamine rakukultuuris on väga keeruline (esmakordselt õnnestus see 2005 aastal). Ka on HCV peremeeste ring väga piiratud (inimesed ja šimpansid) ning erinevalt HBV-st puuduvad HCV-l odavad loommudelid. Selle tõttu pärineb enamus HCV-d puudutavaid andmeid kunstlikest süsteemidest. Ka on HCV poolt kodeeritud valke funktsionaalselt ja struktuurselt väga intensiivselt uuritud – enam kui pooltel HCV genoomi poolt kodeeritud valkudel on tehtud kristallstruktuur-analüüs.
 HCV virion ja genoom HCV virionid sarnanevad flaviviiruste virionidele ja omavad diameetrit ca 50 nm (nukleokapsiid 30 nm). HCV virionidesse kuulub kolm valku: - nukleokapsiidivalk C; -kaks glükoproteiini (E 1 ja E 2). Isenesest pole need partiklid infektsioonilised, infektsiooniline osake on lipoviropartikkel Genoom (9. 4 – 9. 6 kb) on lühem kui teistel Flaviviridae esindajatel. Teda iseloomustab: - genoomi 5’-otsas puudub cap-struktuur (HCV ei kodeeri ka cap-struktuuri sünteesi teostavaid ensüüme – trifosfataasi ja metüültransferaasi). - 5’-NTR on ca 340 b pikkune, väga konserveerunud ja sisaldab (komplementaarses orientatsioonis) positiivse ahela replikatsiooniks olulisi cis-järjestusi. Peale selle paikneb 5’-NTR regioonis IRES element. - genoomi kodeeriv ala koosneb ühest ORF-ist (pikkus ca 3000 koodonit); - genoomi 3’-NTR-is paiknevad: a. lühike (40 b) varieeruv regioon; b. selle järel paikneb varieeruv polü(U)/polü-pürimidiin järjestus; c. genoomi otsas asub väga konserveerunud 98 -st nukleotiidist koosnev järjestus, mille viimased 45 b moodustavad stabiilse stem-loop struktuuri. Kaks viimast (b ja c) elementi on vajalikud HCV genoomi replikatsiooniks. Polü(A) järjestus HCV-l puudub
HCV virion ja genoom HCV virionid sarnanevad flaviviiruste virionidele ja omavad diameetrit ca 50 nm (nukleokapsiid 30 nm). HCV virionidesse kuulub kolm valku: - nukleokapsiidivalk C; -kaks glükoproteiini (E 1 ja E 2). Isenesest pole need partiklid infektsioonilised, infektsiooniline osake on lipoviropartikkel Genoom (9. 4 – 9. 6 kb) on lühem kui teistel Flaviviridae esindajatel. Teda iseloomustab: - genoomi 5’-otsas puudub cap-struktuur (HCV ei kodeeri ka cap-struktuuri sünteesi teostavaid ensüüme – trifosfataasi ja metüültransferaasi). - 5’-NTR on ca 340 b pikkune, väga konserveerunud ja sisaldab (komplementaarses orientatsioonis) positiivse ahela replikatsiooniks olulisi cis-järjestusi. Peale selle paikneb 5’-NTR regioonis IRES element. - genoomi kodeeriv ala koosneb ühest ORF-ist (pikkus ca 3000 koodonit); - genoomi 3’-NTR-is paiknevad: a. lühike (40 b) varieeruv regioon; b. selle järel paikneb varieeruv polü(U)/polü-pürimidiin järjestus; c. genoomi otsas asub väga konserveerunud 98 -st nukleotiidist koosnev järjestus, mille viimased 45 b moodustavad stabiilse stem-loop struktuuri. Kaks viimast (b ja c) elementi on vajalikud HCV genoomi replikatsiooniks. Polü(A) järjestus HCV-l puudub
 HCV infektsiooni algus HCV infektsioonitsüklit sai kuni 2005 aastani uurida ainult nakatatud organismis (kusjuures peale inimese nakatab HCV ainult šimpanse). Peamine HCV replikatsioon leiab aset maksarakkudes ja on küllalt intensiivne (kroonilises infektsioonis moodustub ööpäeva jooksul kuni 1012 HCV virioni), kuid tõenäoliselt üsna vähe patogeene (sarnaselt HBV infektsioonile on ka HCV infektsioonis tekkivate maksakahjustuste peamine põhjus peremehe immuunsüsteemide rünnak). Kroonilises infektsioonis replitseerub HCV ka mingites teistes rakkudes (B- ja T-lümfotsüüdid ja monotsüüdid). HCV-l on teada neli retseptorit, mis kõik on viiruse sisenemiseks vajalikud. Samas pole välistatud, et rakust-rakku liikumiseks kasutatakse muidki mehhanisme. Teada on ka abifaktorite ning ADE-mehhanismi kasutamine. Antiretseptor on E 2 glükoproteiin. HCV sisenemine rakkudesse toimub tõenäoliselt retseptor-vahendatud endotsütoosi ja sellele järgneva p. H-st sõltuva membraanide liitumise teel.
HCV infektsiooni algus HCV infektsioonitsüklit sai kuni 2005 aastani uurida ainult nakatatud organismis (kusjuures peale inimese nakatab HCV ainult šimpanse). Peamine HCV replikatsioon leiab aset maksarakkudes ja on küllalt intensiivne (kroonilises infektsioonis moodustub ööpäeva jooksul kuni 1012 HCV virioni), kuid tõenäoliselt üsna vähe patogeene (sarnaselt HBV infektsioonile on ka HCV infektsioonis tekkivate maksakahjustuste peamine põhjus peremehe immuunsüsteemide rünnak). Kroonilises infektsioonis replitseerub HCV ka mingites teistes rakkudes (B- ja T-lümfotsüüdid ja monotsüüdid). HCV-l on teada neli retseptorit, mis kõik on viiruse sisenemiseks vajalikud. Samas pole välistatud, et rakust-rakku liikumiseks kasutatakse muidki mehhanisme. Teada on ka abifaktorite ning ADE-mehhanismi kasutamine. Antiretseptor on E 2 glükoproteiin. HCV sisenemine rakkudesse toimub tõenäoliselt retseptor-vahendatud endotsütoosi ja sellele järgneva p. H-st sõltuva membraanide liitumise teel.
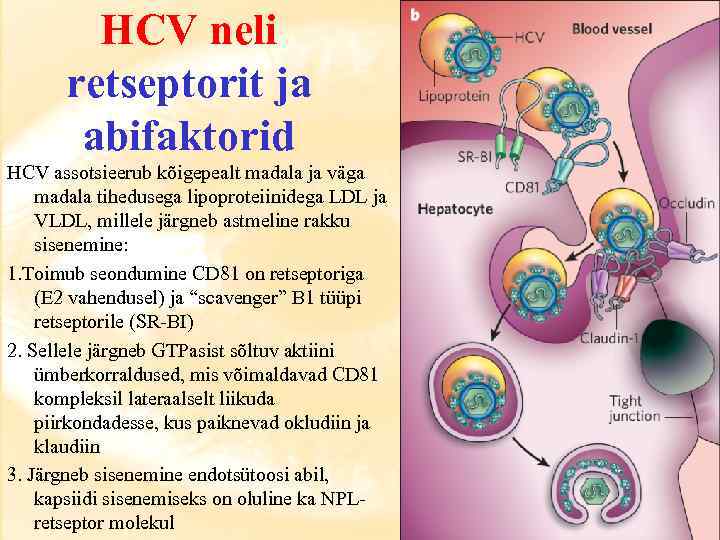 HCV neli retseptorit ja abifaktorid HCV assotsieerub kõigepealt madala ja väga madala tihedusega lipoproteiinidega LDL ja VLDL, millele järgneb astmeline rakku sisenemine: 1. Toimub seondumine CD 81 on retseptoriga (E 2 vahendusel) ja “scavenger” B 1 tüüpi retseptorile (SR-BI) 2. Sellele järgneb GTPasist sõltuv aktiini ümberkorraldused, mis võimaldavad CD 81 kompleksil lateraalselt liikuda piirkondadesse, kus paiknevad okludiin ja klaudiin 3. Järgneb sisenemine endotsütoosi abil, kapsiidi sisenemiseks on oluline ka NPLretseptor molekul
HCV neli retseptorit ja abifaktorid HCV assotsieerub kõigepealt madala ja väga madala tihedusega lipoproteiinidega LDL ja VLDL, millele järgneb astmeline rakku sisenemine: 1. Toimub seondumine CD 81 on retseptoriga (E 2 vahendusel) ja “scavenger” B 1 tüüpi retseptorile (SR-BI) 2. Sellele järgneb GTPasist sõltuv aktiini ümberkorraldused, mis võimaldavad CD 81 kompleksil lateraalselt liikuda piirkondadesse, kus paiknevad okludiin ja klaudiin 3. Järgneb sisenemine endotsütoosi abil, kapsiidi sisenemiseks on oluline ka NPLretseptor molekul
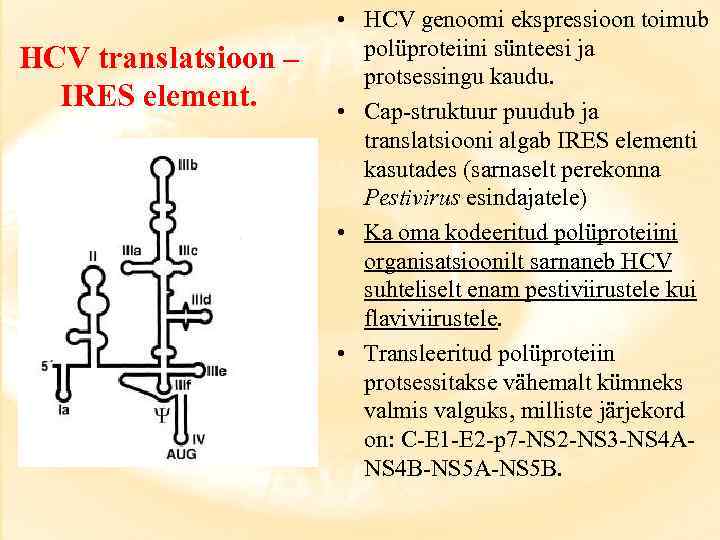 HCV translatsioon – IRES element. • HCV genoomi ekspressioon toimub polüproteiini sünteesi ja protsessingu kaudu. • Cap-struktuur puudub ja translatsiooni algab IRES elementi kasutades (sarnaselt perekonna Pestivirus esindajatele) • Ka oma kodeeritud polüproteiini organisatsioonilt sarnaneb HCV suhteliselt enam pestiviirustele kui flaviviirustele. • Transleeritud polüproteiin protsessitakse vähemalt kümneks valmis valguks, milliste järjekord on: C-E 1 -E 2 -p 7 -NS 2 -NS 3 -NS 4 ANS 4 B-NS 5 A-NS 5 B.
HCV translatsioon – IRES element. • HCV genoomi ekspressioon toimub polüproteiini sünteesi ja protsessingu kaudu. • Cap-struktuur puudub ja translatsiooni algab IRES elementi kasutades (sarnaselt perekonna Pestivirus esindajatele) • Ka oma kodeeritud polüproteiini organisatsioonilt sarnaneb HCV suhteliselt enam pestiviirustele kui flaviviirustele. • Transleeritud polüproteiin protsessitakse vähemalt kümneks valmis valguks, milliste järjekord on: C-E 1 -E 2 -p 7 -NS 2 -NS 3 -NS 4 ANS 4 B-NS 5 A-NS 5 B.
 HCV polüproteiini protsessing. Protsessing on sõltuv peremeesraku mikrosoomsetest membraanidest ja on vähemalt osaliselt ko-translatsiooniline protsess. Polüproteiini struktuurse osa protsessingut teostab peremehe signaal-peptidaas (mustad rombid) Mittestruktuurse osa protessingut teostavad: - tsink-sõltuv metall-proteaas (NS 2 -NS 3, lõikab in cis iseennast polüproteiinist lahti, tume nool) - NS 3 seriin-proteaas (tühi nool), mis lõikab ülejäänud saite ja mille aktiivsuseks on vajalik ka kofaktori NS 4 A olemasolu.
HCV polüproteiini protsessing. Protsessing on sõltuv peremeesraku mikrosoomsetest membraanidest ja on vähemalt osaliselt ko-translatsiooniline protsess. Polüproteiini struktuurse osa protsessingut teostab peremehe signaal-peptidaas (mustad rombid) Mittestruktuurse osa protessingut teostavad: - tsink-sõltuv metall-proteaas (NS 2 -NS 3, lõikab in cis iseennast polüproteiinist lahti, tume nool) - NS 3 seriin-proteaas (tühi nool), mis lõikab ülejäänud saite ja mille aktiivsuseks on vajalik ka kofaktori NS 4 A olemasolu.
 HCV valgud C-valk on HCV kapsiidivalk (tugevasti aluseliste omadustega valk). Virionide moodustamisel seondub C-valk viiruse genoomse RNA-ga ja E 1 glükoproteiiniga. Andmed C-valgu muude funktsioonide kohta on vastukäivaid. On näidatud, et: - C-valgu trankeeritud vormid liiguvad tuuma ja mõjutavad seal geeniekspressiooni; - C-valk interageerub TNF ja lümfotoksin- retseptoritega (moduleerib peremehe viirus -vastast reaktsiooni? ); - C-valk võib koos raku ras-onkovalguga transformeerida roti primaarseid fibroblaste. E 1 ja E 2 (31 ja 70 k. Da) on transmembraansed glükoproteiinid. Rakus paiknevad E 1 ja E 2 endomembraanidel (mitte plasmamembraanil). E 1 ja E 2 on olulised virionide valmimisel, virionide seondumisel ja sisenemisel rakkudesse: - E 1 ja E 2 moodustavad nakatatud rakkude membraanis heterodimeere; - E 1 valgus (ah jäägid 264 -290) asub fusion-peptiid; - E 2 valk on HCV antiretseptor ja seondab HCV retseptorit CD 81 (tetraspanin). E 2 valk on oluline viirus-nakatatud rakkude kaitsmisel peremehe immuunsüsteemi eest: - E 2 valgus asub hüpervarieeruv regioon, mis kujutab endast kaitset peremehe immuunsüsteemi eest (escape-mutantide tekkimine infektsiooni käigus); - E 2 valk surub maha PKR funktsiooni. p 7 valgu kuulumine virionidesse pole üheselt selge, ta kujutab endast ioonkanali valku
HCV valgud C-valk on HCV kapsiidivalk (tugevasti aluseliste omadustega valk). Virionide moodustamisel seondub C-valk viiruse genoomse RNA-ga ja E 1 glükoproteiiniga. Andmed C-valgu muude funktsioonide kohta on vastukäivaid. On näidatud, et: - C-valgu trankeeritud vormid liiguvad tuuma ja mõjutavad seal geeniekspressiooni; - C-valk interageerub TNF ja lümfotoksin- retseptoritega (moduleerib peremehe viirus -vastast reaktsiooni? ); - C-valk võib koos raku ras-onkovalguga transformeerida roti primaarseid fibroblaste. E 1 ja E 2 (31 ja 70 k. Da) on transmembraansed glükoproteiinid. Rakus paiknevad E 1 ja E 2 endomembraanidel (mitte plasmamembraanil). E 1 ja E 2 on olulised virionide valmimisel, virionide seondumisel ja sisenemisel rakkudesse: - E 1 ja E 2 moodustavad nakatatud rakkude membraanis heterodimeere; - E 1 valgus (ah jäägid 264 -290) asub fusion-peptiid; - E 2 valk on HCV antiretseptor ja seondab HCV retseptorit CD 81 (tetraspanin). E 2 valk on oluline viirus-nakatatud rakkude kaitsmisel peremehe immuunsüsteemi eest: - E 2 valgus asub hüpervarieeruv regioon, mis kujutab endast kaitset peremehe immuunsüsteemi eest (escape-mutantide tekkimine infektsiooni käigus); - E 2 valk surub maha PKR funktsiooni. p 7 valgu kuulumine virionidesse pole üheselt selge, ta kujutab endast ioonkanali valku
 HCV valgud NS 2 (23 k. Da) NS 2 sisaldab tsüsteiin-proteinaaset domeeni, mis interageerub NS 3 valgu 180 -st N -terminaalsest ah. jäägist koosneva domeeniga ja moodustab aktiivse, tsink-ioonide poolt aktiveeritava proteaasi, mis teostab NS 2/3 vahelise saidi protsessingut. NS 3 (70 k. Da) on seriin-proteaas (N-terminaalne osa) ja RNA helikaas/NTPase (C-terminaalne osa). NS 3 moodustabiilse kompleksi NS 4 A kofaktoriga (see seondub NS 3 N-terminaalse regiooniga), mis aktiveerib NS 3 proteaase ja helikaaset aktiivsust. Peale selle on HCV NS 3 -el kirjeldatud veel muidki funktsioone: - HCV NS 3 -l on kirjeldatud nõrgad transformeerivad omadused -HCV NS 3 proteaas surub maha actinomycin-D indutseeritud apoptoosi. -HCV NS 3 proteaas on peremehe innate immune response inhibiitor ja blokeerib tsütoplasmaatilistel helikaasidelt algavat signaalülekannet. NS 4 A (8 k. Da) on NS 3 valgu kofaktoriks. NS 4 B (30 k. Da) on hüdrofoobne valk (funktsioon teadmata). NS 5 A (58 k. DA) on membraanidega seotud fosfoproteiin. On teada, et: - NS 5 A blokeerib (seondades ja inhibeerides PKR-i) interferoonide toimet. - NS 5 A on vajalik HCV RNA replikatsiooniks. NS 5 B (68 k. Da) on HCV Rd. Rp. Individuaalne HCV NS 5 B on maatritsi suhtes üsna ebaspetsiifiline ensüüm. Rakkudes seondub HCV NS 5 B perinukleaarsetele membraanidele ja interageerub NS 3 -, NS 4 A, NS 4 B- ja NS 5 A-valkude ning HCV genoomse RNA-ga.
HCV valgud NS 2 (23 k. Da) NS 2 sisaldab tsüsteiin-proteinaaset domeeni, mis interageerub NS 3 valgu 180 -st N -terminaalsest ah. jäägist koosneva domeeniga ja moodustab aktiivse, tsink-ioonide poolt aktiveeritava proteaasi, mis teostab NS 2/3 vahelise saidi protsessingut. NS 3 (70 k. Da) on seriin-proteaas (N-terminaalne osa) ja RNA helikaas/NTPase (C-terminaalne osa). NS 3 moodustabiilse kompleksi NS 4 A kofaktoriga (see seondub NS 3 N-terminaalse regiooniga), mis aktiveerib NS 3 proteaase ja helikaaset aktiivsust. Peale selle on HCV NS 3 -el kirjeldatud veel muidki funktsioone: - HCV NS 3 -l on kirjeldatud nõrgad transformeerivad omadused -HCV NS 3 proteaas surub maha actinomycin-D indutseeritud apoptoosi. -HCV NS 3 proteaas on peremehe innate immune response inhibiitor ja blokeerib tsütoplasmaatilistel helikaasidelt algavat signaalülekannet. NS 4 A (8 k. Da) on NS 3 valgu kofaktoriks. NS 4 B (30 k. Da) on hüdrofoobne valk (funktsioon teadmata). NS 5 A (58 k. DA) on membraanidega seotud fosfoproteiin. On teada, et: - NS 5 A blokeerib (seondades ja inhibeerides PKR-i) interferoonide toimet. - NS 5 A on vajalik HCV RNA replikatsiooniks. NS 5 B (68 k. Da) on HCV Rd. Rp. Individuaalne HCV NS 5 B on maatritsi suhtes üsna ebaspetsiifiline ensüüm. Rakkudes seondub HCV NS 5 B perinukleaarsetele membraanidele ja interageerub NS 3 -, NS 4 A, NS 4 B- ja NS 5 A-valkude ning HCV genoomse RNA-ga.
 HCV replikatsioon ja virionide moodustamine RNA replikatsioon. NS 3, NS 4 A, NS 4 B, NS 5 A ja NS 5 B moodustavad perinukleaarsete ER membraanidega seotud replikaasi kompleksi, mille omadused on sarnased flaviviiruste replikaasi kompleksile. Tõenäoliselt kuulub kompleksi ka raku poolseid faktoreid. Nakatunud rakkudes sünteesitakse kuni 5000 RNA koopiat viiruse RNA-d, seejuures positiivseid ahelaid sünteesitakse 5 -10 korda rohkem kui negatiivseid ahelaid. Virionide valmimine ja vabanemine. HCV virionide moodustamine on seotud replikatsioonikompleksite ja lipiidi-tilkade (LD) struktuuridega. LD- seondavad viiruse core-valku, mis omakorda seondab mittestruktuurseid valke. Selle tulemusena interakteeruvad LD-d otseselt replikatsioonikompleksitega ja nende poolt sünteesitavate genoomidega.
HCV replikatsioon ja virionide moodustamine RNA replikatsioon. NS 3, NS 4 A, NS 4 B, NS 5 A ja NS 5 B moodustavad perinukleaarsete ER membraanidega seotud replikaasi kompleksi, mille omadused on sarnased flaviviiruste replikaasi kompleksile. Tõenäoliselt kuulub kompleksi ka raku poolseid faktoreid. Nakatunud rakkudes sünteesitakse kuni 5000 RNA koopiat viiruse RNA-d, seejuures positiivseid ahelaid sünteesitakse 5 -10 korda rohkem kui negatiivseid ahelaid. Virionide valmimine ja vabanemine. HCV virionide moodustamine on seotud replikatsioonikompleksite ja lipiidi-tilkade (LD) struktuuridega. LD- seondavad viiruse core-valku, mis omakorda seondab mittestruktuurseid valke. Selle tulemusena interakteeruvad LD-d otseselt replikatsioonikompleksitega ja nende poolt sünteesitavate genoomidega.
 HCV ja onkogenees. HCV primaarne infektsioon läheb ligi 70% juhtudel üle krooniliseks infektsiooniks. Suur osa (20 -30%) kroonilise HCV infektsiooni juhtudest viib maksatsirroosi ja järgnevalt maksavähi (hepatocellular carcinoma, HCC) tekkimisele. HCV infektsioonist põhjustatud HCC tekkimise aeg on keskmiselt 20 – 30 aastat. Kasvajarakkudes ei esine alati HCV genoome, mistõttu oletatakse, et HCC tekkimine on kaudse mehhanismi tulemus (sarnaselt HBV-ga). Samas ei saa veel täielikult välistada ka mingite HCV geeniproduktide otsest rolli HCC tekkimises. Peamised kandidaadid sellise faktori rollile on C-valk, NS 3 -valk, NS 4 B või NS 5 A.
HCV ja onkogenees. HCV primaarne infektsioon läheb ligi 70% juhtudel üle krooniliseks infektsiooniks. Suur osa (20 -30%) kroonilise HCV infektsiooni juhtudest viib maksatsirroosi ja järgnevalt maksavähi (hepatocellular carcinoma, HCC) tekkimisele. HCV infektsioonist põhjustatud HCC tekkimise aeg on keskmiselt 20 – 30 aastat. Kasvajarakkudes ei esine alati HCV genoome, mistõttu oletatakse, et HCC tekkimine on kaudse mehhanismi tulemus (sarnaselt HBV-ga). Samas ei saa veel täielikult välistada ka mingite HCV geeniproduktide otsest rolli HCC tekkimises. Peamised kandidaadid sellise faktori rollile on C-valk, NS 3 -valk, NS 4 B või NS 5 A.
 HCV teraapia aastani 2010
HCV teraapia aastani 2010
 Esimesed litsenseeritud NS 3/4 A inhibiitorid Telaprevir (ülal) ja boceprevir (all) said kasutusloa 2011 mais. Mõlemad on HCV 1 b spetsiifilised proteaasi inhibiitorid (vähemal määral mõjuvad ka HCV 1 a genotüübile) ja mimikreerivad NS 3/4 A substraati. Ensüüm neid ei lõika, selle asemel seonduvad nad kovalentselt sihtmärgile ja inaktiveerivad selle. Efektiivsus koos interferooni ja ribaviriiniga on ca 7080% (30% parem kui neid ühendeid mitte kasutades). Probleemid on samuti sarnased: 1. Mõlemal on tugevad kõrvalefektid (sh. lööve) 2. Võetakse (suu kaudu) kolm korda päevas, ravikuur 12 nädalat 3. Ilma ribaviriini ja interferoonita kasutada ei saa (tekib resistentsus) 4. Identsed resistentsuse profiilid 5. Kallid (>30 000 EUR ravikuuri kohta) 6. Kasutamise protokoll on keeruline mis loob võimaluse ravivigade tekkimiseks
Esimesed litsenseeritud NS 3/4 A inhibiitorid Telaprevir (ülal) ja boceprevir (all) said kasutusloa 2011 mais. Mõlemad on HCV 1 b spetsiifilised proteaasi inhibiitorid (vähemal määral mõjuvad ka HCV 1 a genotüübile) ja mimikreerivad NS 3/4 A substraati. Ensüüm neid ei lõika, selle asemel seonduvad nad kovalentselt sihtmärgile ja inaktiveerivad selle. Efektiivsus koos interferooni ja ribaviriiniga on ca 7080% (30% parem kui neid ühendeid mitte kasutades). Probleemid on samuti sarnased: 1. Mõlemal on tugevad kõrvalefektid (sh. lööve) 2. Võetakse (suu kaudu) kolm korda päevas, ravikuur 12 nädalat 3. Ilma ribaviriini ja interferoonita kasutada ei saa (tekib resistentsus) 4. Identsed resistentsuse profiilid 5. Kallid (>30 000 EUR ravikuuri kohta) 6. Kasutamise protokoll on keeruline mis loob võimaluse ravivigade tekkimiseks
 HCV NS 5 B inhibiitorid: ajalugu ja kaasaeg ► NM 283 on prodrug, mis rakus muudetakse CTP analoogiks. Selline ühend surus viiruse tiitrit maha kuni 10 -korda, kuid efekt oli lühiajaline: kiiresti tekkis resistentsus viiruse polümeraas “õppis” vahet tegama tõelisel substraadil ja substraadi analoogil. Resistentsuse tekkimiseks piisas ühest punktmutatsioonist. ►Sofosbuvir (Solvadi, GS-7977, PSI-7977) inhibeerib kõiki HCV genotüüpe, omab kõrget aktiivsust ja väga kõrget resistentsus-barjääri. Sai kasutusloa 2013 novembris ja kujunes kõigi aegade suurima müügieduga ravimiks. Kõrvalefektid on väikesed, ei vaja interferooni ja ribaviriini kaasmanustamist. Kasutatakse koos NS 5 A inhibiitori ledipasvir’ iga, efektiivsus on sellisel ravil >95%. Kallis, ravi võib kesta kuni 168 päeva, 1 tablet maksab 1000 dollarit
HCV NS 5 B inhibiitorid: ajalugu ja kaasaeg ► NM 283 on prodrug, mis rakus muudetakse CTP analoogiks. Selline ühend surus viiruse tiitrit maha kuni 10 -korda, kuid efekt oli lühiajaline: kiiresti tekkis resistentsus viiruse polümeraas “õppis” vahet tegama tõelisel substraadil ja substraadi analoogil. Resistentsuse tekkimiseks piisas ühest punktmutatsioonist. ►Sofosbuvir (Solvadi, GS-7977, PSI-7977) inhibeerib kõiki HCV genotüüpe, omab kõrget aktiivsust ja väga kõrget resistentsus-barjääri. Sai kasutusloa 2013 novembris ja kujunes kõigi aegade suurima müügieduga ravimiks. Kõrvalefektid on väikesed, ei vaja interferooni ja ribaviriini kaasmanustamist. Kasutatakse koos NS 5 A inhibiitori ledipasvir’ iga, efektiivsus on sellisel ravil >95%. Kallis, ravi võib kesta kuni 168 päeva, 1 tablet maksab 1000 dollarit


