Санжаровська.ppt
- Количество слайдов: 12
Портфолiо Тема: Будова речовини. Пiдготувала учениця 7 -Ф класу Санжаровська Валерiя
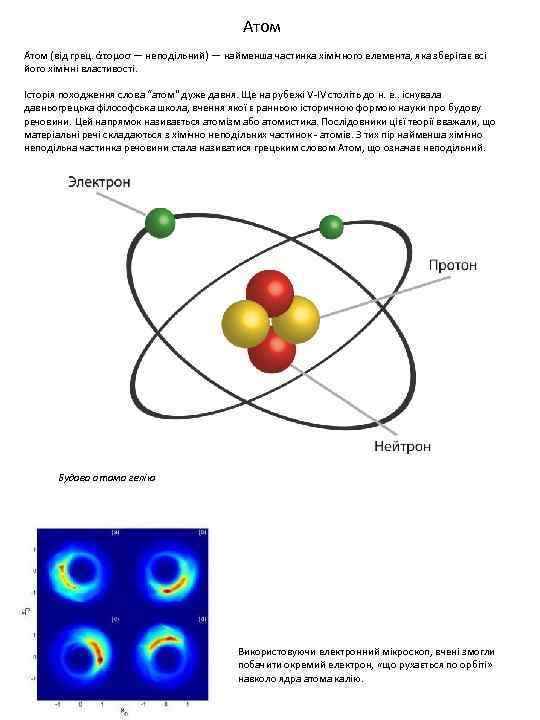
Атом А том (від грец. άτομοσ — неподільний) — найменша частинка хімічного елемента, яка зберігає всі його хімічні властивості. Історія походження слова “атом" дуже давня. Ще на рубежі V-IV століть до н. е. . існувала давньогрецька філософська школа, вчення якої є ранньою історичною формою науки про будову речовини. Цей напрямок називається атомізм або атомистика. Послідовники цієї теорії вважали, що матеріальні речі складаються з хімічно неподільних частинок - атомів. З тих пір найменша хімічно неподільна частинка речовини стала називатися грецьким словом Атом, що означає неподільний. Будова атома гелію Використовуючи електронний мікроскоп, вчені змогли побачити окремий електрон, «що рухається по орбіті» навколо ядра атома калію.

Будова і властивості атома Ядро атома складається з позитивно заряджених протонів і незаряджених нейтронів. Якщо число протонів в ядрі збігається з числом електронів, то атом в цілому виявляється електрично нейтральним. В іншому випадку він володіє деяким позитивним або негативним зарядом і називається іоном. Атоми класифікуються за кількістю протонів і нейтронів в ядрі: кількість протонів визначає належність атома деякому хімічному елементу, а число нейтронів - ізотопу цього елемента. Розміри атомів демонструють наступні приклади. Людське волосся по товщині в мільйон разів більше атома вуглецю. Одна крапля води містить 2 секстильйонів (2 × 1021) атомів кисню, і в два рази більше атомів водню. Один карат алмаза з масою 0, 2 г складається з 10 секстильйонів атомів вуглецю. Якби яблуко можна було збільшити до розмірів Землі, то атоми досягли б початкових розмірів яблука.

Молекула У порівнянні з різноманіттям речовин число атомів вельми обмежене. Атоми можуть різним чином з'єднуватися один з одним. Як з букв алфавіту можна скласти сотні тисяч слів, так з одних і тих самих атомів утворюються молекули або кристали величезної кількості різних речовин, з яких складається навколишній світ. Молекула - це дрібна частка речовини, що володіє властивостями цієї речовини. Так, молекула цукру - солодка, а солі - солона. Існує умовний розподіл речовин на прості і складні. Молекули простих речовин складаються з атомів одного виду. Приклади: азот, кисень, аргон, озон. Молекули складних речовин складаються з атомів двох і більше видів: вуглекислий газ, вода, терпінеол. Часто фізичне тіло складається з молекул кількох різних речовин. Таке фізичне тіло називається сумішшю. Наприклад, повітря - суміш декількох простих і складних речовин. Не потрібно плутати складну речовину з сумішшю. Складна речовина, якщо вона складається з молекул тільки одного виду, сумішшю не є. Моделі молекул і назви речовин, що входять до складу лісового повітря: 1 - азот, 2 - кисень, 3 аргон, 4 - вуглекислий газ, 5 - вода, 6 - озон (утворюється з кисню при грозових розрядах), 7 - терпінеол (виділяється хвойними деревами). . Проста речовина складається з атомів лише одного виду або з молекул, побудованих з атомів одного виду. Складна речовина складається з молекул, побудованих з атомів різних видів. Сумішшю називається речовина, що складається з молекул (або атомів) двох або декількох речовин. Речовини, що становлять суміш, можуть бути простими і складними.

Тепловий рух - процес хаотичного (безладного) руху часток, що утворюють речовину. Найчастіше розглядається тепловий рух атомів і молекул. Хаотичність - найважливіша риса теплового руху. Найважливішими доказами існування руху молекул є Броунівський рух і дифузія. Тепловий рух атомів Броунівський рух - в природознавстві, безладний рух мікроскопічних, видимих, зважених в рідині (або газі) часток (броунівської частки) твердої речовини (порошинки, крупинки суспензії, частинки пилку рослини і так далі), що викликається тепловим рухом частинок рідини (або газу). Не слід змішувати поняття «броунівський рух» і «тепловий рух» : броунівський рух є наслідком і свідченням існування теплового руху. Броунівський рух наночастинок у краплі води Це явище відкрито Р. Броуном в 1827 році, коли він проводив дослідження пилку рослин. Він, зокрема, цікавився, як пилок бере участь у процесі запліднення. Роздивляючись пилок під мікроскопом Броун зазначив, що найдрібніші тверді крупинки, які ледве можна було розгледіти у краплі води, безперервно тремтять і пересуваються з місця на місце. Він встановив, що ці рухи, за його словами, «не пов'язані ні з потоками в рідині, ні з її поступовим випаровуванням, а притаманні самим частинкам» .

Дифузія лат. diffusio - розповсюдження, розтікання, розсіювання) - процес взаємного проникнення молекул однієї речовини між молекулами іншої , призводить до мимовільного вирівнювання їх концентрацій по всьому займаному обсягу. У деяких ситуаціях одна з речовин вже має вирівняну концентрацію і говорять про дифузію однієї речовини в іншу. При цьому перенесення речовини відбувається з області з високою концентрацією в область з низькою концентрацією (проти градієнту концентрації) Прикладом дифузії може служити перемішування газів (наприклад, поширення запахів) або рідин (якщо у воду капнути чорнила, то рідина через деякий час стане рівномірно пофарбованою). Інший приклад пов'язаний з твердим тілом: атоми дотичних металів перемішуються на кордоні дотику. Важливу роль дифузія частинок грає у фізиці плазми. Зазвичай під дифузією розуміють процеси, що супроводжуються перенесенням матерії, однак іноді дифузійними називають також інші процеси перенесення: теплопровідність, в'язке тертя і т. д. Швидкість протікання дифузії залежить від багатьох факторів. Так, у разі металевого стержня теплова дифузія проходить дуже швидко. Якщо ж стрижень виготовлений з синтетичного матеріалу, теплова дифузія протікає повільно. Дифузія молекул в загальному випадку протікає ще повільніше. Наприклад, якщо шматочок цукру опустити на дно склянки з водою і воду не перемішувати, то пройде кілька тижнів, перш ніж розчин стане однорідним. Ще повільніше відбувається дифузія одного твердої речовини в іншу. Наприклад, якщо мідь покрити золотом, то буде відбуватиметься дифузія золота в мідь, але при нормальних умовах (кімнатна температура та атмосферний тиск) золотовмісний шар досягне товщини в кілька мікронів тільки через кілька тисяч років. Схема дифузії через напівпроникну мембрану

Взаємодія молекул Міжмолекулярна взаємодія, взаємодія між електрично нейтральними молекулами або атомами; визначає існування рідин і молекулярних кристалів, відмінність реальних газів від ідеальних і виявляється в різноманітних фізичних явищах. Міжмолекулярна взаємодія залежить відстані між молекулами і, як правило, описується потенційною енергією взаємодії U (r) (потенціалом міжмолекулярної взаємодії), так як саме середня потенційна енергія взаємодії визначає стан і багато властивостей речовини. Вперше міжмолекулярну взаємодію взяв до уваги Я. Д. ван дер Ваальс (1873) для пояснення властивостей реальних газів і рідин. Ван дер Ваальс припустив, що на малих відстанях між молекулами діють сили відштовхування, які із збільшенням відстані змінюються силами тяжіння. На основі цих уявлень, навіть не розглядаючи кількісної залежності міжмолекулярної взаємодії відстані, він отримав так зване Ван-дер-Ваальса рівняння стану реального газу. Міжмолекулярна взаємодія має електричну природу і складається з сил тяжіння (орієнтаційних, індукційних і дисперсійних) і сил відштовхування. Приклади взаємодії молекул. . Фізику процесу полірування намагався прояснити ще І. Ньютон, однак лише недавні дослідження пролили на нього світло. Виявляється, при сильному натиску видаляються цілі шматочки матеріалу з полірованої поверхні, при слабкому - лише окремі молекули. . Водомірка, спираючись на воду кінчиками лапок, не змочується водою, здатна не тільки ковзати по воді, але і робити величезні стрибки, не прориваючи поверхневого шару. . Довгий циліндричний шар рідини нестійкий. Про це немов відомо павуку, формує нитку павутини: липка рідина утворює циліндричну оболонку навколо серцевини нитки і незабаром розпадається на крихітні кульки, до яких і прилипають комахи. . Молекулярні сили швидко змінюються з відстанню. Тяжіння молекул при збільшенні відстані між ними в 2 рази слабшає в 128 разів!. . . «Розтягнути» молекули кисню за витратами енергії раз в 50 легше, ніж «розірвати» саму молекулу. . Уявлення, розроблені в одній галузі фізики, часто вдало «кочують» в інші. Так, розглядаючи ядро урану як рідку заряджену краплю. Я. І. Френкель показав в 1939 році, що вона повинна виявити колосальний поверхневий натяг. Така, краплинна модель ядра дозволила пояснити, наприклад, як відбувається розподіл ядер урану. . Абсолютно чисті і гладкі поверхні при зіткненні можуть самі собою злипнутися. Коли тільки почалися польоти космічних кораблів з екіпажами на борту, існувала реальна небезпека, що металева підошва черевика космонавта може мимоволі «приклеїтися» до металевої обшивки корабля.

Агрегатні стани речовини Агрегатний стан - стан речовини, що характеризується певними якісними властивостями: здатністю чи нездатністю зберігати об'єм та форму, наявністю або відсутністю далекого і ближнього порядку та іншими. Зміна агрегатного стану може супроводжуватися стрибкоподібною зміною вільної енергії, ентропії, густини і інших основних фізичних властивостей. Виділяють три основні агрегатних стани: тверде тіло, рідина та газ. Тверде тіло Стан, що характеризується здатністю зберігати об'єм та форму. Атоми твердого тіла здійснюють лише невеликі коливання навколо стану рівноваги. Рідина Стан речовини, при якому вона має малу стискаємість, тобто добре зберігає об'єм, проте не здатна зберігати форму. Рідина легко приймає форму судини, в якiй вона поміщена. Атоми або молекули рідини здійснюють коливання поблизу стану рівноваги, замкнені іншими атомами, і часто перескакують на інші вільні місця. Газ Стан, що характеризується хорошою стискаємістю, , відсутністю здатності зберігати як обсяг, так і форму. Газ прагне зайняти весь обсяг, йому наданий. Атоми або молекули газу ведуть себе відносно вільно, відстані між ними набагато більше їх розмірів.

Кристалічні і аморфні тіла За своїм фізичними властивостями і молекулярною структурою тверді тіла поділяються на два класи - аморфні та кристалічні. Характерною особливістю аморфних тіл є їх iзотропность, тобто незалежність всіх фізичних властивостей (механічних, оптичних і т. д. ) від напрямку зовнішньої дії. Молекули і атоми в ізотропних твердих тілах розташовуються хаотично, утворюючи лише невеликі локальні групи, які містять кілька частинок (ближній порядок). Прикладами аморфних тіл можуть служити скло, різні затверділі смоли (бурштин), пластики і т. д. Якщо аморфне тіло нагрівати, то воно поступово розм'якшується, і перехід в рідкий стан займає значний інтервал температур. У кристалічних тілах частки розташовуються в строгому порядку, утворюючи просторові періодично повторювані структури в усьому обсязі тіла. Для наочного подання таких структур використовуються просторові кристалічні решітки, у вузлах яких розташовуються центри атомів або молекул даної речовини. Найчастіше кристалічна решітка будується з іонів (позитивно і негативно заряджених) атомів, які входять до складу молекули даної речовини. Наприклад, грати кухонної солі містить іони Na + і Cl-, не об'єднані попарно в молекули Na. Cl (рис. 3. 6. 1). Такі кристали називаються іонними. Кристалічна решітка кухонної солі Прості кристалічні решітки: 1 - проста кубічна решітка, 2 - гранецентрована кубічна решітка, 3 об'емноцентрірована кубічна решітка, 4 гексагональна решітка

Теплове розширення тел Тепловим розширенням називається ефект зміни розмірів тіла з зміною температури постійному тиску. Це явище для твердих тіл обумовлено несиметричністю потенціалу взаємодії атомів речовини в решітці, що призводить до ангармонізм коливань атомів щодо середнього положення. Для газів це обумовлено збільшенням кінетичної енергії молекул і атомів. Переважна більшість речовин при нагріванні розширюється. Це легко пояснити з позиції механічної теорії теплоти, оскільки при нагріванні молекули або атоми речовини починають рухатися швидше. У твердих тілах атоми починають з більшою амплітудою коливатися навколо свого середнього положення в кристалічній решітці, і їм потрібно більше вільного простору. В результаті тіло розширюється. Так само і рідини і гази, здебільшого, розширюються з підвищенням температури через збільшення швидкості теплового руху вільних молекул Для інженерів теплове розширення - життєво важливе явище. Проектуючи сталевий міст через річку в місті з континентальним кліматом, не можна не враховувати можливого перепаду температур в межах від -40 ° C до +40 ° C протягом року. Такі перепади викличуть зміну загальної довжини мосту аж до декількох метрів, і, щоб міст не вздиблювався влітку і не відчував потужних навантажень на розрив взимку, проектувальники становлять міст з окремих секцій, поєднуючи їх спеціальними термічними буферними зчленуваннями, які входять у зачеплення, представляють собою , але не з'єднані жорстко у ряди зуби, які щільно змикаються в спеку і достатньо широко розходяться в холоднечу. На довгому мосту може налічуватися досить багато таких буферів.

Інвар (лат. invariabilis - незмінний) - сплав, що складається з нікелю (Ni, 36%) і заліза (Fe, інше). Сплав володiє малим температурним коефіцієнтом лінійного розширення і практично не розширюється в інтервалі температур від -100 до +100 ° C. Ефект зникнення теплового розширення матеріалу виникає у зв'язку з тим, що Магнітострикція точно компенсує теплове розширення. Коефіцієнт теплового розширення 1, 2 × 10 -6 / ° C на проміжку від -20 до 100 ° C. Дуже чисті сплави (Co <0, 1%) мають ще менший коефіцієнт лінійного розширення 0, 62 -0, 65 × 10 -6 / ° C. Перший з відкритих iнварних сплавів, був знайдений швейцарським ученим Ш. Гійомом в 1899 році. У 1920 році він отримав Нобелівську премію з фізики за відкриття важливого сплаву для виробництва точних інструментів та приладів. Використовується в точному приладобудуванні для виготовлення мірних дротів в геодезії, еталонів довжини, деталей годинникових механізмів (маятників хронометрів, пружин), деталей барографiв і висотомірів та ін. Зовнішній вигляд сплаву інвару: сріблясто-сірий з металевим блиском

Бiметалева пласти на Біметалева пластина - пластина, виготовлена з біметалу або з механічно з'єднаних шматків двох різних металів. Як правило, використовується як основна частина термомеханічного датчика. Являє собою відрізок стрічки з біметалу. Один кінець стрічки, як правило, нерухомо закріплений в пристрої, а інший - переміщається в залежності від температури пластини. Зустрічаються пристрої, що складаються з 2 пластин різновидних металів, закріплених одними кінцями і сполучених (клепкою, пайкою або зварюванням) в інших кінцях. При зміні температури з'єднаний кінець пластин переміщається. Працездатні в дуже широкому діапазоні температур. Якщо обидва кінці біметалічної пластини з'єднані заклепками, при збільшенні температури пластина згинається. Застосування. Термостати та захисні пристрої Зiгнена біметалічна пластина управляє електричними контактами, замикаючими або розмикаючими ланцюг підігрівача. (У випадку захисних пристроїв - відключають електроживлення навантаження). Можуть зводити-розводити контакти поступово (дешева ненадійна конструкція - контакти іскрять і обгорають), а можуть спрацьовувати стрибком (механічна біфуркація), відразу переміщаючи контакт на кілька міліметрів (клацання від таких перемикань чутні при роботі прасок).
Санжаровська.ppt