Раздел 1 вопросы 5 - 8.ppt
- Количество слайдов: 13
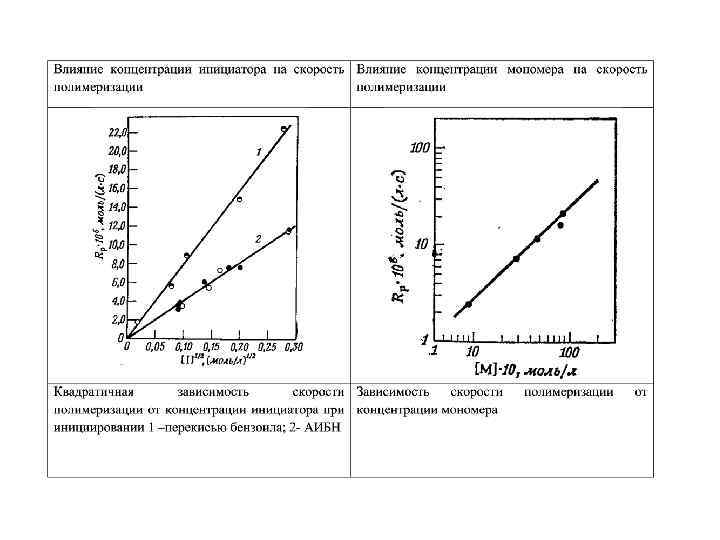
 Понятие о критической температуре с точки зрения уравнения термодинамики. Зависимость среднечисловой степени полимеризации от температуры Термодинамика полимеризации Предмет изучения термодинамики полимеризации – изменение энергии реакционной системы, обусловленное превращением мономера в полимер. При этом рассматривают: - условия область изменения термодинамических факторов (температуры, давления и т. п. ), при которых принципиально возможно образование полимера; -а при определённых условиях: - предельную глубину превращения мономера в полимер; -состояние равновесия в реакционной системе; -тепловые эффекты полимеризации. -влияние температуры, давления и т. п. на ход процесса полимеризации в реальных условиях и на качество (структуру, ММР) получаемого продукта. Условием самопроизвольного протекания является уменьшение в ходе процесса энергии Гиббса ∆G , зависящей, от изменений в этом процессе энтальпии ∆H и энтропии ∆ S: ∆G = ∆H + T∆S < О
Понятие о критической температуре с точки зрения уравнения термодинамики. Зависимость среднечисловой степени полимеризации от температуры Термодинамика полимеризации Предмет изучения термодинамики полимеризации – изменение энергии реакционной системы, обусловленное превращением мономера в полимер. При этом рассматривают: - условия область изменения термодинамических факторов (температуры, давления и т. п. ), при которых принципиально возможно образование полимера; -а при определённых условиях: - предельную глубину превращения мономера в полимер; -состояние равновесия в реакционной системе; -тепловые эффекты полимеризации. -влияние температуры, давления и т. п. на ход процесса полимеризации в реальных условиях и на качество (структуру, ММР) получаемого продукта. Условием самопроизвольного протекания является уменьшение в ходе процесса энергии Гиббса ∆G , зависящей, от изменений в этом процессе энтальпии ∆H и энтропии ∆ S: ∆G = ∆H + T∆S < О
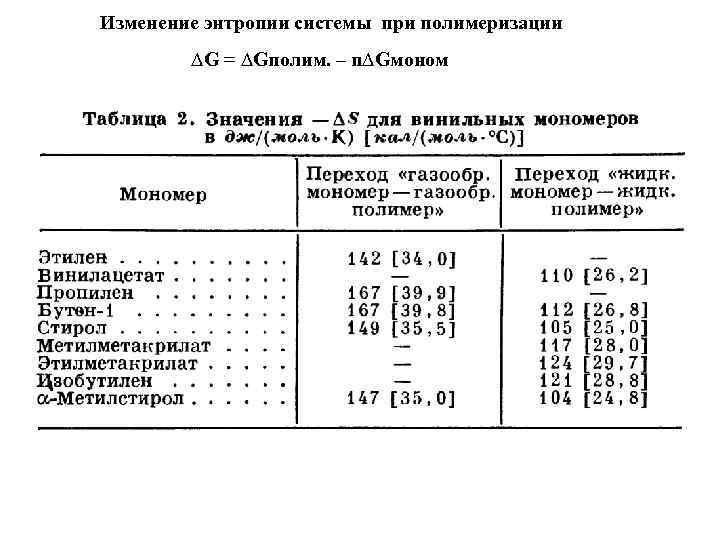 Изменение энтропии системы при полимеризации ∆G = ∆Gполим. – n∆Gмоном
Изменение энтропии системы при полимеризации ∆G = ∆Gполим. – n∆Gмоном
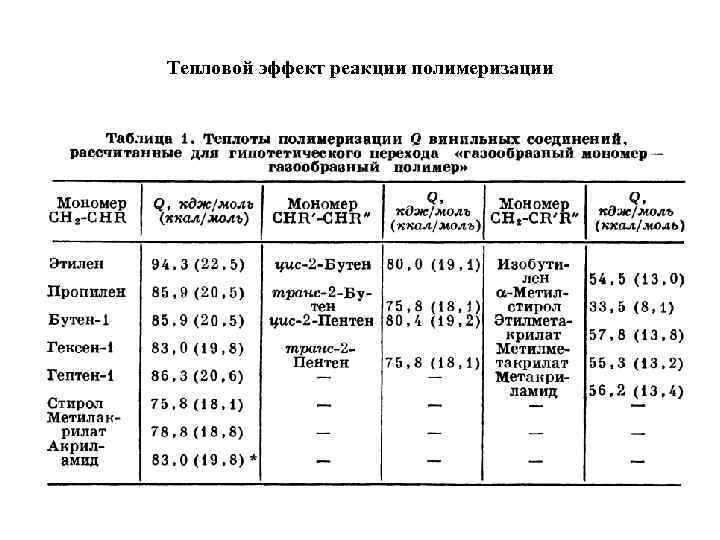 Тепловой эффект реакции полимеризации
Тепловой эффект реакции полимеризации
 Следствием различия знаков изменения составляющих энергии Гиббса для процесса полимеризации является критическая температура Тcr, которая соответствует равновесному состоянию системы при которой полимер не м. б. получен. Если ∆G = О = ∆Н - T∆S То критическая температура Тcr = ∆Н/∆S Константа равновесия реакции (термодинамическая – т. е. выраженная через активность реагентов) Ka связана с изменением свободной энергии в ходе реакции соотношеним: ∆G = -RT lg Ka т. е. при некой заданной постоянной температуре каждый раз будет устанавливаться равновесие полимер-мономер при определённой концентрации мономера – равновесной для данной температуры. Критическая температура зависит от стандартных изменений энтальпии и энтропии и равновесной концентрации мономера [M]р (формула Тобольского): Тcr = ∆Нт / (∆S°т + R lg [M]р)
Следствием различия знаков изменения составляющих энергии Гиббса для процесса полимеризации является критическая температура Тcr, которая соответствует равновесному состоянию системы при которой полимер не м. б. получен. Если ∆G = О = ∆Н - T∆S То критическая температура Тcr = ∆Н/∆S Константа равновесия реакции (термодинамическая – т. е. выраженная через активность реагентов) Ka связана с изменением свободной энергии в ходе реакции соотношеним: ∆G = -RT lg Ka т. е. при некой заданной постоянной температуре каждый раз будет устанавливаться равновесие полимер-мономер при определённой концентрации мономера – равновесной для данной температуры. Критическая температура зависит от стандартных изменений энтальпии и энтропии и равновесной концентрации мономера [M]р (формула Тобольского): Тcr = ∆Нт / (∆S°т + R lg [M]р)
![Критическая температура зависит от стандартных изменений энтальпии и энтропии и равновесной концентрации мономера [M]р Критическая температура зависит от стандартных изменений энтальпии и энтропии и равновесной концентрации мономера [M]р](https://present5.com/presentation/8008385_161895799/image-5.jpg) Критическая температура зависит от стандартных изменений энтальпии и энтропии и равновесной концентрации мономера [M]р (формула Тобольского): Тcr = ∆Нт / (∆S°т + R lg [M]р) Эта формула показывает, что в идеальных условиях критическая температура является функцией лишь природы мономер. Она зависит от строения молекул мономера и полимера, их агрегатного состояния. В этой формуле не учитывается: - теплота растворения мономера в растворителе; - теплота взаимодействия полимера со средой; - теплота кристаллизации полимера.
Критическая температура зависит от стандартных изменений энтальпии и энтропии и равновесной концентрации мономера [M]р (формула Тобольского): Тcr = ∆Нт / (∆S°т + R lg [M]р) Эта формула показывает, что в идеальных условиях критическая температура является функцией лишь природы мономер. Она зависит от строения молекул мономера и полимера, их агрегатного состояния. В этой формуле не учитывается: - теплота растворения мономера в растворителе; - теплота взаимодействия полимера со средой; - теплота кристаллизации полимера.
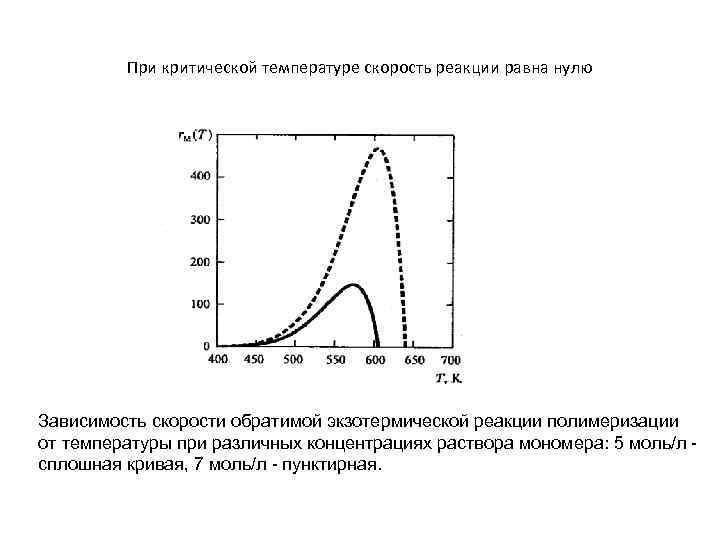 При критической температуре скорость реакции равна нулю Зависимость скорости обратимой экзотермической реакции полимеризации от температуры при различных концентрациях раствора мономера: 5 моль/л сплошная кривая, 7 моль/л - пунктирная.
При критической температуре скорость реакции равна нулю Зависимость скорости обратимой экзотермической реакции полимеризации от температуры при различных концентрациях раствора мономера: 5 моль/л сплошная кривая, 7 моль/л - пунктирная.
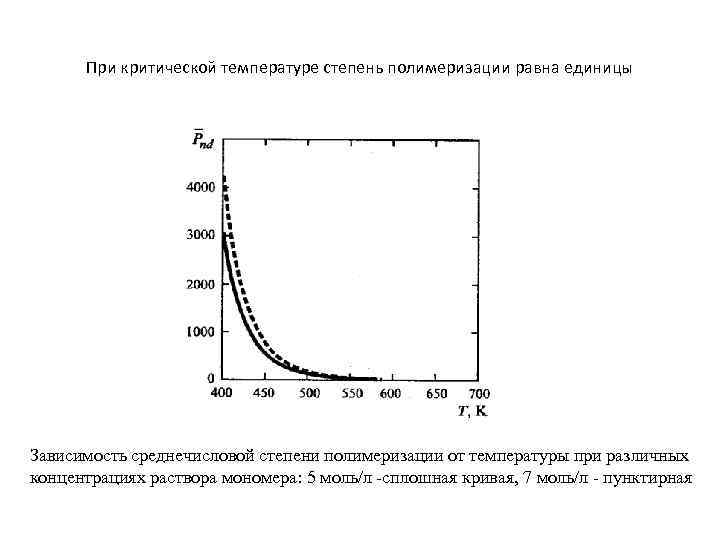 При критической температуре степень полимеризации равна единицы Зависимость среднечисловой степени полимеризации от температуры при различных концентрациях раствора мономера: 5 моль/л -сплошная кривая, 7 моль/л - пунктирная
При критической температуре степень полимеризации равна единицы Зависимость среднечисловой степени полимеризации от температуры при различных концентрациях раствора мономера: 5 моль/л -сплошная кривая, 7 моль/л - пунктирная
 Термодинамика полиприсоединения и поликонденсации Управление величиной выхода полимера возможно путем смещения равновесия в сторону продуктов реакции: -изменении константы равновесия с помощью температуры; -применения избытка одного из исходных веществ; -удаления одного из продуктов реакции; -и (для реакций, идущих с изменением объема) изменении давления или введения инертных веществ
Термодинамика полиприсоединения и поликонденсации Управление величиной выхода полимера возможно путем смещения равновесия в сторону продуктов реакции: -изменении константы равновесия с помощью температуры; -применения избытка одного из исходных веществ; -удаления одного из продуктов реакции; -и (для реакций, идущих с изменением объема) изменении давления или введения инертных веществ
 Постулаты кинетики радикальной полимеризации. Лимитирующие стадии радикальной цепной по лимеризации Скорости химической реакции. Динамика перехода химической системы из начального состояния (мономеры) в конечное (полимеры) описываются законами классической химической кинетики. Скорость химической реакции определяется как изменение количества ключевого вещества (Х) в единицу времени в единице реакционного объема r = + 1/V × d[A]/ dτ , где: A – кол-во вещества Х в молях, V – объем реакционной массы Если объем реакционной смеси в ходе реакции заметно не изменяется, его можно считать постоянной величиной и ввести под знак дифференциала. Тогда уравнение скорости данной реакции будет определяться как изменение концентрации вещества А в реакции второго смешанного порядка (первого порядка по каждому из реагентов) во времени и будет иметь вид: r = + d[A]/ dτ = k [A][B], k- константа скорости химической реакций, определяемая по уравнению Аррениуса: k = А ехр (Е/RT)
Постулаты кинетики радикальной полимеризации. Лимитирующие стадии радикальной цепной по лимеризации Скорости химической реакции. Динамика перехода химической системы из начального состояния (мономеры) в конечное (полимеры) описываются законами классической химической кинетики. Скорость химической реакции определяется как изменение количества ключевого вещества (Х) в единицу времени в единице реакционного объема r = + 1/V × d[A]/ dτ , где: A – кол-во вещества Х в молях, V – объем реакционной массы Если объем реакционной смеси в ходе реакции заметно не изменяется, его можно считать постоянной величиной и ввести под знак дифференциала. Тогда уравнение скорости данной реакции будет определяться как изменение концентрации вещества А в реакции второго смешанного порядка (первого порядка по каждому из реагентов) во времени и будет иметь вид: r = + d[A]/ dτ = k [A][B], k- константа скорости химической реакций, определяемая по уравнению Аррениуса: k = А ехр (Е/RT)
 Кинетика радикальной полимеризации Постулаты 1. Принцип равной реакционной способности макрорадикалов 2. Длинноцепочечное приближение 3. Принцип (квази) стационарности
Кинетика радикальной полимеризации Постулаты 1. Принцип равной реакционной способности макрорадикалов 2. Длинноцепочечное приближение 3. Принцип (квази) стационарности
 Лимитирующими стадиями радикальной цепной полимеризации могут быть: • Зарождение активного центра роста макромолекулы за счет взаимодействия радикала инициатора с мономером. Наиболее распространённым является инициирование радикальной полимеризации с помощью инициаторов, которые при нагревании распадаются на два осколка, которые взаимодействуют с молекулой мономера, образуя активный центр роста макромолекулы • Рост активной макромолекулы в результате многократного присоединения молекул мономера к активному центру • Обрыв цепи с образованием неактивных макромолекул путем: -рекомбинации (взаимодействия) макрорадикалов - диспропорционирования макрорадикалов (обмена атомом водорода между ними). -передачи цепи на мономер или полимер или на растворитель Где Х – или мономер, или полимер, или растворитель
Лимитирующими стадиями радикальной цепной полимеризации могут быть: • Зарождение активного центра роста макромолекулы за счет взаимодействия радикала инициатора с мономером. Наиболее распространённым является инициирование радикальной полимеризации с помощью инициаторов, которые при нагревании распадаются на два осколка, которые взаимодействуют с молекулой мономера, образуя активный центр роста макромолекулы • Рост активной макромолекулы в результате многократного присоединения молекул мономера к активному центру • Обрыв цепи с образованием неактивных макромолекул путем: -рекомбинации (взаимодействия) макрорадикалов - диспропорционирования макрорадикалов (обмена атомом водорода между ними). -передачи цепи на мономер или полимер или на растворитель Где Х – или мономер, или полимер, или растворитель
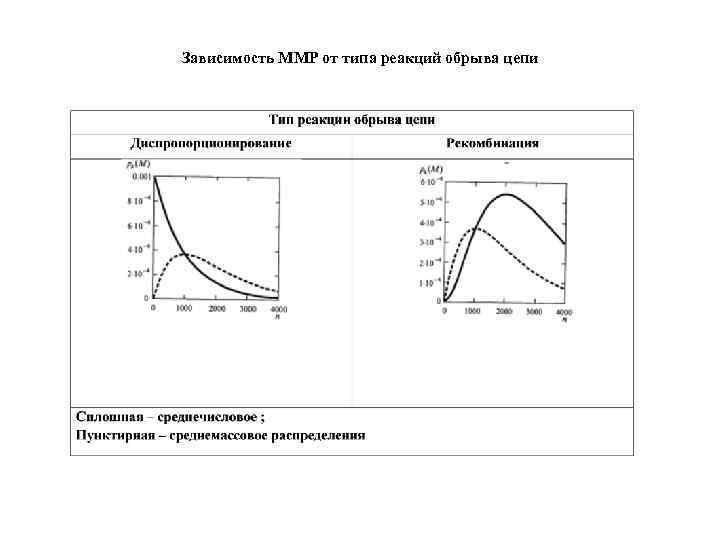 Зависимость ММР от типа реакций обрыва цепи
Зависимость ММР от типа реакций обрыва цепи