получение технической целлюлозы.pptx
- Количество слайдов: 19
 ПОЛУЧЕНИЕ ТЕХНИЧЕСКОЙ ЦЕЛЛЮЛОЗЫ РАХМАТУЛЛИН Р. Р.
ПОЛУЧЕНИЕ ТЕХНИЧЕСКОЙ ЦЕЛЛЮЛОЗЫ РАХМАТУЛЛИН Р. Р.
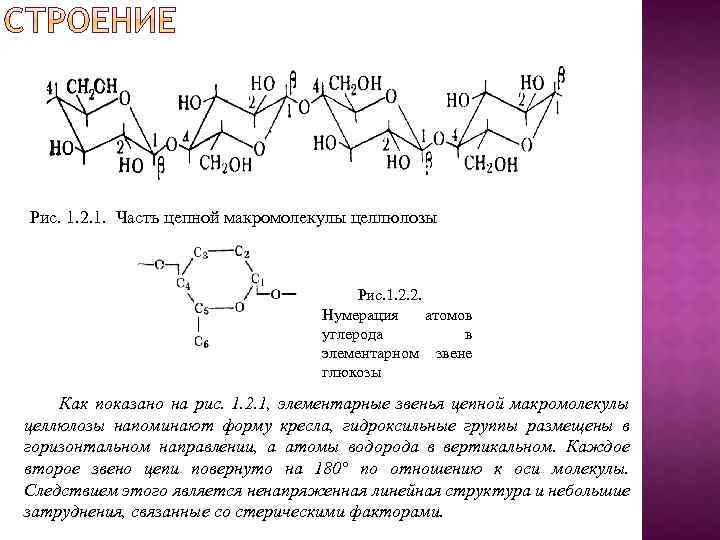 Рис. 1. 2. 1. Часть цепной макромолекулы целлюлозы Рис. 1. 2. 2. Нумерация атомов углерода в элементарном звене глюкозы Как показано на рис. 1. 2. 1, элементарные звенья цепной макромолекулы целлюлозы напоминают форму кресла, гидроксильные группы размещены в горизонтальном направлении, а атомы водорода в вертикальном. Каждое второе звено цепи повернуто на 180° по отношению к оси молекулы. Следствием этого является ненапряженная линейная структура и небольшие затруднения, связанные со стерическими факторами.
Рис. 1. 2. 1. Часть цепной макромолекулы целлюлозы Рис. 1. 2. 2. Нумерация атомов углерода в элементарном звене глюкозы Как показано на рис. 1. 2. 1, элементарные звенья цепной макромолекулы целлюлозы напоминают форму кресла, гидроксильные группы размещены в горизонтальном направлении, а атомы водорода в вертикальном. Каждое второе звено цепи повернуто на 180° по отношению к оси молекулы. Следствием этого является ненапряженная линейная структура и небольшие затруднения, связанные со стерическими факторами.
 Классификация технических целлюлоз по выходу и степени провара В соответствии с величиной выхода технические целлюлозы делятся на три основные категории: продукт с выходом примерно от 80 до 60% от массы исходного растительного сырья называется полуцеллюлозой; с выходом от_60 до 50% — целлюлозой высокого выхода; С ВЫХОДОМ ОТ 50 40% — целлюлозой нормального выхода. до По степени провара, характеризующей остаточное содержание лигнина, целлюлозы нормального выхода могут быть разделены на несколько групп: целлюлозы жесткие, содержащие примерно от 3 до 8% лигнина; среднежесткие, содержащие от 1, 5 до 3% лигнина; мягкие, содержание остаточного лигнина в которых не превышает 1, 5%.
Классификация технических целлюлоз по выходу и степени провара В соответствии с величиной выхода технические целлюлозы делятся на три основные категории: продукт с выходом примерно от 80 до 60% от массы исходного растительного сырья называется полуцеллюлозой; с выходом от_60 до 50% — целлюлозой высокого выхода; С ВЫХОДОМ ОТ 50 40% — целлюлозой нормального выхода. до По степени провара, характеризующей остаточное содержание лигнина, целлюлозы нормального выхода могут быть разделены на несколько групп: целлюлозы жесткие, содержащие примерно от 3 до 8% лигнина; среднежесткие, содержащие от 1, 5 до 3% лигнина; мягкие, содержание остаточного лигнина в которых не превышает 1, 5%.
 Решающее значение при выборе сырья имеют: содержание в нем клетчатки; структурные особенности составляющих его волокон; возможность применять к нему промышленные способы обработки; качество волокнистого продукта, получаемого в результате этой обработки; распространенность растительного сырья; удобство и стоимость его сбора, доставки, хранения и т. п. Из хвойных древесных пород наибольшее применение имеют ель, сосна, пихта, из лиственных — тополь разных видов, осина, береза, бук и некоторые другие. Из недревесного сырья используется солома культурных злаков — ржи, пшеницы, ячменя, риса, кукурузы и т. п. За рубежом распространена целлюлоза из эспарто — травы, произрастающей на севере Африки и в Ис пании, а в странах Юго Восточной Азии и Южной Америки для получения целлюлозы широко используют бамбук и багассу — отжатые после экстракции стебли сахарного тростника. К недревесному сырью относятся также хлопок, лен, конопля, джут и др. , используемые преимущественно в виде текстильных отходов (тряпья). Кроме того, сырьем для получения целлюлозы могут служить и многочисленные дикорастущие однолетние растения — тростник, кендырь, чий и пр.
Решающее значение при выборе сырья имеют: содержание в нем клетчатки; структурные особенности составляющих его волокон; возможность применять к нему промышленные способы обработки; качество волокнистого продукта, получаемого в результате этой обработки; распространенность растительного сырья; удобство и стоимость его сбора, доставки, хранения и т. п. Из хвойных древесных пород наибольшее применение имеют ель, сосна, пихта, из лиственных — тополь разных видов, осина, береза, бук и некоторые другие. Из недревесного сырья используется солома культурных злаков — ржи, пшеницы, ячменя, риса, кукурузы и т. п. За рубежом распространена целлюлоза из эспарто — травы, произрастающей на севере Африки и в Ис пании, а в странах Юго Восточной Азии и Южной Америки для получения целлюлозы широко используют бамбук и багассу — отжатые после экстракции стебли сахарного тростника. К недревесному сырью относятся также хлопок, лен, конопля, джут и др. , используемые преимущественно в виде текстильных отходов (тряпья). Кроме того, сырьем для получения целлюлозы могут служить и многочисленные дикорастущие однолетние растения — тростник, кендырь, чий и пр.
 Полуцеллюлоза, целлюлоза высокого выхода, небеленая целлюлоза различной степени провара, беленая, полубеленая и облагороженная целлюлоза представляют собой полуфабрикаты, которые находят широкое практическое применение для выработки самых разнообразных видов бумаги и картона (93% всей вырабатываемой в мире целлюлозы). Целлюлоза служит сырьем: Для химической переработки на искусственное волокно, получаемое в основном вискозным, а частично ацетатным и медноаммиачным методами. На кинопленку. Пластические массы Бездымный порох Целлофан другие продукты на основе сложных и простых эфиров целлюлозы.
Полуцеллюлоза, целлюлоза высокого выхода, небеленая целлюлоза различной степени провара, беленая, полубеленая и облагороженная целлюлоза представляют собой полуфабрикаты, которые находят широкое практическое применение для выработки самых разнообразных видов бумаги и картона (93% всей вырабатываемой в мире целлюлозы). Целлюлоза служит сырьем: Для химической переработки на искусственное волокно, получаемое в основном вискозным, а частично ацетатным и медноаммиачным методами. На кинопленку. Пластические массы Бездымный порох Целлофан другие продукты на основе сложных и простых эфиров целлюлозы.
 Общепринятой системы классификации способов делигнификации в настоящее время не существует, но все специалисты считают, что в основу такой классификации должны быть положены вид и свойства применяемых химических реагентов, а в случае использования нескольких реагентов — последовательность обработки ими растительного материала. Исходя из этого, можно разделить все известные способы получения целлюлозы на шесть следующих групп: кислотные (сульфитный, бисульфитный и азотнокислотный) щелочные (натронный, сульфатный щелочно сульфитный и известковомолочный) нейтральные(моносульфитный и гидротропный) окислительные (кислородно щелочной, кислородно аммиачный) ступенчатые (бисульфитно сульфитный, моносульфитно сульфитный и сульфитно сульфитный) комбинированные.
Общепринятой системы классификации способов делигнификации в настоящее время не существует, но все специалисты считают, что в основу такой классификации должны быть положены вид и свойства применяемых химических реагентов, а в случае использования нескольких реагентов — последовательность обработки ими растительного материала. Исходя из этого, можно разделить все известные способы получения целлюлозы на шесть следующих групп: кислотные (сульфитный, бисульфитный и азотнокислотный) щелочные (натронный, сульфатный щелочно сульфитный и известковомолочный) нейтральные(моносульфитный и гидротропный) окислительные (кислородно щелочной, кислородно аммиачный) ступенчатые (бисульфитно сульфитный, моносульфитно сульфитный и сульфитно сульфитный) комбинированные.
 Сульфитные варочные процессы — это обработка щепы варочными растворами, содержащими свободную сернистую кислоту и ее соли, при температуре — 150° С. Катионами в этих солях могут быть кальций (нерастворимое основание), магний (полурастворимое основание), натрий и аммоний (растворимые основания). Сульфитные варочные процессы подразделяют следующим образом: 1. Сульфитная варка (кислая сульфитная варка), которая проводится при р. Н 1, 5— 3, 0. Варочный раствор содержит бисульфиты и избыток растворенного SO 2. Применяется любое основание. 2. Бисульфитная варка, которая проводится при р. Н 4, 0— 5, 0. Варочный раствор содержит бисульфиты натрия, магния или аммония. 3. Моносульфитная (нейтрально сульфитная) варка, которая проводится при р. Н 6, 0— 9, 5. Варочный раствор содержит сульфиты и бисульфиты натрия, магния или аммония. 4. Варка с водным раствором SO 2. 5. Ступенчатые варки с различными комбинациями ступеней.
Сульфитные варочные процессы — это обработка щепы варочными растворами, содержащими свободную сернистую кислоту и ее соли, при температуре — 150° С. Катионами в этих солях могут быть кальций (нерастворимое основание), магний (полурастворимое основание), натрий и аммоний (растворимые основания). Сульфитные варочные процессы подразделяют следующим образом: 1. Сульфитная варка (кислая сульфитная варка), которая проводится при р. Н 1, 5— 3, 0. Варочный раствор содержит бисульфиты и избыток растворенного SO 2. Применяется любое основание. 2. Бисульфитная варка, которая проводится при р. Н 4, 0— 5, 0. Варочный раствор содержит бисульфиты натрия, магния или аммония. 3. Моносульфитная (нейтрально сульфитная) варка, которая проводится при р. Н 6, 0— 9, 5. Варочный раствор содержит сульфиты и бисульфиты натрия, магния или аммония. 4. Варка с водным раствором SO 2. 5. Ступенчатые варки с различными комбинациями ступеней.
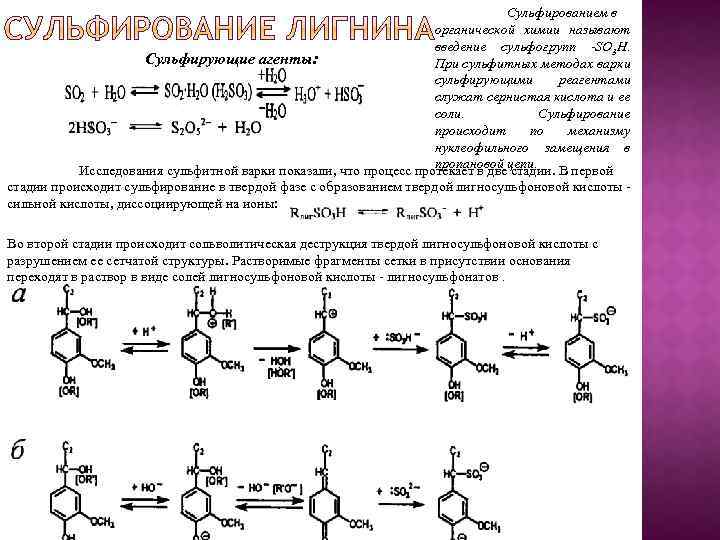 Сульфированием в органической химии называют введение сульфогрупп -SO 3 Н. Сульфирующие агенты: При сульфитных методах варки сульфирующими реагентами служат сернистая кислота и ее соли. Сульфирование происходит по механизму нуклеофильного замещения в пропановой стадии. Исследования сульфитной варки показали, что процесс протекает в двецепи. В первой стадии происходит сульфирование в твердой фазе с образованием твердой лигносульфоновой кислоты сильной кислоты, диссоциирующей на ионы: Во второй стадии происходит сольволитическая деструкция твердой лигносульфоновой кислоты с разрушением ее сетчатой структуры. Растворимые фрагменты сетки в присутствии основания переходят в раствор в виде солей лигносульфоновой кислоты лигносульфонатов.
Сульфированием в органической химии называют введение сульфогрупп -SO 3 Н. Сульфирующие агенты: При сульфитных методах варки сульфирующими реагентами служат сернистая кислота и ее соли. Сульфирование происходит по механизму нуклеофильного замещения в пропановой стадии. Исследования сульфитной варки показали, что процесс протекает в двецепи. В первой стадии происходит сульфирование в твердой фазе с образованием твердой лигносульфоновой кислоты сильной кислоты, диссоциирующей на ионы: Во второй стадии происходит сольволитическая деструкция твердой лигносульфоновой кислоты с разрушением ее сетчатой структуры. Растворимые фрагменты сетки в присутствии основания переходят в раствор в виде солей лигносульфоновой кислоты лигносульфонатов.
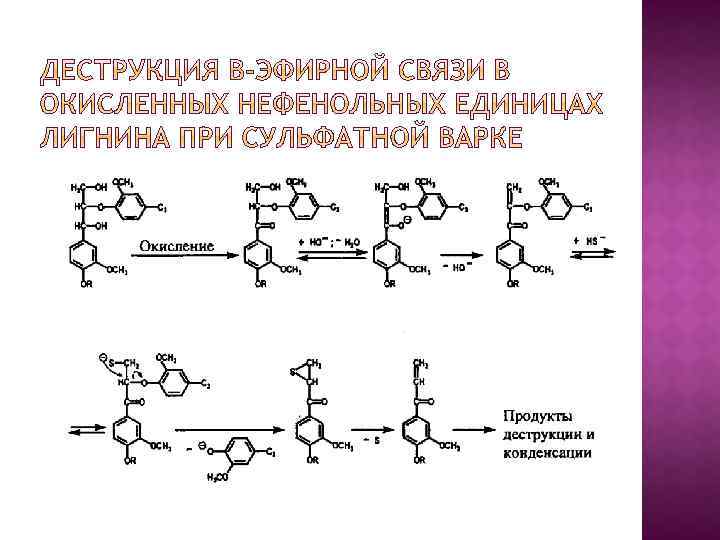
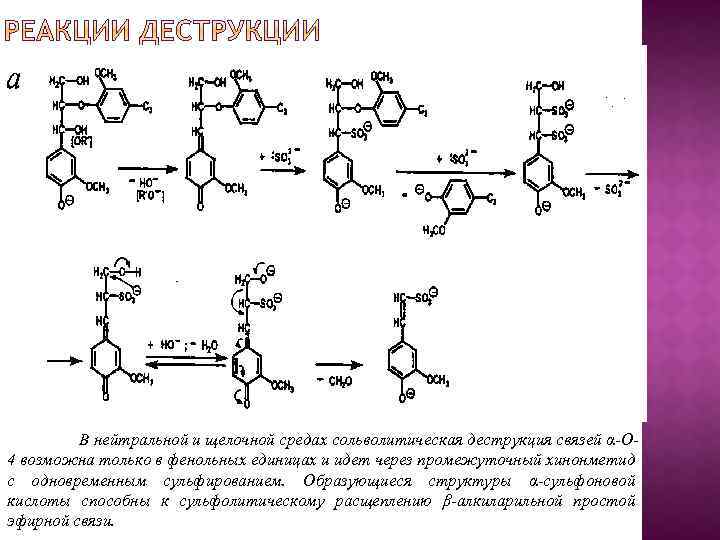 В нейтральной и щелочной средах сольволитическая деструкция связей α-О 4 возможна только в фенольных единицах и идет через промежуточный хинонметид с одновременным сульфированием. Образующиеся структуры α-сульфоновой кислоты способны к сульфолитическому расщеплению β-алкиларильной простой эфирной связи.
В нейтральной и щелочной средах сольволитическая деструкция связей α-О 4 возможна только в фенольных единицах и идет через промежуточный хинонметид с одновременным сульфированием. Образующиеся структуры α-сульфоновой кислоты способны к сульфолитическому расщеплению β-алкиларильной простой эфирной связи.
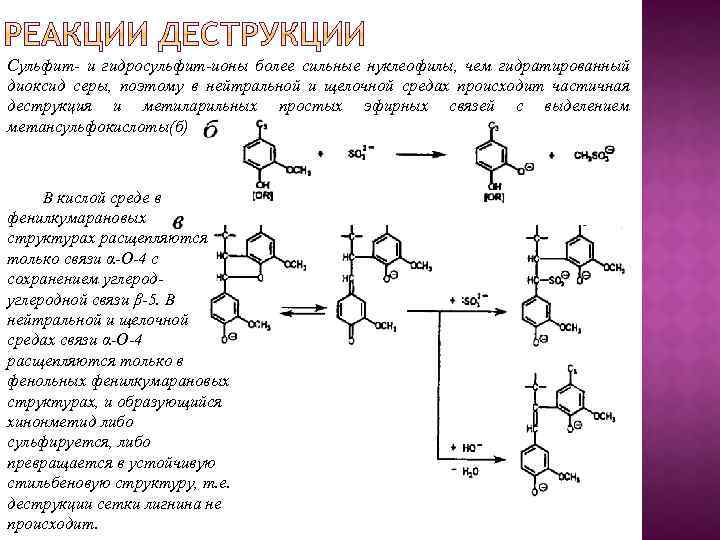 Сульфит- и гидросульфит-ионы более сильные нуклеофилы, чем гидратированный диоксид серы, поэтому в нейтральной и щелочной средах происходит частичная деструкция и метиларильных простых эфирных связей с выделением метансульфокислоты(б) В кислой среде в фенилкумарановых структурах расщепляются только связи α-О-4 с сохранением углеродной связи β-5. В нейтральной и щелочной средах связи α-О-4 расщепляются только в фенольных фенилкумарановых структурах, и образующийся хинонметид либо сульфируется, либо превращается в устойчивую стильбеновую структуру, т. е. деструкции сетки лигнина не происходит.
Сульфит- и гидросульфит-ионы более сильные нуклеофилы, чем гидратированный диоксид серы, поэтому в нейтральной и щелочной средах происходит частичная деструкция и метиларильных простых эфирных связей с выделением метансульфокислоты(б) В кислой среде в фенилкумарановых структурах расщепляются только связи α-О-4 с сохранением углеродной связи β-5. В нейтральной и щелочной средах связи α-О-4 расщепляются только в фенольных фенилкумарановых структурах, и образующийся хинонметид либо сульфируется, либо превращается в устойчивую стильбеновую структуру, т. е. деструкции сетки лигнина не происходит.
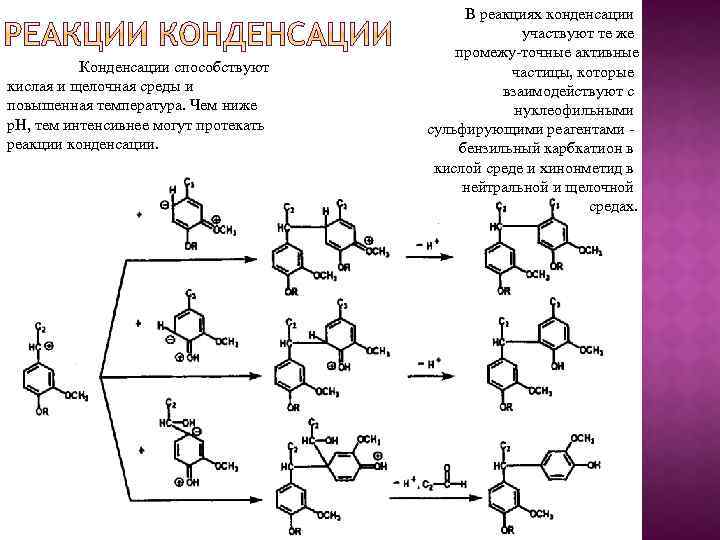 Конденсации способствуют кислая и щелочная среды и повышенная температура. Чем ниже р. Н, тем интенсивнее могут протекать реакции конденсации. В реакциях конденсации участвуют те же промежу точные активные частицы, которые взаимодействуют с нуклеофильными сульфирующими реагентами бензильный карбкатион в кислой среде и хинонметид в нейтральной и щелочной средах.
Конденсации способствуют кислая и щелочная среды и повышенная температура. Чем ниже р. Н, тем интенсивнее могут протекать реакции конденсации. В реакциях конденсации участвуют те же промежу точные активные частицы, которые взаимодействуют с нуклеофильными сульфирующими реагентами бензильный карбкатион в кислой среде и хинонметид в нейтральной и щелочной средах.
 Конденсацию лигнина вызывают и ионы тиосульфата, образующиеся, например, при восстановлении НSOз углеводами При этом сшивка фрагментов лигнина происходит из за образования сульфидных мостиков.
Конденсацию лигнина вызывают и ионы тиосульфата, образующиеся, например, при восстановлении НSOз углеводами При этом сшивка фрагментов лигнина происходит из за образования сульфидных мостиков.
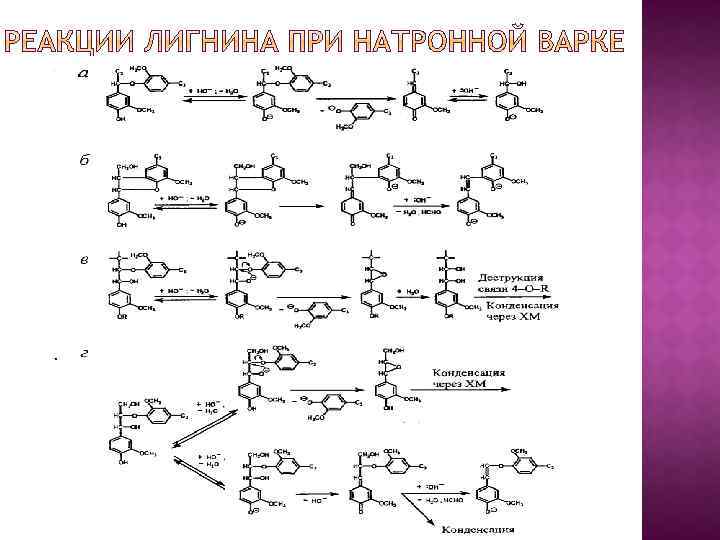
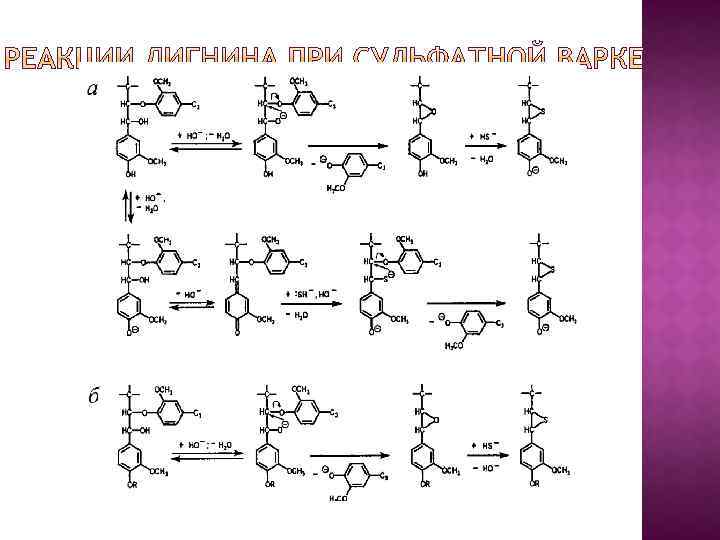
 Существуют два основных метода щелочной варки: натронный и сульфатный. При натронной варке варочный раствор содержит гидроксид натрия Na. ОН, а при сульфатной варке гидроксид натрия и сульфид натрия (Na. ОН + Na 2 S). При щелочных методах варки с лигнином протекают две конкури рующие реакции: статистическая сольволитическая деструкция (деградация) и конденсация. Однако при натронной варке в варочном растворе нет сильного нуклеофила, который бы обеспечил защиту от конденсации. Поэтому натронную варку применяют ограниченно лишь для получения технической целлюлозы из древесины лиственных пород и некоторых видов однолетнего растительного сырья. Сульфатная варка дает определенные преимущества по сравнению с натронной. Сульфид натрия служит как бы резервной щелочью. По мере расходования Na. ОН на варку равновесие реакции гидролиза сульфида натрия сдвигается вправо. Поэтому варку можно вести при меньшей щелочности, т. е. в более мягких условиях. Предполагают, что Na 2 S в какой то мере как восстановитель защищает полисахариды от щелочной деполимеризации. Все это способствует увеличению выхода технической целлюлозы. И самое главное, присутствующий в сульфатном варочном растворе сильный «внешний» нуклеофил НS существенно изменяет поведение лигнина обеспечивает защиту от конденсации и более полную его деструкцию, т. е. способствует делигнификации.
Существуют два основных метода щелочной варки: натронный и сульфатный. При натронной варке варочный раствор содержит гидроксид натрия Na. ОН, а при сульфатной варке гидроксид натрия и сульфид натрия (Na. ОН + Na 2 S). При щелочных методах варки с лигнином протекают две конкури рующие реакции: статистическая сольволитическая деструкция (деградация) и конденсация. Однако при натронной варке в варочном растворе нет сильного нуклеофила, который бы обеспечил защиту от конденсации. Поэтому натронную варку применяют ограниченно лишь для получения технической целлюлозы из древесины лиственных пород и некоторых видов однолетнего растительного сырья. Сульфатная варка дает определенные преимущества по сравнению с натронной. Сульфид натрия служит как бы резервной щелочью. По мере расходования Na. ОН на варку равновесие реакции гидролиза сульфида натрия сдвигается вправо. Поэтому варку можно вести при меньшей щелочности, т. е. в более мягких условиях. Предполагают, что Na 2 S в какой то мере как восстановитель защищает полисахариды от щелочной деполимеризации. Все это способствует увеличению выхода технической целлюлозы. И самое главное, присутствующий в сульфатном варочном растворе сильный «внешний» нуклеофил НS существенно изменяет поведение лигнина обеспечивает защиту от конденсации и более полную его деструкцию, т. е. способствует делигнификации.
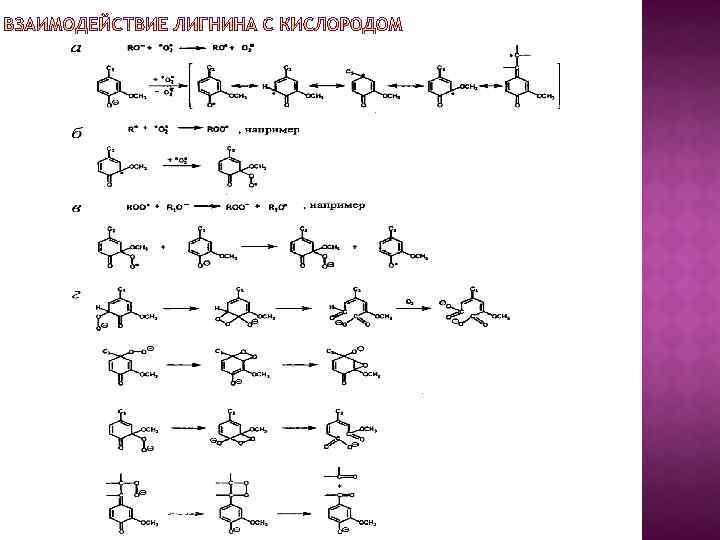
 При взаимодействии Na. ОН со свободными фенольными гидроксилами лигнина образуются феноляты и лигнин переходит в отработанный варочный раствор (черный щелок) в виде фенолятов Из черного щелока можно осадить щелочной лигнин (натронный или сульфатный) подкислением минеральной кислотой (НСl, Н 2 SО 4) и даже слабой угольной кислотой. Под действием Na. ОН в лигнине расщепляются связи С О С алкил О арил, алкил О алкил и алкил О углевод с образованием растворимых фрагментов лигнина с новыми свободными фенольными гидроксилами. Связи арил О арил устойчивы. В растворе происходит дальнейшая деструкция фрагментов сетки до низкомолекулярных продуктов, не осаждаемых при подкислении. Образуется «водорастворимый лигнин» , составляющий до 25% всего лигнина.
При взаимодействии Na. ОН со свободными фенольными гидроксилами лигнина образуются феноляты и лигнин переходит в отработанный варочный раствор (черный щелок) в виде фенолятов Из черного щелока можно осадить щелочной лигнин (натронный или сульфатный) подкислением минеральной кислотой (НСl, Н 2 SО 4) и даже слабой угольной кислотой. Под действием Na. ОН в лигнине расщепляются связи С О С алкил О арил, алкил О алкил и алкил О углевод с образованием растворимых фрагментов лигнина с новыми свободными фенольными гидроксилами. Связи арил О арил устойчивы. В растворе происходит дальнейшая деструкция фрагментов сетки до низкомолекулярных продуктов, не осаждаемых при подкислении. Образуется «водорастворимый лигнин» , составляющий до 25% всего лигнина.