083eee5c52e3298be92054f5fb738d17.ppt
- Количество слайдов: 14
 Получение персонализированных клеточных препаратов на основе антигенактивированных дендритных клеток и антиген-специфических Т лимфоцитов, предотвращающих рецидив опухоли. Руководитель исследования: Сенников С. В. , д. м. н. , профессор, руководитель лаборатории молекулярной иммунологии НИИФКИ Организация: Федеральное государственное бюджетное научное учреждение «Научно-исследовательский институт фундаментальной и клинической иммунологии» (НИИФКИ) Науки о жизни
Получение персонализированных клеточных препаратов на основе антигенактивированных дендритных клеток и антиген-специфических Т лимфоцитов, предотвращающих рецидив опухоли. Руководитель исследования: Сенников С. В. , д. м. н. , профессор, руководитель лаборатории молекулярной иммунологии НИИФКИ Организация: Федеральное государственное бюджетное научное учреждение «Научно-исследовательский институт фундаментальной и клинической иммунологии» (НИИФКИ) Науки о жизни
 Цели и задачи исследования Цели проекта: Разработка лабораторного регламента получения клеточных препаратов на основе антиген-активированных дендритных клеток и антиген-специфических Т-лимфоцитов для предотвращения рецидива опухоли. Задачи проекта: 1. Разработка лабораторного регламента культивирования зрелых дендритных клеток (ДК) у больных раком молочной железы (РМЖ), колоректальным раком (КРР) и немелкоклеточным раком легкого (НМРЛ). 3. Разработка методики создания ДНК-конструкций, кодирующей эпитопы опухоль-ассоциированных антигенов (ОАА) для различных эпителиальных форм злокачественных новообразований. 4. Разработка методики доставки антигенного материала в дендритные клетки. 5. Разработка лабораторного регламента получения фракции активированных мононуклеарных клеток больных РМЖ, КРР и НМРЛ, обладающих противоопухолевой цитотоксической активностью против опухолевых клеток и лабораторного регламента использования факторов-регуляторов активности клеточных препаратов. 6. Разработка лабораторного регламента получения антиген-специфических цитотоксических Т-лимфоцитов, обладающих противоопухолевой цитотоксической активностью против клеток РМЖ. 7. Создание опытного образца ДНК-конструкции, кодирующей эпитопы ОАА, в количестве, достаточном для проведения доклинических исследований. 8. Разработка плана и проведение доклинических исследований; 9. Разработка проекта протокола клинического исследования клеточного препарата для медицинского применения. <Номер соглашения> 2
Цели и задачи исследования Цели проекта: Разработка лабораторного регламента получения клеточных препаратов на основе антиген-активированных дендритных клеток и антиген-специфических Т-лимфоцитов для предотвращения рецидива опухоли. Задачи проекта: 1. Разработка лабораторного регламента культивирования зрелых дендритных клеток (ДК) у больных раком молочной железы (РМЖ), колоректальным раком (КРР) и немелкоклеточным раком легкого (НМРЛ). 3. Разработка методики создания ДНК-конструкций, кодирующей эпитопы опухоль-ассоциированных антигенов (ОАА) для различных эпителиальных форм злокачественных новообразований. 4. Разработка методики доставки антигенного материала в дендритные клетки. 5. Разработка лабораторного регламента получения фракции активированных мононуклеарных клеток больных РМЖ, КРР и НМРЛ, обладающих противоопухолевой цитотоксической активностью против опухолевых клеток и лабораторного регламента использования факторов-регуляторов активности клеточных препаратов. 6. Разработка лабораторного регламента получения антиген-специфических цитотоксических Т-лимфоцитов, обладающих противоопухолевой цитотоксической активностью против клеток РМЖ. 7. Создание опытного образца ДНК-конструкции, кодирующей эпитопы ОАА, в количестве, достаточном для проведения доклинических исследований. 8. Разработка плана и проведение доклинических исследований; 9. Разработка проекта протокола клинического исследования клеточного препарата для медицинского применения. <Номер соглашения> 2
 Актуальность и новизна В настоящее время эффективность современной иммунотерапии и профилактики рецидивов неопластических процессов заключается в коррекции нарушений презентации антигена и генерации антиген-специфических цитотоксических Тлимфоцитов. Ключевая роль в активации противоопухолевого клеточного иммунитета принадлежит дендритным клеткам (ДК), которые распознают и представляют антигены в комплексе с молекулами HLA I и II класса Т- и В-лимфоцитам, экспрессируют большое количество молекул HLA I и II классов и ко-стимуляторных факторов (CD 80, CD 86), способствующих эффективной презентации ОАА. Перспективным подходом к лечению рака является активная иммунотерапия, которая в настоящее время представляется неотъемлемой частью современной клинической практики. Поскольку главная цель иммунотерапии при онкологии заключается в обеспечении сильного и устойчивого опухолеспецифического иммунного ответа, достижение подобных результатов возможно через стимуляцию CD 4+ и CD 8+ Т-клеток. CD 8+ Т-лимфоциты являются главными эффекторными клетками противоракового иммунного ответа, образование которых зависит от подходящего антигена-мишени и эффективной презентации данного антигена иммунной системе пациента с участием антигенпрезентирующих клеток (АПК). Дендритные клетки являются наиболее эффективными АПК и единственными клетками, способными представлять новые антигены неактивированным Т-клеткам. Поэтому применение аутологичных дендритных клеток, трансфицированных уникальными ДНК-вакцинными конструкциями, кодирующими искусственные полиэпитопные белки-иммуногены, представляет собой эффективный инструмент для презентации антигенов иммунной системе пациента. <Номер соглашения>
Актуальность и новизна В настоящее время эффективность современной иммунотерапии и профилактики рецидивов неопластических процессов заключается в коррекции нарушений презентации антигена и генерации антиген-специфических цитотоксических Тлимфоцитов. Ключевая роль в активации противоопухолевого клеточного иммунитета принадлежит дендритным клеткам (ДК), которые распознают и представляют антигены в комплексе с молекулами HLA I и II класса Т- и В-лимфоцитам, экспрессируют большое количество молекул HLA I и II классов и ко-стимуляторных факторов (CD 80, CD 86), способствующих эффективной презентации ОАА. Перспективным подходом к лечению рака является активная иммунотерапия, которая в настоящее время представляется неотъемлемой частью современной клинической практики. Поскольку главная цель иммунотерапии при онкологии заключается в обеспечении сильного и устойчивого опухолеспецифического иммунного ответа, достижение подобных результатов возможно через стимуляцию CD 4+ и CD 8+ Т-клеток. CD 8+ Т-лимфоциты являются главными эффекторными клетками противоракового иммунного ответа, образование которых зависит от подходящего антигена-мишени и эффективной презентации данного антигена иммунной системе пациента с участием антигенпрезентирующих клеток (АПК). Дендритные клетки являются наиболее эффективными АПК и единственными клетками, способными представлять новые антигены неактивированным Т-клеткам. Поэтому применение аутологичных дендритных клеток, трансфицированных уникальными ДНК-вакцинными конструкциями, кодирующими искусственные полиэпитопные белки-иммуногены, представляет собой эффективный инструмент для презентации антигенов иммунной системе пациента. <Номер соглашения>
 Описание исследования Для решения задач проекты были использованы следующие методики и решения: -для получения зрелых дендритных клеток использованы моноциты периферической крови онкобольных, которые были получены посредством их повышенной адгезии к пластику и их дальнейшее культивирование в присутствии rh. GM-CSF, rh. IL-4 и rh. TNF-a. - для создания ДНК-конструкций, кодируюшей эпитопы ОАА для различных эпителиальных форм злокачественных новообразований были отобраны основные ОАА, гиперэкспрессирующиеся на опухолевых клетках при РМЖ, КРР, НМРЛ. Используя современные базы данных был обоснован выбор антигенов, необходимых для создания генетических конструкций и последующего формирования эффективного противоопухолевого иммунного ответа. На основе использования специализированного программного обеспечения (в том числе и собственного оригинального) выбраны терапевтически наиболее эффективные антигенные детерминанты, узнаваемые цитотоксическими клетками. <Номер соглашения> 4
Описание исследования Для решения задач проекты были использованы следующие методики и решения: -для получения зрелых дендритных клеток использованы моноциты периферической крови онкобольных, которые были получены посредством их повышенной адгезии к пластику и их дальнейшее культивирование в присутствии rh. GM-CSF, rh. IL-4 и rh. TNF-a. - для создания ДНК-конструкций, кодируюшей эпитопы ОАА для различных эпителиальных форм злокачественных новообразований были отобраны основные ОАА, гиперэкспрессирующиеся на опухолевых клетках при РМЖ, КРР, НМРЛ. Используя современные базы данных был обоснован выбор антигенов, необходимых для создания генетических конструкций и последующего формирования эффективного противоопухолевого иммунного ответа. На основе использования специализированного программного обеспечения (в том числе и собственного оригинального) выбраны терапевтически наиболее эффективные антигенные детерминанты, узнаваемые цитотоксическими клетками. <Номер соглашения> 4
 Описание исследования -для получения фракции активированных лимфоцитов, популяция ДК, нагруженных ОАА, будет сокультивирована с аутологичными МНК, в соотношении 1: 10. Основная оценка эффективность формирования специфического цитотоксического иммунного ответа проводилась по оценке развития прямого цитотоксического эффекта против опухолевых клеток (клеточные линии или аутологичные опухолевые клетки) с помощью колориметрического метода определения содержания лактатдегидрогеназы, а также метода проточной цитометрии с прижизненной меткой опухолевых клеток. - получение популяции антиген-специфических Т-клеток без активирования поверхностных молекул рецепторов основано натехнологии стрептамеров, которая заключается в выделения антигенспецифических Т-клеток из общей фракции МНК крови методом выделения на колонках с магнитными бусами, после чего маркерные молекулы удаляли путем связывания с биотином. <Номер соглашения> 5
Описание исследования -для получения фракции активированных лимфоцитов, популяция ДК, нагруженных ОАА, будет сокультивирована с аутологичными МНК, в соотношении 1: 10. Основная оценка эффективность формирования специфического цитотоксического иммунного ответа проводилась по оценке развития прямого цитотоксического эффекта против опухолевых клеток (клеточные линии или аутологичные опухолевые клетки) с помощью колориметрического метода определения содержания лактатдегидрогеназы, а также метода проточной цитометрии с прижизненной меткой опухолевых клеток. - получение популяции антиген-специфических Т-клеток без активирования поверхностных молекул рецепторов основано натехнологии стрептамеров, которая заключается в выделения антигенспецифических Т-клеток из общей фракции МНК крови методом выделения на колонках с магнитными бусами, после чего маркерные молекулы удаляли путем связывания с биотином. <Номер соглашения> 5
 Результаты исследования - разработан лабораторный регламент получения зрелых антигенактивированных дендритных клеток, - создана ДНК-конструкция, кодирующая эпитопы опухоль-ассоциированных антигенов колоректального рака (КРР), рака молочной железы (РМЖ) и немелкоклеточного рака легкого (НМРЛ), - разработан лабораторный регламент получения фракции активированных мононуклеарных клеток больных РМЖ, КРР и НМРЛ, обладающих противоопухолевой цитотоксической активностью против опухолевых клеток и использования факторов-регуляторов активности клеточных препаратов. -разработан лабораторный регламент получения антиген-специфических цитотоксических Т-лимфоцитов, обладающих противоопухолевой цитотоксической активностью против клеток рака молочной железы. За время выполнения проекта опубликовано 7 статей в журналах, индексируемый в Scopus и/или Web of Science, и 2 статьи, в настоящее время, находятся на рассмотрении в редакциях журналов, индексируемых в Scopus и/или Web of Science. Подготовлены и отправлены на регистрацию в Роспатент 3 заявки на патент РФ на изобретение. <Номер соглашения> 6
Результаты исследования - разработан лабораторный регламент получения зрелых антигенактивированных дендритных клеток, - создана ДНК-конструкция, кодирующая эпитопы опухоль-ассоциированных антигенов колоректального рака (КРР), рака молочной железы (РМЖ) и немелкоклеточного рака легкого (НМРЛ), - разработан лабораторный регламент получения фракции активированных мононуклеарных клеток больных РМЖ, КРР и НМРЛ, обладающих противоопухолевой цитотоксической активностью против опухолевых клеток и использования факторов-регуляторов активности клеточных препаратов. -разработан лабораторный регламент получения антиген-специфических цитотоксических Т-лимфоцитов, обладающих противоопухолевой цитотоксической активностью против клеток рака молочной железы. За время выполнения проекта опубликовано 7 статей в журналах, индексируемый в Scopus и/или Web of Science, и 2 статьи, в настоящее время, находятся на рассмотрении в редакциях журналов, индексируемых в Scopus и/или Web of Science. Подготовлены и отправлены на регистрацию в Роспатент 3 заявки на патент РФ на изобретение. <Номер соглашения> 6
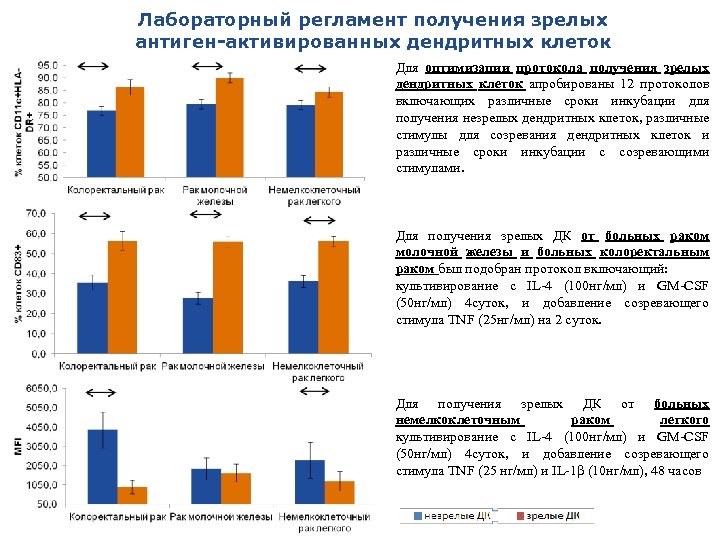 Лабораторный регламент получения зрелых антиген-активированных дендритных клеток Для оптимизации протокола получения зрелых дендритных клеток апробированы 12 протоколов включающих различные сроки инкубации для получения незрелых дендритных клеток, различные стимулы для созревания дендритных клеток и различные сроки инкубации с созревающими стимулами. Для получения зрелых ДК от больных раком молочной железы и больных колоректальным раком был подобран протокол включающий: культивирование с IL-4 (100 нг/мл) и GM-CSF (50 нг/мл) 4 суток, и добавление созревающего стимула TNF (25 нг/мл) на 2 суток. Для получения зрелых ДК от больных немелкоклеточным раком легкого культивирование с IL-4 (100 нг/мл) и GM-CSF (50 нг/мл) 4 суток, и добавление созревающего стимула TNF (25 нг/мл) и IL-1β (10 нг/мл), 48 часов
Лабораторный регламент получения зрелых антиген-активированных дендритных клеток Для оптимизации протокола получения зрелых дендритных клеток апробированы 12 протоколов включающих различные сроки инкубации для получения незрелых дендритных клеток, различные стимулы для созревания дендритных клеток и различные сроки инкубации с созревающими стимулами. Для получения зрелых ДК от больных раком молочной железы и больных колоректальным раком был подобран протокол включающий: культивирование с IL-4 (100 нг/мл) и GM-CSF (50 нг/мл) 4 суток, и добавление созревающего стимула TNF (25 нг/мл) на 2 суток. Для получения зрелых ДК от больных немелкоклеточным раком легкого культивирование с IL-4 (100 нг/мл) и GM-CSF (50 нг/мл) 4 суток, и добавление созревающего стимула TNF (25 нг/мл) и IL-1β (10 нг/мл), 48 часов
 Создание ДНК-конструкции, кодирующей эпитопы опухольассоциированных антигенов для различных эпителиальных форм злокачественных новообразований. Все экспериментальные образцы ДНК-конструкций, кодирующих эпитопы ОАА для различных форм злокачественных новообразований, были наработаны в количестве, достаточном для проведения всех необходимых экспериментов и исследований с материалом от больных раком молочной железы, колоректальным раком и немелкоклеточным раком легкого, и очищены от эндотоксинов с подтверждением правильности нуклеотидной последовательности секвенированием. ДНК-конструкции (в количестве 5 мг каждой) кодируют 323 эпитопа от 26 ОАА: pmax-CTL 1: содержит эпитопы из HER-2 (31), mammaglobin-A (13), NY-BR-1 (19) и h. Mena (8); pmax-CTL 2: эпитопы из WT 1 (12), теломеразы h. TERT (23), survivin (6), p 53 (23) и MUC 1 (13); pmax-CTL 3: эпитопы из MAGE-A 10 (11), NY-ESO-1 (9) и MUC-1 (9); pmax-CTL 4: эпитопы из MAGE-A 3 (11), PRAME (12), Ep. CAM (4) и MUC-1 (9); pmax-CTL 5: эпитопы из Ep. CAM (4), CEA (11), Guanylyl Cyclase C (11) и 5 T 4 (8); pmax-CTL 6: эпитопы из Legumain (7), VEGFR-1 (10), VEGFR-2 (10), FAP (9) и Fos-related antigen-1 (5); pmax-CTL 7: эпитопы из Brachyury (9), SOX 2 (4), Snail 1 (4) и Snail 2 (4); pmax-Poly. Th: эпитопы из HER 2 (2), h. TERT (1), p 53 (3), WT 1 (1), NY-ESO-1 (1), VEGFR-2 (1), survivin (4) и MAGE-A 3 (1); Чистота ДНК-конструкции составляет 99%. <Номер соглашения> 8
Создание ДНК-конструкции, кодирующей эпитопы опухольассоциированных антигенов для различных эпителиальных форм злокачественных новообразований. Все экспериментальные образцы ДНК-конструкций, кодирующих эпитопы ОАА для различных форм злокачественных новообразований, были наработаны в количестве, достаточном для проведения всех необходимых экспериментов и исследований с материалом от больных раком молочной железы, колоректальным раком и немелкоклеточным раком легкого, и очищены от эндотоксинов с подтверждением правильности нуклеотидной последовательности секвенированием. ДНК-конструкции (в количестве 5 мг каждой) кодируют 323 эпитопа от 26 ОАА: pmax-CTL 1: содержит эпитопы из HER-2 (31), mammaglobin-A (13), NY-BR-1 (19) и h. Mena (8); pmax-CTL 2: эпитопы из WT 1 (12), теломеразы h. TERT (23), survivin (6), p 53 (23) и MUC 1 (13); pmax-CTL 3: эпитопы из MAGE-A 10 (11), NY-ESO-1 (9) и MUC-1 (9); pmax-CTL 4: эпитопы из MAGE-A 3 (11), PRAME (12), Ep. CAM (4) и MUC-1 (9); pmax-CTL 5: эпитопы из Ep. CAM (4), CEA (11), Guanylyl Cyclase C (11) и 5 T 4 (8); pmax-CTL 6: эпитопы из Legumain (7), VEGFR-1 (10), VEGFR-2 (10), FAP (9) и Fos-related antigen-1 (5); pmax-CTL 7: эпитопы из Brachyury (9), SOX 2 (4), Snail 1 (4) и Snail 2 (4); pmax-Poly. Th: эпитопы из HER 2 (2), h. TERT (1), p 53 (3), WT 1 (1), NY-ESO-1 (1), VEGFR-2 (1), survivin (4) и MAGE-A 3 (1); Чистота ДНК-конструкции составляет 99%. <Номер соглашения> 8
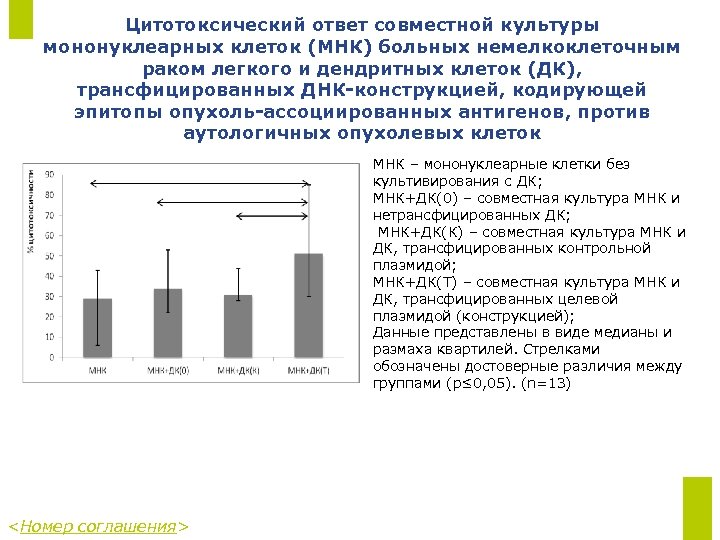 Цитотоксический ответ совместной культуры мононуклеарных клеток (МНК) больных немелкоклеточным раком легкого и дендритных клеток (ДК), трансфицированных ДНК-конструкцией, кодирующей эпитопы опухоль-ассоциированных антигенов, против аутологичных опухолевых клеток МНК – мононуклеарные клетки без культивирования с ДК; МНК+ДК(0) – совместная культура МНК и нетрансфицированных ДК; МНК+ДК(К) – совместная культура МНК и ДК, трансфицированных контрольной плазмидой; МНК+ДК(Т) – совместная культура МНК и ДК, трансфицированных целевой плазмидой (конструкцией); Данные представлены в виде медианы и размаха квартилей. Стрелками обозначены достоверные различия между группами (p≤ 0, 05). (n=13) <Номер соглашения>
Цитотоксический ответ совместной культуры мононуклеарных клеток (МНК) больных немелкоклеточным раком легкого и дендритных клеток (ДК), трансфицированных ДНК-конструкцией, кодирующей эпитопы опухоль-ассоциированных антигенов, против аутологичных опухолевых клеток МНК – мононуклеарные клетки без культивирования с ДК; МНК+ДК(0) – совместная культура МНК и нетрансфицированных ДК; МНК+ДК(К) – совместная культура МНК и ДК, трансфицированных контрольной плазмидой; МНК+ДК(Т) – совместная культура МНК и ДК, трансфицированных целевой плазмидой (конструкцией); Данные представлены в виде медианы и размаха квартилей. Стрелками обозначены достоверные различия между группами (p≤ 0, 05). (n=13) <Номер соглашения>
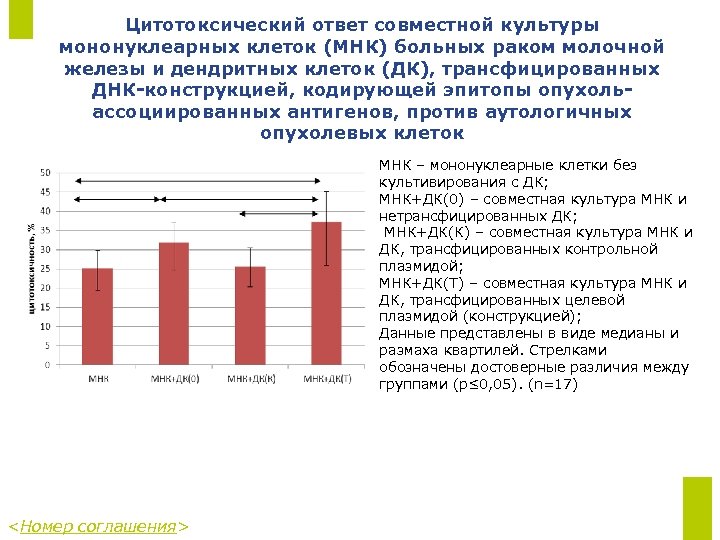 Цитотоксический ответ совместной культуры мононуклеарных клеток (МНК) больных раком молочной железы и дендритных клеток (ДК), трансфицированных ДНК-конструкцией, кодирующей эпитопы опухольассоциированных антигенов, против аутологичных опухолевых клеток МНК – мононуклеарные клетки без культивирования с ДК; МНК+ДК(0) – совместная культура МНК и нетрансфицированных ДК; МНК+ДК(К) – совместная культура МНК и ДК, трансфицированных контрольной плазмидой; МНК+ДК(Т) – совместная культура МНК и ДК, трансфицированных целевой плазмидой (конструкцией); Данные представлены в виде медианы и размаха квартилей. Стрелками обозначены достоверные различия между группами (p≤ 0, 05). (n=17) <Номер соглашения>
Цитотоксический ответ совместной культуры мононуклеарных клеток (МНК) больных раком молочной железы и дендритных клеток (ДК), трансфицированных ДНК-конструкцией, кодирующей эпитопы опухольассоциированных антигенов, против аутологичных опухолевых клеток МНК – мононуклеарные клетки без культивирования с ДК; МНК+ДК(0) – совместная культура МНК и нетрансфицированных ДК; МНК+ДК(К) – совместная культура МНК и ДК, трансфицированных контрольной плазмидой; МНК+ДК(Т) – совместная культура МНК и ДК, трансфицированных целевой плазмидой (конструкцией); Данные представлены в виде медианы и размаха квартилей. Стрелками обозначены достоверные различия между группами (p≤ 0, 05). (n=17) <Номер соглашения>
 Цитотоксический ответ совместной культуры мононуклеарных клеток (МНК) больных колоректальным раком и дендритных клеток (ДК), трансфицированных ДНКконструкцией, кодирующей эпитопы опухольассоциированных антигенов, против аутологичных опухолевых клеток МНК – мононуклеарные клетки без культивирования с ДК; МНК+ДК(0) – совместная культура МНК и нетрансфицированных ДК; МНК+ДК(К) – совместная культура МНК и ДК, трансфицированных контрольной плазмидой; МНК+ДК(Т) – совместная культура МНК и ДК, трансфицированных целевой плазмидой (конструкцией); Данные представлены в виде медианы и размаха квартилей. Стрелками обозначены достоверные различия между группами (p≤ 0, 05). (n=110) <Номер соглашения>
Цитотоксический ответ совместной культуры мононуклеарных клеток (МНК) больных колоректальным раком и дендритных клеток (ДК), трансфицированных ДНКконструкцией, кодирующей эпитопы опухольассоциированных антигенов, против аутологичных опухолевых клеток МНК – мононуклеарные клетки без культивирования с ДК; МНК+ДК(0) – совместная культура МНК и нетрансфицированных ДК; МНК+ДК(К) – совместная культура МНК и ДК, трансфицированных контрольной плазмидой; МНК+ДК(Т) – совместная культура МНК и ДК, трансфицированных целевой плазмидой (конструкцией); Данные представлены в виде медианы и размаха квартилей. Стрелками обозначены достоверные различия между группами (p≤ 0, 05). (n=110) <Номер соглашения>
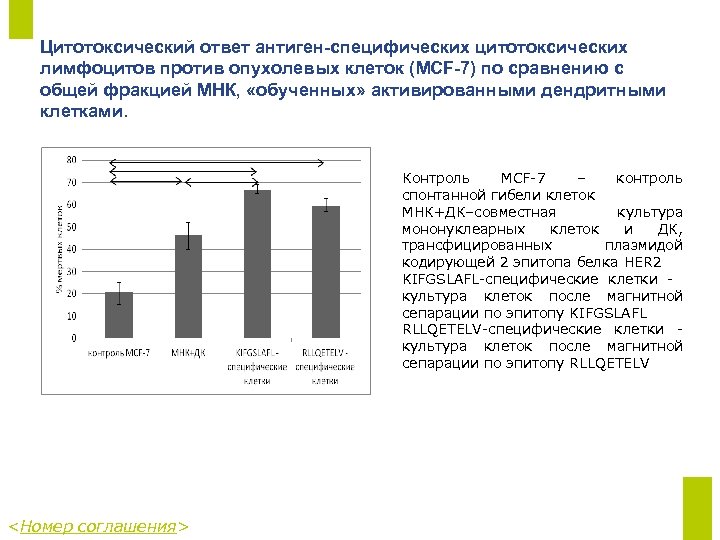 Цитотоксический ответ антиген-специфических цитотоксических лимфоцитов против опухолевых клеток (MCF-7) по сравнению с общей фракцией МНК, «обученных» активированными дендритными клетками. Контроль MCF-7 – контроль cпонтанной гибели клеток МНК+ДК–совместная культура мононуклеарных клеток и ДК, трансфицированных плазмидой кодирующей 2 эпитопа белка HER 2 KIFGSLAFL-специфические клетки культура клеток после магнитной сепарации по эпитопу KIFGSLAFL RLLQETELV-специфические клетки культура клеток после магнитной сепарации по эпитопу RLLQETELV <Номер соглашения>
Цитотоксический ответ антиген-специфических цитотоксических лимфоцитов против опухолевых клеток (MCF-7) по сравнению с общей фракцией МНК, «обученных» активированными дендритными клетками. Контроль MCF-7 – контроль cпонтанной гибели клеток МНК+ДК–совместная культура мононуклеарных клеток и ДК, трансфицированных плазмидой кодирующей 2 эпитопа белка HER 2 KIFGSLAFL-специфические клетки культура клеток после магнитной сепарации по эпитопу KIFGSLAFL RLLQETELV-специфические клетки культура клеток после магнитной сепарации по эпитопу RLLQETELV <Номер соглашения>
 Практическая значимость исследования Потребителями научно-технических результатов ПНИ являются ИП (ЗАО «Компания Витамакс» ), а также другие медицинские и научные центры, медицинские лечебнопрофилактические учреждения, оказывающие высокоспециализированную медицинскую помощь. Перспективы практического использования результатов проекта: - проведение ограниченных клинических исследований по оценке эффективности разработанных технологий совместно с индустриальным партнером, - продажа неисключительной лицензии на технологию получения и применения клеточного препарата индустриальному партнеру, - создание на базе лечебно-профилактических учреждений и медицинских центров лабораторий по созданию персонифицированных клеточных препаратов для проведения иммунотерапии онкологических больных. <Номер соглашения> 13
Практическая значимость исследования Потребителями научно-технических результатов ПНИ являются ИП (ЗАО «Компания Витамакс» ), а также другие медицинские и научные центры, медицинские лечебнопрофилактические учреждения, оказывающие высокоспециализированную медицинскую помощь. Перспективы практического использования результатов проекта: - проведение ограниченных клинических исследований по оценке эффективности разработанных технологий совместно с индустриальным партнером, - продажа неисключительной лицензии на технологию получения и применения клеточного препарата индустриальному партнеру, - создание на базе лечебно-профилактических учреждений и медицинских центров лабораторий по созданию персонифицированных клеточных препаратов для проведения иммунотерапии онкологических больных. <Номер соглашения> 13
 Спасибо за внимание! Докладчик: Курилин В. В. , старший научный сотрудник лаборатории молекулярной иммунологии НИИФКИ (тел. 8(383)2221910) Исследование выполнено в рамках программы ФЦП «Исследования и разработки по приоритетным направлениям развития научно-технологического комплекса России на 2014— 2020 годы» Результаты исследования представлены на стенде <номер стенда> <Номер соглашения> 14
Спасибо за внимание! Докладчик: Курилин В. В. , старший научный сотрудник лаборатории молекулярной иммунологии НИИФКИ (тел. 8(383)2221910) Исследование выполнено в рамках программы ФЦП «Исследования и разработки по приоритетным направлениям развития научно-технологического комплекса России на 2014— 2020 годы» Результаты исследования представлены на стенде <номер стенда> <Номер соглашения> 14


