32 Получение и хим. свойства алканов.ppt
- Количество слайдов: 10

ПОЛУЧЕНИЕ И ХИМИЧЕСКИЕ СВОЙСТВА АЛКАНОВ.
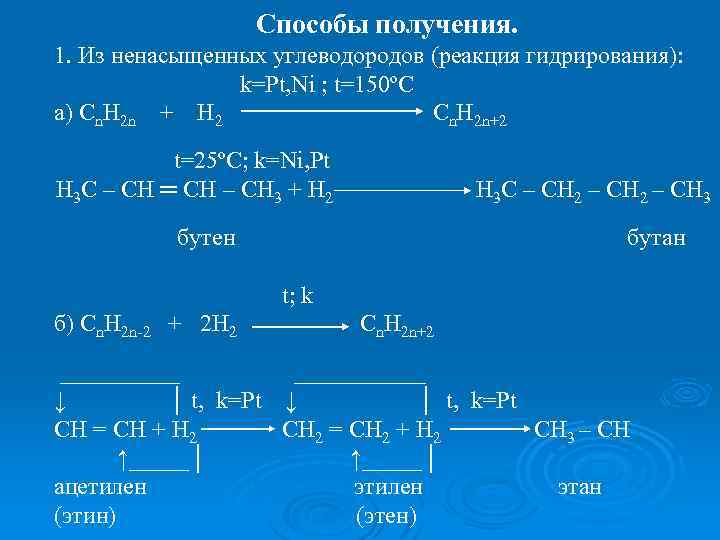
Способы получения. 1. Из ненасыщенных углеводородов (реакция гидрирования): k=Pt, Ni ; t=150ºC а) Cn. H 2 n + H 2 Cn. H 2 n+2 t=25ºC; k=Ni, Pt Н 3 С – СН ═ СН – СН 3 + Н 2 Н 3 С – СН 2 – СН 3 бутен бутан t; k б) Сn. H 2 n-2 + 2 H 2 Cn. H 2 n+2 ___________ ↓ │ t, k=Pt CH = CH + H 2 CH 2 = CH 2 + H 2 CH 3 – CH ↑_____│ ацетилен этан (этин) (этен)

2. Из галогенопроизводных (реакция Вюрца). Этой реакцией пользуются, когда необходимо увеличить углеродную цепь. t˚ R – Hal + 2 Na + R – Hal R – R + 2 Na. Hal t˚ 2 CH 3 I+ 2 Na H 3 C – CH 3 + 2 Na. I иодметан этан • Из солей карбоновых кислот: t˚ СН 3 COONa + Na. O H Na 2 CO 3 + CH 4↑ ацетат натрия крист. 4. Прямой синтез из углерода и водорода t=400 -500ºC, K=Ni С + 2 Н 2 СН 4 5. Из нефти, природного газа. 6. Из карбида алюминия: Al 4 C 3 + 12 H 2 O 4 Al(OH)3 + 3 CH 4↑

7. Синтез из угарного газа и водорода: p, t=200 -300ºC, K=Co, Fe n. CO + ( 2 n+1 ) H 2 —————→ Cn. H 2 n+2 + n. H 2 Этим способом получают алканы от С 6 до С 10. Химические свойства. Алканы, по словам Коновалова, «химические мертвецы» . Для них характерны реакции замещения. Реакции замещения: 1. Галогенирование. Эта реакция является фотохимической реакцией: свет СН 4 + Сl 2 ——→ CH 3 Cl + Cl 2 ——→ - HCl хлорметан свет ——→ CH 2 Cl 2 + Cl 2——→ CHCl 3 -HCl трихлорметан дихлорметан ( хлороформ )

свет СНCl 3 + Cl 2 ———→ CCl 4 - HCl четыреххлористый углерод тетрахлорметан Эта реакция протекает по свободнорадикальному механизму. Впервые этот механизм был изучен русским химиком Семеновым. Такие реакции называют часто цепными реакциями. 2. Нитрование ( реакция Коновалова ): CH 3 СН 3 │ t=140ºC │ Н 3 С—СН 2—СН 3+HNO 3→H 3 C—CH 2—CH 3 10 % - H 2 O 3 -метилпентан ( HO—NO 2 ) азотная кислота │ NO 2 3 -метил-3 -нитропентан Правило Зайцева: ” Отщепление атомов водорода всегда происходит от наименее гидрогенизированного атома углерода”.

3. Сульфирование: СН 3 │ H 2 SO 4 t │ СН 3—СН 2—С—СН 3+НО—SO 3 H →СН 3—СН 2—С—СН 3 │ конц. │ Н SO 3 H 2 -метилбутан 2 -метил-2 -бутансульфокислота II. Горение: t t t а)СН 4+2 О 2→СО 2↑+2 Н 2 О б)2 СН 4+3 О 2→ 2 СО+4 Н 2 О в)СН 4+О 2→С+2 Н 2 О избыток недост. III. Разложение: t=1000ºC CH 4————→ C+2 H 2↑ IV. Дегидрирование ( отщепление водорода ) t=1500ºС 2 СН 4 ——————→С 2 Н 2 + 3 Н 2↑ ацетилен недост.
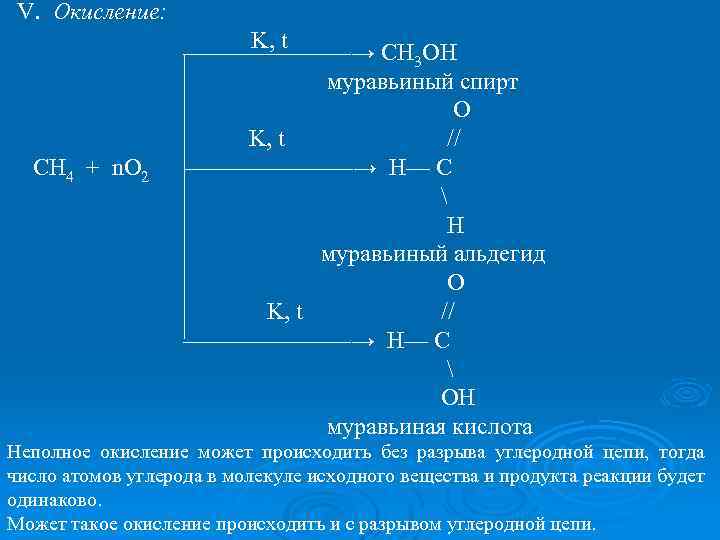
V. Окисление: СН 4 + n. O 2 K, t ———————→ CH 3 OH муравьиный спирт O K, t // ———————→ H— C H муравьиный альдегид O K, t // ———————→ H— C OH муравьиная кислота Неполное окисление может происходить без разрыва углеродной цепи, тогда число атомов углерода в молекуле исходного вещества и продукта реакции будет одинаково. Может такое окисление происходить и с разрывом углеродной цепи.
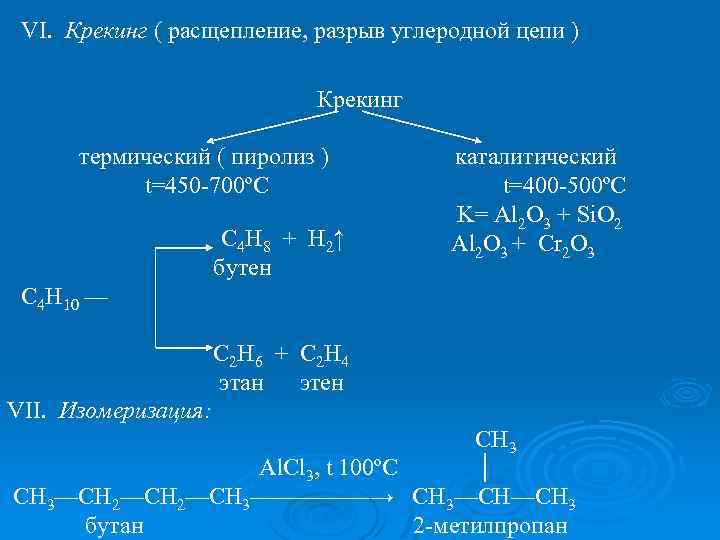
VI. Крекинг ( расщепление, разрыв углеродной цепи ) Крекинг термический ( пиролиз ) t=450 -700ºC C 4 H 8 + H 2↑ бутен каталитический t=400 -500ºC K= Al 2 O 3 + Si. O 2 Al 2 O 3 + Cr 2 O 3 C 4 H 10 — С 2 Н 6 + С 2 Н 4 этан этен VII. Изомеризация: СН 3 Al. Cl 3, t 100ºC │ СН 3—СН 2—СН 3—————→ СН 3—СН—СН 3 бутан 2 -метилпропан

Отдельные представители алканов и их применение. 1. СН 4 – метан. Бесцветный газ, без запаха, малорастворим в воде, легче воздуха, называют его ”болотным газом”, так как образуется при гниении растительных остатков на дне болот без доступа воздуха, входит в состав нефтяного, природного газа, используется в органическом синтезе, как топливо. 2. С 2 Н 6 – этан. Бесцветный газ, без запаха, мало растворим в воде, проявляет слабое наркотическое действие, используется как сырье в органическом синтезе. 3. С 3 Н 8 – пропан Бесцветные газы, легко сжимаются, в быту используются кактопливо (балонный газ), используется как автомобильное топливо. Бутан используют для получения бутадиена, С 4 Н 10 – бутан который является сырьем для производства синтетического каучука.

4. Вазелиновое масло – смесь жидких алканов до С 15. Бесцветная жидкость без запаха, без вкуса, используется в медицине и парфюмерии. Его используют в технике как основу кислотностойких и неокисляющихся смазочных масел. 5. Вазелин – смесь жидких и твердых алканов до С 25. Используется в косметике и в медицине как мазевая основа, в физиотерапевтических процедурах. 6. Парафин – смесь твердых алканов с С 18 до С 35. Применяется для пропитки материалов (бумаги, ткани, древесины). В медицине используют для физиотерапевтических процедур. Озокерит, горный воск – природная смесь высших алканов. В медицине используют для физиотерапевтических процедур.
32 Получение и хим. свойства алканов.ppt