Получение и свойства коллоидных растворов2.ppt
- Количество слайдов: 30
 Получение и свойства коллоидных растворов Тема 2
Получение и свойства коллоидных растворов Тема 2
 Что такое коллоидные растворы? • Коллоидными растворами (золями) называются высокодисперсные гетерогенные системы, в которых хотя бы одно вещество находится в коллоидном состоянии. • Коллоидное состояние – это высокодисперсное состояние, когда вещество раздроблено до частиц размерами 10 -9 – 10 -7 м. • Среда, в которой распределены частицы дисперсной фазы, называется дисперсионной средой.
Что такое коллоидные растворы? • Коллоидными растворами (золями) называются высокодисперсные гетерогенные системы, в которых хотя бы одно вещество находится в коллоидном состоянии. • Коллоидное состояние – это высокодисперсное состояние, когда вещество раздроблено до частиц размерами 10 -9 – 10 -7 м. • Среда, в которой распределены частицы дисперсной фазы, называется дисперсионной средой.
 СПОСОБЫ ПОЛУЧЕНИЯ КОЛЛОИДНЫХ РАСТВОРОВ Необходимые условия: 1) Нерастворимость или очень малая растворимость вещества дисперсной фазы в дисперсионной среде. 2) Наличие в среде веществ, которые способны стабилизировать частицы дисперсной фазы – стабилизаторов.
СПОСОБЫ ПОЛУЧЕНИЯ КОЛЛОИДНЫХ РАСТВОРОВ Необходимые условия: 1) Нерастворимость или очень малая растворимость вещества дисперсной фазы в дисперсионной среде. 2) Наличие в среде веществ, которые способны стабилизировать частицы дисперсной фазы – стабилизаторов.
 • Диспергационные методы – это способы получение коллоидных растворов путем дробления (диспергирования) крупных кусков до агрегатов коллоидных размеров. • Различают механическое, ультразвуковое, электрическое диспергирование.
• Диспергационные методы – это способы получение коллоидных растворов путем дробления (диспергирования) крупных кусков до агрегатов коллоидных размеров. • Различают механическое, ультразвуковое, электрическое диспергирование.
 Конденсационные методы – это способы получения коллоидных растворов путем объединения (конденсации) молекул и ионов в агрегаты коллоидных размеров.
Конденсационные методы – это способы получения коллоидных растворов путем объединения (конденсации) молекул и ионов в агрегаты коллоидных размеров.
![Конденсационные методы Это могут быть реакции восстановления, окисления, гидролиза, обмена: K 4[Fe(CN)6] + 2 Конденсационные методы Это могут быть реакции восстановления, окисления, гидролиза, обмена: K 4[Fe(CN)6] + 2](https://present5.com/presentation/3/11724273_69881534.pdf-img/11724273_69881534.pdf-6.jpg) Конденсационные методы Это могут быть реакции восстановления, окисления, гидролиза, обмена: K 4[Fe(CN)6] + 2 Cu. Cl 2 =↓ Cu 2[Fe(CN)6 + 4 KCl золь
Конденсационные методы Это могут быть реакции восстановления, окисления, гидролиза, обмена: K 4[Fe(CN)6] + 2 Cu. Cl 2 =↓ Cu 2[Fe(CN)6 + 4 KCl золь
 • Метод пептизации. Измельченный материал или промытый осадок вещества, полученный в результате химической реакции осаждения, промывают небольшим количеством раствора пептизатора, в результате образуется высокодисперсная система. Пептизация – это нарушение связей между слипшимися частицами. Чем слабее эти связи, тем легче происходит пептизация. •
• Метод пептизации. Измельченный материал или промытый осадок вещества, полученный в результате химической реакции осаждения, промывают небольшим количеством раствора пептизатора, в результате образуется высокодисперсная система. Пептизация – это нарушение связей между слипшимися частицами. Чем слабее эти связи, тем легче происходит пептизация. •
 Почему образуются коллоидные растворы? Что является их структурной единицей?
Почему образуются коллоидные растворы? Что является их структурной единицей?
 КОЛЛОИДНАЯ ЧАСТИЦА МИЦЕЛЛА
КОЛЛОИДНАЯ ЧАСТИЦА МИЦЕЛЛА
 Что такое коллоидная частица? Коллоидная частица имеет заряд. Объясняет строение коллоидной частицы ТЕОРИЯ ДВОЙНОГО ЭЛЕКТРИЧЕСКОГО СЛОЯ.
Что такое коллоидная частица? Коллоидная частица имеет заряд. Объясняет строение коллоидной частицы ТЕОРИЯ ДВОЙНОГО ЭЛЕКТРИЧЕСКОГО СЛОЯ.
 Теории ДЭС • теория Гельмгольца-Перрена (1879); • теория Гуи-Чепмена (1910 -1913); • теория Штерна (1924). Отличие между этими теориями сводится, в основном, к различному рассмотрению структуры слоя противоионов
Теории ДЭС • теория Гельмгольца-Перрена (1879); • теория Гуи-Чепмена (1910 -1913); • теория Штерна (1924). Отличие между этими теориями сводится, в основном, к различному рассмотрению структуры слоя противоионов
 Теория Штерна • 1. ДЭС образован потенциалопределяющими ионами, находящимися на поверхности твердой частицы и эквивалентным количеством противоионов, находящихся в дисперсионной среде вблизи поверхности твердой частицы. • 2. Потенциалопределяющие ионы прочно связаны с твердой частицей хемосорбционными силами и равномерно распределены по ее поверхности. • 3. Дисперсионная среда рассматривается как непрерывная бесструктурная среда, характеризуемая диэлектрической проницаемостью ε и вязкостью μ.
Теория Штерна • 1. ДЭС образован потенциалопределяющими ионами, находящимися на поверхности твердой частицы и эквивалентным количеством противоионов, находящихся в дисперсионной среде вблизи поверхности твердой частицы. • 2. Потенциалопределяющие ионы прочно связаны с твердой частицей хемосорбционными силами и равномерно распределены по ее поверхности. • 3. Дисперсионная среда рассматривается как непрерывная бесструктурная среда, характеризуемая диэлектрической проницаемостью ε и вязкостью μ.
 ДЭС 4. ДЭС рассматривается как плоско-параллельный. 5. Слой противоионов, компенсирующих заряд твердой поверхности, имеет сложное строение и состоит из двух частей: плотного слоя (адсорбционного слоя или слоя Гельмгольца) и диффузного слоя (слоя Гуи).
ДЭС 4. ДЭС рассматривается как плоско-параллельный. 5. Слой противоионов, компенсирующих заряд твердой поверхности, имеет сложное строение и состоит из двух частей: плотного слоя (адсорбционного слоя или слоя Гельмгольца) и диффузного слоя (слоя Гуи).
 ДЭС Адсорбционный слой противоионов примыкает к заряженной поверхности твердой частицы и имеет толщину порядка радиуса сольватированного противоиона d. • 6.
ДЭС Адсорбционный слой противоионов примыкает к заряженной поверхности твердой частицы и имеет толщину порядка радиуса сольватированного противоиона d. • 6.
 ДЭС • Противоионы, которые находятся в этом пространстве, называются адсорбционными противоионами. Они связаны с заряженной твердой частицей двумя видами сил – адсорбционными и электростатическими. Эта связь является настолько прочной, что противоионы адсорбционного слоя перемещаются вместе с твердой частицей и не отрываются от нее, образуя с ней единое кинетическое целое – коллоидную частицу
ДЭС • Противоионы, которые находятся в этом пространстве, называются адсорбционными противоионами. Они связаны с заряженной твердой частицей двумя видами сил – адсорбционными и электростатическими. Эта связь является настолько прочной, что противоионы адсорбционного слоя перемещаются вместе с твердой частицей и не отрываются от нее, образуя с ней единое кинетическое целое – коллоидную частицу
 ДЭС • 7. Диффузный слой имеет толщину δ, его образуют те противоионы, которые находятся за пределами адсорбционного слоя. Эти противоионы притягиваются к частице только электростатическими силами, следовательно, они связаны с частицей менее прочно, чем противоионы адсорбционного слоя. При движении дисперсной частицы они от нее отрываются.
ДЭС • 7. Диффузный слой имеет толщину δ, его образуют те противоионы, которые находятся за пределами адсорбционного слоя. Эти противоионы притягиваются к частице только электростатическими силами, следовательно, они связаны с частицей менее прочно, чем противоионы адсорбционного слоя. При движении дисперсной частицы они от нее отрываются.
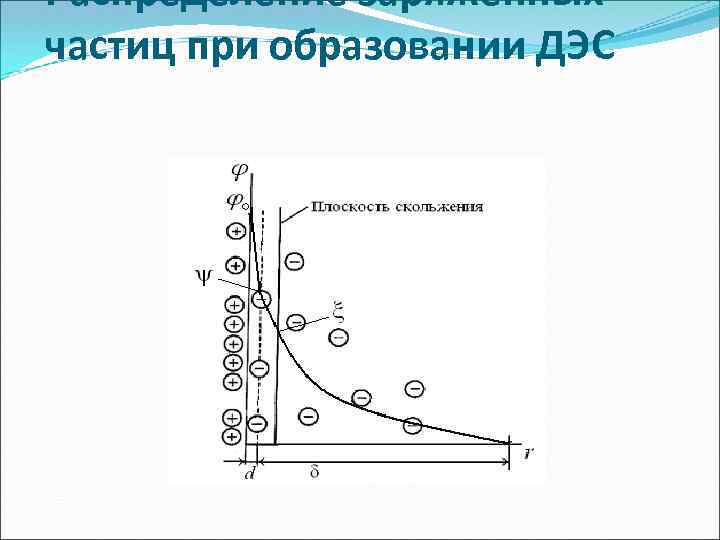 Распределение заряженных частиц при образовании ДЭС
Распределение заряженных частиц при образовании ДЭС
 ПРИМЕР • Коллоидный раствор получен в результате реакции обмена при смешивании равных объемов раствора 0, 0005 н Ag. NO 3 и раствора KJ 0, 0001 н. • Известно, что вещества взаимодействуют между собой в эквивалентных количествах: 0, 0005 н 0, 0001 н Ag. NO 3 + KJ = Ag. J + KNO 3
ПРИМЕР • Коллоидный раствор получен в результате реакции обмена при смешивании равных объемов раствора 0, 0005 н Ag. NO 3 и раствора KJ 0, 0001 н. • Известно, что вещества взаимодействуют между собой в эквивалентных количествах: 0, 0005 н 0, 0001 н Ag. NO 3 + KJ = Ag. J + KNO 3
 Мицелла в избытке (0, 0004 н) остается нитрат серебра. Обычно вещества, взятые в избытке, стабилизаторами, в являются данном случае им будет Ag. NO 3.
Мицелла в избытке (0, 0004 н) остается нитрат серебра. Обычно вещества, взятые в избытке, стабилизаторами, в являются данном случае им будет Ag. NO 3.
 Мицелла в результате реакции образуются молекулы (0, 0001 н) иодида серебра, которые, конденсируясь, образуют ядро мицеллы [m Ag. J]
Мицелла в результате реакции образуются молекулы (0, 0001 н) иодида серебра, которые, конденсируясь, образуют ядро мицеллы [m Ag. J]
 Мицелла • По правилу Панета-Фаянса на любой твердой поверхности адсорбируются родственные ионы. • Адсорбция носит избирательный характер. • Ионы серебра Ag+. Эти ионы плотно прилегают к ядру и называются потенциалопределяющими. (m. Ag. J)n. Ag+. • Частица приобретает положительный заряд.
Мицелла • По правилу Панета-Фаянса на любой твердой поверхности адсорбируются родственные ионы. • Адсорбция носит избирательный характер. • Ионы серебра Ag+. Эти ионы плотно прилегают к ядру и называются потенциалопределяющими. (m. Ag. J)n. Ag+. • Частица приобретает положительный заряд.
 Правило Панета-Фаянса • В кристалле всегда имеются дефекты: в узлах кристаллической решетки могут отсутствовать некоторые ионы. Это приводит к нарушению электронейтральности. • Адсорбироваться будут ионы из раствора, которые образуют с ионами кристаллической решетки труднорастворимые соли. Будут таким образом, действовать силы электростатического притяжения и химического сродства.
Правило Панета-Фаянса • В кристалле всегда имеются дефекты: в узлах кристаллической решетки могут отсутствовать некоторые ионы. Это приводит к нарушению электронейтральности. • Адсорбироваться будут ионы из раствора, которые образуют с ионами кристаллической решетки труднорастворимые соли. Будут таким образом, действовать силы электростатического притяжения и химического сродства.
 Правило Панета-Фаянса На поверхности твердого тела адсорбируются ионы, способные достраивать кристаллическую решетку. Это ионы, которые входят в состав кристаллической решетки твердого тела или изоморфны им. Cl¯, Br¯, CNS¯
Правило Панета-Фаянса На поверхности твердого тела адсорбируются ионы, способные достраивать кристаллическую решетку. Это ионы, которые входят в состав кристаллической решетки твердого тела или изоморфны им. Cl¯, Br¯, CNS¯
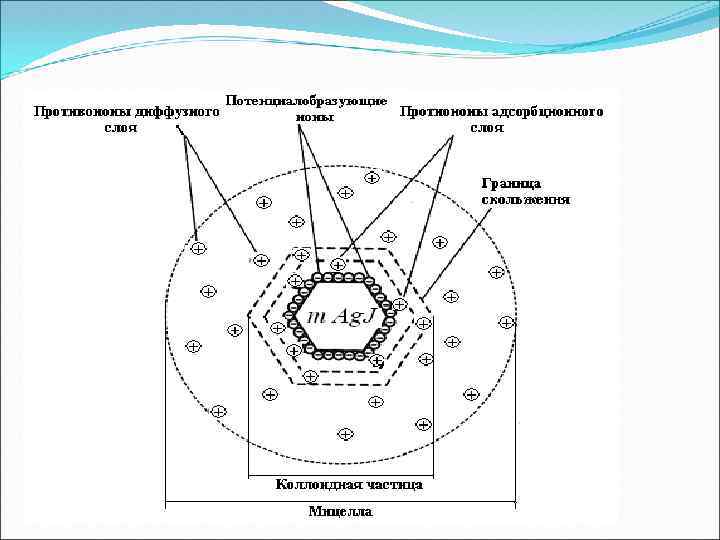 Строение мицеллы
Строение мицеллы
 Мицелла
Мицелла
 Другой механизм возникновения ДЭС Диссоциация электролита. Al(OH)₃ =Al. OH+H⁺→Al³⁺+H₂O Поверхность заряжается положительно =Al. OH+OH¯→Al-O‾+H₂O Поверхность заряжается отрицательно
Другой механизм возникновения ДЭС Диссоциация электролита. Al(OH)₃ =Al. OH+H⁺→Al³⁺+H₂O Поверхность заряжается положительно =Al. OH+OH¯→Al-O‾+H₂O Поверхность заряжается отрицательно
 УСТОЙЧИВОСТЬ КОЛЛОИДНЫХ РАСТВОРОВ Коллоидные растворы неустойчивые образования из-за большой величины свободной поверхностной энергии. Различают кинетическую и агрегативную неустойчивость. Агрегативная неустойчивость проявляется в коагуляции, слипании частиц с последующим оседанием.
УСТОЙЧИВОСТЬ КОЛЛОИДНЫХ РАСТВОРОВ Коллоидные растворы неустойчивые образования из-за большой величины свободной поверхностной энергии. Различают кинетическую и агрегативную неустойчивость. Агрегативная неустойчивость проявляется в коагуляции, слипании частиц с последующим оседанием.
 Действие электролитов на коагуляцию коллоидных растворов Все электролиты способны разрушать коллоидные растворы при определенных концентрациях. Минимальная концентрация электролита, вызывающая коагуляцию, называется порогом коагуляции. Коагулирующим является ион, по знаку противоположный заряду частицы.
Действие электролитов на коагуляцию коллоидных растворов Все электролиты способны разрушать коллоидные растворы при определенных концентрациях. Минимальная концентрация электролита, вызывающая коагуляцию, называется порогом коагуляции. Коагулирующим является ион, по знаку противоположный заряду частицы.
 Порог коагуляции
Порог коагуляции
 Причина коагуляции При добавлении к золю электролитов происходит сжатие двойного электрического слоя, понижается электрокинетический потенциал: золь теряет свою устойчивость и наступает коагуляция.
Причина коагуляции При добавлении к золю электролитов происходит сжатие двойного электрического слоя, понижается электрокинетический потенциал: золь теряет свою устойчивость и наступает коагуляция.


