 Положение металлов в ПС, строение их атомов и кристаллов. Общие физические свойства металлов
Положение металлов в ПС, строение их атомов и кристаллов. Общие физические свойства металлов
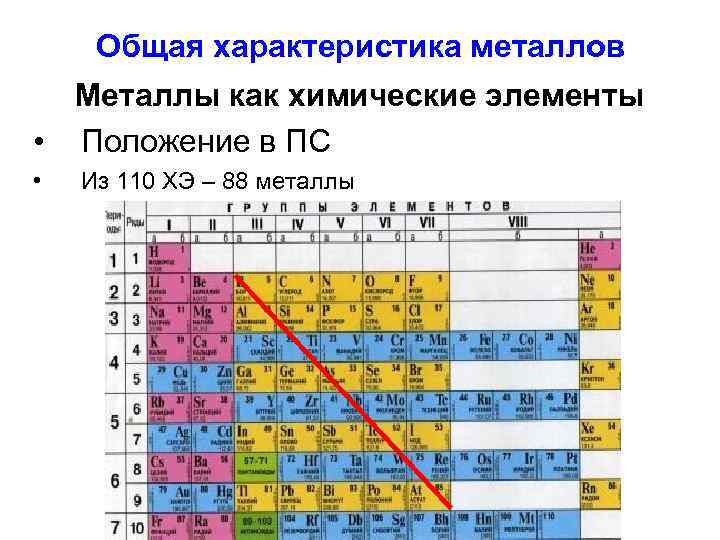 Общая характеристика металлов Металлы как химические элементы • Положение в ПС • Из 110 ХЭ – 88 металлы
Общая характеристика металлов Металлы как химические элементы • Положение в ПС • Из 110 ХЭ – 88 металлы
 • I , III группы (исключая H и B) • все ХЭ побочных подгрупп • многие ХЭ главных подгрупп: IV группа – Ge, Sn, Pb Их соединения V группа – Sb, Bi амфотерны VI группа – Po
• I , III группы (исключая H и B) • все ХЭ побочных подгрупп • многие ХЭ главных подгрупп: IV группа – Ge, Sn, Pb Их соединения V группа – Sb, Bi амфотерны VI группа – Po
 2. Строение атомов металлов • Малое число е- на внешнем энергетическом уровне : 1 – 2 е- у большинства металлов 3 е- - главная п/группа, 3 группа Запишите электронные формулы атомов Na, Ca, Al Na – 1 s 22 p 63 s 1 Ca – 1 s 22 p 63 s 23 p 64 s 2 Al – 1 s 22 p 63 s 23 p 1
2. Строение атомов металлов • Малое число е- на внешнем энергетическом уровне : 1 – 2 е- у большинства металлов 3 е- - главная п/группа, 3 группа Запишите электронные формулы атомов Na, Ca, Al Na – 1 s 22 p 63 s 1 Ca – 1 s 22 p 63 s 23 p 64 s 2 Al – 1 s 22 p 63 s 23 p 1
 • Есть свободные орбитали • Большой радиус атомов: R(Me) >> R(Неме)
• Есть свободные орбитали • Большой радиус атомов: R(Me) >> R(Неме)
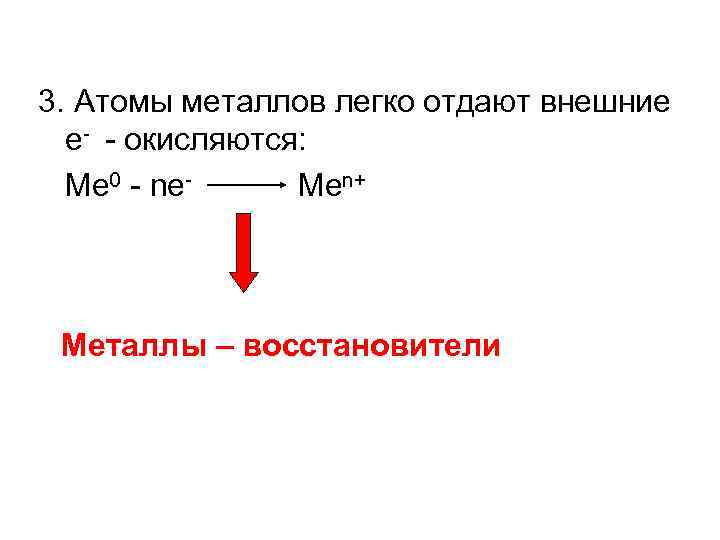 3. Атомы металлов легко отдают внешние е- - окисляются: Ме 0 - nе. Меn+ Металлы – восстановители
3. Атомы металлов легко отдают внешние е- - окисляются: Ме 0 - nе. Меn+ Металлы – восстановители
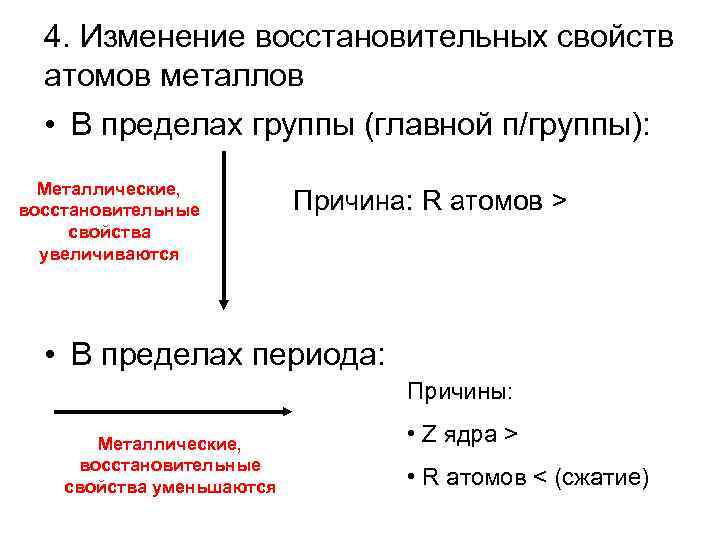 4. Изменение восстановительных свойств атомов металлов • В пределах группы (главной п/группы): Металлические, восстановительные свойства увеличиваются Причина: R атомов > • В пределах периода: Причины: Металлические, восстановительные свойства уменьшаются • Z ядра > • R атомов < (сжатие)
4. Изменение восстановительных свойств атомов металлов • В пределах группы (главной п/группы): Металлические, восстановительные свойства увеличиваются Причина: R атомов > • В пределах периода: Причины: Металлические, восстановительные свойства уменьшаются • Z ядра > • R атомов < (сжатие)