Лекция Структура белковой молекулы.ppt
- Количество слайдов: 44



Полипептидная теория строения белковой молекулы впервые предложена Э. Фишером на базе выдвинутых А. Я. Данилевским идей о роли – СО – NH – связей в строении белка. Согласно полипептидной теории белковые молекулы представляют собой гигантские полипептиды, построенные из многих десятков либо сотен остатков аминокислот.

Доказательства полиептидной теории 1. В нативных белках удается обнаружить очень небольшое число свободных аминных и карбоксильных групп 2. При гидролизе белков идет постепенное освобождение аминных и карбоксильных групп в строгом соотношении 1: 1 3. Биурет (H 2 N – CO – NH 2) и все белки дают биуретовую реакцию, что говорит о наличии в белковой молекуле пептидных связей 4. Полипептидная природа ряда белков – инсулина, рибонуклеазы и др. , - подтверждена химическим синтезом этих белков 5. При рентгеноструктурном анализе строения белков, проводимом при разрешении в 1, 4 -2, 0 Å, удается наблюдать непрерывную полипептидную цепь с характерным для исследуемого белка расположением аминокислотных остатков в ней
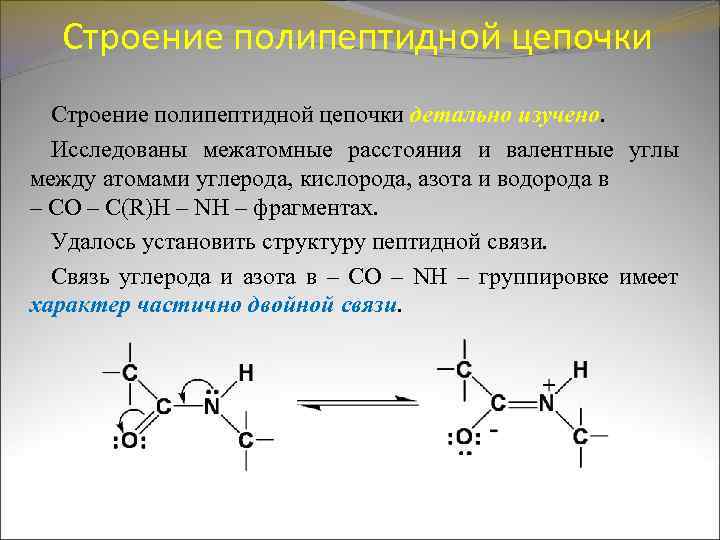
Строение полипептидной цепочки детально изучено. Исследованы межатомные расстояния и валентные углы между атомами углерода, кислорода, азота и водорода в – СО – С(R)Н – NH – фрагментах. Удалось установить структуру пептидной связи. Связь углерода и азота в – СО – NH – группировке имеет характер частично двойной связи.

В результате сопряжения пептидная связь имеет плоскую конфигурацию: • все четыре атома (C, N, O, H) лежат в одной плоскости и вращение относительно плоскости пептидной связи ограничено • кислород – С = О группы и водород – NHгруппировки располагаются в транс-положении относительно связи –C–N Хребет полипептидной цепи составлен из ряда жестких плоскостей, чередующихся с группировками = CHR.
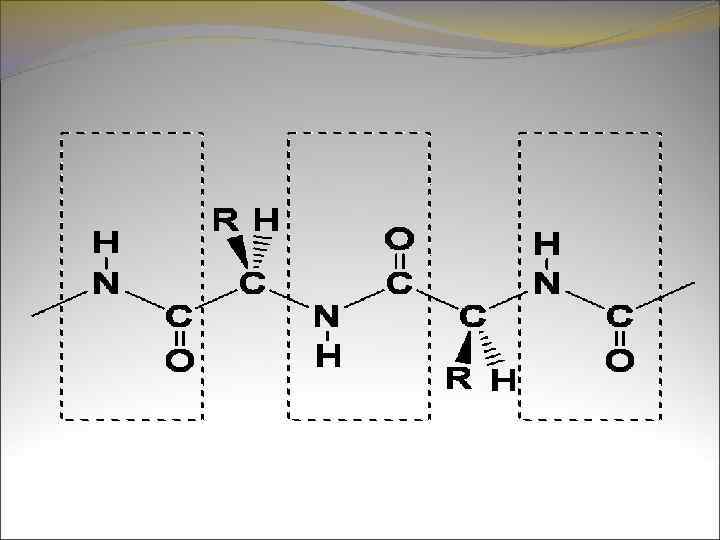

Главная, монотонно построенная из – NH – CO – фрагментов цепь (хребет) окружена разнообразными по своей химической природе боковыми цепями радикалов. Характер радикалов оказывает большое влияние на пространственную конфигурацию полипептидной цепи, определяет круг химических реакций, свойственных белковым телам, и оказывает наряду с другими факторами существенное влияние на функциональную активность белков.


Под первичной структурой белка понимают последовательность в расположении аминокислотных остатков в одной или нескольких полипептидных цепях, составляющих молекулу белка.

Схема определения первичной структуры белка

Расшифровку первичной структуры белка начинают с определения числа полипептидных цепей в молекуле путем определения числа N– и С– концевых аминокислот в молекуле белка. Для определения аминокислотного остатка, которым начинается белковая молекула (N– концевой остаток со свободной α-аминогруппой) пользуются методом Сенджера. Раствор белка обрабатывают динитрофторбензолом, который, взаимодействуя со свободной аминогруппой, образует динитрофенильное производное (ДНФ-производное) белка:
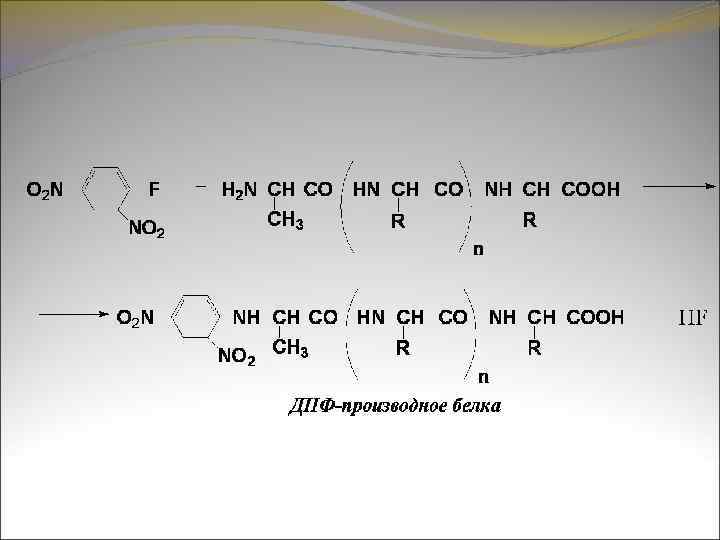

После гидролиза лишь одна аминокислота распавшаяся до свободных аминокислот белковой молекулы будет находится в гидролизате в виде ДНФ-аминокислоты:

Ферментативный метод Состоит в обработке препарата ферментами – амино- или карбоксипептидазой.

После определения числа полипептидных цепей приступают к изучению первичной структуры индивидуальных полипептидных цепей. Используют метод частичного (неполного) гидролиза белка. Гидролизуется лишь некоторое число строго определенных пептидных связей. Трипсин: R 1 – аргинин, лизин; Химотрипсин: R 1 – фенилаланин, тирозин, триптофан; Пепсин: R 2 – фенилаланин, тирозин, триптофан, аспарагиновая кислота, глутаминовая кислота, лейцин

Полипептидная цепь распадается на ряд пептидов, каждый из которых составлен всего из нескольких аминокислотных остатков. Пептиды отделяют друг от друга и в каждом из них определяют последовательность аминокислот физическими, химическими и ферментативными методами.

Физические методы Среди физических методов определения последовательности расположения аминокислотных остатков в белковой молекуле большое значение приобретает сейчас метод рентгеноструктурного анализа. Он позволяет различить ( «увидеть» ) отдельные аминокислотные остатки в молекуле белка. Этим способом удается идентифицировать последовательно примерно 70 % аминокислотных остатков в белковой молекуле.

На основании данных о порядке чередования аминокислот в отдельных пептидах воссоздают первичную структуру полипептидной цепи белка, т. е. определяют его первичную структуру.

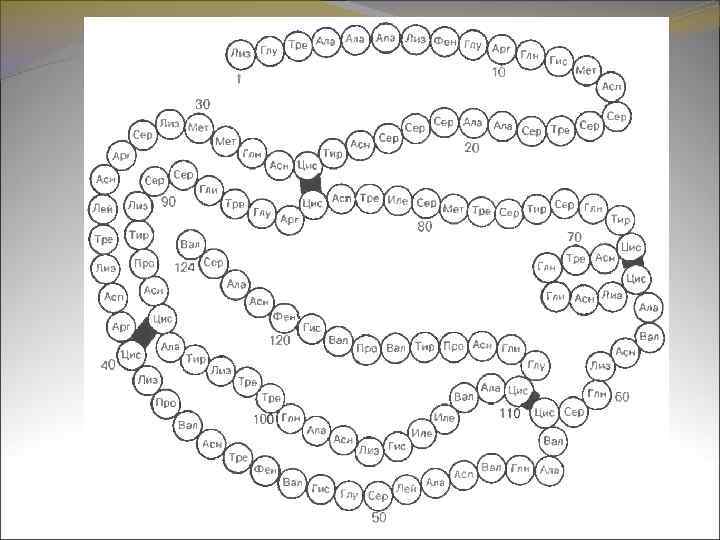
В настоящее время число белков с изученной первичной структурой приближается к двум тысячам. Примером белка с изученной первичной структурой является рибонуклеаза. Это фермент, ускоряющий реакцию распада фосфодиэфирных связей в молекулах рибонуклеиновой кислоты. При молекулярной массе в 13700 рибонуклеаза содержит 124 аминокислотных остатка.
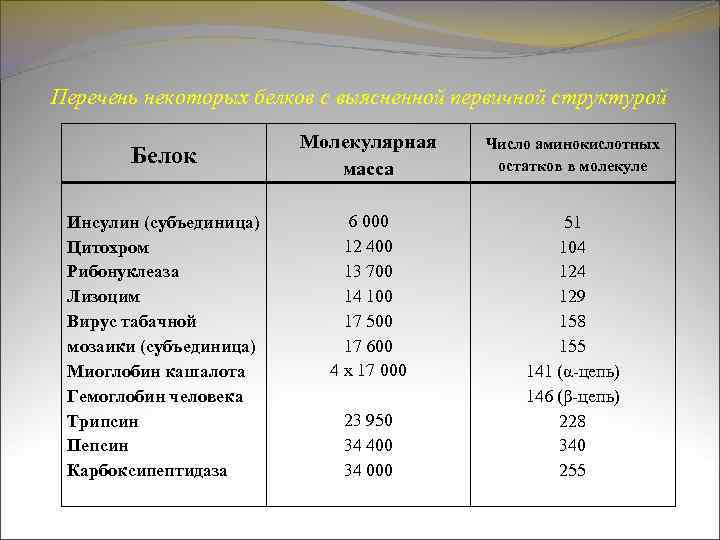
Перечень некоторых белков с выясненной первичной структурой Белок Инсулин (субъединица) Цитохром Рибонуклеаза Лизоцим Вирус табачной мозаики (субъединица) Миоглобин кашалота Гемоглобин человека Трипсин Пепсин Карбоксипептидаза Молекулярная масса Число аминокислотных остатков в молекуле 6 000 12 400 13 700 14 100 17 500 17 600 4 х 17 000 51 104 129 158 155 141 (α-цепь) 146 (β-цепь) 228 340 255 23 950 34 400 34 000

В некоторых случаях молекулы простейших белков построены из двух и более полипептидных цепей, соединенных друг с другом ковалентными связями. Примером такого рода может служить молекула инсулина. Она составлена из 51 аминокислотных остатков, соединенных в две полипептидные цепи (А и Б), которые в свою очередь связаны друг с другом двумя дисульфидными мостиками.
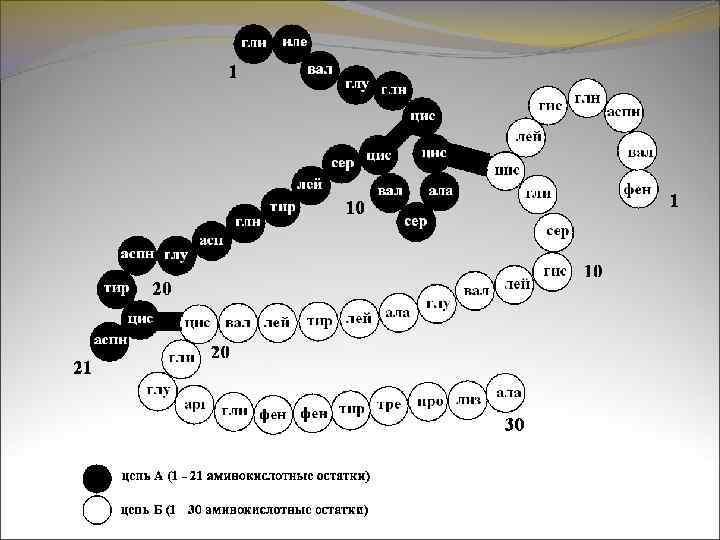

Расшифровка первичной структуры ряда белков является большим успехом в белковой химии. Благодаря этому белки теперь предстают перед нами как вещества со строго определенной химической формулой и строением.


Данные рентгеноструктурного анализа ряда белков указали на наличие в полипептидных цепях регулярно свернутых и закономерно закрученных участков. Удалось установить, что полипептидная цепь в молекулах подавляющего числа белков свернута в виде спирали. Считают, что наиболее вероятным типом спирали является так называемая α-спираль.
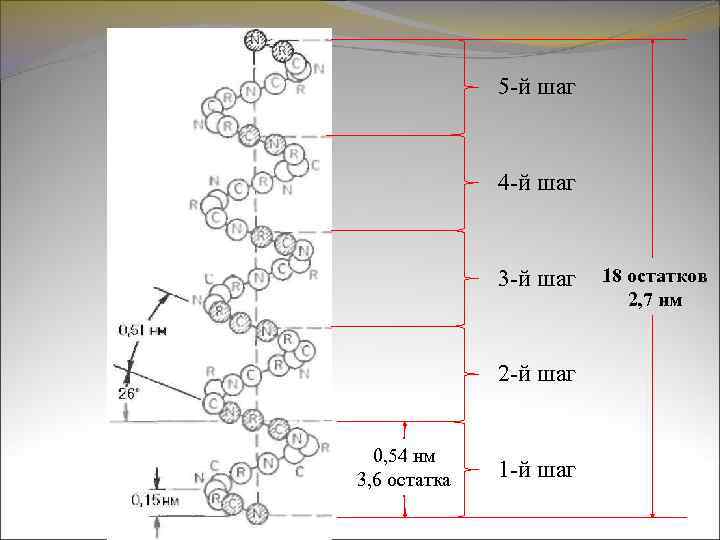
5 -й шаг 4 -й шаг 3 -й шаг 2 -й шаг 0, 54 нм 3, 6 остатка 1 -й шаг 18 остатков 2, 7 нм

α-спираль характеризуется предельно плотной упаковкой скрученной полипептидной цепи. На каждый виток правозакрученной αспирали приходится 3, 6 аминокислотных остатка. Шаг спирали (расстояние между витками) составляет 5, 4 Å, а угол подъема витка равен 26 О. Период идентичности составляет 27 Å (18 аминокислотных остатков).

Под вторичной структурой белковой молекулы подразумевают ту или иную конфигурацию, характерную для одной или нескольких полипептидных цепей, входящих в состав молекулы. Спирализованные участки полипептидной цепи закономерно чередуются с неспирализованными.


Под третичной структурой белковой молекулы понимают общее расположение в пространстве составляющих молекулу одной или нескольких полипептидных цепей. В настоящее время установлена третичная структура более ста белков. Первая модель молекулы белка – миоглобина, отражающая его третичную структуру, была создана Кендрю с сотрудниками в 1957 г.
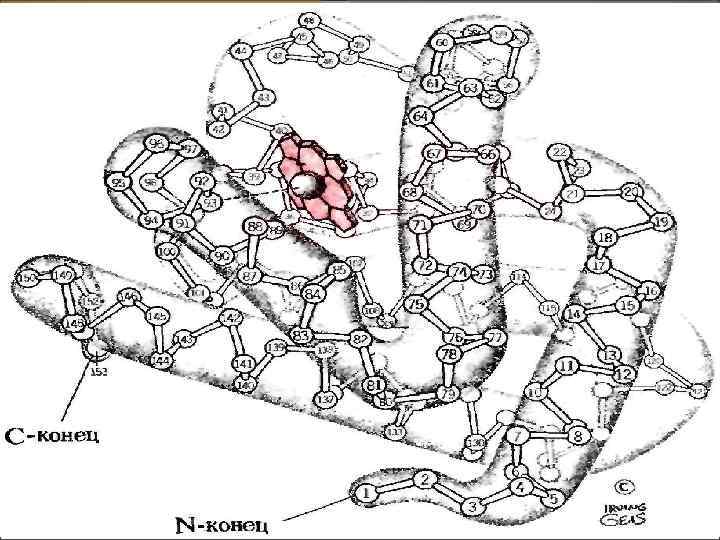

Третичная структура белковой молекулы определяется ее первичной структурой. Поддержание характерного для третичной структуры расположения полипептидной цепи в пространстве принадлежит взаимодействию радикалов аминокислот друг с другом. Наибольший вклад в поддержание третичной структуры белка принадлежит силам слабого взаимодействия: 1. Гидрофобным, возникающим при сближении в пространстве неполярных радикалов (фенилаланина, изолейцина и др. ) 2. Водородным, в образовании которых участвуют радикалы-доноры протонов (тирозин, серин и др. ) и радикалы-акцепторы протонов (глутаминовая, аспарагиновая кислоты и др. ).
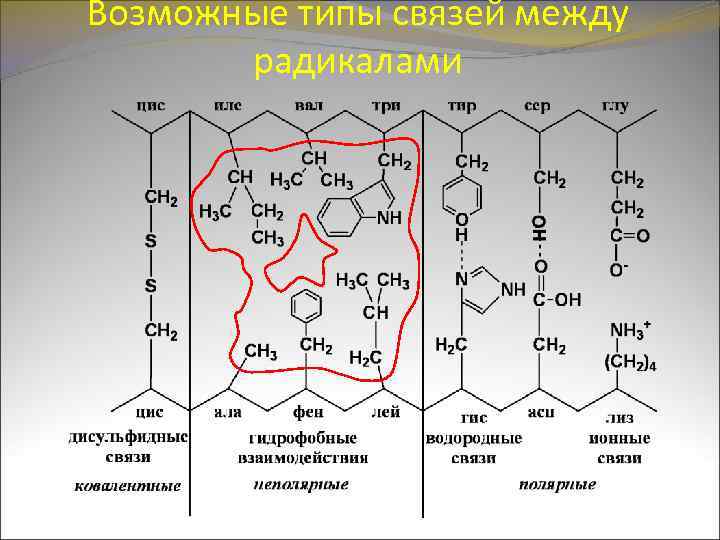
Возможные типы связей между радикалами

Третичная структура белковой молекулы возникает автоматически. Движущей силой является взаимодействие аминокислотных радикалов с молекулами воды. При этом гидрофобные радикалы вталкиваются внутрь белковой молекулы, а гидрофильные ориентируются в сторону растворителя – воды. Биологическая активность белков зависит от сохранения присущей им в нативном состоянии третичной структуры молекулы.


Многие белки имеют субъединичное строение. Взаимное пространственное расположение субъединиц в единой белковой молекуле называют четвертичной структурой белка. В настоящее время изучена четвертичная структура нескольких сотен белков.

Гемоглобин Молекула гемоглобина (М = 68 000) построена из четырех субъединиц с молекулярной массой в 17 000 каждая. Субъединицы попарно идентичны и были названы субъединицами типа α и β. Субъединица типа α составлена из 141 аминокислотного остатка, β – из 146. Четыре субъединицы (2 α и 2 β) соединяются в единую молекулу гемоглобина. Возникает почти шаровидная молекула с параметрами 50 х 55 х 64 Å.
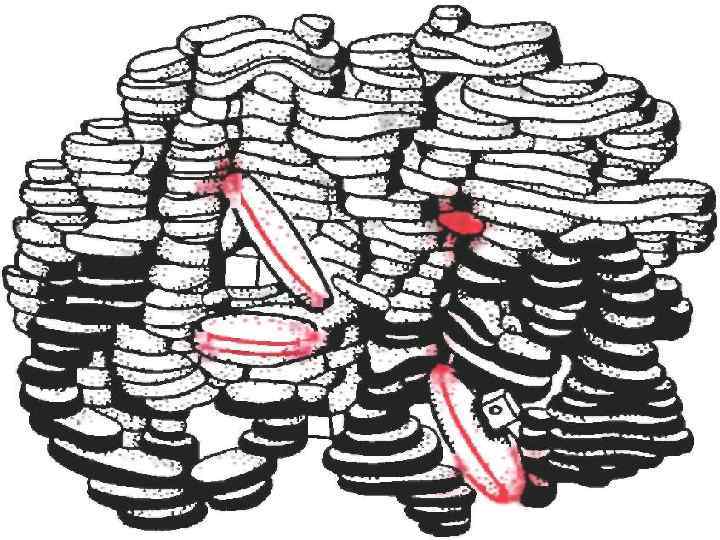

Вирус табачной мозаики Гигантская молекула (М = 40 000) содержит небольшое количество (около 6%) рибонуклеиновой кислоты, остальное белок. Белковая часть складывается из 2130 субъединиц с молекулярной массой 17 500 каждая. Молекула представляет собой полую палочку длиной около 3000 Å, толщиной примерно 170 Å, в центре отверстие диаметром в 40 Å. Каждая субъединица имеет размеры 20 х 70 Å. Субъединицы расположены по спирали. Шаг витка – 16 субъединиц. Молекула нуклеиновой кислоты проходит между рядами субъединиц.


Белковые молекулы, составленные из субъединиц, принято называть мультимерами, а сами субъединицы – протомерами. Наиболее часто в составе мультимера насчитывается 2 или 4 субъединицы. Объединение протомеров в молекулу мультимера осуществляется самопроизвольно. Предполагают, что в молекуле каждого протомера есть специфические участки (контактные площадки). Поддержание четвертичной структуры белков обеспечивают – ковалентные, ионные и силы слабых взаимодействий. Наибольший вклад вносят силы слабых взаимодействий (гидрофобные взаимодействия и водородные связи).

Незначительное изменение первичной структуры белка или стандартных условий в клетке приводит к изменению функциональной активности белков.
Лекция Структура белковой молекулы.ppt