Полимеры как кровезаменители.ppt
- Количество слайдов: 38

Полимеры как кровезаменители. Биоразлагаемая электроника. Подготовил Вишневский Дмитрий
Крове- и плазмозаменители Введенные в кровяное русло кровезамещающие жидкости (водные растворы высокомолекулярных веществ) должны временно выполнять роль крови как своеобразного «жидкого органа» .

Отсюда вытекают особые требования к полимерамкровезаменителям: − длительно удерживаться в кровяном русле, для чего молярная масса полимера должна быть достаточно высокой; − полностью выводиться из организма или вступать в обмен веществ; − обладать постоянными физико-химическими свойствами ( осмотическим давлением, вязкостью и др. ), близкими по значению соответствующим показателям плазмы крови; − не вызывать гемолиза (распада) или агглютинации (склеивания) эритроцитов; − не быть анафилактогенными; − не вызывать сенсибилизации организма при повторном введении; − быть нетоксичными, непирогенными; − легко стерилизоваться и выдерживать достаточно длительные сроки хранения.

Основные функции кровезаменителей: − заполнение кровяного русла, обеспечивающее поддержание постоянного давления в нем; − удаление из организма токсичных веществ различного происхождения; − перенос энергетически питательных веществ. Кровезаменители по выполняемым ими лечебным функциям делят на три главные группы: 1) противошоковые; 2) дезинтоксикационные; 3) препараты парентерального питания.
Соответственно различаются и некоторые требования к полимерным веществам. В качестве препаратов противошокового действия можно использовать полимеры с достаточно высокой молекулярной массой (оптимально 30000 - 60000), что обеспечивает длительное пребывание полимера в организме для восстановления гемодинамики. Дезинтоксикаторы эффективны при сравнительно низкой молекулярной массе (10000— 20000), т. к. они должны быстро выводиться из организма, унося токсичные вещества. Для препаратов третьей группы этот показатель не регламентируется, т. к. они в организме расщепляются и ассимилируются (усваиваются).

Кровезаменители противошокового действия. Наиболее широко используют для получения таких кровезаменителей плазму нативной крови, декстран, поливинилпирролидон и желатину. Из них готовятся следующие препараты: полиглюкин – 6 % - ный солевой раствор продукта частичного гидролиза соляной кислотой нативного декстрана, синтезируемого определенным штаммом бактерии ( наиболее эффективна фракция с молекулярной массой 55000 ± 15000); гемовинил - 3, 5 % - ный солевой раствор фракции поливинилпирролидона с молекулярной массой 30000 - 40000; желатиноль – 8 % - ный раствор частично гидролизованной желатины, в его состав входят различные полипептиды, с молекулярной массой от 5000 и выше; раствор БК-8 получают из гетерогенных белков, специально обработанных с целью лишения их антигенных свойств. За рубежом широко применяют препарат гемацел, получаемый путем гидролиза и последующего ресинтеза пептидных цепей желатины(молекулярная масса около 35 000).

Кровезаменители для дезинтоксикации. Дезинтоксикационный эффект, или свойство растворов полимеров выводить из организма токсины бактериального и иного происхождения, обусловливается способностью макромолекул сорбировать или связывать в комплексы вещества различной природы. Наиболее эффективными препаратами являются: гемодез – 6 % - ный раствор низкомолекулярного поливинилпирролидона с молекулярной массой 12000 - 27000 (до 80 % препарата выводится почками в течение первых 4 часов); поливиниловый спирт с молекулярной массой 10000; реополиглюкин - низкомолекулярные фракции гидролизата декстрана с молекулярной массой около 35000. Все кровезаменители готовят на физиологическом растворе с доведением р. Н до 5 - 7. В качестве других компонентов кровезаменителей, приближающих их по свойствам к крови (достижение изотоничности и изоионичности) и обуславливающих дополнительный лечебный эффект, применяют глюкозу, лактат натрия, соли Nа, К, Са, Mg и др.
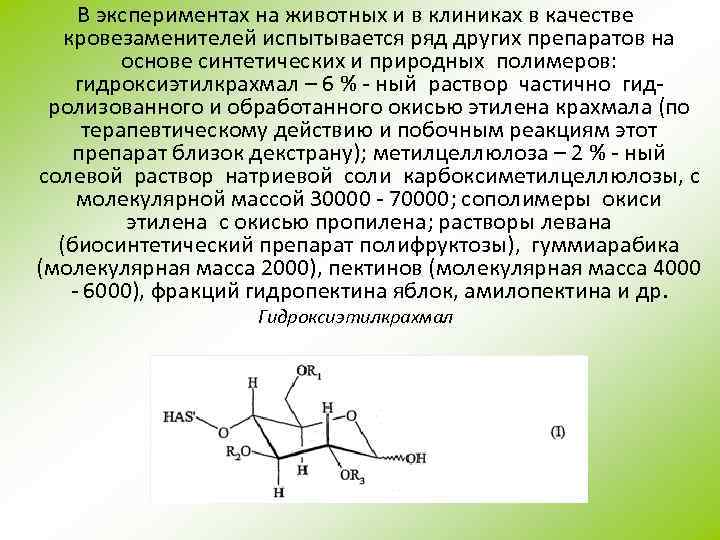
В экспериментах на животных и в клиниках в качестве кровезаменителей испытывается ряд других препаратов на основе синтетических и природных полимеров: гидроксиэтилкрахмал – 6 % - ный раствор частично гидролизованного и обработанного окисью этилена крахмала (по терапевтическому действию и побочным реакциям этот препарат близок декстрану); метилцеллюлоза – 2 % - ный солевой раствор натриевой соли карбоксиметилцеллюлозы, с молекулярной массой 30000 - 70000; сополимеры окиси этилена с окисью пропилена; растворы левана (биосинтетический препарат полифруктозы), гуммиарабика (молекулярная масса 2000), пектинов (молекулярная масса 4000 - 6000), фракций гидропектина яблок, амилопектина и др. Гидроксиэтилкрахмал
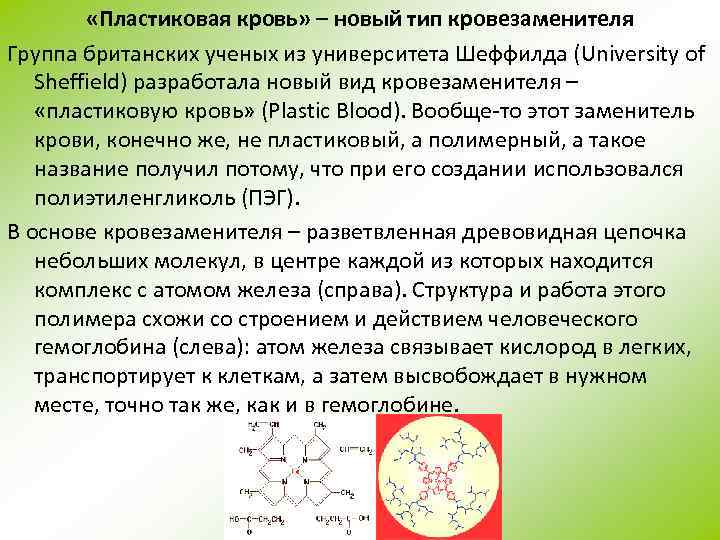
«Пластиковая кровь» – новый тип кровезаменителя Группа британских ученых из университета Шеффилда (University of Sheffield) разработала новый вид кровезаменителя – «пластиковую кровь» (Plastic Blood). Вообще-то этот заменитель крови, конечно же, не пластиковый, а полимерный, а такое название получил потому, что при его создании использовался полиэтиленгликоль (ПЭГ). В основе кровезаменителя – разветвленная древовидная цепочка небольших молекул, в центре каждой из которых находится комплекс с атомом железа (справа). Структура и работа этого полимера схожи со строением и действием человеческого гемоглобина (слева): атом железа связывает кислород в легких, транспортирует к клеткам, а затем высвобождает в нужном месте, точно так же, как и в гемоглобине.
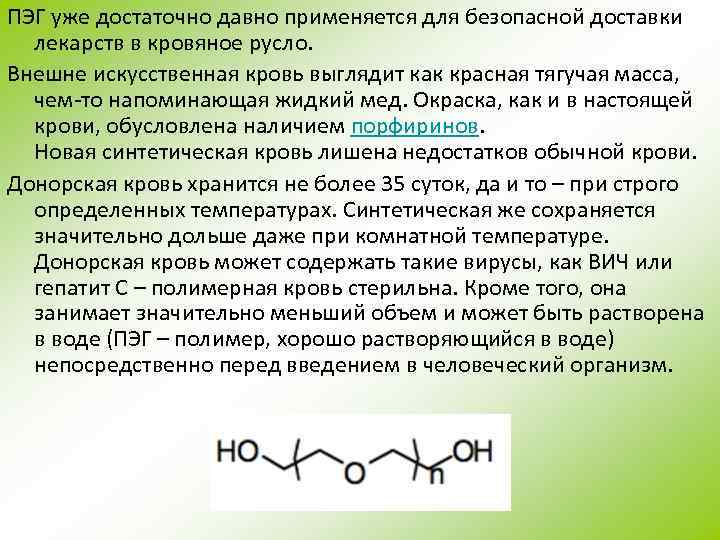
ПЭГ уже достаточно давно применяется для безопасной доставки лекарств в кровяное русло. Внешне искусственная кровь выглядит как красная тягучая масса, чем-то напоминающая жидкий мед. Окраска, как и в настоящей крови, обусловлена наличием порфиринов. Новая синтетическая кровь лишена недостатков обычной крови. Донорская кровь хранится не более 35 суток, да и то – при строго определенных температурах. Синтетическая же сохраняется значительно дольше даже при комнатной температуре. Донорская кровь может содержать такие вирусы, как ВИЧ или гепатит C – полимерная кровь стерильна. Кроме того, она занимает значительно меньший объем и может быть растворена в воде (ПЭГ – полимер, хорошо растворяющийся в воде) непосредственно перед введением в человеческий организм.
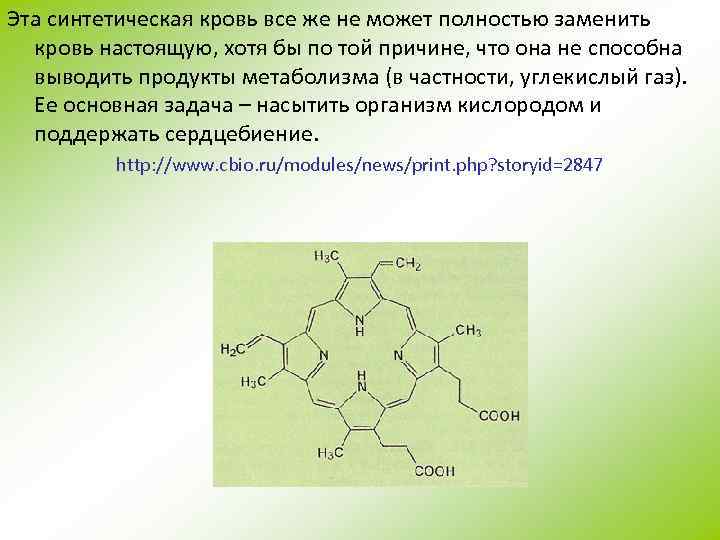
Эта синтетическая кровь все же не может полностью заменить кровь настоящую, хотя бы по той причине, что она не способна выводить продукты метаболизма (в частности, углекислый газ). Ее основная задача – насытить организм кислородом и поддержать сердцебиение. http: //www. cbio. ru/modules/news/print. php? storyid=2847

Искусственные клетки крови из полимеров Группа специалистов из Калифорнийского университета разработала красные кровяные тельца из полимеров, удивительно близкие к реальным. Их двояковыгнутый "шинообразный" вид объясняется формой, которую реальные эритроциты принимают в человеческом теле. Не так давно красные кровяные тельца были впервые выращены в лаборатории. Теперь же появился и их искусственный вариант. Синтетические эритроциты успешно имитируют характеристики и основные функции настоящих клеток, в том числе мягкость, гибкость и способность переносить кислород. http: //www. cpvis. ru/newspapir/ntnews/224 -nt 0009. html

В пресс-релизе университета учёные сообщают, что синтетические красные кровяные тельца (s. RBCs) отлично справляются с "перевозкой" веществ по всему организму, что было доказано экспериментально, с прикреплением молекулы гемоглобина к поверхности полимерной клетки и последующим наблюдением. s. RBC-клетки могут использоваться в будущем для доставки лекарственных препаратов и переливания людям вместо настоящей крови в случае необходимости - но перед этим, разумеется, понадобится ещё много дополнительных тестов. Сделать искусственные эритроциты специалистам удалось так: вначале был создан похожий по форме на пончик полимерный шаблон, который покрыли несколькими слоями гемоглобина и других белков, затем сам шаблон удалили, осталась белковая оболочка. В результате все искусственные клетки имеют одинаковый размер и гибкость и могут нести столько же кислорода, сколько и настоящие. В опубликованной в PNAS статье авторы высказывают предположение, что их методика может быть также использована для разработки частиц, имитирующих форму и свойства больных клеток, например при серповидно-клеточной анемии.
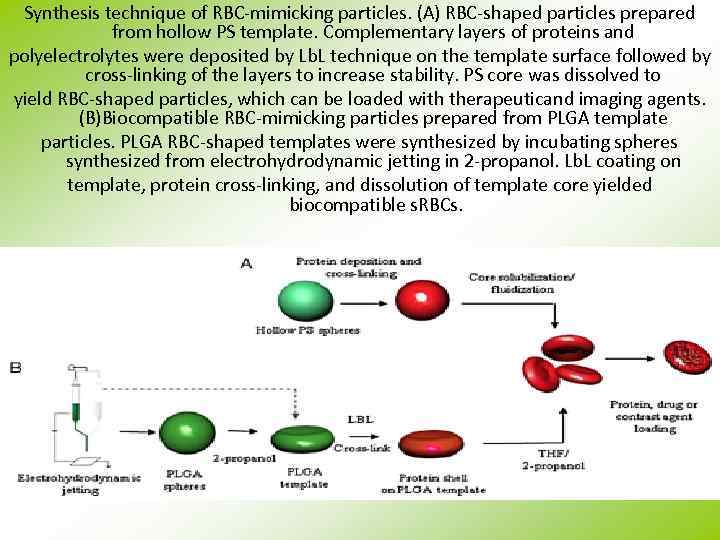
Synthesis technique of RBC-mimicking particles. (A) RBC-shaped particles prepared from hollow PS template. Complementary layers of proteins and polyelectrolytes were deposited by Lb. L technique on the template surface followed by cross-linking of the layers to increase stability. PS core was dissolved to yield RBC-shaped particles, which can be loaded with therapeuticand imaging agents. (B)Biocompatible RBC-mimicking particles prepared from PLGA template particles. PLGA RBC-shaped templates were synthesized by incubating spheres synthesized from electrohydrodynamic jetting in 2 -propanol. Lb. L coating on template, protein cross-linking, and dissolution of template core yielded biocompatible s. RBCs.

SEM micrographs of RBC-mimicking particles synthesized using hollow PS template particles. (A) BSA/PAH was deposited on template particles by Lb. L technique, and the layers were cross-linked. Particles were exposed to. THF toyield s. RBCs. Inset shows close up. (B) Hb/PSS-based s. RBCs preparedby. Lb. L technique. (C) s. RBCs prepared by adsorption of Hb on template particles. (Scale bars, 1 μm. ) (Inset, 500 nm. )
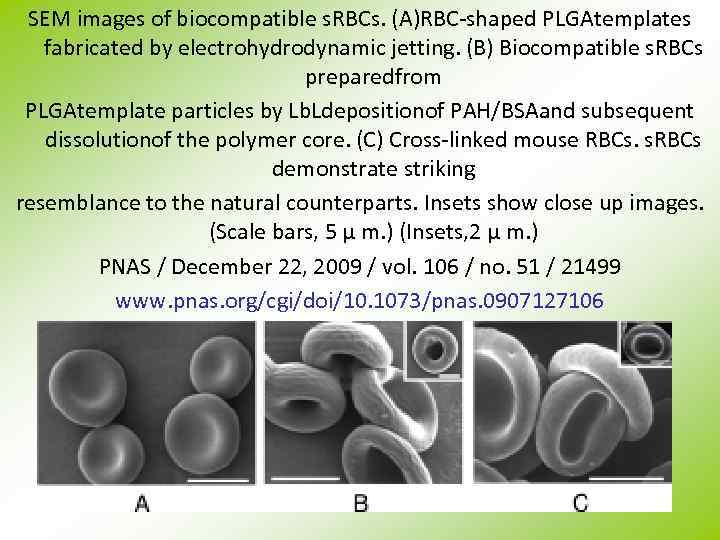
SEM images of biocompatible s. RBCs. (A)RBC-shaped PLGAtemplates fabricated by electrohydrodynamic jetting. (B) Biocompatible s. RBCs preparedfrom PLGAtemplate particles by Lb. Ldepositionof PAH/BSAand subsequent dissolutionof the polymer core. (C) Cross-linked mouse RBCs. s. RBCs demonstrate striking resemblance to the natural counterparts. Insets show close up images. (Scale bars, 5 μ m. ) (Insets, 2 μ m. ) PNAS / December 22, 2009 / vol. 106 / no. 51 / 21499 www. pnas. org/cgi/doi/10. 1073/pnas. 0907127106

Группа исследователей из университета Case Western Reserve в Огайо сообщила о создании синтетических тромбоцитов. Искусственные клетки станут отличными помощникам в ситуациях, когда необходимо предотвратить кровопотерю. Строго говоря, созданные учёными полиэстеровые "сферы" – это не сами тромбоциты, а миниатюрные помощники, аналогичные им по функциям, но уступающие диаметром примерно в десять раз. Сфера несёт молекулу полиэтиленгликоля, своеобразный наконечник, в котором содержатся три основные аминокислоты. Идея здесь заключается в том, что сферы будут придерживаться тромбоцитов и помогать им собираться в сгустки, действуя по принципу катализаторов.

Синтетические "ускорители" потенциально более выгодны для переливания, чем натуральные тромбоциты, полученные из донорской крови, – последние имеют срок годности всего 5 дней и подвержены риску бактериальной инфекции. Как сообщается в статье, опубликованной в Science Translational Medicine, учёные протестировали своё изобретение на крысах. Животным был произведён надрез бедренной артерии. Обычно в таких случаях для остановки кровотечения требуется около 4 минут, однако внутривенная инъекция синтетических тромбоцитов сразу же после надреза сократила этот промежуток времени на 23%. http: //www. zdorovieinfo. ru/exclusive/99253/357458/

Наносервис: доставка лекарства прямо в клетку Исследователи из Принстонского Университета (Princeton University) создали частицы, которые могут доставлять лекарство глубоко в раковые клетки или больные клетки легких и не затрагивать здоровые клетки. Только от 100 до 300 нм шириной — более чем в 100 раз тоньше, чем человеческий волос — частицы могут быть загружены лекарством или меткой, например, золотом или магнетитом, для усиления возможностей компьютерной томографии и магнитного резонанса. Новый метод, названный «Мгновенное наноосаждение» позволяет исследователям смешивать лекарства и материалы, которые инкапсулируют их. Подобные методы смешивания использовались и раньше, чтобы создать новые выгодные фармацевтические продукты. Команда из Принстонского Университета, которая включает профессоров химической технологии Янниса Кеврекидиса (Yannis Kevrekidis) и Атанасиоса Панагитопопулоса (Athanassios Panagiotopoulos), является первой, которая применила данную технологию к созданию наночастиц, частиц размером в несколько миллиардных метра.

Наночастицы являются слишком большими, чтобы пройти через мембрану нормальных клеток, но они легко пройдут через большие дефекты в капиллярах, возникающих при быстром росте опухолей. Успех наноосаждения зависит в значительной степени от факта, что некоторые молекулы являются гидрофобными, в то время как другие — гидрофильными. Гидрофобные вещества, типа масла, плохо смешиваются с водой. Много фармацевтических препаратов, включая современные препараты от рака, являются гидрофобными, что мешает доставлять лекарства через кровь, которая состоит в основном из воды. В методе наноосаждения два потока жидкости направляются друг к другу в ограниченной области. Первый поток состоит из органического растворителя, который содержит лекарства и метки, а так же молекулы полимеров. Цепь полимера походит на ожерелье жемчуга, половина из которого гидрофобна, а другая гидрофильна. Второй поток жидкости содержит чистую воду.

Когда потоки сталкиваются, гидрофобные лекарства, металлические метки и полимеры осаждаются из раствора, так как не растворимы в воде. Полимеры немедленно самособираются вокруг лекарства или метки, образуя покрытие с внешней растянутой гидрофильньной частью и внутренней гидрофобной частью, куда попадает и лекарство. Тщательно регулируя концентрации веществ и скорость смешения, исследователи могут контролировать размер наночастиц. Растянутый гидрофильньный слой полимера препятствует коагуляции частиц и предотвращает распознавание иммунной системой, давая возможность им циркулировать вместе с кровотоком. Гидрофобная внутренняя часть частиц гарантирует, что они не будут разрушены окружающей водой, хотя молекулы воды с течением долгого времени разрушат наночастицы, уничтожая лекарство. Профессор Прадхомм

В лаборатории определено точное время, которое требуется для разрушения наночастиц водой. Ученые сделали частицы еще более стойкими к ранней деградации, добавляя гидрофобные вещества, включая витамин Е, к лекарствам и меткам перед заключением их в частицы. http: //www. nanonewsnet. ru/articles/2007/nanoservis-dostavkalekarstva-pryamo-v-kletku Один из видов доставки лекарствс помощью наночастиц
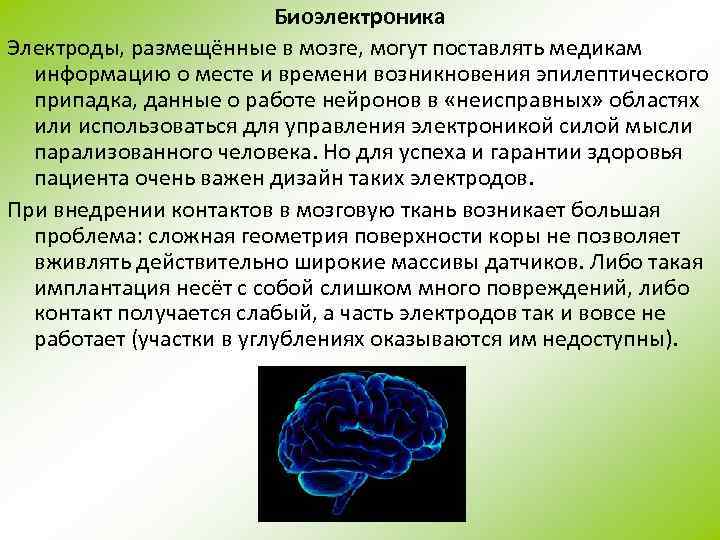
Биоэлектроника Электроды, размещённые в мозге, могут поставлять медикам информацию о месте и времени возникновения эпилептического припадка, данные о работе нейронов в «неисправных» областях или использоваться для управления электроникой силой мысли парализованного человека. Но для успеха и гарантии здоровья пациента очень важен дизайн таких электродов. При внедрении контактов в мозговую ткань возникает большая проблема: сложная геометрия поверхности коры не позволяет вживлять действительно широкие массивы датчиков. Либо такая имплантация несёт с собой слишком много повреждений, либо контакт получается слабый, а часть электродов так и вовсе не работает (участки в углублениях оказываются им недоступны).

Учёным не составляет труда произвести тонкие контакты и проводки, скажем, из золота. При толщине в считанные микрометры они будут достаточно мягкими, чтобы повторять рельеф коры. Но сначала их ведь необходимо как-то пристроить на место работы с высокой точностью, не смяв и не порвав тонкий металл. Такой строительной основой для нового типа имплантата стал субстрат из фиброина натурального шёлка, взятого из кокона шёлкопряда Bombyx mori. Материал этот достаточно упругий и прочный, чтобы устройством можно было манипулировать в ходе хирургической операции, но при этом достаточно мягкий, чтобы снизить риск травмы.

Поверх шёлковой подложки авторы новой технологии разместили тонкую сетку из полиимида (был использован материал каптон — kapton), она служит для электрической изоляции и для формирования правильного рисунка из проводящих дорожек и контактов. При контакте с внутренней средой организма (а также при добавлении физиологического раствора) белок шёлковой основы начал растворяться. Оставшийся свободным ажурный каркас из тонких проводков и контактов, сидящий на полимерной сетке, за счёт действия капиллярных сил начал изгибаться, точно повторяя форму коры мозга в данном месте, словно термоусадочная упаковка. Теперь он плотно прилегал к ней, в то же время не повреждая. kapton

Изготовление имплантата начинается с размещения каптона на обработанной стеклянной пластине (1). Сначала вырезаются дорожки, потом добавляются проводники, полимер снимается со стекла (2) и совмещается с шёлковой основой (3). С одной из сторон решётки, содержащей 30 контактов (4), присоединяется плоский набор проводков (5), идущих к чипу (6), занятому первичной обработкой сигналов (иллюстрации Dae-Hyeong Kim et al. /Nature Materials).

Варьируя предварительную обработку шёлкового материала, исследователи добились регулировки времени рассасывания основы чипа в пределах от нескольких минут до часов. Эта регулировка должна пригодиться при выполнении сложных операций на мозге. Решающей проверкой стала имплантация таких сэндвичей в мозг взрослых кошек. Учёные поместили электроды в зрительную кору животных. Регистрируя ток от нервных клеток при визуальной стимуляции (кошкам показывали различные картинки), экспериментаторы доказали, что тонкая сетка, высаженная на коре при помощи шёлковой основы, даёт самый чёткий и подробный сигнал в сравнении с традиционными толстыми проволочными электродами. Главное преимущество нового имплантата (на снимке он показан на модели мозга) – умение «затекать» в складки и борозды коры, формируя плотный, но при этом не травмирующий живую ткань интерфейс между мозгом и электродами

Важно, что на участке имплантации не наблюдалось никакого воспаления по меньшей мере за все четыре недели опыта. Создание интегрированных систем такого типа требует построения по аналогичному принципу биосовместимых цифровых чипов, а также — источников питания. Был построен опытный образец чипа на шёлке, содержащего кремниевые транзисторы, и проверен на лабораторных животных (правда, ещё не на мозге). Аналогично учёные пробуют создать ультратонкие аккумуляторы, сводящие к минимуму воздействие на живую ткань. http: //www. membrana. ru/particle/1134

Создана разлагаемая в теле человека электроника Биоразлагаемые микросхемы, способные практически бесследно исчезнуть внутри тела пациента после выполнения своей задачи, открывают новую главу в медицинских имплантатах. Действующий прототип продемонстрировала профессор Чжэнань Бао (Zhenan Bao) из Стэнфорда. Исследовательская группа Бао построила первую в мире транзисторную микросхему, полностью составленную из биоразлагаемых и нейтральных для человека материалов. В ней даже для построения логических элементов не используется кремний: вместо него авторы устройства применили безопасные для организма полимеры, биологический полупроводник, схожий с пигментом меланином, и микроскопические порции серебра и золота. Биоразлагаемый микрочип.

Новая микросхема устойчива в воде, однако начинает разлагаться, когда попадает в условия, идентичные внутренностям человеческого тела, а именно – в солевой раствор плюс слабощелочную среду. Полное исчезновение транзисторов и всей схемы в целом происходит за 70 дней. Единственное, что остаётся в теле на месте бывшего электронного имплантата, — несколько невидимых глазу контактов из благородных металлов с поперечником всего в десятки нанометров каждый. По замыслу авторов проекта, прежде чем такая схема растворится внутри тела, она успеет выполнить возложенную на неё миссию. К тому же её можно будет покрыть дополнительным слоем биоразлагаемого материала (авторы изучают несколько вариантов), который обеспечит запрограммированную задержку между имплантацией и началом разложения собственно микросхемы.
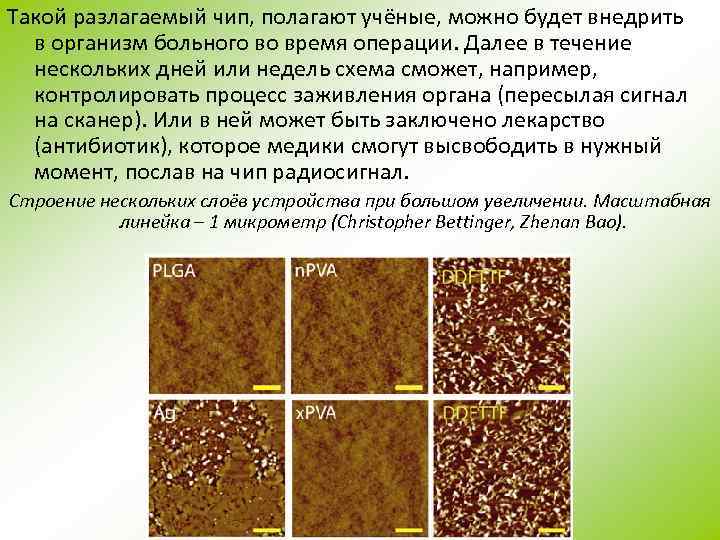
Такой разлагаемый чип, полагают учёные, можно будет внедрить в организм больного во время операции. Далее в течение нескольких дней или недель схема сможет, например, контролировать процесс заживления органа (пересылая сигнал на сканер). Или в ней может быть заключено лекарство (антибиотик), которое медики смогут высвободить в нужный момент, послав на чип радиосигнал. Строение нескольких слоёв устройства при большом увеличении. Масштабная линейка – 1 микрометр (Christopher Bettinger, Zhenan Bao).

Экспериментальный биоразлагаемый чип в исходном виде, а также после 10, 30, 40, 50 и 70 дней пребывания в растворе, идентичном внутренней среде человеческого тела. Масштабная линейка – 5 миллиметров (фотографии Christopher Bettinger).

Работа над разлагаемым чипом-имплантатом ещё не завершена. Так, пока в качестве одного из его компонентов создатели схемы применили тонкую плёнку из поливинилового спирта (это полимер, способный к биологическому разложению). Но из-за него чип вынужден работать при достаточно высоком напряжении. Оно само по себе не опасное, но приводит к разложению некоторых молекул воды, оказавшихся поблизости. А это уже не слишком-то благоприятно для организма. Потому авторы чипа ведут поиск замены для данного материала. В частности, они экспериментируют с липидными мембранами. http: //www. membrana. ru/particle/14371

Биодеградируемая смола заменит повреждённые органы Первый в мире биоразлагаемый материал, пригодный для применения совместно с компьютерной стереолитографией, позволит в будущем создавать высококачественные биоинженерные имплантаты, готовые заменить повреждённые или вышедшие из строя органы или фрагменты тканей человеческого тела. Лазерная стереолитография основана на эффекте выборочной полимеризации материала под действием луча, управляемого компьютером. Так создают различные пластмассовые детали и макеты — быстро, с высокой точностью, с обилием очень тонких элементов и без литьевых форм. Образец нового материала, из которого при помощи лазера выращен высокопористый кубик

Если у человека отказывает клапан сердца, можно отсканировать его в 3 D при помощи томографа, а полученную цифровую модель направить в аппарат для стереолитографии — своего рода трёхмерный принтер. Только в новом клапане следует предусмотреть разветвлённую сеть отверстий и каналов микроскопического масштаба. Их можно засеять культурой из клеток, взятых у самого пациента. А затем — имплантировать клапан человеку. Поры в полимерной основе послужат строительными лесами для дальнейшего размножения клеток (по каналам же будут поступать питательные вещества). В конце концов полимер распадётся, а на месте останутся только естественные ткани — новый клапан, такой же как прежний. Искусственный клапан сердца (1980 год)

Аналогично можно восстановить повреждённую кость и так далее. Именно о таком применении нового материала мечтают исcледователи из Нидерландов, представившие биоразлагаемый фотополимеризуемый состав на основе полилактидов. http: //www. membrana. ru/particle/13850 Тот же куб, отснятый при разном увеличении и с помощью разной техники съёмки. Масштабные линейки – 500 микрометров. На снимке D можно заметить культуру костных клеток. На врезке слева вверху – пример машины для стереолитографии Полилактид

В случаях закупорки сосудов и тромбозов уже применяются специальные каркасы из полимерного материала, поддерживающие стенки сосудов.

Полимеры как кровезаменители.ppt