410-Тема-2-Растворы-полимеров.ppt
- Количество слайдов: 36
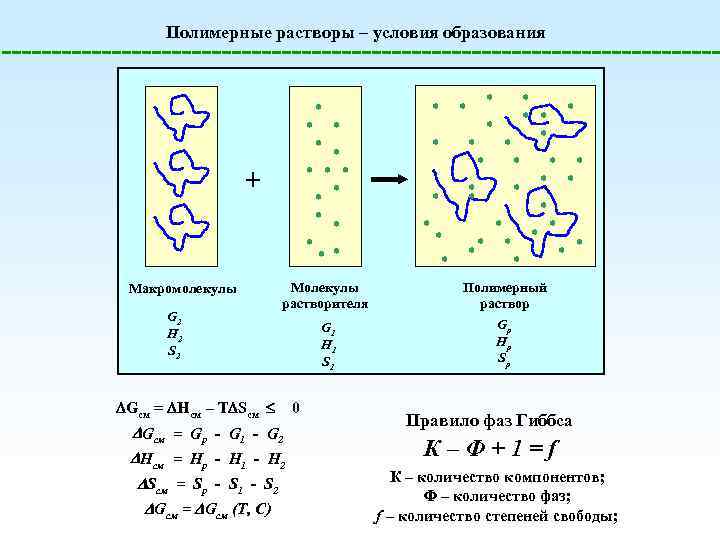
Полимерные растворы – условия образования + Макромолекулы G 2 H 2 S 2 Молекулы растворителя Gсм = Hсм – T Sсм 0 Gсм = Gр - G 1 - G 2 Hсм = Hр - H 1 - H 2 Sсм = Sр - S 1 - S 2 Gсм = Gсм (Т, С) G 1 H 1 S 1 Полимерный раствор Gр Hр Sр Правило фаз Гиббса К–Ф+1=f К – количество компонентов; Ф – количество фаз; f – количество степеней свободы;
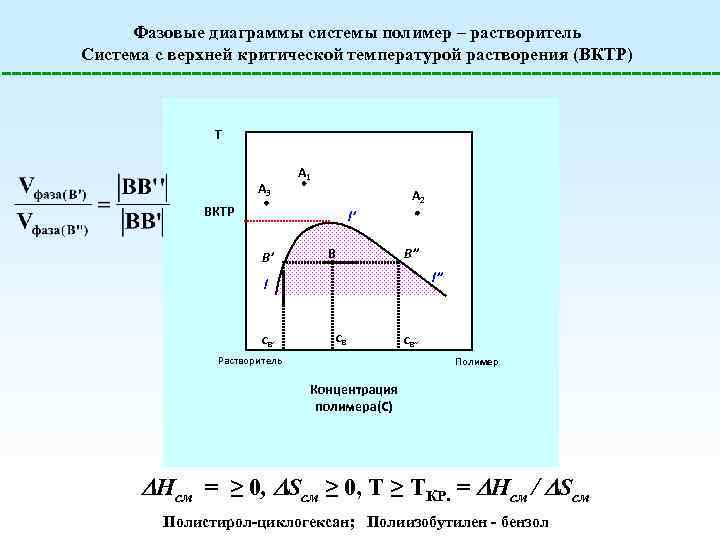
Фазовые диаграммы системы полимер – растворитель Система с верхней критической температурой растворения (ВКТР) T A 3 A 1 A 2 ВКТР l’ B’ B B’’ l СB’ СB Растворитель СB’’ Полимер Концентрация полимера(С) Hсм = ≥ 0, Sсм ≥ 0, T ≥ TКР. = Hсм / Sсм Полистирол-циклогексан; Полиизобутилен - бензол
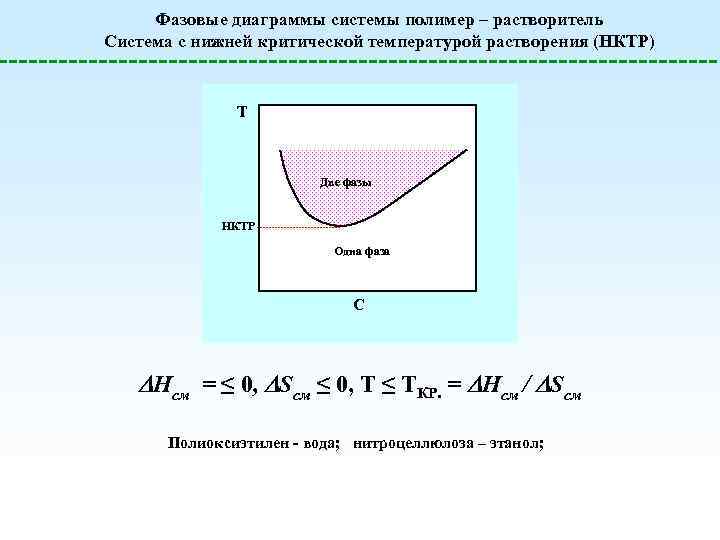
Фазовые диаграммы системы полимер – растворитель Система с нижней критической температурой растворения (НКТР) T Две фазы НКТР Одна фаза С Hсм = ≤ 0, Sсм ≤ 0, T ≤ TКР. = Hсм / Sсм Полиоксиэтилен - вода; нитроцеллюлоза – этанол;

Фазовые диаграммы системы полимер – растворитель Системы с НКТР и ВКТР A T Б T ВКТР Две фазы Одна фаза Две фазы НКТР Одна фаза ВКТР Две фазы НКТР Полипропиленоксид - вода С ВКТР ≥ НКТР С ВКТР ≤ НКТР
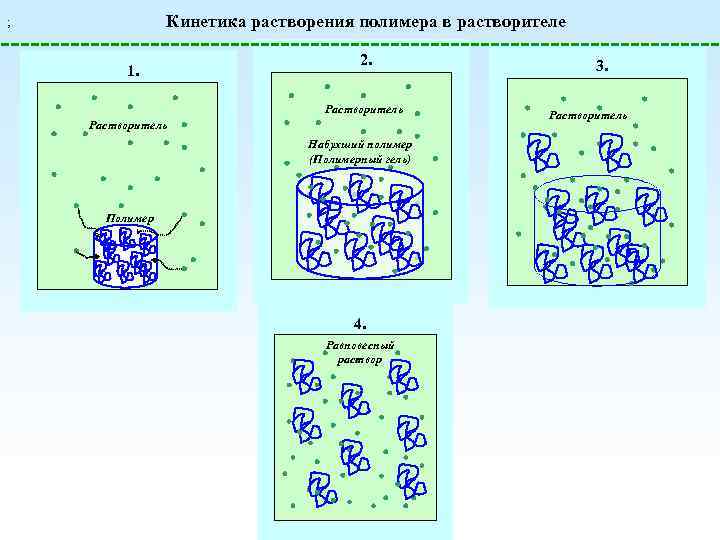
Кинетика растворения полимера в растворителе ; 1. 2. Растворитель Набухший полимер (Полимерный гель) Полимер 4. Равновесный раствор 3. Растворитель
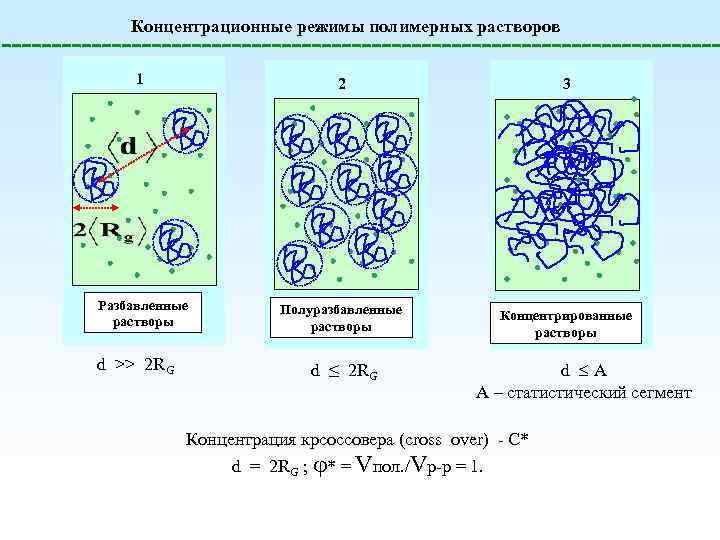
Концентрационные режимы полимерных растворов 1 2 Разбавленные растворы d >> 2 RG 3 Полуразбавленные растворы Концентрированные растворы d ≤ 2 RG d А А – статистический сегмент Концентрация крсоссовера (cross over) - C* d = 2 RG ; * = Vпол. /Vр-р = 1.
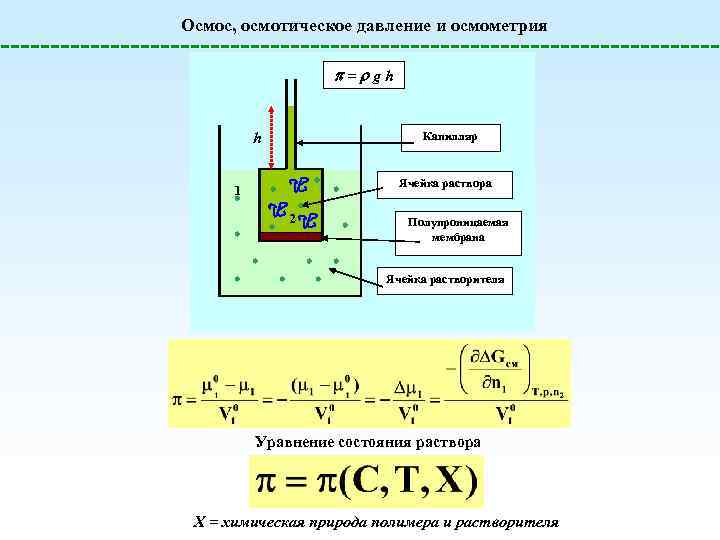
Осмос, осмотическое давление и осмометрия = g h h Капилляр Ячейка раствора 1 2 Полупроницаемая мембрана Ячейка растворителя Уравнение состояния раствора Х = химическая природа полимера и растворителя
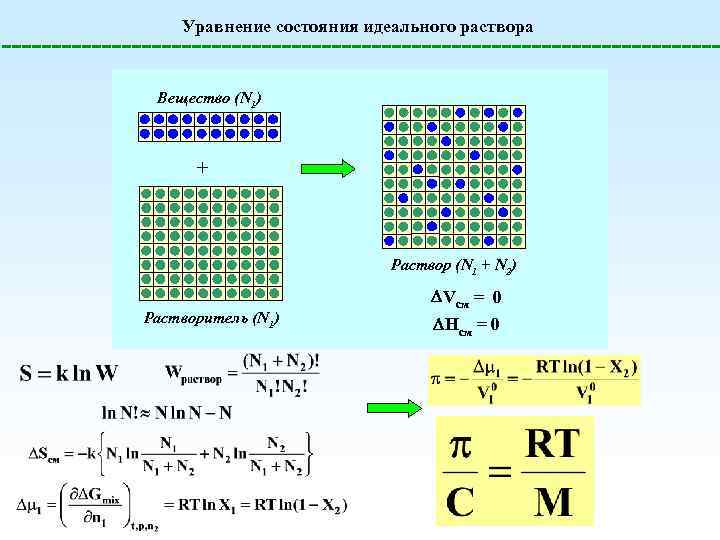
Уравнение состояния идеального раствора Вещество (N 1) + Раствор (N 1 + N 2) Растворитель (N 1) Vсм = 0 Hсм = 0
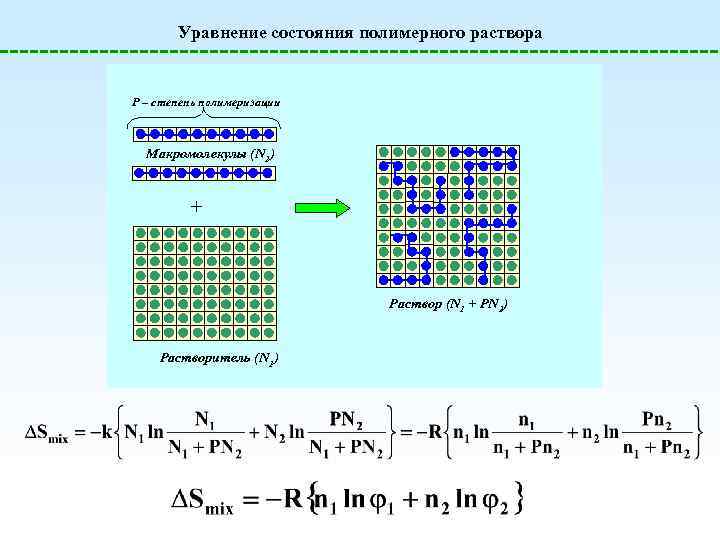
Уравнение состояния полимерного раствора P – степень полимеризации Макромолекулы (N 2) + Раствор (N 1 + PN 2) Растворитель (N 1)
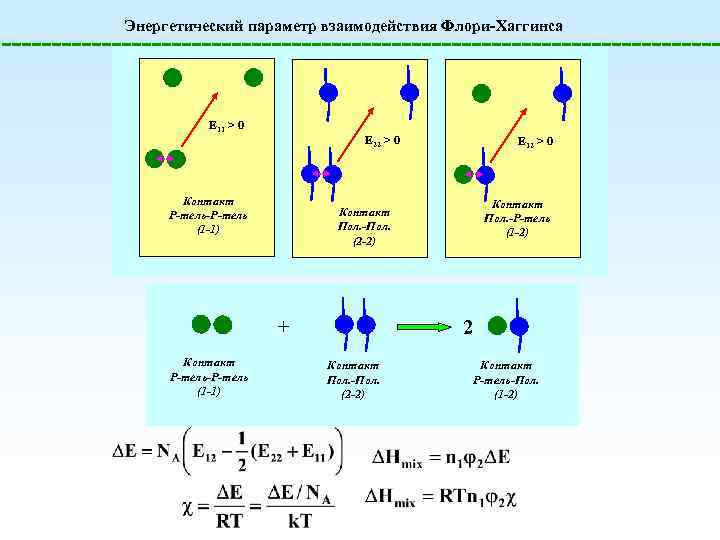
Энергетический параметр взаимодействия Флори-Хаггинса E 11 > 0 E 22 > 0 Контакт Р-тель-Р-тель (1 -1) Контакт Пол. -Р-тель (1 -2) Контакт Пол. -Пол. (2 -2) + Контакт Р-тель-Р-тель (1 -1) E 12 > 0 2 Контакт Пол. -Пол. (2 -2) Контакт Р-тель-Пол. (1 -2)

Уравнение состояния полимерного раствора

Определения -температуры для данной системы полимер - растворитель I -температура - температура, при которой раствор полимера формально подчиняется законам идеальных растворов (законы Рауля, Вант-Гоффа и др. ) I I -температура - критическая температура растворения полимера с бесконечно большой молекулярной массой. III -температура - температура, при которой исключенный объём клубка (u) равен нулю. Исключенный объем – область пространства, в которую данный клубок исключает проникновение других клубков. В -условиях клубок принимает такие размеры, какие он принял бы, если бы растворителя не было совсем.

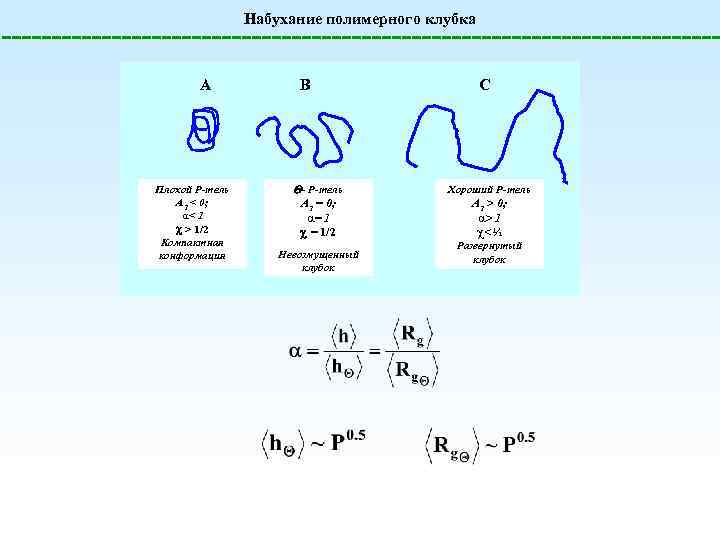
Набухание полимерного клубка A Плохой Р-тель A 2 < 0; < 1 > 1/2 Компактная конформация B - Р-тель A 2 = 0; = 1/2 Невозмущенный клубок C Хороший Р-тель A 2 > 0; > 1 c< ½ Развернутый клубок
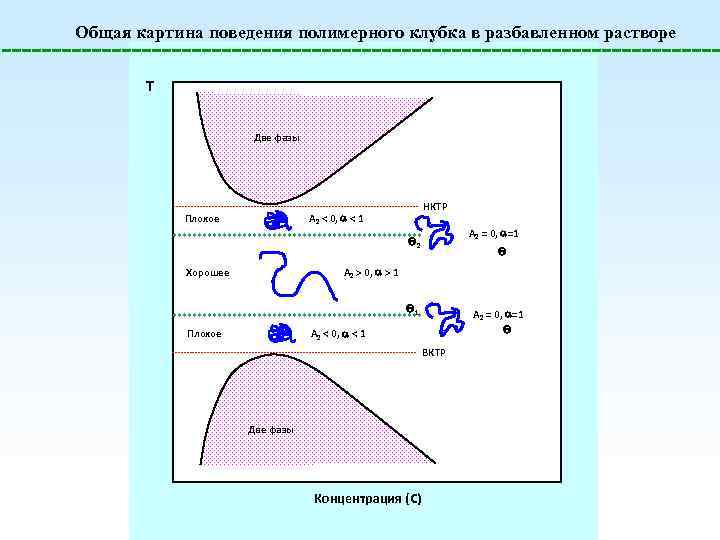
Общая картина поведения полимерного клубка в разбавленном растворе T Две фазы НКТР A 2 < 0, < 1 Плохое A 2 = 0, =1 2 A 2 > 0, > 1 Хорошее 1 A 2 = 0, =1 A 2 < 0, < 1 Плохое ВКТР Две фазы Концентрация (C)
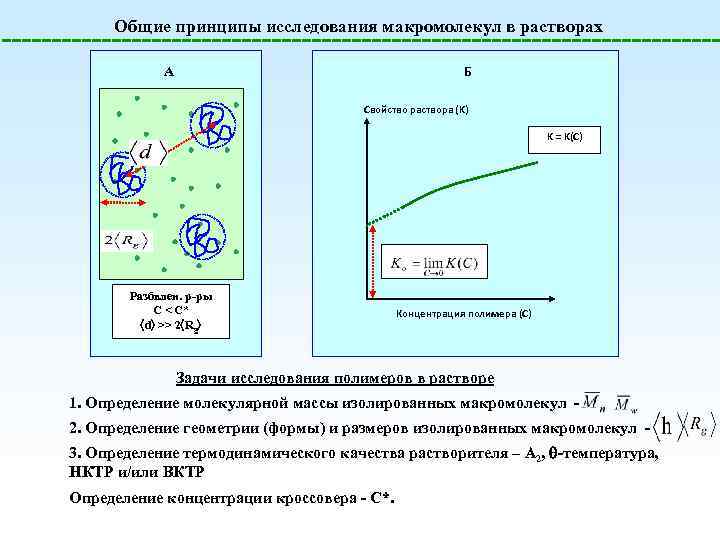
Общие принципы исследования макромолекул в растворах Б A Свойство раствора (K) K = K(C) Разбвлен. р-ры C < C* d >> 2 Rg Концентрация полимера (C) Задачи исследования полимеров в растворе 1. Определение молекулярной массы изолированных макромолекул - 2. Определение геометрии (формы) и размеров изолированных макромолекул 3. Определение термодинамического качества растворителя – A 2, -температура, НКТР и/или ВКТР Определение концентрации кроссовера - С*.
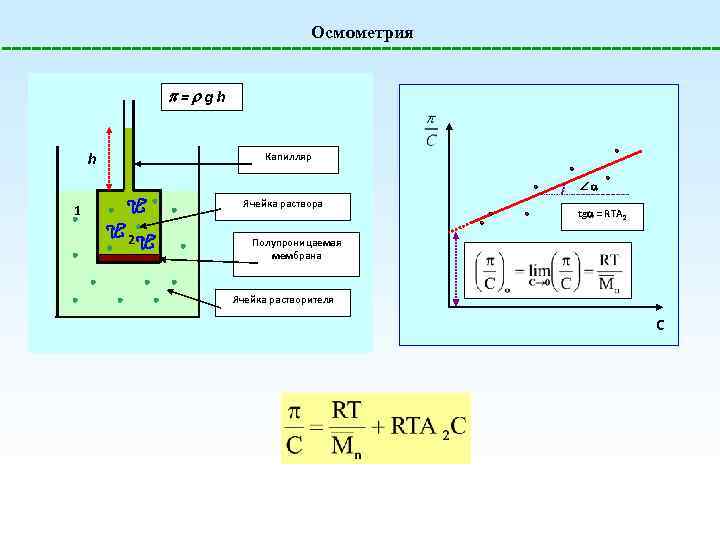
Осмометрия = gh h Капилляр Ячейка раствора 1 2 tg = RTA 2 Полупроницаемая мембрана Ячейка растворителя C
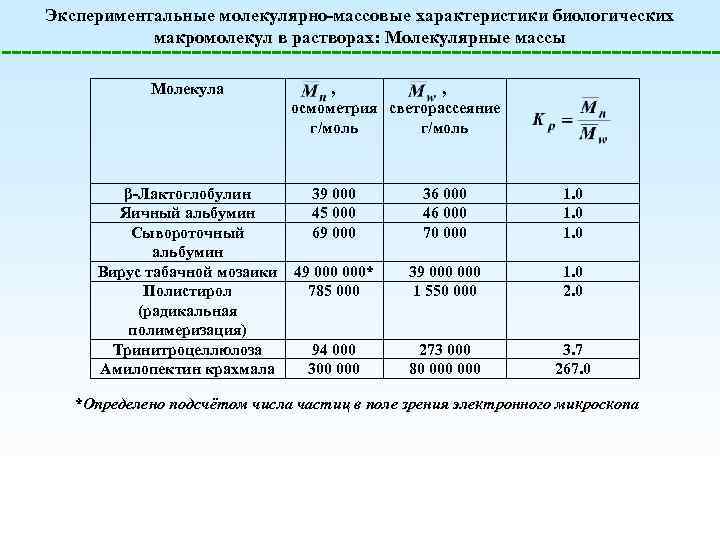
Экспериментальные молекулярно-массовые характеристики биологических макромолекул в растворах: Молекулярные массы Молекула β-Лактоглобулин Яичный альбумин Сывороточный альбумин Вирус табачной мозаики Полистирол (радикальная полимеризация) Тринитроцеллюлоза Амилопектин крахмала , , осмометрия светорассеяние г/моль 39 000 45 000 69 000 36 000 46 000 70 000 1. 0 49 000* 785 000 39 000 1 550 000 1. 0 2. 0 94 000 300 000 273 000 80 000 3. 7 267. 0 *Определено подсчётом числа частиц в поле зрения электронного микроскопа
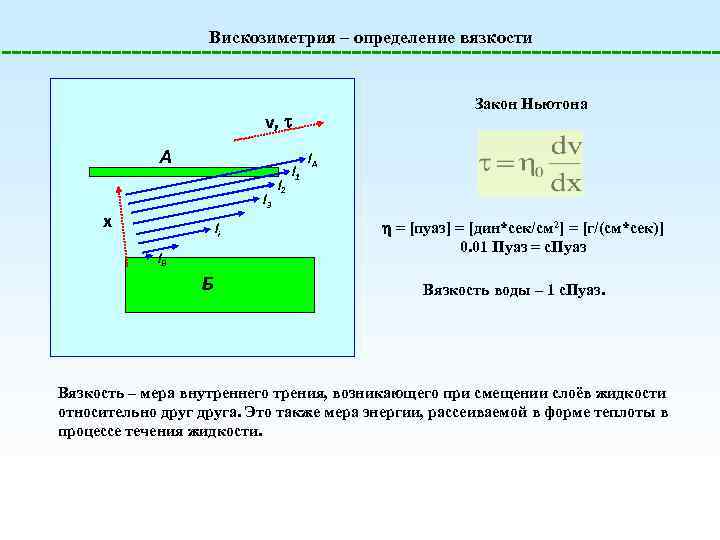
Вискозиметрия – определение вязкости Закон Ньютона v, A l 3 x li l. B Б l 2 l 1 l. A = [пуаз] = [дин*сек/см 2] = [г/(см*сек)] 0. 01 Пуаз = с. Пуаз Вязкость воды – 1 с. Пуаз. Вязкость – мера внутреннего трения, возникающего при смещении слоёв жидкости относительно друга. Это также мера энергии, рассеиваемой в форме теплоты в процессе течения жидкости.
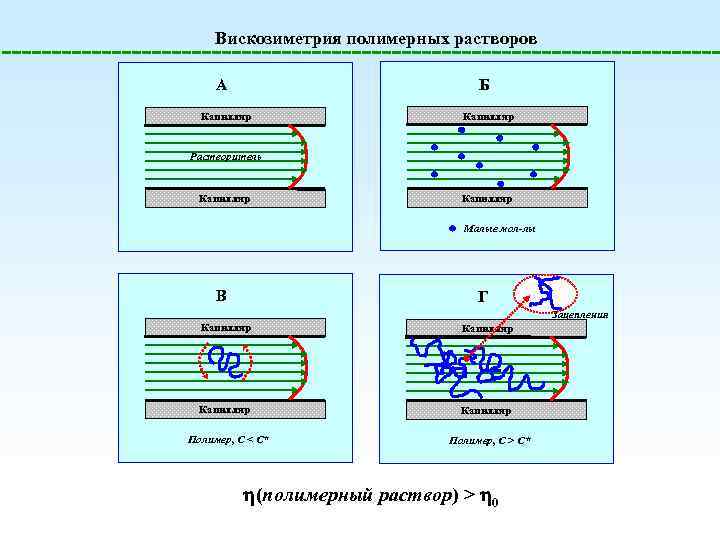
Вискозиметрия полимерных растворов Б A Капилляр Растворитель Капилляр Малые мол-лы В Г Зацепления Капилляр Полимер, C < C* Полимер, C > C* (полимерный раствор) > 0
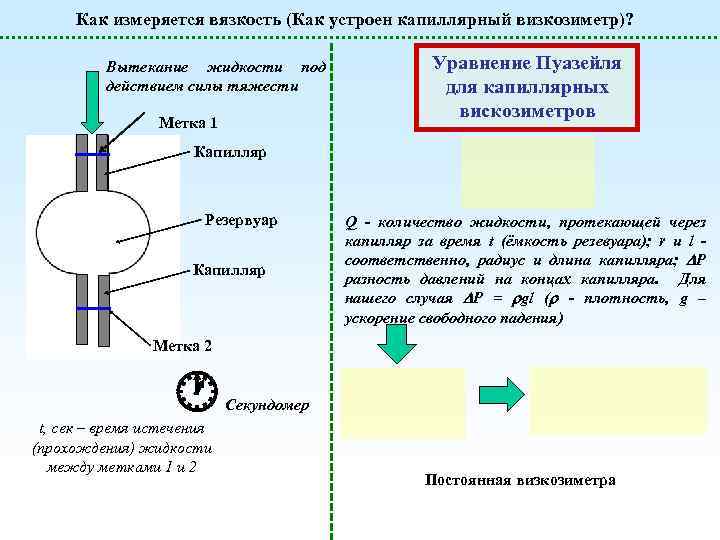
Как измеряется вязкость (Как устроен капиллярный визкозиметр)? Вытекание жидкости под действием силы тяжести Метка 1 Уравнение Пуазейля для капиллярных вискозиметров Капилляр Резервуар Капилляр Q - количество жидкости, протекающей через капилляр за время t (ёмкость резевуара); r и l соответственно, радиус и длина капилляра; Р разность давлений на концах капилляра. Для нашего случая Р = gl ( - плотность, g – ускорение свободного падения) Метка 2 t, сек – время истечения (прохождения) жидкости между метками 1 и 2 Секундомер Постоянная визкозиметра

Что такое удельная, приведенная и характеристическая вязкость? Как их определить экспериментально? Каковы единицы их измерения? Зачем нужны эти понятия? Допущение: для разбавленных растворов: o (плотность раствора равна плотности растворителя t – время истечения раствора полимера, t 0 – время УДЕЛЬНАЯ истечения чистого ВЯЗКОСТЬ: растворителя Единицы измерения – безразмерная; Физический смысл – относительный прирост вязкости за счёт введения полимера (исключает влияние вязкости растворителя на прирост вязкости раствора ПРИВЕДЕННАЯ ВЯЗКОСТЬ: С – весовая концентрация полимера в г/дл или г/см 3 Единицы измерения – дл/г или см 3/г; Физический смысл – исключает концентрационный вклад в прирост вязкости ХАРАКТЕРИСТИЧЕСКАЯ ВЯЗКОСТЬ [ ]: Единицы измерения – дл/г или см 3/г; Характеристическая вязкость – это приведенная вязкость при бесконечном разбавлении. Физический смысл – характеризует молекулярные свойства отдельных клубков.
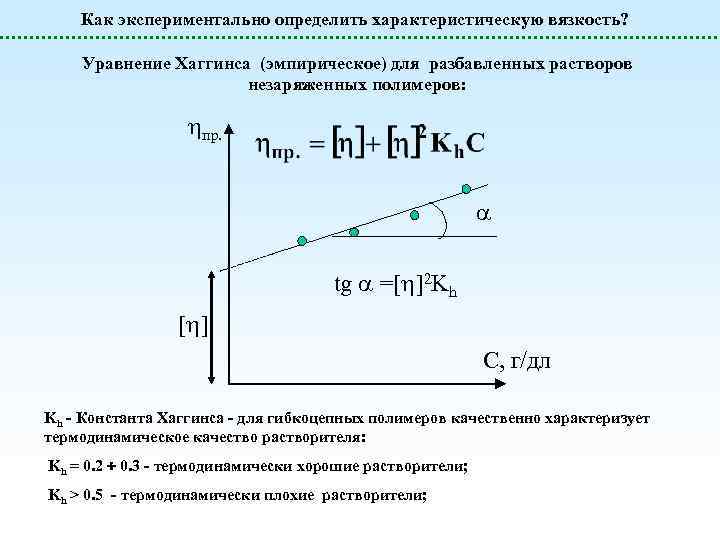
Как экспериментально определить характеристическую вязкость? Уравнение Хаггинса (эмпирическое) для разбавленных растворов незаряженных полимеров: пр. tg =[ ]2 Kh [ ] С, г/дл Kh - Константа Хаггинса - для гибкоцепных полимеров качественно характеризует термодинамическое качество растворителя: Kh = 0. 2 0. 3 - термодинамически хорошие растворители; Kh > 0. 5 - термодинамически плохие растворители;
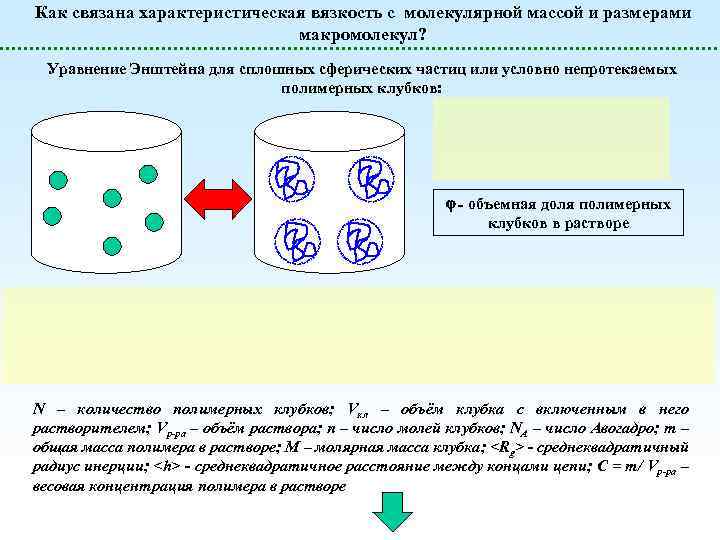
Как связана характеристическая вязкость с молекулярной массой и размерами макромолекул? Уравнение Энштейна для сплошных сферических частиц или условно непротекаемых полимерных клубков: - объемная доля полимерных клубков в растворе N – количество полимерных клубков; Vкл – объём клубка с включенным в него растворителем; Vр-ра – объём раствора; n – число молей клубков; NA – число Авогадро; m – общая масса полимера в растворе; M – молярная масса клубка; <Rg> - среднеквадратичный радиус инерции; <h> - среднеквадратичное расстояние между концами цепи; С = m/ Vр-ра – весовая концентрация полимера в растворе
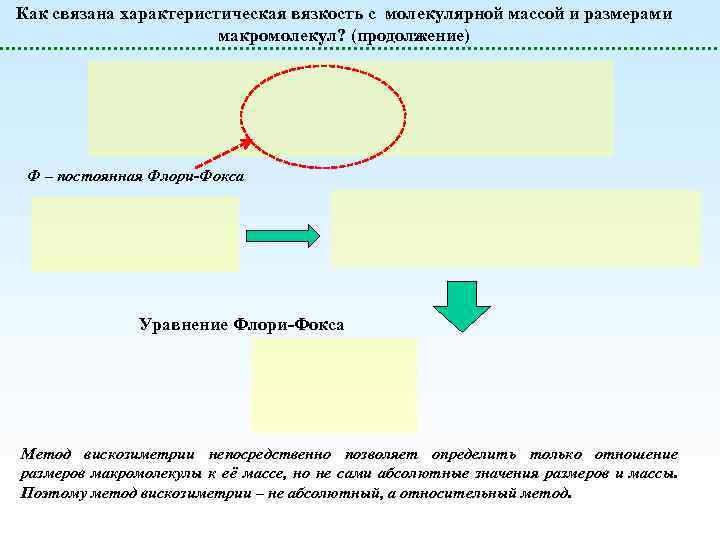
Как связана характеристическая вязкость с молекулярной массой и размерами макромолекул? (продолжение) Ф – постоянная Флори-Фокса Уравнение Флори-Фокса Метод вискозиметрии непосредственно позволяет определить только отношение размеров макромолекулы к её массе, но не сами абсолютные значения размеров и массы. Поэтому метод вискозиметрии – не абсолютный, а относительный метод.
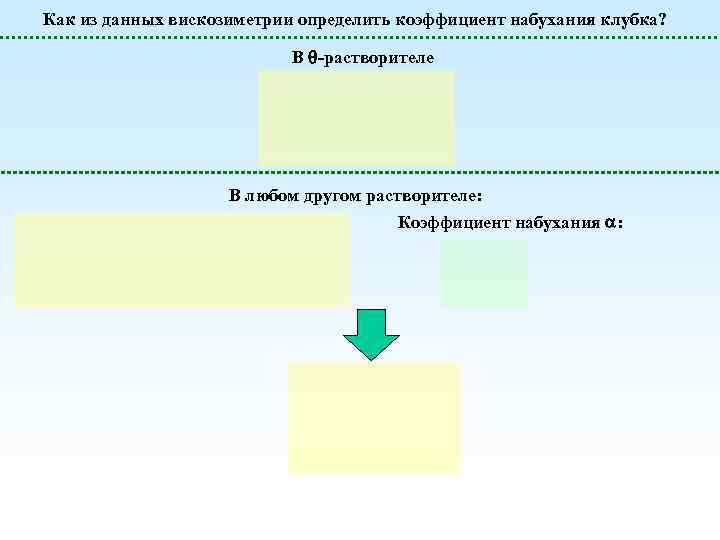
Как из данных вискозиметрии определить коэффициент набухания клубка? В -растворителе В любом другом растворителе: Коэффициент набухания :
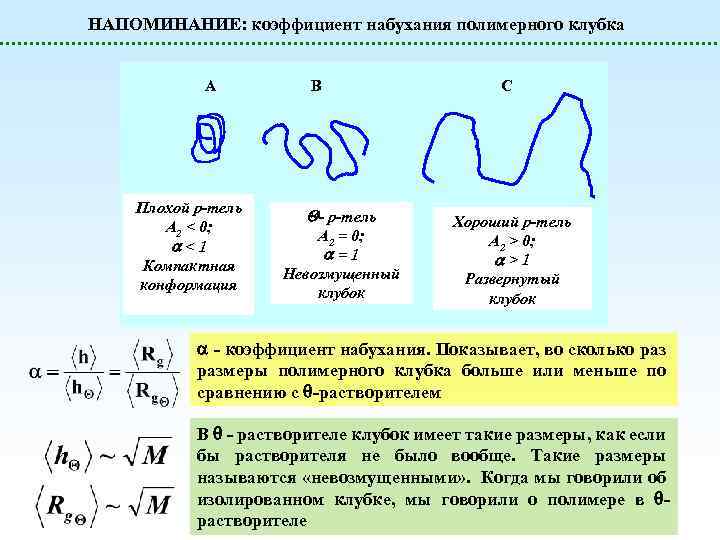
НАПОМИНАНИЕ: коэффициент набухания полимерного клубка A Плохой р-тель A 2 < 0; <1 Компактная конформация B - р-тель A 2 = 0; =1 Невозмущенный клубок C Хороший р-тель A 2 > 0; >1 Развернутый клубок - коэффициент набухания. Показывает, во сколько размеры полимерного клубка больше или меньше по сравнению с -растворителем В - растворителе клубок имеет такие размеры, как если бы растворителя не было вообще. Такие размеры называются «невозмущенными» . Когда мы говорили об изолированном клубке, мы говорили о полимере в растворителе
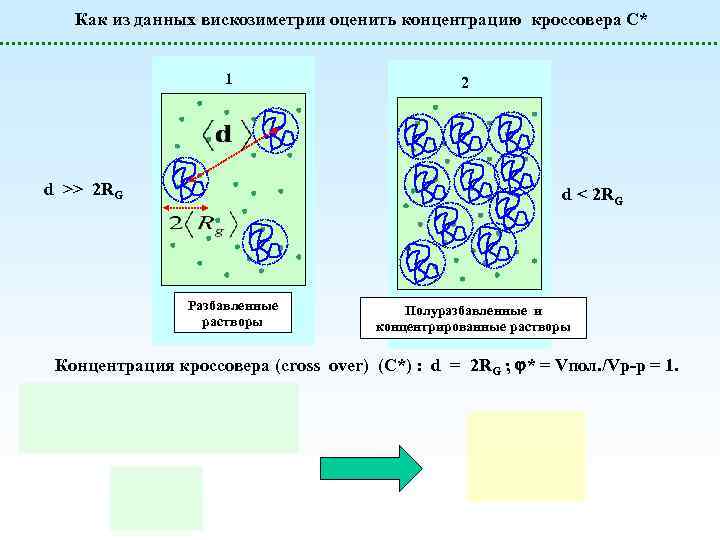
Как из данных вискозиметрии оценить концентрацию кроссовера С* 1 d >> 2 RG 2 d < 2 RG Разбавленные растворы Полуразбавленные и концентрированные растворы Концентрация кроссовера (cross over) (C*) : d = 2 RG ; * = Vпол. /Vр-р = 1.

Можно ли из данных вискозиметрии определить молекулярную массу полимера? Можно исключить <h> и сделать характеристическую вязкость функцией одной переменной – молекулярной массы М. Уравнение Марка-Куна-Хаувинка К и а – постоянные для данной системы полимер-растворитель при постоянной температуре Как получить значения К и а? Они берутся из калибровки: для серии полимерных образцов разных молекулярных масс (определенных другими методами) экспериментально определяются значения [ ]. Строится зависимость lg[ ] от lg. M. Полученные значения К и а заносятся в справочники и используются для определения молекулярной массы полимерных образцов данной химической структуры. tg = a - Средневязкостная молекулярная масса
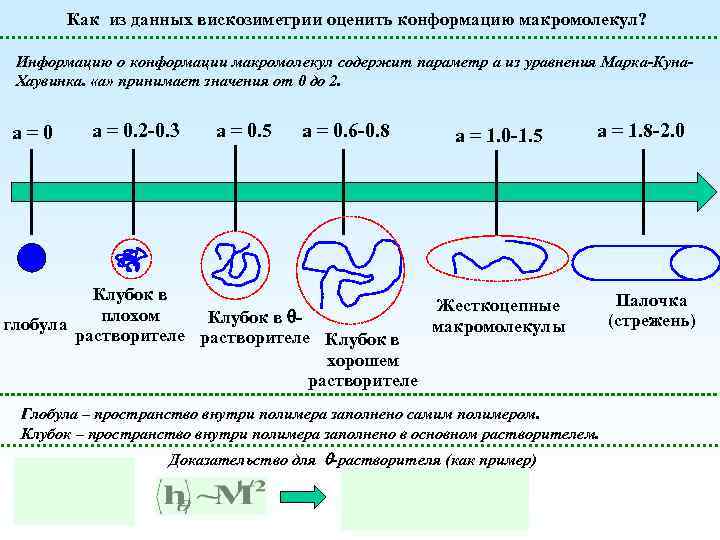
Как из данных вискозиметрии оценить конформацию макромолекул? Информацию о конформации макромолекул содержит параметр а из уравнения Марка-Куна. Хаувинка. «а» принимает значения от 0 до 2. а = 0. 2 -0. 3 а = 0. 5 а = 0. 6 -0. 8 а = 1. 0 -1. 5 а = 1. 8 -2. 0 Клубок в Жесткоцепные плохом Клубок в - глобула макромолекулы растворителе Клубок в хорошем растворителе Глобула – пространство внутри полимера заполнено самим полимером. Клубок – пространство внутри полимера заполнено в основном растворителем. Доказательство для -растворителя (как пример) Палочка (стрежень)
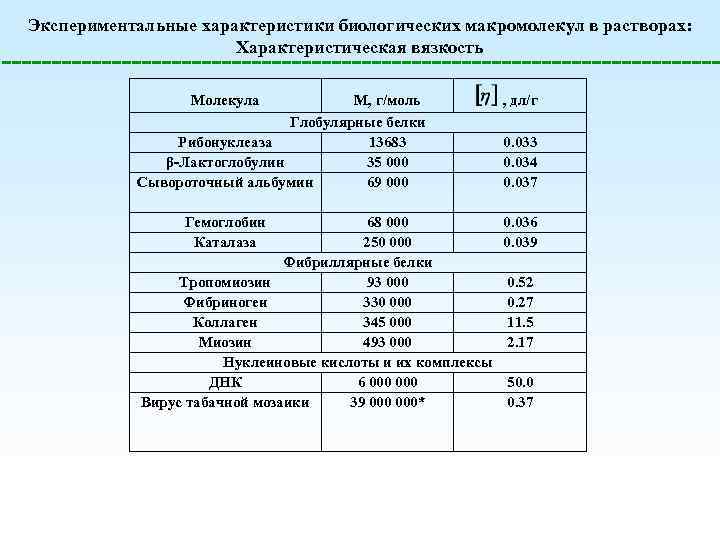
Экспериментальные характеристики биологических макромолекул в растворах: Характеристическая вязкость Молекула М, г/моль Глобулярные белки Рибонуклеаза 13683 β-Лактоглобулин 35 000 Сывороточный альбумин 69 000 Гемоглобин Каталаза 68 000 250 000 Фибриллярные белки Тропомиозин 93 000 Фибриноген 330 000 Коллаген 345 000 Миозин 493 000 Нуклеиновые кислоты и их комплексы ДНК 6 000 Вирус табачной мозаики 39 000* , дл/г 0. 033 0. 034 0. 037 0. 036 0. 039 0. 52 0. 27 11. 5 2. 17 50. 0 0. 37
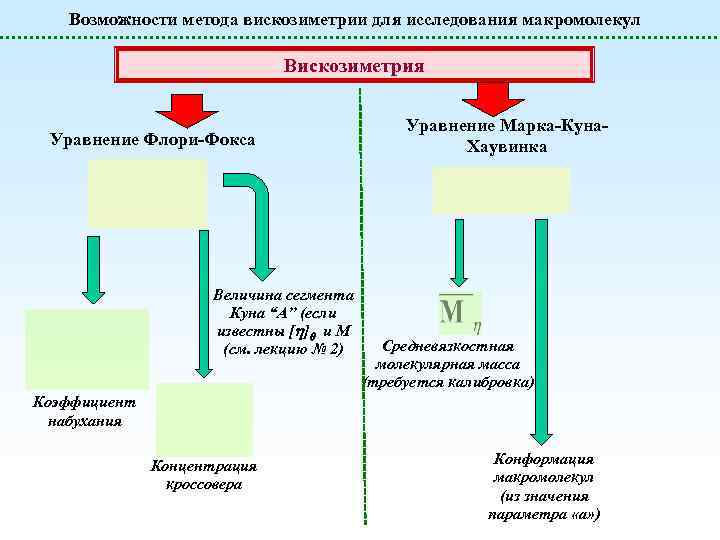
Возможности метода вискозиметрии для исследования макромолекул Вискозиметрия Уравнение Флори-Фокса Величина сегмента Куна “A” (если известны [ ] и M (см. лекцию № 2) Уравнение Марка-Куна. Хаувинка Средневязкостная молекулярная масса (требуется калибровка) Коэффициент набухания Концентрация кроссовера Конформация макромолекул (из значения параметра «а» )
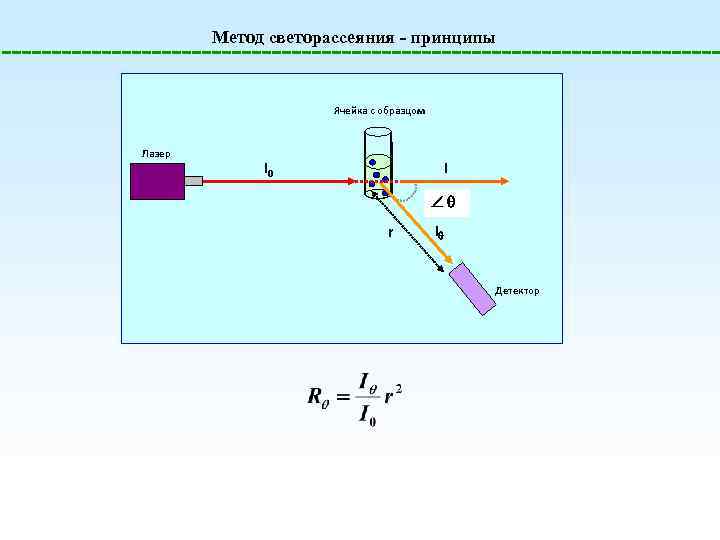
Метод светорассеяния - принципы Ячейка с образцом Лазер I 0 I r I Детектор
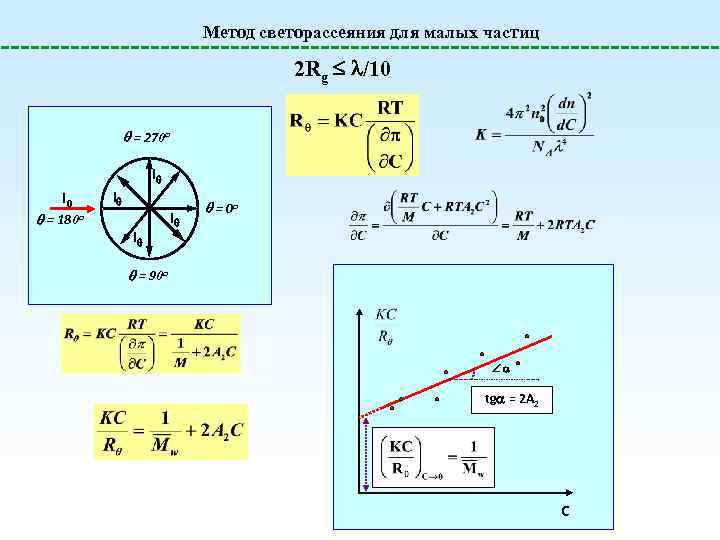
Метод светорассеяния для малых частиц 2 Rg /10 = 270 o I = I 0 180 o I I I = 0 o = 90 o tg = 2 A 2 C
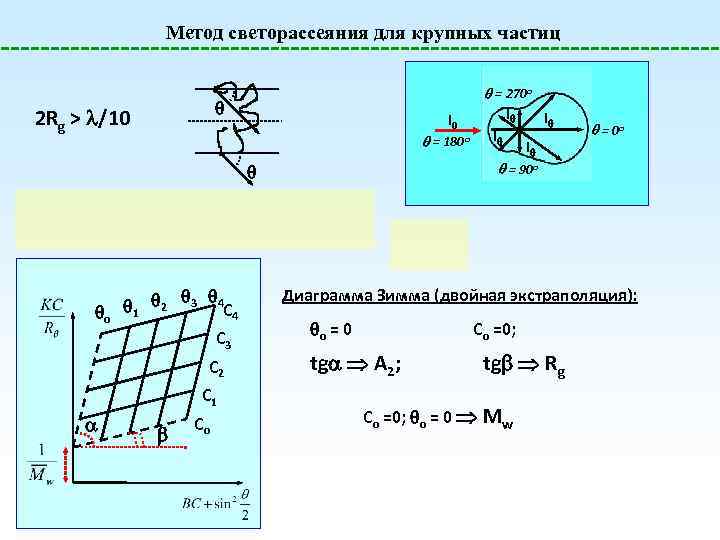
Метод светорассеяния для крупных частиц = 270 o 2 Rg > /10 = o C 3 C 2 C 1 Co 180 o I I = 0 o = 90 o 1 2 3 4 C 4 I 0 Диаграмма Зимма (двойная экстраполяция): о = 0 Со =0; tg A 2; tg Rg Со =0; о = 0 Mw
410-Тема-2-Растворы-полимеров.ppt