Поглотительная способность.ppt
- Количество слайдов: 35

Поглотительная способность почвы

Автором термина «поглотительная способность почвы» является К. К. Гедройц Поглотительная способность – способность почвы задерживать «соединения или части их, находящиеся в растворенном состоянии, а так же коллоидально распыленные частицы минерального и органического вещества, живые микроорганизмы и грубые суспензии» .

Виды поглотительной способности 1. Механическая – способность задерживать крупные твердые частицы, размер которых превышает диаметр почвенных пор. 2. Физическая – изменение концентрации молекул растворенного вещества на поверхности твердых частиц почвы 3. Химическая – способность образовывать нерастворимые соединения за счет химической реакции катионов с анионами 4. Биологическая – способность микроорганизмов и растений поглощать из почвенного раствора различные вещества 5. Физико-химическая (обменная) – способность обменивать некоторую часть катионов, содержащихся в твердой фазе на эквивалентное количество катионов, находящихся в соприкасающемся с нею растворе

Механическая поглотительная способность – свойство почвы, как всякого пористого тела, задерживать в своей толще различные частицы, находящиеся в фильтрующейся через почву воде. Это происходит благодаря наличию в почве сложной системы пор, капилляров и ходов корней, которые нередко заканчиваются тупиками. Механическая поглотительная способность зависит от: 1. Гранулометрического состава 2. Агрегатного состава (структуры) почвы 3. Плотности сложения

Биологическая поглотительная способность почвы Этот вид поглотительной способности характеризуется высокой избирательностью поглощения. Живые организмы способны усваивать элементы различной доступности, не только находящиеся в почвенном растворе, но и даже те из них, которые находятся в кристаллической решетке первичных и вторичных минералов. Особое значение этот вид поглотительной способности будет иметь на почвах легкого гранулометрического состава, где проявление других видов поглотительной способности ограничено.

Физическая поглотительная способность почвы Поверхностно-активные вещества – вещества, способные снижать поверхностное натяжение. К ним относятся спирты, органические кислоты, многие высокомолекулярные органические соединения, в том числе и гумусовые кислоты. В результате проявления поглотительной физической сорбции создаются предпосылки для последующего более прочного закрепления органических соединений минеральными компонентами путем адгезии (склеивания) при высыхании почв. Большинство минеральных солей, кислот и щелочей увеличивают поверхностное натяжение воды, в связи с чем концентрация их по мере приближения к границе раздела дисперсной фазы и дисперсионной среды снижается, т. е. проявляется отрицательная физическая сорбция.

Химическая поглотительная способность почвы. Химическая поглотительная способность (хемосорбция) заключается в образовании труднорастворимых соединений при взаимодействии отдельных компонентов почвы с формированием новой твердой фазы. Из катионов чаще всего нерастворимые соединения дают Ca 2+, Mg 2+, Al 3+, Fe 3+, а среди анионов – СО 32–, РО 43–, SO 42–. Например, при внесении фосфорных удобрений в кислые почвы алюминий, присутствующий в почвенном растворе, будет образовывать с фосфат–ионом труднорастворимое соединение выпадающее в осадок: 2 Al 3+ + Ca (H 2 PO 4)2 → 2 Al. PO 4 + Ca 2+ + 4 H+ При поступлении соды в почву, содержащую соли кальция, также образуется новая твердая фаза, представленная карбонатом кальция Na 2 CO 3 + Ca. SO 4 → Na 2 SO 4 + Ca. CO 3
Образование осадков возможно и на поверхности почвенных частиц при взаимодействии ионов, способных к взаимному осаждению. Такая сорбция получила название осадочной. Типичный пример – сорбция фосфатов на поверхности гидроксидов железа и алюминия: + → + + +2 К химическому поглощению относится и комплексообразовательная сорбция. Когда за счет образования координационной связи происходит связывание поливалентных ионов почвенного раствора органическим веществом, которое сорбировано твердой фазой почвы:
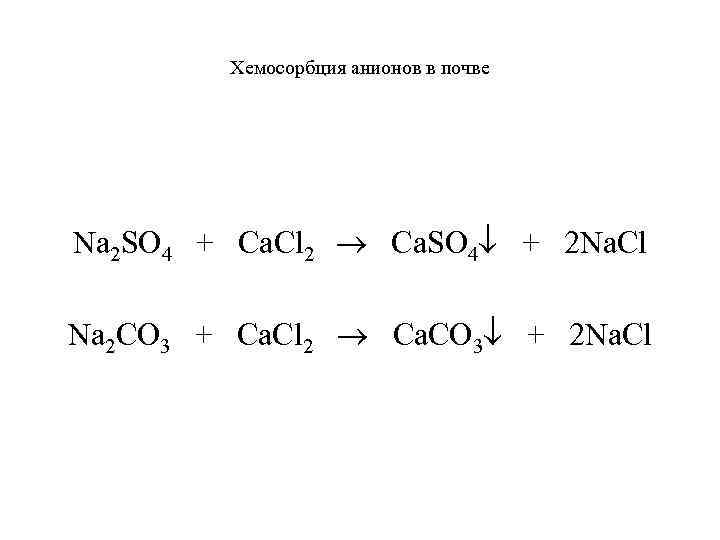
Хемосорбция анионов в почве Na 2 SO 4 + Ca. Cl 2 Ca. SO 4 + 2 Na. Cl Na 2 CO 3 + Ca. Cl 2 Ca. CO 3 + 2 Na. Cl

Физико-химическая поглотительная способность почвы. Физико-химическая, или обменная, поглотительная способность (ионообменная сорбция) – способность почвы обменивать ионы, находящиеся в компенсирующем слое коллоидов на эквивалентное количество ионов почвенного раствора. Важнейшую роль в ее проявлении играет почвенный поглощающий комплекс (ППК). ППК представляет собой совокупность нерастворимых в воде органических, минеральных и органо–минеральных соединений, находящихся преимущественно в высокодисперсном состоянии и обладающих высокой реакционной и ионообменной способностью.

Почвенные коллоиды Коллоиды – это наиболее дисперсная часть твердой фазы почвы, размеры их лежат в пределах 0, 2 – 0, 001 мкм. С коллоидами непосредственно связаны физико-химические и химические свойства почвы, они играют важную роль в качестве цементирующих и клеящих веществ при формировании почвенной структуры, от характера которой зависит вводно-воздушный режим почвы, с коллоидами связана динамика питательных веществ, закрепление в почве органического вещества и биофильных элементов. Минеральные коллоиды состоят преимущественно из вторичных минералов. Преобладают среди них кристаллические глинистые минералы: монтмориллонит, каолинит, гидрослюды, смешанослойные минералы и др. Органические коллоиды состоят в основном из гумусовых веществ и белков. В коллоидно–дисперсном состоянии могут находиться полисахариды, белки, лигнин и некоторые другие соединения, а также клетки наиболее мелких бактерий, диаметр которых лежит в пределах размеров коллоидных частиц Органо–минеральные коллоиды как правило формируются в результате взаимодействия гумусовых веществ с глинистыми минералами и осажденными формами полутораоксидов.
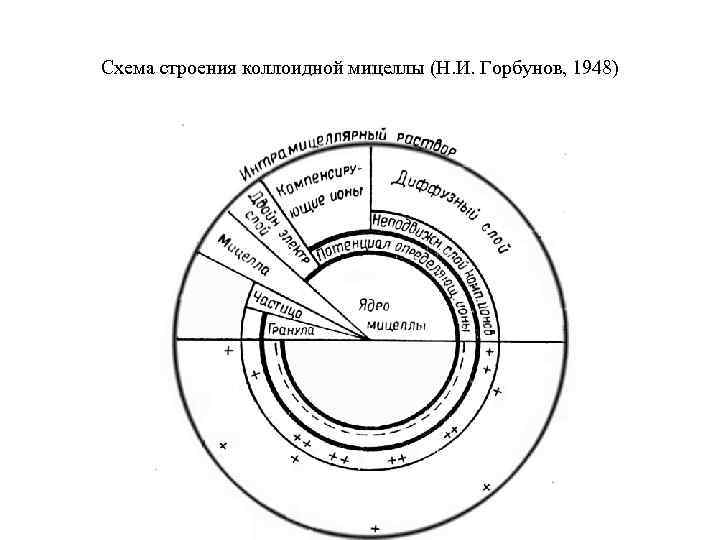
Схема строения коллоидной мицеллы (Н. И. Горбунов, 1948)

Свойства почвенных коллоидов • • • Коллоиды, имеющие в потенциалопределяющем слое отрицательно заряженные ионы, называются ацидоидами и несут отрицательный заряд. Коллоиды, имеющие в потенциалопределяющем слое положительно заряженные ионы, называются базоидами. Они несут положительный заряд и способны к поглощению и обмену анионов. Некоторые коллоиды способны менять знак заряда: в кислой среде они заряжены положительно, в щелочной – отрицательно. Такие коллоиды называются амфолитоидами или амфотерными коллоидами. Коллоиды, сильно гидратирующиеся , то есть способные удерживать мощные водные пленки, называются гидрофильными. К ним можно отнести аморфную кремнекислоту, минералы группы монтмориллонита, гумусовые кислоты. Коллоиды, слабо гидратирующиеся, называются гидрофобными. К ним относятся гидроксиды железа и алюминия, минералы группы каолинита и другие вещества. Важнейшим свойством почвенных коллоидов является их агрегативная устойчивость, то есть способность коллоидной системы сохранять неизменной степень дисперсности. В почве коллоиды могут находиться в состоянии золя, или во взвешенном состоянии, разделенные жидкой фазой, что обусловлено наличием электрического заряда (электрокинетического потенциала) и гидратной оболочки на поверхности частиц. Если заряд коллоидов снижается, а гидратная оболочка уменьшается, коллоиды начинают взаимодействовать между собой, что ведет к слипанию частиц и выпадению их в осадок в виде геля. Это явление называется коагуляцией. Для некоторых коллоидов характерна способность к обратному переходу из геля в золь. Это явление носит название пептизация. Коллоиды, которые могут легко переходить из золя в гель и обратно называют обратимыми.

Схема формирования отрицательно заряженных коллоидов гидроксидов железа и алюминия Fe(OH)3 + OH– H 2 Fe. O 3– + H 2 O Al(OH)3 + OH– H 2 Al. O 3– + H 2 O

Схема формирования положительно заряженных коллоидов гидроксидов железа и алюминия Fe(OH)3 + H+ Fe(OH)2+ + H+ + ОН– Fe(OH)2+ + H 2 O Al(OH)3 + H+ Al(OH)2+ + H 2 O

Лиотропный ряд катионов (К. К. Гедройц) Li+ < Na+ < NH 4+ < K+ < Mg+ +< H+ < Ca+ + < Ba+ + < Al+ + + < Fe+ + +
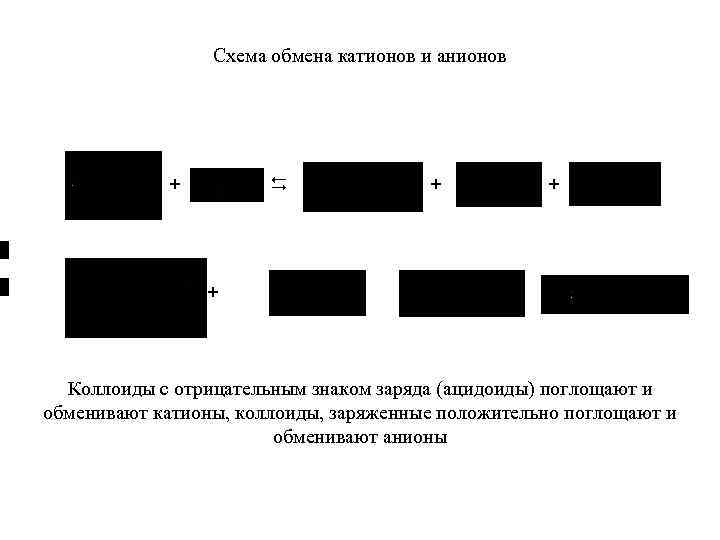
Схема обмена катионов и анионов D + + + D + + Коллоиды с отрицательным знаком заряда (ацидоиды) поглощают и обменивают катионы, коллоиды, заряженные положительно поглощают и обменивают анионы

Закономерности обменного поглощения • • • Обычно в обменных реакциях в почвах принимают участие следующие катионы: Na+, K+, NH 4+, Ca 2+, Mg 2+, Al 3+, H+. В небольшом количестве обменном состоянии могут находиться медь, цинк, двухвалентное железо и другие элементы. Наиболее хорошо изучены обменные реакции, протекающие с участием Ca 2+, Mg 2+, Na+, K+. Обмен катионов в почве подчиняется следующим закономерностям: 1. Эквивалентность и полная обратимость обмена между поглощенными катионами твердой фазы почвы и катионами почвенного раствора. 2. При одинаковой концентрации ионов в растворе энергия их поглощения возрастает с увеличением валентности иона, поскольку по мере увеличения валентности катионы образуют с анионами потенциалопределяющего слоя (COO– Si. O 32–, Al. O 2– и др. ) все менее диссоциированные соединения. 3. У ионов с одинаковой валентностью энергия поглощения возрастает с увеличением атомной массы. 4. Энергия поглощения зависит от радиуса негидратированного иона. Чем меньше радиус иона, тем больше плотность его заряда, тем сильнее гидратируется ион. Большие гидратные оболочки препятствуют взаимодействию катионов с ионами потенциалопределяющего слоя.

Интенсивность поглощения катионов почвой (К. К. Гедройц, 1975) Li+ < Na+ < NH 4+ < K+ < Rb+ < Cs+ < Mg 2+ <H+ < Ca 2+ < Ba 2+ < Al 3+ < Fе 3+

Интенсивность поглощения анионов почвой Cl– NO 3–<SO 42–<CO 32–<PO 43– (H 2 PO 4–, HPO 42–) <Si. O 44– (Si. O 33–) <OH–

Важнейшее свойство почвы это реакция среды. Она обусловлена наличием и соотношением в почвенном растворе водородных (Н+) и гидроксильных (ОН–) ионов. Различают почвы: • очень сильнокислые – р. НKCl < 4, 0; • сильнокислые – 4, 1 – 4, 5; • среднекислые – 4, 6 – 5, 0; • слабокислые – 5, 1 – 5, 5; • нейтральные – 5, 6 – 7, 4; • слабощелочные – р. НН 2 О 7, 5 – 8, 0; • среднещелочные – 8, 1 – 8, 5; • сильнощелочные – 8, 6 – 10, 0; • резкощелочные – 10, 1 – 12, 0.

Виды почвенной кислотности • Кислотность почв – способность почв нейтрализовать копоненты щелочной природы, подкислять воду и растворы нейтральных солей. Различают следующие формы или виды почвенной кислотности: 1) актуальная кислотность; 2) потенциальная кислотность( подразделяется на обменную и гидролитическую).

Актуальная кислотность. Представляет собой кислотность почвенного раствора. Измеряется она величиной р. Н водной вытяжки или водной суспензии (р. НН 2 О) при соотношении почва — вода 1: 2, 5. В разных почвах показатель актуальной кислотности колеблется от 3 до 7.

Потенциальная кислотность. Обменная кислотность проявляется при обработке почвы раствором нейтральной соли, обычно 1 н КCl, при этом происходит эквивалентный обмен катионов нейтральной соли на катионы водорода и алюминия, находящихся в компенсирующем слое коллоидов: Образующаяся в результате обменных реакций соль Al. Cl 3 в водном растворе гидролитически расщепляется: [ППК 3 -]Al 3+ + 3 KCl = [ППК 3 -]К 3+ + Al. Cl 3 +H 2 O = Al(OH)3 + 3 HCl

Гидролитическая кислотность. При обработке почвы раствором нейтральной соли вытесняются не все поглощенные ионы водорода. Более полное вытеснение ионов водорода и других кислотных ионов происходит при взаимодействии почвы с раствором гидролитически щелочной соли, например, СН 3 COONa. D Гидролитическая кислотность, как правило, больше обменной и может рассматриваться как суммарная кислотность почвы, состоящая из актуальной и потенциальной кислотности. Выражается она в миллиграмм-эквивалентах на 100 г почвы.

Обменное поглощение катионов Обменным поглощением (обменной сорбцией) катионов называется способность катионов диффузного слоя коллоидов обмениваться на эквивалентное количество катионов почвенного раствора. В обменном состоянии в почвах обычно находятся Ca 2+, Mg 2+, Na+, K+, H+, Al 3+, NH 4+, в незначительных количествах — Fe 2+, Mn 2+, а также Li+, Sr+ и др. Общее количество всех поглощённых (обменных) катионов называется емкостью катионного обмена (ЕКО), которая выражается в милиграммэквивалентах на 100 г почвы.

В составе ППК разных областей основную роль играют катионы: • Для почв экстрагумидных и гумидных областей (Ку) 1 в Са 2+, Мg 2+, Н+, АL 3+; • для семигумидных с Ку < 1 — Са 2+, Мg 2+ • и для почв аридных областей с Ку < 0, 5 — Са 2+, Мg 2+, Na+, иногда с существенным участием К+.
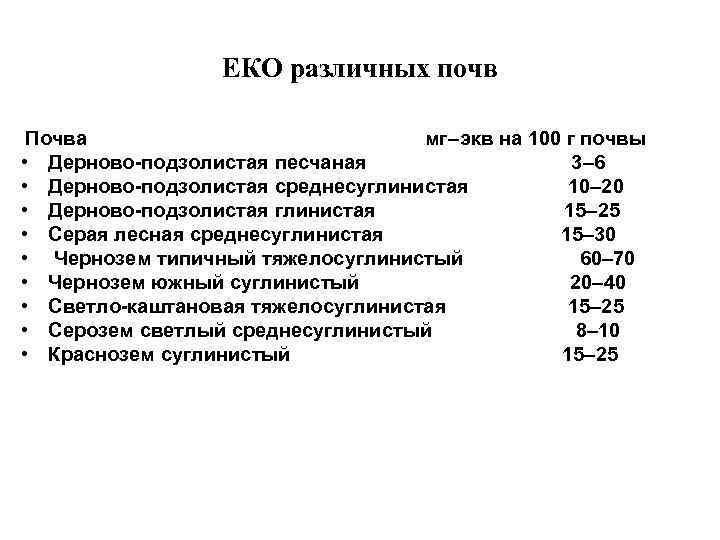
ЕКО различных почв Почва мг–экв на 100 г почвы • Дерново-подзолистая песчаная 3– 6 • Дерново-подзолистая среднесуглинистая 10– 20 • Дерново-подзолистая глинистая 15– 25 • Серая лесная среднесуглинистая 15– 30 • Чернозем типичный тяжелосуглинистый 60– 70 • Чернозем южный суглинистый 20– 40 • Светло-каштановая тяжелосуглинистая 15– 25 • Серозем светлый среднесуглинистый 8– 10 • Краснозем суглинистый 15– 25

Известкование кислых почв Устраняющее избыточную кислотность и способствующее насыщению ППК кальцием. При внесении в почву извести (Са. СО 3) она реагирует с углекислотой почвенного раствора и переходит в гидрокарбонат кальция, который взаимодействует с почвой: + 2 Сa(HCO 3)2= + H 2 O + 4 CO 2 + Al(OH)3

Щелочность почв Различают актуальную (активную) и потенциальную щёлочность почв. Актуальная щелочность обусловлена наличием в почвенном растворе гидролитически щелочных солей (Na 2 CO 3, Na. HCO 3, Ca(HCO 3)2), при диссоциации которых образуется гидроксильный ион. Щелочность почв принято оценивать только по значениям актуальной щелочности, которую определяют в водной вытяжке или суспензии потенциометрически, при этом она выражается в единицах р. Н.

Потенциальная щелочность • обусловлена наличием в ППК обменного натрия, который может вытесняться водородом углекислоты, а образующаяся в почвенном растворе сода подщелачивает его.

• Эффективным приемом повышения плодородия почв с щелочной реакцией является химическая мелиорация. В качестве мелиоранта широко применяется гипс и различные гипсосодержащие вещества.

• Общее содержание всех обменных катионов, кроме Н+ и А 13+, называют суммой обменных оснований. Исходя из этого, все почвы можно разделить на две большие группы: почвы насыщенные основаниями и почвы ненасыщенные основаниями. • Почвы насыщенные основаниями не содержат в ППК ионы Н+ и А 13+. Обменные катионы представлены только обменными основаниями — Са 2+, Mg 2+, Na+, K+, NH 4+. Количество их соответствует величине реальной емкости обмена. • Почвы ненасыщенные основаниями всегда содержат некоторое количество обменных Н+ и А 13+, поэтому сумма обменных оснований у них меньше емкости обмена.

Для относительной оценки количества содержащихся в них обменных оснований используется показатель – степень насыщенности почвы основаниями (V). При V более 80% почвы не нуждаются в известковании, При 50 -80 % потребность — средняя и слабая при V менее 50% высокая
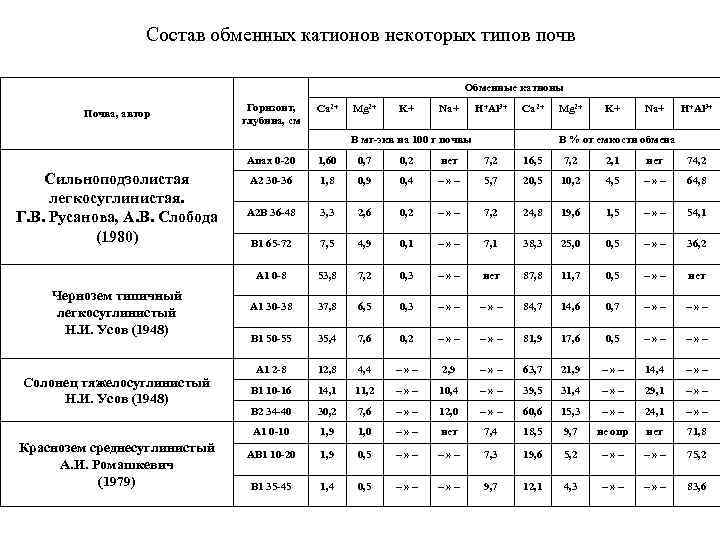
Состав обменных катионов некоторых типов почв Обменные катионы Почва, автор Горизонт, глубина, см Са 2+ Mg 2+ K+ Na+ H+Al 3+ Са 2+ В мг-экв на 100 г почвы Mg 2+ K+ Na+ H+Al 3+ В % от емкости обмена Апах 0 -20 Солонец тяжелосуглинистый Н. И. Усов (1948) Краснозем среднесуглинистый А. И. Ромашкевич (1979) 0, 2 нет 7, 2 16, 5 7, 2 2, 1 нет 74, 2 А 2 30 -36 1, 8 0, 9 0, 4 –» – 5, 7 20, 5 10, 2 4, 5 –» – 64, 8 А 2 В 36 -48 3, 3 2, 6 0, 2 –» – 7, 2 24, 8 19, 6 1, 5 –» – 54, 1 В 1 65 -72 7, 5 4, 9 0, 1 –» – 7, 1 38, 3 25, 0 0, 5 –» – 36, 2 53, 8 7, 2 0, 3 –» – нет 87, 8 11, 7 0, 5 –» – нет А 1 30 -38 37, 8 6, 5 0, 3 –» – 84, 7 14, 6 0, 7 –» – В 1 50 -55 35, 4 7, 6 0, 2 –» – 81, 9 17, 6 0, 5 –» – А 1 2 -8 12, 8 4, 4 –» – 2, 9 –» – 63, 7 21, 9 –» – 14, 4 –» – В 1 10 -16 14, 1 11, 2 –» – 10, 4 –» – 39, 5 31, 4 –» – 29, 1 –» – В 2 34 -40 30, 2 7, 6 –» – 12, 0 –» – 60, 6 15, 3 –» – 24, 1 –» – А 1 0 -10 Чернозем типичный легкосуглинистый Н. И. Усов (1948) 0, 7 А 1 0 -8 Сильноподзолистая легкосуглинистая. Г. В. Русанова, А. В. Слобода (1980) 1, 60 1, 9 1, 0 –» – нет 7, 4 18, 5 9, 7 не опр нет 71, 8 АВ 1 10 -20 1, 9 0, 5 –» – 7, 3 19, 6 5, 2 –» – 75, 2 В 1 35 -45 1, 4 0, 5 –» – 9, 7 12, 1 4, 3 –» – 83, 6
Поглотительная способность.ppt