Подгруппа титана1.ppt
- Количество слайдов: 37

Подгруппа титана Элементы IV Б группы: титан, цирконий, гафний Сопоставление электронных конфигураций, величин радиусов, энергии ионизации, характерных степеней окисления, координационных чисел атомов элементов IV А и IV Б групп. Получение, применение и сопоставление физических и химических свойств простых веществ. Сопоставление строения и свойств однотипных соединений в ряду Э(IV) - Э(III) - Э(II). Комплексные соединения. Разделение соединений циркония и гафния. Диаграмма ВЭ-СО для соединений титана. Аква- и гидроксокомплексы элементов I А, II A, III А и IV Б подгрупп. Перекисные соединения титана. Применение соединений титана, циркония и гафния

Общая характеристика В подгруппу титана входят элементы побочной подгруппы IV группы — титан, цирконий, гафний и резерфордий. Металлические свойства выражены у этих элементов сильнее, чем у металлов главной подгруппы четвертой группы — олова и свинца. Атомы элементов подгруппы титана имеют на наружном слое по два электрона, а на втором — по 10 электронов, из которых два — на s-подуровне. Поэтому наиболее характерная степень окисления металлов подгруппы титана равна +4. Ti 3 d 24 s 2 Zr 4 d 25 s 2 Hf 4 f 145 d 26 s 2

Первые три элемента данной подгруппы находятся в природе в заметных количествах. Они относятся к тугоплавким металлам. Последний представитель — резерфордий — радиоактивный элемент. У него нет стабильных изотопов. Его физические и химические свойства не изучены. Все три элемента подгруппы относятся к истинным металлам, проявляют хорошую электропроводность, обладают положительным электродным потенциалом, образуют типичные соли. Металличность в подгруппе несколько возрастает от титана к гафнию, химическая связь в их галогенидах и некоторых других солях типично ковалентная. Они могут проявлять также степень окисления II и III, но из этих состояний легко окисляются до степени окисления IV.

Титан является кайносимметричным элементом, его 3 d-электроны значительно прочнее связаны с атомным ядром. Поэтому 3 -й и 4 -й потенциалы ионизации титана немного превосходят таковые его гомологов, именно поэтому титан проявляет низшие степени окисления. Цирконий и гафний функционируют в характерной степени окисления +4, а низшие степени окисления нестабильны. В этой группе происходит усиление химической благородности металлов с увеличением атомного номера элемента. В главных подгруппах и в подгруппе скандия сверху вниз нарастают металлические свойства, а начиная именно с подгруппы титана наблюдается обратная закономерность. Это связано с тем, что между IIIВ- и IVВ-группами вклиниваются семейства f-элементов. При этом валентные 6 s-электроны тяжелых элементов подгрупп титана, ванадия и т. д, следующих за лантаноидами, обнаруживают эффект проникновения сквозь двойной слой из 5 d- и 4 f-электронов. Этим обусловлено ослабление металлических свойств гафния, тантала, вольфрама и т. д. На этой особенности основана интерпретация закономерностей изменения степеней окисления, кислотно-основных и окислительно-восстановительных свойств в группах d-элементов.

Металлохимия элементов подгруппы титана Титан, цирконий и гафний образуют непрерывные твердые растворы друг с другом в обеих модификациях. Тройная система Ti-Zr-Hf является единственным примером системы, в которой реализуются два вида непрерывных твердых трехкомпонентных растворов в двух модификациях. По мере увеличения различия в электронной конфигурации атомов растворимость элементов в титане и его аналогах уменьшается и появляется возможность образования промежуточных фаз с металлическими свойствами. Например, рассматривая системы титана с элементами 3 d-ряда, замечаем, что в первых трех системах (Ti-Sc, Ti-V, Ti-Cr) наблюдается полная взаимная растворимость при высоких температурах (β-Ti). Растворимость последующих элементов в β-титане непрерывно уменьшается (Mn – 27, Fe – 22, Co – 14, Ni – 13, Cu – 13 ат. долей, %). Для циркония и гафния характерны те же закономерности. Благодаря металлохимии титан и его аналоги обладают способностью сильно поглощать водород.

Т. к атомные радиусы углерода и азота больше, чем водорода, то и температуры плавления больше, чем температуры плавления самих металлов. • Ti Zr Hf • ЭС, °С 3150 3530 3890 • ЭN, °С 3205 2980 3300
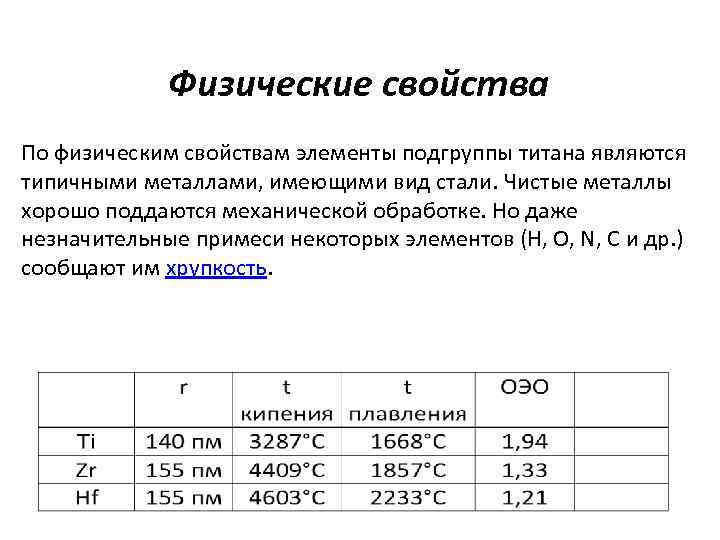
Физические свойства По физическим свойствам элементы подгруппы титана являются типичными металлами, имеющими вид стали. Чистые металлы хорошо поддаются механической обработке. Но даже незначительные примеси некоторых элементов (Н, О, N, C и др. ) сообщают им хрупкость.

При обычных условиях они кристаллизуются в ГПУструктуре, с повышением температуры увеличивается энтропия и происходит перестройка в более рыхлую структуру ОЦК. Высокие температуры плавления этой подгруппы свидетельствует о металлоковалентном (а не чисто металлическом) характере связей в кристаллах. При этом температура плавления в ряду Ti-Zr-Hf Возрастает в противоположность закономерности, наблюдающейся в главной подгруппе ( в ряду C-Si-Ge-Sn. Pb)

Титан (Titanium).

Титан (Titanium). Титан лёгкий металл серебристо-белого цвета, очень распространен в природе, встречается в минералах ильменит (Fe. Ti. O 3) и рутил (Ti. O 2). Значительные количества титана содержат также некоторые железные руды, в частности уральские титаномагнетиты. При обычной температуре покрывается защитной пассивирующей плёнкой оксида Ti. O 2. Существует в двух кристаллических модификациях: α-Ti с гексагональной плотноупакованной решёткой, β-Ti с кубической объёмно-центрированной упаковкой, температура полиморфного превращения α↔β 883 °C.

Все титанаты малорастворимы в воде. Оксид Титана (IV), титановые кислоты (осадки), а также титанаты растворяются в серной кислоте с образованием растворов, содержащих титанилсульфат Ti. OSO 4. При разбавлении и нагревании растворов в результате гидролиза осаждается Н 2 Тi. O 3, из которой получают оксид Титана (IV). При добавлении перекиси водорода в кислые растворы, содержащие соединения Ti (IV), образуются перекисные (надтитановые) кислоты состава Н 4 Тi. O 5 и H 4 Ti. O 8 и соответствующие им соли; эти соединения окрашены в желтый или оранжевокрасный цвет (в зависимости от концентрации Титана), что используется для аналитического определения Титана.

Химические свойства Ti Устойчив к коррозии благодаря оксидной плёнке, но при измельчении в порошок, а также в тонкой стружке или проволоке титан пирофорен. Титан устойчив к разбавленным растворам многих кислот и щелочей (кроме HF, H 3 PO 4 и концентрированной H 2 SO 4). 2 Ti + 4 H 2 SO 4 = Ti 2(SO 4)4 + 4 H 2 Легко реагирует даже со слабыми кислотами в присутствии комплексообразователей, например, с плавиковой кислотой HF он взаимодействует благодаря образованию комплексного аниона [Ti. F 6]2− 3 Ti + 18 НF + 4 HNO 3 = 3 H 2[Ti. F 6] + 4 NO + 8 H 2 O При нагревании на воздухе до 1200 °C Ti загорается с образованием Ti. O 2 Ti + O 2 = Ti. O 2

В обычных условиях титан мало активен, но при высокой температуре легко соединяется с галогенами, кислородом, серой, азотом, кремнием, водородом. . 3 Ti + 4 HNO 3 + H 2 O= 3 H 2 Ti. O 3 + 4 NO 2 Ti + H 2 = 2 Ti. H(t=400 -600°C) Ti + 2 Cl 2 = Ti. Cl 4 Ti + 2 Br 2 = Ti. Br 4 Ti + 2 S = Ti. S 2 Ti + N 2 = Ti. N (t>700°C) 3 Ti + 2 N 2 = Ti 3 N 4 Ti + C = Ti. C Ti + В = Ti. В

Получение Ti магнийтермический метод: Ti. Cl 4 + 2 Mg = Ti + 2 Mg. Cl 2 Магнийтермический метод позволяет создать крупное промышленное производство Титана с замкнутым технологическим циклом, так как образующийся при восстановлении побочный продукт - хлорид магния направляется на электролиз для получения магния и хлора.

Применение Ti Основная часть Титана расходуется на нужды авиационной и ракетной техники и морского судостроения. Сплавы Титана с железом, известные под названием "ферротитан" (20 -50% Титана), в металлургии качественных сталей и специальных сплавов служат легирующей добавкой и раскислителем. Технический Титан идет на изготовление емкостей, химические реакторов, трубопроводов, арматуры, насосов и других изделий, работающих в агрессивных средах, например, в химическом машиностроении.

Часы из титанового сплава Титановый памятник Гагарину на Ленинском проспекте в Москве

Ti. O 2 устойчивый, тугоплавкий оксид, мало растворим в воде и в разбавленных растворах кислот и щелочей. Получение: Ti + O 2 = Ti. O 2 (t=1200°С) Х. С: 6 Тi. O 2 = О 2 + 2 Тi 3 O 5 (Ti. O 2·Ti 2 O 3) синий цвет, t>2200°С Ti. O 2 + 2 Na. OH = Na 2 Ti. O 3(метатитанат натрия) +H 2 O Ti. O 2 + 2 Cl 2 = Ti. Cl 4 + 2 CO 2 Ti. O 2 + H 2 = Ti 2 O 3 + H 2 O Применение: применяется при изготовлении тугоплавких стёкол, входит в состав эмалей, глазурей и фарфоровой массы

Оксиды Ti. O 2 -943, 5 Zr. O 2 -1080, 3 Hf. O 2 -1135, 9 ΔH 298°, к. Дж/моль

Ti. Cl 4 - газ При конденсации образуется жидкость, похожая на Si. Cl 4, но имеет более высокую температуру кипения, что объясняется различием в строении молекул (у Si. Cl 4 тетраэдрическая, а у Ti. Cl 4 искаженная структура). Ti. Cl 4 + 4 HF = Ti. F 4 + 4 HCl Ti. Cl 4 + 4 Na. OH = Ti(OH)4 + 4 Na. Cl Среди других галогенидов известны Ti. I 2 , Ti. I 3, Ti. I 4 Ti. Cl 4 + H 2 = 2 Ti. Cl 3 + 2 HCl Получение: Ti. O 2 + 2 Cl 2 = Ti. Cl 4 + O 2 (при повышенных температурах в присутствии углерода) Ti(OH)4 – амфотерный гидроксид. При переходе к Zr(OH)4 и Hf(OH)4 основные свойства усиливаются. Эти соединения имеют переменный состав ЭО 2*х. Н 2 О. Не взаимодействуют с концентрированными растворами щелочей, т. к кислотные свойства выражены очень слабо. 2 Ti(OH)3 + O 2 + H 2 O = 2 Ti(OH)4 + H 2 O 2 Сульфиды: Ti. Cl 4 + H 2 S = Ti. S + 4 HCl (на холоду) Ti. Cl 4 + 2 H 2 S = Ti. S 2 + 4 HCl (при нагревании)

Некоторые свойства галогенидов титана : Теплота образования, Цвет t плавления, °С к. Дж/моль Ti. F 4 1643 бесцв. -23 Ti. Cl 4 803 бесцв. +39 Ti. Br 4 681 жёлт. +159 Ti. I 4 510 тёмно-красн. • t кипения, °С 283 136 231 377

Цирконий (Zirconium)

Цирконий (Zirconium) блестящий металл серебристо-серого цвета. Обладает высокой пластичностью, устойчив к коррозии. Существует в двух кристаллических модификациях: α-Zr с гексагональной решёткой типа магния, β-Zr с кубической объёмноцентрированной решёткой типа α-Fe, температура перехода α↔β 863 °C. Цирконий встречается главным образом в виде минералов цирконила (Zr. Si. O 4) и бадделеита (Zr. O 2

Х. С Цирконий устойчив в воде до 300 °C Zr + 2 H 2 O = Zr. O 2 + 2 H 2 При высоких t взаимодействует: Zr + 3 S = Zr. S 3 Zr + 3 Se = Zr. Se 3 Zr + 3 Te = Zr. Te 3 Zr + 2 Cl 2 = Zr. Cl 4 Zr + P = Zr. P Zr + 2 P = Zr. P 2(t>1000°C)

Нитраты для титана не характерны. Для циркония известен нитрат цирконила Zr. O(NO 3)2*2 H 2 O и особенно характерен нитрат дицирконила Zr 2 O 3(NO 3)2*2 H 2 O Характерны фосфаты - Zr 3(PO 4)4, пирофосфаты – Zr. P 2 O 7 ортосиликаты – Zr. Si. O 4

Zr. B 2 Диборид циркония Zr. B 2 — тугоплавкое соединение. Диборид циркония в промышленности синтезируют как из тетрахлорида циркония: Zr. Cl 4 + 2 BBr 3 + 5 H 2 = Zr. B 2 + 4 HCl + 6 HBr

Получение Хлоридный процесс: (t сублимации 331°C) Zr. O 2 + 2 Cl 2 = Zr. Cl 4 + 2 CO Zr. Cl 4 + 2 Mg = Zr + 2 Mg. Cl 2

Применение • цирконий применяется в ядерных реакторах, в виде сплавов применяется в качестве облицовки ядерных стержней (ТВЭЛ) в ядерных реакторах. Малые количества гафния и циркония применяются в сплавах обоих элементов для улучшения их свойств.

Гафний (Hafnium)

Гафний (Hafnium) — тяжёлый тугоплавкий серебристо-белый металл. Порошкообразный - темно-серый, почти черный, матовый. Ниже 1740°С устойчив α-Hf, решетка гексаген, типа Mg; выше 1740°С устойчив β-Hf, решетка кубическая типа Fе. Для гафния отдельные минералы пока не найдены. В виде примеси (порядка 1 атомн. %) он всегда содержится в рудах Zr.

• Соединения двухвалентного гафния • Hf. Br 2 — твёрдое вещество чёрного цвета, самовоспламеняющееся на воздухе. Разлагается при температуре 400 °C на гафний и тетрабромид гафния. Получают диспропорционированием трибромида гафния в вакууме при нагревании. • Hf(HPO 4)2 — белый осадок, растворимый в серной и фтороводородной кислотах. Получают обработкой растворов солей гафния (II) ортофосфорной кислотой. • Соединения трёхвалентного гафния • Hf. Br 3 — чёрно-синее твёрдое вещество. Диспропорционирует при 400 °C на дибромид и тетрабромид гафния. Получают восстановлением тетрабромида гафния при нагревании в атмосфере водорода или с металлическим алюминием.

• Соединения четырёхвалентного гафния Hf. O 2 — бесцветные моноклинные кристаллы (плотность — 9, 98 г/см³) или бесцветные тетрагональные кристаллы (плотность — 10, 47 г/см³). Последние имеют tпл 2900 °C, малорастворимы в воде, диамагнитны, обладают более осно вным характером, чем Zr. O 2 и обнаруживают каталитические свойства. Получают нагреванием металлического гафния в кислороде или прокаливанием гидроксида, диоксалата, дисульфата гафния. Hf(OH)4 — белый осадок, растворяющийся при добавлении щёлочей и пероксида водорода с образованием пероксогафниатов. Получают глубоким гидролизом солей четырёхвалентного гафния при нагревании или обработкой растворов солей гафния (IV) щёлочами.

Hf. F 4 — бесцветные кристаллы. tпл 1025 °C, плотность — 7, 13 г/см³. Растворим в воде. Получают термическим разложением соединения (NH 4)2[Hf. F 6] в токе азота при 300 °C. Hf. Cl 4 — белый порошок, сублимирующийся при 317 °C. tпл 432 °C. Получают действием хлора на металлический гафний, карбид гафния или смесь оксида гафния (II) с углем. Hf. Br 4 — бесцветные кристаллы. Сублимируются при 322 °C. tпл 420 °C. Получают действием паров брома на нагретую до 500 °C смесь оксида гафния (II) с углем. Hf. I 4 — жёлтые кристаллы. Сублимирует при 427 °C и термически диссоциирует при 1400 °C. Получается взаимодействием гафния с иодом при 300 °C.

Х. С. Hf + Br 2 = Hf. Br 2 2 Hf + 3 Br 2 = 2 Hf. Br 3 Hf + O 2 = Hf. O 2 (t) Hf + 2 Cl 2 = Hf. Cl 4 Hf + 2 F 2 = Hf. F 4 Hf + 2 Br 2 = Hf. Br 4 Hf + 2 I 2 = Hf. I 4 Известны фосфаты гафния – Hf 3(PO 4)4 пирофосфаты - Hf. P 2 O 7 ортосиликаты - Hf. Si. O 4

Получение Среднее содержание гафния в земной коре около 4 г/т. Ввиду отсутствия у гафния собственных минералов и постоянного сопутствия его цирконию, его получают путём переработки циркониевых руд, где он содержится в количестве 2, 5 % от веса циркония (циркон содержит 4 % Hf. O 2, бадделеит 4 — 6 % Hf. O 2).

Применение основное применение - производство сплавов для аэрокосмической техники, атомная промышленность. А также в атомной технике, в оптике, используется для производства высококачественных многослойных рентгеновских зеркал.
![Комплексные соединения Ti. Cl 4 + 4 SO 3 = [Ti(SO 4)2] + 2 Комплексные соединения Ti. Cl 4 + 4 SO 3 = [Ti(SO 4)2] + 2](https://present5.com/presentation/3/26498445_93977330.pdf-img/26498445_93977330.pdf-36.jpg)
Комплексные соединения Ti. Cl 4 + 4 SO 3 = [Ti(SO 4)2] + 2 SO 2 Cl 2 (нейтральный комплекс) аква-комплекс титана(III) [Ti(H 2 O)6]3+ ЭO 2 + 6 HF = H 2[ЭF 6] + 2 H 2 O или ЭO 2 + 3 H 2 C 2 O 4 = H 2[Э(C 2 O 4)3] + 2 H 2 O Э + 6 HF = H 2[ЭF 6] + 2 H 2 или Э + 3 H 2 C 2 O 4 = H 2[Э(C 2 O 4)3] + 2 H 2 3 Э + 4 HNO 3 + 18 HCl = 3 H 2[ЭCl 6] + 4 NO + 8 H 2 O ок-ль источник лигандов

Применение металлов • Практическое значение Ti и Zr особенно велико для металлургии. Присадка титана придает стали твердость и эластичность, а присадка циркония сильно повышает ее твердость и вязкость. За последнее время стало быстро развиваться использование титана в самолетостроении, а циркония – при сооружении ядерных реакторов. Соединения обоих элементов находят применение в различных отраслях промышленности. Гафний и его соединения пока почти не используются в металлургии.
Подгруппа титана1.ppt