 Подготовка к РКМ 8 класс
Подготовка к РКМ 8 класс
 1. Классифицируйте вещества: 1) SO 2 2) Mg(OH)2 3) HNO 3 4) Na. NO 3 5) H 3 PO 4 6) Ca. O 7) Na 2 O 8) Cu 9) Cl 2 10) Fe. Cl 3 11) Na. OH 12) HCl 13) H 2 SO 4 14) Ca. CO 3
1. Классифицируйте вещества: 1) SO 2 2) Mg(OH)2 3) HNO 3 4) Na. NO 3 5) H 3 PO 4 6) Ca. O 7) Na 2 O 8) Cu 9) Cl 2 10) Fe. Cl 3 11) Na. OH 12) HCl 13) H 2 SO 4 14) Ca. CO 3
 2. Запишите уравнения реакций: С какими из выше перечисленных веществ будет реагировать раствор серной кислоты? Б) С какими из выше перечисленных веществ будет реагировать раствор гидроксида натрия ? А)
2. Запишите уравнения реакций: С какими из выше перечисленных веществ будет реагировать раствор серной кислоты? Б) С какими из выше перечисленных веществ будет реагировать раствор гидроксида натрия ? А)
 3. Запишите уравнения возможных реакций: 1) Оксид калия + вода 2) Нитрат магния + гидроксид натрия 3) Медь + серная кислота 4) Цинк + соляная кислота 5) Карбонат натрия + азотная кислота 6) Хлорид натрия + гидроксид калия 7) Серная кислота + оксид меди (ll)
3. Запишите уравнения возможных реакций: 1) Оксид калия + вода 2) Нитрат магния + гидроксид натрия 3) Медь + серная кислота 4) Цинк + соляная кислота 5) Карбонат натрия + азотная кислота 6) Хлорид натрия + гидроксид калия 7) Серная кислота + оксид меди (ll)
 4. Задача. Определите массу соли, полученной при взаимодействии 60 г гидроксида натрия с углекислым газом.
4. Задача. Определите массу соли, полученной при взаимодействии 60 г гидроксида натрия с углекислым газом.
 5. Определите концентрацию раствора, полученного при растворении 25 г соли в 155 г воды.
5. Определите концентрацию раствора, полученного при растворении 25 г соли в 155 г воды.
 6. В растворе массой 240 г содержится 80 г соли. Определите концентрацию данного раствора.
6. В растворе массой 240 г содержится 80 г соли. Определите концентрацию данного раствора.
 7. 1) Как изменяются металлические свойства в ряду элементов: А) Mg Al Si Б) Mg Ca Sr В) N B Li 2) В ряду элементов : S O F А) увеличивается число валентных электронов Б) увеличивается число электронных уровней В) увеличиваются неметаллические свойства Г) увеличивается радиус атомов
7. 1) Как изменяются металлические свойства в ряду элементов: А) Mg Al Si Б) Mg Ca Sr В) N B Li 2) В ряду элементов : S O F А) увеличивается число валентных электронов Б) увеличивается число электронных уровней В) увеличиваются неметаллические свойства Г) увеличивается радиус атомов
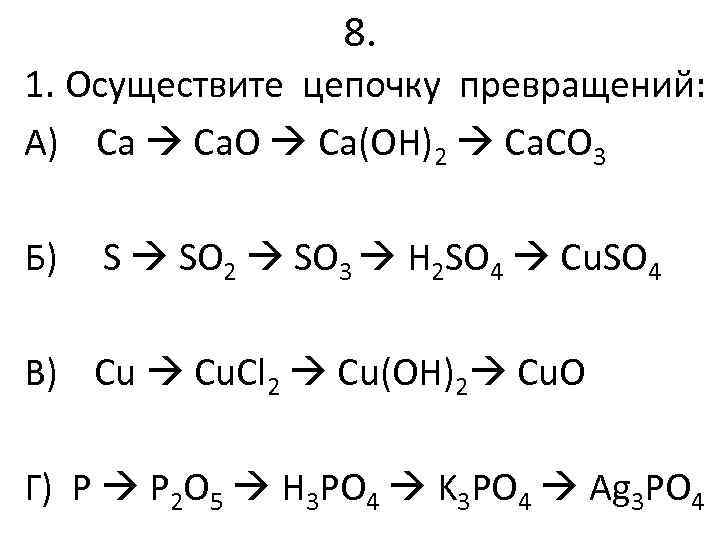 8. 1. Осуществите цепочку превращений: А) Ca Ca. O Ca(OH)2 Ca. CO 3 Б) S SO 2 SO 3 H 2 SO 4 Cu. SO 4 В) Cu Cu. Cl 2 Cu(OH)2 Cu. O Г) P P 2 O 5 H 3 PO 4 K 3 PO 4 Ag 3 PO 4
8. 1. Осуществите цепочку превращений: А) Ca Ca. O Ca(OH)2 Ca. CO 3 Б) S SO 2 SO 3 H 2 SO 4 Cu. SO 4 В) Cu Cu. Cl 2 Cu(OH)2 Cu. O Г) P P 2 O 5 H 3 PO 4 K 3 PO 4 Ag 3 PO 4