подготовка к к.р. 9-2.pptx
- Количество слайдов: 19

Подготовка к контрольной работе по теме «Металлы» 9 класс ГБОУ СОШ № 365 Фрунзенского района Санкт – Петербурга учитель химии Солощева Н. В.

Уважаемые ребята! У Вас есть возможность хорошо подготовиться к контрольной работе. Вы можете выполнить предложенные задания и узнать правильный ответ по щелчку мыши. УДАЧИ!!!

Часть А Тестовые задания с выбором ответа

1. Электронная формула атома магния А. 1 s 22 p 63 s 2 Б. 1 s 22 s 2 В. 1 s 22 s 1 Г. 1 s 22 p 1

2. Электронная формула внешнего энергетического уровня атомов элементов главной подгруппы III группы Периодической системы. А. ns 2 np 2 Б. ns 2 np 1 В. ns 2 Г. ns 1

3. Тип химической связи в простом веществе магнии: А. Ионная Б. Ковалентная неполярная В. Ковалентная полярная Г. Металлическая

4. Простое вещество с наиболее ярко выраженными металлическими свойствами: А. Натрий Б. Рубидий В. Калий Г. Литий

5. Радиус атомов элементов 2 -го периода с увеличением заряда ядра от щелочного металла к галогену: А. Изменяется периодически Б. Не изменяется В. Уменьшается Г. Увеличивается

6. Атом кальция отличается от иона кальция: А. Зарядом ядра Б. Радиусом частицы В. Числом протонов Г. Числом нейтронов

7. Наиболее энергично взаимодействует с водой: А. Натрий Б. Литий В. Калий Г. Рубидий

8. С разбавленной серной кислотой не взаимодействует: А. Платина Б. Железо В. Магний Г. Никель

9. Гидроксид цинка взаимодействует с веществом, формула которого: А. KOH Б. Ca. O В. KNO 3 Г. Ba. SO 4

10. Ряд, все вещества в котором взаимодействуют с алюминием: А. HCl, H 2 SO 4, Na. OH Б. Ca. O, HCl, HNO 3 В. KOH, Mg. O, H 3 PO 4 Г. H 2, O 2, CO 2

Часть Б Задания со свободным ответом

11. Предложите три способа получения гидроксида натрия. 2 Na + 2 H 2 O = 2 Na. OH + H 2 Na 2 O + H 2 O = 2 Na. OH электролиз Na. Cl + H 2 O = 2 Na. OH + H 2 + Cl 2
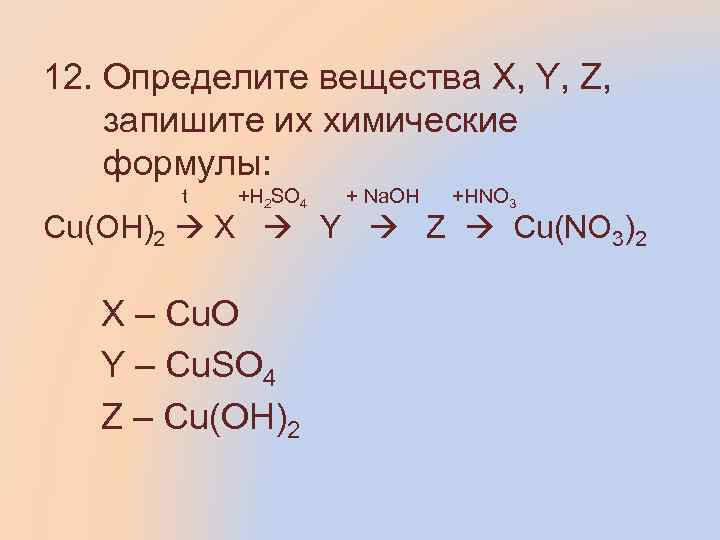
12. Определите вещества X, Y, Z, запишите их химические формулы: t +H 2 SO 4 + Na. OH +HNO 3 Cu(OH)2 X Y Z Cu(NO 3)2 X – Cu. O Y – Cu. SO 4 Z – Cu(OH)2

13. Как, используя любые реактивы (вещества) и кальций, получить оксид, основание, соль? Составьте уравнения реакций в молекулярном виде. 2 Ca + O 2 = 2 Ca. O Ca + 2 H 2 O = Ca(OH)2 + H 2 Ca + Cl 2 = Ca. Cl 2

15. Рассчитайте массу железа, которую можно получить из 120 г оксида железа (III). Fe 2 O 3 + 3 H 2 = 2 Fe + 3 H 2 O 84 г

подготовка к к.р. 9-2.pptx