Подготовка к к.р. - 2.ppt
- Количество слайдов: 15

Подготовка к контрольной работе № 2
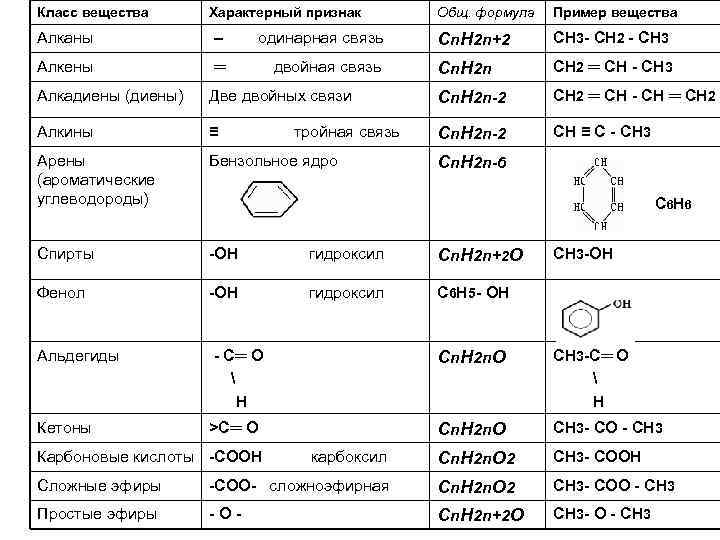
Класс вещества Характерный признак Общ. формула Пример вещества Cn. H 2 n+2 СН 3 - СН 2 - СН 3 Cn. H 2 n СН 2 ═ СН - СН 3 Алканы – одинарная связь Алкены ═ двойная связь Алкадиены (диены) Две двойных связи Cn. H 2 n-2 СН 2 ═ СН - СН ═ СН 2 Алкины ≡ Cn. H 2 n-2 СН ≡ С - СН 3 Арены (ароматические углеводороды) Бензольное ядро Спирты -ОН гидроксил Cn. H 2 n+2 О Фенол -ОН гидроксил С 6 Н 5 - ОН Альдегиды - С═ О Н Cn. H 2 n. О СН 3 -С═ О Н Кетоны >С═ О Cn. H 2 n. О СН 3 - СО - СН 3 карбоксил Cn. H 2 n. О 2 СН 3 - СООН Сложные эфиры -СОО- сложноэфирная Cn. H 2 n. О 2 СН 3 - СОО - СН 3 Простые эфиры -О- Cn. H 2 n+2 О СН 3 - О - СН 3 тройная связь Cn. H 2 n-6 С 6 Н 6 Карбоновые кислоты -СООН СН 3 -ОН

• Гомологи – вещества одного класса (схожее строение и свойства), различающиеся по составу на одну или несколько групп СН 2: СН 3 –СН 3 и СН 3 –СН 2 – СН 3 • Изомеры – вещества одинакового состава, но разного строения, отличающиеся по свойствам: СН 3 –СН 2 – ОН СН 3 –СН 2 –О – СН 3 У этих двух веществ одинаковый состав С 3 Н 8 О
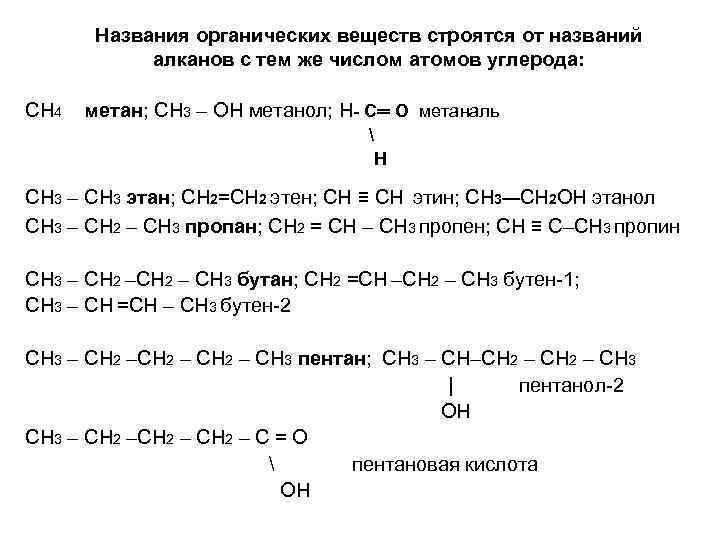
Названия органических веществ строятся от названий алканов с тем же числом атомов углерода: СН 4 метан; СН 3 – ОН метанол; Н- С═ О метаналь Н СН 3 – СН 3 этан; CH 2=CH 2 этен; CH ≡ CH этин; CH 3—CH 2 OH этанол СН 3 – СН 2 – СН 3 пропан; СН 2 = СН – СН 3 пропен; СН ≡ С–СН 3 пропин СН 3 – СН 2 – СН 3 бутан; СН 2 =СН –СН 2 – СН 3 бутен-1; СН 3 – СН =СН – СН 3 бутен-2 СН 3 – СН 2 – СН 3 пентан; СН 3 – СН–СН 2 – СН 3 | пентанол-2 ОН СН 3 – СН 2 – С = О пентановая кислота ОН
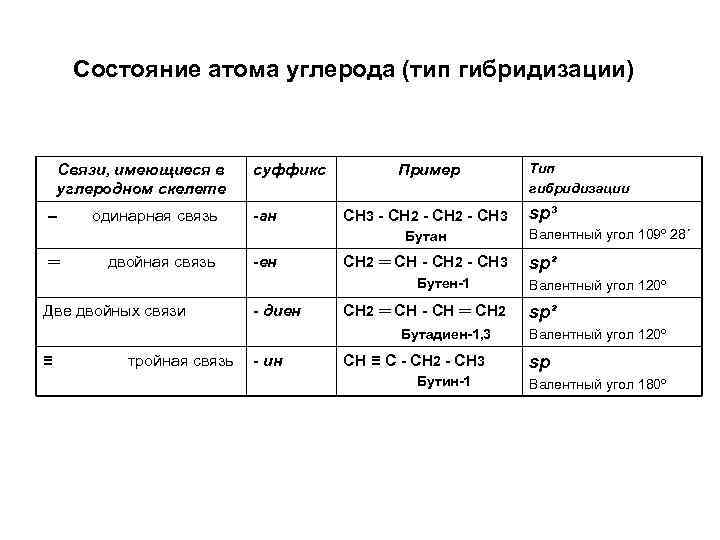
Состояние атома углерода (тип гибридизации) Связи, имеющиеся в углеродном скелете – одинарная связь суффикс -ан Пример СН 3 - СН 2 - СН 3 Бутан ═ двойная связь -ен СН 2 ═ СН - СН 2 - СН 3 Бутен-1 Две двойных связи - диен СН 2 ═ СН - СН ═ СН 2 Бутадиен-1, 3 ≡ тройная связь - ин СН ≡ С - СН 2 - СН 3 Бутин-1 Тип гибридизации sp³ Валентный угол 109º 28´ sp² Валентный угол 120º sp Валентный угол 180º
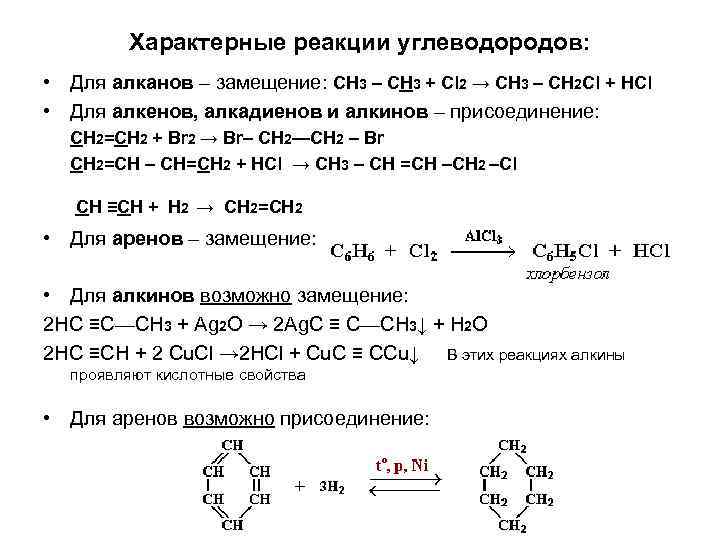
Характерные реакции углеводородов: • Для алканов – замещение: CH 3 – CH 3 + Cl 2 → CH 3 – CH 2 Cl + HCl • Для алкенов, алкадиенов и алкинов – присоединение: CH 2=CH 2 + Br 2 → Br– CH 2—CH 2 – Br CH 2=CH – CH=CH 2 + HCl → CH 3 – CH =CH –CH 2 –Cl CH ≡CH + Н 2 → CH 2=CH 2 • Для аренов – замещение: • Для алкинов возможно замещение: 2 HC ≡C—CH 3 + Ag 2 O → 2 Ag. C ≡ C—CH 3↓ + H 2 O 2 HC ≡CH + 2 Cu. Cl → 2 HCl + Cu. C ≡ CCu↓ В этих реакциях алкины проявляют кислотные свойства • Для аренов возможно присоединение:
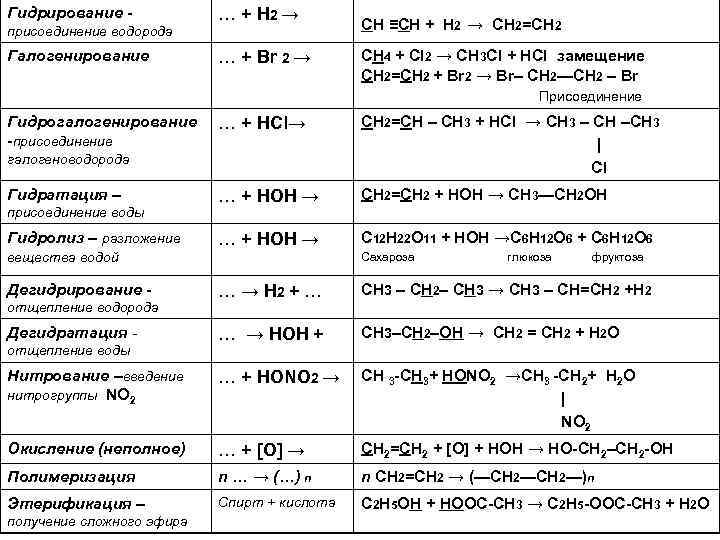
Гидрирование присоединение водорода Галогенирование … + Н 2 → … + Br 2 → CH ≡CH + Н 2 → CH 2=CH 2 CH 4 + Cl 2 → CH 3 Cl + HCl замещение CH 2=CH 2 + Br 2 → Br– CH 2—CH 2 – Br Присоединение Гидрогалогенирование -присоединение … + НCl→ CH 2=CH – CH 3 + HCl → CH 3 – CH –CH 3 | Cl … + НОН → CH 2=CH 2 + HOН → CH 3—CH 2 OH … + НОН → С 12 Н 22 О 11 + HOН →С 6 Н 12 О 6 + С 6 Н 12 О 6 галогеноводорода Гидратация – присоединение воды Гидролиз – разложение вещества водой Дегидрирование - Сахароза глюкоза фруктоза … → Н 2 + … CH 3 – CH 2– CH 3 → CH 3 – CH=CH 2 +H 2 … → НОН + CH 3–CH 2–OH → СН 2 = СН 2 + H 2 O Нитрование –введение нитрогруппы NO 2 … + НОNO 2 → CH 3 -CH 3+ HОNO 2 →CH 3 -CH 2+ H 2 O | NO 2 Окисление (неполное) … + [О] → CH 2=CH 2 + [O] + HOН → HO-CH 2–CH 2 -OH Полимеризация n … → (…) n n CH 2=CH 2 → (—CH 2—)n Этерификация – Спирт + кислота C 2 H 5 OH + НООС-СН 3 → С 2 Н 5 -ООС-СН 3 + H 2 O отщепление водорода Дегидратация отщепление воды получение сложного эфира

• Именные реакции: Реакция Кучерова – получение уксусного альдегида (ацетальдегида) гидратацией ацетилена (этина): CH ≡ CH + HOН → CH 2=CH → CH 3 —C =O │ изомеризация ОН H Реакция Вюрца – получение алканов из галогенпроизводных: СН 3 - Сl + 2 Na + Cl -CH 3 → 2 Na. Cl + СН 3 - CH 3 • Правило Марковникова – присоединении молекул галогеноводородов и других водородсодержащих веществ несимметричного строения к молекулам непредельных углеводородов водород присоединяется к наиболее гидрогенизированному атому углерода: CH 2=CH – CH 3 + HCl → CH 3 – CH –CH 3 | Cl

Первичный атом углерода связан с одним атомом углерода: СН 3–СН 2 - СН 3 У первичного спирта группа ОН связана с первичным атомом «С» : СН 3–СН 2 - СН 2 - ОН • Вторичный атом углерода связан еще с двумя : СН 3 – СН 2 - СН 3 у вторичного спирта группа ОН связана со вторичным атомом «С» : СН 3 – СН- СН 3 | ОН Третичный атом углерода связан еще с с тремя: СН 3 – СН - СН 3 | СН 3 У третичного спирта группа ОН связана с третичным атомом углерода: СН 3 | СН 3 – С - СН 3 | ОН Четвертичный атом углерода связан еще с четырьмя : СН 3 | СН 3 – С - СН 3 | СН 3

Кислотные свойства Объясняются наличием подвижного атома водорода и проявляются в реакциях замены атома водорода на атом металла: 2 HC ≡C—CH 3 + Ag 2 O → 2 Ag. C ≡ C—CH 3↓ + H 2 O 2 HC ≡CH + 2 Cu. Cl → 2 HCl + Cu. C ≡ CCu↓ В этих реакциях алкины проявляют кислотные свойства Спирты и фенолы также проявляют кислотные свойства: • C 2 H 5 OH +Na→ С 2 Н 5 -ОNa + H 2 • C 6 H 5 OH +Na→ С 2 Н 5 -ОNa + H 2 У карбоновых кислот такие свойства проявляются во взаимодействии с металлами, гидроксидами металлов, солями: 2 C 2 H 5 СOOH + 2 Na→ 2 С 2 Н 5 -COОNa + H 2 C 2 H 5 СOOH +Na. OH→ С 2 Н 5 -COОNa + H 2 O 2 C 2 H 5 СOOH +Na 2 CO 3→ 2 С 2 Н 5 -COОNa + H 2 O + CO 2
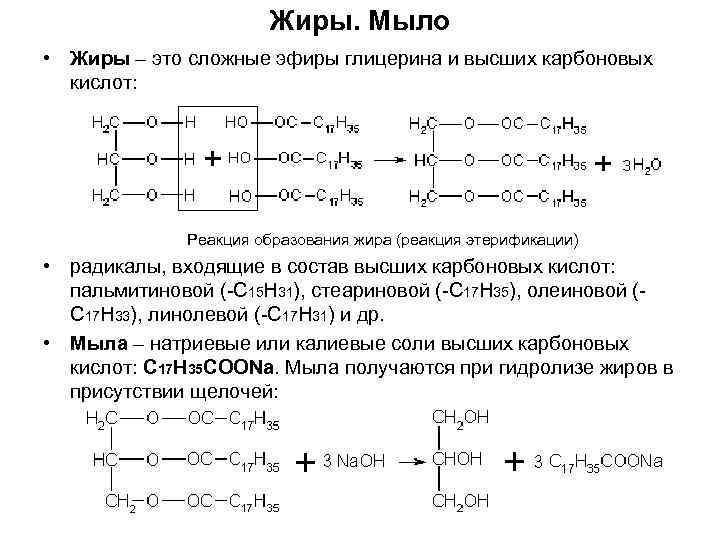
Жиры. Мыло • Жиры – это сложные эфиры глицерина и высших карбоновых кислот: Реакция образования жира (реакция этерификации) • радикалы, входящие в состав высших карбоновых кислот: пальмитиновой (-С 15 Н 31), стеариновой (-С 17 Н 35), олеиновой (С 17 Н 33), линолевой (-С 17 Н 31) и др. • Мыла – натриевые или калиевые соли высших карбоновых кислот: C 17 H 35 COONa. Мыла получаются при гидролизе жиров в присутствии щелочей:
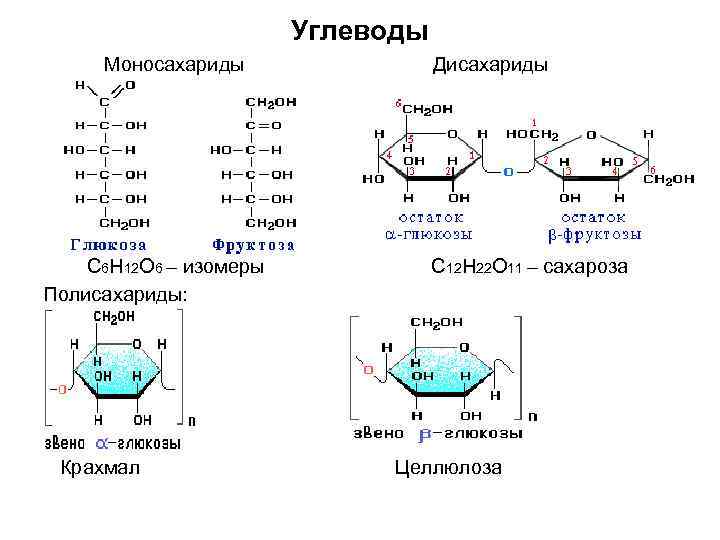
Углеводы Моносахариды С 6 Н 12 О 6 – изомеры Полисахариды: Крахмал Дисахариды С 12 Н 22 О 11 – сахароза Целлюлоза

Качественные реакции • На алкены, алкины, алкадиены – обесцвечивание бромной воды: CH 2=CH 2 + Br 2 → Br– CH 2—CH 2 – Br – обесцвечивание раствора перманганата калия: CH 2=CH 2 + [O] + HOН → HO-CH 2–CH 2 -OH На многоатомные спирты – растворение голубого осадка Cu(OH)2 и образование синего раствора CH 2 -OH | СН-ОН + | СН 2 - ОН СН 2 -О НО | Cu → CH – O / НО/ | СН 2 - ОН + 2 H 2 O На фенол – образование фиолетовой окраски при взаимодействии с Fe. Cl 3 : С 6 Н 5 ОН + Fe. Cl 3 →(С 6 Н 5 О)3 Fe + 3 НCl – с бромной водой (раствор обесцвечивается и выпадает белый осадок): С 6 Н 5 ОН + 3 Br 2 → С 6 Н 2 Вr 3(ОН) +3 НBr
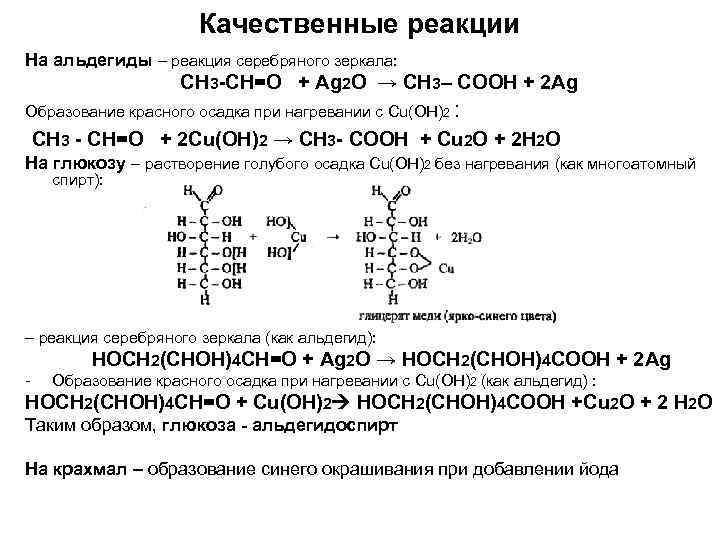
Качественные реакции На альдегиды – реакция серебряного зеркала: СН 3 -СН=О + Ag 2 O → СН 3– СОOH + 2 Ag Образование красного осадка при нагревании с Cu(OH)2 : СН 3 - СН=О + 2 Сu(ОН)2 → СН 3 - СООН + Cu 2 O + 2 Н 2 O На глюкозу – растворение голубого осадка Cu(OH)2 без нагревания (как многоатомный спирт): – реакция серебряного зеркала (как альдегид): HOCH 2(CHOH)4 CH=O + Ag 2 O → HOCH 2(CHOH)4 COOH + 2 Ag - Образование красного осадка при нагревании с Cu(OH)2 (как альдегид) : НОСН 2(СНОН)4 СН=О + Cu(OH)2 НОСН 2(СНОН)4 СOОН +Cu 2 O + 2 H 2 O Таким образом, глюкоза - альдегидоспирт На крахмал – образование синего окрашивания при добавлении йода

Полимеры: • Получение полиэтилена, полипропилена: n CH 2=CH 2 → (—CH 2—)n полиэтилен n CH 2=СН—CH 3 → n CH 2=СН → (—CH 2—CH—)n полипропилен │ │ CH 3 • Получение синтетических каучуков: n. CH 2=CH-CH=CH 2 → (-CH 2 -CH=CH-CH 2 -)n каучук бутадиеновый • • Природные полимеры – биополимеры (C 6 H 10 O 5)n– целлюлоза и крахмал Получение искусственных полимеров химической обработкой природных полимеров (биополимеров): [C 6 H 7 O 2(OH)3]n + 3 n. НОNО 2 →[C 6 H 7 O 2(ONO 2)3]n + 3 n. Н 2 О нитроцеллюлоза – сырье для производства целлулоида и пороха [C 6 H 7 O 2(OH)3]n + 3 n. СН 3 СООН → [C 6 H 7 O 2(OCOCH 3)3]n + 3 n. Н 2 О триацетат целлюлозы – сырье для производства искусственного волокна – ацетатного шелка
Подготовка к к.р. - 2.ppt