Подготовка к ЕГЭ (демо-версия 2011).ppt
- Количество слайдов: 94
 Подготовка к ЕГЭ по химии Демо-версия ЕГЭ-2011 Автор: Репетацких Дмитрий Николаевич Магнитогорск, 2011
Подготовка к ЕГЭ по химии Демо-версия ЕГЭ-2011 Автор: Репетацких Дмитрий Николаевич Магнитогорск, 2011
 Работа с материалом Для начала работы нажмите кнопку F 5 на клавиатуре или выберите показ слайдов на ленте сверху Для перемещения между слайдами используйте гиперссылки Для перемещения по слайду используйте либо стрелку вправо на клавиатуре, либо левую кнопку мыши, либо колесико прокрутки
Работа с материалом Для начала работы нажмите кнопку F 5 на клавиатуре или выберите показ слайдов на ленте сверху Для перемещения между слайдами используйте гиперссылки Для перемещения по слайду используйте либо стрелку вправо на клавиатуре, либо левую кнопку мыши, либо колесико прокрутки
 Инструкция Часть А состоит из 30 заданий. На каждое задание только 1 ответ правильный. Часть В состоит из 10 заданий. Ответом на задания B 1 -B 10 является последовательность 4 цифр, B 6 -B 8 – последовательность 3 цифр, B 9 -B 10 – число, включая запятые Часть С состоит из 3 заданий без вариантов ответа. Желаю успеха
Инструкция Часть А состоит из 30 заданий. На каждое задание только 1 ответ правильный. Часть В состоит из 10 заданий. Ответом на задания B 1 -B 10 является последовательность 4 цифр, B 6 -B 8 – последовательность 3 цифр, B 9 -B 10 – число, включая запятые Часть С состоит из 3 заданий без вариантов ответа. Желаю успеха
 А 1 А 11 А 21 В 1 А 2 А 12 А 22 В 2 А 3 А 13 А 23 В 3 А 4 А 14 А 24 В 4 А 5 А 15 А 25 В 5 А 6 А 16 А 26 В 6 А 7 А 17 А 27 В 7 А 8 А 18 А 28 В 8 А 9 А 19 А 29 В 9 А 10 А 20 А 30 В 10 С 1 С 2 С 3 С 4 С 5
А 1 А 11 А 21 В 1 А 2 А 12 А 22 В 2 А 3 А 13 А 23 В 3 А 4 А 14 А 24 В 4 А 5 А 15 А 25 В 5 А 6 А 16 А 26 В 6 А 7 А 17 А 27 В 7 А 8 А 18 А 28 В 8 А 9 А 19 А 29 В 9 А 10 А 20 А 30 В 10 С 1 С 2 С 3 С 4 С 5
 К выбору Следующее Задание A 1 задания задание А 1. Элемент, электронная конфигурация атома которого 1 s 22 p 63 s 23 p 2, образует водородное соединение 1) CH 4 2) Si. H 4 3) H 2 O 4) H 2 S К объяснению A 1
К выбору Следующее Задание A 1 задания задание А 1. Элемент, электронная конфигурация атома которого 1 s 22 p 63 s 23 p 2, образует водородное соединение 1) CH 4 2) Si. H 4 3) H 2 O 4) H 2 S К объяснению A 1
 К выбору Следующее Задание A 2 задания задание А 2. В каком ряду химические элементы расположены в порядке уменьшения их атомного радиуса? 1) Li → Be → B → C 2) Ar → Cl → S → P 3) Si → Al → Mg → Na 4) Ne → F → O → N К объяснению A 2
К выбору Следующее Задание A 2 задания задание А 2. В каком ряду химические элементы расположены в порядке уменьшения их атомного радиуса? 1) Li → Be → B → C 2) Ar → Cl → S → P 3) Si → Al → Mg → Na 4) Ne → F → O → N К объяснению A 2
 К выбору Следующее Задание A 3 задания задание А 3. Основные свойства наиболее выражены у оксида 1) бериллия 2) магния 3) алюминия 4) калия К объяснению A 3
К выбору Следующее Задание A 3 задания задание А 3. Основные свойства наиболее выражены у оксида 1) бериллия 2) магния 3) алюминия 4) калия К объяснению A 3
 К выбору Следующее Задание A 4 задания задание А 4. Соединения состава Na 2 ЭО 4 образует каждый из двух элементов: 1) сера и хлор 2) сера и хром 3) хром и азот 4) фосфор и хлор К объяснению A 4
К выбору Следующее Задание A 4 задания задание А 4. Соединения состава Na 2 ЭО 4 образует каждый из двух элементов: 1) сера и хлор 2) сера и хром 3) хром и азот 4) фосфор и хлор К объяснению A 4
 К выбору Следующее Задание A 5 задания задание А 5. Ковалентная неполярная связь характерна для каждого из двух веществ: 1) водорода и хлора 2) воды и алмаза 3) меди и азота 4) брома и метана К объяснению A 5
К выбору Следующее Задание A 5 задания задание А 5. Ковалентная неполярная связь характерна для каждого из двух веществ: 1) водорода и хлора 2) воды и алмаза 3) меди и азота 4) брома и метана К объяснению A 5
 К выбору Следующее Задание A 6 задания задание А 6. Азот проявляет степень окисления +3 в каждом из двух соединений: 1) N 2 O 3 и NH 3 2) NH 4 Cl и N 2 O 3) HNO 2 и N 2 H 4 4) Na. NO 2 и N 2 O 3 К объяснению A 6
К выбору Следующее Задание A 6 задания задание А 6. Азот проявляет степень окисления +3 в каждом из двух соединений: 1) N 2 O 3 и NH 3 2) NH 4 Cl и N 2 O 3) HNO 2 и N 2 H 4 4) Na. NO 2 и N 2 O 3 К объяснению A 6
 К выбору Следующее Задание A 7 задания задание А 7. Хлорид бария имеет кристаллическую решетку 1) атомную 2) металлическую 3) ионную 4) молекулярную К объяснению A 7
К выбору Следующее Задание A 7 задания задание А 7. Хлорид бария имеет кристаллическую решетку 1) атомную 2) металлическую 3) ионную 4) молекулярную К объяснению A 7
 К выбору Задание A 8 задания А 8. В перечне веществ: А) СH 4 Б) H 2 S В) СH 3 COOH Г) NH 3 Д) H 5 IO 6 Е) K 2 HPO 4 к классу кислот относятся 1) АБВ 2) БBД 3) БГД 4) ВДЕ К объяснению A 8 Следующее задание
К выбору Задание A 8 задания А 8. В перечне веществ: А) СH 4 Б) H 2 S В) СH 3 COOH Г) NH 3 Д) H 5 IO 6 Е) K 2 HPO 4 к классу кислот относятся 1) АБВ 2) БBД 3) БГД 4) ВДЕ К объяснению A 8 Следующее задание
 К выбору Следующее Задание A 9 задания задание А 9. Химическая реакция протекает между 1) Cu и Zn. Cl 2 (р-р) 2) Zn и Cu. SO 4 (р-р) 3) Fe и Al(NO 3)3 (р-р) 4) Ag и Fe. SO 4 (р-р) К объяснению A 9
К выбору Следующее Задание A 9 задания задание А 9. Химическая реакция протекает между 1) Cu и Zn. Cl 2 (р-р) 2) Zn и Cu. SO 4 (р-р) 3) Fe и Al(NO 3)3 (р-р) 4) Ag и Fe. SO 4 (р-р) К объяснению A 9
 К выбору Задание A 10 задания А 10. Оксид углерода (IV) реагирует с 1) гидроксидом кальция 2) хлоридом меди (II) 3) оксидом серы (VI) 4) оксидом хрома (VI) К объяснению A 10 Следующее задание
К выбору Задание A 10 задания А 10. Оксид углерода (IV) реагирует с 1) гидроксидом кальция 2) хлоридом меди (II) 3) оксидом серы (VI) 4) оксидом хрома (VI) К объяснению A 10 Следующее задание
 К выбору Следующее Задание A 11 задания задание А 11. Гидроксид алюминия при обычных условиях взаимодействует с каждым из двух веществ: 1) HCl и Na. NO 3 2) HNO 3 и Ba(OH)2 3) KOH и Na. Cl 4) Na. OH и Ca. CO 3 К объяснению A 11
К выбору Следующее Задание A 11 задания задание А 11. Гидроксид алюминия при обычных условиях взаимодействует с каждым из двух веществ: 1) HCl и Na. NO 3 2) HNO 3 и Ba(OH)2 3) KOH и Na. Cl 4) Na. OH и Ca. CO 3 К объяснению A 11
 К выбору Следующее Задание A 12 задания задание А 12. Раствор карбоната калия реагирует с 1) нитратом кальция 2) оксидом магния 3) оксидом углерода (II) 4) хлоридом натрия К объяснению A 12
К выбору Следующее Задание A 12 задания задание А 12. Раствор карбоната калия реагирует с 1) нитратом кальция 2) оксидом магния 3) оксидом углерода (II) 4) хлоридом натрия К объяснению A 12
 К выбору Задание A 13 задания А 13. В схеме превращений Fe 2 O 3 Fe Fe. SO 4 веществами «X» и «Y» являются: 1) X – H 2 и Y – H 2 SO 4(конц. ) 2) X – C и Y – Na 2 SO 4(р-р) 3) X – Cu и Y – H 2 SO 4(разб. ) 4) X – Al и Y – H 2 SO 4(разб. ) К объяснению A 13 Следующее задание
К выбору Задание A 13 задания А 13. В схеме превращений Fe 2 O 3 Fe Fe. SO 4 веществами «X» и «Y» являются: 1) X – H 2 и Y – H 2 SO 4(конц. ) 2) X – C и Y – Na 2 SO 4(р-р) 3) X – Cu и Y – H 2 SO 4(разб. ) 4) X – Al и Y – H 2 SO 4(разб. ) К объяснению A 13 Следующее задание
 К выбору Следующее Задание A 14 задания задание А 14. Структурная формула углеводорода, имеющего цис-, транс-изомеры 1) СН 2 = СН – СН 2 – СН 3 2) СН 3 – СН = СН – СН 3 3) СН 3 – СН = СН 2 4) СН 2 = СН 2 К объяснению A 14
К выбору Следующее Задание A 14 задания задание А 14. Структурная формула углеводорода, имеющего цис-, транс-изомеры 1) СН 2 = СН – СН 2 – СН 3 2) СН 3 – СН = СН – СН 3 3) СН 3 – СН = СН 2 4) СН 2 = СН 2 К объяснению A 14
 К выбору Следующее Задание A 15 задания задание А 15. С каждым из веществ: водой, бромоводородом, водородом – может реагировать 1) пропан 2) метанол 3) этан 4) бутен-1 К объяснению A 15
К выбору Следующее Задание A 15 задания задание А 15. С каждым из веществ: водой, бромоводородом, водородом – может реагировать 1) пропан 2) метанол 3) этан 4) бутен-1 К объяснению A 15
 К выбору Следующее Задание A 16 задания задание А 16. Верны ли следующие суждения о феноле? А. Фенол взаимодействует с бромной водой. Б. Фенол проявляет только основные свойства. 1) верно только А 2) верно только Б 3) верны оба суждения 4) оба суждения неверны К объяснению A 16
К выбору Следующее Задание A 16 задания задание А 16. Верны ли следующие суждения о феноле? А. Фенол взаимодействует с бромной водой. Б. Фенол проявляет только основные свойства. 1) верно только А 2) верно только Б 3) верны оба суждения 4) оба суждения неверны К объяснению A 16
 К выбору Следующее Задание A 17 задания задание А 17. С уксусной кислотой взаимодействует каждое из двух веществ: 1) Na. ОН и СО 2 2) Na. ОН и Na 2 СO 3 3) С 2 Н 4 и С 2 Н 5 ОН 4) CO и С 2 Н 5 ОН К объяснению A 17
К выбору Следующее Задание A 17 задания задание А 17. С уксусной кислотой взаимодействует каждое из двух веществ: 1) Na. ОН и СО 2 2) Na. ОН и Na 2 СO 3 3) С 2 Н 4 и С 2 Н 5 ОН 4) CO и С 2 Н 5 ОН К объяснению A 17
 К выбору Следующее Задание A 18 задания задание А 18. В одну стадию бутан можно получить из 1) бутанола-1 2) бутановой кислоты 3) бутена-1 4) бутанола-2 К объяснению A 18
К выбору Следующее Задание A 18 задания задание А 18. В одну стадию бутан можно получить из 1) бутанола-1 2) бутановой кислоты 3) бутена-1 4) бутанола-2 К объяснению A 18
 К выбору Следующее Задание A 19 задания задание А 19. Пентанол-1 образуется в результате взаимодействия 1) пентана с гидроксидом натрия 2) пентена-1 с водой 3) пентаналя с водородом 4) 1 -хлорпентана с гидроксидом меди (II) К объяснению A 19
К выбору Следующее Задание A 19 задания задание А 19. Пентанол-1 образуется в результате взаимодействия 1) пентана с гидроксидом натрия 2) пентена-1 с водой 3) пентаналя с водородом 4) 1 -хлорпентана с гидроксидом меди (II) К объяснению A 19
 К выбору Задание задания А 20. В схеме превращений CH 3 OH → X → HCOOH веществом «Х» является 1) CH 3 Cl 2) CH 3 CHO 3) H 3 C – O – CH 3 4) HCHO К объяснению A 20 Следующее задание
К выбору Задание задания А 20. В схеме превращений CH 3 OH → X → HCOOH веществом «Х» является 1) CH 3 Cl 2) CH 3 CHO 3) H 3 C – O – CH 3 4) HCHO К объяснению A 20 Следующее задание
 К выбору Следующее Задание A 21 задания задание А 21. Взаимодействие оксида серы (IV) с кислородом относится к реакциям 1) соединения, экзотермическим 2) замещения, экзотермическим 3) обмена, эндотермическим 4) соединения, эндотермическим К объяснению A 21
К выбору Следующее Задание A 21 задания задание А 21. Взаимодействие оксида серы (IV) с кислородом относится к реакциям 1) соединения, экзотермическим 2) замещения, экзотермическим 3) обмена, эндотермическим 4) соединения, эндотермическим К объяснению A 21
 К выбору Задание A 22 задания А 22. Увеличению скорости реакции 2 Fe + 3 Cl 2(г) = 2 Fe. Cl 3 способствует 1) понижение давления 2) уменьшение концентрации Cl 2 3) охлаждение системы 4) повышение температуры К объяснению A 22 Следующее задание
К выбору Задание A 22 задания А 22. Увеличению скорости реакции 2 Fe + 3 Cl 2(г) = 2 Fe. Cl 3 способствует 1) понижение давления 2) уменьшение концентрации Cl 2 3) охлаждение системы 4) повышение температуры К объяснению A 22 Следующее задание
 К выбору Следующее Задание A 23 задания задание А 23. Химическое равновесие в системе C 4 H 8(г) + H 2(г) C 4 H 10(г) + Q смещается в сторону исходных веществ в результате 1) увеличения концентрации водорода 2) повышения температуры 3) повышения давления 4) использования катализатора К объяснению A 23
К выбору Следующее Задание A 23 задания задание А 23. Химическое равновесие в системе C 4 H 8(г) + H 2(г) C 4 H 10(г) + Q смещается в сторону исходных веществ в результате 1) увеличения концентрации водорода 2) повышения температуры 3) повышения давления 4) использования катализатора К объяснению A 23
 К выбору Следующее Задание A 24 задания задание А 24. Наибольшее количество ионов образуется при электролитической диссоциации 1 моль 1) хлорида калия 2) нитрата железа (III) 3) сульфата алюминия 4) карбоната натрия К объяснению A 24
К выбору Следующее Задание A 24 задания задание А 24. Наибольшее количество ионов образуется при электролитической диссоциации 1 моль 1) хлорида калия 2) нитрата железа (III) 3) сульфата алюминия 4) карбоната натрия К объяснению A 24
 К выбору Следующее Задание A 25 задания задание А 25. Осадок образуется при взаимодействии растворов сульфата калия и 1) Na. OH 2) HCl 3) Ba(OH)2 4) NH 3 К объяснению A 25
К выбору Следующее Задание A 25 задания задание А 25. Осадок образуется при взаимодействии растворов сульфата калия и 1) Na. OH 2) HCl 3) Ba(OH)2 4) NH 3 К объяснению A 25
 К выбору Следующее Задание A 26 задания задание А 26. Одинаковую реакцию среды имеют растворы карбоната натрия и 1) нитрата бария 2) силиката калия 3) сульфата натрия 4) хлорида алюминия К объяснению A 26
К выбору Следующее Задание A 26 задания задание А 26. Одинаковую реакцию среды имеют растворы карбоната натрия и 1) нитрата бария 2) силиката калия 3) сульфата натрия 4) хлорида алюминия К объяснению A 26
 К выбору Следующее Задание A 27 задания задание А 27. Окислительно-восстановительной не является реакция 1) 4 KCl. O 3 KCl + 3 KCl. O 4 2) Са. СО 3 Ca. O + CO 2 3) NH 4 NO 3 N 2 O + 2 H 2 O 4) H 2 S S + H 2 К объяснению A 27
К выбору Следующее Задание A 27 задания задание А 27. Окислительно-восстановительной не является реакция 1) 4 KCl. O 3 KCl + 3 KCl. O 4 2) Са. СО 3 Ca. O + CO 2 3) NH 4 NO 3 N 2 O + 2 H 2 O 4) H 2 S S + H 2 К объяснению A 27
 К выбору Следующее Задание A 28 задания задание А 28. Верны ли следующие суждения о моющих средствах? А. Растворы мыла имеют щелочную среду. Б. Водные растворы мыла не теряют моющих свойств в жесткой воде. 1) верно только А 2) верно только Б 3) верны оба суждения 4) оба суждения неверны К объяснению A 28
К выбору Следующее Задание A 28 задания задание А 28. Верны ли следующие суждения о моющих средствах? А. Растворы мыла имеют щелочную среду. Б. Водные растворы мыла не теряют моющих свойств в жесткой воде. 1) верно только А 2) верно только Б 3) верны оба суждения 4) оба суждения неверны К объяснению A 28
 К выбору Следующее Задание A 29 задания задание А 29. Каучук образуется при полимеризации 1) стирола 2) этилена 3) бутена-2 4) изопрена К объяснению A 29
К выбору Следующее Задание A 29 задания задание А 29. Каучук образуется при полимеризации 1) стирола 2) этилена 3) бутена-2 4) изопрена К объяснению A 29
 К выбору Следующее Задание A 30 задания задание А 30. Какой объем (н. у. ) кислорода потребуется для полного сгорания 10 л (н. у. ) ацетилена? 1) 20 л 2) 5 л 3) 50 л 4) 25 л К объяснению A 30
К выбору Следующее Задание A 30 задания задание А 30. Какой объем (н. у. ) кислорода потребуется для полного сгорания 10 л (н. у. ) ацетилена? 1) 20 л 2) 5 л 3) 50 л 4) 25 л К объяснению A 30
 К выбору Следующее Задание B 1 задания задание В 1. Установите соответствие между молекулярной формулой вещества и классом органических соединений, к которому оно относится. МОЛЕКУЛЯРНАЯ ФОРМУЛА СОЕДИНЕНИЙ A) C 4 H 6 Б) C 4 H 8 O 2 В) C 7 H 8 Г) C 5 H 10 O 5 К объяснению B 1 КЛАСС ОРГАНИЧЕСКИХ 1) углеводы 2) арены 3) алкины 4) сложные эфиры 5) альдегиды
К выбору Следующее Задание B 1 задания задание В 1. Установите соответствие между молекулярной формулой вещества и классом органических соединений, к которому оно относится. МОЛЕКУЛЯРНАЯ ФОРМУЛА СОЕДИНЕНИЙ A) C 4 H 6 Б) C 4 H 8 O 2 В) C 7 H 8 Г) C 5 H 10 O 5 К объяснению B 1 КЛАСС ОРГАНИЧЕСКИХ 1) углеводы 2) арены 3) алкины 4) сложные эфиры 5) альдегиды
 К выбору Следующее Задание B 2 задания задание В 2. Установите соответствие между уравнением реакции и формулой вещества, которое в данной реакции является окислителем. УРАВНЕНИЕ РЕАКЦИИ ОКИСЛИТЕЛЬ А) H 2 S + I 2 = S + 2 HI 1) I 2 Б) 2 S + С = СS 2 2) SO 3 В) 2 SO 3 + 2 KI = I 2 + SO 2 + K 2 SO 4 3) S Г) S + 3 NO 2 = SO 3 + 3 NO 4) HI 5) H 2 S 6) NO 2 К объяснению B 2
К выбору Следующее Задание B 2 задания задание В 2. Установите соответствие между уравнением реакции и формулой вещества, которое в данной реакции является окислителем. УРАВНЕНИЕ РЕАКЦИИ ОКИСЛИТЕЛЬ А) H 2 S + I 2 = S + 2 HI 1) I 2 Б) 2 S + С = СS 2 2) SO 3 В) 2 SO 3 + 2 KI = I 2 + SO 2 + K 2 SO 4 3) S Г) S + 3 NO 2 = SO 3 + 3 NO 4) HI 5) H 2 S 6) NO 2 К объяснению B 2
 К выбору Следующее Задание B 3 задания задание В 3. Установите соответствие между формулой соли и продуктом, который образуется на инертном аноде при электролизе ее водного раствора. ФОРМУЛА СОЛИ ПРОДУКТ НА АНОДЕ А) Cu. SO 4 1) азот Б) K 2 S 2) сера В) Ba. Cl 2 3) хлор Г) Pb(NO 3)2 4) металл 5) кислород 6) водород К объяснению B 3
К выбору Следующее Задание B 3 задания задание В 3. Установите соответствие между формулой соли и продуктом, который образуется на инертном аноде при электролизе ее водного раствора. ФОРМУЛА СОЛИ ПРОДУКТ НА АНОДЕ А) Cu. SO 4 1) азот Б) K 2 S 2) сера В) Ba. Cl 2 3) хлор Г) Pb(NO 3)2 4) металл 5) кислород 6) водород К объяснению B 3
 К выбору Следующее Задание B 4 задания задание В 4. Установите соответствие между названием соли и отношением ее к гидролизу. НАЗВАНИЕ СОЛИ A) хлорид цинка Б) сульфид калия В) нитрат натрия Г) нитрат меди К объяснению B 4 ОТНОШЕНИЕ К ГИДРОЛИЗУ 1) гидролизуется по катиону 2) гидролизуется по аниону 3) гидролизуется по катиону и аниону 4) не гидролизуется
К выбору Следующее Задание B 4 задания задание В 4. Установите соответствие между названием соли и отношением ее к гидролизу. НАЗВАНИЕ СОЛИ A) хлорид цинка Б) сульфид калия В) нитрат натрия Г) нитрат меди К объяснению B 4 ОТНОШЕНИЕ К ГИДРОЛИЗУ 1) гидролизуется по катиону 2) гидролизуется по аниону 3) гидролизуется по катиону и аниону 4) не гидролизуется
 К выбору Следующее Задание B 5 задания задание В 5. Установите соответствие между простым веществом и реагентами, с каждым из которых оно может взаимодействовать. НАЗВАНИЕ ВЕЩЕСТВА РЕАГЕНТЫ A) алюминий Б) кислород В) сера Г) натрий К объяснению B 5 1) Fe 2 O 3, HNO 3(р-р), Na. OH(р-р) 2) Fe, HNO 3, H 2 3) HI, Fe, P 2 O 3 4) C 2 H 2, H 2 O, Cl 2 5) Ca. Cl 2, KOH, HCl
К выбору Следующее Задание B 5 задания задание В 5. Установите соответствие между простым веществом и реагентами, с каждым из которых оно может взаимодействовать. НАЗВАНИЕ ВЕЩЕСТВА РЕАГЕНТЫ A) алюминий Б) кислород В) сера Г) натрий К объяснению B 5 1) Fe 2 O 3, HNO 3(р-р), Na. OH(р-р) 2) Fe, HNO 3, H 2 3) HI, Fe, P 2 O 3 4) C 2 H 2, H 2 O, Cl 2 5) Ca. Cl 2, KOH, HCl
 К выбору Следующее Задание B 6 задания задание В 6. Взаимодействие пропена и бромоводорода в обычных условиях 1) протекает по правилу В. В. Марковникова 2) приводит к образованию 2 -бромпропана 3) относится к реакциям замещения 4) не сопровождается разрывом π-связи 5) осуществляется по ионному механизму 6) приводит к образованию 2, 2 -дибромпропана К объяснению B 6
К выбору Следующее Задание B 6 задания задание В 6. Взаимодействие пропена и бромоводорода в обычных условиях 1) протекает по правилу В. В. Марковникова 2) приводит к образованию 2 -бромпропана 3) относится к реакциям замещения 4) не сопровождается разрывом π-связи 5) осуществляется по ионному механизму 6) приводит к образованию 2, 2 -дибромпропана К объяснению B 6
 К выбору Задание B 7 задания В 7. Ацетальдегид взаимодействует с 1) H 2 2) CH 4 3) HBr 4) CH 3 OH 5) C 6 H 5 NO 2 6) Cu(OH)2 К объяснению B 7 Следующее задание
К выбору Задание B 7 задания В 7. Ацетальдегид взаимодействует с 1) H 2 2) CH 4 3) HBr 4) CH 3 OH 5) C 6 H 5 NO 2 6) Cu(OH)2 К объяснению B 7 Следующее задание
 К выбору Следующее Задание B 8 задания задание В 8. В отличие от сахарозы, глюкоза 1) реагирует с кислородом 2) реагирует с серной кислотой (конц. ) 3) восстанавливается водородом 4) окисляется аммиачным раствором оксида серебра 5) реагирует с уксусной кислотой 6) окисляется гидроксидом меди (II) К объяснению B 8
К выбору Следующее Задание B 8 задания задание В 8. В отличие от сахарозы, глюкоза 1) реагирует с кислородом 2) реагирует с серной кислотой (конц. ) 3) восстанавливается водородом 4) окисляется аммиачным раствором оксида серебра 5) реагирует с уксусной кислотой 6) окисляется гидроксидом меди (II) К объяснению B 8
 К выбору Следующее Задание B 9 задания задание В 9. К раствору хлорида кальция массой 140 г с массовой долей 5% добавили 10 г этой же соли. Массовая доля соли в полученном растворе равна ______ %. (Запишите число с точностью до десятых. ) К объяснению B 9
К выбору Следующее Задание B 9 задания задание В 9. К раствору хлорида кальция массой 140 г с массовой долей 5% добавили 10 г этой же соли. Массовая доля соли в полученном растворе равна ______ %. (Запишите число с точностью до десятых. ) К объяснению B 9
 К выбору Следующее Задание B 10 задания задание В 10. Какой объем (н. у. ) сероводорода выделился при взаимодействии 0, 3 моль сульфида железа (II) с избытком соляной кислоты? (Запишите число с точностью до сотых. ) К объяснению B 10
К выбору Следующее Задание B 10 задания задание В 10. Какой объем (н. у. ) сероводорода выделился при взаимодействии 0, 3 моль сульфида железа (II) с избытком соляной кислоты? (Запишите число с точностью до сотых. ) К объяснению B 10
 К выбору Следующее Задание C 1 задания задание С 1. Используя метод электронного баланса, составьте уравнение реакции I 2 + K 2 SO 3 + … → K 2 SO 4 + …+ Н 2 О. Определите окислитель и восстановитель. К объяснению C 1
К выбору Следующее Задание C 1 задания задание С 1. Используя метод электронного баланса, составьте уравнение реакции I 2 + K 2 SO 3 + … → K 2 SO 4 + …+ Н 2 О. Определите окислитель и восстановитель. К объяснению C 1
 К выбору Следующее Задание C 2 задания задание С 2. Даны вещества: дихромат калия, серная кислота (конц. ), фторид натрия, гидроксид рубидия. Напишите уравнения четырех возможных реакций между всеми предложенными веществами, не повторяя пары реагентов. К объяснению C 2
К выбору Следующее Задание C 2 задания задание С 2. Даны вещества: дихромат калия, серная кислота (конц. ), фторид натрия, гидроксид рубидия. Напишите уравнения четырех возможных реакций между всеми предложенными веществами, не повторяя пары реагентов. К объяснению C 2
 К выбору задания Задание C 3 Следующее задание С 3. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения: X 1 CH 3 Br X 2 X 3 HCHO X 4. К объяснению C 3
К выбору задания Задание C 3 Следующее задание С 3. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения: X 1 CH 3 Br X 2 X 3 HCHO X 4. К объяснению C 3
 К выбору Следующее Задание C 4 задания задание С 4. Нитрит калия массой 8, 5 г внесли при нагревании в 270 г раствора бромида аммония с массовой долей 12%. Какой объем (н. у. ) азота выделится при этом и какова массовая доля бромида аммония в получившемся растворе? К объяснению C 4
К выбору Следующее Задание C 4 задания задание С 4. Нитрит калия массой 8, 5 г внесли при нагревании в 270 г раствора бромида аммония с массовой долей 12%. Какой объем (н. у. ) азота выделится при этом и какова массовая доля бромида аммония в получившемся растворе? К объяснению C 4
 К выбору Задание C 5 задания С 5. Определите молекулярную формулу ацетиленового углеводорода, если молярная масса продукта его реакции с избытком бромоводорода в 4 раза больше, чем молярная масса исходного углеводорода. К объяснению C 5
К выбору Задание C 5 задания С 5. Определите молекулярную формулу ацетиленового углеводорода, если молярная масса продукта его реакции с избытком бромоводорода в 4 раза больше, чем молярная масса исходного углеводорода. К объяснению C 5
 Вернуться к заданию Объяснение А 1 Следующее задание Заряд ядра атома равен порядковому номеру хим. элемента (пример: у Al +13) Количество электронных слоев (энергетических уровней) равно номеру периода (пример: Cr – 4 слоя) В первом электронном слое может поместиться 2 электрона, во втором - 8 Количество электронов во внешнем электронном слое (внешнем энергетическом уровне) равно: для элементов главных подгрупп: номеру группы (пример: у Al 3 электрона); для элементов побочных подгрупп: 2 (пример: у Cr 2 электрона) Первые 2 электрона любого электронного уровня – s-электроны, следующие 6 электронов – p-электроны, оставшиеся – d-электроны (у элементов после La есть еще f-электроны) Al Al +13 2 8 3 1 s 2 2 p 6 3 s 2 3 p 1 1 s 22 p 63 s 23 p 2 - 14 электронов Cr Cr +24 2 8 12 2 1 s 2 2 p 6 3 s 2 3 p 6 3 d 4 4 s 2 Под номером 14 в таблице Менделеева находится кремний
Вернуться к заданию Объяснение А 1 Следующее задание Заряд ядра атома равен порядковому номеру хим. элемента (пример: у Al +13) Количество электронных слоев (энергетических уровней) равно номеру периода (пример: Cr – 4 слоя) В первом электронном слое может поместиться 2 электрона, во втором - 8 Количество электронов во внешнем электронном слое (внешнем энергетическом уровне) равно: для элементов главных подгрупп: номеру группы (пример: у Al 3 электрона); для элементов побочных подгрупп: 2 (пример: у Cr 2 электрона) Первые 2 электрона любого электронного уровня – s-электроны, следующие 6 электронов – p-электроны, оставшиеся – d-электроны (у элементов после La есть еще f-электроны) Al Al +13 2 8 3 1 s 2 2 p 6 3 s 2 3 p 1 1 s 22 p 63 s 23 p 2 - 14 электронов Cr Cr +24 2 8 12 2 1 s 2 2 p 6 3 s 2 3 p 6 3 d 4 4 s 2 Под номером 14 в таблице Менделеева находится кремний
 Вернуться к заданию Объяснение А 2 Для металлов главных подгрупп: Чем ближе к Fr, тем: Чем ближе к F, тем: - больше радиус атома - меньше радиус атома - сильнее металлические свойства -сильнее неметал-меньше электроотрицательность лические свойства -у металлов: сильнее основные - больше электросвойства оксида и гидроксида отрицательность Следующее задание Чем ближе к At, тем: -у неметаллов: сильнее кислотные свойства бескислородных кислот У металлов из побочных подгрупп металлические свойства слабее, чем у соседних металлов из главных подгрупп (например: Cu – ближе к Fr, чем K, но K проявляет более сильные металлические свойства, у него больше радиус атома, меньше электроотрицательность) 1) Li → Be → B → C - приближение к F, радиус атома уменьшается 2) Ar → Cl → S → P - приближение к Fr, радиус атома увеличивается 3) Si → Al → Mg → Na - приближение к Fr, радиус атома увеличивается 4) Ne → F → O → N - приближение к Fr, радиус атома увеличивается
Вернуться к заданию Объяснение А 2 Для металлов главных подгрупп: Чем ближе к Fr, тем: Чем ближе к F, тем: - больше радиус атома - меньше радиус атома - сильнее металлические свойства -сильнее неметал-меньше электроотрицательность лические свойства -у металлов: сильнее основные - больше электросвойства оксида и гидроксида отрицательность Следующее задание Чем ближе к At, тем: -у неметаллов: сильнее кислотные свойства бескислородных кислот У металлов из побочных подгрупп металлические свойства слабее, чем у соседних металлов из главных подгрупп (например: Cu – ближе к Fr, чем K, но K проявляет более сильные металлические свойства, у него больше радиус атома, меньше электроотрицательность) 1) Li → Be → B → C - приближение к F, радиус атома уменьшается 2) Ar → Cl → S → P - приближение к Fr, радиус атома увеличивается 3) Si → Al → Mg → Na - приближение к Fr, радиус атома увеличивается 4) Ne → F → O → N - приближение к Fr, радиус атома увеличивается
 Вернуться к заданию Объяснение А 3 Для металлов главных подгрупп: Чем ближе к Fr, тем: Чем ближе к F, тем: - больше радиус атома - меньше радиус атома - сильнее металлические свойства -сильнее неметал-меньше электроотрицательность лические свойства -у металлов: сильнее основные - больше электросвойства оксида и гидроксида отрицательность Следующее задание Чем ближе к At, тем: -у неметаллов: сильнее кислотные свойства бескислородных кислот Из перечисленных элементов (Be, Mg, Al, K) ближе всех в францию расположен K, значит он образует оксид с самыми сильными основными свойствами
Вернуться к заданию Объяснение А 3 Для металлов главных подгрупп: Чем ближе к Fr, тем: Чем ближе к F, тем: - больше радиус атома - меньше радиус атома - сильнее металлические свойства -сильнее неметал-меньше электроотрицательность лические свойства -у металлов: сильнее основные - больше электросвойства оксида и гидроксида отрицательность Следующее задание Чем ближе к At, тем: -у неметаллов: сильнее кислотные свойства бескислородных кислот Из перечисленных элементов (Be, Mg, Al, K) ближе всех в францию расположен K, значит он образует оксид с самыми сильными основными свойствами
 Вернуться к заданию Объяснение А 4 Следующее задание Для веществ, состоящих из двух химических элементов действует правило: элемент ближе к F имеет отрицательную степ. окисл. , а элемент дальше – положительную. Положительная степ. окисл. равна номеру группы (например, Al+3), отрицательная степ. окисл. может быть только у неметалла и считается по правилу: №группы минус восемь (например, у As-3) Водород в соединениях проявляет степень окисления +1 (кроме гидридов Na. H-1, Ca. H 2 -1 и т. д. ), кислород -2 (кроме O+2 F 2 и пероксидов H 2 O 2 -1, Ba. O 2 -1 и т. д. ) Щелочные металлы (Li, Na, K, Rb, Cs, Fr) – всегда +1 Be, Mg и щелочноземельные металлы (Ca, Sr, Ba, Ra) – всегда +2 В любой молекуле сумма степеней окисления должна быть равна нулю. +1 +6 -2 Na 2 ЭО 4 2+ 8 - Степень окисления +6 характерна для элементов 6 группы: серы, хрома, селена …, а также для некоторых других (например, железа)
Вернуться к заданию Объяснение А 4 Следующее задание Для веществ, состоящих из двух химических элементов действует правило: элемент ближе к F имеет отрицательную степ. окисл. , а элемент дальше – положительную. Положительная степ. окисл. равна номеру группы (например, Al+3), отрицательная степ. окисл. может быть только у неметалла и считается по правилу: №группы минус восемь (например, у As-3) Водород в соединениях проявляет степень окисления +1 (кроме гидридов Na. H-1, Ca. H 2 -1 и т. д. ), кислород -2 (кроме O+2 F 2 и пероксидов H 2 O 2 -1, Ba. O 2 -1 и т. д. ) Щелочные металлы (Li, Na, K, Rb, Cs, Fr) – всегда +1 Be, Mg и щелочноземельные металлы (Ca, Sr, Ba, Ra) – всегда +2 В любой молекуле сумма степеней окисления должна быть равна нулю. +1 +6 -2 Na 2 ЭО 4 2+ 8 - Степень окисления +6 характерна для элементов 6 группы: серы, хрома, селена …, а также для некоторых других (например, железа)
 Вернуться к заданию Объяснение А 5 Следующее задание Ионная связь – между металлом и неметаллом или между металлом и кислотным остатком. Примеры: Na 2 O, K 2 CO 3 Металлическая связь – металлы. Примеры: Ba, Al Ковалентная полярная связь – между разными неметаллами. Примеры: SO 2, HBr Ковалентная неполярная связь – между одинаковыми неметаллами. Примеры: O 3, H 2 Донорно-акцепторная связь – за счет неподеленной электронной пары. Примеры: NH 4 Cl и другие соединения аммония. Водородная – это связь между ионом водорода одном молекулы и ионом N, O или F другой молекулы. Возникает между молекулами: а) воды H 2 O; б) аммиака NH 3; в) фтороводорода HF; г) спиртов. 1) этан CH 3 -CH 3 - водородные связи не образует 2) бензол - водородные связи не образует 3) водород H 2 - водородные связи не образует 4) этанол (этиловый спирт) C 2 H 5 OH -образует водородные связи
Вернуться к заданию Объяснение А 5 Следующее задание Ионная связь – между металлом и неметаллом или между металлом и кислотным остатком. Примеры: Na 2 O, K 2 CO 3 Металлическая связь – металлы. Примеры: Ba, Al Ковалентная полярная связь – между разными неметаллами. Примеры: SO 2, HBr Ковалентная неполярная связь – между одинаковыми неметаллами. Примеры: O 3, H 2 Донорно-акцепторная связь – за счет неподеленной электронной пары. Примеры: NH 4 Cl и другие соединения аммония. Водородная – это связь между ионом водорода одном молекулы и ионом N, O или F другой молекулы. Возникает между молекулами: а) воды H 2 O; б) аммиака NH 3; в) фтороводорода HF; г) спиртов. 1) этан CH 3 -CH 3 - водородные связи не образует 2) бензол - водородные связи не образует 3) водород H 2 - водородные связи не образует 4) этанол (этиловый спирт) C 2 H 5 OH -образует водородные связи
 Вернуться к заданию Объяснение А 6 Следующее задание Для веществ, состоящих из двух химических элементов действует правило: элемент ближе к F имеет отрицательную степ. окисл. , а элемент дальше – положительную. Положительная степ. окисл. равна номеру группы (например, Al+3), отрицательная степ. окисл. может быть только у неметалла и считается по правилу: №группы минус восемь (например, у As-3) Водород в соединениях проявляет степень окисления +1 (кроме гидридов Na. H-1, Ca. H 2 -1 и т. д. ), кислород -2 (кроме соединения со фтором O+2 F 2 и пероксидов H 2 O 2 -1, Ba. O 2 -1 и т. д. ) Щелочные металлы (Li, Na, K, Rb, Cs, Fr) – всегда +1 Be, Mg и щелочноземельные металлы (Ca, Sr, Ba, Ra) – всегда +2 +3 -2 1) N 2 O 3 +1+3 -2 3) HNO 2 -3 +1 NH 3 -2 +1 N 2 H 4 -3 +1 -1 2) NH 4 Cl +1 +3 -2 4) Na. NO 2 +1 -2 N 2 O +3 -2 N 2 O 3
Вернуться к заданию Объяснение А 6 Следующее задание Для веществ, состоящих из двух химических элементов действует правило: элемент ближе к F имеет отрицательную степ. окисл. , а элемент дальше – положительную. Положительная степ. окисл. равна номеру группы (например, Al+3), отрицательная степ. окисл. может быть только у неметалла и считается по правилу: №группы минус восемь (например, у As-3) Водород в соединениях проявляет степень окисления +1 (кроме гидридов Na. H-1, Ca. H 2 -1 и т. д. ), кислород -2 (кроме соединения со фтором O+2 F 2 и пероксидов H 2 O 2 -1, Ba. O 2 -1 и т. д. ) Щелочные металлы (Li, Na, K, Rb, Cs, Fr) – всегда +1 Be, Mg и щелочноземельные металлы (Ca, Sr, Ba, Ra) – всегда +2 +3 -2 1) N 2 O 3 +1+3 -2 3) HNO 2 -3 +1 NH 3 -2 +1 N 2 H 4 -3 +1 -1 2) NH 4 Cl +1 +3 -2 4) Na. NO 2 +1 -2 N 2 O +3 -2 N 2 O 3
 Вернуться к заданию Объяснение. А 7 Следующее задание Существует 4 типа строения (кристаллических решеток): Тип Вещества с такой решеткой Свойства ковкость, пластичность, тягучесть, металлический блеск, электро- и металлическая металлы и сплавы теплопроводность большинство солей, высокие твердость и прочность, высокие основания, температуры плавления и кипения, часто ионная оксиды металлов хорошая растворимость алмаз, графит; B, Si, Ge (крист); высокие твердость и прочность, высокие Si. O 2 (кремнезем, кварц, горный температуры плавления и кипения, атомная хрусталь); P (красный) нерастворимость органические вещества; P(белый) малые твердость и прочность, низкие температуры плавления и кипения, молекулярная прост. в-ва – неметаллы; H 2 O, CO 2, HCl, H 2 S и т. д. летучесть, низкая электропроводность Хлорид бария Ba. Cl 2 – соль, значит ионная кристаллическая решетка
Вернуться к заданию Объяснение. А 7 Следующее задание Существует 4 типа строения (кристаллических решеток): Тип Вещества с такой решеткой Свойства ковкость, пластичность, тягучесть, металлический блеск, электро- и металлическая металлы и сплавы теплопроводность большинство солей, высокие твердость и прочность, высокие основания, температуры плавления и кипения, часто ионная оксиды металлов хорошая растворимость алмаз, графит; B, Si, Ge (крист); высокие твердость и прочность, высокие Si. O 2 (кремнезем, кварц, горный температуры плавления и кипения, атомная хрусталь); P (красный) нерастворимость органические вещества; P(белый) малые твердость и прочность, низкие температуры плавления и кипения, молекулярная прост. в-ва – неметаллы; H 2 O, CO 2, HCl, H 2 S и т. д. летучесть, низкая электропроводность Хлорид бария Ba. Cl 2 – соль, значит ионная кристаллическая решетка
 Вернуться к заданию Объяснение А 8 Следующее задание Кислоты – вещества, состоящие из ионов водорода и кислотных остатков А) СH 4 - метан (класс: Алканы) - сероводородная кислота. Состоит из ионов водорода H+ Б) H 2 S и кислотного остатка S 2 - (сульфид). (класс: Кислоты) - уксусная кислота. Состоит из ионов водорода H+ В) СH 3 COOH и кислотного остатка CH 3 COO- (ацетат) (класс: Кислоты) Г) NH 3 - аммиак. Не содержит кислотного остатка, не кислота Д) H 5 IO 6 Состоит из ионов водорода H+ и кислотного остатка IO 65 -. (класс: Кислоты) Состоит из ионов металла калия K+, ионов водорода H+ Е) K 2 HPO 4 и кислотного остатка PO 43 - (фосфат) (класс: Кислые соли)
Вернуться к заданию Объяснение А 8 Следующее задание Кислоты – вещества, состоящие из ионов водорода и кислотных остатков А) СH 4 - метан (класс: Алканы) - сероводородная кислота. Состоит из ионов водорода H+ Б) H 2 S и кислотного остатка S 2 - (сульфид). (класс: Кислоты) - уксусная кислота. Состоит из ионов водорода H+ В) СH 3 COOH и кислотного остатка CH 3 COO- (ацетат) (класс: Кислоты) Г) NH 3 - аммиак. Не содержит кислотного остатка, не кислота Д) H 5 IO 6 Состоит из ионов водорода H+ и кислотного остатка IO 65 -. (класс: Кислоты) Состоит из ионов металла калия K+, ионов водорода H+ Е) K 2 HPO 4 и кислотного остатка PO 43 - (фосфат) (класс: Кислые соли)
 Вернуться к заданию Объяснение А 9 Следующее задание 1) Cu и Zn. Cl 2 (р-р) Cu – менее активный металл, чем Zn, реакция невозможна 2) Zn и Cu. SO 4 (р-р) Zn – более активный металл, чем Cu, может вытеснить медь из ее соли Zn + Cu. SO 4 = Zn 2+ SO 42 - + Cu 0 3) Fe и Al(NO 3)3 (р-р) Fe – менее активный металл, чем Al, реакция невозможна 4) Ag и Fe. SO 4 (р-р) Ag – менее активный металл, чем Fe, реакция невозможна
Вернуться к заданию Объяснение А 9 Следующее задание 1) Cu и Zn. Cl 2 (р-р) Cu – менее активный металл, чем Zn, реакция невозможна 2) Zn и Cu. SO 4 (р-р) Zn – более активный металл, чем Cu, может вытеснить медь из ее соли Zn + Cu. SO 4 = Zn 2+ SO 42 - + Cu 0 3) Fe и Al(NO 3)3 (р-р) Fe – менее активный металл, чем Al, реакция невозможна 4) Ag и Fe. SO 4 (р-р) Ag – менее активный металл, чем Fe, реакция невозможна
 Вернуться к заданию Объяснение А 10 Следующее задание Оксид углерода (IV) CO 2 – кислотный оксид 1) CO 2 + Ca(OH)2 = Ca. CO 3 + H 2 O CO 2 – кислотный оксид, Ca(OH)2 – основание. Основания реагируют с кислотными оксидами. При этом образуются соль и вода 2) CO 2 + Cu. Cl 2 ≠ Соли с оксидами не реагируют 3) CO 2 + SO 3 ≠ SO 3 – кислотный оксид. Кислотные оксиды между собой не реагируют 4) CO 2 + Cr. O 3 ≠ Cr. O 3 – кислотный оксид. Кислотные оксиды между собой не реагируют
Вернуться к заданию Объяснение А 10 Следующее задание Оксид углерода (IV) CO 2 – кислотный оксид 1) CO 2 + Ca(OH)2 = Ca. CO 3 + H 2 O CO 2 – кислотный оксид, Ca(OH)2 – основание. Основания реагируют с кислотными оксидами. При этом образуются соль и вода 2) CO 2 + Cu. Cl 2 ≠ Соли с оксидами не реагируют 3) CO 2 + SO 3 ≠ SO 3 – кислотный оксид. Кислотные оксиды между собой не реагируют 4) CO 2 + Cr. O 3 ≠ Cr. O 3 – кислотный оксид. Кислотные оксиды между собой не реагируют
 Вернуться к заданию Объяснение А 11 Следующее задание Гидроксид алюминия Al(OH)3 – амфотерный гидроксид 3 HCl = Al. Cl 3 + 3 H 2 O Амфотерные гидроксиды Al(OH)3 + реагируют с кислотами Al(OH)3 + Na. NO 3 ≠ Амфотерные гидроксиды не реагируют с солями Амфотерные гидроксиды Al(OH)3 +3 HNO 3 = Al(NO 3)3 + 3 H 2 O реагируют с кислотами 2 Al(OH)3 + Ba(OH)2 = Ba(Al. O 2)2 +4 H 2 O Амфотерные гидроксиды реагируют со щелочами Al(OH)3 + Na. OH = Al(OH)3 + Na. Cl ≠ Амфотерные гидроксиды Na. Al. O 2 +2 H 2 O реагируют со щелочами Амфотерные гидроксиды не реагируют с солями Al(OH)3 + KOH = Al(OH)3 + Ca. CO 3 ≠ Амфотерные гидроксиды KAl. O 2 +2 H 2 O реагируют со щелочами Амфотерные гидроксиды не реагируют с солями
Вернуться к заданию Объяснение А 11 Следующее задание Гидроксид алюминия Al(OH)3 – амфотерный гидроксид 3 HCl = Al. Cl 3 + 3 H 2 O Амфотерные гидроксиды Al(OH)3 + реагируют с кислотами Al(OH)3 + Na. NO 3 ≠ Амфотерные гидроксиды не реагируют с солями Амфотерные гидроксиды Al(OH)3 +3 HNO 3 = Al(NO 3)3 + 3 H 2 O реагируют с кислотами 2 Al(OH)3 + Ba(OH)2 = Ba(Al. O 2)2 +4 H 2 O Амфотерные гидроксиды реагируют со щелочами Al(OH)3 + Na. OH = Al(OH)3 + Na. Cl ≠ Амфотерные гидроксиды Na. Al. O 2 +2 H 2 O реагируют со щелочами Амфотерные гидроксиды не реагируют с солями Al(OH)3 + KOH = Al(OH)3 + Ca. CO 3 ≠ Амфотерные гидроксиды KAl. O 2 +2 H 2 O реагируют со щелочами Амфотерные гидроксиды не реагируют с солями
 Вернуться к заданию Объяснение А 12 Следующее задание Карбонат калия K 2 CO 3 - соль K 2 CO 3 + Ca(NO 3)2 = Реакция возможна, т. к. Ca. CO 3↓ +2 KNO 3 образуется осадок K 2 CO 3 + Mg. O ≠ Соли с оксидами не реагируют K 2 CO 3 + CO ≠ Соли с оксидами не реагируют K 2 CO 3 + Na. Cl ≠ Реакция невозможна, т. к. не образуются осадок, газ или вода (KCl – растворим, Na 2 CO 3 – растворим)
Вернуться к заданию Объяснение А 12 Следующее задание Карбонат калия K 2 CO 3 - соль K 2 CO 3 + Ca(NO 3)2 = Реакция возможна, т. к. Ca. CO 3↓ +2 KNO 3 образуется осадок K 2 CO 3 + Mg. O ≠ Соли с оксидами не реагируют K 2 CO 3 + CO ≠ Соли с оксидами не реагируют K 2 CO 3 + Na. Cl ≠ Реакция невозможна, т. к. не образуются осадок, газ или вода (KCl – растворим, Na 2 CO 3 – растворим)
 Вернуться к заданию Объяснение А 13 Fe 2 O 3 Fe Следующее задание Fe. SO 4 Железо из оксида можно восстановить H 2, C, Al (медью нельзя): Fe 2 O 3 + 3 H 2 = 3 H 2 O + 2 Fe 2 O 3 + 3 C = 3 CO 2 + 4 Fe Fe 2 O 3 + 2 Al = Al 2 O 3 + 2 Fe HNO 3 и H 2 SO 4 (конц. ) являются окислительными кислотами (реагируют с металлами правее H). Чаще всего HNO 3 (конц. ) восстанавливается до NO 2, HNO 3 (разб. ) → NO, H 2 SO 4 (конц. ) → SO 2 2 Fe + 6 H 2 SO 4(конц. ) = Fe 2(SO 4)3 + 3 SO 2 + 6 H 2 O Fe + Na 2 SO 4 (р-р) ≠ Fe – менее активный металл, чем Na Fe + H 2 SO 4(разб. ) = Fe. SO 4 + H 2 SO 4 (разб. ) не является окислительной кислотой (реагирует с металлами только левее H).
Вернуться к заданию Объяснение А 13 Fe 2 O 3 Fe Следующее задание Fe. SO 4 Железо из оксида можно восстановить H 2, C, Al (медью нельзя): Fe 2 O 3 + 3 H 2 = 3 H 2 O + 2 Fe 2 O 3 + 3 C = 3 CO 2 + 4 Fe Fe 2 O 3 + 2 Al = Al 2 O 3 + 2 Fe HNO 3 и H 2 SO 4 (конц. ) являются окислительными кислотами (реагируют с металлами правее H). Чаще всего HNO 3 (конц. ) восстанавливается до NO 2, HNO 3 (разб. ) → NO, H 2 SO 4 (конц. ) → SO 2 2 Fe + 6 H 2 SO 4(конц. ) = Fe 2(SO 4)3 + 3 SO 2 + 6 H 2 O Fe + Na 2 SO 4 (р-р) ≠ Fe – менее активный металл, чем Na Fe + H 2 SO 4(разб. ) = Fe. SO 4 + H 2 SO 4 (разб. ) не является окислительной кислотой (реагирует с металлами только левее H).
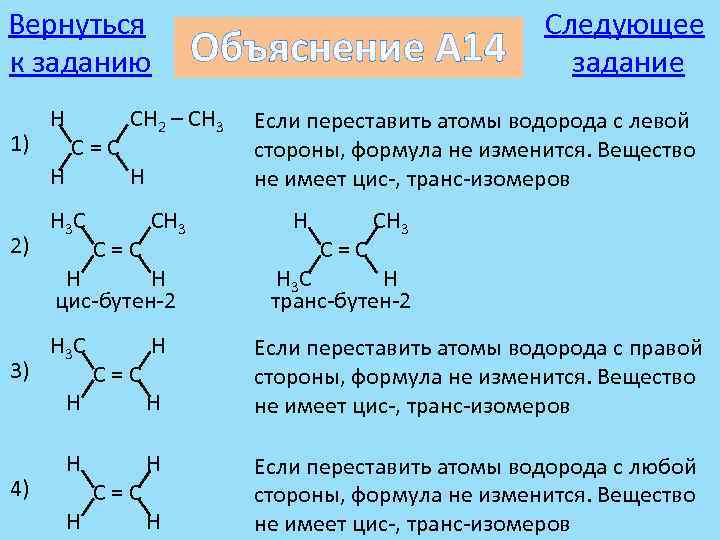 Вернуться к заданию 1) H H 2) C=C H 3 C CH 2 – CH 3 H C=C CH 3 H H цис-бутен-2 3) H 3 C H 4) H H Объяснение А 14 C=C H H Следующее задание Если переставить атомы водорода с левой стороны, формула не изменится. Вещество не имеет цис-, транс-изомеров H C=C CH 3 C H транс-бутен-2 Если переставить атомы водорода с правой стороны, формула не изменится. Вещество не имеет цис-, транс-изомеров Если переставить атомы водорода с любой стороны, формула не изменится. Вещество не имеет цис-, транс-изомеров
Вернуться к заданию 1) H H 2) C=C H 3 C CH 2 – CH 3 H C=C CH 3 H H цис-бутен-2 3) H 3 C H 4) H H Объяснение А 14 C=C H H Следующее задание Если переставить атомы водорода с левой стороны, формула не изменится. Вещество не имеет цис-, транс-изомеров H C=C CH 3 C H транс-бутен-2 Если переставить атомы водорода с правой стороны, формула не изменится. Вещество не имеет цис-, транс-изомеров Если переставить атомы водорода с любой стороны, формула не изменится. Вещество не имеет цис-, транс-изомеров
 Вернуться к заданию Объяснение А 15 Следующее задание С каждым из веществ: водой, бромоводородом, водородом – могут реагировать только вещества, содержащие в молекуле двойную или тройную связь между атомами углерода Из приведенных вариантов подходит только бутен-1 CH 2 – CH 3 + H 2 O → CH 3 – CH 2 – CH 3 2 H OH CH 2 – CH 3 + HBr → CH 3 – CH 2 – CH 3 2 H Br CH 2 – CH 3 + H 2 → CH 3 – CH 2 – CH 3 2 H H
Вернуться к заданию Объяснение А 15 Следующее задание С каждым из веществ: водой, бромоводородом, водородом – могут реагировать только вещества, содержащие в молекуле двойную или тройную связь между атомами углерода Из приведенных вариантов подходит только бутен-1 CH 2 – CH 3 + H 2 O → CH 3 – CH 2 – CH 3 2 H OH CH 2 – CH 3 + HBr → CH 3 – CH 2 – CH 3 2 H Br CH 2 – CH 3 + H 2 → CH 3 – CH 2 – CH 3 2 H H
 Вернуться к заданию Объяснение А 16 1. С очень активными металлами 2 C 6 H 5 OH + 2 Na → 2 C 6 H 5 ONa + H 2 2. Со щелочами C 6 H 5 OH+Na. OH→C 6 H 5 ONa+H 2 O C 6 H 5 OH+HCl≠ {C 2 H 5 OH + Na. OH ≠ C 2 H 5 OH +HCl →C 2 H 5 Cl + H 2 O} Фенол 3. Гидрирование, галогенирование, нитрование, с галогеналканами – теже, что и у аренов 4. Поликонденсация формальдегид + фенол → фенолформальдегидная смола C 6 H 5 OH + Br 2 → белый осадок C 6 H 5 OH + Fe. Cl 3 → темно-фиолетовый цвет Следующее задание Из хлорбензола Cl OH + Na. OH → + Na. Cl Фенол взаимодействует с бромной водой Фенол обладает кислотными свойствами (может реагировать с основаниями, но не может реагировать с кислотами)
Вернуться к заданию Объяснение А 16 1. С очень активными металлами 2 C 6 H 5 OH + 2 Na → 2 C 6 H 5 ONa + H 2 2. Со щелочами C 6 H 5 OH+Na. OH→C 6 H 5 ONa+H 2 O C 6 H 5 OH+HCl≠ {C 2 H 5 OH + Na. OH ≠ C 2 H 5 OH +HCl →C 2 H 5 Cl + H 2 O} Фенол 3. Гидрирование, галогенирование, нитрование, с галогеналканами – теже, что и у аренов 4. Поликонденсация формальдегид + фенол → фенолформальдегидная смола C 6 H 5 OH + Br 2 → белый осадок C 6 H 5 OH + Fe. Cl 3 → темно-фиолетовый цвет Следующее задание Из хлорбензола Cl OH + Na. OH → + Na. Cl Фенол взаимодействует с бромной водой Фенол обладает кислотными свойствами (может реагировать с основаниями, но не может реагировать с кислотами)
 Вернуться к заданию Объяснение А 17 Уксусная кислота CH 3 COOH или CH 3 – C 1) O Следующее задание OH CH 3 COOH + Na. OH → CH 3 COONa + H 2 O Кислоты реагируют с основаниями CH 3 COOH + CO 2 ≠ CO 2 – кислотный оксид, с кислотами не реагирует CH 3 COOH + Na. OH → CH 3 COONa + H 2 O Кислоты реагируют с основаниями 2) Кислоты реагируют с карбона 2 CH 3 COOH + Na 2 CO 3 → 2 CH 3 COONa + H 2 CO 3 CO 2 O+ тами, образуется газ CO 2 CH 3 COOH + CH 2=CH 2 ≠ C 2 H 4 (этилен) с кислотами не реагирует C 2 H 5 OH – спирт. Спирты вступают с 3) CH 3 COOH + C 2 H 5 OH → CH 3 COOC 2 H 5 + H 2 O кислотами в реакцию этерификации (образуется сложный эфир) CH 3 COOH + CO ≠ CO – несолеобразующий оксид, с кислотами не реагирует 4) C 2 H 5 OH – спирт. Спирты вступают с CH 3 COOH + C 2 H 5 OH → CH 3 COOC 2 H 5 + H 2 O кислотами в реакцию этерификации (образуется сложный эфир)
Вернуться к заданию Объяснение А 17 Уксусная кислота CH 3 COOH или CH 3 – C 1) O Следующее задание OH CH 3 COOH + Na. OH → CH 3 COONa + H 2 O Кислоты реагируют с основаниями CH 3 COOH + CO 2 ≠ CO 2 – кислотный оксид, с кислотами не реагирует CH 3 COOH + Na. OH → CH 3 COONa + H 2 O Кислоты реагируют с основаниями 2) Кислоты реагируют с карбона 2 CH 3 COOH + Na 2 CO 3 → 2 CH 3 COONa + H 2 CO 3 CO 2 O+ тами, образуется газ CO 2 CH 3 COOH + CH 2=CH 2 ≠ C 2 H 4 (этилен) с кислотами не реагирует C 2 H 5 OH – спирт. Спирты вступают с 3) CH 3 COOH + C 2 H 5 OH → CH 3 COOC 2 H 5 + H 2 O кислотами в реакцию этерификации (образуется сложный эфир) CH 3 COOH + CO ≠ CO – несолеобразующий оксид, с кислотами не реагирует 4) C 2 H 5 OH – спирт. Спирты вступают с CH 3 COOH + C 2 H 5 OH → CH 3 COOC 2 H 5 + H 2 O кислотами в реакцию этерификации (образуется сложный эфир)
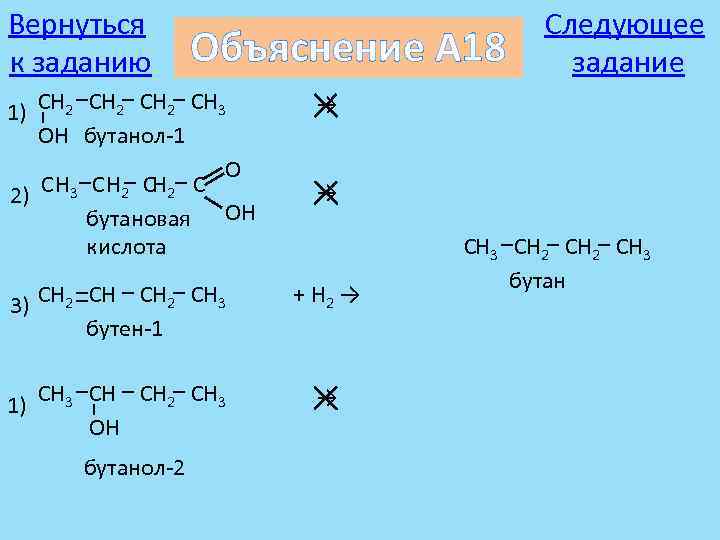 Вернуться к заданию Объяснение А 18 1) CH 2 CH 3 OH бутанол-1 O C H 3 C H 2 C 2) бутановая OH кислота → → 3) CH 2 CH 3 бутен-1 + H 2 → 1) CH 3 CH CH 2 CH 3 OH → бутанол-2 Следующее задание CH 3 CH 2 CH 3 бутан
Вернуться к заданию Объяснение А 18 1) CH 2 CH 3 OH бутанол-1 O C H 3 C H 2 C 2) бутановая OH кислота → → 3) CH 2 CH 3 бутен-1 + H 2 → 1) CH 3 CH CH 2 CH 3 OH → бутанол-2 Следующее задание CH 3 CH 2 CH 3 бутан
 Вернуться к заданию Объяснение. А 19 Следующее задание 1) CH 3 -CH 2 -CH 3 + Na. OH ≠ пентан 2) CH 2 CH 3 + H 2 O → CH 2 CH 3 3 пентен-1 H OH пентанол-2 O + H 2 → CH 3 -CH 2 -CH 2 OH 3) C H 3 C H 2 CH 2 C OH пентаналь пентанол-1 4) CH 2 CH 3 + Cu(OH)2 ≠ Cl 1 -хлорпентан
Вернуться к заданию Объяснение. А 19 Следующее задание 1) CH 3 -CH 2 -CH 3 + Na. OH ≠ пентан 2) CH 2 CH 3 + H 2 O → CH 2 CH 3 3 пентен-1 H OH пентанол-2 O + H 2 → CH 3 -CH 2 -CH 2 OH 3) C H 3 C H 2 CH 2 C OH пентаналь пентанол-1 4) CH 2 CH 3 + Cu(OH)2 ≠ Cl 1 -хлорпентан
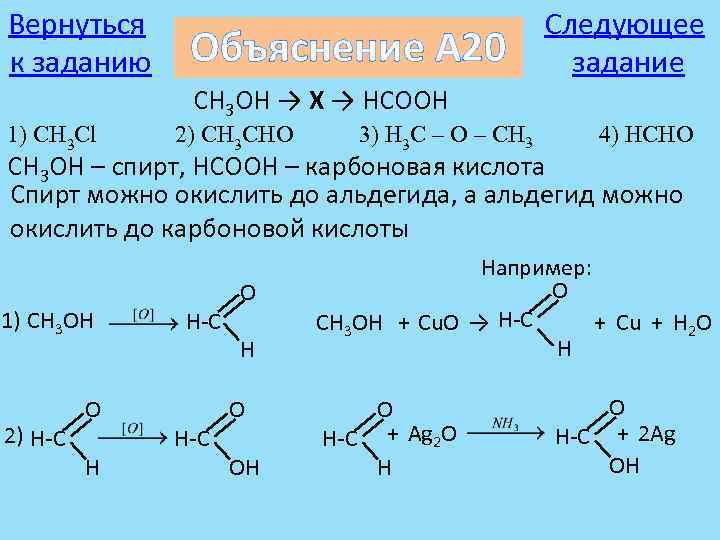 Вернуться к заданию Объяснение А 20 Следующее задание CH 3 OH → X → HCOOH 1) CH 3 Cl 2) CH 3 CHO 3) H 3 C – O – CH 3 4) HCHO CH 3 OH – спирт, HCOOH – карбоновая кислота Спирт можно окислить до альдегида, а альдегид можно окислить до карбоновой кислоты 1) CH 3 OH 2) H-C O H O OH Например: O CH 3 OH + Cu. O → H-C + Cu + H 2 O H O H-C + Ag 2 O H O H-C + 2 Ag OH
Вернуться к заданию Объяснение А 20 Следующее задание CH 3 OH → X → HCOOH 1) CH 3 Cl 2) CH 3 CHO 3) H 3 C – O – CH 3 4) HCHO CH 3 OH – спирт, HCOOH – карбоновая кислота Спирт можно окислить до альдегида, а альдегид можно окислить до карбоновой кислоты 1) CH 3 OH 2) H-C O H O OH Например: O CH 3 OH + Cu. O → H-C + Cu + H 2 O H O H-C + Ag 2 O H O H-C + 2 Ag OH
 Вернуться к заданию 2 SO 2 Объяснение А 21 + O 2 → оксид серы (IV) Следующее задание 2 SO 3 оксид серы (VI) Из двух веществ получилось одно – реакция соединения Реакции с кислородом без катализатора – это реакции горения Все реакции горения – экзотермические (идут с выделением тепла) Исключение: N 2 + O 2 = 2 NO
Вернуться к заданию 2 SO 2 Объяснение А 21 + O 2 → оксид серы (IV) Следующее задание 2 SO 3 оксид серы (VI) Из двух веществ получилось одно – реакция соединения Реакции с кислородом без катализатора – это реакции горения Все реакции горения – экзотермические (идут с выделением тепла) Исключение: N 2 + O 2 = 2 NO
 Вернуться к заданию Объяснение А 22 Следующее задание 1. С наибольшей скоростью протекают реакции в растворах. 2. В реакциях замещения с большей скоростью реагируют более активные металлы Способы увеличения скорости химических реакций: 1) нагревание; 2) использование катализатора; 3) увеличение площади соприкосновения реагирующих фаз (измельчение); 4) увеличение концентрации компонента; 5) для газов: увеличение давления;
Вернуться к заданию Объяснение А 22 Следующее задание 1. С наибольшей скоростью протекают реакции в растворах. 2. В реакциях замещения с большей скоростью реагируют более активные металлы Способы увеличения скорости химических реакций: 1) нагревание; 2) использование катализатора; 3) увеличение площади соприкосновения реагирующих фаз (измельчение); 4) увеличение концентрации компонента; 5) для газов: увеличение давления;
 Вернуться к заданию Объяснение А 23 Следующее задание При увеличении давления, равновесие реакции смещается в ту сторону, где меньше моль газов Если в реакции тепло выделяется (+Q), то увеличение температуры смещает равновесие в обратную сторону При увеличении концентраций исходных веществ, равновесие смещается в сторону продуктов реакции C 4 H 8(г) + H 2(г) C 4 H 10(г) + Q 1) При увеличении концентрации водорода равновесие будет смещаться вправо (образование C 4 H 10) 2) В реакции тепло выделяется (+Q). Значит повышение температуры будет смещать равновесие влево(образование C 4 H 8 и H 2) 3) В левой части 2 моль газов, а в правой 1. Значит увеличение давления будет смещать равновесие вправо (образование C 4 H 10) 4) Катализатор влияет только на скорость химической реакции. Равновесие реакции от катализатора не зависит
Вернуться к заданию Объяснение А 23 Следующее задание При увеличении давления, равновесие реакции смещается в ту сторону, где меньше моль газов Если в реакции тепло выделяется (+Q), то увеличение температуры смещает равновесие в обратную сторону При увеличении концентраций исходных веществ, равновесие смещается в сторону продуктов реакции C 4 H 8(г) + H 2(г) C 4 H 10(г) + Q 1) При увеличении концентрации водорода равновесие будет смещаться вправо (образование C 4 H 10) 2) В реакции тепло выделяется (+Q). Значит повышение температуры будет смещать равновесие влево(образование C 4 H 8 и H 2) 3) В левой части 2 моль газов, а в правой 1. Значит увеличение давления будет смещать равновесие вправо (образование C 4 H 10) 4) Катализатор влияет только на скорость химической реакции. Равновесие реакции от катализатора не зависит
 Вернуться к заданию Объяснение А 24 Неэлектролиты 1. Все оксиды (Na 2 O, SO 3, Al 2 O 3 …) 2. Большинство органических соединений (CH 4, C 2 H 5 OH, C 6 H 12 O 6 …), кроме карбоновых кислот 3. Неметаллы (S, P, Cl 2, O 2 …) Слабые электролиты 1. Слабые кислоты (H 2 S, HF, H 2 CO 3 …) 2. Нерастворимые основания (Mg(OH)2, Al(OH)3, Fe(OH)2 …) 3. Нерастворимые соли (Ba. SO 4, Ag. Cl, Ca. CO 3 …) Следующее задание Сильные электролиты 1. Сильные кислоты (HCl, HBr, HI, HNO 3, H 2 SO 4, HCl. O 4) 2. Щёлочи (растворимые основания) (Li. OH, Na. OH, KOH, Rb. OH, Cs. OH, Ca(OH)2, Sr(OH)2, Ba(OH)2) 3. Растворимые соли (KCl, Na 2 CO 3, Ba(NO 3)2 …) Диссоциация – это распад молекул электролита на ионы. Например: H 2 SO 4 2 H+ +SO 42 H 2 Si. O 3 Диссоциируют только сильные электролиты Диссоциация может происходить ступенчато. Например: 1) H 2 SO 4 ↔ H+ +HSO 42) HSO 4 - ↔ H+ + SO 421) KCl K+ + Clобразуется 2 моль ионов (1 моль K+ и 1 моль Cl-) образуется 4 моль ионов (1 моль Fe 3+ и 3 моль NO 3 -) 2) Fe(NO 3)3 Fe 3+ + 3 NO 3 - 3) Al 2(SO 4)3 2 Al 3+ + 3 SO 42 - образуется 5 моль ионов (2 моль Al 3+ и 3 моль SO 42 -) 4) Na 2 CO 3 2 Na+ + CO 32 - образуется 3 моль ионов (2 моль Na+ и 1 моль CO 32 -
Вернуться к заданию Объяснение А 24 Неэлектролиты 1. Все оксиды (Na 2 O, SO 3, Al 2 O 3 …) 2. Большинство органических соединений (CH 4, C 2 H 5 OH, C 6 H 12 O 6 …), кроме карбоновых кислот 3. Неметаллы (S, P, Cl 2, O 2 …) Слабые электролиты 1. Слабые кислоты (H 2 S, HF, H 2 CO 3 …) 2. Нерастворимые основания (Mg(OH)2, Al(OH)3, Fe(OH)2 …) 3. Нерастворимые соли (Ba. SO 4, Ag. Cl, Ca. CO 3 …) Следующее задание Сильные электролиты 1. Сильные кислоты (HCl, HBr, HI, HNO 3, H 2 SO 4, HCl. O 4) 2. Щёлочи (растворимые основания) (Li. OH, Na. OH, KOH, Rb. OH, Cs. OH, Ca(OH)2, Sr(OH)2, Ba(OH)2) 3. Растворимые соли (KCl, Na 2 CO 3, Ba(NO 3)2 …) Диссоциация – это распад молекул электролита на ионы. Например: H 2 SO 4 2 H+ +SO 42 H 2 Si. O 3 Диссоциируют только сильные электролиты Диссоциация может происходить ступенчато. Например: 1) H 2 SO 4 ↔ H+ +HSO 42) HSO 4 - ↔ H+ + SO 421) KCl K+ + Clобразуется 2 моль ионов (1 моль K+ и 1 моль Cl-) образуется 4 моль ионов (1 моль Fe 3+ и 3 моль NO 3 -) 2) Fe(NO 3)3 Fe 3+ + 3 NO 3 - 3) Al 2(SO 4)3 2 Al 3+ + 3 SO 42 - образуется 5 моль ионов (2 моль Al 3+ и 3 моль SO 42 -) 4) Na 2 CO 3 2 Na+ + CO 32 - образуется 3 моль ионов (2 моль Na+ и 1 моль CO 32 -
 Вернуться к заданию Объяснение А 25 Следующее задание 1) K 2 SO 4 + Na. OH → KOH + Na 2 SO 4 Реакция невозможна, т. к. не образуется ни осадка, ни газа, ни воды 1) K 2 SO 4 + HCl Реакция невозможна, т. к. не образуется ни осадка, ни газа, ни воды → KCl + H 2 SO 4 1) K 2 SO 4 + Ba(OH)2 → 2 KOH + Ba. SO 4 ↓ 1) K 2 SO 4 + NH 3 ≠ Аммиак реагирует только с водой, кислотами, кислородом и активными металлами
Вернуться к заданию Объяснение А 25 Следующее задание 1) K 2 SO 4 + Na. OH → KOH + Na 2 SO 4 Реакция невозможна, т. к. не образуется ни осадка, ни газа, ни воды 1) K 2 SO 4 + HCl Реакция невозможна, т. к. не образуется ни осадка, ни газа, ни воды → KCl + H 2 SO 4 1) K 2 SO 4 + Ba(OH)2 → 2 KOH + Ba. SO 4 ↓ 1) K 2 SO 4 + NH 3 ≠ Аммиак реагирует только с водой, кислотами, кислородом и активными металлами
 Вернуться к заданию Объяснение А 26 Следующее задание Сильные кислоты: HCl, HBr, HI, HNO 3, H 2 SO 4, HCl. O 4 Сильные основания (щелочи) - гидроксиды щелочных и щелочноземельных металлов: Li. OH, Na. OH, KOH, Rb. OH, Cs. OH, Ca(OH)2, Sr(OH)2 и Ba(OH)2 Карбонат натрия 1) образован из сильного основания Na 2 CO 3 Na. OH и слабой кислоты H CO 2 3 образован из сильного основания Ba(NO 3)2 Ba(OH) и сильной кислоты HNO 2 3 - щелочная среда - нейтральная среда K 2 Si. O 3 образован из сильного основания KOH и слабой кислоты H 2 Si. O 3 - щелочная среда 3) Na 2 SO 4 образован из сильного основания Na. OH и сильной кислоты H 2 SO 4 - нейтральная среда 4) Al. Cl 3 образован из слабого основания Al(OH)3 и сильной кислоты HCl - кислая среда 2)
Вернуться к заданию Объяснение А 26 Следующее задание Сильные кислоты: HCl, HBr, HI, HNO 3, H 2 SO 4, HCl. O 4 Сильные основания (щелочи) - гидроксиды щелочных и щелочноземельных металлов: Li. OH, Na. OH, KOH, Rb. OH, Cs. OH, Ca(OH)2, Sr(OH)2 и Ba(OH)2 Карбонат натрия 1) образован из сильного основания Na 2 CO 3 Na. OH и слабой кислоты H CO 2 3 образован из сильного основания Ba(NO 3)2 Ba(OH) и сильной кислоты HNO 2 3 - щелочная среда - нейтральная среда K 2 Si. O 3 образован из сильного основания KOH и слабой кислоты H 2 Si. O 3 - щелочная среда 3) Na 2 SO 4 образован из сильного основания Na. OH и сильной кислоты H 2 SO 4 - нейтральная среда 4) Al. Cl 3 образован из слабого основания Al(OH)3 и сильной кислоты HCl - кислая среда 2)
 Вернуться к заданию Объяснение А 27 Окислитель – отбирает электроны Например: Cu+2 + 2 e → Cu 0 N+5 + 3 e → N+2 1) 4 KCl+5 O 3 2) Са. СО 3 3) N-3 H 4 N+5 O 3 4) H 2+1 S-2 KCl-1 + 3 KCl+7 O 4 Ca. O + CO 2 Восстановитель – отдает электроны Например: Na 0 – 1 e → Na+1 S-2 – 8 e → S+6 степ. окисл. хлора изменилась степ. окисл. не изменились N 2+1 O + 2 H 2 O S 0 + H 2 0 Следующее задание степ. окисл. азота изменились степ. окисл. водорода и серы изменились
Вернуться к заданию Объяснение А 27 Окислитель – отбирает электроны Например: Cu+2 + 2 e → Cu 0 N+5 + 3 e → N+2 1) 4 KCl+5 O 3 2) Са. СО 3 3) N-3 H 4 N+5 O 3 4) H 2+1 S-2 KCl-1 + 3 KCl+7 O 4 Ca. O + CO 2 Восстановитель – отдает электроны Например: Na 0 – 1 e → Na+1 S-2 – 8 e → S+6 степ. окисл. хлора изменилась степ. окисл. не изменились N 2+1 O + 2 H 2 O S 0 + H 2 0 Следующее задание степ. окисл. азота изменились степ. окисл. водорода и серы изменились
 Вернуться к заданию жир Объяснение А 28 щелочь + (можно заменить K 2 CO 3 или Na 2 CO 3) Следующее задание мыло = (соль высшей + жирной кислоты) глицерин Натриевые мыла – твердые, калиевые - жидкие Чем больше глицерина в мыле, тем сильнее эффект увлажнения (меньше вреда коже), но хуже моющие свойства Поскольку мыло состоит из остатка щелочи (сильного основания) и высшей жирной кислоты (слабой), то его среда щелочная Жесткая – это вода с большим содержанием солей Ca 2+ и Mg 2+. Из-за жесткой воды: 1) плохо растворяется мыло; 2) образуется накипь, известковый налет, которыми забиваются трубы, котлы и т. п. ; 3) сушится кожа, секутся волосы
Вернуться к заданию жир Объяснение А 28 щелочь + (можно заменить K 2 CO 3 или Na 2 CO 3) Следующее задание мыло = (соль высшей + жирной кислоты) глицерин Натриевые мыла – твердые, калиевые - жидкие Чем больше глицерина в мыле, тем сильнее эффект увлажнения (меньше вреда коже), но хуже моющие свойства Поскольку мыло состоит из остатка щелочи (сильного основания) и высшей жирной кислоты (слабой), то его среда щелочная Жесткая – это вода с большим содержанием солей Ca 2+ и Mg 2+. Из-за жесткой воды: 1) плохо растворяется мыло; 2) образуется накипь, известковый налет, которыми забиваются трубы, котлы и т. п. ; 3) сушится кожа, секутся волосы
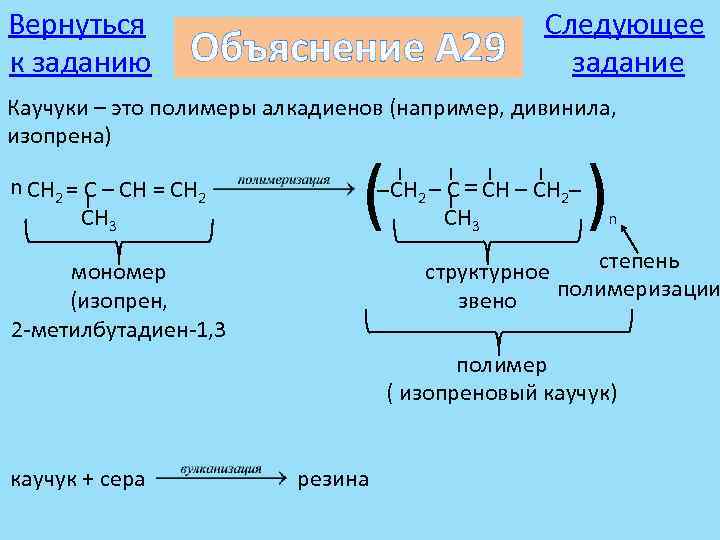 Вернуться к заданию Объяснение А 29 Следующее задание Каучуки – это полимеры алкадиенов (например, дивинила, изопрена) n CH 2 = C – CH = CH 2 CH 3 ( CH 2 – CH 2 CH 3 ) n степень структурное полимеризации звено мономер (изопрен, 2 -метилбутадиен-1, 3 полимер ( изопреновый каучук) каучук + сера резина
Вернуться к заданию Объяснение А 29 Следующее задание Каучуки – это полимеры алкадиенов (например, дивинила, изопрена) n CH 2 = C – CH = CH 2 CH 3 ( CH 2 – CH 2 CH 3 ) n степень структурное полимеризации звено мономер (изопрен, 2 -метилбутадиен-1, 3 полимер ( изопреновый каучук) каучук + сера резина
 Вернуться к заданию Дано: V (CH≡CH) = 10 л V (O 2) - ? Объяснение А 30 Следующее задание Решение: 2 CH≡CH + 5 O 2 → 4 CO 2 + 2 H 2 O Порядок расчета по 10 = объем. При n(CH≡CH) = V -= количеству вещества: молярный 0, 446 моль Vm 22, 4 1) найти количество известного вещества; н. у. равен 22, 4 л/моль 2) найти количество неизвестного n(CH≡CH) (составить пропорцию); вещества n(O 2) = 5 2 3) найти искомую величину. n(CH≡CH) 5 0, 446 5 = 1, 116 моль n(O 2) = = 2 2 V(O 2)= n Vm = 1, 116 Ответ: 25 л 22, 4 = 25 л
Вернуться к заданию Дано: V (CH≡CH) = 10 л V (O 2) - ? Объяснение А 30 Следующее задание Решение: 2 CH≡CH + 5 O 2 → 4 CO 2 + 2 H 2 O Порядок расчета по 10 = объем. При n(CH≡CH) = V -= количеству вещества: молярный 0, 446 моль Vm 22, 4 1) найти количество известного вещества; н. у. равен 22, 4 л/моль 2) найти количество неизвестного n(CH≡CH) (составить пропорцию); вещества n(O 2) = 5 2 3) найти искомую величину. n(CH≡CH) 5 0, 446 5 = 1, 116 моль n(O 2) = = 2 2 V(O 2)= n Vm = 1, 116 Ответ: 25 л 22, 4 = 25 л
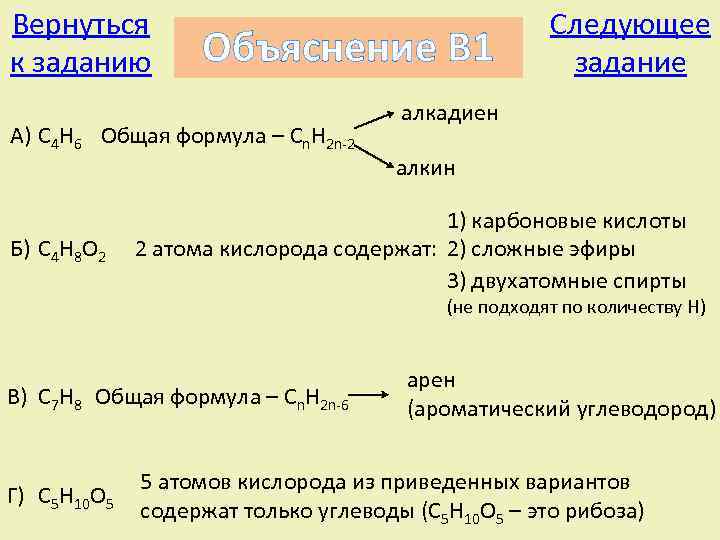 Вернуться к заданию Объяснение В 1 А) C 4 H 6 Общая формула – Cn. H 2 n-2 Б) C 4 H 8 O 2 Следующее задание алкадиен алкин 1) карбоновые кислоты 2 атома кислорода содержат: 2) сложные эфиры 3) двухатомные спирты (не подходят по количеству H) В) C 7 H 8 Общая формула – Cn. H 2 n-6 Г) C 5 H 10 O 5 арен (ароматический углеводород) 5 атомов кислорода из приведенных вариантов содержат только углеводы (C 5 H 10 O 5 – это рибоза)
Вернуться к заданию Объяснение В 1 А) C 4 H 6 Общая формула – Cn. H 2 n-2 Б) C 4 H 8 O 2 Следующее задание алкадиен алкин 1) карбоновые кислоты 2 атома кислорода содержат: 2) сложные эфиры 3) двухатомные спирты (не подходят по количеству H) В) C 7 H 8 Общая формула – Cn. H 2 n-6 Г) C 5 H 10 O 5 арен (ароматический углеводород) 5 атомов кислорода из приведенных вариантов содержат только углеводы (C 5 H 10 O 5 – это рибоза)
 Вернуться к заданию Объяснение В 2 Следующее задание Окислитель – отбирает электроны Восстановитель – отдает электроны Например: Cu+2 + 2 e → Cu 0 Например: Na 0 – 1 e → Na+1 N+5 + 3 e → N+2 S-2 – 8 e → S+6 У Н степ. окисл. в соединениях всегда +1, кроме гидридов (Na. H-1, Ca. H 2 -1) У О степ. окисл. в соединениях всегда -2, кроме пероксидов (H 2 O 2 -1, Na 2 O 2 -1), фторида кислорода (O+2 F 2) У щелочных (Li, Na, K, Rb, Cs и Fr) металлов степ. окисл. в соединениях всегда +1; у щелочноземельных металлов (Ca, Sr, Ba, Ra) +2 Во всех простых веществах степ. окисл. всегда равна 0 (Ba 0, O 30) +1 -2 0 0 +1 -1 А) H 2 S + I 2 = S + 2 H I 0 0 H 2 S – восстановитель, I 2 - окислитель +4 -2 Б) 2 S + С = С S 2 +6 -2 +1 -1 0 S – окислитель, C - восстановитель +4 -2 +1 +6 -2 В) 2 S O 3 + 2 K I = I 2 + S O 2 + K 2 S O 4 0 +4 -2 +6 -2 +2 -2 Г) S + 3 N O 2 = S O 3 + 3 N O SO 3 – окислитель, KI - восстановитель S – восстановитель, NO 2 - окислитель
Вернуться к заданию Объяснение В 2 Следующее задание Окислитель – отбирает электроны Восстановитель – отдает электроны Например: Cu+2 + 2 e → Cu 0 Например: Na 0 – 1 e → Na+1 N+5 + 3 e → N+2 S-2 – 8 e → S+6 У Н степ. окисл. в соединениях всегда +1, кроме гидридов (Na. H-1, Ca. H 2 -1) У О степ. окисл. в соединениях всегда -2, кроме пероксидов (H 2 O 2 -1, Na 2 O 2 -1), фторида кислорода (O+2 F 2) У щелочных (Li, Na, K, Rb, Cs и Fr) металлов степ. окисл. в соединениях всегда +1; у щелочноземельных металлов (Ca, Sr, Ba, Ra) +2 Во всех простых веществах степ. окисл. всегда равна 0 (Ba 0, O 30) +1 -2 0 0 +1 -1 А) H 2 S + I 2 = S + 2 H I 0 0 H 2 S – восстановитель, I 2 - окислитель +4 -2 Б) 2 S + С = С S 2 +6 -2 +1 -1 0 S – окислитель, C - восстановитель +4 -2 +1 +6 -2 В) 2 S O 3 + 2 K I = I 2 + S O 2 + K 2 S O 4 0 +4 -2 +6 -2 +2 -2 Г) S + 3 N O 2 = S O 3 + 3 N O SO 3 – окислитель, KI - восстановитель S – восстановитель, NO 2 - окислитель
 Вернуться к заданию Объяснение В 3 Следующее задание Электролиз растворов активные металлы, не выделяются на катоде, вместо них выделяется H 2 металлы средней активности, на катоде выделяются одновременно металл и H 2 OH-, NO 2 -, NO 3 -, SO 32 -, SO 42 -, CO 32 -, Si. O 32 -, PO 43 -… и Fвыделяется O 2 неактивные металлы, выделяются на катоде Cl-, Br-, I-, S 2 выделяются: Cl 2, Br 2, I 2, S A) Cu. SO 4 Cu – неактивный металл, выделяется на катоде Б) K 2 S K – активный металл, на катоде выделяется H 2 В) Ba. Cl 2 Ba – активный металл, на катоде выделяется H 2 Pb – металл средней активности, на катоде выделяется одновременно Pb и H 2 Г) Pb(NO 3)2
Вернуться к заданию Объяснение В 3 Следующее задание Электролиз растворов активные металлы, не выделяются на катоде, вместо них выделяется H 2 металлы средней активности, на катоде выделяются одновременно металл и H 2 OH-, NO 2 -, NO 3 -, SO 32 -, SO 42 -, CO 32 -, Si. O 32 -, PO 43 -… и Fвыделяется O 2 неактивные металлы, выделяются на катоде Cl-, Br-, I-, S 2 выделяются: Cl 2, Br 2, I 2, S A) Cu. SO 4 Cu – неактивный металл, выделяется на катоде Б) K 2 S K – активный металл, на катоде выделяется H 2 В) Ba. Cl 2 Ba – активный металл, на катоде выделяется H 2 Pb – металл средней активности, на катоде выделяется одновременно Pb и H 2 Г) Pb(NO 3)2
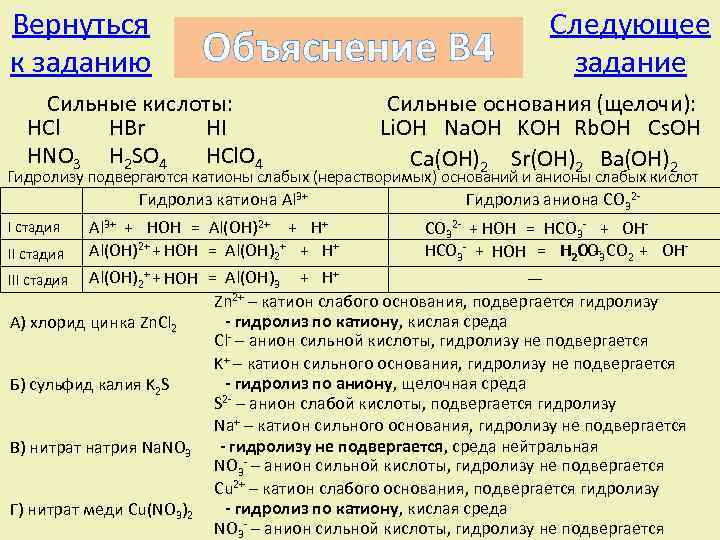 Вернуться к заданию Объяснение В 4 Сильные кислоты: HCl HBr HI HNO 3 H 2 SO 4 HCl. O 4 Следующее задание Сильные основания (щелочи): Li. OH Na. OH KOH Rb. OH Cs. OH Ca(OH)2 Sr(OH)2 Ba(OH)2 Гидролизу подвергаются катионы слабых (нерастворимых) оснований и анионы слабых кислот Гидролиз катиона Al 3+ I стадия II стадия Al 3+ + HOH = Al(OH)2+ + H+ Al(OH)2+ + HOH = Al(OH)2+ + H+ Гидролиз аниона CO 32 - + HOH = HCO 3 - + OHHCO 3 - + HOH = H 2 O +3 CO 2 + OHCO Al(OH)2+ + HOH = Al(OH)3 + H+ — Zn 2+ – катион слабого основания, подвергается гидролизу - гидролиз по катиону, кислая среда А) хлорид цинка Zn. Cl 2 Cl- – анион сильной кислоты, гидролизу не подвергается K+ – катион сильного основания, гидролизу не подвергается - гидролиз по аниону, щелочная среда Б) сульфид калия K 2 S 2 - – анион слабой кислоты, подвергается гидролизу S Na+ – катион сильного основания, гидролизу не подвергается - гидролизу не подвергается, среда нейтральная В) нитрат натрия Na. NO 3 - – анион сильной кислоты, гидролизу не подвергается Cu 2+ – катион слабого основания, подвергается гидролизу - гидролиз по катиону, кислая среда Г) нитрат меди Cu(NO 3)2 NO 3 - – анион сильной кислоты, гидролизу не подвергается III стадия
Вернуться к заданию Объяснение В 4 Сильные кислоты: HCl HBr HI HNO 3 H 2 SO 4 HCl. O 4 Следующее задание Сильные основания (щелочи): Li. OH Na. OH KOH Rb. OH Cs. OH Ca(OH)2 Sr(OH)2 Ba(OH)2 Гидролизу подвергаются катионы слабых (нерастворимых) оснований и анионы слабых кислот Гидролиз катиона Al 3+ I стадия II стадия Al 3+ + HOH = Al(OH)2+ + H+ Al(OH)2+ + HOH = Al(OH)2+ + H+ Гидролиз аниона CO 32 - + HOH = HCO 3 - + OHHCO 3 - + HOH = H 2 O +3 CO 2 + OHCO Al(OH)2+ + HOH = Al(OH)3 + H+ — Zn 2+ – катион слабого основания, подвергается гидролизу - гидролиз по катиону, кислая среда А) хлорид цинка Zn. Cl 2 Cl- – анион сильной кислоты, гидролизу не подвергается K+ – катион сильного основания, гидролизу не подвергается - гидролиз по аниону, щелочная среда Б) сульфид калия K 2 S 2 - – анион слабой кислоты, подвергается гидролизу S Na+ – катион сильного основания, гидролизу не подвергается - гидролизу не подвергается, среда нейтральная В) нитрат натрия Na. NO 3 - – анион сильной кислоты, гидролизу не подвергается Cu 2+ – катион слабого основания, подвергается гидролизу - гидролиз по катиону, кислая среда Г) нитрат меди Cu(NO 3)2 NO 3 - – анион сильной кислоты, гидролизу не подвергается III стадия
 Вернуться к заданию Объяснение В 5 Следующее задание реакция возможна Железо Fe Al только следующие оксида чем Fe + Fe 2 O 3 == Al 2 O 3 +образует – более активный 2 металл, Fe. O и. Fe 2 O 3 реагируют ≠ неметаллы (за некоторыми исключениями) с оксидами не реагирует с HNO 3 – окислительная кислота, = Na. NO 34+NO+H+O HNOметаллами. NOобразованием NOот NO с Al(NO 3+H 2 O+NOHобразованием NO в зависимости или )3 + NO 2 (NO, 3 N 2 окислительная кислота, реагирует O – O, NH 4 с 3 или NO + HNO 3 (р-р) ≠ H 2 SO 2 концентрации кислотыя 2 2 из металлов со щелочами реагирует только + Na. OH (р-р)=≠Na[Al(OH)4 с]+H 2 Al и нек. не реагируют со щелочами ≠ неметаллы основаниями другие металлы Al и нек. другие металлы O образовывать с неметаллами кислородом до собой + Fe == металлы могут реагируютокисляется. NHно между собой не реагируют Fe 3 O 4 ≠≠ Fe. S металлы образовывать сплавы, NO в зависимостине реагируют Fe. O + Feмогут. Железо (NO, N сплавы, но между железной окалины 2 3 от 4 3 H 2 (NO или в ==Al(NO 3)43+3+HOO+NOили NOв 2 O, зависимости концентрации HNO 3) 3) H 2 SO +H 2 O 2++ (NO NO 2 2 зависимости от от концентрации HNO + HNO 3 = Na. NO ≠ концентрации кислоты Na металл левее H, + HI = Al. I 3 ++H 22 HI ––сильный восстановитель, окисляется кислородом = теоретически реакция возможна реагирует с водой и кислотами Na. I + HI 2 Al –металл левее H, реагирует с водой и кислотами H 2 O В) S + Fe=≠Fe. S металлы O 3 образовывать сплавы, но между собой не реагируют Г) Na =≠ Fe. O + Fe 2 могут А) Al 2 Б) O кислотные –некоторыми исключениями) с оксидами не реагируют ≠неметаллы (заоксиды металлами не реагируют «+3» не высшая степ. окисл. фосфора + P 2 O 3 ≠=≠ Pкислотныеоксиды ссметаллами не реагируют 2 O 5 ацетилен реакция с O 2 без катализатора – это реакция горения. алкины реагируют очень активными алкины не реагируют только + C 2 H 2 ≠→ CH≡CNaреагирует с серой с очень активными металлами H 2 O =≠CO 2 + H 2 O + H 2 углеводороды горят ссобразованием CO 2 металлами Все + + H 2 O = Al(OH)3+HHAl –Na – металл левее. H, реагируетссводой и и кислотами = Na. OH + 2 2 металлы ≠ ≠ сера с водой не реагирует левее H, реагирует водой кислотами = Na. Cl металлы реагируют неметаллами Al. Cl 3 с кислородом не реагируют + Cl 2 ≠ SCl 4 или металлы зависимостисот количества хлора = галогены SCl 6 в реагируютс неметаллами Na менее активный металл, неметаллы активный металл, чем Ca + Ca. Cl 2 ≠ Кислород с солями не реагирует чем Ca с солями не реагируют ≠ Al – – менее(за некоторыми исключениями) Al и нек. другие металлы + KOH =≠ K[Al(OH)4]+H 2 (или KAl. Oреагирует только со щелочами = из металлов со щелочами 2 + H 2) реагируют Al и нек. другие ≠ реакция возможна кислоты (кроме сильных окислителей и HCl окислительная левее H, реагирует неметаллами не реагирует = Al. Cl 3 – не. H 2 Al. Na металл кислота, сне реагируют водой кислотами + HCl ≠ Na. Cl++H 2 – – металл левее. H, реагируетссводой и и кислотами восстановителей) с неметаллами металлы реагируют неметаллами + H 2 == Al. H 3 неметаллы реагируют между собой = HHOS металлы реагируют смежду собой Na. H неметаллыреагируют неметаллами 22
Вернуться к заданию Объяснение В 5 Следующее задание реакция возможна Железо Fe Al только следующие оксида чем Fe + Fe 2 O 3 == Al 2 O 3 +образует – более активный 2 металл, Fe. O и. Fe 2 O 3 реагируют ≠ неметаллы (за некоторыми исключениями) с оксидами не реагирует с HNO 3 – окислительная кислота, = Na. NO 34+NO+H+O HNOметаллами. NOобразованием NOот NO с Al(NO 3+H 2 O+NOHобразованием NO в зависимости или )3 + NO 2 (NO, 3 N 2 окислительная кислота, реагирует O – O, NH 4 с 3 или NO + HNO 3 (р-р) ≠ H 2 SO 2 концентрации кислотыя 2 2 из металлов со щелочами реагирует только + Na. OH (р-р)=≠Na[Al(OH)4 с]+H 2 Al и нек. не реагируют со щелочами ≠ неметаллы основаниями другие металлы Al и нек. другие металлы O образовывать с неметаллами кислородом до собой + Fe == металлы могут реагируютокисляется. NHно между собой не реагируют Fe 3 O 4 ≠≠ Fe. S металлы образовывать сплавы, NO в зависимостине реагируют Fe. O + Feмогут. Железо (NO, N сплавы, но между железной окалины 2 3 от 4 3 H 2 (NO или в ==Al(NO 3)43+3+HOO+NOили NOв 2 O, зависимости концентрации HNO 3) 3) H 2 SO +H 2 O 2++ (NO NO 2 2 зависимости от от концентрации HNO + HNO 3 = Na. NO ≠ концентрации кислоты Na металл левее H, + HI = Al. I 3 ++H 22 HI ––сильный восстановитель, окисляется кислородом = теоретически реакция возможна реагирует с водой и кислотами Na. I + HI 2 Al –металл левее H, реагирует с водой и кислотами H 2 O В) S + Fe=≠Fe. S металлы O 3 образовывать сплавы, но между собой не реагируют Г) Na =≠ Fe. O + Fe 2 могут А) Al 2 Б) O кислотные –некоторыми исключениями) с оксидами не реагируют ≠неметаллы (заоксиды металлами не реагируют «+3» не высшая степ. окисл. фосфора + P 2 O 3 ≠=≠ Pкислотныеоксиды ссметаллами не реагируют 2 O 5 ацетилен реакция с O 2 без катализатора – это реакция горения. алкины реагируют очень активными алкины не реагируют только + C 2 H 2 ≠→ CH≡CNaреагирует с серой с очень активными металлами H 2 O =≠CO 2 + H 2 O + H 2 углеводороды горят ссобразованием CO 2 металлами Все + + H 2 O = Al(OH)3+HHAl –Na – металл левее. H, реагируетссводой и и кислотами = Na. OH + 2 2 металлы ≠ ≠ сера с водой не реагирует левее H, реагирует водой кислотами = Na. Cl металлы реагируют неметаллами Al. Cl 3 с кислородом не реагируют + Cl 2 ≠ SCl 4 или металлы зависимостисот количества хлора = галогены SCl 6 в реагируютс неметаллами Na менее активный металл, неметаллы активный металл, чем Ca + Ca. Cl 2 ≠ Кислород с солями не реагирует чем Ca с солями не реагируют ≠ Al – – менее(за некоторыми исключениями) Al и нек. другие металлы + KOH =≠ K[Al(OH)4]+H 2 (или KAl. Oреагирует только со щелочами = из металлов со щелочами 2 + H 2) реагируют Al и нек. другие ≠ реакция возможна кислоты (кроме сильных окислителей и HCl окислительная левее H, реагирует неметаллами не реагирует = Al. Cl 3 – не. H 2 Al. Na металл кислота, сне реагируют водой кислотами + HCl ≠ Na. Cl++H 2 – – металл левее. H, реагируетссводой и и кислотами восстановителей) с неметаллами металлы реагируют неметаллами + H 2 == Al. H 3 неметаллы реагируют между собой = HHOS металлы реагируют смежду собой Na. H неметаллыреагируют неметаллами 22
 Вернуться к заданию CH 2 CH Объяснение В 6 Следующее задание CH 3 + HBr → CH 2 CH CH 3 3 H Br 2 -бромпропан Правило Марковникова: присоединении галогенводородов или воды к алкенам или алкинам атом водорода присоединяется атому углерода, соединенному с большим количествам атомов водорода (в месте разрыва двойной связи. ) В реакции из двух веществ получается одно – реакция соединения σ-связи – все первые, π-связи – вторые и третьи. В данном случае, была одна πсвязь, она разорвалась По ионному механизму присоединяются: H 2 O, HF, HCl, HBr, HI и Cl 2 при 5000 С; по радикальному механизму: H 2, F 2, Cl 2, Br 2, I 2
Вернуться к заданию CH 2 CH Объяснение В 6 Следующее задание CH 3 + HBr → CH 2 CH CH 3 3 H Br 2 -бромпропан Правило Марковникова: присоединении галогенводородов или воды к алкенам или алкинам атом водорода присоединяется атому углерода, соединенному с большим количествам атомов водорода (в месте разрыва двойной связи. ) В реакции из двух веществ получается одно – реакция соединения σ-связи – все первые, π-связи – вторые и третьи. В данном случае, была одна πсвязь, она разорвалась По ионному механизму присоединяются: H 2 O, HF, HCl, HBr, HI и Cl 2 при 5000 С; по радикальному механизму: H 2, F 2, Cl 2, Br 2, I 2
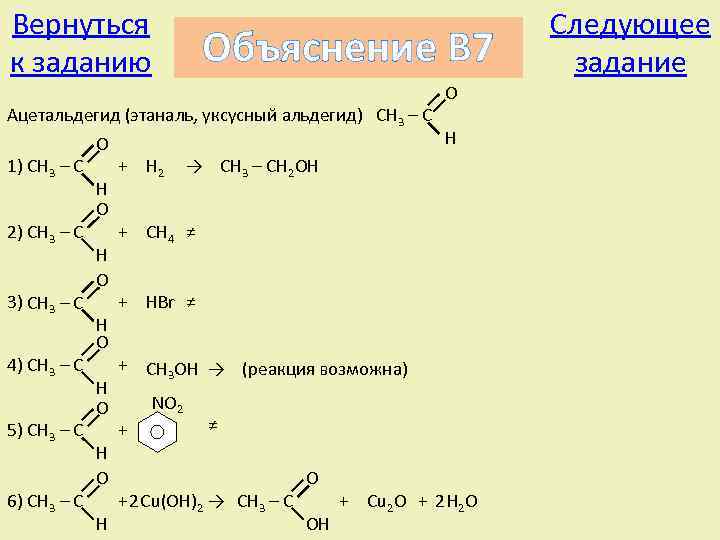 Вернуться к заданию Объяснение В 7 O Ацетальдегид (этаналь, уксусный альдегид) CH 3 – C H O 1) CH 3 – C + H 2 → CH 3 – CH 2 OH H O 2) CH 3 – C + CH 4 ≠ H O 3) CH 3 – C + HBr ≠ H O 4) CH 3 – C + CH 3 OH → (реакция возможна) H NO 2 O ≠ 5) CH 3 – C + H O O 6) CH 3 – C + 2 Cu(OH)2 → CH 3 – C + Cu 2 O + 2 H 2 O H OH Следующее задание
Вернуться к заданию Объяснение В 7 O Ацетальдегид (этаналь, уксусный альдегид) CH 3 – C H O 1) CH 3 – C + H 2 → CH 3 – CH 2 OH H O 2) CH 3 – C + CH 4 ≠ H O 3) CH 3 – C + HBr ≠ H O 4) CH 3 – C + CH 3 OH → (реакция возможна) H NO 2 O ≠ 5) CH 3 – C + H O O 6) CH 3 – C + 2 Cu(OH)2 → CH 3 – C + Cu 2 O + 2 H 2 O H OH Следующее задание
 Вернуться к заданию Объяснение В 8 Глюкоза C 6 H 12 O 6 содержит альдегидную группу - C O Следующее задание и 5 гидроксильных групп -OH H Сахароза C 12 H 22 O 11 также содержит гидроксильные группы, но не содержит альдегидных групп 1) Глюкоза окисляется кислородом (по альдегидной группе), а сахароза нет 2) H 2 SO 4 (конц. ) может отнимать воду и от глюкозы, и от сахарозы 3) Глюкоза может восстанавливаться водородом (по альдегидной группе), а сахароза нет 4) Глюкоза может окисляться аммиачным раствором оксида серебра (по альдегидной группе), а сахароза нет 5) И глюкоза, и сахароза могут реагировать с кислотами 6) Все многоатомные спирты (в том числе глюкоза и сахароза) могут реагировать с гидроксидом меди (II)
Вернуться к заданию Объяснение В 8 Глюкоза C 6 H 12 O 6 содержит альдегидную группу - C O Следующее задание и 5 гидроксильных групп -OH H Сахароза C 12 H 22 O 11 также содержит гидроксильные группы, но не содержит альдегидных групп 1) Глюкоза окисляется кислородом (по альдегидной группе), а сахароза нет 2) H 2 SO 4 (конц. ) может отнимать воду и от глюкозы, и от сахарозы 3) Глюкоза может восстанавливаться водородом (по альдегидной группе), а сахароза нет 4) Глюкоза может окисляться аммиачным раствором оксида серебра (по альдегидной группе), а сахароза нет 5) И глюкоза, и сахароза могут реагировать с кислотами 6) Все многоатомные спирты (в том числе глюкоза и сахароза) могут реагировать с гидроксидом меди (II)
 Вернуться к заданию Объяснение В 9 mвещества ω= mраствора (смеси) mв-ва = mр-ра (смеси) × ω m 1 (Ca. Cl 2) = mр-ра 1 × ω1= 140 × 0, 05 = 7 г ω2 (Ca. Cl 2) = 7 + 10 140 + 10 = 0, 1133 = 11, 33% Ответ с точностью до десятых: 11, 3% Следующее задание
Вернуться к заданию Объяснение В 9 mвещества ω= mраствора (смеси) mв-ва = mр-ра (смеси) × ω m 1 (Ca. Cl 2) = mр-ра 1 × ω1= 140 × 0, 05 = 7 г ω2 (Ca. Cl 2) = 7 + 10 140 + 10 = 0, 1133 = 11, 33% Ответ с точностью до десятых: 11, 3% Следующее задание
 Вернуться к заданию Объяснение Fe. S + 2 HCl = Fe. Cl 2 + H 2 S n(Fe. S)= n(H 2 S) 0, 3 = n(H 2 S) 1 1 n(H 2 S) = 0, 3 моль V(H 2 S)= n Vm = 0, 3 22, 4= 6, 72 л Ответ с точностью до сотых: 6, 72 л В 10 Следующее задание
Вернуться к заданию Объяснение Fe. S + 2 HCl = Fe. Cl 2 + H 2 S n(Fe. S)= n(H 2 S) 0, 3 = n(H 2 S) 1 1 n(H 2 S) = 0, 3 моль V(H 2 S)= n Vm = 0, 3 22, 4= 6, 72 л Ответ с точностью до сотых: 6, 72 л В 10 Следующее задание
 Вернуться к заданию Объяснение С 1 Следующее задание I 2 + K 2 SO 3 +2 KOH → K 2 SO 4 + 2 KI + Н 2 О S I 2 +4 0 -2 e → S +2 e → 2 I +6 -1 2 1 восстановитель, окисление 2 1 окислитель, восстановление Сначала определим неизвестные продукты В левой части есть восстановитель (K 2 SO 3→K 2 SO 4), значит I 2 будет окислителем. Осталось определить среду (кислота, H 2 O или щелочь) В правой части уже присутствует H 2 O, значит средой будет являться кислота либо щелочь. Удобно взять щелочь KOH Восстановленная форма йода будет соединяться со средой (с KOH) Составим схемы окисления и восстановления Расставим коэффициенты, чтобы уравнять левую и правую части
Вернуться к заданию Объяснение С 1 Следующее задание I 2 + K 2 SO 3 +2 KOH → K 2 SO 4 + 2 KI + Н 2 О S I 2 +4 0 -2 e → S +2 e → 2 I +6 -1 2 1 восстановитель, окисление 2 1 окислитель, восстановление Сначала определим неизвестные продукты В левой части есть восстановитель (K 2 SO 3→K 2 SO 4), значит I 2 будет окислителем. Осталось определить среду (кислота, H 2 O или щелочь) В правой части уже присутствует H 2 O, значит средой будет являться кислота либо щелочь. Удобно взять щелочь KOH Восстановленная форма йода будет соединяться со средой (с KOH) Составим схемы окисления и восстановления Расставим коэффициенты, чтобы уравнять левую и правую части
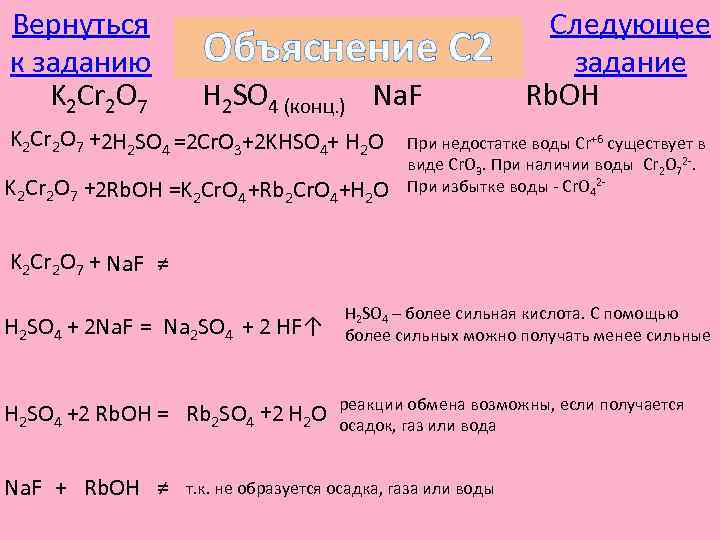 Вернуться к заданию K 2 Cr 2 O 7 Объяснение С 2 H 2 SO 4 (конц. ) Na. F K 2 Cr 2 O 7 +2 H 2 SO 4 =2 Cr. O 3+2 KHSO 4+ H 2 O K 2 Cr 2 O 7 +2 Rb. OH =K 2 Cr. O 4 +Rb 2 Cr. O 4+H 2 O Следующее задание Rb. OH При недостатке воды Cr+6 существует в виде Cr. O 3. При наличии воды Cr 2 O 72 -. При избытке воды - Cr. O 42 - K 2 Cr 2 O 7 + Na. F ≠ H 2 SO 4 + 2 Na. F = Na 2 SO 4 + 2 HF↑ H 2 SO 4 +2 Rb. OH = Rb 2 SO 4 +2 H 2 O Na. F + Rb. OH ≠ H 2 SO 4 – более сильная кислота. С помощью более сильных можно получать менее сильные реакции обмена возможны, если получается осадок, газ или вода т. к. не образуется осадка, газа или воды
Вернуться к заданию K 2 Cr 2 O 7 Объяснение С 2 H 2 SO 4 (конц. ) Na. F K 2 Cr 2 O 7 +2 H 2 SO 4 =2 Cr. O 3+2 KHSO 4+ H 2 O K 2 Cr 2 O 7 +2 Rb. OH =K 2 Cr. O 4 +Rb 2 Cr. O 4+H 2 O Следующее задание Rb. OH При недостатке воды Cr+6 существует в виде Cr. O 3. При наличии воды Cr 2 O 72 -. При избытке воды - Cr. O 42 - K 2 Cr 2 O 7 + Na. F ≠ H 2 SO 4 + 2 Na. F = Na 2 SO 4 + 2 HF↑ H 2 SO 4 +2 Rb. OH = Rb 2 SO 4 +2 H 2 O Na. F + Rb. OH ≠ H 2 SO 4 – более сильная кислота. С помощью более сильных можно получать менее сильные реакции обмена возможны, если получается осадок, газ или вода т. к. не образуется осадка, газа или воды
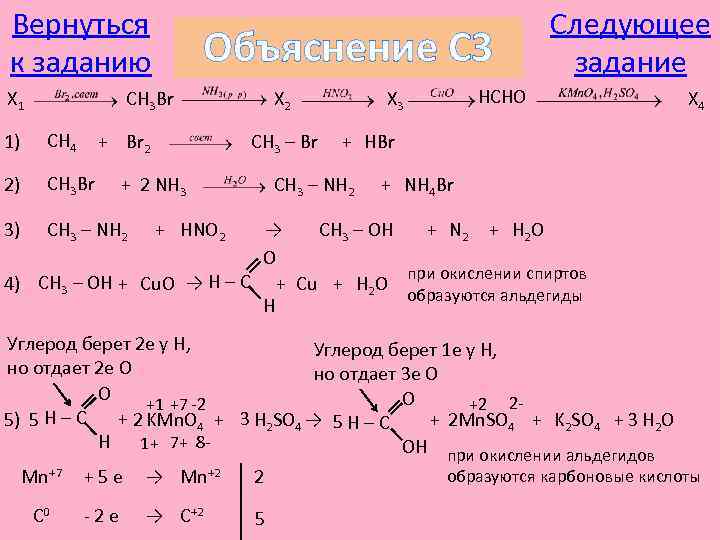 Вернуться к заданию X 1 Объяснение С 3 CH 3 Br 1) CH 4 2) CH 3 Br 3) CH 3 – NH 2 + Br 2 X 2 CH 3 – Br + 2 NH 3 Следующее задание HCHO X 3 X 4 + HBr CH 3 – NH 2 + NH 4 Br + HNO 2 → CH 3 – OH + N 2 + H 2 O O при окислении спиртов 4) CH 3 – OH + Cu. O → H – C + Cu + H 2 O образуются альдегиды H Углерод берет 2 e у H, Углерод берет 1 e у H, но отдает 2 e O но отдает 3 e O O O +1 +7 -2 +2 2+ 2 KMn. O 4 + 3 H 2 SO 4 → 5 H – C 5) 5 H – C + 2 Mn. SO 4 + K 2 SO 4 + 3 H 2 O H 1+ 7+ 8 OH Mn+7 +5 e → Mn+2 2 C 0 -2 e → C+2 5 при окислении альдегидов образуются карбоновые кислоты
Вернуться к заданию X 1 Объяснение С 3 CH 3 Br 1) CH 4 2) CH 3 Br 3) CH 3 – NH 2 + Br 2 X 2 CH 3 – Br + 2 NH 3 Следующее задание HCHO X 3 X 4 + HBr CH 3 – NH 2 + NH 4 Br + HNO 2 → CH 3 – OH + N 2 + H 2 O O при окислении спиртов 4) CH 3 – OH + Cu. O → H – C + Cu + H 2 O образуются альдегиды H Углерод берет 2 e у H, Углерод берет 1 e у H, но отдает 2 e O но отдает 3 e O O O +1 +7 -2 +2 2+ 2 KMn. O 4 + 3 H 2 SO 4 → 5 H – C 5) 5 H – C + 2 Mn. SO 4 + K 2 SO 4 + 3 H 2 O H 1+ 7+ 8 OH Mn+7 +5 e → Mn+2 2 C 0 -2 e → C+2 5 при окислении альдегидов образуются карбоновые кислоты
 Вернуться к заданию Объяснение С 4 Следующее задание Нитрит калия массой 8, 5 г внесли при нагревании в 270 г раствора бромида аммония с массовой долей 12%. Какой объем (н. у. ) азота выделится при этом и какова массовая доля бромида аммония в получившемся растворе? Дано: Решение: KNO 2 + NH 4 Br = N 2 + KBr + 2 H 2 O m (KNO 2) = 8, 5 г 391432 m 8, 5 = молярная массамоль по табл. Менделеева = 0, 1 считается mр (NH 4 Br) = 270 г n(KNO 2) = M 85 270 • 12 ω (NH 4 Br) = 12% = 32, 4 г m(NH 4 Br) = 100 14 4 80 V (N 2) - ? m 32, 4 n(NH 4 Br)= = = 0, 33 моль ω (NH 4 Br) - ? M 98 KNO 2 в недостатке, n(N 2) = 0, 1 моль V(N 2) = n • Vm = 0, 1 • молярный объем при н. у. всегда равен 22, 4 л/моль 22, 4 = 2, 24 л m(конечной смеси) = m(KNO 2) + mр(NH 4 Br) – m(N 2) n(NH 4 Br непрореагировавшего) = 0, 23 моль m(NH 4 Br непрореагировавшего) = n • M = 0, 23 • 98 = 22, 54 г 28 m(N 2) = n • M = 0, 1 • 28 = 2, 8 г m(вещества) 22, 54 ω(NH 4 Br) = = = 0, 082 = 8, 2 % m(смеси) 8, 5 + 270 – 2, 8 Ответы: 1) V(N 2) = 2, 24 л; 2) ω(NH 4 Br) = 8, 2%
Вернуться к заданию Объяснение С 4 Следующее задание Нитрит калия массой 8, 5 г внесли при нагревании в 270 г раствора бромида аммония с массовой долей 12%. Какой объем (н. у. ) азота выделится при этом и какова массовая доля бромида аммония в получившемся растворе? Дано: Решение: KNO 2 + NH 4 Br = N 2 + KBr + 2 H 2 O m (KNO 2) = 8, 5 г 391432 m 8, 5 = молярная массамоль по табл. Менделеева = 0, 1 считается mр (NH 4 Br) = 270 г n(KNO 2) = M 85 270 • 12 ω (NH 4 Br) = 12% = 32, 4 г m(NH 4 Br) = 100 14 4 80 V (N 2) - ? m 32, 4 n(NH 4 Br)= = = 0, 33 моль ω (NH 4 Br) - ? M 98 KNO 2 в недостатке, n(N 2) = 0, 1 моль V(N 2) = n • Vm = 0, 1 • молярный объем при н. у. всегда равен 22, 4 л/моль 22, 4 = 2, 24 л m(конечной смеси) = m(KNO 2) + mр(NH 4 Br) – m(N 2) n(NH 4 Br непрореагировавшего) = 0, 23 моль m(NH 4 Br непрореагировавшего) = n • M = 0, 23 • 98 = 22, 54 г 28 m(N 2) = n • M = 0, 1 • 28 = 2, 8 г m(вещества) 22, 54 ω(NH 4 Br) = = = 0, 082 = 8, 2 % m(смеси) 8, 5 + 270 – 2, 8 Ответы: 1) V(N 2) = 2, 24 л; 2) ω(NH 4 Br) = 8, 2%
 Вернуться к заданию Объяснение С 5 К выбору задания Определите молекулярную формулу ацетиленового углеводорода, если молярная масса продукта его реакции с избытком бромоводорода в 4 раза больше, чем молярная масса исходного углеводорода. CH≡CH CH≡C - … ацетиленовые углеводороды (алкины) Cn. H 2 n-2 общая формула алкинов Пример реакции алкинов с избытком бромоводорода: CH≡CH + 2 HBr → CH 2 Br – CH 2 Br Cn. H 2 n-2 + 2 HBr → Cn. H 2 n. Br 2 M(Cn. H 2 n-2) = 12 n + 2 n-2 = 14 n-2 14 n+160 14 n-2 = 4 56 n – 8 = 14 n + 160 Ответ: C 4 H 6 M(Cn. H 2 n. Br 2) = 12 n + 160 = 14 n+160 (14 n-2) • 4 = 14 n + 160 42 n = 168 n=4
Вернуться к заданию Объяснение С 5 К выбору задания Определите молекулярную формулу ацетиленового углеводорода, если молярная масса продукта его реакции с избытком бромоводорода в 4 раза больше, чем молярная масса исходного углеводорода. CH≡CH CH≡C - … ацетиленовые углеводороды (алкины) Cn. H 2 n-2 общая формула алкинов Пример реакции алкинов с избытком бромоводорода: CH≡CH + 2 HBr → CH 2 Br – CH 2 Br Cn. H 2 n-2 + 2 HBr → Cn. H 2 n. Br 2 M(Cn. H 2 n-2) = 12 n + 2 n-2 = 14 n-2 14 n+160 14 n-2 = 4 56 n – 8 = 14 n + 160 Ответ: C 4 H 6 M(Cn. H 2 n. Br 2) = 12 n + 160 = 14 n+160 (14 n-2) • 4 = 14 n + 160 42 n = 168 n=4


