ЕГЭ (demo-2008).pptx
- Количество слайдов: 130
 Подготовка к ЕГЭ по химии Демо-версия ЕГЭ-2008 Автор: Репетацких Дмитрий Николаевич Магнитогорск, 2011
Подготовка к ЕГЭ по химии Демо-версия ЕГЭ-2008 Автор: Репетацких Дмитрий Николаевич Магнитогорск, 2011
 СПРАВОЧНЫЕ ТАБЛИЦЫ 1. Периодическая система химических элементов Д. И. Менделеева 2. Таблица растворимости 3. Ряд напряжений металлов 4. Простые вещества- металлы, неметаллы 5. Оксиды 6. Кислоты и кислотные остатки К выбору задания
СПРАВОЧНЫЕ ТАБЛИЦЫ 1. Периодическая система химических элементов Д. И. Менделеева 2. Таблица растворимости 3. Ряд напряжений металлов 4. Простые вещества- металлы, неметаллы 5. Оксиды 6. Кислоты и кислотные остатки К выбору задания
 А 1 А 11 А 21 В 1 А 2 А 12 А 22 В 2 А 3 А 13 А 23 В 3 А 4 А 14 А 24 В 4 А 5 А 15 А 25 В 5 А 6 А 16 А 26 В 6 А 7 А 17 А 27 В 7 А 8 А 18 А 28 В 8 А 9 А 19 А 29 В 9 А 10 А 20 А 30 В 10 С 1 С 2 С 3 С 4 С 5
А 1 А 11 А 21 В 1 А 2 А 12 А 22 В 2 А 3 А 13 А 23 В 3 А 4 А 14 А 24 В 4 А 5 А 15 А 25 В 5 А 6 А 16 А 26 В 6 А 7 А 17 А 27 В 7 А 8 А 18 А 28 В 8 А 9 А 19 А 29 В 9 А 10 А 20 А 30 В 10 С 1 С 2 С 3 С 4 С 5
 А 1. Число электронов в ионе железа Fe 2+ равно 1) 54 2) 28 3) 58 4) 24 Справочные таблицы Следующее задание К выбору задания
А 1. Число электронов в ионе железа Fe 2+ равно 1) 54 2) 28 3) 58 4) 24 Справочные таблицы Следующее задание К выбору задания
 А 2. Среди элементов VIА группы максимальный радиус атома имеет 1) кислород 2) сера 3) теллур 4) полоний Справочные таблицы Следующее задание К выбору задания
А 2. Среди элементов VIА группы максимальный радиус атома имеет 1) кислород 2) сера 3) теллур 4) полоний Справочные таблицы Следующее задание К выбору задания
 А 3. Водородная связь образуется между молекулами 1) этана 2) бензола 3) водорода 4) этанола Справочные таблицы Следующее задание К выбору задания
А 3. Водородная связь образуется между молекулами 1) этана 2) бензола 3) водорода 4) этанола Справочные таблицы Следующее задание К выбору задания
 А 4. Степень окисления, равную + 4, атом серы имеет в соединении 1) H 2 SO 4 2) Fe. S 2 3) H 2 SO 3 4) Na. HSO 4 Справочные таблицы Следующее задание К выбору задания
А 4. Степень окисления, равную + 4, атом серы имеет в соединении 1) H 2 SO 4 2) Fe. S 2 3) H 2 SO 3 4) Na. HSO 4 Справочные таблицы Следующее задание К выбору задания
 А 5. Веществом молекулярного строения является 1) озон 2) оксид бария 3) графит 4) сульфид калия Справочные таблицы Следующее задание К выбору задания
А 5. Веществом молекулярного строения является 1) озон 2) оксид бария 3) графит 4) сульфид калия Справочные таблицы Следующее задание К выбору задания
 А 6. Амфотерным гидроксидом и кислотой соответственно являются 1) H 2 SO 4 и Zn(OH)Cl 2) Ca(OH)2 и HCl 3) KHSO 4 и Na. OH 4) Al(OH)3 и HNO 3 Справочные таблицы Следующее задание К выбору задания
А 6. Амфотерным гидроксидом и кислотой соответственно являются 1) H 2 SO 4 и Zn(OH)Cl 2) Ca(OH)2 и HCl 3) KHSO 4 и Na. OH 4) Al(OH)3 и HNO 3 Справочные таблицы Следующее задание К выбору задания
 А 7. В каком ряду химические элементы расположены в порядке усиления металлических свойств? 1) Na, Mg, Al 2) Al, Mg, Na 3) Cа, Mg, Be 4) Mg, Be, Cа Справочные таблицы Следующее задание К выбору задания
А 7. В каком ряду химические элементы расположены в порядке усиления металлических свойств? 1) Na, Mg, Al 2) Al, Mg, Na 3) Cа, Mg, Be 4) Mg, Be, Cа Справочные таблицы Следующее задание К выбору задания
 А 8. Формула высшего оксида хлора 1) Cl 2 O 2) Cl. O 2 3) Cl 2 O 6 4) Cl 2 O 7 Справочные таблицы Следующее задание К выбору задания
А 8. Формула высшего оксида хлора 1) Cl 2 O 2) Cl. O 2 3) Cl 2 O 6 4) Cl 2 O 7 Справочные таблицы Следующее задание К выбору задания
 А 9. Верны ли следующие суждения о меди? А. Для меди характерны степени окисления + 1 и + 2 Б. Медь вытесняет цинк из раствора сульфата цинка 1) верно только А 2) верно только Б 3) верны оба суждения 4) оба суждения неверны Справочные таблицы Следующее задание К выбору задания
А 9. Верны ли следующие суждения о меди? А. Для меди характерны степени окисления + 1 и + 2 Б. Медь вытесняет цинк из раствора сульфата цинка 1) верно только А 2) верно только Б 3) верны оба суждения 4) оба суждения неверны Справочные таблицы Следующее задание К выбору задания
 А 10. Оксид кальция взаимодействует с каждым из трех веществ: 1) кислород, вода, серная кислота 2) соляная кислота, углекислый газ, вода 3) оксид магния, оксид серы (IV), аммиак 4) железо, азотная кислота, оксид фосфора (V) Справочные таблицы Следующее задание К выбору задания
А 10. Оксид кальция взаимодействует с каждым из трех веществ: 1) кислород, вода, серная кислота 2) соляная кислота, углекислый газ, вода 3) оксид магния, оксид серы (IV), аммиак 4) железо, азотная кислота, оксид фосфора (V) Справочные таблицы Следующее задание К выбору задания
 А 11. Гидроксид хрома (III) взаимодействует с каждым из двух веществ: 1) СО 2 и HCl 2) Si. О 2 и Cu(OH)2 3) NО и Na. NO 3 4) H 2 SO 4 и Na. OH Справочные таблицы Следующее задание К выбору задания
А 11. Гидроксид хрома (III) взаимодействует с каждым из двух веществ: 1) СО 2 и HCl 2) Si. О 2 и Cu(OH)2 3) NО и Na. NO 3 4) H 2 SO 4 и Na. OH Справочные таблицы Следующее задание К выбору задания
 А 12. Карбонат кальция реагирует с 1) HCl 2) Mg. O 3) Pb 4) H 2 O Справочные таблицы Следующее задание К выбору задания
А 12. Карбонат кальция реагирует с 1) HCl 2) Mg. O 3) Pb 4) H 2 O Справочные таблицы Следующее задание К выбору задания
 А 13. В схеме превращений Ba Ba(OH)2 Ba. Cl 2 веществами «X» и «Y» соответственно являются 1) KOH и HCl 2) Na. OH и Cl 2 3) H 2 O и KCl 4) H 2 O и HCl Справочные таблицы Следующее задание К выбору задания
А 13. В схеме превращений Ba Ba(OH)2 Ba. Cl 2 веществами «X» и «Y» соответственно являются 1) KOH и HCl 2) Na. OH и Cl 2 3) H 2 O и KCl 4) H 2 O и HCl Справочные таблицы Следующее задание К выбору задания
 А 14. Алкины являются структурными изомерами 1) алкадиенов 2) алканов 3) циклоалканов 4) алкенов Справочные таблицы Следующее задание К выбору задания
А 14. Алкины являются структурными изомерами 1) алкадиенов 2) алканов 3) циклоалканов 4) алкенов Справочные таблицы Следующее задание К выбору задания
 А 15. В молекуле какого вещества все атомы углерода находятся в состоянии sp 2 -гибридизации? 1) гексана 2) гексена 3) этана 4) этена Справочные таблицы Следующее задание К выбору задания
А 15. В молекуле какого вещества все атомы углерода находятся в состоянии sp 2 -гибридизации? 1) гексана 2) гексена 3) этана 4) этена Справочные таблицы Следующее задание К выбору задания
 А 16. Характерной реакцией для многоатомных взаимодействие с 1) H 2 2) Сu 3) Ag 2 O (NH 3 р-р) 4) Cu(OH)2 Справочные таблицы Следующее задание К выбору задания
А 16. Характерной реакцией для многоатомных взаимодействие с 1) H 2 2) Сu 3) Ag 2 O (NH 3 р-р) 4) Cu(OH)2 Справочные таблицы Следующее задание К выбору задания
 А 17. Уксусная кислота не взаимодействует с 1) Cu. O 2) Cu(OH)2 3) Na 2 CO 3 4) Na 2 SO 4 Справочные таблицы К выбору задания
А 17. Уксусная кислота не взаимодействует с 1) Cu. O 2) Cu(OH)2 3) Na 2 CO 3 4) Na 2 SO 4 Справочные таблицы К выбору задания
 А 18. В схеме превращений C 6 H 5 CH 3 → X → C 6 H 5 - CH 2 - OH веществом «Х» является 1) C 6 H 5 OH 2) C 6 H 5 - CH 2 Cl 3) C 6 H 5 Cl 4) C 6 H 5 COOH Справочные таблицы К выбору задания
А 18. В схеме превращений C 6 H 5 CH 3 → X → C 6 H 5 - CH 2 - OH веществом «Х» является 1) C 6 H 5 OH 2) C 6 H 5 - CH 2 Cl 3) C 6 H 5 Cl 4) C 6 H 5 COOH Справочные таблицы К выбору задания
 А 19. К реакциям замещения относится взаимодействие 1) этена и воды 2) брома и водорода 3) брома и пропана 4) метана и кислорода Справочные таблицы Следующее задание К выбору задания
А 19. К реакциям замещения относится взаимодействие 1) этена и воды 2) брома и водорода 3) брома и пропана 4) метана и кислорода Справочные таблицы Следующее задание К выбору задания
 А 20. С наибольшей скоростью при комнатной температуре протекает реакция между 1) Ag. NO 3(р-р) и Na. Cl(р-р) 2) Ca. СО 3 и HCl (р-р) 3) Zn и H 2 SO 4 4) Mg и O 2 Справочные таблицы Следующее задание К выбору задания
А 20. С наибольшей скоростью при комнатной температуре протекает реакция между 1) Ag. NO 3(р-р) и Na. Cl(р-р) 2) Ca. СО 3 и HCl (р-р) 3) Zn и H 2 SO 4 4) Mg и O 2 Справочные таблицы Следующее задание К выбору задания
 А 21. В системе 2 CO (г) + O 2 (г) <=>2 CO 2 (г) + Q смещению химического равновесия в сторону исходных веществ будет способствовать 1) увеличение давления 2) увеличение концентрации оксида углерода (IV) 3) уменьшение температуры 4) увеличение концентрации кислорода Справочные таблицы Следующее задание К выбору задания
А 21. В системе 2 CO (г) + O 2 (г) <=>2 CO 2 (г) + Q смещению химического равновесия в сторону исходных веществ будет способствовать 1) увеличение давления 2) увеличение концентрации оксида углерода (IV) 3) уменьшение температуры 4) увеличение концентрации кислорода Справочные таблицы Следующее задание К выбору задания
 А 22. В каком ряду все указанные вещества являются неэлектролитами? 1) этанол, хлорид калия, сульфат бария 2) рибоза, гидроксид калия, ацетат натрия 3) сахароза, глицерин, метанол 4) сульфат натрия, глюкоза, уксусная кислота Справочные таблицы Следующее задание К выбору задания
А 22. В каком ряду все указанные вещества являются неэлектролитами? 1) этанол, хлорид калия, сульфат бария 2) рибоза, гидроксид калия, ацетат натрия 3) сахароза, глицерин, метанол 4) сульфат натрия, глюкоза, уксусная кислота Справочные таблицы Следующее задание К выбору задания
 А 23. С выпадением осадка протекает реакция ионного обмена между растворами 1) гидроксида натрия и хлорида бария 2) сульфата хрома (III) и гидроксида калия 3) нитрата кальция и бромида натрия 4) хлорида аммония и нитрата алюминия Справочные таблицы К выбору задания
А 23. С выпадением осадка протекает реакция ионного обмена между растворами 1) гидроксида натрия и хлорида бария 2) сульфата хрома (III) и гидроксида калия 3) нитрата кальция и бромида натрия 4) хлорида аммония и нитрата алюминия Справочные таблицы К выбору задания
 А 24. В какой реакции оксид серы (IV) является восстановителем? 1)SO 2 + 2 Na. OH = Na 2 SO 3 + H 2 O 2)SO 2 + 2 H 2 S = 3 S + 2 H 2 O 3)SO 2 + H 2 O <=> H 2 SO 3 4)2 SO 2 + O 2 <=> 2 SO 3 Справочные таблицы К выбору задания
А 24. В какой реакции оксид серы (IV) является восстановителем? 1)SO 2 + 2 Na. OH = Na 2 SO 3 + H 2 O 2)SO 2 + 2 H 2 S = 3 S + 2 H 2 O 3)SO 2 + H 2 O <=> H 2 SO 3 4)2 SO 2 + O 2 <=> 2 SO 3 Справочные таблицы К выбору задания
 А 25. Щелочную реакцию среды имеет раствор каждой из двух солей: 1) КCl и Na 2 S 2) К 2 Si. O 3 и Na 2 CO 3 3) Fe. Cl 2 и NН 4 Cl 4) Cu. SO 4 и Na 2 SO 4 Справочные таблицы Следующее задание К выбору задания
А 25. Щелочную реакцию среды имеет раствор каждой из двух солей: 1) КCl и Na 2 S 2) К 2 Si. O 3 и Na 2 CO 3 3) Fe. Cl 2 и NН 4 Cl 4) Cu. SO 4 и Na 2 SO 4 Справочные таблицы Следующее задание К выбору задания
 А 26. Верны ли следующие суждения о свойствах углеводородов? А. Алканы вступают в реакции полимеризации Б. Этилен обесцвечивает раствор перманганата калия 1) верно только А 2) верно только Б 3) верны оба суждения 4) оба суждения неверны Справочные таблицы Следующее задание К выбору задания
А 26. Верны ли следующие суждения о свойствах углеводородов? А. Алканы вступают в реакции полимеризации Б. Этилен обесцвечивает раствор перманганата калия 1) верно только А 2) верно только Б 3) верны оба суждения 4) оба суждения неверны Справочные таблицы Следующее задание К выбору задания
 А 27. Пропанол-1 образуется в результате реакции, схема которой 1) СН 3 СН 2 СНО + H 2 → 2) СН 3 СН 2 СНО + Cu(OH)2 → 3) СН 3 - СН 2 Сl + H 2 O → 4) СН 3 СН 2 СНО + Ag 2 O → Справочные таблицы Следующее задание К выбору задания
А 27. Пропанол-1 образуется в результате реакции, схема которой 1) СН 3 СН 2 СНО + H 2 → 2) СН 3 СН 2 СНО + Cu(OH)2 → 3) СН 3 - СН 2 Сl + H 2 O → 4) СН 3 СН 2 СНО + Ag 2 O → Справочные таблицы Следующее задание К выбору задания
 А 28. Белки приобретают желтую окраску под действием 1) HNO 3 (конц. ) 2) Cu(OH)2 3) H 2 SO 4 (конц. ) 4) [Ag(NH 3)2]OH Справочные таблицы Следующее задание К выбору задания
А 28. Белки приобретают желтую окраску под действием 1) HNO 3 (конц. ) 2) Cu(OH)2 3) H 2 SO 4 (конц. ) 4) [Ag(NH 3)2]OH Справочные таблицы Следующее задание К выбору задания
 А 29. Сырьем для получения метанола в промышленности служат 1) CO и H 2 2) HCHO и H 2 3) CH 3 Cl и Na. OH 4) HCOOH и Na. OH Справочные таблицы Следующее задание К выбору задания
А 29. Сырьем для получения метанола в промышленности служат 1) CO и H 2 2) HCHO и H 2 3) CH 3 Cl и Na. OH 4) HCOOH и Na. OH Справочные таблицы Следующее задание К выбору задания
 А 30. Согласно термохимическому уравнению реакции 2 СО(г) + О 2(г) = 2 СО 2(г) + 566 к. Дж при сжигании оксида углерода (II) выделилось 152 к. Дж теплоты. Объем (н. у. ) сгоревшего газа составил 1) 6 л 2) 12 л 3) 44, 8 л 4) 120 л Справочные таблицы Следующее задание К выбору задания
А 30. Согласно термохимическому уравнению реакции 2 СО(г) + О 2(г) = 2 СО 2(г) + 566 к. Дж при сжигании оксида углерода (II) выделилось 152 к. Дж теплоты. Объем (н. у. ) сгоревшего газа составил 1) 6 л 2) 12 л 3) 44, 8 л 4) 120 л Справочные таблицы Следующее задание К выбору задания
 В 1. Установите соответствие между названием органического соединения и классом, к которому оно принадлежит A) 1, 2 -диметилбензол Б) гексанол-3 B) метилформиат Г) стирол (2 балла) Справочные таблицы На страницу с объяснением 1) 2) 3) 4) 5) 6) сложные эфиры углеводороды спирты карбоновые кислоты аминокислоты простые эфиры К выбору задания Следующее задание
В 1. Установите соответствие между названием органического соединения и классом, к которому оно принадлежит A) 1, 2 -диметилбензол Б) гексанол-3 B) метилформиат Г) стирол (2 балла) Справочные таблицы На страницу с объяснением 1) 2) 3) 4) 5) 6) сложные эфиры углеводороды спирты карбоновые кислоты аминокислоты простые эфиры К выбору задания Следующее задание
 В 2. Установите соответствие между формулой вещества и степенью окисления углерода в нем А) CH 2 Cl 2 Б) HCHO В) HCOONa Г) CBr 4 1) – 4 2) – 2 3) 0 4) + 2 5) + 4 (2 балла) Справочные таблицы На страницу с объяснением К выбору задания Следующее задание
В 2. Установите соответствие между формулой вещества и степенью окисления углерода в нем А) CH 2 Cl 2 Б) HCHO В) HCOONa Г) CBr 4 1) – 4 2) – 2 3) 0 4) + 2 5) + 4 (2 балла) Справочные таблицы На страницу с объяснением К выбору задания Следующее задание
 В 3. Установите соответствие между формулой вещества и продуктом, который образуется на катоде в результате электролиза его водного раствора A) Cu(NO 3)2 1) металл Б) Ag. NO 3 2) водород B) Сa. Cl 2 3) кислород Г) Na 2 SO 4 4) хлор 5) оксид серы (IV) 6) оксид азота (IV) (2 балла) Справочные таблицы К выбору задания На страницу с объяснением Следующее задание
В 3. Установите соответствие между формулой вещества и продуктом, который образуется на катоде в результате электролиза его водного раствора A) Cu(NO 3)2 1) металл Б) Ag. NO 3 2) водород B) Сa. Cl 2 3) кислород Г) Na 2 SO 4 4) хлор 5) оксид серы (IV) 6) оксид азота (IV) (2 балла) Справочные таблицы К выбору задания На страницу с объяснением Следующее задание
 В 4. Установите соответствие между названием соли и её способностью к гидролизу A) карбонат натрия Б) хлорид аммония B) сульфат калия Г) сульфид алюминия (2 балла) 1) гидролиз по катиону 2) гидролиз по аниону 3) гидролиз по катиону и аниону 4) гидролизу не подвергается Справочные таблицы На страницу с объяснением К выбору задания Следующее задание
В 4. Установите соответствие между названием соли и её способностью к гидролизу A) карбонат натрия Б) хлорид аммония B) сульфат калия Г) сульфид алюминия (2 балла) 1) гидролиз по катиону 2) гидролиз по аниону 3) гидролиз по катиону и аниону 4) гидролизу не подвергается Справочные таблицы На страницу с объяснением К выбору задания Следующее задание
 В 5. Установите соответствие между реагирующими веществами и продуктами реакций A) KHCO 3 + KOH → Б) KHCO 3 + HCl→ B) K 2 CO 3 + HNO 3→ Г) K 2 CO 3 + Ва. Cl 2→ (2 балла) Справочные таблицы На страницу с объяснением 1) 2) 3) 4) 5) KNO 3 + CO 2 + H 2 O KNO 3 + CO + H 2 O K 2 CO 3 + H 2 O KCl + H 2 O + CO 2 Ва. СO 3+KCl К выбору задания Следующее задание
В 5. Установите соответствие между реагирующими веществами и продуктами реакций A) KHCO 3 + KOH → Б) KHCO 3 + HCl→ B) K 2 CO 3 + HNO 3→ Г) K 2 CO 3 + Ва. Cl 2→ (2 балла) Справочные таблицы На страницу с объяснением 1) 2) 3) 4) 5) KNO 3 + CO 2 + H 2 O KNO 3 + CO + H 2 O K 2 CO 3 + H 2 O KCl + H 2 O + CO 2 Ва. СO 3+KCl К выбору задания Следующее задание
 В 6. С водородом взаимодействует каждое из двух веществ: 1) бензол, пропан; 2) бутен, этан; 3) дивинил, этен; 4) стирол, бутадиен-1, 3; 5) дихлорэтан, бутан; 6) этин, бутин-1. (2 балла) Справочные таблицы На страницу с объяснением К выбору задания Следующее задание
В 6. С водородом взаимодействует каждое из двух веществ: 1) бензол, пропан; 2) бутен, этан; 3) дивинил, этен; 4) стирол, бутадиен-1, 3; 5) дихлорэтан, бутан; 6) этин, бутин-1. (2 балла) Справочные таблицы На страницу с объяснением К выбору задания Следующее задание
 В 7. Метанол взаимодействует с веществами: 1) бромоводород; 2) карбонат натрия; 3) глицин; 4) гидроксид железа (III); 5) бензол; 6) метановая кислота. (2 балла) Справочные таблицы На страницу с объяснением К выбору задания Следующее задание
В 7. Метанол взаимодействует с веществами: 1) бромоводород; 2) карбонат натрия; 3) глицин; 4) гидроксид железа (III); 5) бензол; 6) метановая кислота. (2 балла) Справочные таблицы На страницу с объяснением К выбору задания Следующее задание
 В 8. И с анилином, и с аланином способны реагировать 1) кислород; 2) бромоводород; 3) этан; 4) пропен; 5) серная кислота; 6) гидроксид калия. (2 балла) Справочные таблицы На страницу с объяснением К выбору задания Следующее задание
В 8. И с анилином, и с аланином способны реагировать 1) кислород; 2) бромоводород; 3) этан; 4) пропен; 5) серная кислота; 6) гидроксид калия. (2 балла) Справочные таблицы На страницу с объяснением К выбору задания Следующее задание
 В 9. Определите массу воды, которую надо добавить к 20 г раствора уксусной кислоты с массовой долей 70% для получения раствора уксуса с массовой долей 3% (Запишите число с точностью до целых) (1 балл) Справочные таблицы На страницу с объяснением К выбору задания Следующее задание
В 9. Определите массу воды, которую надо добавить к 20 г раствора уксусной кислоты с массовой долей 70% для получения раствора уксуса с массовой долей 3% (Запишите число с точностью до целых) (1 балл) Справочные таблицы На страницу с объяснением К выбору задания Следующее задание
 В 10. Рассчитайте массу свинца, полученного в результате взаимодействия 6, 6 г цинка с избытком раствора нитрата свинца Ответ: _____ г. (Запишите число с точностью до целых) (1 балл) Справочные таблицы На страницу с объяснением К выбору задания Следующее задание
В 10. Рассчитайте массу свинца, полученного в результате взаимодействия 6, 6 г цинка с избытком раствора нитрата свинца Ответ: _____ г. (Запишите число с точностью до целых) (1 балл) Справочные таблицы На страницу с объяснением К выбору задания Следующее задание
 С 1. Используя метод электронного баланса, составьте уравнение реакции KMn. O 4+H 2 S + H 2 SO 4→Mn. SO 4+S+. . . . Определите окислитель и восстановитель. (3 балла) Справочные таблицы На страницу с объяснением К выбору задания Следующее задание
С 1. Используя метод электронного баланса, составьте уравнение реакции KMn. O 4+H 2 S + H 2 SO 4→Mn. SO 4+S+. . . . Определите окислитель и восстановитель. (3 балла) Справочные таблицы На страницу с объяснением К выбору задания Следующее задание
 С 2. Даны вещества: - алюминий; - оксид марганца (IV); -водный раствор сульфата меди (II); - концентрированная соляная кислота. Напишите уравнения четырех возможных реакций между этими веществами. (4 балла) Справочные таблицы На страницу с объяснением К выбору задания Следующее задание
С 2. Даны вещества: - алюминий; - оксид марганца (IV); -водный раствор сульфата меди (II); - концентрированная соляная кислота. Напишите уравнения четырех возможных реакций между этими веществами. (4 балла) Справочные таблицы На страницу с объяснением К выбору задания Следующее задание
 С 3. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения: Ca. C 2→этин→этаналь (5 баллов) X 1 X 2 X 3 Справочные таблицы На страницу с объяснением К выбору задания Следующее задание
С 3. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения: Ca. C 2→этин→этаналь (5 баллов) X 1 X 2 X 3 Справочные таблицы На страницу с объяснением К выбору задания Следующее задание
 С 4. Сероводород объемом 5, 6 л (н. у. ) прореагировал без остатка с 59, 02 мл раствора КOH с массовой долей 20% (плотность 1, 186 г/мл) Определите массу соли, полученной в результате этой химической реакции (4 балла) Справочные таблицы На страницу с объяснением К выбору задания Следующее задание
С 4. Сероводород объемом 5, 6 л (н. у. ) прореагировал без остатка с 59, 02 мл раствора КOH с массовой долей 20% (плотность 1, 186 г/мл) Определите массу соли, полученной в результате этой химической реакции (4 балла) Справочные таблицы На страницу с объяснением К выбору задания Следующее задание
 С 5. При взаимодействии 25, 5 г предельной одноосновной кислоты с избытком раствора гидрокарбоната натрия выделилось 5, 6 л (н. у. ) газа Определите молекулярную формулу кислоты. (3 балла) Справочные таблицы На страницу с объяснением К выбору задания
С 5. При взаимодействии 25, 5 г предельной одноосновной кислоты с избытком раствора гидрокарбоната натрия выделилось 5, 6 л (н. у. ) газа Определите молекулярную формулу кислоты. (3 балла) Справочные таблицы На страницу с объяснением К выбору задания
 Вернуться к заданию Правильно На страницу с объяснением Следующее задание
Вернуться к заданию Правильно На страницу с объяснением Следующее задание
 Вернуться к заданию Не правильно Следующее задание Заряд ядра атома равен порядковому номеру (у Fe № 26) Количество электронных слоев (энергетических уровней) равно номеру периода (у железа их 4, т. к. четвертый период) Количество электронов во внешнем электронном слое (внешнем энергетическом уровне) равно: для элементов главных подгрупп: номеру группы; для элементов побочных подгрупп: 2 Fe – элемент побочной подгруппы, значит на внешнем уровне имеет 2 электрона Количество протонов равно порядковому номеру (у железа 26 протонов) Количество электронов тоже равно порядковому номеру (у железа 26 электронов) Количество нейтронов равно: масса атома минус порядковый номер (у железа: 56 – 26 = 30 нейтронов) Заряд « 2+» означает, что в атоме железа недостает 2 электронов: Fe 0 +26 Fe 2+ +26 2 8 14 2 2 8 12 2 Fe 0 1 s 2 2 p 6 3 s 2 3 p 6 3 d 6 4 s 2 Fe 2+1 s 2 2 p 6 3 s 2 3 p 6 3 d 4 4 s 2
Вернуться к заданию Не правильно Следующее задание Заряд ядра атома равен порядковому номеру (у Fe № 26) Количество электронных слоев (энергетических уровней) равно номеру периода (у железа их 4, т. к. четвертый период) Количество электронов во внешнем электронном слое (внешнем энергетическом уровне) равно: для элементов главных подгрупп: номеру группы; для элементов побочных подгрупп: 2 Fe – элемент побочной подгруппы, значит на внешнем уровне имеет 2 электрона Количество протонов равно порядковому номеру (у железа 26 протонов) Количество электронов тоже равно порядковому номеру (у железа 26 электронов) Количество нейтронов равно: масса атома минус порядковый номер (у железа: 56 – 26 = 30 нейтронов) Заряд « 2+» означает, что в атоме железа недостает 2 электронов: Fe 0 +26 Fe 2+ +26 2 8 14 2 2 8 12 2 Fe 0 1 s 2 2 p 6 3 s 2 3 p 6 3 d 6 4 s 2 Fe 2+1 s 2 2 p 6 3 s 2 3 p 6 3 d 4 4 s 2
 Вернуться к заданию Правильно На страницу с объяснением Следующее задание
Вернуться к заданию Правильно На страницу с объяснением Следующее задание
 Вернуться к заданию Не правильно Чем ближе к Fr, тем: - больше радиус атома; - сильнее металлические свойства; -меньше электроотрицательность; -сильнее основные свойства гидроксида. Чем ближе к F, тем: - меньше радиус атома; -сильнее неметаллические свойства; - больше электроотрицательность. Следующее задание Чем ближе к At, тем: -сильнее кислотные свойства гидроксида. Из элементов VIА (то есть главной подгруппы шестой группы) ближе всех к Fr находится полоний Po
Вернуться к заданию Не правильно Чем ближе к Fr, тем: - больше радиус атома; - сильнее металлические свойства; -меньше электроотрицательность; -сильнее основные свойства гидроксида. Чем ближе к F, тем: - меньше радиус атома; -сильнее неметаллические свойства; - больше электроотрицательность. Следующее задание Чем ближе к At, тем: -сильнее кислотные свойства гидроксида. Из элементов VIА (то есть главной подгруппы шестой группы) ближе всех к Fr находится полоний Po
 Вернуться к заданию Правильно На страницу с объяснением Следующее задание
Вернуться к заданию Правильно На страницу с объяснением Следующее задание
 Вернуться к заданию Не правильно Следующее задание Ионная связь – между металлом и неметаллом или между металлом и кислотным остатком. Примеры: Na 2 O, K 2 CO 3 Металлическая связь – между металлами. Примеры: Ba, Al Ковалентная полярная связь – между разными неметаллами. Примеры: SO 2, HBr Ковалентная неполярная связь – между одинаковыми неметаллами. Примеры: O 3, H 2 Донорно-акцепторная связь – за счет неподеленной электронной пары. Примеры: NH 4 Cl и другие соединения аммония. Водородная – это связь между ионом водорода одном молекулы и ионом N, O или F другой молекулы. Возникает между молекулами: а) воды H 2 O; б) аммиака NH 3; в) фтороводорода HF; г) спиртов. - водородные связи не образует 1) этан CH 3 -CH 3 - водородные связи не образует 2) бензол - водородные связи не образует 3) водород H 2 4) этанол (этиловый спирт) C 2 H 5 OH -образует водородные связи
Вернуться к заданию Не правильно Следующее задание Ионная связь – между металлом и неметаллом или между металлом и кислотным остатком. Примеры: Na 2 O, K 2 CO 3 Металлическая связь – между металлами. Примеры: Ba, Al Ковалентная полярная связь – между разными неметаллами. Примеры: SO 2, HBr Ковалентная неполярная связь – между одинаковыми неметаллами. Примеры: O 3, H 2 Донорно-акцепторная связь – за счет неподеленной электронной пары. Примеры: NH 4 Cl и другие соединения аммония. Водородная – это связь между ионом водорода одном молекулы и ионом N, O или F другой молекулы. Возникает между молекулами: а) воды H 2 O; б) аммиака NH 3; в) фтороводорода HF; г) спиртов. - водородные связи не образует 1) этан CH 3 -CH 3 - водородные связи не образует 2) бензол - водородные связи не образует 3) водород H 2 4) этанол (этиловый спирт) C 2 H 5 OH -образует водородные связи
 Вернуться к заданию Правильно На страницу с объяснением Следующее задание
Вернуться к заданию Правильно На страницу с объяснением Следующее задание
 Вернуться к заданию Не правильно Следующее задание Степень окисления – это условный заряд атома. Пример: Na+1 Сумма степеней окисления всех атомов в молекуле равна 0 Валентность – это число связей, которыми атом соединяется с другими атомами. Пример: в CH 4 валентность углерода равна 4 У Н валентность всегда равна 1, степень окисления почти всегда +1 У О валентность всегда равна 2, степень окисления почти всегда -2 У щелочных (Li, Na, K, Rb, Cs и Fr) металлов степень окисления всегда +1, валентность 1; у щелочноземельных металлов (Ca, Sr, Ba, Ra) степень окисления всегда +2, валентность 2 1) серная кислота H 2 SO 4. Степ. окисл. серы +6 2) серный колчедан Fe. S 2. Степ. окисл. серы +1 3) сернистая кислота H 2 SO 3. Степ. окисл. серы +4 4) гидрокарбонат натрия Na. HSO 4. Степ. окисл. серы +6 Примеры нахождения степеней окисления
Вернуться к заданию Не правильно Следующее задание Степень окисления – это условный заряд атома. Пример: Na+1 Сумма степеней окисления всех атомов в молекуле равна 0 Валентность – это число связей, которыми атом соединяется с другими атомами. Пример: в CH 4 валентность углерода равна 4 У Н валентность всегда равна 1, степень окисления почти всегда +1 У О валентность всегда равна 2, степень окисления почти всегда -2 У щелочных (Li, Na, K, Rb, Cs и Fr) металлов степень окисления всегда +1, валентность 1; у щелочноземельных металлов (Ca, Sr, Ba, Ra) степень окисления всегда +2, валентность 2 1) серная кислота H 2 SO 4. Степ. окисл. серы +6 2) серный колчедан Fe. S 2. Степ. окисл. серы +1 3) сернистая кислота H 2 SO 3. Степ. окисл. серы +4 4) гидрокарбонат натрия Na. HSO 4. Степ. окисл. серы +6 Примеры нахождения степеней окисления
 Вернуться к заданию Правильно На страницу с объяснением Следующее задание
Вернуться к заданию Правильно На страницу с объяснением Следующее задание
 Вернуться к заданию Не правильно Следующее задание Существует 4 типа строения (кристаллических решеток): Типы кристаллических решёток: Na Ca Fe Al металлическая Na. Cl Ca. SO 4 Fe 3(PO 4)2 Al(NO 3)3 ионная Алмаз, графит кристаллические бор, кремний, германий песок, кремнезём, кварц, горный хрусталь красный фосфор атомная H 2 O, CO 2, HCl, H 2 S H 2, O 2, Cl 2, N 2, I 2, O 3, P 4, S 8 большинство орг. соед. белый фосфор молекулярная Металлическая. Таким типом кристаллической решётки обладают все металлы и некоторые сплавы. Свойства: ковкость, пластичность, электро- и теплопроводность, металлический блеск. Ионная. Все соединения с ионной связью (все соли), некоторые оксиды и гидроксиды металлов. Свойства: высокие твёрдость и прочность, высокие температуры плавления и кипения, нелетучесть, часто хорошая растворимость. Атомная. Таких соединений очень мало. Узлы решётки соединены очень прочными ковалентными связями. Свойства: очень высокие температуры плавления, большая твёрдость, нерастворимость. Молекулярная. Таким типом решётки обладают многие простые вещества, состоящие из двух и более атомов, и сложные вещества, связанные ковалентной связью. Свойства: малая твёрдость, низкие температуры плавления, летучесть, низкая электропроводность, растворимость. 1) Озон O 3 – простое вещество-неметалл, значит молекулярное строение 2) Оксид бария Ba. O – оксид металла, значит ионное строение 3) Графит С – атомное строение 4) Сульфид калия K 2 S – соль, значит ионное строение
Вернуться к заданию Не правильно Следующее задание Существует 4 типа строения (кристаллических решеток): Типы кристаллических решёток: Na Ca Fe Al металлическая Na. Cl Ca. SO 4 Fe 3(PO 4)2 Al(NO 3)3 ионная Алмаз, графит кристаллические бор, кремний, германий песок, кремнезём, кварц, горный хрусталь красный фосфор атомная H 2 O, CO 2, HCl, H 2 S H 2, O 2, Cl 2, N 2, I 2, O 3, P 4, S 8 большинство орг. соед. белый фосфор молекулярная Металлическая. Таким типом кристаллической решётки обладают все металлы и некоторые сплавы. Свойства: ковкость, пластичность, электро- и теплопроводность, металлический блеск. Ионная. Все соединения с ионной связью (все соли), некоторые оксиды и гидроксиды металлов. Свойства: высокие твёрдость и прочность, высокие температуры плавления и кипения, нелетучесть, часто хорошая растворимость. Атомная. Таких соединений очень мало. Узлы решётки соединены очень прочными ковалентными связями. Свойства: очень высокие температуры плавления, большая твёрдость, нерастворимость. Молекулярная. Таким типом решётки обладают многие простые вещества, состоящие из двух и более атомов, и сложные вещества, связанные ковалентной связью. Свойства: малая твёрдость, низкие температуры плавления, летучесть, низкая электропроводность, растворимость. 1) Озон O 3 – простое вещество-неметалл, значит молекулярное строение 2) Оксид бария Ba. O – оксид металла, значит ионное строение 3) Графит С – атомное строение 4) Сульфид калия K 2 S – соль, значит ионное строение
 Вернуться к заданию Правильно На страницу с объяснением Следующее задание
Вернуться к заданию Правильно На страницу с объяснением Следующее задание
 Вернуться к заданию Не правильно Амфотерные оксиды: Be. O, Zn. O, Pb. O, Al 2 O 3, Cr 2 O 3, Fe 2 O 3 Основные оксиды: оксиды металлов Несолеобразующие оксиды: N 2 O, NO, CO, Si. O Кислотные оксиды: оксиды неметаллов и металлов в степенях окисления +5, +6, +7 Следующее задание Амфотерные гидроксиды: Be(OH)2, Zn (OH)2, Pb (OH)2, Al (OH)3, Cr (OH)3, Fe (OH)3 Основания: Cu(OH)2, Na. OH, Ca(OH)2 и т. д. Щелочи – гидроксиды щелочных (Li. OH, Na. OH, KOH, Cs. OH и Rb. OH) и щелочноземельных (Ca(OH)2, Sr(OH)2 и Ba(OH)2) металлов Кислоты: H 3 PO 4, HCl, H 2 SO 4 и т. д. 1) H 2 SO 4 – кислота Zn(OH)Cl – основная соль 2) Ca(OH)2 – основание, щелочь HCl - кислота 3) KHSO 4 – кислая соль Na. OH – основание, щелочь 4) Al(OH)3 – амфотерный гидроксид HNO 3 - кислота
Вернуться к заданию Не правильно Амфотерные оксиды: Be. O, Zn. O, Pb. O, Al 2 O 3, Cr 2 O 3, Fe 2 O 3 Основные оксиды: оксиды металлов Несолеобразующие оксиды: N 2 O, NO, CO, Si. O Кислотные оксиды: оксиды неметаллов и металлов в степенях окисления +5, +6, +7 Следующее задание Амфотерные гидроксиды: Be(OH)2, Zn (OH)2, Pb (OH)2, Al (OH)3, Cr (OH)3, Fe (OH)3 Основания: Cu(OH)2, Na. OH, Ca(OH)2 и т. д. Щелочи – гидроксиды щелочных (Li. OH, Na. OH, KOH, Cs. OH и Rb. OH) и щелочноземельных (Ca(OH)2, Sr(OH)2 и Ba(OH)2) металлов Кислоты: H 3 PO 4, HCl, H 2 SO 4 и т. д. 1) H 2 SO 4 – кислота Zn(OH)Cl – основная соль 2) Ca(OH)2 – основание, щелочь HCl - кислота 3) KHSO 4 – кислая соль Na. OH – основание, щелочь 4) Al(OH)3 – амфотерный гидроксид HNO 3 - кислота
 Вернуться к заданию Правильно На страницу с объяснением Следующее задание
Вернуться к заданию Правильно На страницу с объяснением Следующее задание
 Вернуться к заданию Не правильно Чем ближе к Fr, тем: - больше радиус атома - сильнее металлические свойства -меньше электроотрицательность -сильнее основные свойства гидроксида Чем ближе к F, тем: - меньше радиус атома -сильнее неметаллические свойства - больше электроотрицательность Следующее задание Чем ближе к At, тем: -сильнее кислотные свойства гидроксида 1) Na, Mg, Al – приближение к F, мет. свойства ослабевают 2) Al, Mg, Na– приближение к Fr, мет. свойства усиливаются 3) Cа, Mg, Be– приближение к F, мет. свойства ослабевают 4) Mg, Be, Cа– приближение к F, мет. свойства ослабевают
Вернуться к заданию Не правильно Чем ближе к Fr, тем: - больше радиус атома - сильнее металлические свойства -меньше электроотрицательность -сильнее основные свойства гидроксида Чем ближе к F, тем: - меньше радиус атома -сильнее неметаллические свойства - больше электроотрицательность Следующее задание Чем ближе к At, тем: -сильнее кислотные свойства гидроксида 1) Na, Mg, Al – приближение к F, мет. свойства ослабевают 2) Al, Mg, Na– приближение к Fr, мет. свойства усиливаются 3) Cа, Mg, Be– приближение к F, мет. свойства ослабевают 4) Mg, Be, Cа– приближение к F, мет. свойства ослабевают
 Вернуться к заданию Правильно На страницу с объяснением Следующее задание
Вернуться к заданию Правильно На страницу с объяснением Следующее задание
 Вернуться к заданию Не правильно Следующее задание Высший – это оксид элемента в максимальной степени окисления Примеры: SO 3 – высший оксид серы, т. к. сера находится в степени окисления +6, а это ее максимальная степень окисления (S находится VIA группе) Na 2 O – высший оксид натрия, т. к. натрий находится в степени окисления +1, а это его максимальная степень окисления (Na находится IA группе) Cl находится в VIIA группе, значит его максимальная степень окисления +7 +7 -2 Cl 2 О 7 У О валентность всегда равна 2, степень окисления почти всегда -2
Вернуться к заданию Не правильно Следующее задание Высший – это оксид элемента в максимальной степени окисления Примеры: SO 3 – высший оксид серы, т. к. сера находится в степени окисления +6, а это ее максимальная степень окисления (S находится VIA группе) Na 2 O – высший оксид натрия, т. к. натрий находится в степени окисления +1, а это его максимальная степень окисления (Na находится IA группе) Cl находится в VIIA группе, значит его максимальная степень окисления +7 +7 -2 Cl 2 О 7 У О валентность всегда равна 2, степень окисления почти всегда -2
 Вернуться к заданию Правильно На страницу с объяснением Следующее задание
Вернуться к заданию Правильно На страницу с объяснением Следующее задание
 Вернуться к заданию Не правильно Следующее задание Некоторые степени окисления элементов побочных подгрупп Железо: Fe 0 Fe+2 Fe+3 Fe+6 Хром: Cr 0 Cr+2 Cr+3 Cr+6 Марганец: Mn 0 Mn+2 Mn+3 Mn+4 Mn+5 Mn+6 Mn+7 Цинк: Zn 0 Zn+2 Медь: Cu 0 Cu+1 Cu+2 Ряд напряжений металлов показывает активность металлов Li, K, Ba, Ca, Na – очень активные металлы: реагируют с водой без нагревания; с кислотами реагируют очень бурно; От Mg до Pb – металлы средней активности: реагируют с водой при нагревании; с кислотами реагируют относительно медленно; Правее H 2 – неактивные металлы: с водой не реагируют даже при нагревании; с обычными кислотами не реагируют; с необычными (H 2 SO 4 (конц. ) и HNO 3) реагируют медь, ртуть и серебро; Золото – почти ни с чем не реагирует Более активные металлы вытесняют менее активные из их солей Медь – менее активный металл, чем цинк, значит не вытесняет его из солей
Вернуться к заданию Не правильно Следующее задание Некоторые степени окисления элементов побочных подгрупп Железо: Fe 0 Fe+2 Fe+3 Fe+6 Хром: Cr 0 Cr+2 Cr+3 Cr+6 Марганец: Mn 0 Mn+2 Mn+3 Mn+4 Mn+5 Mn+6 Mn+7 Цинк: Zn 0 Zn+2 Медь: Cu 0 Cu+1 Cu+2 Ряд напряжений металлов показывает активность металлов Li, K, Ba, Ca, Na – очень активные металлы: реагируют с водой без нагревания; с кислотами реагируют очень бурно; От Mg до Pb – металлы средней активности: реагируют с водой при нагревании; с кислотами реагируют относительно медленно; Правее H 2 – неактивные металлы: с водой не реагируют даже при нагревании; с обычными кислотами не реагируют; с необычными (H 2 SO 4 (конц. ) и HNO 3) реагируют медь, ртуть и серебро; Золото – почти ни с чем не реагирует Более активные металлы вытесняют менее активные из их солей Медь – менее активный металл, чем цинк, значит не вытесняет его из солей
 Вернуться к заданию Правильно На страницу с объяснением Следующее задание
Вернуться к заданию Правильно На страницу с объяснением Следующее задание
 Вернуться к заданию Не правильно Следующее задание Оксид кальция Ca. O – основный оксид. С кислородом реагируют оксиды, в которых элемент находится не в Ca. O + O 2 ≠ максимальной степени окисления Оксиды реагируют с водой, если образуется Ca. O + H 2 O = Ca(OH)2 растворимый гидроксид Ca. O + H 2 SO 4 = Ca. SO 4 + H 2 O Ca. O – основный оксид, H 2 SO 4 - кислота Ca. O + 2 HCl = Ca. Cl 2 + H 2 O Ca. O – основный оксид, HCl - кислота Ca. O + CO 2 = Ca. CO 3 Ca. O – основный оксид, CO 2 – кислотный оксид Ca. O + Mg. O ≠ Ca. O – основный оксид, Mg. O – тоже основный оксид Ca. O + SO 2 = Ca. SO 3 Ca. O – основный оксид, SO 2 – кислотный оксид Ca. O + NH 3 ≠ Аммиак NH 3 реагирует только с водой, кислотами и кислородом Ca. O + Fe ≠ Fe–менее активный металл, чем Ca, значит не вытесняет его Ca. O – основный оксид, HNO 3 - кислота Ca. O + 2 HNO 3 = Ca(NO 3)2 + H 2 O 3 Ca. O + P 2 O 5 = Ca 3(PO 4)2 Ca. O – основный оксид, P 2 O 5 – кислотный оксид
Вернуться к заданию Не правильно Следующее задание Оксид кальция Ca. O – основный оксид. С кислородом реагируют оксиды, в которых элемент находится не в Ca. O + O 2 ≠ максимальной степени окисления Оксиды реагируют с водой, если образуется Ca. O + H 2 O = Ca(OH)2 растворимый гидроксид Ca. O + H 2 SO 4 = Ca. SO 4 + H 2 O Ca. O – основный оксид, H 2 SO 4 - кислота Ca. O + 2 HCl = Ca. Cl 2 + H 2 O Ca. O – основный оксид, HCl - кислота Ca. O + CO 2 = Ca. CO 3 Ca. O – основный оксид, CO 2 – кислотный оксид Ca. O + Mg. O ≠ Ca. O – основный оксид, Mg. O – тоже основный оксид Ca. O + SO 2 = Ca. SO 3 Ca. O – основный оксид, SO 2 – кислотный оксид Ca. O + NH 3 ≠ Аммиак NH 3 реагирует только с водой, кислотами и кислородом Ca. O + Fe ≠ Fe–менее активный металл, чем Ca, значит не вытесняет его Ca. O – основный оксид, HNO 3 - кислота Ca. O + 2 HNO 3 = Ca(NO 3)2 + H 2 O 3 Ca. O + P 2 O 5 = Ca 3(PO 4)2 Ca. O – основный оксид, P 2 O 5 – кислотный оксид
 Вернуться к заданию Правильно На страницу с объяснением Следующее задание
Вернуться к заданию Правильно На страницу с объяснением Следующее задание
 Вернуться к заданию Не правильно Следующее задание Гидроксид хрома (III) Cr(OH)3 – амфотерный гидроксид Амфотерные гидроксиды реагируют только с оксидами, Cr(OH)3 + CO 2 ≠ которым соответствуют сильные гидроксиды Амфотерные гидроксиды Cr(OH)3 + 3 HCl = Cr. Cl 3 + 3 H 2 O Cr(OH)3 + Si. O 2 ≠ реагируют с кислотами Амфотерные гидроксиды реагируют только с оксидами, которым соответствуют сильные гидроксиды Амфотерные гидроксиды реагируют только со щелочами Cr(OH)3 + Cu(OH)2 ≠ (Li. OH, Na. OH, KOH, Rb. OH, Cs. OH, Ca(OH) , Sr(OH) , Ba(OH) ) 2 2 2 NO – несолеобразующий оксид, вступает только в Cr(OH)3 + NO ≠ окислительно-восстановительные реакции Cr(OH)3 + Na. NO 3 ≠ Амфотерные гидроксиды не реагируют с солями Амфотерные гидроксиды 2 Cr(OH)3 +3 H 2 SO 4 = Cr 2(SO 4)3 + 3 H 2 O реагируют с кислотами Cr(OH)3 + Na. OH = Na. Cr. O 2 +2 H 2 O Амфотерные гидроксиды реагируют со щелочами
Вернуться к заданию Не правильно Следующее задание Гидроксид хрома (III) Cr(OH)3 – амфотерный гидроксид Амфотерные гидроксиды реагируют только с оксидами, Cr(OH)3 + CO 2 ≠ которым соответствуют сильные гидроксиды Амфотерные гидроксиды Cr(OH)3 + 3 HCl = Cr. Cl 3 + 3 H 2 O Cr(OH)3 + Si. O 2 ≠ реагируют с кислотами Амфотерные гидроксиды реагируют только с оксидами, которым соответствуют сильные гидроксиды Амфотерные гидроксиды реагируют только со щелочами Cr(OH)3 + Cu(OH)2 ≠ (Li. OH, Na. OH, KOH, Rb. OH, Cs. OH, Ca(OH) , Sr(OH) , Ba(OH) ) 2 2 2 NO – несолеобразующий оксид, вступает только в Cr(OH)3 + NO ≠ окислительно-восстановительные реакции Cr(OH)3 + Na. NO 3 ≠ Амфотерные гидроксиды не реагируют с солями Амфотерные гидроксиды 2 Cr(OH)3 +3 H 2 SO 4 = Cr 2(SO 4)3 + 3 H 2 O реагируют с кислотами Cr(OH)3 + Na. OH = Na. Cr. O 2 +2 H 2 O Амфотерные гидроксиды реагируют со щелочами
 Вернуться к заданию Правильно На страницу с объяснением Следующее задание
Вернуться к заданию Правильно На страницу с объяснением Следующее задание
 Вернуться к заданию Не правильно Следующее задание Карбонат кальция Ca. CO 3 - соль Ca. CO 3 + 2 HCl = Ca. Cl 2 + Реакция возможна, т. к. H 2 O +3 CO 2 образуется газ CO Ca. CO 3 + Mg. O ≠ Соли с оксидами не реагируют Ca. CO 3 + Pb Pb – менее активный металл, чем Ca ≠ Ca. CO 3 + H 2 O ≠ Соли в воде растворяются, многие подвергаются гидролизу. Ca. CO 3 – нерастворимая соль, гидролизу не подвергаются
Вернуться к заданию Не правильно Следующее задание Карбонат кальция Ca. CO 3 - соль Ca. CO 3 + 2 HCl = Ca. Cl 2 + Реакция возможна, т. к. H 2 O +3 CO 2 образуется газ CO Ca. CO 3 + Mg. O ≠ Соли с оксидами не реагируют Ca. CO 3 + Pb Pb – менее активный металл, чем Ca ≠ Ca. CO 3 + H 2 O ≠ Соли в воде растворяются, многие подвергаются гидролизу. Ca. CO 3 – нерастворимая соль, гидролизу не подвергаются
 Вернуться к заданию Правильно На страницу с объяснением Следующее задание
Вернуться к заданию Правильно На страницу с объяснением Следующее задание
 Вернуться к заданию Не правильно Ba Ba + KOH ≠ Ba(OH)2 Следующее задание Ba. Cl 2 Металлы с основаниями не реагируют Ba + Na. OH ≠ Металлы с основаниями не реагируют Металлы левее H реагируют Ba + 2 H 2 O = Ba(OH)2 + H 2 с водой и кислотами Ba(OH)2 + 2 HCl = Ba. Cl 2 +2 H 2 O Ba(OH)2 – основание, щелочь HCl - кислота Ba(OH)2 + Cl 2 ≠ Основания с неметаллами не реагируют Ba(OH)2 + KCl ≠ Реакция невозможна, т. к. не образуется ни осадка, ни газа, ни воды
Вернуться к заданию Не правильно Ba Ba + KOH ≠ Ba(OH)2 Следующее задание Ba. Cl 2 Металлы с основаниями не реагируют Ba + Na. OH ≠ Металлы с основаниями не реагируют Металлы левее H реагируют Ba + 2 H 2 O = Ba(OH)2 + H 2 с водой и кислотами Ba(OH)2 + 2 HCl = Ba. Cl 2 +2 H 2 O Ba(OH)2 – основание, щелочь HCl - кислота Ba(OH)2 + Cl 2 ≠ Основания с неметаллами не реагируют Ba(OH)2 + KCl ≠ Реакция невозможна, т. к. не образуется ни осадка, ни газа, ни воды
 Вернуться к заданию Правильно На страницу с объяснением Следующее задание
Вернуться к заданию Правильно На страницу с объяснением Следующее задание
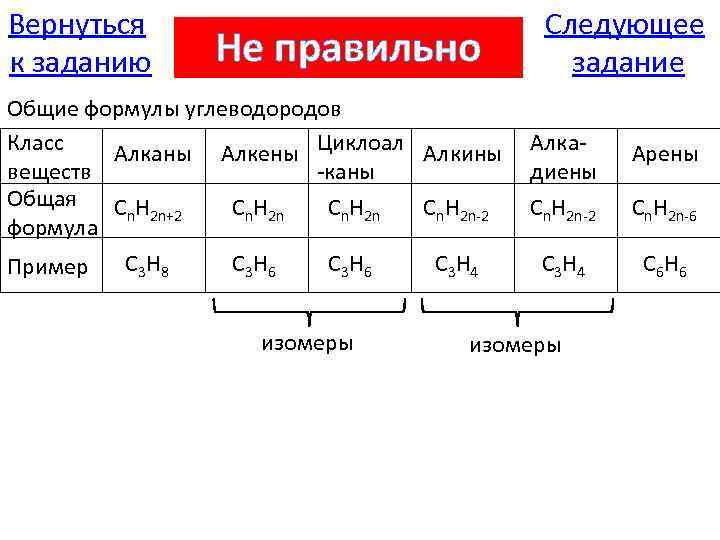 Вернуться к заданию Не правильно Общие формулы углеводородов Класс Алканы Алкены Циклоал Алкины веществ -каны Общая Cn. H 2 n+2 Cn. H 2 n-2 формула Пример C 3 H 8 C 3 H 6 изомеры C 3 H 4 Следующее задание Алкадиены Арены Cn. H 2 n-2 Cn. H 2 n-6 C 3 H 4 C 6 H 6 изомеры
Вернуться к заданию Не правильно Общие формулы углеводородов Класс Алканы Алкены Циклоал Алкины веществ -каны Общая Cn. H 2 n+2 Cn. H 2 n-2 формула Пример C 3 H 8 C 3 H 6 изомеры C 3 H 4 Следующее задание Алкадиены Арены Cn. H 2 n-2 Cn. H 2 n-6 C 3 H 4 C 6 H 6 изомеры
 Вернуться к заданию Правильно На страницу с объяснением Следующее задание
Вернуться к заданию Правильно На страницу с объяснением Следующее задание
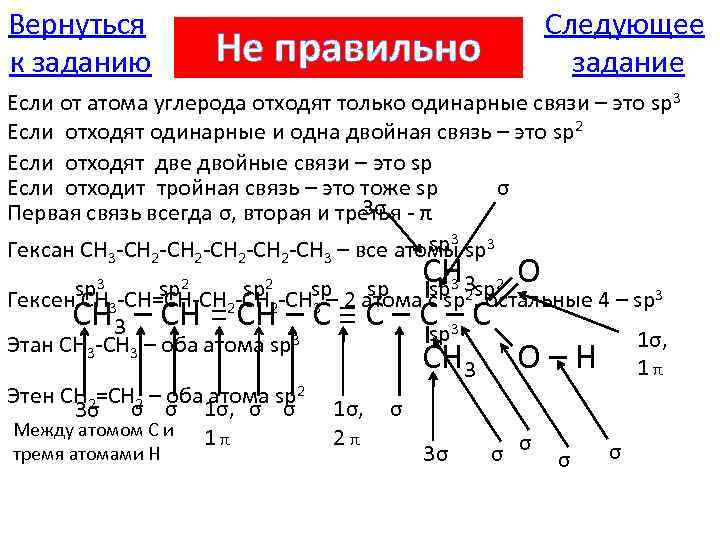 Вернуться к заданию Следующее задание Не правильно Если от атома углерода отходят только одинарные связи – это sp 3 Если отходят одинарные и одна двойная связь – это sp 2 Если отходят две двойные связи – это sp Если отходит тройная связь – это тоже sp σ 3σ Первая связь всегда σ, вторая и третья - π sp 3 Гексан CH 3 -CH 2 -CH 3 – все атомы CH 3 sp 2 O sp 2 атома с sp 2, остальные 4 – sp 3 sp sp 3 Гексен CH 3 -CH=CH-CH 2 -CH 3 – CH = CH – C ≡ C – C sp 3 3 1σ, Этан CH 3 -CH 3 – оба атома sp CH 3 O – H 1 π sp 3 sp 2 Этен CH 2=CH 2 – оба атома sp 2 3σ σ σ 1σ, σ σ Между атомом С и 1 π тремя атомами Н 1σ, 2π σ 3σ σ σ
Вернуться к заданию Следующее задание Не правильно Если от атома углерода отходят только одинарные связи – это sp 3 Если отходят одинарные и одна двойная связь – это sp 2 Если отходят две двойные связи – это sp Если отходит тройная связь – это тоже sp σ 3σ Первая связь всегда σ, вторая и третья - π sp 3 Гексан CH 3 -CH 2 -CH 3 – все атомы CH 3 sp 2 O sp 2 атома с sp 2, остальные 4 – sp 3 sp sp 3 Гексен CH 3 -CH=CH-CH 2 -CH 3 – CH = CH – C ≡ C – C sp 3 3 1σ, Этан CH 3 -CH 3 – оба атома sp CH 3 O – H 1 π sp 3 sp 2 Этен CH 2=CH 2 – оба атома sp 2 3σ σ σ 1σ, σ σ Между атомом С и 1 π тремя атомами Н 1σ, 2π σ 3σ σ σ
 Вернуться к заданию Правильно На страницу с объяснением Следующее задание
Вернуться к заданию Правильно На страницу с объяснением Следующее задание
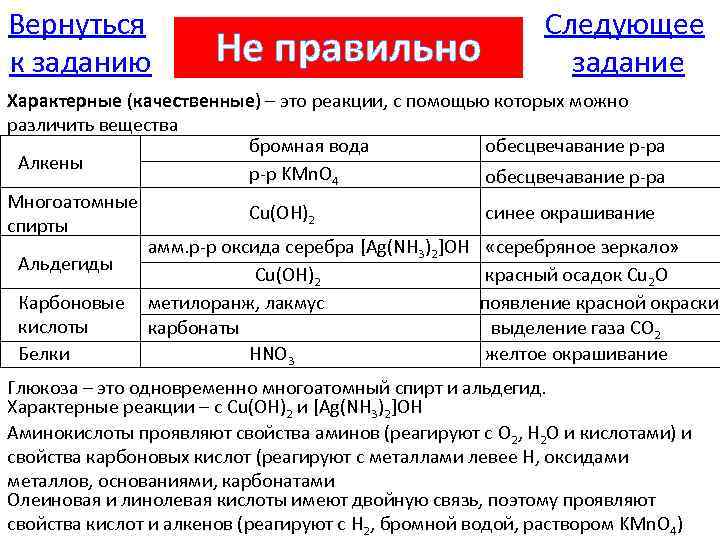 Вернуться к заданию Не правильно Следующее задание Характерные (качественные) – это реакции, с помощью которых можно различить вещества бромная вода обесцвечавание р-ра Алкены р-р KMn. O 4 обесцвечавание р-ра Многоатомные Cu(OH)2 синее окрашивание спирты амм. р-р оксида серебра [Ag(NH 3)2]OH «серебряное зеркало» Альдегиды Cu(OH)2 красный осадок Cu 2 O Карбоновые метилоранж, лакмус появление красной окраски кислоты карбонаты выделение газа CO 2 Белки HNO 3 желтое окрашивание Глюкоза – это одновременно многоатомный спирт и альдегид. Характерные реакции – с Cu(OH)2 и [Ag(NH 3)2]OH Аминокислоты проявляют свойства аминов (реагируют с O 2, H 2 O и кислотами) и свойства карбоновых кислот (реагируют с металлами левее Н, оксидами металлов, основаниями, карбонатами Олеиновая и линолевая кислоты имеют двойную связь, поэтому проявляют свойства кислот и алкенов (реагируют с H 2, бромной водой, раствором KMn. O 4)
Вернуться к заданию Не правильно Следующее задание Характерные (качественные) – это реакции, с помощью которых можно различить вещества бромная вода обесцвечавание р-ра Алкены р-р KMn. O 4 обесцвечавание р-ра Многоатомные Cu(OH)2 синее окрашивание спирты амм. р-р оксида серебра [Ag(NH 3)2]OH «серебряное зеркало» Альдегиды Cu(OH)2 красный осадок Cu 2 O Карбоновые метилоранж, лакмус появление красной окраски кислоты карбонаты выделение газа CO 2 Белки HNO 3 желтое окрашивание Глюкоза – это одновременно многоатомный спирт и альдегид. Характерные реакции – с Cu(OH)2 и [Ag(NH 3)2]OH Аминокислоты проявляют свойства аминов (реагируют с O 2, H 2 O и кислотами) и свойства карбоновых кислот (реагируют с металлами левее Н, оксидами металлов, основаниями, карбонатами Олеиновая и линолевая кислоты имеют двойную связь, поэтому проявляют свойства кислот и алкенов (реагируют с H 2, бромной водой, раствором KMn. O 4)
 Вернуться к заданию Правильно На страницу с объяснением Следующее задание
Вернуться к заданию Правильно На страницу с объяснением Следующее задание
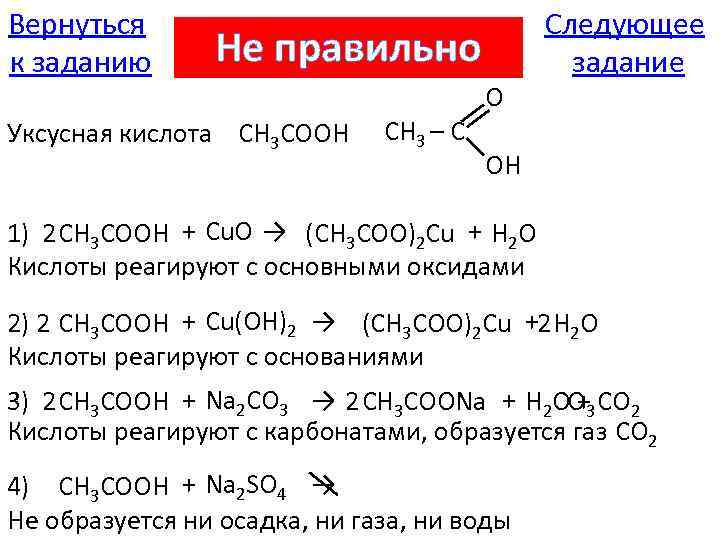 Вернуться к заданию Не правильно Уксусная кислота CH 3 COOH CH 3 – C O Следующее задание OH 1) 2 CH 3 COOH + Cu. O → (CH 3 COO)2 Cu + H 2 O Кислоты реагируют с основными оксидами 2) 2 CH 3 COOH + Cu(OH)2 → (CH 3 COO)2 Cu +2 H 2 O Кислоты реагируют с основаниями 3) 2 CH 3 COOH + Na 2 CO 3 → 2 CH 3 COONa + H 2 CO 3 CO 2 O+ Кислоты реагируют с карбонатами, образуется газ CO 2 4) CH 3 COOH + Na 2 SO 4 → Не образуется ни осадка, ни газа, ни воды
Вернуться к заданию Не правильно Уксусная кислота CH 3 COOH CH 3 – C O Следующее задание OH 1) 2 CH 3 COOH + Cu. O → (CH 3 COO)2 Cu + H 2 O Кислоты реагируют с основными оксидами 2) 2 CH 3 COOH + Cu(OH)2 → (CH 3 COO)2 Cu +2 H 2 O Кислоты реагируют с основаниями 3) 2 CH 3 COOH + Na 2 CO 3 → 2 CH 3 COONa + H 2 CO 3 CO 2 O+ Кислоты реагируют с карбонатами, образуется газ CO 2 4) CH 3 COOH + Na 2 SO 4 → Не образуется ни осадка, ни газа, ни воды
 Вернуться к заданию Правильно На страницу с объяснением Следующее задание
Вернуться к заданию Правильно На страницу с объяснением Следующее задание
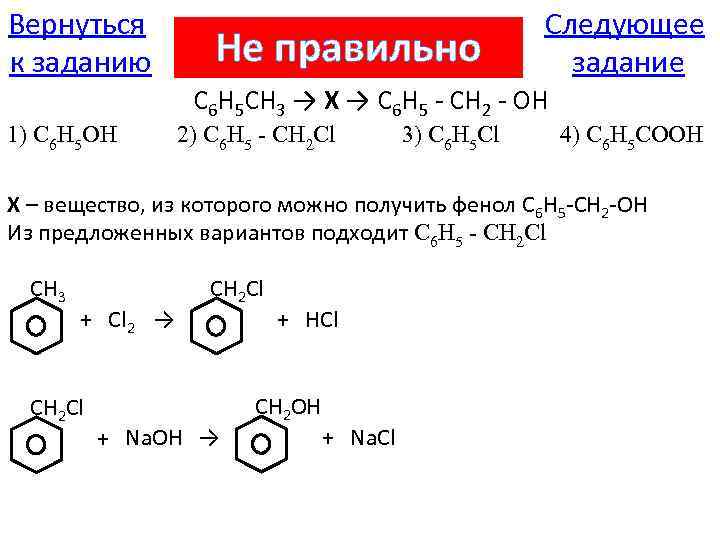 Вернуться к заданию Не правильно Следующее задание C 6 H 5 CH 3 → X → C 6 H 5 - CH 2 - OH 1) C 6 H 5 OH 2) C 6 H 5 - CH 2 Cl 3) C 6 H 5 Cl 4) C 6 H 5 COOH X – вещество, из которого можно получить фенол C 6 H 5 -CH 2 -OH Из предложенных вариантов подходит C 6 H 5 - CH 2 Cl CH 3 + Cl 2 → CH 2 Cl + Na. OH → + HCl CH 2 OH + Na. Cl
Вернуться к заданию Не правильно Следующее задание C 6 H 5 CH 3 → X → C 6 H 5 - CH 2 - OH 1) C 6 H 5 OH 2) C 6 H 5 - CH 2 Cl 3) C 6 H 5 Cl 4) C 6 H 5 COOH X – вещество, из которого можно получить фенол C 6 H 5 -CH 2 -OH Из предложенных вариантов подходит C 6 H 5 - CH 2 Cl CH 3 + Cl 2 → CH 2 Cl + Na. OH → + HCl CH 2 OH + Na. Cl
 Вернуться к заданию Правильно На страницу с объяснением Следующее задание
Вернуться к заданию Правильно На страницу с объяснением Следующее задание
 Вернуться к заданию 1) 2) Следующее задание Не правильно CH 2=CH 2 + H 2 O → CH 3 -CH 2 OH - реакция соединения этен, этилен Br 2 + H 2 → 2 HBr - реакция соединения 3) CH 3 -CH 2 -CH 3 + Br 2 → CH 3 -CHBr-CH 3 + HBr пропан бром заместил водород, реакция замещения 4) CH 4 +2 O 2 → CO 2 + 2 H 2 O - не реакция замещения
Вернуться к заданию 1) 2) Следующее задание Не правильно CH 2=CH 2 + H 2 O → CH 3 -CH 2 OH - реакция соединения этен, этилен Br 2 + H 2 → 2 HBr - реакция соединения 3) CH 3 -CH 2 -CH 3 + Br 2 → CH 3 -CHBr-CH 3 + HBr пропан бром заместил водород, реакция замещения 4) CH 4 +2 O 2 → CO 2 + 2 H 2 O - не реакция замещения
 Вернуться к заданию Правильно На страницу с объяснением Следующее задание
Вернуться к заданию Правильно На страницу с объяснением Следующее задание
 Вернуться к заданию Не правильно Следующее задание 1. С наибольшей скоростью протекают реакции в растворах. Пример: реакция Ba. Cl 2 (р-р) + H 2 SO 4 (р-р) = Ba. SO 4 + 2 HCl (р-р) протекает почти мгновенно В ионном виде записываются только взаимодействующие ионы: Ba 2+ + SO 42 - = Ba. SO 4 Если в реакции 1 раствор, такая реакция идет с меньшей скоростью, чем между 2 растворами 2. В реакциях замещения с большей скоростью реагируют более активные металлы Пример: кальций взаимодействует с соляной кислотой быстрее, чем цинк
Вернуться к заданию Не правильно Следующее задание 1. С наибольшей скоростью протекают реакции в растворах. Пример: реакция Ba. Cl 2 (р-р) + H 2 SO 4 (р-р) = Ba. SO 4 + 2 HCl (р-р) протекает почти мгновенно В ионном виде записываются только взаимодействующие ионы: Ba 2+ + SO 42 - = Ba. SO 4 Если в реакции 1 раствор, такая реакция идет с меньшей скоростью, чем между 2 растворами 2. В реакциях замещения с большей скоростью реагируют более активные металлы Пример: кальций взаимодействует с соляной кислотой быстрее, чем цинк
 Вернуться к заданию Правильно На страницу с объяснением Следующее задание
Вернуться к заданию Правильно На страницу с объяснением Следующее задание
 Вернуться к заданию Не правильно Следующее задание При увеличении давления, равновесие реакции смещается в ту сторону, где меньше моль газов Если в реакции тепло выделяется (+Q), то увеличение температуры смещает равновесие в обратную сторону При увеличении концентраций исходных веществ, равновесие смещается в сторону продуктов реакции 2 CO (г) + O 2 (г) <=>2 CO 2 (г) + Q 1) В левой части 3 моль газов, а в правой 2. Значит увеличение давления будет смещать равновесие вправо (образование CO 2) 2) Увеличение концентрации оксида углерода (IV), т. е. CO 2 будет смещать равновесие влево (образование CO и O 2) 3) В реакции тепло выделяется (+Q). Значит уменьшение температуры будет смещать равновесие вправо (образование CO 2) 4) Увеличение концентрации кислорода О 2 (исходного вещества) будет смещать равновесие вправо (образование CO 2)
Вернуться к заданию Не правильно Следующее задание При увеличении давления, равновесие реакции смещается в ту сторону, где меньше моль газов Если в реакции тепло выделяется (+Q), то увеличение температуры смещает равновесие в обратную сторону При увеличении концентраций исходных веществ, равновесие смещается в сторону продуктов реакции 2 CO (г) + O 2 (г) <=>2 CO 2 (г) + Q 1) В левой части 3 моль газов, а в правой 2. Значит увеличение давления будет смещать равновесие вправо (образование CO 2) 2) Увеличение концентрации оксида углерода (IV), т. е. CO 2 будет смещать равновесие влево (образование CO и O 2) 3) В реакции тепло выделяется (+Q). Значит уменьшение температуры будет смещать равновесие вправо (образование CO 2) 4) Увеличение концентрации кислорода О 2 (исходного вещества) будет смещать равновесие вправо (образование CO 2)
 Вернуться к заданию Правильно На страницу с объяснением Следующее задание
Вернуться к заданию Правильно На страницу с объяснением Следующее задание
 Вернуться к заданию Не правильно Следующее задание C 2 H 5 OH (этанол) – органическое вещество, неэлектролит 1) KCl (хлорид калия)– растворимая соль, сильный электролит Ba. SO 4 (сульфат бария) – нерастворимая соль, слабый электролит C 5 H 10 O 5 (рибоза) – органическое вещество, неэлектролит 2) KOH (гидроксид калия) – щелочь, сильный электролит CH 3 COONa (ацетат натрия) – растворимая соль, сильный электролит C 12 H 22 O 11 (сахароза) – органическое вещество, неэлектролит 3) CH 2(OH)-CH 2(OH) (глицерин)–органическое вещество, неэлектролит CH 3 OH (метанол) – органическое вещество, неэлектролит Na 2 SO 4 (сульфат натрия) – растворимая соль, сильный электролит 4) C 6 H 12 O 6 (глюкоза) – органическое вещество, неэлектролит CH 3 COOH (уксусная кислота)–слабая кислота, слабый электролит
Вернуться к заданию Не правильно Следующее задание C 2 H 5 OH (этанол) – органическое вещество, неэлектролит 1) KCl (хлорид калия)– растворимая соль, сильный электролит Ba. SO 4 (сульфат бария) – нерастворимая соль, слабый электролит C 5 H 10 O 5 (рибоза) – органическое вещество, неэлектролит 2) KOH (гидроксид калия) – щелочь, сильный электролит CH 3 COONa (ацетат натрия) – растворимая соль, сильный электролит C 12 H 22 O 11 (сахароза) – органическое вещество, неэлектролит 3) CH 2(OH)-CH 2(OH) (глицерин)–органическое вещество, неэлектролит CH 3 OH (метанол) – органическое вещество, неэлектролит Na 2 SO 4 (сульфат натрия) – растворимая соль, сильный электролит 4) C 6 H 12 O 6 (глюкоза) – органическое вещество, неэлектролит CH 3 COOH (уксусная кислота)–слабая кислота, слабый электролит
 Вернуться к заданию Правильно На страницу с объяснением Следующее задание
Вернуться к заданию Правильно На страницу с объяснением Следующее задание
 Вернуться к заданию Не правильно Следующее задание 1) гидроксид натрия и хлорид бария реакция невозможна, т. к. не образуется Na. OH + Ba. Cl 2 ≠ ни осадка, ни газа, ни воды 2) сульфат хрома (III) и гидроксид натрия реакция возможна, т. к. Cr 2(SO 4)3 +6 KOH = 2 Cr(OH)3 +3 K 2 SO 4 образуется осадок Cr(OH) 3 3) нитрат кальция и бромид натрия реакция невозможна, т. к. не образуется Ca(NO 3)2 + Na. Br ≠ ни осадка, ни газа, ни воды 4) хлорид аммония и нитрат алюминия реакция невозможна, т. к. не образуется NH 4 Cl + Al(NO 3)3 ≠ ни осадка, ни газа, ни воды
Вернуться к заданию Не правильно Следующее задание 1) гидроксид натрия и хлорид бария реакция невозможна, т. к. не образуется Na. OH + Ba. Cl 2 ≠ ни осадка, ни газа, ни воды 2) сульфат хрома (III) и гидроксид натрия реакция возможна, т. к. Cr 2(SO 4)3 +6 KOH = 2 Cr(OH)3 +3 K 2 SO 4 образуется осадок Cr(OH) 3 3) нитрат кальция и бромид натрия реакция невозможна, т. к. не образуется Ca(NO 3)2 + Na. Br ≠ ни осадка, ни газа, ни воды 4) хлорид аммония и нитрат алюминия реакция невозможна, т. к. не образуется NH 4 Cl + Al(NO 3)3 ≠ ни осадка, ни газа, ни воды
 Вернуться к заданию Правильно На страницу с объяснением Следующее задание
Вернуться к заданию Правильно На страницу с объяснением Следующее задание
 Вернуться к заданию Не правильно Окислитель – отбирает электроны Например: Cu+2 + 2 e → Cu 0 N+5 + 3 e → N+2 1) S+4 O 2 + 2 Na. OH = Na 2 S+4 O 3 + H 2 O 2) S+4 O 2 + 2 H 2 S = 3 S 0 + 2 H 2 O Следующее задание Восстановитель – отдает электроны Например: Na 0 – 1 e → Na+1 S-2 – 8 e → S+6 степ. окисл. не изменились сера перешла из степ. окисл. +4 в 0, т. е. S+4 + 4 e → S 0 забирают электроны окислители 3) SO 2 + H 2 O <=> H 2 SO 3 степ. окисл. не изменились 4) 2 S+4 O 2 + O 2 <=> 2 S+6 O 3 сера перешла из степ. окисл. +4 в +6, т. е. S+4 - 2 e → S+6 отдают электроны восстановители
Вернуться к заданию Не правильно Окислитель – отбирает электроны Например: Cu+2 + 2 e → Cu 0 N+5 + 3 e → N+2 1) S+4 O 2 + 2 Na. OH = Na 2 S+4 O 3 + H 2 O 2) S+4 O 2 + 2 H 2 S = 3 S 0 + 2 H 2 O Следующее задание Восстановитель – отдает электроны Например: Na 0 – 1 e → Na+1 S-2 – 8 e → S+6 степ. окисл. не изменились сера перешла из степ. окисл. +4 в 0, т. е. S+4 + 4 e → S 0 забирают электроны окислители 3) SO 2 + H 2 O <=> H 2 SO 3 степ. окисл. не изменились 4) 2 S+4 O 2 + O 2 <=> 2 S+6 O 3 сера перешла из степ. окисл. +4 в +6, т. е. S+4 - 2 e → S+6 отдают электроны восстановители
 Вернуться к заданию Правильно На страницу с объяснением Следующее задание
Вернуться к заданию Правильно На страницу с объяснением Следующее задание
 Вернуться к заданию Не правильно Следующее задание Сильные кислоты: HCl, HBr, HI, HNO 3, H 2 SO 4, HCl. O 4 Сильные основания (щелочи) - гидроксиды щелочных и щелочноземельных металлов: Li. OH, Na. OH, KOH, Rb. OH, Cs. OH, Ca(OH)2, Sr(OH)2 и Ba(OH)2 образована из сильного основания KOH - нейтральная среда KCl и сильной кислоты HCl 1) образована из сильного основания Na. OH Na 2 S - щелочная среда и слабой кислоты H S 2 2) 3) 4) K 2 Si. O 3 Na 2 CO 3 Fe. Cl 2 NH 4 Cl Cu. SO 4 Na 2 SO 4 образована из сильного основания KOH и слабой кислоты H 2 Si. O 3 образована из сильного основания Na. OH и слабой кислоты H 2 CO 3 образована из слабого основания Fe(OH)2 и сильной кислоты HCl образована из слабого основания NH 4 OH и сильной кислоты HCl образована из слабого основания Cu(OH)2 и сильной кислоты H 2 SO 4 образована из сильного основания Na. OH и сильной кислоты H 2 SO 4 - щелочная среда - кислая среда - нейтральная среда
Вернуться к заданию Не правильно Следующее задание Сильные кислоты: HCl, HBr, HI, HNO 3, H 2 SO 4, HCl. O 4 Сильные основания (щелочи) - гидроксиды щелочных и щелочноземельных металлов: Li. OH, Na. OH, KOH, Rb. OH, Cs. OH, Ca(OH)2, Sr(OH)2 и Ba(OH)2 образована из сильного основания KOH - нейтральная среда KCl и сильной кислоты HCl 1) образована из сильного основания Na. OH Na 2 S - щелочная среда и слабой кислоты H S 2 2) 3) 4) K 2 Si. O 3 Na 2 CO 3 Fe. Cl 2 NH 4 Cl Cu. SO 4 Na 2 SO 4 образована из сильного основания KOH и слабой кислоты H 2 Si. O 3 образована из сильного основания Na. OH и слабой кислоты H 2 CO 3 образована из слабого основания Fe(OH)2 и сильной кислоты HCl образована из слабого основания NH 4 OH и сильной кислоты HCl образована из слабого основания Cu(OH)2 и сильной кислоты H 2 SO 4 образована из сильного основания Na. OH и сильной кислоты H 2 SO 4 - щелочная среда - кислая среда - нейтральная среда
 Вернуться к заданию Правильно На страницу с объяснением Следующее задание
Вернуться к заданию Правильно На страницу с объяснением Следующее задание
 Вернуться к заданию Не правильно Алканы вступают в реакции: 1) горения; Следующее задание 2) дегидрирования; 3) с галогенами (замещение); 4) изомеризации 2) окисления; Алкены вступают в реакции: 1) горения; 3) дегидрирования; 4) полимеризации; 5) присоединения по двойной связи (гидрогалогенирования, гидратации, галогенирования) 6)качественные реакции (обесцвечивает р-ры KMn. O 4 и бромной воды) 2) тримеризации; Алкины вступают в реакции: 1) горения; 3) окисления; 4) в реакцию Кучерова 5) присоединения по двойной связи (гидрогалогенирования, гидратации, галогенирования) 6)качественные реакции (обесцвечивает р-ры KMn. O 4 и бромной воды) Алкадиены вступают в реакции: 1) горения; 2) окисления; 3) дегидрирования; 4) полимеризации; 5) присоединения по двойной связи (гидрогалогенирования, гидратации, галогенирования) 6)качественные реакции (обесцвечивает р-ры KMn. O 4 и бромной воды) 1) алканы не вступают в реакции полимеризации, т. к. не имеют двойных связей 2) этилен – алкен, значит обесцвечивает раствор KMn. O 4
Вернуться к заданию Не правильно Алканы вступают в реакции: 1) горения; Следующее задание 2) дегидрирования; 3) с галогенами (замещение); 4) изомеризации 2) окисления; Алкены вступают в реакции: 1) горения; 3) дегидрирования; 4) полимеризации; 5) присоединения по двойной связи (гидрогалогенирования, гидратации, галогенирования) 6)качественные реакции (обесцвечивает р-ры KMn. O 4 и бромной воды) 2) тримеризации; Алкины вступают в реакции: 1) горения; 3) окисления; 4) в реакцию Кучерова 5) присоединения по двойной связи (гидрогалогенирования, гидратации, галогенирования) 6)качественные реакции (обесцвечивает р-ры KMn. O 4 и бромной воды) Алкадиены вступают в реакции: 1) горения; 2) окисления; 3) дегидрирования; 4) полимеризации; 5) присоединения по двойной связи (гидрогалогенирования, гидратации, галогенирования) 6)качественные реакции (обесцвечивает р-ры KMn. O 4 и бромной воды) 1) алканы не вступают в реакции полимеризации, т. к. не имеют двойных связей 2) этилен – алкен, значит обесцвечивает раствор KMn. O 4
 Вернуться к заданию Правильно На страницу с объяснением Следующее задание
Вернуться к заданию Правильно На страницу с объяснением Следующее задание
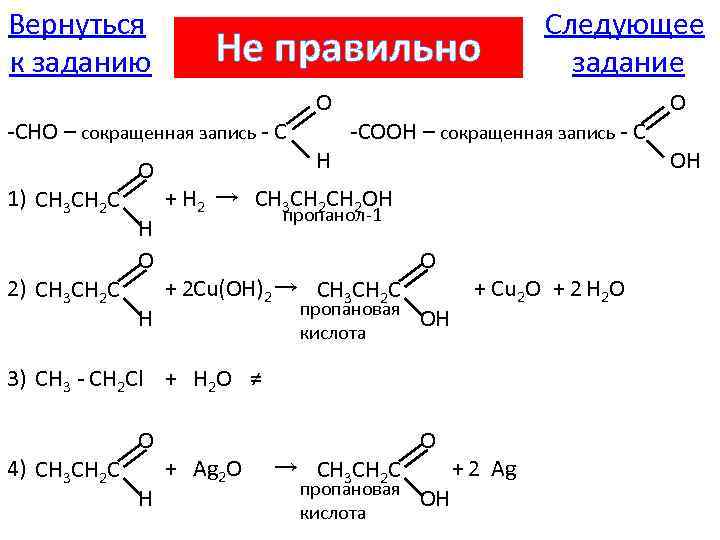 Вернуться к заданию Не правильно -CHO – сокращенная запись - C 1) CH 3 CH 2 C 2) CH 3 CH 2 C O H O H -COOH – сокращенная запись - C + H 2 → CH 3 CH 2 OH пропанол-1 + 2 Cu(OH)2 → CH 3 CH 2 C пропановая кислота O OH + Cu 2 O + 2 H 2 O 3) СН 3 - СН 2 Сl + H 2 O ≠ 4) CH 3 CH 2 C O H Следующее задание + Ag 2 O → CH 3 CH 2 C пропановая кислота O OH + 2 Ag O OH
Вернуться к заданию Не правильно -CHO – сокращенная запись - C 1) CH 3 CH 2 C 2) CH 3 CH 2 C O H O H -COOH – сокращенная запись - C + H 2 → CH 3 CH 2 OH пропанол-1 + 2 Cu(OH)2 → CH 3 CH 2 C пропановая кислота O OH + Cu 2 O + 2 H 2 O 3) СН 3 - СН 2 Сl + H 2 O ≠ 4) CH 3 CH 2 C O H Следующее задание + Ag 2 O → CH 3 CH 2 C пропановая кислота O OH + 2 Ag O OH
 Вернуться к заданию Правильно На страницу с объяснением Следующее задание
Вернуться к заданию Правильно На страницу с объяснением Следующее задание
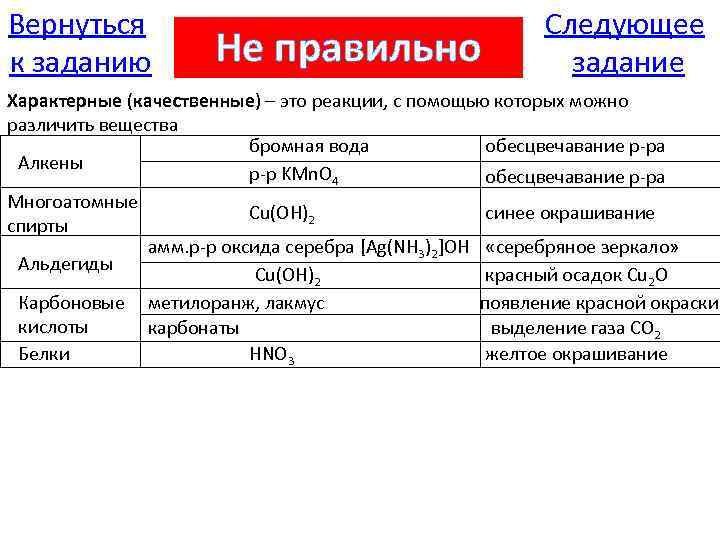 Вернуться к заданию Не правильно Следующее задание Характерные (качественные) – это реакции, с помощью которых можно различить вещества бромная вода обесцвечавание р-ра Алкены р-р KMn. O 4 обесцвечавание р-ра Многоатомные Cu(OH)2 синее окрашивание спирты амм. р-р оксида серебра [Ag(NH 3)2]OH «серебряное зеркало» Альдегиды Cu(OH)2 красный осадок Cu 2 O Карбоновые метилоранж, лакмус появление красной окраски кислоты карбонаты выделение газа CO 2 Белки HNO 3 желтое окрашивание
Вернуться к заданию Не правильно Следующее задание Характерные (качественные) – это реакции, с помощью которых можно различить вещества бромная вода обесцвечавание р-ра Алкены р-р KMn. O 4 обесцвечавание р-ра Многоатомные Cu(OH)2 синее окрашивание спирты амм. р-р оксида серебра [Ag(NH 3)2]OH «серебряное зеркало» Альдегиды Cu(OH)2 красный осадок Cu 2 O Карбоновые метилоранж, лакмус появление красной окраски кислоты карбонаты выделение газа CO 2 Белки HNO 3 желтое окрашивание
 Вернуться к заданию Правильно На страницу с объяснением Следующее задание
Вернуться к заданию Правильно На страницу с объяснением Следующее задание
 Вернуться к заданию Не правильно Следующее задание Получение некоторых веществ: Водород H 2 - из воды (электролизом) Азот N 2 из воздуха Кислород O 2 - из воздуха Аммиак NH 3 - из азота N 2 и водорода H 2 Серная кислота H 2 SO 4 - из серы и серосодержащих веществ по схеме: Fe. S 2 S SO 2 SO 3 H 2 S Метанол CH 3 OH - из синтез-газа (смеси CO и H 2)
Вернуться к заданию Не правильно Следующее задание Получение некоторых веществ: Водород H 2 - из воды (электролизом) Азот N 2 из воздуха Кислород O 2 - из воздуха Аммиак NH 3 - из азота N 2 и водорода H 2 Серная кислота H 2 SO 4 - из серы и серосодержащих веществ по схеме: Fe. S 2 S SO 2 SO 3 H 2 S Метанол CH 3 OH - из синтез-газа (смеси CO и H 2)
 Вернуться к заданию Правильно На страницу с объяснением Следующее задание
Вернуться к заданию Правильно На страницу с объяснением Следующее задание
 Вернуться к заданию Не правильно Следующее задание 2 СО(г) + О 2(г) = 2 СО 2(г) + 566 к. Дж В уравнении: угарного газа – 2 моль, выделяется 566 к. Дж теплоты В условии: выделяется 152 к. Дж теплоты 2 моль CO - 566 к. Дж Х моль CO - 152 к. Дж 2 × 152 = 0, 537 моль Х= 566 V (CO) = n × Vm = 0, 537 × 22, 4 = 12 л
Вернуться к заданию Не правильно Следующее задание 2 СО(г) + О 2(г) = 2 СО 2(г) + 566 к. Дж В уравнении: угарного газа – 2 моль, выделяется 566 к. Дж теплоты В условии: выделяется 152 к. Дж теплоты 2 моль CO - 566 к. Дж Х моль CO - 152 к. Дж 2 × 152 = 0, 537 моль Х= 566 V (CO) = n × Vm = 0, 537 × 22, 4 = 12 л
 Вернуться к заданию CH 3 1) CH 3 Следующее задание - ароматический углеводород (арен) 1, 2 -диметилбензол о-ксилол - спирт (предельный – нет двойных, 2) CH 3 -CH 2 -CH 3 тройных связей; одноатомный – одна OH гексанол-3 группа –OH) O 3) H-C - сложный эфир O – CH 3 метилформиат метиловый эфир муравьиной кислота CH=CH 2 4) - ароматический углеводород (арен) винилбензол стирол
Вернуться к заданию CH 3 1) CH 3 Следующее задание - ароматический углеводород (арен) 1, 2 -диметилбензол о-ксилол - спирт (предельный – нет двойных, 2) CH 3 -CH 2 -CH 3 тройных связей; одноатомный – одна OH гексанол-3 группа –OH) O 3) H-C - сложный эфир O – CH 3 метилформиат метиловый эфир муравьиной кислота CH=CH 2 4) - ароматический углеводород (арен) винилбензол стирол
 Вернуться к заданию А) CH 2 Cl 2 Б) HCHO В) HCOONa Г) CBr 4 Следующее задание Cl ближе к F, значит перетягивает к себе электроны от C C ближе к F, чем H, значит перетягивает электроны от 2 атомов H, но 2 атома хлора перетягивают электроны от C 0 +1 -1 значит: C H 2 Cl 2 O ближе к F, значит перетягивает к себе электроны от C C ближе к F, чем H, значит перетягивает электроны от 2 атомов H, но атом кислорода перетягивает 2 электрона от C +1 0 +1 -2 значит: H C H O O ближе к F, значит перетягивает к себе электроны от C и Na C ближе к F, чем H, значит перетягивает электрон от атома H Один атом O перетягивает 2 электрона от атома C, другой перетягивает 1 электрон от C и 1 электрон от H +1+2 -2 -2 +1 значит: H C O O Na Br ближе к F, значит перетягивает к себе электроны от атома C +4 -1 значит: CBr 4
Вернуться к заданию А) CH 2 Cl 2 Б) HCHO В) HCOONa Г) CBr 4 Следующее задание Cl ближе к F, значит перетягивает к себе электроны от C C ближе к F, чем H, значит перетягивает электроны от 2 атомов H, но 2 атома хлора перетягивают электроны от C 0 +1 -1 значит: C H 2 Cl 2 O ближе к F, значит перетягивает к себе электроны от C C ближе к F, чем H, значит перетягивает электроны от 2 атомов H, но атом кислорода перетягивает 2 электрона от C +1 0 +1 -2 значит: H C H O O ближе к F, значит перетягивает к себе электроны от C и Na C ближе к F, чем H, значит перетягивает электрон от атома H Один атом O перетягивает 2 электрона от атома C, другой перетягивает 1 электрон от C и 1 электрон от H +1+2 -2 -2 +1 значит: H C O O Na Br ближе к F, значит перетягивает к себе электроны от атома C +4 -1 значит: CBr 4
 Вернуться к заданию Активные металлы, не могут выделяться на катоде, вместо них выделяется H 2 Металлы средней Неактивные металлы, активности, на катоде выделяются одновременно металл и H 2 OH-, NO 2 -, NO 3 -, SO 32 -, SO 42 -, CO 32 -, Si. O 32 -, PO 43 -, CH 3 COO- … и Fкислородсодержащие анионы и фторид не окисляются на аноде вместо них выделяется O 2 A) Cu(NO 3)2 Б) Ag. NO 3 В) Сa. Cl 2 Г) Na 2 SO 4 Следующее задание Cl-, Br-, I-, S 2 бескислородные анионы окисляются на аноде выделяются: Cl 2, Br 2, I 2, S Cu – неактивный металл, выделяется на катоде Ag – неактивный металл, выделяется на катоде Ca – активный металл, на катоде выделяется H 2 Na – активный металл, на катоде выделяется H 2
Вернуться к заданию Активные металлы, не могут выделяться на катоде, вместо них выделяется H 2 Металлы средней Неактивные металлы, активности, на катоде выделяются одновременно металл и H 2 OH-, NO 2 -, NO 3 -, SO 32 -, SO 42 -, CO 32 -, Si. O 32 -, PO 43 -, CH 3 COO- … и Fкислородсодержащие анионы и фторид не окисляются на аноде вместо них выделяется O 2 A) Cu(NO 3)2 Б) Ag. NO 3 В) Сa. Cl 2 Г) Na 2 SO 4 Следующее задание Cl-, Br-, I-, S 2 бескислородные анионы окисляются на аноде выделяются: Cl 2, Br 2, I 2, S Cu – неактивный металл, выделяется на катоде Ag – неактивный металл, выделяется на катоде Ca – активный металл, на катоде выделяется H 2 Na – активный металл, на катоде выделяется H 2
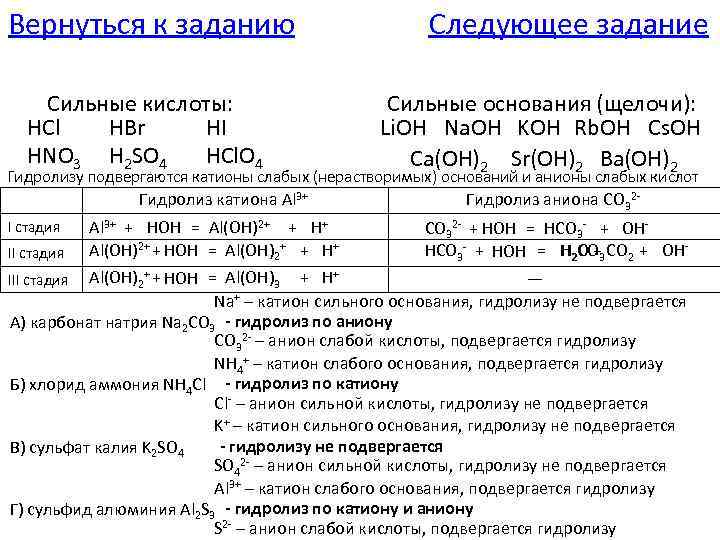 Вернуться к заданию Сильные кислоты: HCl HBr HI HNO 3 H 2 SO 4 HCl. O 4 Следующее задание Сильные основания (щелочи): Li. OH Na. OH KOH Rb. OH Cs. OH Ca(OH)2 Sr(OH)2 Ba(OH)2 Гидролизу подвергаются катионы слабых (нерастворимых) оснований и анионы слабых кислот Гидролиз катиона Al 3+ I стадия II стадия Al 3+ + HOH = Al(OH)2+ + H+ Al(OH)2+ + HOH = Al(OH)2+ + H+ Гидролиз аниона CO 32 - + HOH = HCO 3 - + OHHCO 3 - + HOH = H 2 O +3 CO 2 + OHCO Al(OH)2+ + HOH = Al(OH)3 + H+ — Na+ – катион сильного основания, гидролизу не подвергается А) карбонат натрия Na 2 CO 3 - гидролиз по аниону CO 32 - – анион слабой кислоты, подвергается гидролизу NH 4+ – катион слабого основания, подвергается гидролизу Б) хлорид аммония NH 4 Cl - гидролиз по катиону Cl- – анион сильной кислоты, гидролизу не подвергается K+ – катион сильного основания, гидролизу не подвергается - гидролизу не подвергается В) сульфат калия K 2 SO 42 - – анион сильной кислоты, гидролизу не подвергается Al 3+ – катион слабого основания, подвергается гидролизу Г) сульфид алюминия Al 2 S 3 - гидролиз по катиону и аниону S 2 - – анион слабой кислоты, подвергается гидролизу III стадия
Вернуться к заданию Сильные кислоты: HCl HBr HI HNO 3 H 2 SO 4 HCl. O 4 Следующее задание Сильные основания (щелочи): Li. OH Na. OH KOH Rb. OH Cs. OH Ca(OH)2 Sr(OH)2 Ba(OH)2 Гидролизу подвергаются катионы слабых (нерастворимых) оснований и анионы слабых кислот Гидролиз катиона Al 3+ I стадия II стадия Al 3+ + HOH = Al(OH)2+ + H+ Al(OH)2+ + HOH = Al(OH)2+ + H+ Гидролиз аниона CO 32 - + HOH = HCO 3 - + OHHCO 3 - + HOH = H 2 O +3 CO 2 + OHCO Al(OH)2+ + HOH = Al(OH)3 + H+ — Na+ – катион сильного основания, гидролизу не подвергается А) карбонат натрия Na 2 CO 3 - гидролиз по аниону CO 32 - – анион слабой кислоты, подвергается гидролизу NH 4+ – катион слабого основания, подвергается гидролизу Б) хлорид аммония NH 4 Cl - гидролиз по катиону Cl- – анион сильной кислоты, гидролизу не подвергается K+ – катион сильного основания, гидролизу не подвергается - гидролизу не подвергается В) сульфат калия K 2 SO 42 - – анион сильной кислоты, гидролизу не подвергается Al 3+ – катион слабого основания, подвергается гидролизу Г) сульфид алюминия Al 2 S 3 - гидролиз по катиону и аниону S 2 - – анион слабой кислоты, подвергается гидролизу III стадия
 Вернуться к заданию Следующее задание A) KHCO 3 + KOH → K 2 CO 3 + H 2 O Б) KHCO 3 + KCl HCl→ + H 2 O +3 CO 2 H 2 CO В) K 2 CO 3 + 2 HNO 3→ 2 KNO 3 + H 2 O +3 CO 2 H 2 CO Г) K 2 CO 3 + Ва. Cl 2→ KCl + Ba. CO 3
Вернуться к заданию Следующее задание A) KHCO 3 + KOH → K 2 CO 3 + H 2 O Б) KHCO 3 + KCl HCl→ + H 2 O +3 CO 2 H 2 CO В) K 2 CO 3 + 2 HNO 3→ 2 KNO 3 + H 2 O +3 CO 2 H 2 CO Г) K 2 CO 3 + Ва. Cl 2→ KCl + Ba. CO 3
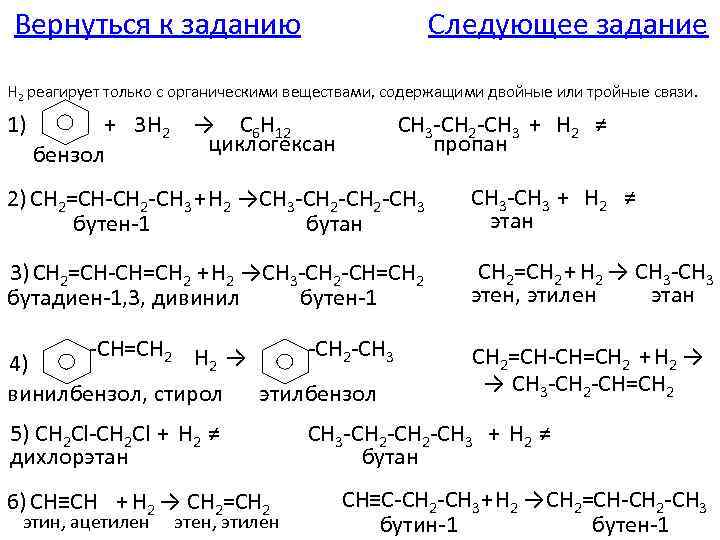 Вернуться к заданию Следующее задание H 2 реагирует только с органическими веществами, содержащими двойные или тройные связи. 1) + 3 H 2 → C 6 H 12 циклогексан бензол CH 3 -CH 2 -CH 3 + H 2 ≠ пропан 2) CH 2=CH-CH 2 -CH 3 +H 2 →CH 3 -CH 2 -CH 3 бутен-1 бутан CH 3 -CH 3 + H 2 ≠ этан 3) CH 2=CH-CH=CH 2 +H 2 →CH 3 -CH 2 -CH=CH 2 бутадиен-1, 3, дивинил бутен-1 CH 2=CH 2 + H 2 → CH 3 -CH 3 этен, этилен этан -CH=CH 2 H → -CH 2 -CH 3 4) 2 винилбензол, стирол этилбензол CH 2=CH-CH=CH 2 +H 2 → → CH 3 -CH 2 -CH=CH 2 5) CH 2 Cl-CH 2 Cl + H 2 ≠ дихлорэтан 6) CH≡CH + H 2 → CH 2=CH 2 этин, ацетилен этен, этилен CH 3 -CH 2 -CH 3 + H 2 ≠ бутан CH≡C-CH 2 -CH 3+H 2 →CH 2=CH-CH 2 -CH 3 бутин-1 бутен-1
Вернуться к заданию Следующее задание H 2 реагирует только с органическими веществами, содержащими двойные или тройные связи. 1) + 3 H 2 → C 6 H 12 циклогексан бензол CH 3 -CH 2 -CH 3 + H 2 ≠ пропан 2) CH 2=CH-CH 2 -CH 3 +H 2 →CH 3 -CH 2 -CH 3 бутен-1 бутан CH 3 -CH 3 + H 2 ≠ этан 3) CH 2=CH-CH=CH 2 +H 2 →CH 3 -CH 2 -CH=CH 2 бутадиен-1, 3, дивинил бутен-1 CH 2=CH 2 + H 2 → CH 3 -CH 3 этен, этилен этан -CH=CH 2 H → -CH 2 -CH 3 4) 2 винилбензол, стирол этилбензол CH 2=CH-CH=CH 2 +H 2 → → CH 3 -CH 2 -CH=CH 2 5) CH 2 Cl-CH 2 Cl + H 2 ≠ дихлорэтан 6) CH≡CH + H 2 → CH 2=CH 2 этин, ацетилен этен, этилен CH 3 -CH 2 -CH 3 + H 2 ≠ бутан CH≡C-CH 2 -CH 3+H 2 →CH 2=CH-CH 2 -CH 3 бутин-1 бутен-1
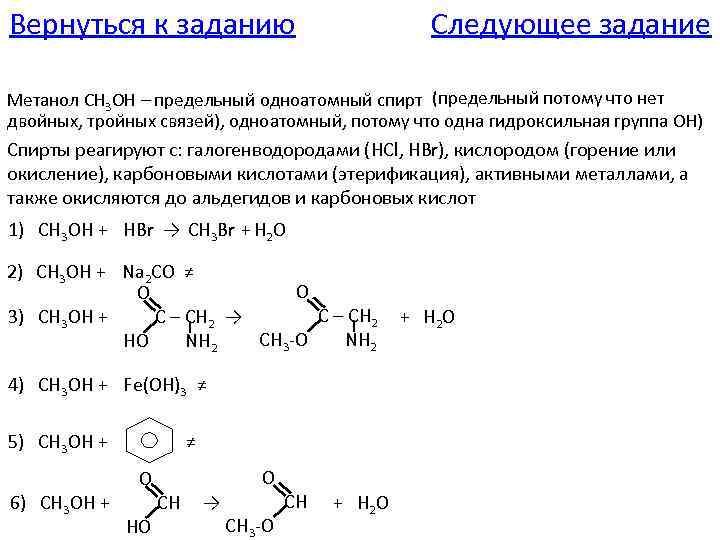 Вернуться к заданию Следующее задание Метанол CH 3 OH – предельный одноатомный спирт (предельный потому что нет двойных, тройных связей), одноатомный, потому что одна гидроксильная группа OH) Спирты реагируют с: галогенводородами (HCl, HBr), кислородом (горение или окисление), карбоновыми кислотами (этерификация), активными металлами, а также окисляются до альдегидов и карбоновых кислот 1) CH 3 OH + HBr → CH 3 Br + H 2 O 2) CH 3 OH + Na 2 CO ≠ O O C – CH 2 → 3) CH 3 OH + CH 3 -O NH 2 HO NH 2 4) CH 3 OH + Fe(OH)3 ≠ 5) CH 3 OH + 6) CH 3 OH + ≠ O HO O CH → CH 3 -O CH + H 2 O
Вернуться к заданию Следующее задание Метанол CH 3 OH – предельный одноатомный спирт (предельный потому что нет двойных, тройных связей), одноатомный, потому что одна гидроксильная группа OH) Спирты реагируют с: галогенводородами (HCl, HBr), кислородом (горение или окисление), карбоновыми кислотами (этерификация), активными металлами, а также окисляются до альдегидов и карбоновых кислот 1) CH 3 OH + HBr → CH 3 Br + H 2 O 2) CH 3 OH + Na 2 CO ≠ O O C – CH 2 → 3) CH 3 OH + CH 3 -O NH 2 HO NH 2 4) CH 3 OH + Fe(OH)3 ≠ 5) CH 3 OH + 6) CH 3 OH + ≠ O HO O CH → CH 3 -O CH + H 2 O
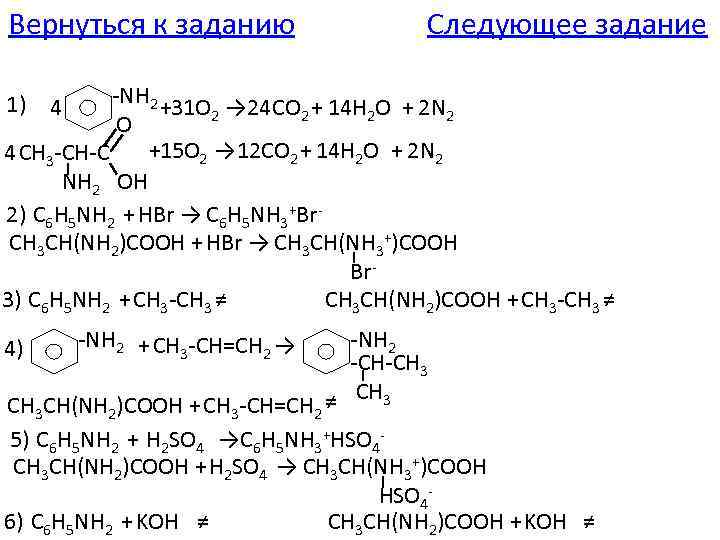 Вернуться к заданию Следующее задание -NH 2 +31 O → 24 CO + 14 H O + 2 N 2 2 O +15 O 2 → 12 CO 2 + 14 H 2 O + 2 N 2 4 CH 3 -CH-C NH 2 OH 2) C 6 H 5 NH 2 +HBr → C 6 H 5 NH 3+Br. CH 3 CH(NH 2)COOH +HBr → CH 3 CH(NH 3+)COOH Br 3) C 6 H 5 NH 2 +CH 3 -CH 3 ≠ CH 3 CH(NH 2)COOH +CH 3 -CH 3 ≠ 1) 4 -NH 2 -CH-CH 3 ≠ CH 3 CH(NH 2)COOH +CH 3 -CH=CH 2 5) C 6 H 5 NH 2 + H 2 SO 4 →C 6 H 5 NH 3+HSO 4 CH 3 CH(NH 2)COOH +H 2 SO 4 → CH 3 CH(NH 3+)COOH HSO 46) C 6 H 5 NH 2 +KOH ≠ CH 3 CH(NH 2)COOH +KOH ≠ 4) -NH 2 +CH 3 -CH=CH 2 →
Вернуться к заданию Следующее задание -NH 2 +31 O → 24 CO + 14 H O + 2 N 2 2 O +15 O 2 → 12 CO 2 + 14 H 2 O + 2 N 2 4 CH 3 -CH-C NH 2 OH 2) C 6 H 5 NH 2 +HBr → C 6 H 5 NH 3+Br. CH 3 CH(NH 2)COOH +HBr → CH 3 CH(NH 3+)COOH Br 3) C 6 H 5 NH 2 +CH 3 -CH 3 ≠ CH 3 CH(NH 2)COOH +CH 3 -CH 3 ≠ 1) 4 -NH 2 -CH-CH 3 ≠ CH 3 CH(NH 2)COOH +CH 3 -CH=CH 2 5) C 6 H 5 NH 2 + H 2 SO 4 →C 6 H 5 NH 3+HSO 4 CH 3 CH(NH 2)COOH +H 2 SO 4 → CH 3 CH(NH 3+)COOH HSO 46) C 6 H 5 NH 2 +KOH ≠ CH 3 CH(NH 2)COOH +KOH ≠ 4) -NH 2 +CH 3 -CH=CH 2 →
 Вернуться к заданию mвещества ω= mраствора (смеси) Следующее задание mв-ва = mр-ра (смеси) × ω m (CH 3 COOH) = mр-ра 1 × ω1= 20 × 0, 7 = 14 г mвещества mраствора (смеси) = ω m(CH 3 COOH) 14 mраствора (смеси)2 = = = 466, 67 г ω2 0, 03 m (воды) = 466, 67 - 20 = 446, 67 г Ответ с точностью до целых: 447
Вернуться к заданию mвещества ω= mраствора (смеси) Следующее задание mв-ва = mр-ра (смеси) × ω m (CH 3 COOH) = mр-ра 1 × ω1= 20 × 0, 7 = 14 г mвещества mраствора (смеси) = ω m(CH 3 COOH) 14 mраствора (смеси)2 = = = 466, 67 г ω2 0, 03 m (воды) = 466, 67 - 20 = 446, 67 г Ответ с точностью до целых: 447
 Вернуться к заданию Zn + Pb(NO 3)2 = Zn(NO 3)2 + Pb 65 m 6, 6 n(Zn) = = = 0, 1 моль M 65 n(Zn) = n(Pb) 0, 1 = n(Pb) 1 1 n(Pb) = 0, 1 моль 207 m(Pb)= n M= 0, 1 207 = 20, 7 г Ответ с точностью до целых: 21 Следующее задание
Вернуться к заданию Zn + Pb(NO 3)2 = Zn(NO 3)2 + Pb 65 m 6, 6 n(Zn) = = = 0, 1 моль M 65 n(Zn) = n(Pb) 0, 1 = n(Pb) 1 1 n(Pb) = 0, 1 моль 207 m(Pb)= n M= 0, 1 207 = 20, 7 г Ответ с точностью до целых: 21 Следующее задание
 Вернуться к заданию Следующее задание 2 KMn. O 4+ 5 H 2 S + 3 H 2 SO 4→ 2 Mn. SO 4+ 5 S+ K 2 SO 4+ 8 H 2 O +7 +2 Mn +5 e → Mn S -2 -2 e → S 0 2 окислитель, восстановление 5 восстановитель, окисление Сначала определим неизвестные продукты В правой части уравнения не хватает K. Калий соединится с молекулами среды, т. е. с SO 42 В ОВР почти всегда присутствует вода. Один из продуктов – H 2 O Составим схемы окисления и восстановления Поставим полученные цифры в уравнение Уравняем остальное
Вернуться к заданию Следующее задание 2 KMn. O 4+ 5 H 2 S + 3 H 2 SO 4→ 2 Mn. SO 4+ 5 S+ K 2 SO 4+ 8 H 2 O +7 +2 Mn +5 e → Mn S -2 -2 e → S 0 2 окислитель, восстановление 5 восстановитель, окисление Сначала определим неизвестные продукты В правой части уравнения не хватает K. Калий соединится с молекулами среды, т. е. с SO 42 В ОВР почти всегда присутствует вода. Один из продуктов – H 2 O Составим схемы окисления и восстановления Поставим полученные цифры в уравнение Уравняем остальное
 Вернуться к заданию Al Следующее задание Mn. O 2 Cu. SO 4 HCl 6 Al +2 Mn. O 2 = 3 Al 2 O 3 +2 Mn Al – более активный металл, чем Mn, значит вытесняет его из соединений 2 Al +3 Cu. SO 4 = Al 2(SO 4)3 +3 Cu Al – более активный металл, чем Cu, значит вытесняет его из соединений 2 Al + 6 HCl =2 Al. Cl 3 +3 H 2 Al –активный металл (левее H), значит вытесняет водород из кислот Mn. O 2 + Cu. SO 4 ≠ амфотерные оксиды не реагируют с солями 2 Mn. O 2 проявляет окислительные свойства 1 окислитель, восстановление 2 1 восстановитель, окисление Mn. O 2 + 4 HCl = Cl 2 + Mn. Cl 2 + 2 H 2 O +4 Mn +2 e -1 2 Cl -2 e Cu. SO 4 + HCl → → ≠ +2 Mn 0 Cl 2 реакции обмена возможны, только если получаются осадок, газ или вода
Вернуться к заданию Al Следующее задание Mn. O 2 Cu. SO 4 HCl 6 Al +2 Mn. O 2 = 3 Al 2 O 3 +2 Mn Al – более активный металл, чем Mn, значит вытесняет его из соединений 2 Al +3 Cu. SO 4 = Al 2(SO 4)3 +3 Cu Al – более активный металл, чем Cu, значит вытесняет его из соединений 2 Al + 6 HCl =2 Al. Cl 3 +3 H 2 Al –активный металл (левее H), значит вытесняет водород из кислот Mn. O 2 + Cu. SO 4 ≠ амфотерные оксиды не реагируют с солями 2 Mn. O 2 проявляет окислительные свойства 1 окислитель, восстановление 2 1 восстановитель, окисление Mn. O 2 + 4 HCl = Cl 2 + Mn. Cl 2 + 2 H 2 O +4 Mn +2 e -1 2 Cl -2 e Cu. SO 4 + HCl → → ≠ +2 Mn 0 Cl 2 реакции обмена возможны, только если получаются осадок, газ или вода
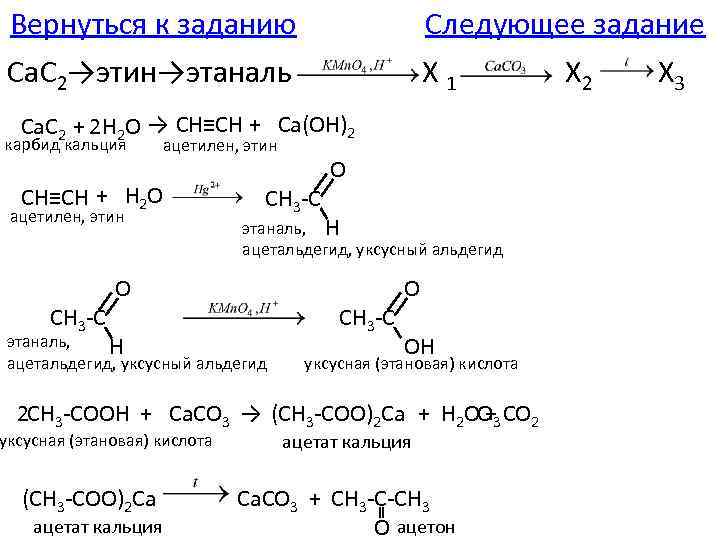 Вернуться к заданию Следующее задание Ca. C 2→этин→этаналь X 1 Ca. C 2 + 2 H 2 O → CH≡CH + Ca(OH)2 карбид кальция ацетилен, этин CH≡CH + H 2 O ацетилен, этин CH 3 -C O этаналь, H ацетальдегид, уксусный альдегид CH 3 -C O OH уксусная (этановая) кислота 2 CH 3 -COOH + Ca. CO 3 → (CH 3 -COO)2 Ca + H 2 CO 3 CO 2 O+ уксусная (этановая) кислота (CH 3 -COO)2 Ca ацетат кальция Ca. CO 3 + CH 3 -C-CH 3 O ацетон X 2 X 3
Вернуться к заданию Следующее задание Ca. C 2→этин→этаналь X 1 Ca. C 2 + 2 H 2 O → CH≡CH + Ca(OH)2 карбид кальция ацетилен, этин CH≡CH + H 2 O ацетилен, этин CH 3 -C O этаналь, H ацетальдегид, уксусный альдегид CH 3 -C O OH уксусная (этановая) кислота 2 CH 3 -COOH + Ca. CO 3 → (CH 3 -COO)2 Ca + H 2 CO 3 CO 2 O+ уксусная (этановая) кислота (CH 3 -COO)2 Ca ацетат кальция Ca. CO 3 + CH 3 -C-CH 3 O ацетон X 2 X 3
 Вернуться к заданию Следующее задание Сероводород объемом 5, 6 л (н. у. ) прореагировал без остатка с 59, 02 мл раствора КOH с массовой долей 20% (плотность 1, 186 г/мл). Определите массу соли, полученной в результате этой химической реакции Порядок решения задач С 4: Решение: 1. Дано: уравнения реакций (иногда для этого требуется рассчитать количества Записать V = 5, 6 = 0, 25 моль Определим возможные реакции V(H 2 S)=17, 4 л n (H 2 S) = веществ) V 2: Вариантов m 22, 4 Vр. Рассчитать количества известных веществ (KOH) = 59, 02 мл 2. H 2 (KOH)= V = 2 S = 59, 02 • 1, 186 = 70 г ω (KOH) = 20% г mр. S + 2 KOH р • Kρр + 2 H 2 O или 3. (KOH) = 1, 186 г/мл ρр Определить количество неизвестного вещества (по. O H 2 S + KOH = KHS + H 2 уравнению реакции) m (KOH) • (для задания ω = 70 • вариант г 4. Определить требуемую величину = mр С 4 второй 0, 2 = 14 вероятнее) m (соли) - ? 39 16 1 m = 14 = 0, 25 моль Рассчитаем количества известных веществ n (KOH) = M 56 Vm – молярный объем H 2 S + н. у. молярный 2 O При KOH = KHS + H объем любого газа равен n 22, 4 л/моль (KHS) = n (KOH) = 0, 25 моль 39 1 32 Выбираем второй вариант уравнения (т. к. в m (KHS) = n • M = 0, 25 • 72 = 18 г первом варианте KOH должно быть в 2 раза Ответ: 18 а в расчетах KOH 0, 25 моль и H S больше, г 2 тоже 0, 25 моль)
Вернуться к заданию Следующее задание Сероводород объемом 5, 6 л (н. у. ) прореагировал без остатка с 59, 02 мл раствора КOH с массовой долей 20% (плотность 1, 186 г/мл). Определите массу соли, полученной в результате этой химической реакции Порядок решения задач С 4: Решение: 1. Дано: уравнения реакций (иногда для этого требуется рассчитать количества Записать V = 5, 6 = 0, 25 моль Определим возможные реакции V(H 2 S)=17, 4 л n (H 2 S) = веществ) V 2: Вариантов m 22, 4 Vр. Рассчитать количества известных веществ (KOH) = 59, 02 мл 2. H 2 (KOH)= V = 2 S = 59, 02 • 1, 186 = 70 г ω (KOH) = 20% г mр. S + 2 KOH р • Kρр + 2 H 2 O или 3. (KOH) = 1, 186 г/мл ρр Определить количество неизвестного вещества (по. O H 2 S + KOH = KHS + H 2 уравнению реакции) m (KOH) • (для задания ω = 70 • вариант г 4. Определить требуемую величину = mр С 4 второй 0, 2 = 14 вероятнее) m (соли) - ? 39 16 1 m = 14 = 0, 25 моль Рассчитаем количества известных веществ n (KOH) = M 56 Vm – молярный объем H 2 S + н. у. молярный 2 O При KOH = KHS + H объем любого газа равен n 22, 4 л/моль (KHS) = n (KOH) = 0, 25 моль 39 1 32 Выбираем второй вариант уравнения (т. к. в m (KHS) = n • M = 0, 25 • 72 = 18 г первом варианте KOH должно быть в 2 раза Ответ: 18 а в расчетах KOH 0, 25 моль и H S больше, г 2 тоже 0, 25 моль)
 Вернуться к заданию К выбору задания При взаимодействии 25, 5 г предельной одноосновной кислоты с избытком раствора гидрокарбоната натрия выделилось 5, 6 л (н. у. ) газа. Определите молекулярную формулу кислоты Порядок решения задач. Решение: С 5: Дано: 1. (C H O )=25, 5 г виде m Записать уравнение в. Cобщем + Na. HCO 3 = Cn. H 2 n-1 O 2 Na +H 2 O +CO 2 n 2 n 2 n. H 2 n. O 2 2. Найти количества известных веществ (иногда в общем виде) V (CO 2) = 59, 02 количества веществ и m 25, 5 3. Приравнять мл решить уравнение = n (Cn. H 2 n. O )= Чтобы записать уравнение нужно 2 определить общую формулы m (соли) - ? M 14 n+32 предельной одноосновной кислоты (предельная – нет двойных, 5, 6 V = = 0, 25 группа n (CO 2) = тройных связей, одноосновная – одна карбоксильнаямоль -COOH) 22, 4 Vm Для примера возьмем бутановую кислоту: штук, вместе 2 их масса 12 n 1 атом C имеет массу 12, в Cn 25, 5 2 атомов C n CH 3 -CH 2 -CH -COOH H 2 n. O Молекулярнаямассу 1, в Cn. H 2 n. OO 2 или Cn. H 2 n. Oштук, вместе их масса 2 n 1 атом H имеет формула: C 4 H 8 2 атомов H 2 n 2 = 0, 25 Любая O имеет массу 16, в Cn. Hреагирует с. O два, вместе их масса 32 карбоновая кислоты 2 n. O 2 атомов карбонатами с 14 n+32 1 атом Итого: молярнаяуглекислого 2 равна 12 n+2 n+32 = 14 n+32 образованием масса Cn. H 2 n. O газа CO 2 0, 25 (14 n+32) = равен Vm (молярный объем) любого • газа при н. у. 25, 5 22, 4 л/моль 3, 5 n + 8 = 25, 5 3, 5 n = 17, 5 n = 5 Ответ: C 5 H 10 O 2
Вернуться к заданию К выбору задания При взаимодействии 25, 5 г предельной одноосновной кислоты с избытком раствора гидрокарбоната натрия выделилось 5, 6 л (н. у. ) газа. Определите молекулярную формулу кислоты Порядок решения задач. Решение: С 5: Дано: 1. (C H O )=25, 5 г виде m Записать уравнение в. Cобщем + Na. HCO 3 = Cn. H 2 n-1 O 2 Na +H 2 O +CO 2 n 2 n 2 n. H 2 n. O 2 2. Найти количества известных веществ (иногда в общем виде) V (CO 2) = 59, 02 количества веществ и m 25, 5 3. Приравнять мл решить уравнение = n (Cn. H 2 n. O )= Чтобы записать уравнение нужно 2 определить общую формулы m (соли) - ? M 14 n+32 предельной одноосновной кислоты (предельная – нет двойных, 5, 6 V = = 0, 25 группа n (CO 2) = тройных связей, одноосновная – одна карбоксильнаямоль -COOH) 22, 4 Vm Для примера возьмем бутановую кислоту: штук, вместе 2 их масса 12 n 1 атом C имеет массу 12, в Cn 25, 5 2 атомов C n CH 3 -CH 2 -CH -COOH H 2 n. O Молекулярнаямассу 1, в Cn. H 2 n. OO 2 или Cn. H 2 n. Oштук, вместе их масса 2 n 1 атом H имеет формула: C 4 H 8 2 атомов H 2 n 2 = 0, 25 Любая O имеет массу 16, в Cn. Hреагирует с. O два, вместе их масса 32 карбоновая кислоты 2 n. O 2 атомов карбонатами с 14 n+32 1 атом Итого: молярнаяуглекислого 2 равна 12 n+2 n+32 = 14 n+32 образованием масса Cn. H 2 n. O газа CO 2 0, 25 (14 n+32) = равен Vm (молярный объем) любого • газа при н. у. 25, 5 22, 4 л/моль 3, 5 n + 8 = 25, 5 3, 5 n = 17, 5 n = 5 Ответ: C 5 H 10 O 2
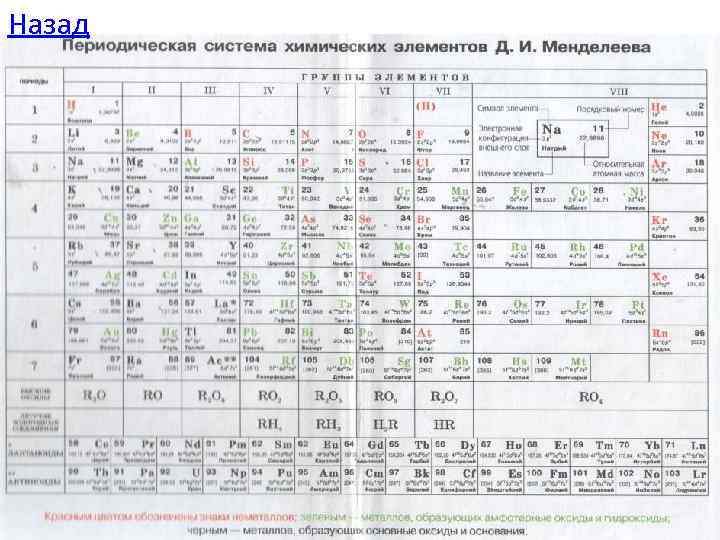 Назад
Назад
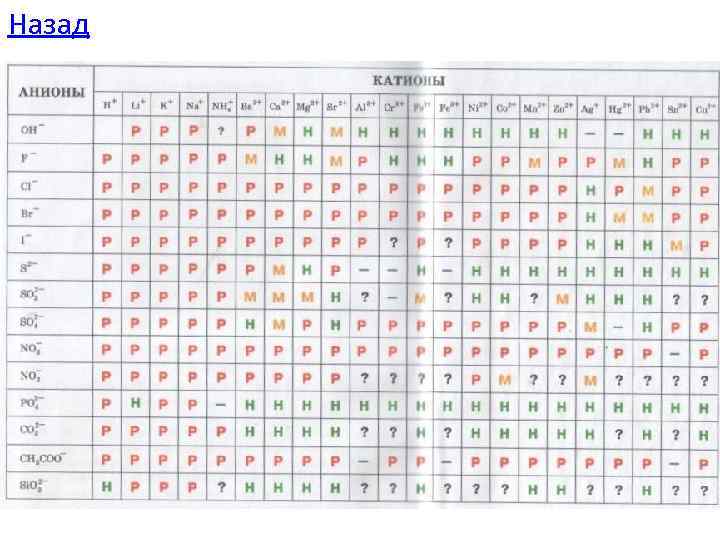 Назад
Назад
 Назад
Назад
 Назад Металлы Неметаллы Li Be Na Mg Al K Ca Cr Mn Fe Cu Zn Ag Ba Pt Au Hg H 2 He B C N 2 O 2 О 3 Cl 2 Ar F 2 Ne Si P S Br 2 I 2 литий бериллий натрий магний алюминий кальций хром марганец железо медь цинк серебро барий платина золото ртуть водород гелий бор углерод азот кислород озон хлор аргон фтор неон кремний фосфор сера бром йод
Назад Металлы Неметаллы Li Be Na Mg Al K Ca Cr Mn Fe Cu Zn Ag Ba Pt Au Hg H 2 He B C N 2 O 2 О 3 Cl 2 Ar F 2 Ne Si P S Br 2 I 2 литий бериллий натрий магний алюминий кальций хром марганец железо медь цинк серебро барий платина золото ртуть водород гелий бор углерод азот кислород озон хлор аргон фтор неон кремний фосфор сера бром йод
 Назад основные (оксиды металлов) Li 2 O оксид лития Na 2 O оксид натрия K 2 O оксид калия Ca. O оксид кальция Sr. O оксид стронция Ba. O оксид бария Mg. O оксид магния Fe. O оксид железа (II) Cu. O оксид меди (II) Оксиды амфотерные Be. O оксид бериллия Zn. O оксид цинка Pb. O оксид свинца (II) Cr 2 O 3 оксид хрома (III) Fe 2 O 3 оксид железа (III) Cr 2 O 3 оксид хрома (III) несолеобразующие N 2 O оксид азота (I) NO оксид азота (II) CO оксид углерода (II), угарный газ Si. O оксид кремния (II) Кислотные (оксиды неметаллов, некоторых металлов в степенях окисления +5, +6 и +7) SO 2 оксид серы (IV) SO 3 оксид серы (VI) NO 2 оксид азота (IV) N 2 O 5 оксид азота (V) CO 2 углекислый газ оксид углерода (IV), P 2 O 5 оксид фосфора (V) Si. O 2 оксид кремния (IV) Cl 2 O 7 оксид хлора (VII)
Назад основные (оксиды металлов) Li 2 O оксид лития Na 2 O оксид натрия K 2 O оксид калия Ca. O оксид кальция Sr. O оксид стронция Ba. O оксид бария Mg. O оксид магния Fe. O оксид железа (II) Cu. O оксид меди (II) Оксиды амфотерные Be. O оксид бериллия Zn. O оксид цинка Pb. O оксид свинца (II) Cr 2 O 3 оксид хрома (III) Fe 2 O 3 оксид железа (III) Cr 2 O 3 оксид хрома (III) несолеобразующие N 2 O оксид азота (I) NO оксид азота (II) CO оксид углерода (II), угарный газ Si. O оксид кремния (II) Кислотные (оксиды неметаллов, некоторых металлов в степенях окисления +5, +6 и +7) SO 2 оксид серы (IV) SO 3 оксид серы (VI) NO 2 оксид азота (IV) N 2 O 5 оксид азота (V) CO 2 углекислый газ оксид углерода (IV), P 2 O 5 оксид фосфора (V) Si. O 2 оксид кремния (IV) Cl 2 O 7 оксид хлора (VII)
 Назад Кислоты и кислотные остатки HF – фтороводородная HCl – хлороводородная, соляная HBr – бромоводородная HI – иодоводородная H 2 S – сероводородная HCH 3 COO – уксусная H 2 SO 3 – сернистая H 2 SO 4 – серная HNO 2 – азотистая HNO 3 – азотная H 2 CO 3 – угольная HPO 3 – метафосфорная H 3 PO 4 – фосфорная (ортофосфорная) H 2 Si. O 3 – кремниевая H 2 Cr. O 4 – хромовая H 2 Cr 2 O 7 – дихромовая HMn. O 4 – марганцовая HCl. O – хлорная F- – фторид Cl- – хлорид Br- – бромид I- – иодид S 2 - – сульфид CH 3 COO- – ацетат SO 32 - – сульфит SO 42 - – сульфат NO 2 - – нитрит NO 3 - – нитрат CO 32 - – карбонат HCO 3 - – гидрокарбонат PO 3 - – метафосфат PO 43 - – фосфат HPO 4 - – гидрофосфат H 2 PO 42 - – дигидрофосфат Si. O 32 - – силикат Cr. O 42 - – хромат Cr 2 O 72 - –дихромат Mn. O 4 - – перманганат Cl. O - – хлорат
Назад Кислоты и кислотные остатки HF – фтороводородная HCl – хлороводородная, соляная HBr – бромоводородная HI – иодоводородная H 2 S – сероводородная HCH 3 COO – уксусная H 2 SO 3 – сернистая H 2 SO 4 – серная HNO 2 – азотистая HNO 3 – азотная H 2 CO 3 – угольная HPO 3 – метафосфорная H 3 PO 4 – фосфорная (ортофосфорная) H 2 Si. O 3 – кремниевая H 2 Cr. O 4 – хромовая H 2 Cr 2 O 7 – дихромовая HMn. O 4 – марганцовая HCl. O – хлорная F- – фторид Cl- – хлорид Br- – бромид I- – иодид S 2 - – сульфид CH 3 COO- – ацетат SO 32 - – сульфит SO 42 - – сульфат NO 2 - – нитрит NO 3 - – нитрат CO 32 - – карбонат HCO 3 - – гидрокарбонат PO 3 - – метафосфат PO 43 - – фосфат HPO 4 - – гидрофосфат H 2 PO 42 - – дигидрофосфат Si. O 32 - – силикат Cr. O 42 - – хромат Cr 2 O 72 - –дихромат Mn. O 4 - – перманганат Cl. O - – хлорат
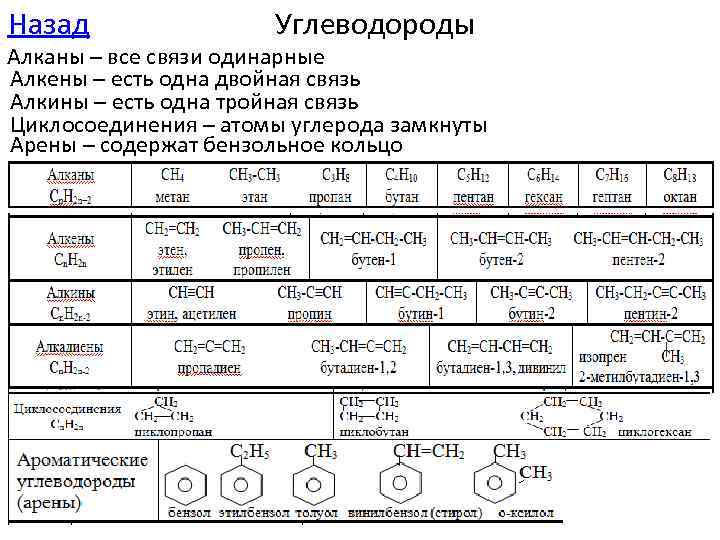 Назад Углеводороды Алканы – все связи одинарные Алкены – есть одна двойная связь Алкины – есть одна тройная связь Циклосоединения – атомы углерода замкнуты Арены – содержат бензольное кольцо
Назад Углеводороды Алканы – все связи одинарные Алкены – есть одна двойная связь Алкины – есть одна тройная связь Циклосоединения – атомы углерода замкнуты Арены – содержат бензольное кольцо


