ПОДГОТОВКА-К-ЕГЭ-А1.ppt
- Количество слайдов: 14
 ПОДГОТОВКА К ЕГЭ, А 1 Валишина Елена, репетитор по химии подготовка к ЕГЭ, А 1 1
ПОДГОТОВКА К ЕГЭ, А 1 Валишина Елена, репетитор по химии подготовка к ЕГЭ, А 1 1
 Теоретический материал СТРОЕНИЕ АТОМА Ядро( протоны p+ и нейтроны n 0) Энергетические уровни (оболочки) Электроны ( е) Планетарная модель (Резерфорд) ¡ Атом электронейтрален N(p+) = N(e-) ¡ Число протонов N(p+) равно заряду ядра (Z) и порядковому номеру элемента N(p+) = Z ¡ Сумма числа нейтронов N(n 0), и числа протонов называется атомной массой и обозначается буквой Аr Ar = Z + N(n 0). подготовка к ЕГЭ, А 1 2
Теоретический материал СТРОЕНИЕ АТОМА Ядро( протоны p+ и нейтроны n 0) Энергетические уровни (оболочки) Электроны ( е) Планетарная модель (Резерфорд) ¡ Атом электронейтрален N(p+) = N(e-) ¡ Число протонов N(p+) равно заряду ядра (Z) и порядковому номеру элемента N(p+) = Z ¡ Сумма числа нейтронов N(n 0), и числа протонов называется атомной массой и обозначается буквой Аr Ar = Z + N(n 0). подготовка к ЕГЭ, А 1 2
 Теоретический материал ИЗОТОПЫ ¡ Химический элемент - вид атомов (совокупность атомов) с одинаковым зарядом ядра (с одинаковым числом протонов в ядре). Изотоп - совокупность атомов одного элемента с одинаковым числом протонов в ядре, но разным числом нейтронов Обозначение отдельного атома или изотопа: (Э - символ элемента), например: 3517 Сl, 3717 Сl, 11 H, 21 H (дейтерий, D, тяжелая вода), 3 H(тритий, Т) 1 подготовка к ЕГЭ, А 1 3
Теоретический материал ИЗОТОПЫ ¡ Химический элемент - вид атомов (совокупность атомов) с одинаковым зарядом ядра (с одинаковым числом протонов в ядре). Изотоп - совокупность атомов одного элемента с одинаковым числом протонов в ядре, но разным числом нейтронов Обозначение отдельного атома или изотопа: (Э - символ элемента), например: 3517 Сl, 3717 Сl, 11 H, 21 H (дейтерий, D, тяжелая вода), 3 H(тритий, Т) 1 подготовка к ЕГЭ, А 1 3
 Теоретический материал АТОМНЫЕ ОРБИТАЛИ (АО) ¡ Атомная орбиталь - состояние электрона в атоме. Условное обозначение орбитали - . Каждой орбитали соответствует электронное облако. Электронное облако - часть пространства, в которой электрон можно обнаружить с вероятностью 90 (или более) процентов. Атомная орбиталь ≡ Электронное облако ¡ Электронная оболочка атома слоистая. Электронный слой образован электронными облаками одинакового размера. Орбитали одного слоя образуют электронный ("энергетический") уровень, их энергии одинаковы у атома водорода, но различаются у других атомов подготовка к ЕГЭ, А 1 4
Теоретический материал АТОМНЫЕ ОРБИТАЛИ (АО) ¡ Атомная орбиталь - состояние электрона в атоме. Условное обозначение орбитали - . Каждой орбитали соответствует электронное облако. Электронное облако - часть пространства, в которой электрон можно обнаружить с вероятностью 90 (или более) процентов. Атомная орбиталь ≡ Электронное облако ¡ Электронная оболочка атома слоистая. Электронный слой образован электронными облаками одинакового размера. Орбитали одного слоя образуют электронный ("энергетический") уровень, их энергии одинаковы у атома водорода, но различаются у других атомов подготовка к ЕГЭ, А 1 4
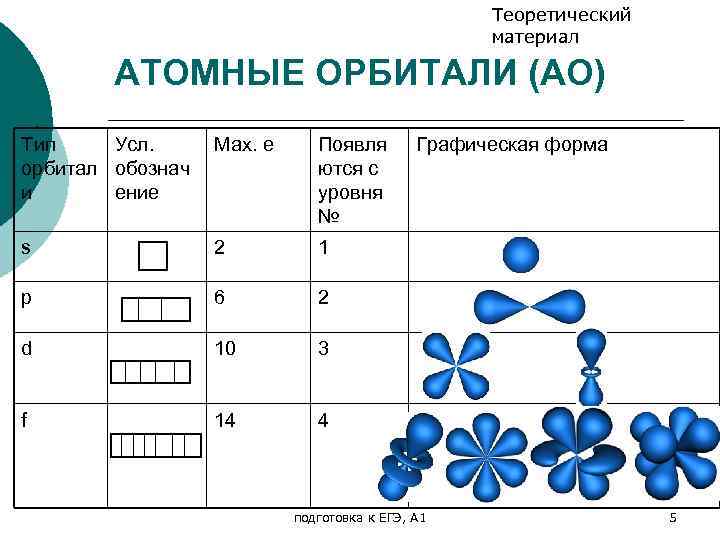 Теоретический материал АТОМНЫЕ ОРБИТАЛИ (АО) ¡ . Тип Усл. орбитал обознач и ение Мах. e Появля ются с уровня № s 2 1 p 6 2 d 10 3 f 14 Графическая форма 4 подготовка к ЕГЭ, А 1 5
Теоретический материал АТОМНЫЕ ОРБИТАЛИ (АО) ¡ . Тип Усл. орбитал обознач и ение Мах. e Появля ются с уровня № s 2 1 p 6 2 d 10 3 f 14 Графическая форма 4 подготовка к ЕГЭ, А 1 5
 Теоретический материал ПОРЯДОК ЗАПОЛНЕНИЯ АТОМНЫХ ОРБИТАЛЕЙ (АО) ¡ Порядок заполнения электронами орбиталей атома определяется тремя законами природы (формулировки даны упрощенно): 1. Принцип наименьшей энергии - электроны заполняют орбитали в порядке возрастания энергии орбиталей 1 s, 2 p, 3 s, 3 p, 4 s, 3 d, 4 p, 5 s, 4 d, 5 p, 6 s, 4 f, 5 d, 6 p, 7 s, 5 f, 6 d, 7 p. . . 2. Принцип Паули - на одной орбитали не может быть больше двух электронов. 3. Правило Хунда - в пределах подуровня электроны сначала заполняют свободные орбитали (по одному), и лишь после этого образуют электронные пары. подготовка к ЕГЭ, А 1 6
Теоретический материал ПОРЯДОК ЗАПОЛНЕНИЯ АТОМНЫХ ОРБИТАЛЕЙ (АО) ¡ Порядок заполнения электронами орбиталей атома определяется тремя законами природы (формулировки даны упрощенно): 1. Принцип наименьшей энергии - электроны заполняют орбитали в порядке возрастания энергии орбиталей 1 s, 2 p, 3 s, 3 p, 4 s, 3 d, 4 p, 5 s, 4 d, 5 p, 6 s, 4 f, 5 d, 6 p, 7 s, 5 f, 6 d, 7 p. . . 2. Принцип Паули - на одной орбитали не может быть больше двух электронов. 3. Правило Хунда - в пределах подуровня электроны сначала заполняют свободные орбитали (по одному), и лишь после этого образуют электронные пары. подготовка к ЕГЭ, А 1 6
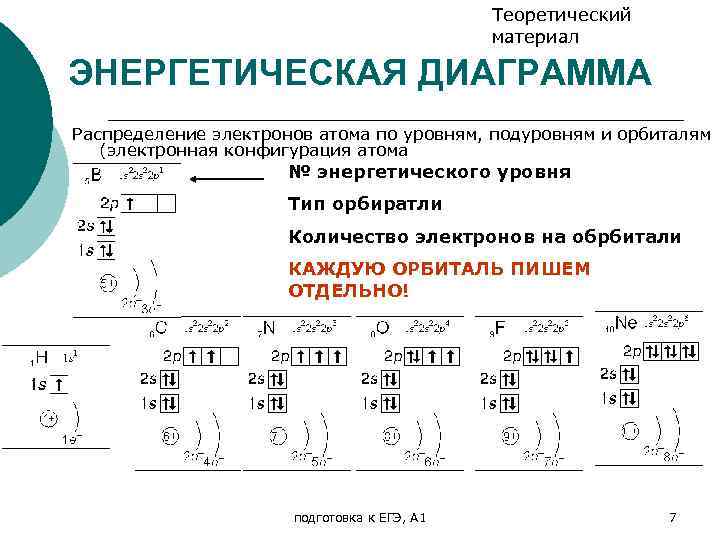 Теоретический материал ЭНЕРГЕТИЧЕСКАЯ ДИАГРАММА Распределение электронов атома по уровням, подуровням и орбиталям (электронная конфигурация атома № энергетического уровня Тип орбиратли Количество электронов на обрбитали КАЖДУЮ ОРБИТАЛЬ ПИШЕМ ОТДЕЛЬНО! подготовка к ЕГЭ, А 1 7
Теоретический материал ЭНЕРГЕТИЧЕСКАЯ ДИАГРАММА Распределение электронов атома по уровням, подуровням и орбиталям (электронная конфигурация атома № энергетического уровня Тип орбиратли Количество электронов на обрбитали КАЖДУЮ ОРБИТАЛЬ ПИШЕМ ОТДЕЛЬНО! подготовка к ЕГЭ, А 1 7
 Практический материал ВАРИАНТЫ ЗАДАНИЙ ¡Тест 1 ¡ 1. Число энергетических слоев и число электронов во внешнем энергетическом слое атомов селена равны соответственно ¡ 1)4, 6 2)3, 6 3)4, 7 4)3, 7 ¡ 2. Химическому элементу соответствует высший оксид состава R 20. Электронная конфигурация внешнего энергетического уровня атома этого элемента имеет вид ¡ 1) ns 2 2) ns 1 3) ns 2 nр1 4) ns 2 nр2 ¡ 3. Ядра атомов изотопов различаются числом ¡ 1) протонов 3) протонов и нейтронов ¡ 2) нейтронов 4) протонов и электронов ¡ 4. Сумма протонов и нейтронов в атоме 65 Zn равна ¡ 1) 30 2) 65 3) 35 4) 40 ¡ 5. Электронную формулу 1 s 22 р63 s 23 р64 s 2 имеет атом элемента ¡I) Ва 2) Мg 3) Са 4) Sr подготовка к ЕГЭ, А 1 8
Практический материал ВАРИАНТЫ ЗАДАНИЙ ¡Тест 1 ¡ 1. Число энергетических слоев и число электронов во внешнем энергетическом слое атомов селена равны соответственно ¡ 1)4, 6 2)3, 6 3)4, 7 4)3, 7 ¡ 2. Химическому элементу соответствует высший оксид состава R 20. Электронная конфигурация внешнего энергетического уровня атома этого элемента имеет вид ¡ 1) ns 2 2) ns 1 3) ns 2 nр1 4) ns 2 nр2 ¡ 3. Ядра атомов изотопов различаются числом ¡ 1) протонов 3) протонов и нейтронов ¡ 2) нейтронов 4) протонов и электронов ¡ 4. Сумма протонов и нейтронов в атоме 65 Zn равна ¡ 1) 30 2) 65 3) 35 4) 40 ¡ 5. Электронную формулу 1 s 22 р63 s 23 р64 s 2 имеет атом элемента ¡I) Ва 2) Мg 3) Са 4) Sr подготовка к ЕГЭ, А 1 8
 Практический материал ВАРИАНТЫ ЗАДАНИЙ ¡Тест 2 ¡ 1. Число энергетических слоев и число электронов во внешнем энергетическом слое атомов хрома равны соответственно ¡ 1) 4, 2 2) 4, 1 3) 4, 6 4) 4, 5 ¡ 2. Электронная формула 1 s 22 р63 s 23 р6 соответствует частице ¡ 1) Li+ 2) К 0 3) Сa 2+ 4) Nа+ ¡ 3. Сумма протонов, нейтронов и электронов в атоме 31 Р равна ¡ 1) 15 2) 16 3) 46 4) 31 ¡ 4. У атома фосфора число электронов на внешнем энергетическом уровне и заряд ядра равны соответственно ¡ 1) 5, 31 2) 5, 15 3) 3, 31 4) 3, 15 ¡ 5. Какую электронную конфигурацию имеет атом наиболее активного металла? ¡I)…. . 3 s 23 р1 2)…. . Зs 2 3)…. . Зs 1 4)…. . 3 s 23 р2 подготовка к ЕГЭ, А 1 9
Практический материал ВАРИАНТЫ ЗАДАНИЙ ¡Тест 2 ¡ 1. Число энергетических слоев и число электронов во внешнем энергетическом слое атомов хрома равны соответственно ¡ 1) 4, 2 2) 4, 1 3) 4, 6 4) 4, 5 ¡ 2. Электронная формула 1 s 22 р63 s 23 р6 соответствует частице ¡ 1) Li+ 2) К 0 3) Сa 2+ 4) Nа+ ¡ 3. Сумма протонов, нейтронов и электронов в атоме 31 Р равна ¡ 1) 15 2) 16 3) 46 4) 31 ¡ 4. У атома фосфора число электронов на внешнем энергетическом уровне и заряд ядра равны соответственно ¡ 1) 5, 31 2) 5, 15 3) 3, 31 4) 3, 15 ¡ 5. Какую электронную конфигурацию имеет атом наиболее активного металла? ¡I)…. . 3 s 23 р1 2)…. . Зs 2 3)…. . Зs 1 4)…. . 3 s 23 р2 подготовка к ЕГЭ, А 1 9
 Практический материал ВАРИАНТЫ ЗАДАНИЙ ¡Тест. З ¡ 1. Число энергетических слоев и число электронов во внешнем энергетическом слое атомов меди равны соответственно ¡ 1) 4, 2 2) 4, 1 3) 4, 9 4) 4, 10 ¡ 2. Химическому элементу соответствует высший оксид состава RО. Электронная конфигурация внешнего энергетического уровня атома этого элемента имеет вид ¡ 1) ns 2 nр1 2) ns 2 3) ns 2 nр3 4) ns 2 nр2 ¡ 3. Число электронов в атоме аргона равно числу электронов в ионе ¡ 1) S 2 - 2) А 13+ 3)Na+ 4) F¡ 4. Самым распространенным оксидом в земной коре является ¡ 1) оксид водорода 3) оксид кремния ¡ 2) оксид углерода (IV) 4) оксид алюминия ¡ 5. Число электронов на внешнем энергетическом уровне атома фосфора в возбужденном состоянии равно ¡ 1) 3 2) 5 3) 2 4) 4 подготовка к ЕГЭ, А 1 10
Практический материал ВАРИАНТЫ ЗАДАНИЙ ¡Тест. З ¡ 1. Число энергетических слоев и число электронов во внешнем энергетическом слое атомов меди равны соответственно ¡ 1) 4, 2 2) 4, 1 3) 4, 9 4) 4, 10 ¡ 2. Химическому элементу соответствует высший оксид состава RО. Электронная конфигурация внешнего энергетического уровня атома этого элемента имеет вид ¡ 1) ns 2 nр1 2) ns 2 3) ns 2 nр3 4) ns 2 nр2 ¡ 3. Число электронов в атоме аргона равно числу электронов в ионе ¡ 1) S 2 - 2) А 13+ 3)Na+ 4) F¡ 4. Самым распространенным оксидом в земной коре является ¡ 1) оксид водорода 3) оксид кремния ¡ 2) оксид углерода (IV) 4) оксид алюминия ¡ 5. Число электронов на внешнем энергетическом уровне атома фосфора в возбужденном состоянии равно ¡ 1) 3 2) 5 3) 2 4) 4 подготовка к ЕГЭ, А 1 10
 Практический материал ВАРИАНТЫ ЗАДАНИЙ ¡Тест 4 ¡ 1. Химическому элементу соответствует высший оксид R 02. Электронная конфигурация внешнего энергетического уровня атома этого элемента имеет вид ¡ 1)ns 2 nр1 2) ns 2 nр4 3) ns 2 nр3 4) ns 2 nр2 ¡ 2. Фосфид-иону соответствует электронная формула ¡ 1) 1 s 22 р63 s 23 р6 3) 1 s 22 р6 ¡ 2) 1 s 22 р63 s 23 р4 4) 1 s 22 р63 s 23 р2 ¡ 3. Сумма протонов и нейтронов в атоме 14 С равна ¡ 1) 14 2) 12 3) 13 4) 15 ¡ 4. У атома кальция число электронов на внешнем энергетическом уровне и заряд ядра равны соответственно ¡ 1) 4, 20 2) 2, 20 3) 4, 40 4) 2, 40 ¡ 5. Число электронов на внешнем энергетическом уровне атома алюминия в возбужденном состоянии равно ¡ 1) 2 2) 4 3) 3 4) 1 подготовка к ЕГЭ, А 1 11
Практический материал ВАРИАНТЫ ЗАДАНИЙ ¡Тест 4 ¡ 1. Химическому элементу соответствует высший оксид R 02. Электронная конфигурация внешнего энергетического уровня атома этого элемента имеет вид ¡ 1)ns 2 nр1 2) ns 2 nр4 3) ns 2 nр3 4) ns 2 nр2 ¡ 2. Фосфид-иону соответствует электронная формула ¡ 1) 1 s 22 р63 s 23 р6 3) 1 s 22 р6 ¡ 2) 1 s 22 р63 s 23 р4 4) 1 s 22 р63 s 23 р2 ¡ 3. Сумма протонов и нейтронов в атоме 14 С равна ¡ 1) 14 2) 12 3) 13 4) 15 ¡ 4. У атома кальция число электронов на внешнем энергетическом уровне и заряд ядра равны соответственно ¡ 1) 4, 20 2) 2, 20 3) 4, 40 4) 2, 40 ¡ 5. Число электронов на внешнем энергетическом уровне атома алюминия в возбужденном состоянии равно ¡ 1) 2 2) 4 3) 3 4) 1 подготовка к ЕГЭ, А 1 11
 Практический материал ВАРИАНТЫ ЗАДАНИЙ ¡Тест 5 ¡ 1. Число энергетических слоев и число электронов во внешнем энергетическом слое атомов железа равны соответственно ¡ 1) 4, 2 2) 4, 8 3) 4, 6 4) 4, 1 ¡ 2. На третьем энергетическом уровне имеется по 8 электронов у каждой из частиц: ¡ 1) Nа+ и Аг 2) S 2 - и Аг 3) F- и Nе 4) Мg 2+ + и S ¡ 3. Сумма протонов, нейтронов и электронов в атоме 12 С равна ¡ 1) 14 2) 18 3) 6 4) 12 ¡ 4. Химический элемент, формула высшего оксида которого R 2 О 7 имеет электронную конфигурацию атома: ¡ 1) 1 s 22 р63 s 1 3) 1 s 22 р63 s 23 р64 s 1 ¡ 2) 1 s 22 р63 s 23 р5 4) 1 s 22 s 2 ¡ 5. Самым распространенным элементом в органических соединениях является ¡ 1) азот 2) фосфор 3) кислород 4) углерод подготовка к ЕГЭ, А 1 Ответы: Тест№ 1: 1 -1, 2 -2, 3 -2, 4 -2, 5 -3 Тест№ 2: 1 -3, 2 -3, 3 -3, 4 -2, 5 -3 Тест№ 3: 1 -3, 2 -2, 3 -1, 4 -3, 5 -2 Тест№ 4: 1 -1, 2 -1, 3 -1, 4 -3, 5 -2 Тест№ 5: 1 -3, 2 -2, 3 -4, 4 -2, 5 -4 12
Практический материал ВАРИАНТЫ ЗАДАНИЙ ¡Тест 5 ¡ 1. Число энергетических слоев и число электронов во внешнем энергетическом слое атомов железа равны соответственно ¡ 1) 4, 2 2) 4, 8 3) 4, 6 4) 4, 1 ¡ 2. На третьем энергетическом уровне имеется по 8 электронов у каждой из частиц: ¡ 1) Nа+ и Аг 2) S 2 - и Аг 3) F- и Nе 4) Мg 2+ + и S ¡ 3. Сумма протонов, нейтронов и электронов в атоме 12 С равна ¡ 1) 14 2) 18 3) 6 4) 12 ¡ 4. Химический элемент, формула высшего оксида которого R 2 О 7 имеет электронную конфигурацию атома: ¡ 1) 1 s 22 р63 s 1 3) 1 s 22 р63 s 23 р64 s 1 ¡ 2) 1 s 22 р63 s 23 р5 4) 1 s 22 s 2 ¡ 5. Самым распространенным элементом в органических соединениях является ¡ 1) азот 2) фосфор 3) кислород 4) углерод подготовка к ЕГЭ, А 1 Ответы: Тест№ 1: 1 -1, 2 -2, 3 -2, 4 -2, 5 -3 Тест№ 2: 1 -3, 2 -3, 3 -3, 4 -2, 5 -3 Тест№ 3: 1 -3, 2 -2, 3 -1, 4 -3, 5 -2 Тест№ 4: 1 -1, 2 -1, 3 -1, 4 -3, 5 -2 Тест№ 5: 1 -3, 2 -2, 3 -4, 4 -2, 5 -4 12
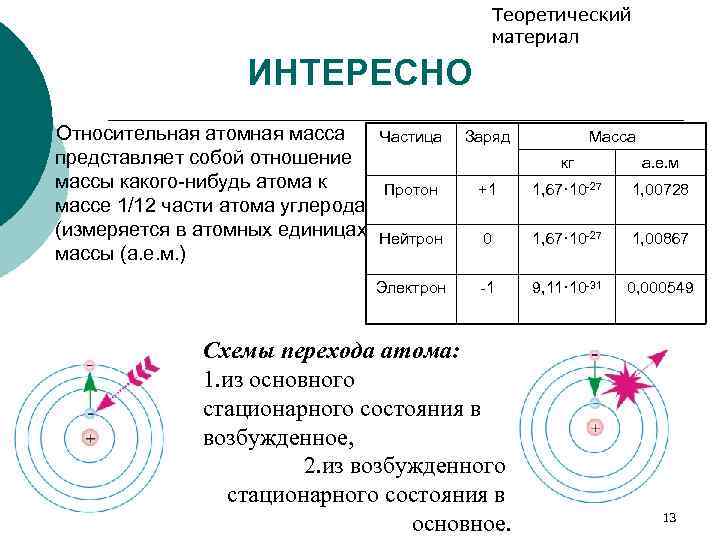 Теоретический материал ИНТЕРЕСНО Относительная атомная масса представляет собой отношение массы какого-нибудь атома к массе 1/12 части атома углерода (измеряется в атомных единицах массы (а. е. м. ) Частица Заряд Масса кг а. е. м Протон +1 1, 67· 10 -27 1, 00728 Нейтрон 0 1, 67· 10 -27 1, 00867 Электрон -1 9, 11· 10 -31 0, 000549 Схемы перехода атома: 1. из основного стационарного состояния в возбужденное, 2. из возбужденного стационарного состояния в подготовка к ЕГЭ, А 1 основное. 13
Теоретический материал ИНТЕРЕСНО Относительная атомная масса представляет собой отношение массы какого-нибудь атома к массе 1/12 части атома углерода (измеряется в атомных единицах массы (а. е. м. ) Частица Заряд Масса кг а. е. м Протон +1 1, 67· 10 -27 1, 00728 Нейтрон 0 1, 67· 10 -27 1, 00867 Электрон -1 9, 11· 10 -31 0, 000549 Схемы перехода атома: 1. из основного стационарного состояния в возбужденное, 2. из возбужденного стационарного состояния в подготовка к ЕГЭ, А 1 основное. 13
 подготовка к ЕГЭ, А 1 14
подготовка к ЕГЭ, А 1 14


