 Подготовка к аттестации. ГОУ гимназия № 1587 ЮАО, Иванова Т. Ю.
Подготовка к аттестации. ГОУ гимназия № 1587 ЮАО, Иванова Т. Ю.
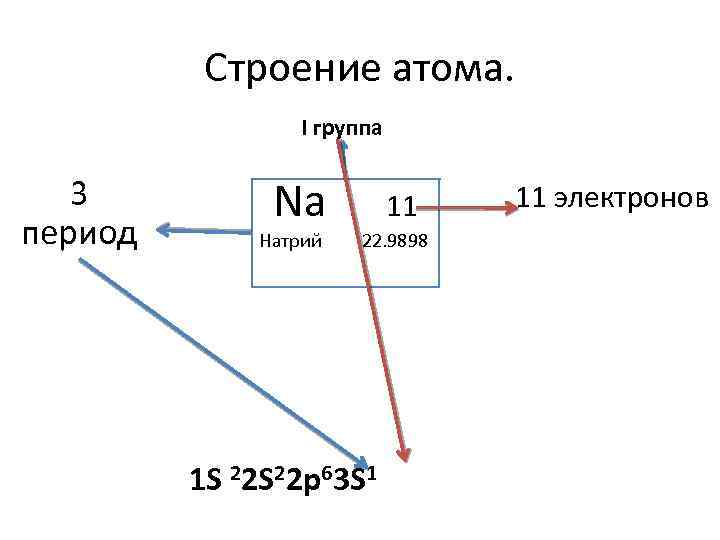 Строение атома. I группа 3 период Na 11 Натрий 22. 9898 1 S 22 p 63 S 1 11 электронов
Строение атома. I группа 3 период Na 11 Натрий 22. 9898 1 S 22 p 63 S 1 11 электронов
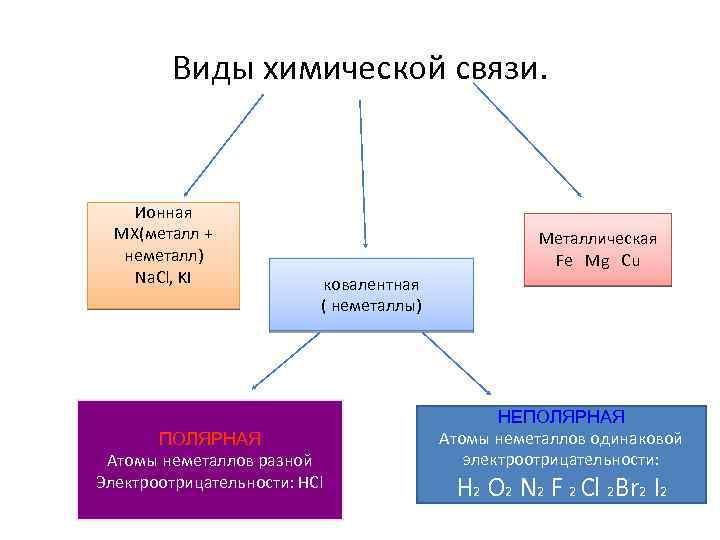 Виды химической связи. Ионная МХ(металл + неметалл) Na. Cl, KI Металлическая Fe Mg Cu ковалентная ( неметаллы) ПОЛЯРНАЯ Атомы неметаллов разной Электроотрицательности: НСl НЕПОЛЯРНАЯ Атомы неметаллов одинаковой электроотрицательности: Н 2 O 2 N 2 F 2 Cl 2 Br 2 I 2
Виды химической связи. Ионная МХ(металл + неметалл) Na. Cl, KI Металлическая Fe Mg Cu ковалентная ( неметаллы) ПОЛЯРНАЯ Атомы неметаллов разной Электроотрицательности: НСl НЕПОЛЯРНАЯ Атомы неметаллов одинаковой электроотрицательности: Н 2 O 2 N 2 F 2 Cl 2 Br 2 I 2
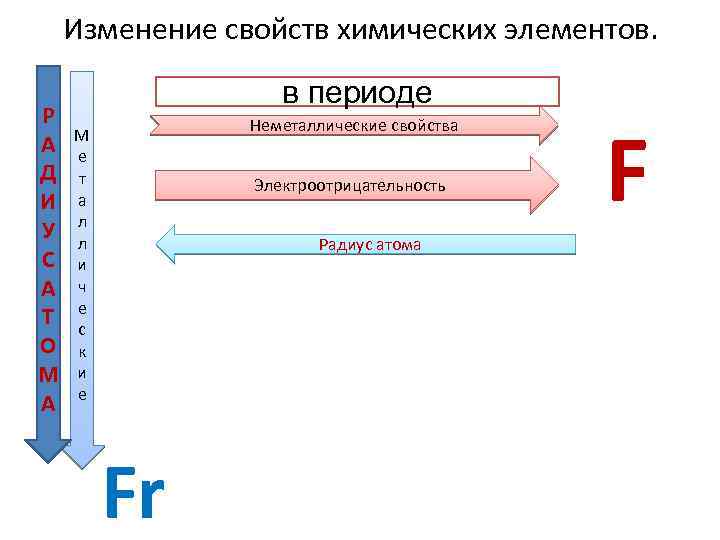 Изменение свойств химических элементов. Р А Д И У С А Т О М А в периоде Неметаллические свойства М е т а л л и ч е с к и е Электроотрицательность Радиус атома Fr F
Изменение свойств химических элементов. Р А Д И У С А Т О М А в периоде Неметаллические свойства М е т а л л и ч е с к и е Электроотрицательность Радиус атома Fr F
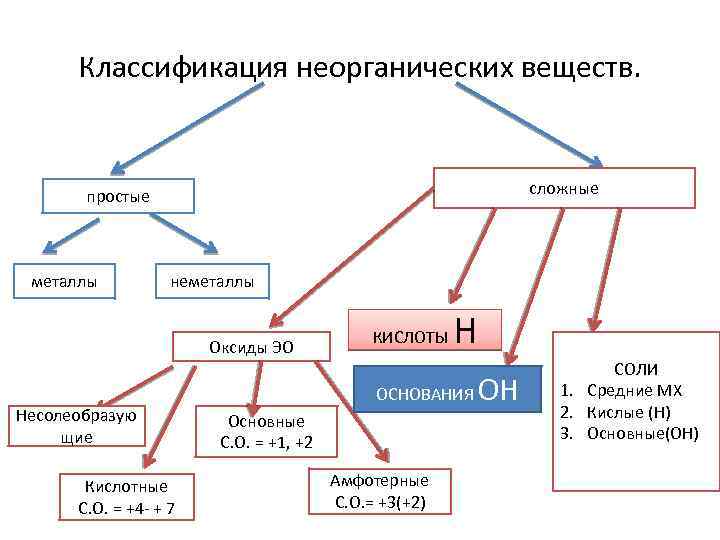 Классификация неорганических веществ. сложные простые металлы неметаллы Оксиды ЭО Несолеобразую щие Кислотные С. О. = +4 - + 7 КИСЛОТЫ Н ОСНОВАНИЯ Основные С. О. = +1, +2 Амфотерные С. О. = +3(+2) ОН СОЛИ 1. Средние МХ 2. Кислые (Н) 3. Основные(ОН)
Классификация неорганических веществ. сложные простые металлы неметаллы Оксиды ЭО Несолеобразую щие Кислотные С. О. = +4 - + 7 КИСЛОТЫ Н ОСНОВАНИЯ Основные С. О. = +1, +2 Амфотерные С. О. = +3(+2) ОН СОЛИ 1. Средние МХ 2. Кислые (Н) 3. Основные(ОН)
 Типы химических реакций. 1. Соединение • 2 Н 2 + О 2 2 H 2 O – ОВР • Mg. O + H 2 O Mg(OH)2 2. Разложение. • 2 Hg. O Hg + O 2 – ОВР • Cu(OH)2 Cu. O + H 2 O 3. Замещение. 2 НCl + Zn Zn. Cl 2 +H 2 – ОВР Cu. O +H 2 Cu + H 2 O- ОВР 4. Обмен. НCl + Na. OH Na. Cl +H 2 O- нейтрализация
Типы химических реакций. 1. Соединение • 2 Н 2 + О 2 2 H 2 O – ОВР • Mg. O + H 2 O Mg(OH)2 2. Разложение. • 2 Hg. O Hg + O 2 – ОВР • Cu(OH)2 Cu. O + H 2 O 3. Замещение. 2 НCl + Zn Zn. Cl 2 +H 2 – ОВР Cu. O +H 2 Cu + H 2 O- ОВР 4. Обмен. НCl + Na. OH Na. Cl +H 2 O- нейтрализация
 Реакции ионного обмена. Электролиты. кислоты • Сильные соли основания • Растворимые в воде • Na. Cl • Растворимые в воде • Na. OH Слабые кислоты: H 2 CO 3; H 2 S; H 2 Si. O 3; HF Н 2 СО 3 H 2 O + CO 2
Реакции ионного обмена. Электролиты. кислоты • Сильные соли основания • Растворимые в воде • Na. Cl • Растворимые в воде • Na. OH Слабые кислоты: H 2 CO 3; H 2 S; H 2 Si. O 3; HF Н 2 СО 3 H 2 O + CO 2
 Условия протекания реакций ионного обмена до конца. 1. Образование воды • Na. OH + HCl H 2 O + Na. Cl 2. Образование осадка • 2 KOH + Cu. Cl 2 Cu(OH)2 + 2 KCl 3. Выделение газа • Na 2 СО 3 + 2 HCl H 2 O + CO 2 + 2 Na. Cl
Условия протекания реакций ионного обмена до конца. 1. Образование воды • Na. OH + HCl H 2 O + Na. Cl 2. Образование осадка • 2 KOH + Cu. Cl 2 Cu(OH)2 + 2 KCl 3. Выделение газа • Na 2 СО 3 + 2 HCl H 2 O + CO 2 + 2 Na. Cl