ПУТИ ПРОГРАММИРУЕМОЙ КЛЕТОЧНОЙ ГИБЕЛИ.ppt
- Количество слайдов: 21
 Подготовила студентка 4 курса Ф-та естествознания Втюрина Д. Л.
Подготовила студентка 4 курса Ф-та естествознания Втюрина Д. Л.
 Это механизм, широко распространенный в различных царствах живого, включая прокариот, который обеспечивает контроль за клеточной популяцией в многоклеточном организме — уравновешивание эффекта пролиферации и элиминации клеток. В 1966 г. в журнале «Science» появилась статья Р. Сандерса, в которой автор высказал предположение, что старение и гибель клеток в эмбрио- и морфогенезе — результат активации особой генетической программы, запускаемой специфическими внутриклеточными и внешними сигналами. В последние годы выделяют несколько типов ПКГ: апоптоз, аутофагическую гибель и программированный некроз (D. Ogier, 2003). В свою очередь, апоптоз может быть подразделен на апоптоз одноядерных клеток и митотическую катастрофу. Описано не менее 5 форм апоптоза как континиума с программируемым некрозом : апоптоз, автохизис, анойкис, параптоз, митапаптоз. Относительно терминологии комитет по спецификации клеточной гибели рекомендует считать некрозом погибшую клетку, независимо от пути развития гибели.
Это механизм, широко распространенный в различных царствах живого, включая прокариот, который обеспечивает контроль за клеточной популяцией в многоклеточном организме — уравновешивание эффекта пролиферации и элиминации клеток. В 1966 г. в журнале «Science» появилась статья Р. Сандерса, в которой автор высказал предположение, что старение и гибель клеток в эмбрио- и морфогенезе — результат активации особой генетической программы, запускаемой специфическими внутриклеточными и внешними сигналами. В последние годы выделяют несколько типов ПКГ: апоптоз, аутофагическую гибель и программированный некроз (D. Ogier, 2003). В свою очередь, апоптоз может быть подразделен на апоптоз одноядерных клеток и митотическую катастрофу. Описано не менее 5 форм апоптоза как континиума с программируемым некрозом : апоптоз, автохизис, анойкис, параптоз, митапаптоз. Относительно терминологии комитет по спецификации клеточной гибели рекомендует считать некрозом погибшую клетку, независимо от пути развития гибели.
 Эволюционно апоптоз возник у прокариот как механизм противовирусной защиты и был закреплен у одноклеточных эукариот. Развитие апоптоза шло параллельно с развитием эукариотических клеток. Механизм современного апоптоза в многоклеточном организме является видоизмененной в эволюции реакции предшественников митохондрий на воздействие факторов, способных вызывать повреждения клетки-хозяина и стремление эндосимбионта выйти из симбиотических отношений.
Эволюционно апоптоз возник у прокариот как механизм противовирусной защиты и был закреплен у одноклеточных эукариот. Развитие апоптоза шло параллельно с развитием эукариотических клеток. Механизм современного апоптоза в многоклеточном организме является видоизмененной в эволюции реакции предшественников митохондрий на воздействие факторов, способных вызывать повреждения клетки-хозяина и стремление эндосимбионта выйти из симбиотических отношений.
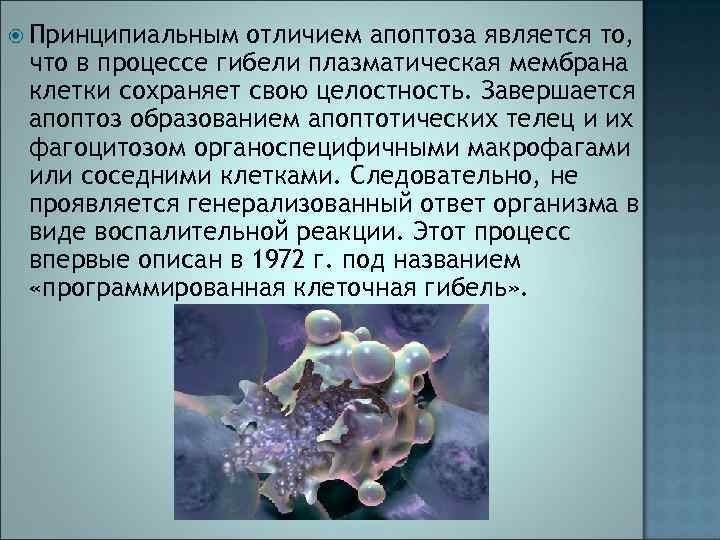 Принципиальным отличием апоптоза является то, что в процессе гибели плазматическая мембрана клетки сохраняет свою целостность. Завершается апоптоз образованием апоптотических телец и их фагоцитозом органоспецифичными макрофагами или соседними клетками. Следовательно, не проявляется генерализованный ответ организма в виде воспалительной реакции. Этот процесс впервые описан в 1972 г. под названием «программированная клеточная гибель» .
Принципиальным отличием апоптоза является то, что в процессе гибели плазматическая мембрана клетки сохраняет свою целостность. Завершается апоптоз образованием апоптотических телец и их фагоцитозом органоспецифичными макрофагами или соседними клетками. Следовательно, не проявляется генерализованный ответ организма в виде воспалительной реакции. Этот процесс впервые описан в 1972 г. под названием «программированная клеточная гибель» .
 Апоптоз появляется в течение эмбрионального развития, особенно в комплексе органов, где субпопуляция клеток избирательно уничтожается. Очень демонстративны в этом отношении организмы, жизненный цикл которых происходит с метаморфозом. У бабочки на стадии куколки происходит апоптоз практически 90% клеток гусеницы, и возникают новые ткани и органы. Нарушение апоптоза в эмбриогенезе может приводить к внутриутробной гибели плода, врожденным уродствам или различным заболеваниям, в том числе злокачественным.
Апоптоз появляется в течение эмбрионального развития, особенно в комплексе органов, где субпопуляция клеток избирательно уничтожается. Очень демонстративны в этом отношении организмы, жизненный цикл которых происходит с метаморфозом. У бабочки на стадии куколки происходит апоптоз практически 90% клеток гусеницы, и возникают новые ткани и органы. Нарушение апоптоза в эмбриогенезе может приводить к внутриутробной гибели плода, врожденным уродствам или различным заболеваниям, в том числе злокачественным.
 При повышении клеточной выживаемости, т. е. ингибировании процессов апоптоза, развиваются рак, аутоиммунные заболевания, нейропролиферативные заболевания (шизофрения и аутизм и др. ). В свою очередь, понижение клеточной выживаемости, следовательно, активация апоптоза, играет роль в патогенезе СПИДа, нейродегенеративных заболеваний (болезни Альцгеймера и Паркинсона), ишемических состояний (инсульт и инфаркт), диабета.
При повышении клеточной выживаемости, т. е. ингибировании процессов апоптоза, развиваются рак, аутоиммунные заболевания, нейропролиферативные заболевания (шизофрения и аутизм и др. ). В свою очередь, понижение клеточной выживаемости, следовательно, активация апоптоза, играет роль в патогенезе СПИДа, нейродегенеративных заболеваний (болезни Альцгеймера и Паркинсона), ишемических состояний (инсульт и инфаркт), диабета.
 Апоптоз обеспечивает гормон-зависимую инволюцию органов у взрослых организмов. Проблема гормональной регуляции апоптоза особенно хорошо изложена в отношении юве-нильного гормона насекомых, гормоне щитовидной железы — тироксине. Во взрослом организме биологическая роль апоптоза сводится к регулированию численности популяции и к элиминации клеток, вредных для организма — мутантных или пораженных вирусом. Другая важная функция апоптоза — удаление клеток-инвалидов и клеток-диссидентов с серьезными нарушениями структуры или функции генетического аппарата, гибели отдельных клеток в опухолях. Существование программы клеточной гибели может быть эффективно использовано в медицине. В частности, стимуляция апоптозной системы — одно из направлений противораковой терапии. С другой стороны, избыточный апоптоз может сам по себе быть причиной гибели клеток иммунной системы, вызванных действием цитотоксических Т-клеток, например при отторжении трансплантата.
Апоптоз обеспечивает гормон-зависимую инволюцию органов у взрослых организмов. Проблема гормональной регуляции апоптоза особенно хорошо изложена в отношении юве-нильного гормона насекомых, гормоне щитовидной железы — тироксине. Во взрослом организме биологическая роль апоптоза сводится к регулированию численности популяции и к элиминации клеток, вредных для организма — мутантных или пораженных вирусом. Другая важная функция апоптоза — удаление клеток-инвалидов и клеток-диссидентов с серьезными нарушениями структуры или функции генетического аппарата, гибели отдельных клеток в опухолях. Существование программы клеточной гибели может быть эффективно использовано в медицине. В частности, стимуляция апоптозной системы — одно из направлений противораковой терапии. С другой стороны, избыточный апоптоз может сам по себе быть причиной гибели клеток иммунной системы, вызванных действием цитотоксических Т-клеток, например при отторжении трансплантата.
 Последние исследования значительно расширили представления об аутофагии как о пути ПКГ, регулирующем рост, гомеостаз, развитие организма в норме и в патологических процессах, молекулярные механизмы которой являются эволюционно консервативными. Аутофагия — это процесс деградации органелл и цитоплазматического материала, который происходит при участии внутриклеточных специализированных мембранных структур — аутофагосом. Аутофагосомы — двухмембранные образования, внутри которых помещается клеточный материал (органеллы или часть цитозоля), подлежащий разрушению.
Последние исследования значительно расширили представления об аутофагии как о пути ПКГ, регулирующем рост, гомеостаз, развитие организма в норме и в патологических процессах, молекулярные механизмы которой являются эволюционно консервативными. Аутофагия — это процесс деградации органелл и цитоплазматического материала, который происходит при участии внутриклеточных специализированных мембранных структур — аутофагосом. Аутофагосомы — двухмембранные образования, внутри которых помещается клеточный материал (органеллы или часть цитозоля), подлежащий разрушению.
 При нехватке питательных соединений в процессе аутофагии начинается утилизация части своих цитозольных белков и органелл как альтернативный источник питания. Нарушения процессов аутофагии вызывают некоторые онкологические, нейродегенеративные заболевания, болезни печени. В условиях физиологической нормы самый высокий уровень аутофагии выявлен в клетках Лейдига яичек крысы. В отличие от апоптоза, который может запускаться в разных фазах клеточного цикла, в том числе и собственно в митозе в форме митотической катастрофы, аутофагическая гибель развивается преимущественно в непролиферирующих клетках (Gg-фаза и терминальная дифференцировка). Аутофагия является альтернативным путем ПКГ в случае, если программа апоптоза не способна реализоваться, но при этом программа аутофагии реализуется через механизм апоптоза. В свою очередь, ингибирование аутофагии вызывает апоптоз.
При нехватке питательных соединений в процессе аутофагии начинается утилизация части своих цитозольных белков и органелл как альтернативный источник питания. Нарушения процессов аутофагии вызывают некоторые онкологические, нейродегенеративные заболевания, болезни печени. В условиях физиологической нормы самый высокий уровень аутофагии выявлен в клетках Лейдига яичек крысы. В отличие от апоптоза, который может запускаться в разных фазах клеточного цикла, в том числе и собственно в митозе в форме митотической катастрофы, аутофагическая гибель развивается преимущественно в непролиферирующих клетках (Gg-фаза и терминальная дифференцировка). Аутофагия является альтернативным путем ПКГ в случае, если программа апоптоза не способна реализоваться, но при этом программа аутофагии реализуется через механизм апоптоза. В свою очередь, ингибирование аутофагии вызывает апоптоз.
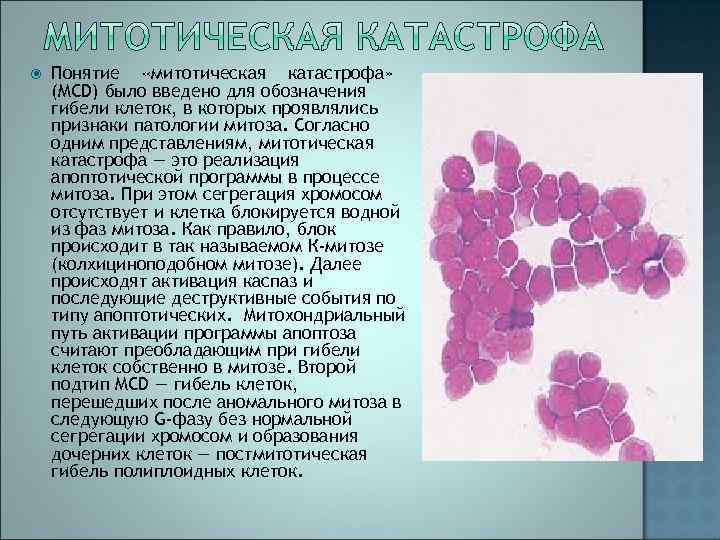 Понятие «митотическая катастрофа» (MCD) было введено для обозначения гибели клеток, в которых проявлялись признаки патологии митоза. Согласно одним представлениям, митотическая катастрофа — это реализация апоптотической программы в процессе митоза. При этом сегрегация хромосом отсутствует и клетка блокируется водной из фаз митоза. Как правило, блок происходит в так называемом К-митозе (колхициноподобном митозе). Далее происходят активация каспаз и последующие деструктивные события по типу апоптотических. Митохондриальный путь активации программы апоптоза считают преобладающим при гибели клеток собственно в митозе. Второй подтип MCD — гибель клеток, перешедших после аномального митоза в следующую G-фазу без нормальной сегрегации хромосом и образования дочерних клеток — постмитотическая гибель полиплоидных клеток.
Понятие «митотическая катастрофа» (MCD) было введено для обозначения гибели клеток, в которых проявлялись признаки патологии митоза. Согласно одним представлениям, митотическая катастрофа — это реализация апоптотической программы в процессе митоза. При этом сегрегация хромосом отсутствует и клетка блокируется водной из фаз митоза. Как правило, блок происходит в так называемом К-митозе (колхициноподобном митозе). Далее происходят активация каспаз и последующие деструктивные события по типу апоптотических. Митохондриальный путь активации программы апоптоза считают преобладающим при гибели клеток собственно в митозе. Второй подтип MCD — гибель клеток, перешедших после аномального митоза в следующую G-фазу без нормальной сегрегации хромосом и образования дочерних клеток — постмитотическая гибель полиплоидных клеток.
 Митотическая катастрофа принципиально отличается от апоптоза одноядерных клеток и аутофагической гибели тем, что нарушение ее программы может существенно повлиять на хромосомный состав клеток. Если в тетраплоидной клетке, возникшей в результате нарушения сегрегации хромосом, механизмы, ведущие к апоптозу или действующие в пункте проверки G-фазы, неактивны, то такая клетка может пройти очередной клеточный цикл и митоз. Как известно, деление полиплоидных клеток часто сопровождается многополюсностью веретена, в результате чего после сегрегации хромосом могут возникать анеуплоидные клетки. Анеуплоидия может вести, в свою очередь, к отсутствию пунктов контроля пролиферации и нарушению механизмов гибели клеток. Клоны потомков таких клеток могут служить основой для трансформации клеток и роста опухолей. Обнаружено, что если сестринские "клетки, образовавшиеся в результате многополюсного митоза и являющиеся анеуплоидными, подвергнуть апоптотическому воздействию, то погибает лишь часть таких клеток. Другие сестринские клетки остаются жизнеспособными, правда, неясно, как долго эти клетки продолжают жить.
Митотическая катастрофа принципиально отличается от апоптоза одноядерных клеток и аутофагической гибели тем, что нарушение ее программы может существенно повлиять на хромосомный состав клеток. Если в тетраплоидной клетке, возникшей в результате нарушения сегрегации хромосом, механизмы, ведущие к апоптозу или действующие в пункте проверки G-фазы, неактивны, то такая клетка может пройти очередной клеточный цикл и митоз. Как известно, деление полиплоидных клеток часто сопровождается многополюсностью веретена, в результате чего после сегрегации хромосом могут возникать анеуплоидные клетки. Анеуплоидия может вести, в свою очередь, к отсутствию пунктов контроля пролиферации и нарушению механизмов гибели клеток. Клоны потомков таких клеток могут служить основой для трансформации клеток и роста опухолей. Обнаружено, что если сестринские "клетки, образовавшиеся в результате многополюсного митоза и являющиеся анеуплоидными, подвергнуть апоптотическому воздействию, то погибает лишь часть таких клеток. Другие сестринские клетки остаются жизнеспособными, правда, неясно, как долго эти клетки продолжают жить.
 Понятие (ПН) сформировалось на основании данных о существовании сигнального пути инициации некроза в ответ на связывание рецепторов с молекулами TNF, на фоне подавления апоптоза. Если у клеток с поврежденной ДНК нарушены механизмы апоптоза, они погибают путем ПН. Это приводит к массивному выбросу индукторов воспаления и к миграции иммунных клеток к очагу поражения. В таких условиях клетки проявляют «некротический» фенотип с признаками частичного хроматолизиса. ПН представляет собой нормальные физиологические процессы, которые становятся деструктивными при неблагоприятных условиях. ПКГ путем ПН снижает риск передачи дочерним клеткам мутаций и способствует активации иммунного ответа ПН, который может запускаться в разных фазах клеточного цикла, в том числе и собственно в митозе в форме митотической катастрофы.
Понятие (ПН) сформировалось на основании данных о существовании сигнального пути инициации некроза в ответ на связывание рецепторов с молекулами TNF, на фоне подавления апоптоза. Если у клеток с поврежденной ДНК нарушены механизмы апоптоза, они погибают путем ПН. Это приводит к массивному выбросу индукторов воспаления и к миграции иммунных клеток к очагу поражения. В таких условиях клетки проявляют «некротический» фенотип с признаками частичного хроматолизиса. ПН представляет собой нормальные физиологические процессы, которые становятся деструктивными при неблагоприятных условиях. ПКГ путем ПН снижает риск передачи дочерним клеткам мутаций и способствует активации иммунного ответа ПН, который может запускаться в разных фазах клеточного цикла, в том числе и собственно в митозе в форме митотической катастрофы.
 В эмбриональный период вольфовы протоки в процессе развития особей женского пола и мюллеровы каналы у особей мужского пола вначале развиваются, а затем подвергаются ПН. Эти процессы, подобно всем другим онтогенетическим событиям, находятся под контролем генов. Также специфическим примером реализации программы ПН в ходе нормального развития организма служит развитие конечностей у птиц (отделение большой берцовой кости от малой и лучевой от локтевой, некроз межпальцевых участков). Для клеток, инфицированных вирусом vaccinia virus, ПН может быть не только вариантом гибели в условиях подавления апоптоза, но и выполнять функцию усиления иммунных реакций в ответ на инфицирование микроорганизмами. Недавние исследования молекулярного механизма ПН доказали, что механизм некротической клеточной гибели эволюционно высококонсервативен и почти одинаков от нематоды до человека. Однако в отличие от механизмов апоптоза механизмы ПН не эволюционировали специфическим образом.
В эмбриональный период вольфовы протоки в процессе развития особей женского пола и мюллеровы каналы у особей мужского пола вначале развиваются, а затем подвергаются ПН. Эти процессы, подобно всем другим онтогенетическим событиям, находятся под контролем генов. Также специфическим примером реализации программы ПН в ходе нормального развития организма служит развитие конечностей у птиц (отделение большой берцовой кости от малой и лучевой от локтевой, некроз межпальцевых участков). Для клеток, инфицированных вирусом vaccinia virus, ПН может быть не только вариантом гибели в условиях подавления апоптоза, но и выполнять функцию усиления иммунных реакций в ответ на инфицирование микроорганизмами. Недавние исследования молекулярного механизма ПН доказали, что механизм некротической клеточной гибели эволюционно высококонсервативен и почти одинаков от нематоды до человека. Однако в отличие от механизмов апоптоза механизмы ПН не эволюционировали специфическим образом.
 Запуск ПКГ может осуществляться как специфическимии цитокинами, гормонами, так и неспецифическими – радиацией, гипертермией, токсичными агентами, оксидантами, излучениями, повреждением мембран, потерей контакта с внеклеточным матриксом, бактериальными токсинами и др. Их влияние на клетки неоднозначно и тканеспецифично: для одних они выступают индуктором, для других – ингибитором.
Запуск ПКГ может осуществляться как специфическимии цитокинами, гормонами, так и неспецифическими – радиацией, гипертермией, токсичными агентами, оксидантами, излучениями, повреждением мембран, потерей контакта с внеклеточным матриксом, бактериальными токсинами и др. Их влияние на клетки неоднозначно и тканеспецифично: для одних они выступают индуктором, для других – ингибитором.
 Индукторами апоптоза считаются гены. К ПН приводят гипертермия, ингибирование фосфорилирования, гликолиза, цикла Кребса, гипоксия, повреждения. Аутофагию запускают отсутствие факторов роста, питательных веществ, наличие поврежденных органелл, гипоксия, бактериальное заражение. Причиной MCD считают нарушение процессов контроля в клетках, повреждения ДНК, нарушения сборки веретена.
Индукторами апоптоза считаются гены. К ПН приводят гипертермия, ингибирование фосфорилирования, гликолиза, цикла Кребса, гипоксия, повреждения. Аутофагию запускают отсутствие факторов роста, питательных веществ, наличие поврежденных органелл, гипоксия, бактериальное заражение. Причиной MCD считают нарушение процессов контроля в клетках, повреждения ДНК, нарушения сборки веретена.
 При аутофагической гибели деятельность аутофагосом и лизосом ведет к тому, что в клетке перевариваются все мембранные органеллы. Апоптоз определяется в единичных или в группах клеток, не сопровождается воспалительной реакцией и протекает в несколько этапов – сигналинг, трансляция сигнала, эффекторная стадия. Морфологические признаки ПН – набухание клеток и мембранных органелл, неспецифическая компактизация и неупорядоченная фрагментация хроматина, денатурация белков, вакуолизация, нарушение мембраны и выход содержимого клеток во внеклеточное пространство. Признаки MCD - отсутствие сегрегации хромосом, конденсация и фрагментация хроматина, клетка блокируется в одной из фаз митоза, нарушается организация веретена и метафазной пластинки.
При аутофагической гибели деятельность аутофагосом и лизосом ведет к тому, что в клетке перевариваются все мембранные органеллы. Апоптоз определяется в единичных или в группах клеток, не сопровождается воспалительной реакцией и протекает в несколько этапов – сигналинг, трансляция сигнала, эффекторная стадия. Морфологические признаки ПН – набухание клеток и мембранных органелл, неспецифическая компактизация и неупорядоченная фрагментация хроматина, денатурация белков, вакуолизация, нарушение мембраны и выход содержимого клеток во внеклеточное пространство. Признаки MCD - отсутствие сегрегации хромосом, конденсация и фрагментация хроматина, клетка блокируется в одной из фаз митоза, нарушается организация веретена и метафазной пластинки.
 Цитотоксические Т-лимфоциты киллеры могут вызвать апоптоз у инфицированных клеток с помощью белка перфорина и гранзима. Полимеризуясь, перфорин образует в цитоплазматической мембране клетки-мишени трансмембранные каналы, по которым внутрь клетки поступают гранзимы(фрагментины) - смесь сериновых протеаз. Существенным компонентом этой смеси является гранзим В – протеолитический фермент, превращающий прокаспазу-3 в активную каспазу-3 с дальнейшей реализацией апоптоза.
Цитотоксические Т-лимфоциты киллеры могут вызвать апоптоз у инфицированных клеток с помощью белка перфорина и гранзима. Полимеризуясь, перфорин образует в цитоплазматической мембране клетки-мишени трансмембранные каналы, по которым внутрь клетки поступают гранзимы(фрагментины) - смесь сериновых протеаз. Существенным компонентом этой смеси является гранзим В – протеолитический фермент, превращающий прокаспазу-3 в активную каспазу-3 с дальнейшей реализацией апоптоза.
 Особую форму апоптоза претерпевают эритроциты млекопитающих. Биогенез эритроцитов из плюропотентной стволовой клетки в костном мозге включает ряд промежуточных этапов. На этапе эритробласта ядро изгоняется (выталкивается) из клетки и пожирается макрофагом. Альтернативный вариант — кариорексис с образованием телец Жолли и их последующий распад и лизис внутри клетки. Безъядерная клетка, называемая ретикулоцитом, в дальнейшем теряет митохондрии и рибосомы и превращается в эритроцит. Потерю ядра эритробластом можно рассматривать как особую форму ядерного апоптоза. Лишенный ядра и митохондрий эритроцит, исполнив свое назначение, по-видимому, включает программу гибели, чтобы после этого поступить в распоряжение макрофагов печени и селезенки с выраженными признаками по пути апоптоза, который реализуется без участия каспаз.
Особую форму апоптоза претерпевают эритроциты млекопитающих. Биогенез эритроцитов из плюропотентной стволовой клетки в костном мозге включает ряд промежуточных этапов. На этапе эритробласта ядро изгоняется (выталкивается) из клетки и пожирается макрофагом. Альтернативный вариант — кариорексис с образованием телец Жолли и их последующий распад и лизис внутри клетки. Безъядерная клетка, называемая ретикулоцитом, в дальнейшем теряет митохондрии и рибосомы и превращается в эритроцит. Потерю ядра эритробластом можно рассматривать как особую форму ядерного апоптоза. Лишенный ядра и митохондрий эритроцит, исполнив свое назначение, по-видимому, включает программу гибели, чтобы после этого поступить в распоряжение макрофагов печени и селезенки с выраженными признаками по пути апоптоза, который реализуется без участия каспаз.
 Таким образом, ПКГ вовлечена в разнообразные биологические события, которые включают морфогенез, тканевой гомеостаз, и устранения дефектных клеток на протяжении всего онтогенетического развития многоклеточного организма. Обнаружено, что возникновение многих тяжелых заболеваний связано с нарушениями различных программ клеточной гибели. ПКГ может определяться типом и уровнем дифференцировки, положением в клеточном цикле, набором присутствующих в микроокружении цитокинов, состоянием энергетической системы. Апоптическая, аутофагическая и некрозпрограммируемая гибель клеток имеет общие молекулярные механизмы, несмотря на некоторые особенности, биохимические и морфологические характеристики их перекрываются, отражая наличие в клетках широкого спектра танатогенных подпрограмм деструкции.
Таким образом, ПКГ вовлечена в разнообразные биологические события, которые включают морфогенез, тканевой гомеостаз, и устранения дефектных клеток на протяжении всего онтогенетического развития многоклеточного организма. Обнаружено, что возникновение многих тяжелых заболеваний связано с нарушениями различных программ клеточной гибели. ПКГ может определяться типом и уровнем дифференцировки, положением в клеточном цикле, набором присутствующих в микроокружении цитокинов, состоянием энергетической системы. Апоптическая, аутофагическая и некрозпрограммируемая гибель клеток имеет общие молекулярные механизмы, несмотря на некоторые особенности, биохимические и морфологические характеристики их перекрываются, отражая наличие в клетках широкого спектра танатогенных подпрограмм деструкции.
 «Биология в школе» , 2011, № 3
«Биология в школе» , 2011, № 3



