Почвоведение_коллоид.ppt
- Количество слайдов: 39
 Почвенные коллоиды, их строение и свойства А. И. Попов
Почвенные коллоиды, их строение и свойства А. И. Попов
 Коллоиды (от греч. kolla — клей + eidos — вид: (дословно) “клееподобные”), или коллоидные системы — дисперсные системы, занимающие промежуточное положение между истинными растворами и грубодисперсными системами Коллоидные дисперсии — диспергированные частицы, размер которых находится в интервале от 1 до 103 нм
Коллоиды (от греч. kolla — клей + eidos — вид: (дословно) “клееподобные”), или коллоидные системы — дисперсные системы, занимающие промежуточное положение между истинными растворами и грубодисперсными системами Коллоидные дисперсии — диспергированные частицы, размер которых находится в интервале от 1 до 103 нм
 В коллоидном состоянии у веществ значительная доля всех молекул находится на поверхности раздела фаз, при этом молекулы коллоидных дисперсий обладают избыточной свободной энергией поэтому у коллоидных систем появляются свойства — поверхностно-активные и электроповерхностные
В коллоидном состоянии у веществ значительная доля всех молекул находится на поверхности раздела фаз, при этом молекулы коллоидных дисперсий обладают избыточной свободной энергией поэтому у коллоидных систем появляются свойства — поверхностно-активные и электроповерхностные
 Поверхностные явления — процессы, происходящие на границе раздела фаз, в межфазном поверхностном слое и возникающие в результате взаимодействия сопряженных фаз
Поверхностные явления — процессы, происходящие на границе раздела фаз, в межфазном поверхностном слое и возникающие в результате взаимодействия сопряженных фаз
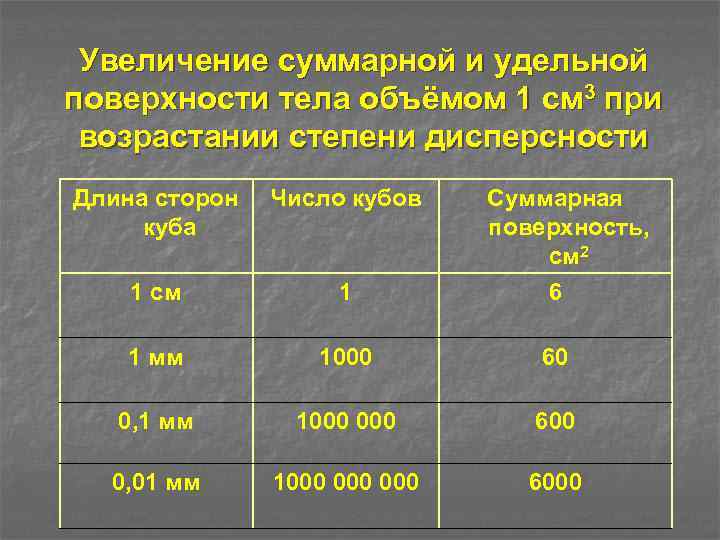 Увеличение суммарной и удельной поверхности тела объёмом 1 см 3 при возрастании степени дисперсности Длина сторон куба Число кубов Суммарная поверхность, см 2 6 1 см 1 1 мм 1000 60 0, 1 мм 1000 600 0, 01 мм 1000 000 6000
Увеличение суммарной и удельной поверхности тела объёмом 1 см 3 при возрастании степени дисперсности Длина сторон куба Число кубов Суммарная поверхность, см 2 6 1 см 1 1 мм 1000 60 0, 1 мм 1000 600 0, 01 мм 1000 000 6000
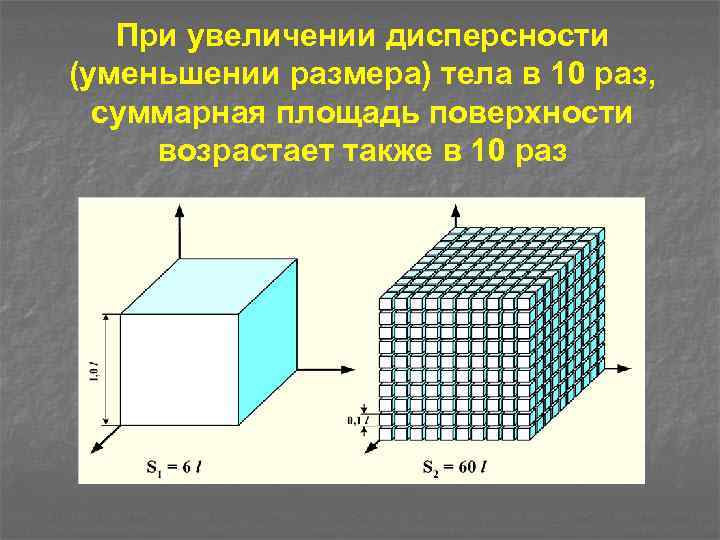 При увеличении дисперсности (уменьшении размера) тела в 10 раз, суммарная площадь поверхности возрастает также в 10 раз
При увеличении дисперсности (уменьшении размера) тела в 10 раз, суммарная площадь поверхности возрастает также в 10 раз
 Удельная поверхность является одним из параметров, определяющих химическую активность почв, так как с увеличением дисперсности частиц их химическая активность возрастает Пример: дерново-подзолистые 29 м 2/г серые лесные 33 м 2/г чернозёмы 48 м 2/г РЭМ-фотография образца илистой фракции с ячеистой микроструктурой; увеличение 2000
Удельная поверхность является одним из параметров, определяющих химическую активность почв, так как с увеличением дисперсности частиц их химическая активность возрастает Пример: дерново-подзолистые 29 м 2/г серые лесные 33 м 2/г чернозёмы 48 м 2/г РЭМ-фотография образца илистой фракции с ячеистой микроструктурой; увеличение 2000
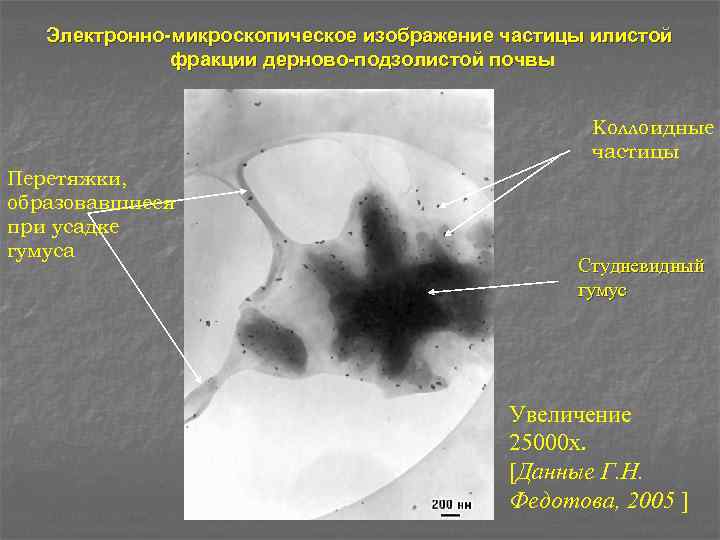 Электронно-микроскопическое изображение частицы илистой фракции дерново-подзолистой почвы Коллоидные частицы Перетяжки, образовавшиеся при усадке гумуса Студневидный гумус Увеличение 25000 х. [Данные Г. Н. Федотова, 2005 ]
Электронно-микроскопическое изображение частицы илистой фракции дерново-подзолистой почвы Коллоидные частицы Перетяжки, образовавшиеся при усадке гумуса Студневидный гумус Увеличение 25000 х. [Данные Г. Н. Федотова, 2005 ]
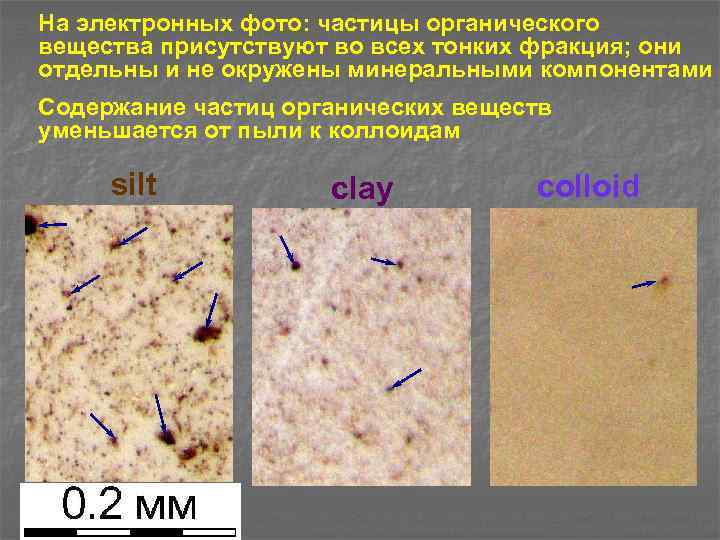 На электронных фото: частицы органического вещества присутствуют во всех тонких фракция; они отдельны и не окружены минеральными компонентами Содержание частиц органических веществ уменьшается от пыли к коллоидам silt clay colloid
На электронных фото: частицы органического вещества присутствуют во всех тонких фракция; они отдельны и не окружены минеральными компонентами Содержание частиц органических веществ уменьшается от пыли к коллоидам silt clay colloid
 Поверхностные явления обусловлены тем, что в поверхностных слоях на межфазных границах вследствие разного состава и строения соприкасающихся фаз и соответственно из-за различия в связях поверхностных атомов и молекул со стороны одной и другой фазы существует ненасыщенное поле межатомных, межмолекулярных сил. По этой причине атомы и молекулы в поверхностных слоях образуют особую структуру, а вещество принимает особое состояние, отличающееся по свойствам от его состояния в объёмах фаз: реакционной способностью, температурой плавления и кипения и другими свойствами
Поверхностные явления обусловлены тем, что в поверхностных слоях на межфазных границах вследствие разного состава и строения соприкасающихся фаз и соответственно из-за различия в связях поверхностных атомов и молекул со стороны одной и другой фазы существует ненасыщенное поле межатомных, межмолекулярных сил. По этой причине атомы и молекулы в поверхностных слоях образуют особую структуру, а вещество принимает особое состояние, отличающееся по свойствам от его состояния в объёмах фаз: реакционной способностью, температурой плавления и кипения и другими свойствами
 Поверхностно-активные вещества — специфические вещества, обладающие очень большой поверхностной активностью по отношению к воде, что является следствием их особого строения. Поверхностно-инактивные вещества — вещества, которые взаимодействуют с водой сильнее, чем молекулы воды между собой. Примером поверхностноинактивных веществ по отношению к воде являются неорганические соли, которые сильно гидратируются
Поверхностно-активные вещества — специфические вещества, обладающие очень большой поверхностной активностью по отношению к воде, что является следствием их особого строения. Поверхностно-инактивные вещества — вещества, которые взаимодействуют с водой сильнее, чем молекулы воды между собой. Примером поверхностноинактивных веществ по отношению к воде являются неорганические соли, которые сильно гидратируются
 Свойства коллоидных систем — поскольку в коллоидном состоянии у веществ значительная доля всех молекул находится на поверхности раздела фаз, при этом молекулы коллоидных дисперсий обладают избыточной свободной энергией
Свойства коллоидных систем — поскольку в коллоидном состоянии у веществ значительная доля всех молекул находится на поверхности раздела фаз, при этом молекулы коллоидных дисперсий обладают избыточной свободной энергией
 Электроповерхностные свойства коллоидных систем — появление на поверхности дисперсной фазы двойного электрического слоя (ДЭС) Частицы дисперсной фазы вместе с двойным электрическим слоем в полярной жидкости (в частности, в воде) образуют мицеллу (ДЭС-мицеллу) Дисперсные частицы способны электростатически связывать ионы из раствора или адсорбировать молекулы растворителя, в результате чего и формируются ДЭС-мицеллы
Электроповерхностные свойства коллоидных систем — появление на поверхности дисперсной фазы двойного электрического слоя (ДЭС) Частицы дисперсной фазы вместе с двойным электрическим слоем в полярной жидкости (в частности, в воде) образуют мицеллу (ДЭС-мицеллу) Дисперсные частицы способны электростатически связывать ионы из раствора или адсорбировать молекулы растворителя, в результате чего и формируются ДЭС-мицеллы
 Вблизи заряженной поверхности гранулы (ядра и потенциал определяющего слоя) группируются противоионы. Последние компенсируют заряд твёрдой фазы (гранулы) и находятся в жидкой фазе ДЭСмицеллы. Одни противоионы — связанные или неподвижные — благодаря адсорбционным и электростатическим силам плотно прилегают к поверхности гранулы мицеллы, отчасти компенсируя её заряд. Другие противоионы вследствие теплового движения могут выходить за пределы мицеллы во внешний раствор
Вблизи заряженной поверхности гранулы (ядра и потенциал определяющего слоя) группируются противоионы. Последние компенсируют заряд твёрдой фазы (гранулы) и находятся в жидкой фазе ДЭСмицеллы. Одни противоионы — связанные или неподвижные — благодаря адсорбционным и электростатическим силам плотно прилегают к поверхности гранулы мицеллы, отчасти компенсируя её заряд. Другие противоионы вследствие теплового движения могут выходить за пределы мицеллы во внешний раствор
 Под воздействием заряда частицы ионы удерживаются во внешнем растворе и образуют диффузный слой. Существование двойного электрического слоя ионов и скачкá электрического потенциала на границе раздела двух фаз играет важную роль не только в процессах адсорбции ионов и ионного обмена, но и во многих других явлениях в почвах
Под воздействием заряда частицы ионы удерживаются во внешнем растворе и образуют диффузный слой. Существование двойного электрического слоя ионов и скачкá электрического потенциала на границе раздела двух фаз играет важную роль не только в процессах адсорбции ионов и ионного обмена, но и во многих других явлениях в почвах
 Образование ДЭС-мицеллы
Образование ДЭС-мицеллы
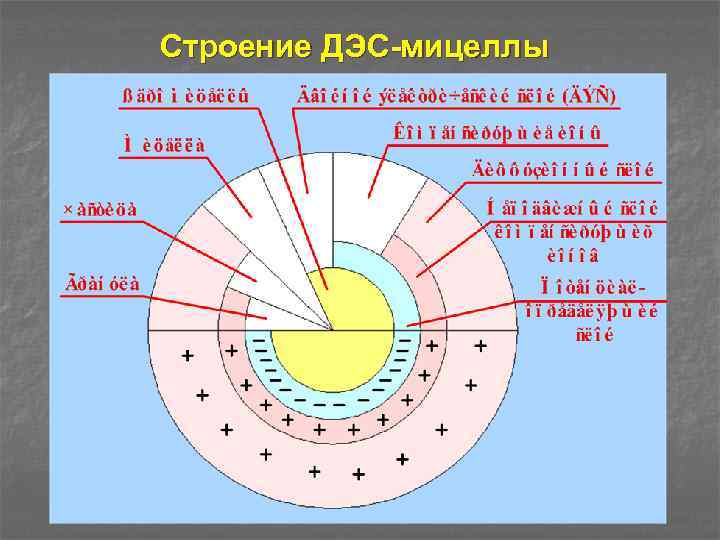 Строение ДЭС-мицеллы
Строение ДЭС-мицеллы
 Различают: n n n Ацитоидные ДЭС-мицеллы Базоидные ДЭС-мицеллы Амфолитоидные ДЭС-мицеллы
Различают: n n n Ацитоидные ДЭС-мицеллы Базоидные ДЭС-мицеллы Амфолитоидные ДЭС-мицеллы
 Дисперсные системы — совокупность дисперсий вместе со средой, в которой они распределены Дисперсии (от лат. dispersus — рассеянный, рассыпанный) — тела с высокоразвитой поверхностью, т. е. раздробленные тела; например, пленки, нити, капилляры и мелкие частицы. Дисперсные системы состоят не меньше чем из двух фаз: дисперсионной среды и дисперсной фазы
Дисперсные системы — совокупность дисперсий вместе со средой, в которой они распределены Дисперсии (от лат. dispersus — рассеянный, рассыпанный) — тела с высокоразвитой поверхностью, т. е. раздробленные тела; например, пленки, нити, капилляры и мелкие частицы. Дисперсные системы состоят не меньше чем из двух фаз: дисперсионной среды и дисперсной фазы
 Дисперсионная среда — сплошная фаза дисперсной системы (жидкая, газообразная или твёрдая) Дисперсная фаза — раздробленная фаза (диспергированные частицы), распределённая в дисперсионной среде
Дисперсионная среда — сплошная фаза дисперсной системы (жидкая, газообразная или твёрдая) Дисперсная фаза — раздробленная фаза (диспергированные частицы), распределённая в дисперсионной среде
 Диспергированные частицы обычно твёрдые, однако могут быть жидкими и газообразными. Эти частицы могут представлять собой отдельные молекулы (ионы) или их агрегаты. Соответственно они образуют молекулярные дисперсии (истинные растворы, аналитические дисперсии), коллоидные дисперсии и грубые дисперсии
Диспергированные частицы обычно твёрдые, однако могут быть жидкими и газообразными. Эти частицы могут представлять собой отдельные молекулы (ионы) или их агрегаты. Соответственно они образуют молекулярные дисперсии (истинные растворы, аналитические дисперсии), коллоидные дисперсии и грубые дисперсии
 Свойства дисперсных систем Характеристика Дисперсии аналитические коллоидные грубые Размер частиц < 1 нм 1 103 нм > 103 нм Движение частиц Очень быстрое тепловое движение Очень быстрое броуновское движение Медленное броуновское движение Коллодиевая мембрана Бумажный фильтр Способность к фильтрации Диффузия Быстрая Медленная — Осмотическое давление Высокое Низкое — Способ наблюдения — Ультрамикроскоп, электронный микроскоп Визуальный, оптический микроскоп
Свойства дисперсных систем Характеристика Дисперсии аналитические коллоидные грубые Размер частиц < 1 нм 1 103 нм > 103 нм Движение частиц Очень быстрое тепловое движение Очень быстрое броуновское движение Медленное броуновское движение Коллодиевая мембрана Бумажный фильтр Способность к фильтрации Диффузия Быстрая Медленная — Осмотическое давление Высокое Низкое — Способ наблюдения — Ультрамикроскоп, электронный микроскоп Визуальный, оптический микроскоп
 Грубодисперсные системы — свободнодисперсные системы с частицами, диаметр которых превышает 10– 6 м Из грубодисперсных систем наиболее распространены системы твердоегазобразное (песок, щебень и др. ).
Грубодисперсные системы — свободнодисперсные системы с частицами, диаметр которых превышает 10– 6 м Из грубодисперсных систем наиболее распространены системы твердоегазобразное (песок, щебень и др. ).
 Почвенные коллоиды — совокупность механических элементов почвы размером от 0, 0001 до 0, 001 мм [ГОСТ 27593 -88 (СТ СЭВ 5298 -85)] Жидкие коллоидные системы — золи, а студнеобразные — гели Различают: обратимые коллоиды (золь гель) и необратимые коллоиды (золь гель)
Почвенные коллоиды — совокупность механических элементов почвы размером от 0, 0001 до 0, 001 мм [ГОСТ 27593 -88 (СТ СЭВ 5298 -85)] Жидкие коллоидные системы — золи, а студнеобразные — гели Различают: обратимые коллоиды (золь гель) и необратимые коллоиды (золь гель)
 Золь (от нем. Sole или от лат. solutio — раствор) — дисперсная система с жидкой дисперсионной средой, представляющая собой жидкий коллоидный раствор. В золе коллоидные частицы движутся более или менее свободно. Каждый золь может быть превращен в соответствующий гель
Золь (от нем. Sole или от лат. solutio — раствор) — дисперсная система с жидкой дисперсионной средой, представляющая собой жидкий коллоидный раствор. В золе коллоидные частицы движутся более или менее свободно. Каждый золь может быть превращен в соответствующий гель
 Гель (от лат. gelare — мерзнуть, застывать или gelo — застываю) — дисперсная система, обладающая некоторыми свойствами твердых тел (способность сохранять форму, прочность, упругость); обычно гели внешне имеют вид студенистых тел
Гель (от лат. gelare — мерзнуть, застывать или gelo — застываю) — дисперсная система, обладающая некоторыми свойствами твердых тел (способность сохранять форму, прочность, упругость); обычно гели внешне имеют вид студенистых тел
 В геле коллоидные частицы связаны друг с другом в рыхлую пространственную сетку и перемещение отдельных частиц затруднено. Структурная сетка и придает гелям механические свойства твердых тел; типичные гели обладают пластичностью и некоторой эластичностью
В геле коллоидные частицы связаны друг с другом в рыхлую пространственную сетку и перемещение отдельных частиц затруднено. Структурная сетка и придает гелям механические свойства твердых тел; типичные гели обладают пластичностью и некоторой эластичностью
 Все дисперсные системы по кинетическим свойствам дисперсной фазы можно разделить на два класса: - свободнодисперсные - связнодисперсные системы
Все дисперсные системы по кинетическим свойствам дисперсной фазы можно разделить на два класса: - свободнодисперсные - связнодисперсные системы
 Свободнодисперсные системы — системы с подвижной дисперсной фазой Связнодисперсные системы — (пористые тела) системы с твердой дисперсионной средой, в которой частицы дисперсионной фазы связаны между собой и не могут свободно перемещаться
Свободнодисперсные системы — системы с подвижной дисперсной фазой Связнодисперсные системы — (пористые тела) системы с твердой дисперсионной средой, в которой частицы дисперсионной фазы связаны между собой и не могут свободно перемещаться
 Процессы в дисперсных системах Сначала в результате конденсации из истинного раствора может образовываться устойчивая свободнодисперсная (мелкоизмельченная) система, в которой дисперсная фаза равномерно распределена по всему объему дисперсной среды. Водные растворы коллоидных дисперсий занимают промежуточное положение между истинными растворами и грубодисперсными системами (например, суспензиями и эмульсиями). Жидкие коллоидные системы являются золями. Частицы дисперсной фазы золей находятся в состоянии броуновского движения и потому седиментационно устойчивы
Процессы в дисперсных системах Сначала в результате конденсации из истинного раствора может образовываться устойчивая свободнодисперсная (мелкоизмельченная) система, в которой дисперсная фаза равномерно распределена по всему объему дисперсной среды. Водные растворы коллоидных дисперсий занимают промежуточное положение между истинными растворами и грубодисперсными системами (например, суспензиями и эмульсиями). Жидкие коллоидные системы являются золями. Частицы дисперсной фазы золей находятся в состоянии броуновского движения и потому седиментационно устойчивы
 Дисперсные системы можно разбить на 3 группы, качественно отличающиеся друг от друга: § Гетерогенные и микрогетерогенные смеси. § Коллоидно-дисперсные системы. § Молекулярно-(ионно)-дисперсные системы, истинные растворы.
Дисперсные системы можно разбить на 3 группы, качественно отличающиеся друг от друга: § Гетерогенные и микрогетерогенные смеси. § Коллоидно-дисперсные системы. § Молекулярно-(ионно)-дисперсные системы, истинные растворы.
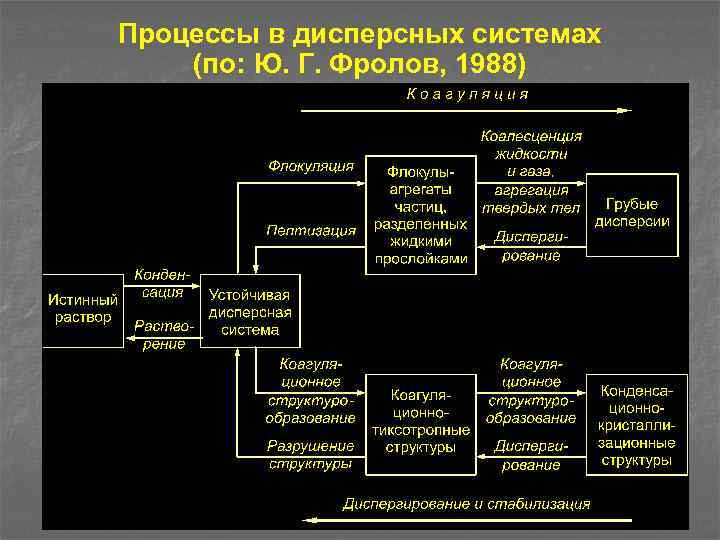 Процессы в дисперсных системах (по: Ю. Г. Фролов, 1988)
Процессы в дисперсных системах (по: Ю. Г. Фролов, 1988)
 Потеря агрегативной устойчивости молекул, входящих в устойчивую дисперсную систему, приводит к коагуляции, первый этап которой состоит в сближении частиц дисперсной фазы и взаимной их фиксации на небольших расстояниях друг от друга. Между частицами остаются прослойки среды. В результате образуются или флокулы (рыхлые хлопьевидные скопления — агрегаты, которые состоят из нескольких частиц, разделенных прослойками среды), или коагуляционные тиксотропные структуры, отличающиеся подвижностью частиц относительно друга под воздействием сравнительно небольших нагрузок (места контактов также разделены прослойками среды)
Потеря агрегативной устойчивости молекул, входящих в устойчивую дисперсную систему, приводит к коагуляции, первый этап которой состоит в сближении частиц дисперсной фазы и взаимной их фиксации на небольших расстояниях друг от друга. Между частицами остаются прослойки среды. В результате образуются или флокулы (рыхлые хлопьевидные скопления — агрегаты, которые состоят из нескольких частиц, разделенных прослойками среды), или коагуляционные тиксотропные структуры, отличающиеся подвижностью частиц относительно друга под воздействием сравнительно небольших нагрузок (места контактов также разделены прослойками среды)
 Коагуляция (от лат. coagulatio — свертывание, затвердение, сгущение) — слипание и слияние частиц или же укрупнение частиц в дисперсных системах, т. е. стремление частиц неустойчивого золя к слипанию с образованием крупных агрегатов частиц. Коалесценция — процесс полного слияния твердых частиц в системах жидкой и газообразной дисперсных системах. Пептизация — процесс образования устойчивой свободнодисперсной системы из осадка или геля (структурированной дисперсной системы)
Коагуляция (от лат. coagulatio — свертывание, затвердение, сгущение) — слипание и слияние частиц или же укрупнение частиц в дисперсных системах, т. е. стремление частиц неустойчивого золя к слипанию с образованием крупных агрегатов частиц. Коалесценция — процесс полного слияния твердых частиц в системах жидкой и газообразной дисперсных системах. Пептизация — процесс образования устойчивой свободнодисперсной системы из осадка или геля (структурированной дисперсной системы)
 Флокуляция — вид коагуляции, при которой мелкие частицы, находящиеся во взвешенном состоянии в жидкой или газовой среде, образуют рыхлые хлопьевидные скопления — флокулы (агрегаты), состоящие из нескольких частиц, разделенных прослойками жидкости. В жидких дисперсных системах (золях, суспензиях, эмульсиях, латексах) происходит под влиянием специально добавляемых веществ — флокулянтов, а также при тепловых, механических, электрических и прочих воздействиях
Флокуляция — вид коагуляции, при которой мелкие частицы, находящиеся во взвешенном состоянии в жидкой или газовой среде, образуют рыхлые хлопьевидные скопления — флокулы (агрегаты), состоящие из нескольких частиц, разделенных прослойками жидкости. В жидких дисперсных системах (золях, суспензиях, эмульсиях, латексах) происходит под влиянием специально добавляемых веществ — флокулянтов, а также при тепловых, механических, электрических и прочих воздействиях
 Более глубокий процесс коагуляции приводит к разрушению прослоек среды (гидратных оболочек) и непосредственному контакту частиц. В результате или образуются жесткие агрегаты из твердых частиц, или происходит полное слияние молекул (структурных единиц) в системах с жидкой или газообразной дисперсной фазой. В концентрированных системах образуются жесткие объемные конденсационные структуры (связнодисперсные системы) твердых тел, которые можно снова превратить в свободнодисперсную систему только с помощью диспергирования, обычно принудительного
Более глубокий процесс коагуляции приводит к разрушению прослоек среды (гидратных оболочек) и непосредственному контакту частиц. В результате или образуются жесткие агрегаты из твердых частиц, или происходит полное слияние молекул (структурных единиц) в системах с жидкой или газообразной дисперсной фазой. В концентрированных системах образуются жесткие объемные конденсационные структуры (связнодисперсные системы) твердых тел, которые можно снова превратить в свободнодисперсную систему только с помощью диспергирования, обычно принудительного
 Изменяя условия существования дисперсных систем (например, концентрацию или температуру), можно осуществлять обратимые переходы: Истинны й раствор (молеку лярный) Золь (свободнод исперсная система) — коллоидны й (мицелляр ный) раствор Гель (связноди сперсная система)
Изменяя условия существования дисперсных систем (например, концентрацию или температуру), можно осуществлять обратимые переходы: Истинны й раствор (молеку лярный) Золь (свободнод исперсная система) — коллоидны й (мицелляр ный) раствор Гель (связноди сперсная система)
 Общая классификация дисперсных систем основана на различии в агрегатном состоянии дисперсионной среды и дисперсной фазы Сочетание трёх агрегатных состояний (твердого, жидкого и газообразного) позволяет выделить девять типов дисперсных систем
Общая классификация дисперсных систем основана на различии в агрегатном состоянии дисперсионной среды и дисперсной фазы Сочетание трёх агрегатных состояний (твердого, жидкого и газообразного) позволяет выделить девять типов дисперсных систем
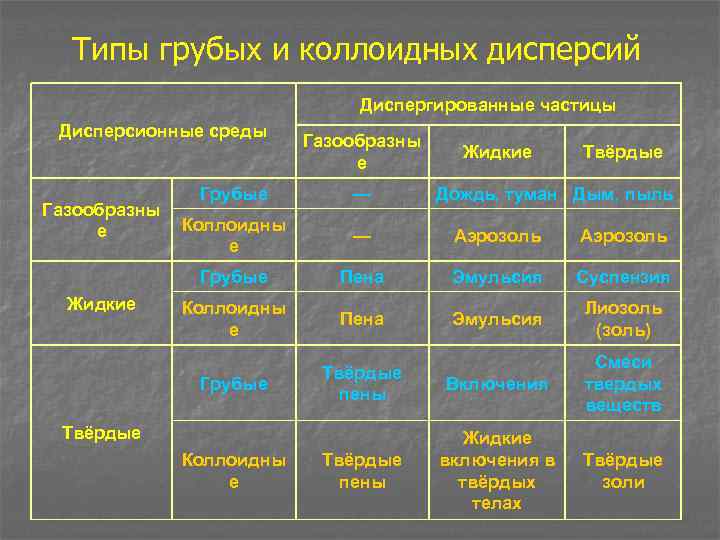 Типы грубых и коллоидных дисперсий Диспергированные частицы Дисперсионные среды Газообразны е Жидкие Твёрдые Коллоидны е — Аэрозоль Пена Эмульсия Суспензия Коллоидны е Пена Эмульсия Лиозоль (золь) Грубые Жидкие — Грубые Газообразны е Грубые Твёрдые пены Включения Смеси твердых веществ Твёрдые пены Жидкие включения в твёрдых телах Твёрдые золи Твёрдые Коллоидны е Дождь, туман Дым, пыль
Типы грубых и коллоидных дисперсий Диспергированные частицы Дисперсионные среды Газообразны е Жидкие Твёрдые Коллоидны е — Аэрозоль Пена Эмульсия Суспензия Коллоидны е Пена Эмульсия Лиозоль (золь) Грубые Жидкие — Грубые Газообразны е Грубые Твёрдые пены Включения Смеси твердых веществ Твёрдые пены Жидкие включения в твёрдых телах Твёрдые золи Твёрдые Коллоидны е Дождь, туман Дым, пыль


