Pnevmonii-Krasnoyarsk_2012.ppt
- Количество слайдов: 159

Пневмония: новые лица известной болезни Малишевский Михаил Владимирович Тюменская медицинская академия г. Красноярск, 10 февраля 2012 года

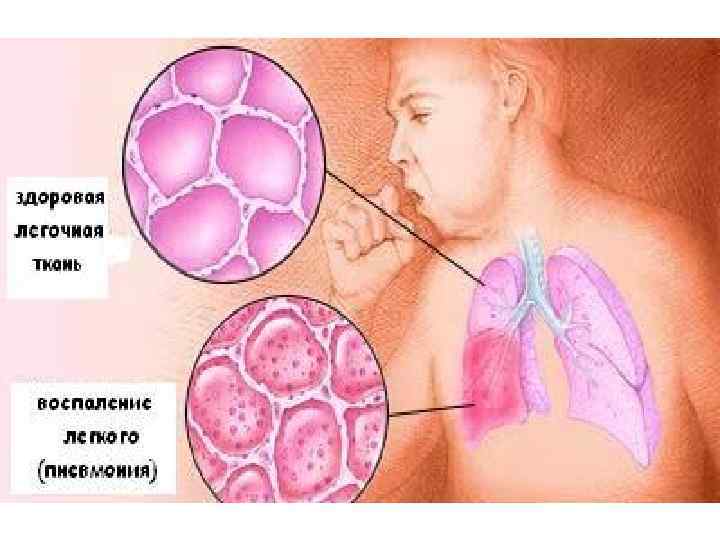

Пневмонии – это группа различных по этиологии, патогенезу, морфологической характеристике острых инфекционных (преимущественно бактериальных) заболеваний, характеризующихся очаговым поражением респираторных отделов легких с обязательным наличием внутриальвеолярной экссудации

Особенности современной пневмонии

1. Рост заболеваемости пневмонией

2. Гиподиагностика пневмоний

3. Рост смертности от пневмоний
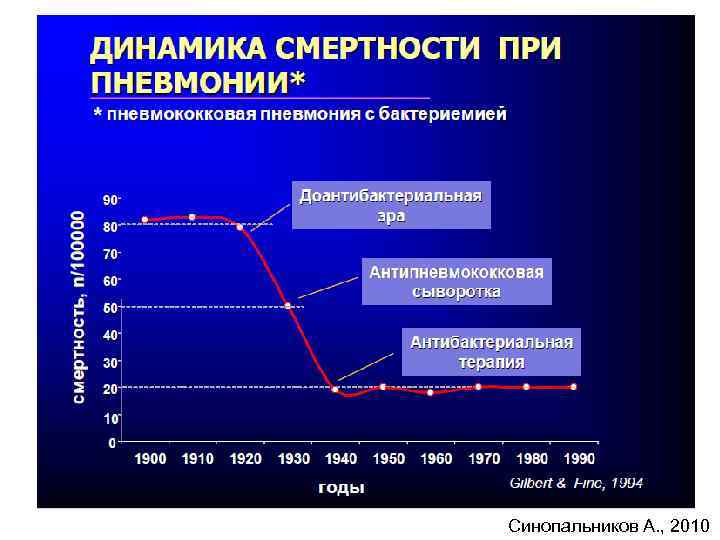
Синопальников А. , 2010

Сидни Шелдон умер 30 января 2007 года в возрасте 89 лет от пневмонии на Ранчо Мираж, Калифорния, США.

В воскресенье, 28 ноября, в возрасте 84 лет во флоридской больнице скончался известный американский актер-комик Лесли Нильсен. По предварительным данным, причиной смерти стала затянувшаяся пневмония.

Знаменитый французский актер Жерар Депардье лишился единственного сына. 37 -летний актер Гийом Депардье в понедельник умер из-за пневмонии в госпитале города Гарш. Смерть актера последовала после заражения вирусом, который спровоцировал скоротечную пневмонию. Гийом был госпитализирован в субботу в Бухаресте, где снимался в фильме "Детство Икара".




4. Возрастной и половой аспекты пневмоний

5. Теория модифицирующих факторов

6. Увеличение частоты тяжелого течения пневмоний

7. Спектр ключевых возбудителей пневмоний

Классификация пневмоний 1. Внебольничная (приобретенная вне лечебного учреждения) пневмония (синонимы: домашняя, амбулаторная) 2. Нозокомиальная (приобретенная в лечебном учреждении) пневмония (синонимы: госпитальная, внутрибольничная) 3. Аспирационная пневмония 4. Пневмония у лиц с тяжелыми нарушениями иммунитета (врожденный иммунодефицит, ВИЧ-инфекция, ятрогенная иммуносупрессия) Чучалин А. Г. , 2006

Классификация пневмоний (Чучалин А. Г. и др. , 2010 г. ) Внебольничная пневмония I. Типичная (у пациентов с отсутствием выраженных нарушений иммунитета): а) бактериальная; б) вирусная; в) грибковая; г) микобактериальная; д) паразитарная. II. У пациентов с выраженными нарушениями иммунитета: а) синдром приобретенного иммунодефицита (СПИД); б) прочие заболевания/патологические состояния. III. Аспирационная пневмония/абсцесс легкого. Нозокомиальная пневмония Пневмония, связанная с оказанием медицинской помощи I. Собственно нозокомиальная I. Пневмония у обитателей домов пневмония. престарелых II. Вентиляторассоциированная II. Прочие категории пациентов: пневмония. а) антибактериальная терапия в III. Нозокомиальная пневмония у предшествующие 3 мес. ; пациентов с выраженными б) госпитализация (по любому нарушениями иммунитета: поводу) в течение ≥ 2 суток в а) у реципиентов донорских предшествующие 90 дней; органов; в) пребывание в других б) у пациентов, получающих учреждениях длительного ухода; цитостатическую терапию. г) хронический диализ в течение ≥ 30 суток; д) обработка раневой поверхности в домашних условиях; е) иммунодефицитные состояния/заболевания.

Классификация пневмоний (Чучалин А. Г. и др. , 2010 г. ) 1. Внебольничная пневмония: I. Типичная (у пациентов с отсутствием выраженных нарушений иммунитета): а) бактериальная; б) вирусная; в) грибковая; г) микобактериальная; д) паразитарная. II. У пациентов с выраженными нарушениями иммунитета: а) синдром приобретенного иммунодефицита (СПИД); б) прочие заболевания/патологические состояния. III. Аспирационная пневмония/абсцесс легкого.

Классификация пневмоний (Чучалин А. Г. и др. , 2010 г. ) 2. Нозокомиальная пневмония: I. Собственно нозокомиальная пневмония. II. Вентиляторассоциированная пневмония. III. Нозокомиальная пневмония у пациентов с выраженными нарушениями иммунитета: а) у реципиентов донорских органов; б) у пациентов, получающих цитостатическую терапию.

Классификация пневмоний (Чучалин А. Г. и др. , 2010 г. ) 3. Пневмония, связанная с оказанием медицинской помощи: I. Пневмония у обитателей домов престарелых II. Прочие категории пациентов: а) антибактериальная терапия в предшествующие 3 мес. ; б) госпитализация (по любому поводу) в течение ≥ 2 суток в предшествующие 90 дней; в) пребывание в других учреждениях длительного ухода; г) хронический диализ в течение ≥ 30 суток; д) обработка раневой поверхности в домашних условиях; е) иммунодефицитные состояния/заболевания.

Назначение некоторых антибиотиков в амбулаторной практике может провоцировать развитие резистентности Опубликовано: Пятница, 27 августа 2010 г. - 09: 05 Согласно результатам недавно завершённого исследования пациенты, получавшие антибиотики в амбулаторной практике для лечения инфекций дыхательных или мочевыводящий путей, имеют более высокий риск устойчивости микроорганизмов к применявшемуся антибиотику при последующих инфекциях. Исследователями из Великобритании был выполнен систематический обзор 4373 публикаций, представленных в Medline, Embase и в Кокрановской базах банных, с целью определения тенденций антибиотикорезистентности микроорганизмов у пациентов, получавших антибиотики в амбулаторной практике. В окончательный мета-анализ было включено 24 исследования со сходными анализируемыми исходами. Среди них было 22 исследования, в которые включались пациенты с инфекциями, и 2 исследования, выполненные у здоровых добровольцев. В анализ были включены 19 обсервационных исследований (из них 2 проспективных) и 5 рандомизированных исследований. Были проанализированы объединённые результаты 5 исследований у 14348 пациентов с инфекциями мочевыводящих путей (ИМП). Объединённый показатель отношения шансов (ОШ) для наличия резистентных бактерий в данной популяции составил 2, 5 (95% доверительный интервал — ДИ от 2, 1 до 2, 9) в течение 2 месяцев после применения антибиотиков и 1, 33 (95% ДИ от 1, 2 до 1, 5) в течение 12 месяцев после лечения. В 7 исследованиях у 2605 участников изучалась антибиотикорезистентность возбудителей инфекций дыхательных путей. Объединённый показатель ОШ для наличия резистентных бактерий в данной популяции составил 2, 4 (95% ДИ от 1, 4 до 3, 9) в течение 2 месяцев после применения антибиотиков и 2, 4 (95% ДИ от 1, 3 до 4, 5) в течение 12 месяцев после лечения. По данным нескольких исследований, в которых было указано количество применявшихся антибиотиков, более длительное лечение и проведение нескольких курсов антимикробной терапии были связаны с более высокой частотой развития резистентности. В одном проспективном исследовании, включённом в мета-анализ, были определены показатели ОШ наличия резистентности после лечения в динамике на протяжении длительного периода наблюдения. Объединённые показатели ОШ составили: 12, 2 (95% ДИ от 6, 8 до 22, 1) через 1 неделю после применения антибиотиков; 6, 1 (2, 8 -3, 4) — через 1 месяц; 3, 6 (2, 2 -6, 0) — через 2 месяца и 2, 2 (1, 3 -3, 6) — через 6 месяцев после лечения. Таким образом, каждый случай применения антибиотиков приводит к достоверному повышению риска антибиотикорезистентности микроорганизмов и распространению носительства резистентных бактерий в популяции, что требует в последующем терапии антибиотиками «второй линии» при лечении инфекций в амбулаторной практике. Полученные результаты ещё раз подчеркивают важность предельно обоснованного и разумного применения антибиотиков при лечении инфекций в амбулаторной практике. Costelloe C. , et al. Effect of antibiotic prescribing in primary care on antimicrobial resistance in individual patients: systematic review and meta-analysis. BMJ 2010; 340: c 2096.

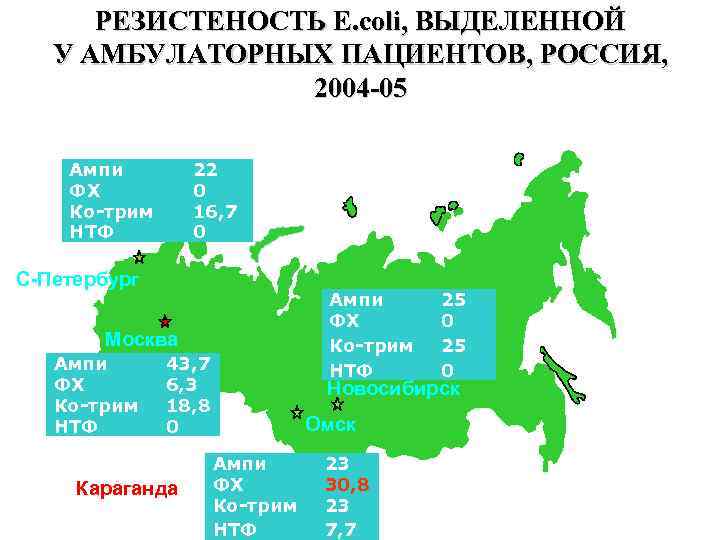
РЕЗИСТЕНОСТЬ E. coli, ВЫДЕЛЕННОЙ У АМБУЛАТОРНЫХ ПАЦИЕНТОВ, РОССИЯ, 2004 -05 Ампи ФХ Ко-трим НТФ 22 0 16, 7 0 С-Петербург Ампи ФХ Ко-трим НТФ Москва Ампи ФХ Ко-трим НТФ 43, 7 6, 3 18, 8 0 Караганда 25 0 Новосибирск Омск Ампи ФХ Ко-трим НТФ 23 30, 8 23 7, 7

ПОПУЛЯЦИОННЫЙ УРОВЕНЬ РЕЗИСТЕНТНОСТИ STREPTOCOCCUS PNEUMONIAE И ИСХОДЫ АНТИБАКТЕРИАЛЬНОЙ ТЕРАПИИ ИНФЕКЦИЙ ДЫХАТЕЛЬНЫЙ ПУТЕЙ · Анализ данных 7252 микробиологических исследований и исходов терапии у 649 552 взрослых пациентов с ИДП · США, 1997 -2000 гг · На популяционном уровне резистентность S. pneumoniae in vitro к макролидам и беталактамам не коррелирует с неэффективностью АБ-терапии Furuno JP Pharmacoepidemiol Drug Saf. 2006 Jan; 15(1): 1 -9

ДВА ЛИЦА РЕЗИСТЕНТНОСТИ Микробиологическое • Сохранение жизнеспособности штамма при концентрации препарата, подавляющей основную часть микробной популяции данного вида Клиническое • Снижение клинического и бактериологическо го эффекта при лечении инфекционной болезни С. В. Сидоренко, 2004

Классификация пневмоний (Чучалин А. Г. и др. , 2010 г. ) 3. Пневмония, связанная с оказанием медицинской помощи: I. Пневмония у обитателей домов престарелых II. Прочие категории пациентов: а) антибактериальная терапия в предшествующие 3 мес. ; б) госпитализация (по любому поводу) в течение ≥ 2 суток в предшествующие 90 дней; в) пребывание в других учреждениях длительного ухода; г) хронический диализ в течение ≥ 30 суток; д) обработка раневой поверхности в домашних условиях; е) иммунодефицитные состояния/заболевания.

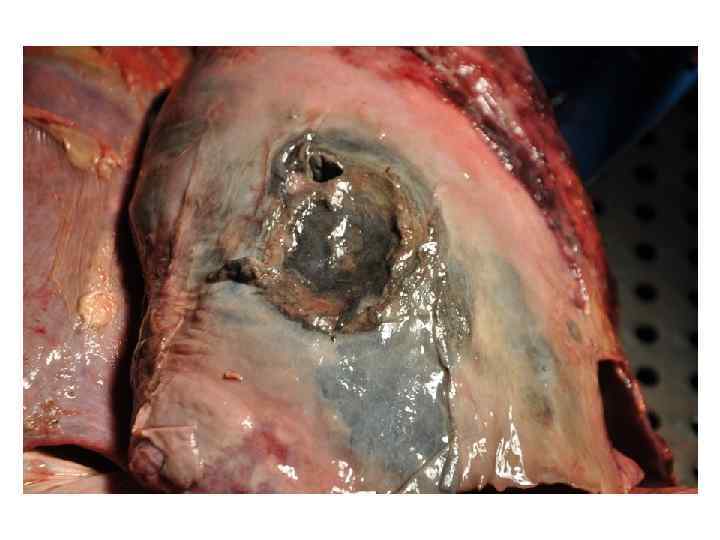
Осложнения пневмоний • • Плевральный выпот Эмпиема плевры Деструкция/абсцедирование легочной ткани Острый респираторный дистресс-синдром Острая дыхательная недостаточность Септический шок Вторичная бактериемия, сепсис, гематогенные очаги отсева • Перикардит, миокардит • Нефрит и др.

Внебольничная пневмония – острое заболевание, возникшее во внебольничных условиях (вне стационара) или диагностированное в первые 48 часов от момента госпитализации или развившееся у пациента, не находящегося в домах сестринского ухода/отделениях длительного медицинского наблюдения ≥ 14 суток, - сопровождающееся симптомами инфекции нижних дыхательных путей (лихорадка, кашель, выделение мокроты, возможно гнойной, боль в грудной клетке, одышка) и рентгенологическими признаками «свежих» очаговоинфильтративных изменений в легких при отсутствии очевидной диагностической альтернативы.

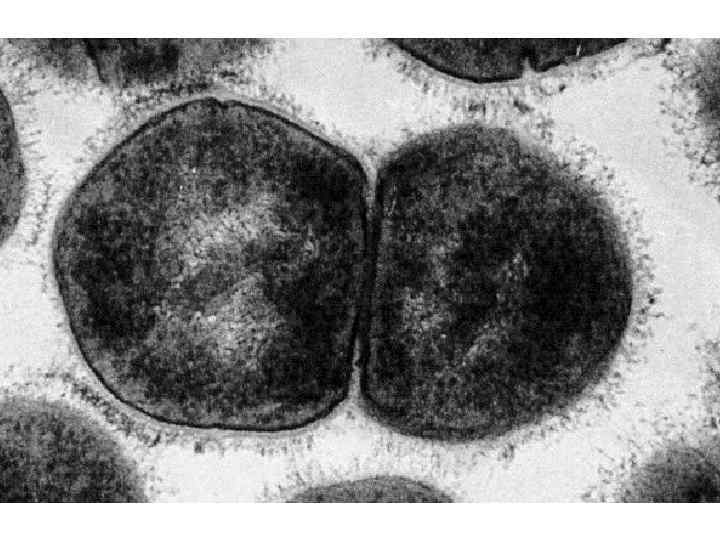
Этиология • S. pneumoniae (30 -50% случаев заболевания)
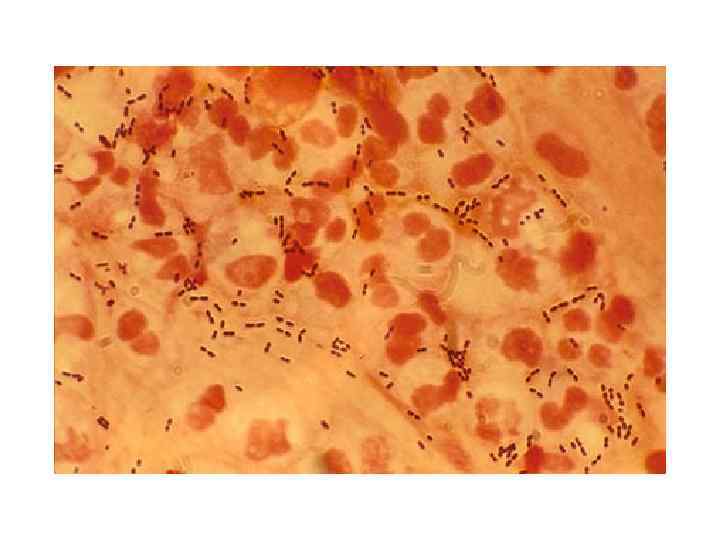

Этиология • S. pneumoniae (30 -50% случаев заболевания) • Атипичные микроорганизмы (8 -30% случаев заболевания)

Этиология • S. pneumoniae (30 -50% случаев заболевания) • Атипичные микроорганизмы (8 -30% случаев заболевания): • Clamydophila pneumoniae
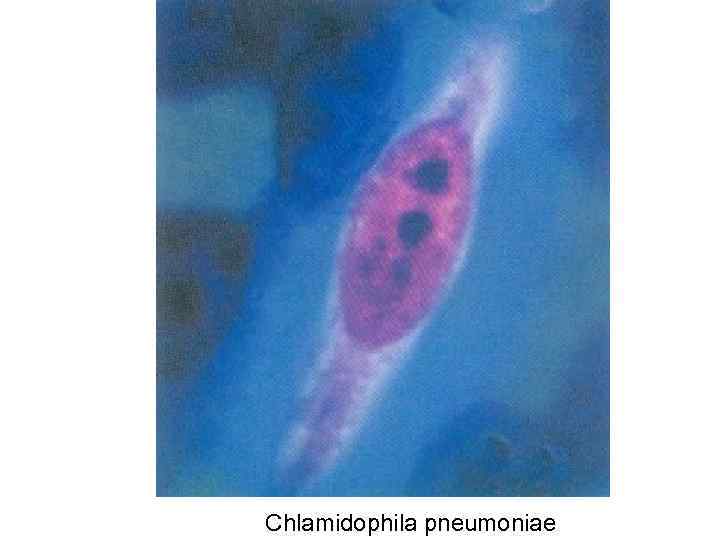
Chlamidophila pneumoniae

Этиология • S. pneumoniae (30 -50% случаев заболевания) • Атипичные микроорганизмы (8 -30% случаев заболевания): • Clamydophila pneumoniae • Mycoplasma pneumoniae
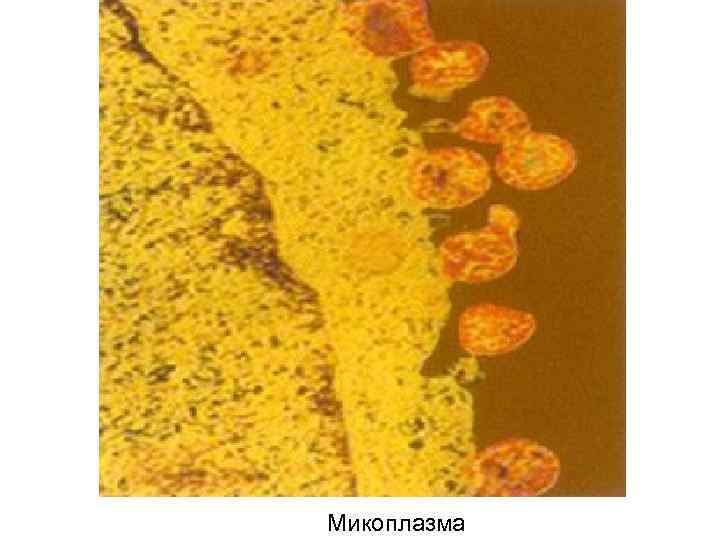
Микоплазма

Этиология • S. pneumoniae (30 -50% случаев заболевания) • Атипичные микроорганизмы (8 -30% случаев заболевания): • Clamydophila pneumoniae • Mycoplasma pneumoniae • Legionella pneumophila
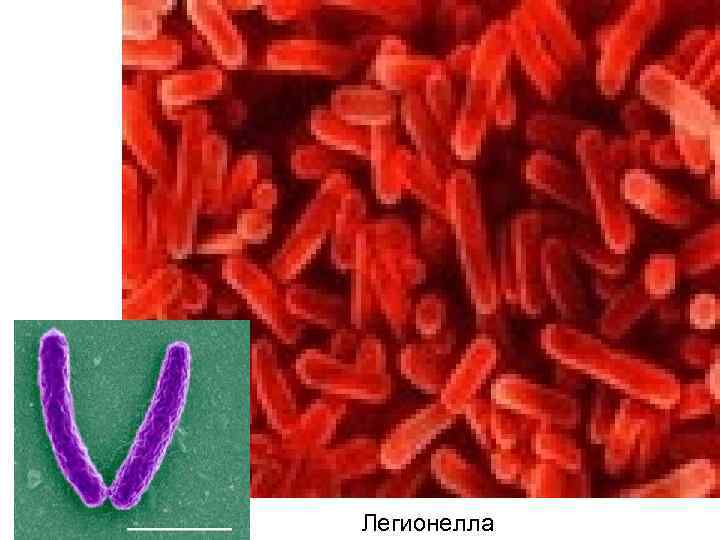
Легионелла

Возбудитель Ligionella pneumophila открыт в 1976 г. , после того как в Филадельфии на съезде легионеров (ветеранов, воевавших в Индокитае) из 221 участника заболело 220, причем в 30 случаях исход был летальным. В 90 -е годы эпидемические вспышки “болезни легионеров” были зафиксированы в Грузии и Прибалтике. Спорадическая заболеваемость, по данным разных авторов, составляет от 1, 5% до 15% всех случаев этиологически верифицированных пневмоний. Восприимчивость к инфекции более 70%. Болеют все, но чаще старики и дети. Легионелла — это грамотрицательная палочка размером до 3 мкм, имеющая жгутики. Место естественного обитания бактерии — пресная вода, организм человека является для возбудителя легионеллеза биологическим тупиком. Последнее ставит под сомнение возможность непосредственной передачи инфекции от человека к человеку. Пути передачи легионеллеза — алиментарный и ингаляционный, сезонность — летне-осенняя. Эпидемическая заболеваемость связывается с контаминацией возбудителем водных систем. Групповые вспышки возможны при проживании вблизи открытых водоемов, посещении бассейнов, контакте с кондиционерами, увлажнителями воздуха, системами принудительной вентиляции (метро, вокзалы, аэропорты, универмаги и др. ). Таким образом, легионеллез — это болезнь больших городов индустриально развитых стран.

Этиология • S. pneumoniae (30 -50% случаев заболевания) • Атипичные микроорганизмы (8 -30% случаев заболевания) • Clamydophila pneumoniae • Mycoplasma pneumoniae • Legionella pneumophila • Редкие возбудители (3 -5%) • Hemophilus influenza • Staphylococcus aureus • Klebsiella pneumoniae

В последнее время наблюдается рост числа ВП, вызываемых внебольничными штаммами MRSA. Продукция данным возбудителем лейкоцидина Panton-Valentine и других токсинов обусловливает развитие осложнений пневмонии (деструкция / абсцедирование легочной ткани, эмпиема плевры, шок, дыхательная недостаточность). Предположение о внебольничном MRSA следует допускать у больных с абсцедированием легочных инфильтратов при отсутствии факторов риска аспирационной пневмонии (злоупотребление алкоголем, нарушение моторики пищевода, нарушение сознания, инсульт, заболевания десен)
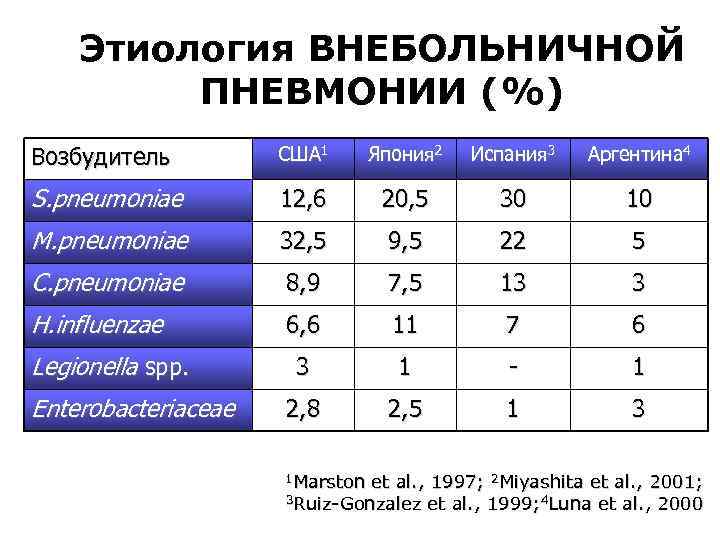
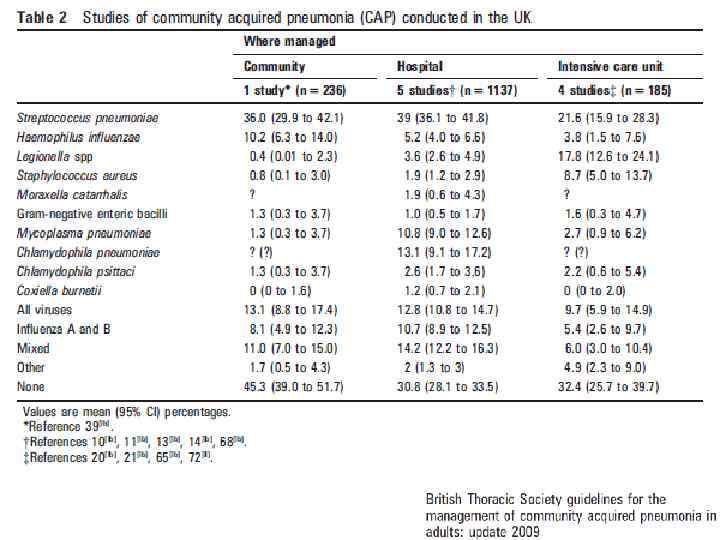
Этиология ВНЕБОЛЬНИЧНОЙ ПНЕВМОНИИ (%) Возбудитель США 1 Япония 2 Испания 3 Аргентина 4 S. pneumoniae 12, 6 20, 5 30 10 M. pneumoniae 32, 5 9, 5 22 5 C. pneumoniae 8, 9 7, 5 13 3 H. influenzae 6, 6 11 7 6 3 1 - 1 2, 8 2, 5 1 3 Legionella spp. Enterobacteriaceae 1 Marston et al. , 1997; 2 Miyashita et al. , 2001; 3 Ruiz-Gonzalez et al. , 1999; 4 Luna et al. , 2000
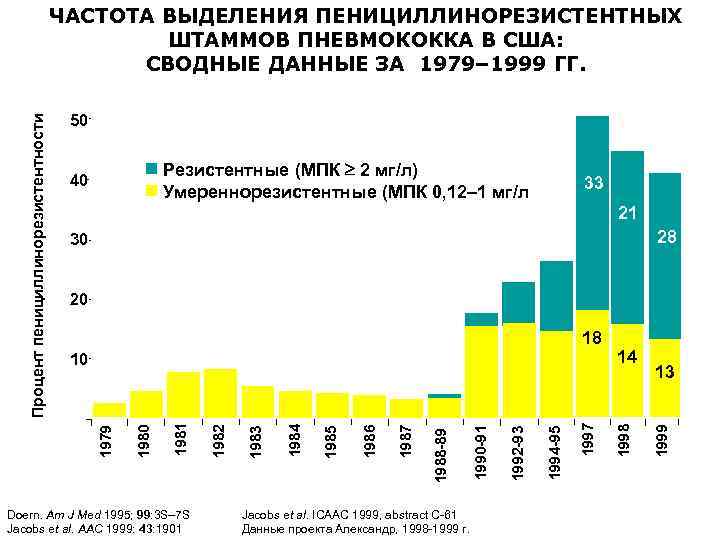
50 Резистентные (МПК 2 мг/л) Умереннорезистентные (МПК 0, 12– 1 мг/л) 40 33 21 28 30 20 Doern. Am J Med 1995; 99: 3 S– 7 S Jacobs et al. AAC 1999: 43: 1901 Jacobs et al. ICAAC 1999, abstract C-61 Данные проекта Александр, 1998 -1999 г. 14 13 1999 1997 1994 -95 1992 -93 1990 -91 1987 1988 -89 Год 1986 1985 1984 1983 1982 1981 0 1980 10 1998 18 1979 Процент пенициллинорезистентности ЧАСТОТА ВЫДЕЛЕНИЯ ПЕНИЦИЛЛИНОРЕЗИСТЕНТНЫХ ШТАММОВ ПНЕВМОКОККА В США: СВОДНЫЕ ДАННЫЕ ЗА 1979– 1999 ГГ.
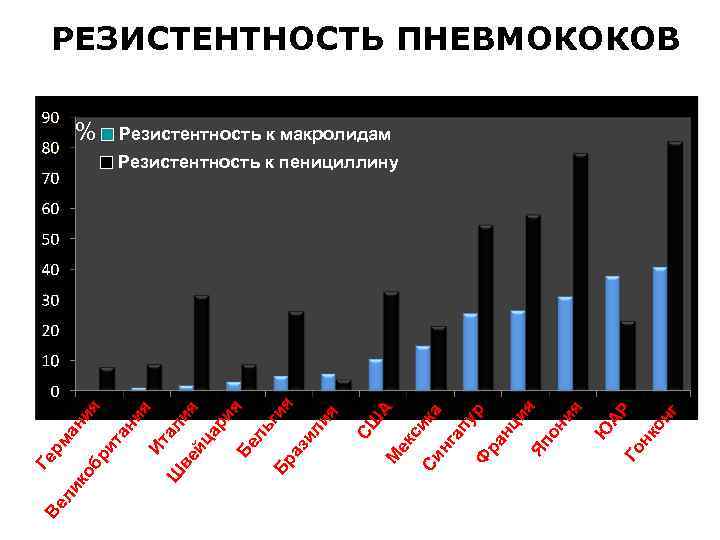
РЕЗИСТЕНТНОСТЬ ПНЕВМОКОКОВ % Резистентность к макролидам Ве ли нг ко Го н Ю АР ап ур Ф ра нц ия Яп он ия а нг ик Си ек с А М СШ Ге рм ан ко ия бр ит ан ия Ит ал Ш ия ве йц ар ия Бе ль ги Бр я аз ил ия Резистентность к пенициллину Данные проекта Александр, 1999 г.
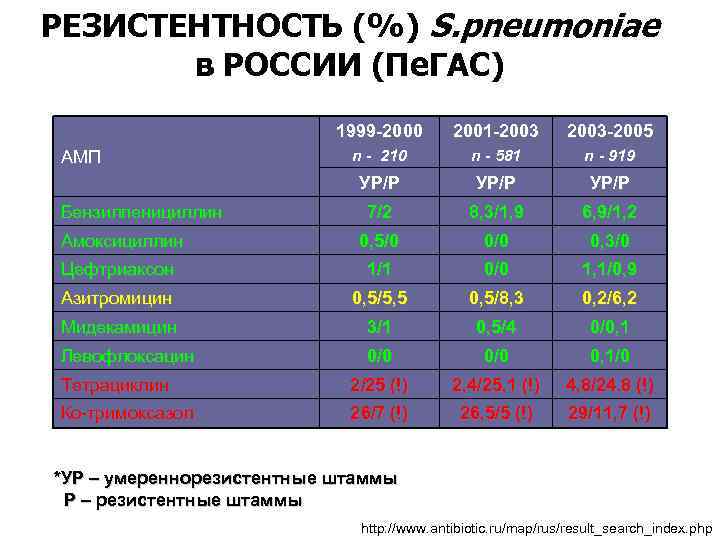
РЕЗИСТЕНТНОСТЬ (%) S. pneumoniae в РОССИИ (Пе. ГАС) 1999 -2000 2001 -2003 -2005 n - 210 n - 581 n - 919 УР/Р 7/2 8, 3/1, 9 6, 9/1, 2 Амоксициллин 0, 5/0 0, 3/0 Цефтриаксон 1/1 0/0 1, 1/0, 9 Азитромицин 0, 5/5, 5 0, 5/8, 3 0, 2/6, 2 Мидекамицин 3/1 0, 5/4 0/0, 1 Левофлоксацин 0/0 0, 1/0 Тетрациклин 2/25 (!) 2, 4/25, 1 (!) 4, 8/24. 8 (!) Ко-тримоксазол 26/7 (!) 26, 5/5 (!) 29/11, 7 (!) АМП Бензилпенициллин *УР – умереннорезистентные штаммы Р – резистентные штаммы http: //www. antibiotic. ru/map/rus/result_search_index. php
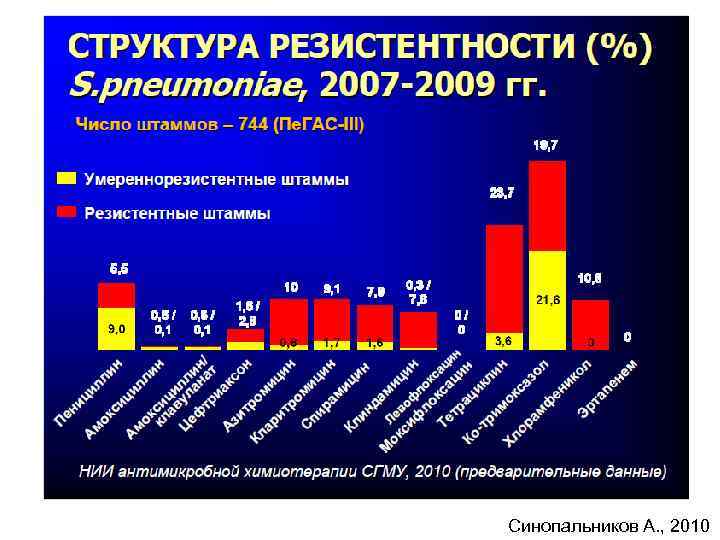
Синопальников А. , 2010
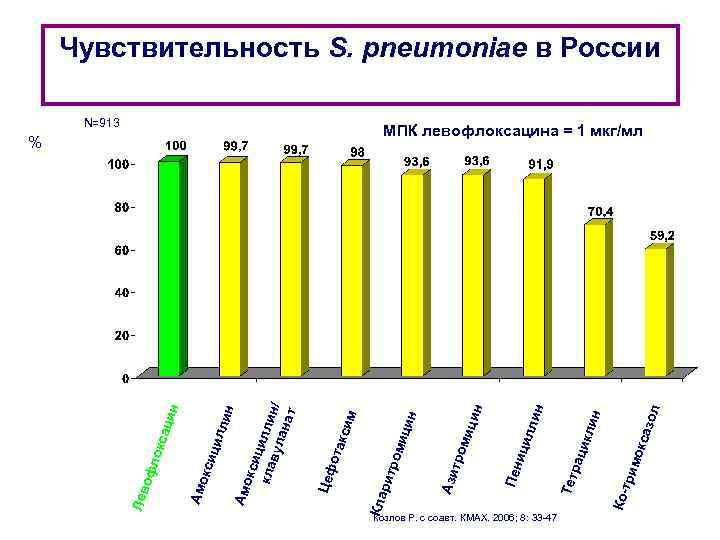
Козлов Р. с соавт. КМАХ. 2006; 8: 33 -47 саз ол ин икл мок три Ко- рац Тет лин цил Пен и ин н ици миц тро Ази ром % рит м N=913 Кла кси ота Цеф кси ц кла илли н вул ана / т Амо лин цил кси Амо ин сац лок оф Лев Чувствительность S. pneumoniae в России МПК левофлоксацина = 1 мкг/мл
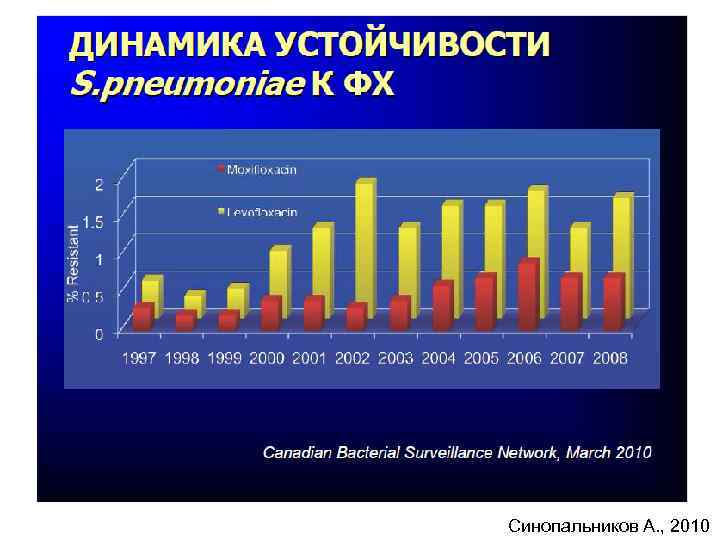
Синопальников А. , 2010
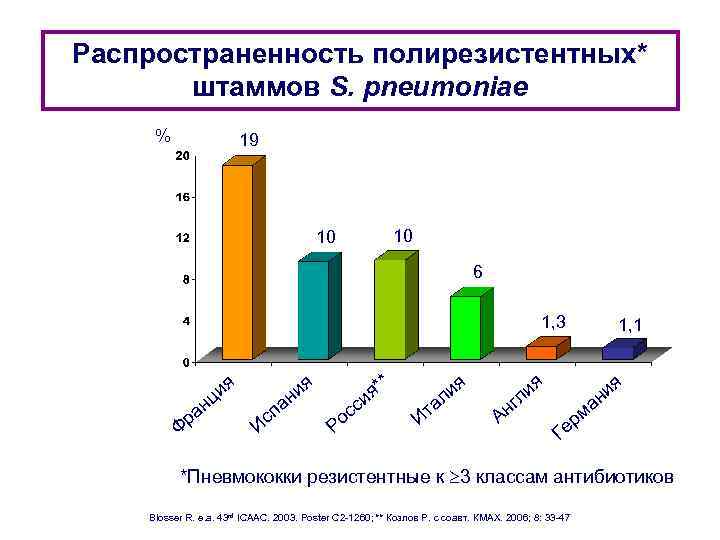
Распространенность полирезистентных* штаммов S. pneumoniae % 19 10 10 6 1, 3 ия ц ан р Ф Ис ия н па * я* и Р сс о Ит ия ал Ан и гл 1, 1 я я и ан рм е Г *Пневмококки резистентные к 3 классам антибиотиков Blosser R. e. a. 43 rd ICAAC. 2003. Poster C 2 -1260; ** Козлов Р. с соавт. КМАХ. 2006; 8: 33 -47

S. pneumoniae: ОСНОВНЫЕ ПРОБЛЕМЫ РЕЗИСТЕНТНОСТИ • Резистентность к пенициллину и другим b-лактамам • Резистентность к макролидам • Полирезистентность (устойчивость к 3 и более классам препаратов), включая: Ø тетрациклины Ø ко-тримоксазол Ø хлорамфеникол Ø фторхинолоны и др.

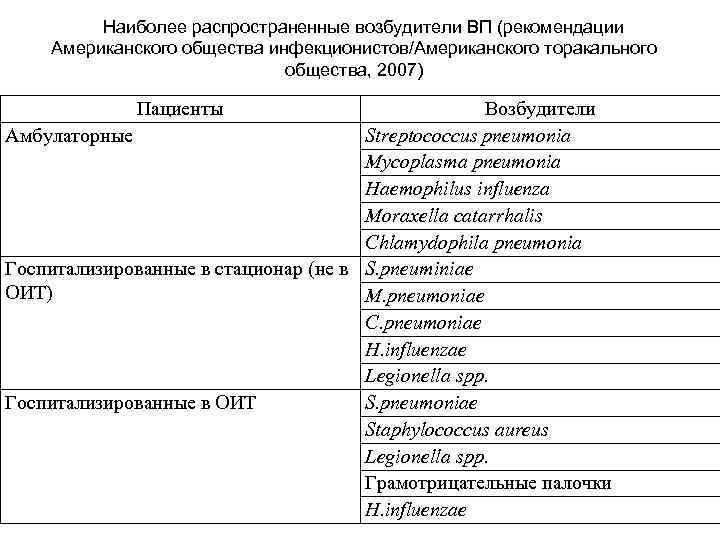
Наиболее распространенные возбудители ВП (рекомендации Американского общества инфекционистов/Американского торакального общества, 2007) Пациенты Возбудители Амбулаторные Streptococcus pneumonia Mycoplasma pneumonia Haemophilus influenza Moraxella catarrhalis Chlamydophila pneumonia Госпитализированные в стационар (не в S. pneuminiae ОИТ) M. pneumoniae C. pneumoniae H. influenzae Legionella spp. Госпитализированные в ОИТ S. pneumoniae Staphylococcus aureus Legionella spp. Грамотрицательные палочки H. influenzae
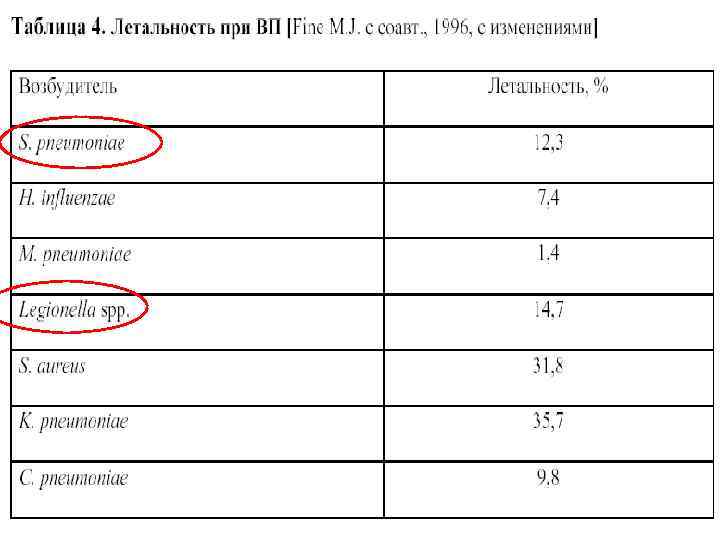
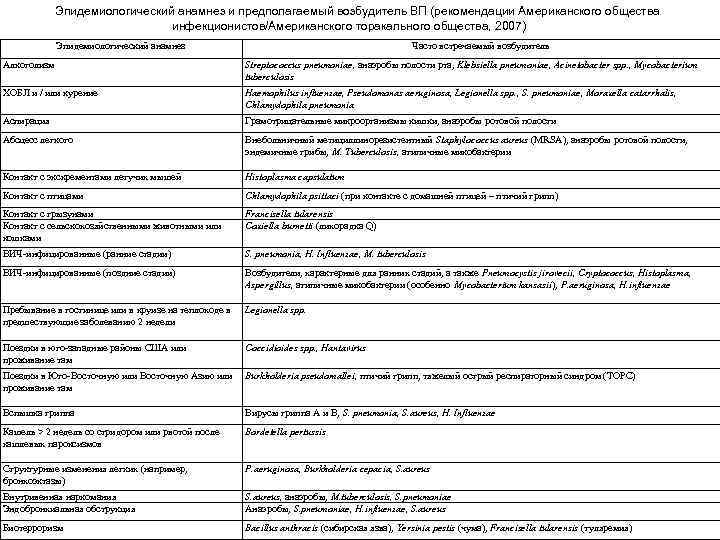
Эпидемиологический анамнез и предполагаемый возбудитель ВП (рекомендации Американского общества инфекционистов/Американского торакального общества, 2007) Эпидемиологический анамнез Часто встречаемый возбудитель Алкоголизм Streptococcus pneumoniae, анаэробы полости рта, Klebsiella pneumoniae, Acinetobacter spp. , Mycobacterium tuberculosis ХОБЛ и / или курение Haemophilus influenzae, Pseudomonas aeruginosa, Legionella spp. , S. pneumoniae, Moraxella catarrhalis, Chlamydophila pneumonia Аспирация Грамотрицательные микроорганизмы кишки, анаэробы ротовой полости Абсцесс легкого Внебольничный метициллинорезистентный Staphylococcus aureus (MRSA), анаэробы ротовой полости, эндемичные грибы, M. Tuberculosis, атипичные микобактерии Контакт с экскрементами летучих мышей Histoplasma capsulatum Контакт с птицами Chlamydophila psittaci (при контакте с домашней птицей – птичий грипп) Контакт с грызунами Контакт с сельскохозяйственными животными или кошками Francisella tularensis Coxiella burnetti (лихорадка Q) ВИЧ-инфицированные (ранние стадии) S. pneumonia, H. Influenzae, M. tuberculosis ВИЧ-инфицированные (поздние стадии) Возбудители, характерные для ранних стадий, а также Pneumocystis jirovecii, Cryptococcus, Histoplasma, Aspergillus, атипичные микобактерии (особенно Mycobacterium kansasii), P. aeruginosa, H. influenzae Пребывание в гостинице или в круизе на теплоходе в предшествующие заболеванию 2 недели Legionella spp. Поездки в юго-западные районы США или проживание там Coccidioides spp. , Hantavirus Поездки в Юго-Восточную или Восточную Азию или Burkholderia pseudomallei, птичий грипп, тяжелый острый респираторный синдром (ТОРС) проживание там Вспышка гриппа Вирусы гриппа А и В, S. pneumonia, S. aureus, H. Influenzae Кашель > 2 недель со стридором или рвотой после кашлевых пароксизмов Bordetella pertussis Структурные изменения легких (например, бронхоэктазы) P. aeruginosa, Burkholderia cepacia, S. aureus Внутривенная наркомания Эндобронхиальная обструкция S. aureus, анаэробы, M. tuberculosis, S. pneumoniae Анаэробы, S. pneumoniae, H. influenzae, S. aureus Биотерроризм Bacillus anthracis (сибирская язва), Yersinia pestis (чума), Francisella tularensis (туляремия)

Нозокомиальная (госпитальная, внутрибольничная) пневмония заболевание, характеризующееся появлением на рентгенограмме «свежих» очагово-инфильтративных изменений в легких спустя 48 ч и более после госпитализации в сочетании с клиническими данными, подтверждающими их инфекционную природу (новая волна лихорадки, гнойная мокрота или гнойное отделяемое трахеобронхиального дерева, лейкоцитоз и пр. ), при исключении инфекций, которые находились в инкубационном периоде на момент поступления больного в стационар.

Эпидемиология • 5 -10 случаев на 1000 госпитализированных • У пациентов на ИВЛ риск НП выше в 20 раз • Летальность при НП колеблется от 30 до 71%

Этиология НП

Этиология НП • Энтеробактерии (Klebsiela pneumonia, Escherichia coli, Enterobacter spp. )

Этиология НП • Энтеробактерии (Klebsiela pneumonia, Escherichia coli, Enterobacter spp. ) • Неферментирующие грам(-) бактерии (P. aeruginosa, Acinetobacter spp. )

Этиология НП • Энтеробактерии (Klebsiela pneumonia, Escherichia coli, Enterobacter spp. ) • Неферментирующие грам(-) бактерии (P. aeruginosa, Acinetobacter spp. ) • Грам(+) кокки (S. aureus, Streptococcus pneumoniae)
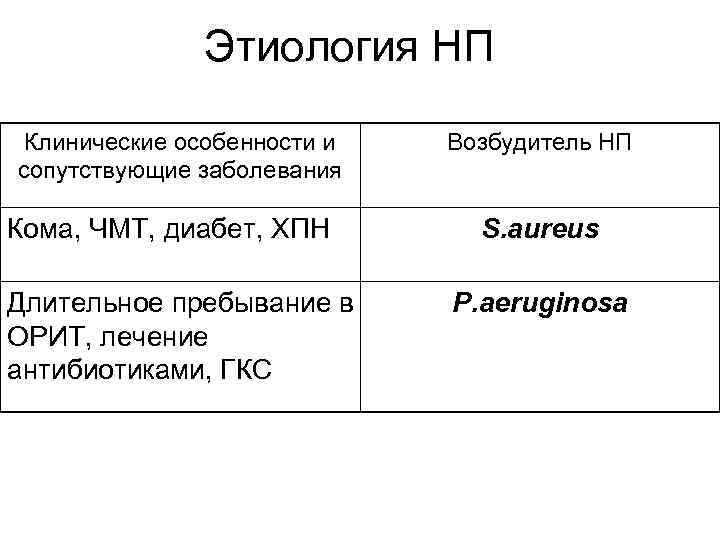
Этиология НП Клинические особенности и сопутствующие заболевания Кома, ЧМТ, диабет, ХПН Длительное пребывание в ОРИТ, лечение антибиотиками, ГКС Возбудитель НП S. aureus P. aeruginosa

Патогенез • Аспирация секрета ротоглотки • Вдыхание аэрозоля, содержащего микроорганизмы • Гематогенное распространение инфекции из внелегочного очага • Непосредственное распространение из соседних пораженных органов

Патогенез В 1 мл слюны содержится до 1 млрд. бактерий, поэтому аспирация даже одной капли слюны может внести в дыхательные пути большое количество микроорганизмов.

Патогенез Пневмококки различных серотипов могут бессимптомно персистировать на слизистых оболочках полости рта и верхних дыхательных путей. Проникновению их в дистальные отделы респираторного тракта препятствуют защитные структуры организма: • лимфоидные миндалины, • бактерицидные свойства слюны и носовой слизи, • мукоцилиарный аппарат трахеобронхиального дерева, • фагоцитарная активность нейтрофилов и альвеолярных макрофагов, • гуморальные факторы бронхиального секрета (иммуноглобулины А и G, система комплемента, лизоцим, интерферон, лактоферрин, ингибиторы протеаз).

Патогенез Ведущее значение в патогенезе пневмоний приобретают факторы, нарушающие динамическое равновесие между макро- и микроорганизмами. К таким неблагоприятным обстоятельствам относятся (эпидемиологический анамнез): • переохлаждение (расстройства микроциркуляции и нарушение мукоцилиарного клиренса), • острые респираторные заболевания (угнетение системы местных защитных факторов), • переутомление, • гиповитаминоз, • стрессовые ситуации, • десинхронозы • другие факторы, нарушающие резистентность организма
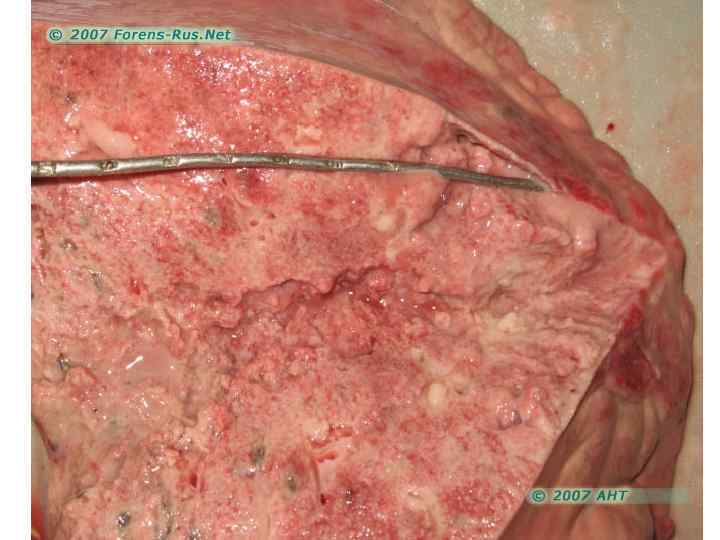
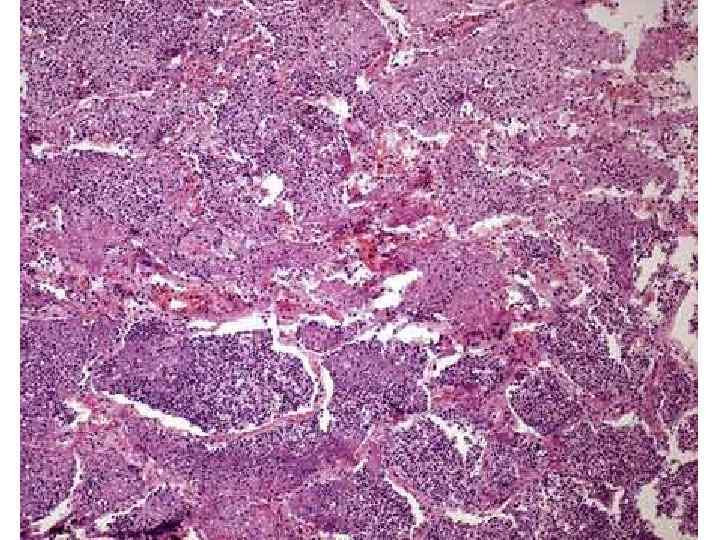
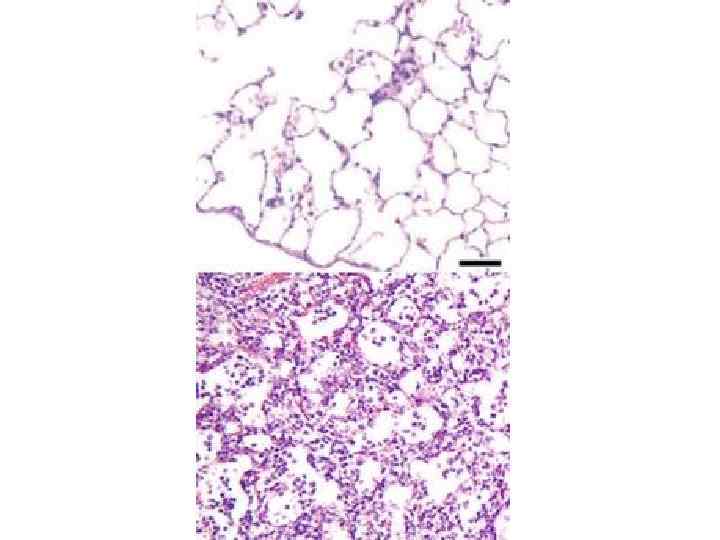

Клиника пневмоний • Легочные проявления • Внелегочные проявления

Клиника пневмоний • Легочные проявления • одышка; • кашель; • выделение мокроты (слизистая, слизисто-гнойная, «ржавая» и т. д. ); • боли при глубоком дыхании; • локальные клинические признаки (притупление перкуторного звука, бронхиальное дыхание, крепитация, шум трения плевры); • локальные рентгенологические признаки • Внелегочные проявления

Клиника пневмоний • Легочные проявления • Внелегочные проявления • • • лихорадка; ознобы и потливость; миалгии; головная боль; цианоз; тахикардия; herpes labialis; кожная сыпь, поражения слизистых (конъюнктивит); спутанность сознания; диарея; желтуха; изменения со стороны периферической крови (лейкоцитоз, сдвиг формулы влево, токсическая зернистость нейтрофилов, повышение СОЭ).

Критерии диагноза • Рентгенологически подтвержденная очаговая инфильтрация легочной ткани • Плюс хотя бы 2 клинических признака: – Острая лихорадка в начале заболевания (to>38, 0 o. C) – Кашель с мокротой – Физические признаки (укорочение перкуторного звука, жесткое везикулярное или бронхиальное дыхание, фокус крепитации и/или мелкопузырчатые хрипы) – Лейкоцитоз > 10 х 109/л и/или палочкоядерный сдвиг (>10%) Чучалин А. Г. , 2010

Критерии диагноза Диагноз ВП является определенным при наличии у больного рентгенологически подтвержденной очаговой инфильтрации легочной ткани и, по крайней мере, двух клинических признаков из числа следующих: а) острая лихорадка в начале заболевания (t 0 > 38, 0°С); б) кашель с мокротой; в) физические признаки (фокус крепитации и/или мелкопузырчатые хрипы, жесткое бронхиальное дыхание, укорочение перкуторного звука); г) лейкоцитоз > 10· 109/л и/или палочкоядерный сдвиг (> 10%). В этой связи следует по возможности стремиться к клинико-рентгенологическому подтверждению диагноза ВП. При этом необходимо учитывать и вероятность известных синдромосходных заболеваний/патологических состояний.

Критерии диагноза Отсутствие или недоступность рентгенологического подтверждения очаговой инфильтрации в легких (рентгенография или крупнокадровая флюорография органов грудной клетки) делает диагноз ВП неточным/неопределенным. При этом диагноз заболевания основывается на учете данных эпидемиологического анамнеза, жалоб и соответствующих локальных симптомов.

Критерии диагноза Если при обследовании пациента с лихорадкой, жалобами на кашель, одышку, отделение мокроты и/или боли в грудной клетке рентгенологическое исследование оказывается недоступным и отсутствует соответствующая локальная симптоматика (укорочение/тупость перкуторного звука над пораженным участком легкого, локально выслушиваемое бронхиальное дыхание, фокус звучных мелкопузырчатых хрипов или инспираторной крепитации, усиление бронхофонии и голосового дрожания), то предположение о ВП становится маловероятным.

Ключевые клинические проявления современной ВП (Чучалин А. Г. , 2006): • В большинстве случаев клинико-рентгенологическая картина заболевания не позволяет судить о вероятном возбудителе ВП. Поэтому разделение ВП на «типичную» (например, пневмококковую) и «атипичную» (микоплазменную или хламидийную) лишено особого клинического значения • У части ослабленных больных и пожилых может не быть таких клинических признаков, как острая лихорадка, боль в грудной клетке и др. Клиническая симптоматика в этих случаях может быть представлена утомляемостью, слабостью, тошнотой, анорексией, болями в животе, нарушением сознания. Нередко ВП начинается симптомами декомпенсации сопутствующих заболеваний (например, ХСН) • Поздняя диагностика и задержка с началом антибактериальной терапии более 4 часов у госпитализированных больных ухудшают прогноз ВП. • Плевральный выпот осложняет течение ВП в 10 -25% и не имеет особого значения в предсказании этиологии заболевания. • Появление полостей деструкции в легких не характерно для пневмококковой, микоплазменной и хламидийной ВП, и свидетельствует в пользу стафилококковой инфекции, аэробных грамотрицательных бактерий и анаэробов. • Ретикулонодулярная инфильтрация в базальных отделах легких характерна для микоплазменной ВП.
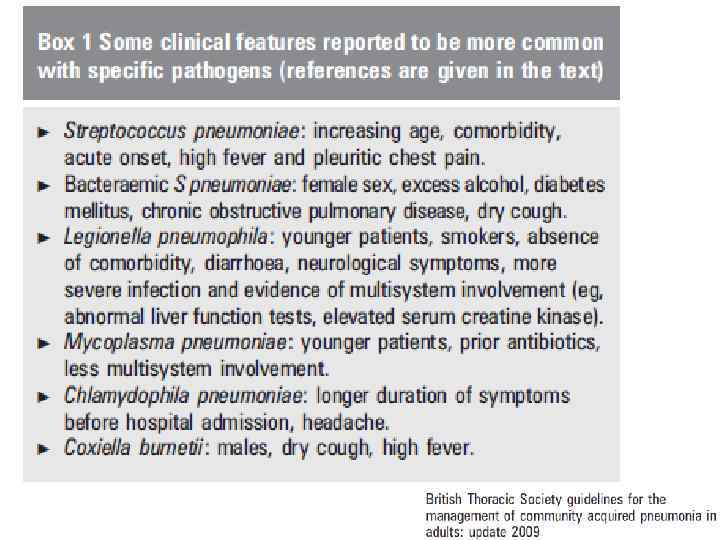

Пневмококк: повышение возраста, сопутствующие заболевания, острое начало, высокая температура и плевральная боль. Бактериемия пневмококковая: женский пол, злоупотребление алкоголем, диабет, хроническая обструктивная болезнь легких, сухой кашель. Легионелла: молодые пациенты, курильщики, отсутствие сопутствующей патологии, понос, неврологическая симптоматика, более тяжелый инфекционный процесс и полиорганное поражение (например, нарушение функции печени, повышенный уровень креатинкиназы). Микоплазма: молодые пациенты, предшествующий прием антибиотиков, меньше мультисистемного участия. Хламидофила: большая продолжительность симптомов до госпитализации, головная боль. Q лихорадка: мужчины, сухой кашель, высокая температура.
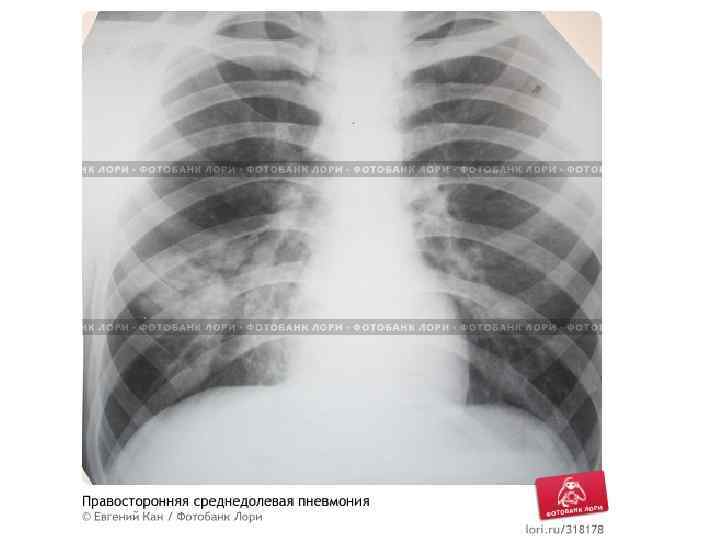
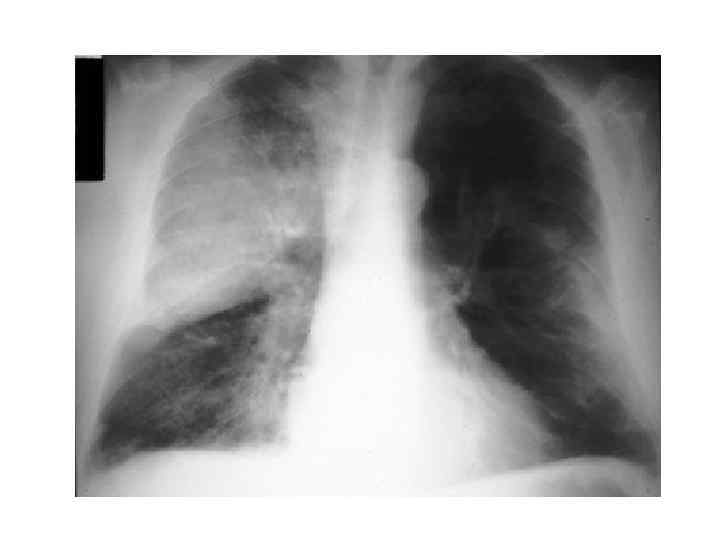
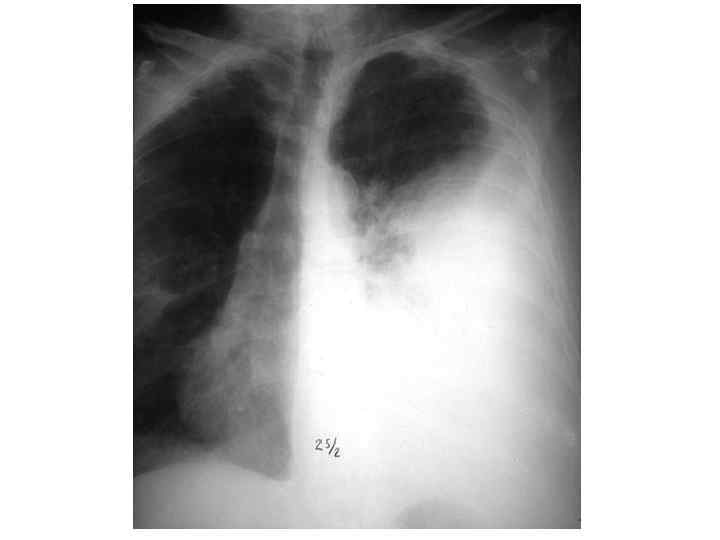
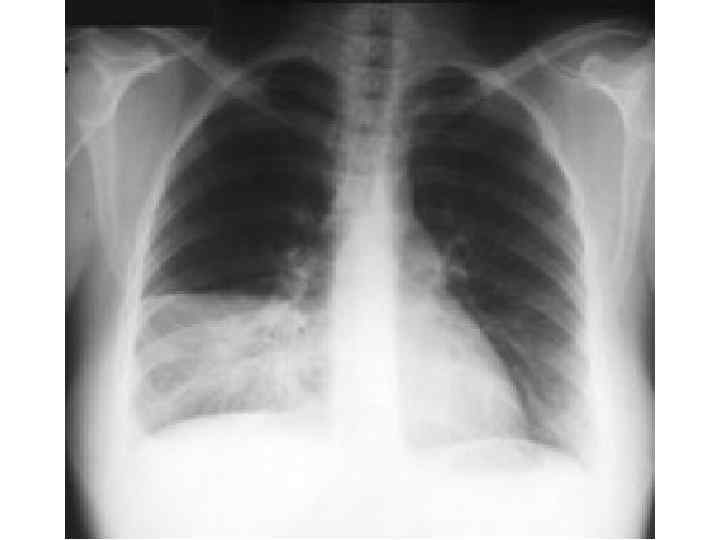
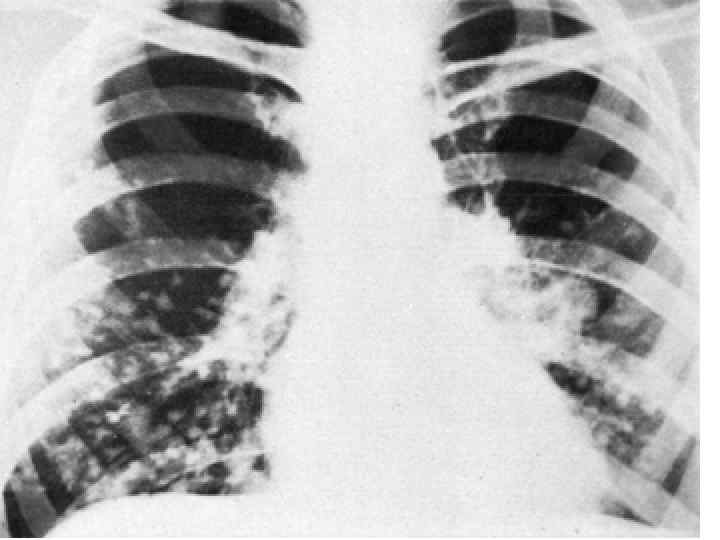
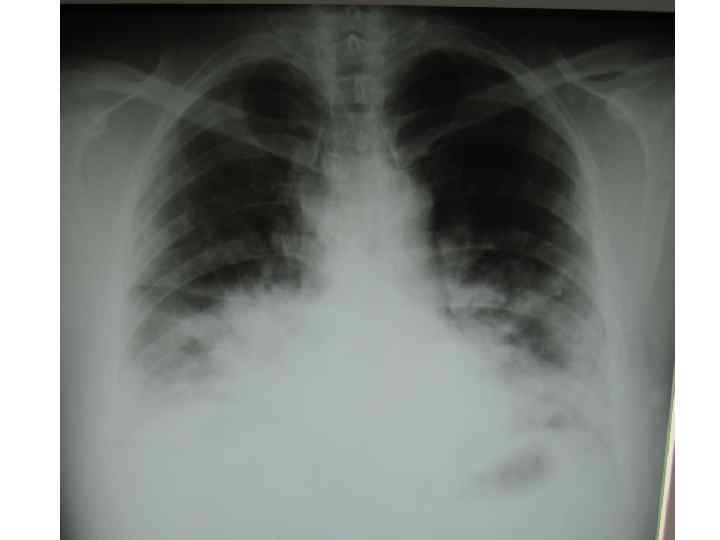
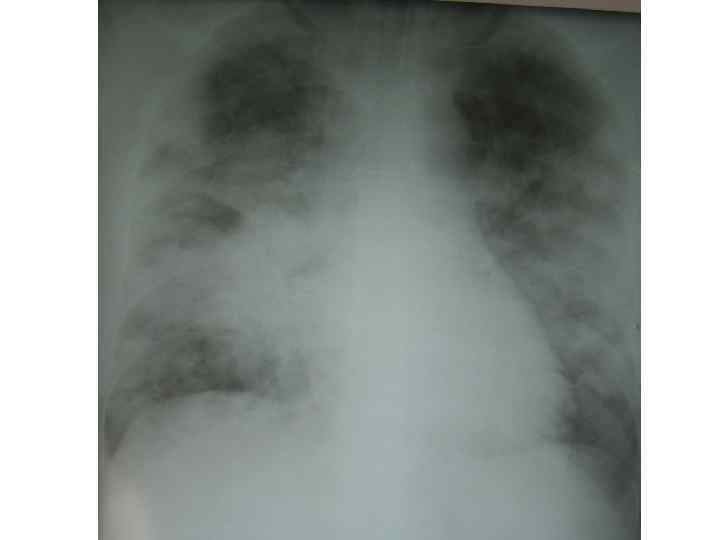
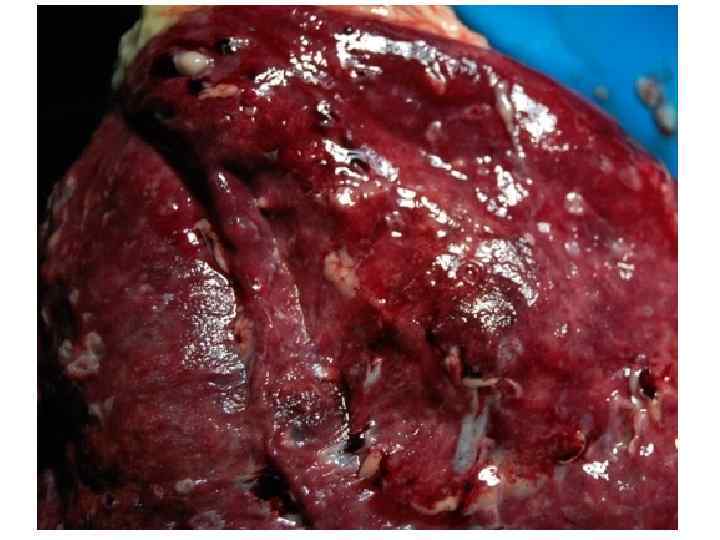
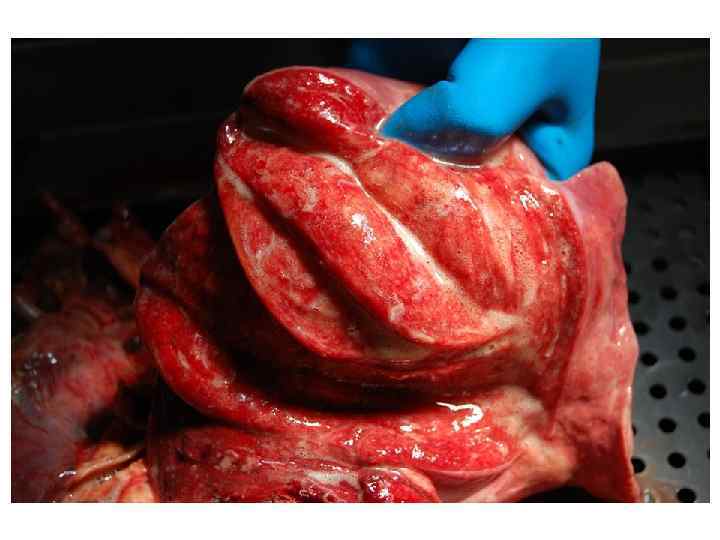
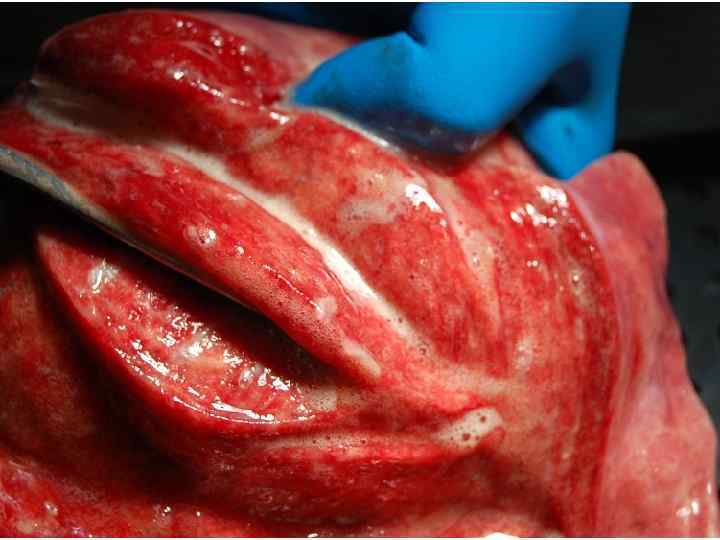


Epidemiological report of pandemic (H 1 N 1) 2009 in the UK; April 2009 – May 2010

Параллельные бактериальные инфекции 1. Параллельные бактериальные инфекции (ПБИ) не были определены в качестве одной из главных особенностей пандемии. 2. Среди 20288 случаев английской пандемии гриппа (H 1 N 1) в общей сложности 76 связаны с ПБИ (0, 4%). 3. Среди инфекционных агентов были определены: • 39 случаев S. pneumoniae, • 34 случаев S. aureus, • 3 случая S. pyogenes. 4. 24 больных из этих случаев, связанных с ПБИ (0, 9%), были госпитализированы, и 16 (67%) закончились смертельным исходом. Epidemiological report of pandemic (H 1 N 1) 2009 in the UK; April 2009 – May 2010

Критерии тяжелого течения Клинические Лабораторные • Острая дыхательная недостаточность (ЧДД≥ 30 в мин) • Гипотензия (АДсист<90 мм рт. ст. ) • Двух- и многодолевое поражение • Нарушение сознания • Внелегочный очаг инфекции • Лейкопения (< 4 х 109/л) • Гипоксемия (Sa. O 2<90%, PO 2<60 мм рт. ст. ) • Гемоглобин < 100 г/л • Гематокрит < 30% • Острая почечная недостаточность (анурия, мочевина > 7, 0 ммоль/л) При наличии хотя бы одного критерия пневмония расценивается как тяжеля!

Критерии тяжести ВП При поступлении пациента с ВП в стационар необходимо, прежде всего, оценить тяжесть его состояния и решить вопрос о месте лечения (амбулаторно, стационарно в отделении общего профиля или ОРИТ). Для отбора больных ВП, которые могут лечиться амбулаторно, рекомендуется использовать шкалы определения тяжести ВП, такие как критерии Британского торакального общества (CURB-65) либо Американские критерии Pneumonia Severe Index – PSI. Оценка неблагоприятного исхода по шкале CURB-65: 1) Нарушение сознания (Confusion) 2) уровень мочевины крови > 7 ммоль/л (Urea) 3) частота дыхания ≥ 30 в мин (Respiratory rate) 4) низкое АД (систолическое < 90 мм рт. ст. или диастолическое ≤ 60 мм рт. ст. ) (Blood pressure) 5) возраст ≥ 65 лет (65). Суммарная оценка по шкале CURB-65 в пределах 0 -1 баллов предполагает лечение ВП в амбулаторных условиях, 2 балла – в стационаре в условиях отделения общего профиля, 3 и более баллов – в ОИТ.
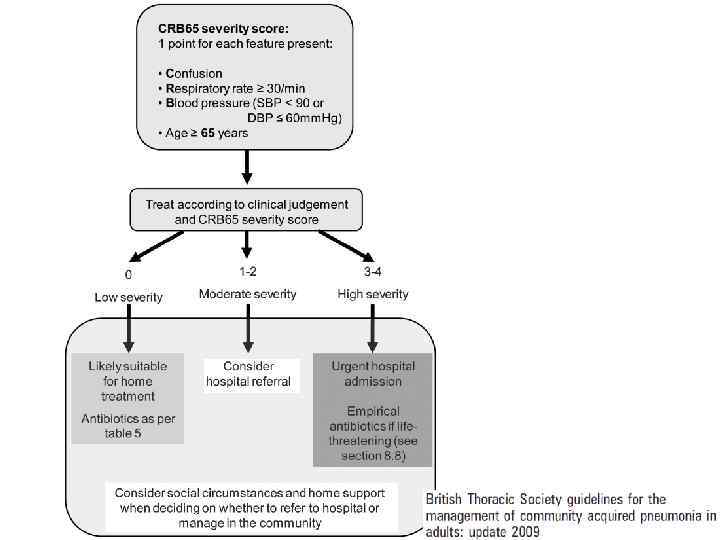
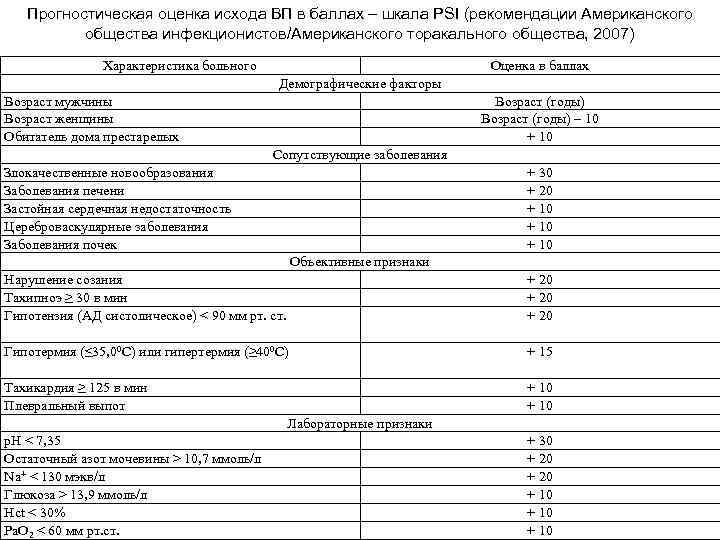
Прогностическая оценка исхода ВП в баллах – шкала PSI (рекомендации Американского общества инфекционистов/Американского торакального общества, 2007) Характеристика больного Оценка в баллах Демографические факторы Возраст мужчины Возраст женщины Обитатель дома престарелых Возраст (годы) – 10 + 10 Сопутствующие заболевания Злокачественные новообразования Заболевания печени Застойная сердечная недостаточность Цереброваскулярные заболевания Заболевания почек + 30 + 20 + 10 Объективные признаки Нарушение созания Тахипноэ ≥ 30 в мин Гипотензия (АД систолическое) < 90 мм рт. ст. + 20 Гипотермия (≤ 35, 00 С) или гипертермия (≥ 400 С) + 15 Тахикардия ≥ 125 в мин Плевральный выпот + 10 Лабораторные признаки p. H < 7, 35 Остаточный азот мочевины > 10, 7 ммоль/л Na+ < 130 мэкв/л Глюкоза > 13, 9 ммоль/л Hct < 30% Pa. O 2 < 60 мм рт. ст. + 30 + 20 + 10
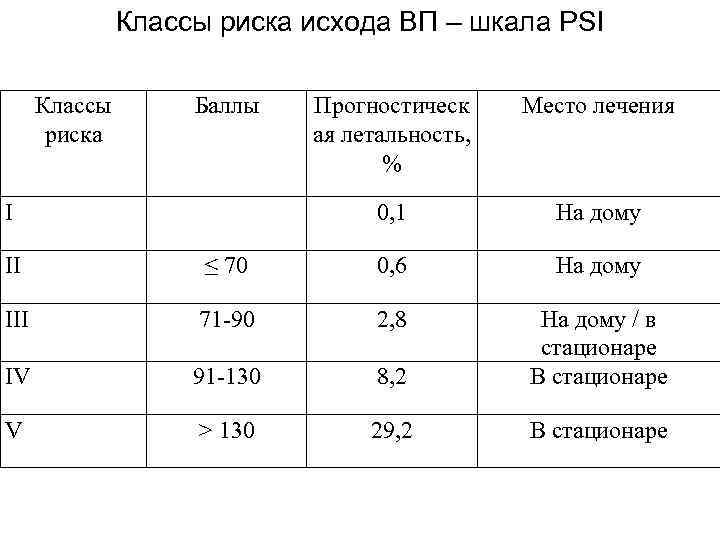
Классы риска исхода ВП – шкала PSI Классы риска Баллы Место лечения 0, 1 I Прогностическ ая летальность, % На дому II ≤ 70 0, 6 На дому III 71 -90 2, 8 IV 91 -130 8, 2 На дому / в стационаре В стационаре V > 130 29, 2 В стационаре
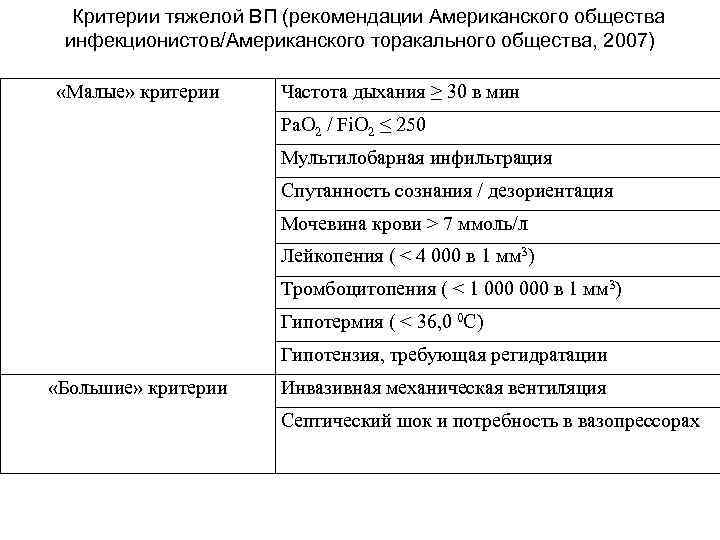
Критерии тяжелой ВП (рекомендации Американского общества инфекционистов/Американского торакального общества, 2007) «Малые» критерии Частота дыхания ≥ 30 в мин Pa. O 2 / Fi. O 2 ≤ 250 Мультилобарная инфильтрация Спутанность сознания / дезориентация Мочевина крови > 7 ммоль/л Лейкопения ( < 4 000 в 1 мм 3) Тромбоцитопения ( < 1 000 в 1 мм 3) Гипотермия ( < 36, 0 0 С) Гипотензия, требующая регидратации «Большие» критерии Инвазивная механическая вентиляция Септический шок и потребность в вазопрессорах

Тяжелая внебольничная пневмония Это особая форма заболевания различной этиологии, проявляющаяся выраженной дыхательной недостаточностью и/или признаками тяжелого сепсиса или септического шока, характеризуется плохим прогнозом и требует проведения интенсивного лечения

Наиболее распространенные возбудители ВП (рекомендации Американского общества инфекционистов/Американского торакального общества, 2007) Пациенты Возбудители Амбулаторные Streptococcus pneumonia Mycoplasma pneumonia Haemophilus influenza Moraxella catarrhalis Chlamydophila pneumonia Госпитализированные в стационар (не в S. pneuminiae ОИТ) M. pneumoniae C. pneumoniae H. influenzae Legionella spp. Госпитализированные в ОИТ S. pneumoniae Staphylococcus aureus Legionella spp. Грамотрицательные палочки H. influenzae
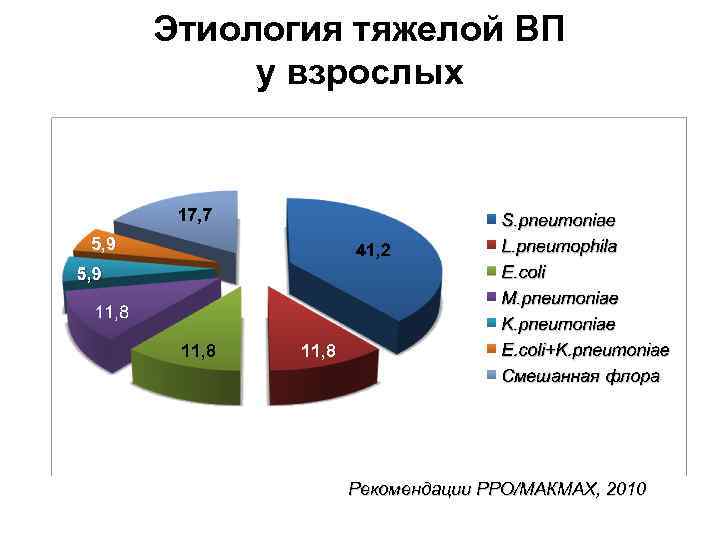
Этиология тяжелой ВП у взрослых 5, 9 11, 8 Рекомендации РРО/МАКМАХ, 2010

Лечение • Этиотропное • Незамедлительное (в течение первых 4 -х часов) • Деэскалационное • Ступенчатое
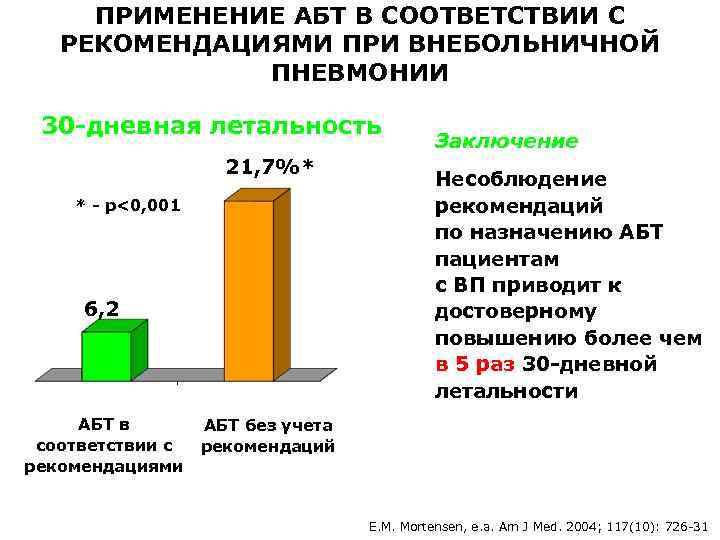
ПРИМЕНЕНИЕ АБТ В СООТВЕТСТВИИ С РЕКОМЕНДАЦИЯМИ ПРИ ВНЕБОЛЬНИЧНОЙ ПНЕВМОНИИ 30 -дневная летальность 21, 7%* * - р<0, 001 6, 2% АБТ в соответствии с рекомендациями Заключение Несоблюдение рекомендаций по назначению АБТ пациентам с ВП приводит к достоверному повышению более чем в 5 раз 30 -дневной летальности АБТ без учета рекомендаций E. M. Mortensen, е. а. Am J Med. 2004; 117(10): 726 -31

Эмпирическая антибактериальная терапия антибиотиком широкого спектра действия с последующей де-эскалацией не приводит к селекции резистентности у грам(-) патогенов у пациентов с вентиляторассоциированной пневмонией Опубликовано: Пятница, 17 сентября 2010 г. - 09: 05 Приверженность тактике де-эксалации (т. е. смена антибактериальной терапии с учётом выделенных патогенов в течение 96 ч) составила 78% для имипенема/циластатина, 77, 2% для тобрамицина и 59% для левофлоксацина. Когда инфекционные заболевания, потребовавшие назначения имипенема/циластатина, были удалены из анализа, комплаентность увеличилась до 92%. Таким образом, ранее начало эмпирической антибактериальной терапии антибиотиком широкого спектра действия с последующей сменой на антибиотик узкого спектра действия в соответствии с выделенным бактериальным возбудителем не приводит к росту антибиотикорезистентности и является обоснованной тактикой ведения пациентов. Hibbard M. L. , Kopelman T. R. , O'Neill P. J. , Maly T. J. , Matthews M. R. , Cox J. C. , Vail S. J. , Quan A. N. , Drachman D. A. Empiric, Broad-Spectrum Antibiotic Therapy with an Aggressive De. Escalation Strategy Does Not Induce Gram-Negative Pathogen Resistance in Ventilator. Associated Pneumonia. Surg Infect (Larchmt). 2010 Sep 6
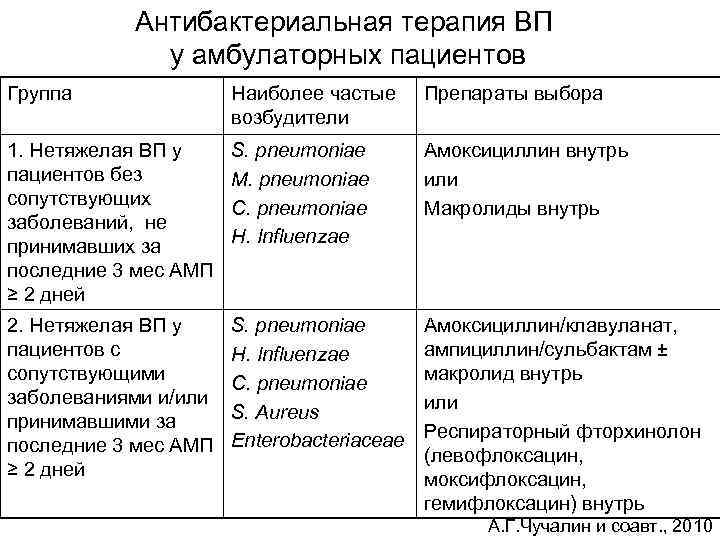
Антибактериальная терапия ВП у амбулаторных пациентов Группа Наиболее частые возбудители Препараты выбора 1. Нетяжелая ВП у пациентов без сопутствующих заболеваний, не принимавших за последние 3 мес АМП ≥ 2 дней S. pneumoniae M. pneumoniae C. pneumoniae H. Influenzae Амоксициллин внутрь или Макролиды внутрь 2. Нетяжелая ВП у пациентов с сопутствующими заболеваниями и/или принимавшими за последние 3 мес АМП ≥ 2 дней S. pneumoniae H. Influenzae C. pneumoniae S. Aureus Enterobacteriaceae Амоксициллин/клавуланат, ампициллин/сульбактам ± макролид внутрь или Респираторный фторхинолон (левофлоксацин, моксифлоксацин, гемифлоксацин) внутрь А. Г. Чучалин и соавт. , 2010
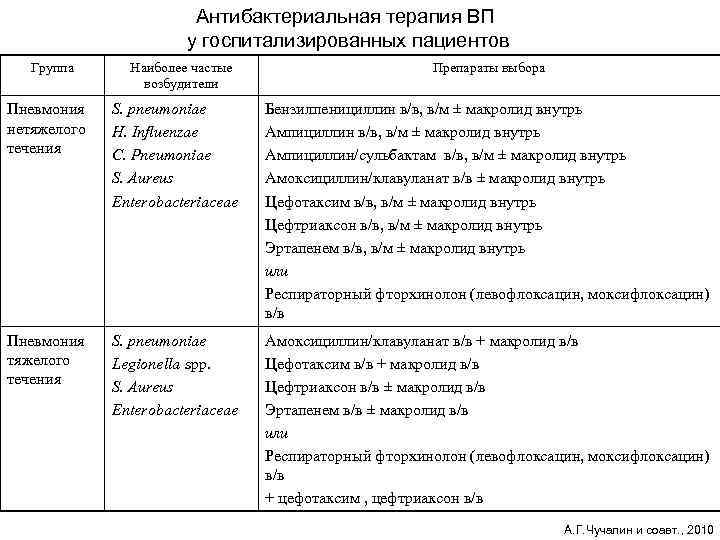
Антибактериальная терапия ВП у госпитализированных пациентов Группа Наиболее частые возбудители Препараты выбора Пневмония нетяжелого течения S. pneumoniae H. Influenzae C. Pneumoniae S. Aureus Enterobacteriaceae Бензилпенициллин в/в, в/м ± макролид внутрь Ампициллин/сульбактам в/в, в/м ± макролид внутрь Амоксициллин/клавуланат в/в ± макролид внутрь Цефотаксим в/в, в/м ± макролид внутрь Цефтриаксон в/в, в/м ± макролид внутрь Эртапенем в/в, в/м ± макролид внутрь или Респираторный фторхинолон (левофлоксацин, моксифлоксацин) в/в Пневмония тяжелого течения S. pneumoniae Legionella spp. S. Aureus Enterobacteriaceae Амоксициллин/клавуланат в/в + макролид в/в Цефотаксим в/в + макролид в/в Цефтриаксон в/в ± макролид в/в Эртапенем в/в ± макролид в/в или Респираторный фторхинолон (левофлоксацин, моксифлоксацин) в/в + цефотаксим , цефтриаксон в/в А. Г. Чучалин и соавт. , 2010
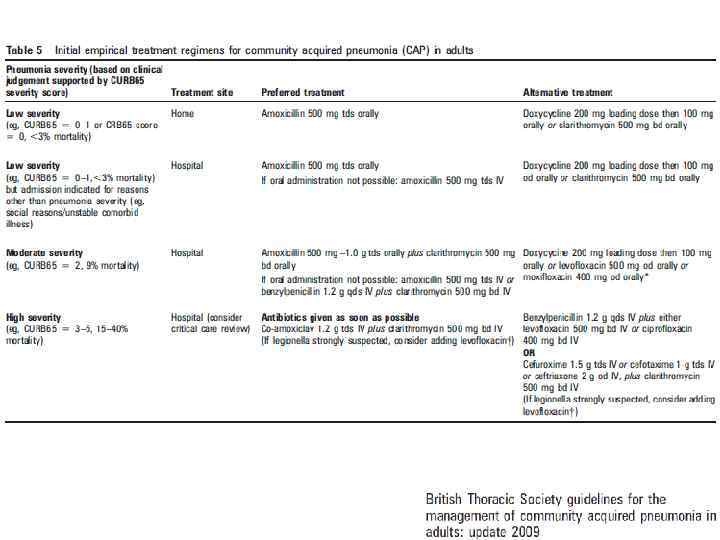
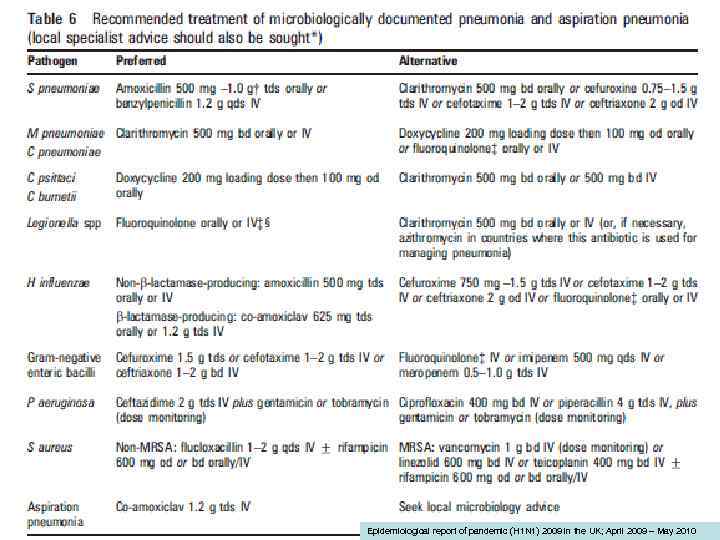
Epidemiological report of pandemic (H 1 N 1) 2009 in the UK; April 2009 – May 2010

В последнее время наблюдается рост числа ВП, вызываемых внебольничными штаммами MRSA. Продукция данным возбудителем лейкоцидина Panton-Valentine и других токсинов обусловливает развитие осложнений пневмонии (деструкция / абсцедирование легочной ткани, эмпиема плевры, шок, дыхательная недостаточность). Предположение о внебольничном MRSA следует допускать у больных с абсцедированием легочных инфильтратов при отсутствии факторов риска аспирационной пневмонии (злоупотребление алкоголем, нарушение моторики пищевода, нарушение сознания, инсульт, заболевания десен)

Epidemiological report of pandemic (H 1 N 1) 2009 in the UK; April 2009 – May 2010

Критерии достаточности антибактериальной терапии ВП • Температура < 37, 5 о. С • Отсутствие интоксикации • Отсутствие дыхательной недостаточности (ЧДД<20 в мин) • Отсутствие гнойной мокроты • Количество лейкоцитов в крови <10 х 109/л • Отсутствие отрицательной динамики на рентгенограмме

Индикаторы качества клинической работы с госпитализированным больным ВП (Чучалин А. Г. и др. , 2010): 1. Рентгенологическое исследование органов грудной клетки при наличии клинических признаков ВП в течение 24 ч с момента госпитализации (если не выполнялось на амбулаторном этапе). 2. Бактериологическое исследование мокроты до назначения антибиотиков. 3. Бактериологическое исследование крови до назначения антибиотиков (у пациентов с тяжелой ВП). 4. Введение первой дозы системного антибиотика в первые 4 ч с момента госпитализации. 5. Соответствие стартового режима антибактериальной терапии национальным рекомендациям. 6. Использование ступенчатой антибактериальной терапии (для пациентов, нуждающихся в парентеральном назначении антибиотиков). 7. Наличие рекомендаций по вакцинации пненвмококковой вакциной пациентам из группы риска. 8. Наличие рекомендаций по вакцинации гриппозной вакциной (в осеннезимний сезон) пациентам из группы риска.
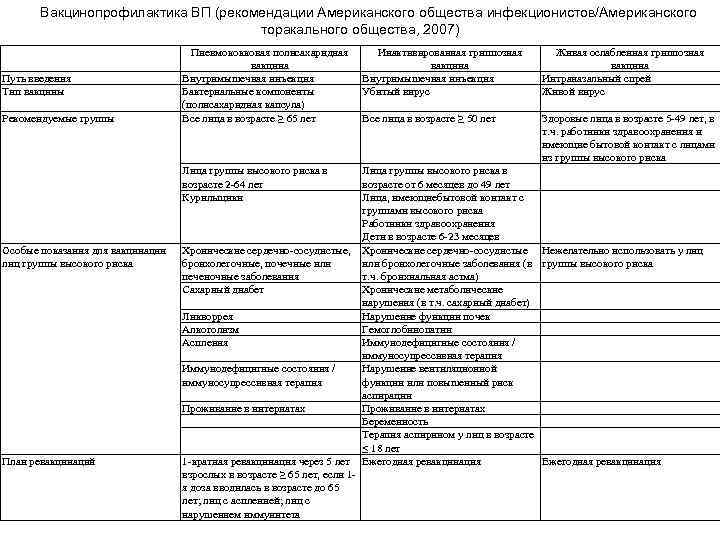
Вакцинопрофилактика ВП (рекомендации Американского общества инфекционистов/Американского торакального общества, 2007) Путь введения Тип вакцины Рекомендуемые группы Пневмококковая полисахаридная вакцина Внутримышечная инъекция Бактериальные компоненты (полисахаридная капсула) Все лица в возрасте ≥ 65 лет Лица группы высокого риска в возрасте 2 -64 лет Курильщики Особые показания для вакцинации лиц группы высокого риска План ревакцинаций Инактивированная гриппозная вакцина Внутримышечная инъекция Убитый вирус Живая ослабленная гриппозная вакцина Интраназальный спрей Живой вирус Все лица в возрасте ≥ 50 лет Здоровые лица в возрасте 5 -49 лет, в т. ч. работники здравоохранения и имеющие бытовой контакт с лицами из группы высокого риска Лица группы высокого риска в возрасте от 6 месяцев до 49 лет Лица, имеющиебытовой контакт с группами высокого риска Работники здравоохранения Дети в возрасте 6 -23 месяцев Хронические сердечно-сосудистые, Хронические сердечно-сосудистые Нежелательно использовать у лиц бронхолегочные, почечные или бронхолегочные заболевания (в группы высокого риска печеночные заболевания т. ч. бронхиальная астма) Сахарный диабет Хронические метаболические нарушения (в т. ч. сахарный диабет) Ликворрея Нарушение функции почек Алкоголизм Гемоглобинопатии Аспления Иммунодефицитные состояния / иммуносупрессивная терапия Иммунодефицитные состояния / Нарушение вентиляционной иммуносупрессивная терапия функции или повышенный риск аспирации Проживание в интернатах Беременность Терапия аспирином у лиц в возрасте ≤ 18 лет 1 -кратная ревакцинация через 5 лет Ежегодная ревакцинация взрослых в возрасте ≥ 65 лет, если 1 я доза вводилась в возрасте до 65 лет; лиц с аспленией; лиц с нарушением иммунитета

Streptococcus pneumoniae: Does Antimicrobial Resistance Matter? : Can Pneumococcal Vaccination Reduce Antimicrobial Resistance? • Six serotypes (i. e. , 4, 6 B, 9 V, 14, 19 F, and 23 F) account for > 80% of IPD in children in the United States[380] and > 50% of IPD in adults. [381] These serotypes also account for a majority of IPD in Europe but are less prevalent in developing countries. [380] Vaccination of high-risk patients (both children and adults), reduces the incidence of IPD[382– 385] and nasopharyngeal carriage by vaccine -related serotypes. [386] Importantly, most penicillin- and macrolide-resistant isolates are derived from five serotypes (6 B, 9 V, 14, 19 F, and 23 F), all of which are encompassed by the 23 -valent vaccine[87] and the 7 -valent conjugate vaccine for pediatric use (PCV 7). [381] Vaccination of highrisk patients (both children and adults), reduced the incidence of IPD, [382– 385] otitis media, [387] and nasopharyngeal carriage by vaccine-related serotypes. [386] Studies in the United States noted a marked decline in IPD among children after the introduction of PCV 7, with a smaller but significant decrease among adults. [382, 385] However, the rate of IPD due to nonvaccine serotypes increased among persons ≥ 2 years of age. [385] Further, after the introduction of the PCV 7 in the United States in 2000, colonization with nonvaccine serogroups has increased. [385, 388, 389] The emergence of drug-resistant isolates of serotypes 15[170] and 19 A[171, 172, 390– 392] reflect "replacement" serotypes not encompassed in vaccines. [393] Reductions in carriage of serotypes encompassed within vaccines may be offset by increases in carriage and IPD due to nonsusceptible serotypes not covered by vaccines. [390– 394] The U. S. SENTRY study found that MDR did not decline after the introduction of PCV 7 due to increased prevalence and acquisition of resistant nonvaccine serotypes. [393] Nonvaccine serotypes have acquired MDR at a rate proportional to the serotype replacement process. Joseph P. Lynch, III, M. D. ; George G. Zhanel, Ph. D. Semin Respir Crit Care Med. 2009; 30(2): 210 -238.

Пневмококк: в чем причина резистентности к антимикробным препаратам? Может ли пневмококковая вакцинация снизить резистентность к антимикробным препаратам? • • • Шесть серотипов (4, 6 B, 9 V, 14, 19 F и 23 F) составляет> 80% IPD у детей в США и > 50% ПН у взрослых. Эти серотипы также актуальны для большинства ПН в Европе, но менее распространены в развивающихся странах. Вакцинация пациентов высокого риска (детей и взрослых) снижает заболеваемость ПН и носоглотки за счет связанных с вакцинами серотипов пневмококков. Важно отметить, что наиболее резистентные к пенициллину и макролидам штаммы пневмококков являются производными от пяти серотипов (6 B, 9 V, 14, 19 F и 23 F), все из которых охватывается 23 валентной вакцины и 7 -валентной конъюгированной вакцины для педиатрического использования (PCV 7). Вакцинация пациентов высокого риска (детей и взрослых) привела к снижению заболеваемости ПН и средним отитом за счет пневмококков, связанных с вакцинальными серотипами. Исследования в Соединенные Штаты также отметили заметное снижение ПН среди детей после введения PCV 7, меньшее снижение среди взрослых. Однако, после введение PCV 7 в Соединенных Штатах в 2000 году, колонизация пневмококков невакцинальных серогрупп увеличилась. Появились лекарственноустойчивые штаммы серотипов 15 и 19 А, что отражает "замену" серотипов пневмококков, не входящих в вакцины. Joseph P. Lynch, III, M. D. ; George G. Zhanel, Ph. D. Semin Respir Crit Care Med. 2009; 30(2): 210 -238.
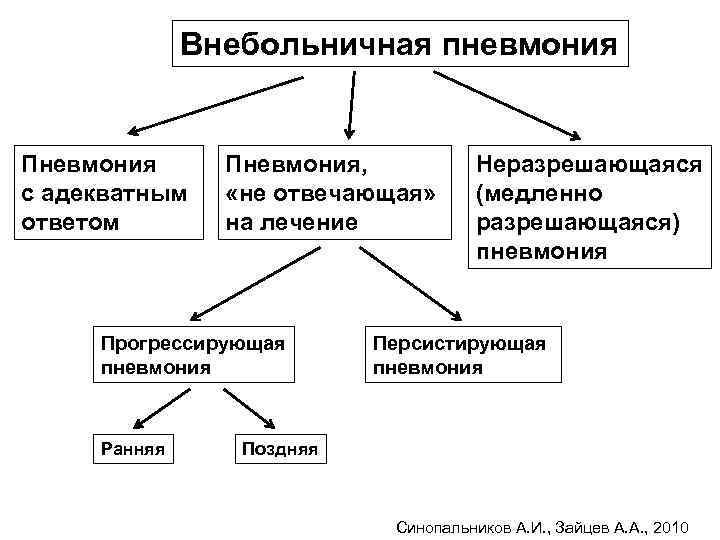
Внебольничная пневмония Пневмония с адекватным ответом Пневмония, «не отвечающая» на лечение Прогрессирующая пневмония Ранняя Неразрешающаяся (медленно разрешающаяся) пневмония Персистирующая пневмония Поздняя Синопальников А. И. , Зайцев А. А. , 2010

Неразрешающаяся (медленно разрешающаяся) пневмония

Неразрешающаяся (медленно разрешающаяся) пневмония – это такой вариант течения ВП, когда на фоне улучшения клинической картины к исходу 4 -й недели от начала заболевания не удается достичь полного рентгенологического разрешения очагово-инфильтративных изменений в легких (Чучалин А. Г. , 2010).

Неразрешающаяся (медленно разрешающаяся) пневмония – это медленный регресс рентгенологических изменений у иммунокомпетентных больных, характеризующийся уменьшением размеров пневмонической инфильтрации менее чем на 50% к исходу 2 -й недели заболевания и неполным разрешением к исходу 4 -й недели от начала заболевания при улучшении клинической картины (снижение температуры и др. ) на фоне проводимой антибактериальной терапии (Kirtland S. H. , Winterbauer R. H. , 1991).

Необходимо подчеркнуть, что у большинства больных ВП к концу 3 -5 суток от начала потенциально эффективной антибактериальной терапии нормализуется температура и регрессируют другие клинические проявления заболевания. При этом рентгенологическая картина выздоровления часто отстает от клинической.

Факторы риска затяжного течения ВП: 1. Возраст старше 55 лет. 2. Алкоголизм. 3. Наличие сопутствующих инвалидизирующих заболеваний (ХОБЛ, ХСН, ХПН, СД, онкопатология и др. ) 4. Тяжелое течение самой ВП. 5. Мультилобарная инфильтрация. 6. Высоковирулентные возбудители заболевания (L. pneumophila, S. Aureus, грамотрицательные энтеробактерии). 7. Курение. 8. Клиническая неэффективность стартовой терапии (сохраняющийся лейкоцитоз и лихорадка). 9. Вторичная бактериемия.

Важное значение имеет дифференциальная диагностика ВП затяжного течения с очаговоинфильтративным туберкулезом легких.
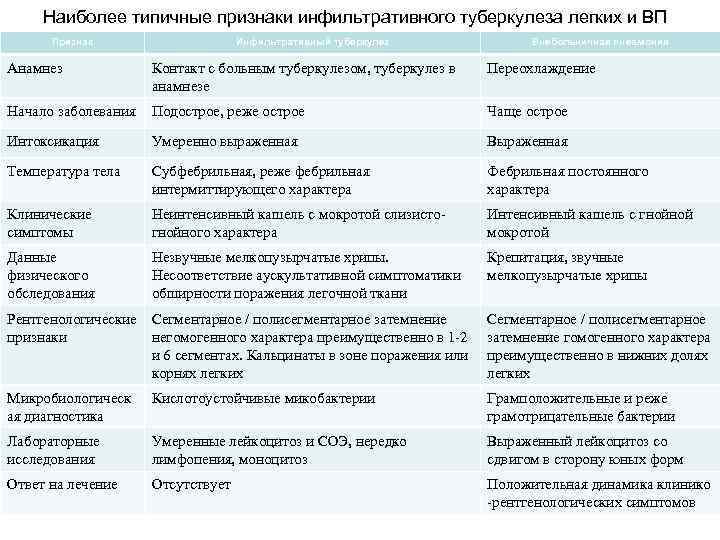
Наиболее типичные признаки инфильтративного туберкулеза легких и ВП Признак Инфильтративный туберкулез Внебольничная пневмония Анамнез Контакт с больным туберкулезом, туберкулез в анамнезе Переохлаждение Начало заболевания Подострое, реже острое Чаще острое Интоксикация Умеренно выраженная Выраженная Температура тела Субфебрильная, реже фебрильная интермиттирующего характера Фебрильная постоянного характера Клинические симптомы Неинтенсивный кашель с мокротой слизистогнойного характера Интенсивный кашель с гнойной мокротой Данные физического обследования Незвучные мелкопузырчатые хрипы. Несоответствие аускультативной симптоматики обширности поражения легочной ткани Крепитация, звучные мелкопузырчатые хрипы Рентгенологические Сегментарное / полисегментарное затемнение признаки негомогенного характера преимущественно в 1 -2 и 6 сегментах. Кальцинаты в зоне поражения или корнях легких Сегментарное / полисегментарное затемнение гомогенного характера преимущественно в нижних долях легких Микробиологическ ая диагностика Кислотоустойчивые микобактерии Грамположительные и реже грамотрицательные бактерии Лабораторные исследования Умеренные лейкоцитоз и СОЭ, нередко лимфопения, моноцитоз Выраженный лейкоцитоз со сдвигом в сторону юных форм Ответ на лечение Отсутствует Положительная динамика клинико -рентгенологических симптомов

Следует иметь в виду широкий круг неинфекционных заболеваний, напоминающих пневмонию и создающих в этой связи известные дифференциально-диагностические трудности:

Новообразования: А. Первичный рак легкого (особенно пневмотическая форма бронхиолоальвеолярного рака). Б. Эндобронхиальные метастазы. В. Аденома бронха. Г. Лимфома Тромбоэмболия легочной артерии и инфаркт легкого Иммунопатологические заболевания: А. Системные васкулиты. Б. Волчаночный пневмонит. В. Аллергический бронхолегочный аспергиллез. Г. Облитерирующий бронхиолит с организующейся пневмонией. Д. Идиопатический легочный фиброз. Е. Эозинофильная пневмония. Ж. Бронхоцентрический гранулематоз. Прочие заболевания/патологические состояния: А. Застойная сердечная недостаточность. Б. Лекарственная (токсическая) пневмопатия. В. Аспирация инородного тела. Г. Саркоидоз. Д. Легочный альвеолярный протеиноз. Е. Липоидная пневмония. Ж. Округлый ателектаз.

Пневмония, «не отвечающая» на лечение

Пневмония, «не отвечающая» на лечение – это такие клинические ситуации, при которых, несмотря на проводимую антибактериальную терапию, не наблюдается адекватный клинический ответ.

Пневмония, «не отвечающая» на лечение Варианты: 1. Прогрессирующая пневмония А. Ранняя - прогрессирование заболевания в первые 72 часа от начала лечения Б. Поздняя - прогрессирование заболевания спустя 72 часа от начала лечения) 2. Персистирующая пневмония (отсутствие улучшения спустя 72 часа от начала лечения)

Причины ранней прогрессирующей пневмонии: 1. Исходно тяжелое течение заболевания 2. Антибиотикорезистентность возбудителей ВП 3. Осложнения ВП (парапневмонический плеврит или эмпиема плевры) и внелегочные очаги инфекции (эндокардит, менингит, артрит) 4. Ошибочный диагноз (ТЭЛА, эндокардит трикуспидального клапана, аспирация, ОРДС, васкулит)

Причины поздней прогрессирующей пневмонии: 1. Нозокомиальная суперинфекция (нозокомиальная пневмония, внелегочная инфекция) 2. Обострение сопутствующих заболеваний 3. Неинфекционные причины (ТЭЛА, ИМ , ХПН)

Причины персистирующей пневмонии: 1. Антибиотикорезистентность возбудителей ВП 2. Нозокомиальная суперинфекция 3. Осложнения ВП (парапневмонический плеврит, эмпиема плевры) 4. Неинфекционные причины (облитерирующий бронхиолит с организующейся пневмонией, ТЭЛА, системные васкулиты, СН, лекарственная лихорадка)

Предикторы неэффективности лечения пневмонии: 1. Проживание в домах престарелых 2. Сопутствующие заболевания печени и ЖКТ 3. Лейкопения и гипонатриемия 4. Мультилобарное поражение легочной ткани 5. Осложнения пневмонии (абсцедирование, плевральный выпот) 6. Тяжелое течение заболевания

Классификация пневмоний (Чучалин А. Г. и др. , 2010 г. ) 3. Пневмония, связанная с оказанием медицинской помощи: I. Пневмония у обитателей домов престарелых II. Прочие категории пациентов: а) антибактериальная терапия в предшествующие 3 мес. ; б) госпитализация (по любому поводу) в течение ≥ 2 суток в предшествующие 90 дней; в) пребывание в других учреждениях длительного ухода; г) хронический диализ в течение ≥ 30 суток; д) обработка раневой поверхности в домашних условиях; е) иммунодефицитные состояния/заболевания.

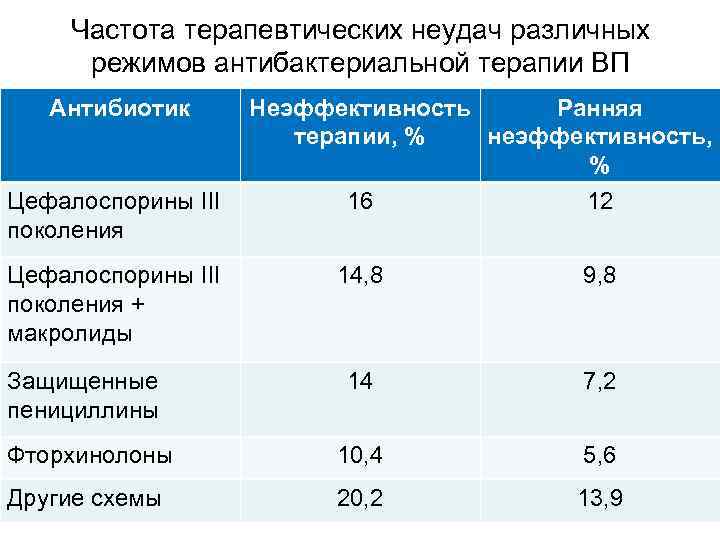
Частота терапевтических неудач различных режимов антибактериальной терапии ВП Антибиотик Неэффективность Ранняя терапии, % неэффективность, % Цефалоспорины III 16 12 поколения Цефалоспорины III поколения + макролиды 14, 8 9, 8 Защищенные пенициллины 14 7, 2 Фторхинолоны 10, 4 5, 6 Другие схемы 20, 2 13, 9

Ошибки антибактериальной терапии ВП у взрослых 1. По выбору препарата нетяжелой ВП Назначение Комментарий Гентамицин Отсутствие активности в отношении пневмококка и атипичных возбудителей Ампициллин внутрь Низкая биодоступность препарата (40%) по сравнению с амоксициллином (75 -93%) Цефазолин Низкая антипневмококковая активность, отсутствие клинически значимой активности в отношении H. influenzae Ципрофлоксацин Низкая активност в отношении S. pneumoniae и M. pneumoniae Доксициклин Высокая резистентность S. pneumoniae в России Респираторные хинолоны Нецелесообразно использование в качестве препаратов выбора при отсутствии факторов риска терапевтической неудачи (сопутствующие заболевания, предшествующий прием антимикробных препаратов)
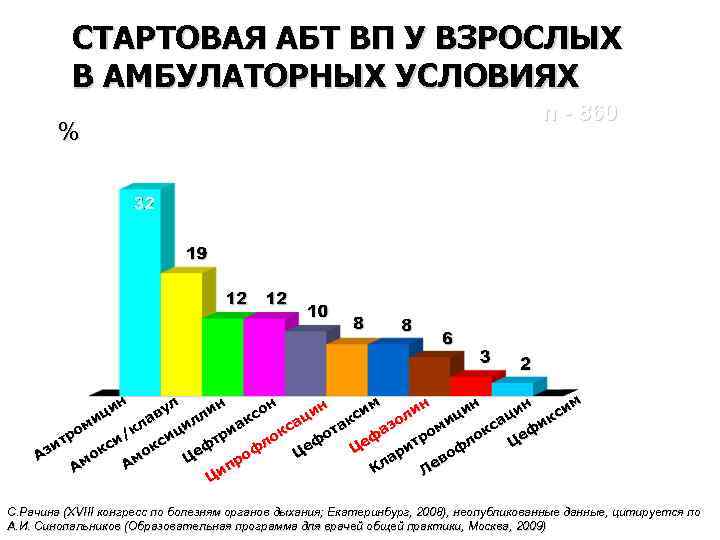
СТАРТОВАЯ АБТ ВП У ВЗРОСЛЫХ В АМБУЛАТОРНЫХ УСЛОВИЯХ % n - 860 . н н н м н ин им ул ц в со си ли ли ци ци ци кс а и к о л и а а и ак кл аз иа ом кс ци кс ом от / р р о еф и о ф р т т и л с т ф Ц л Це кс зи ф ок еф ри Це оф о о А а Ц в Ам пр Ам Кл Ле и Ц C. Рачина (XVIII конгресс по болезням органов дыхания; Екатеринбург, 2008), неопубликованные данные, цитируется по C. Рачина (XVIII дыхания; А. И. Синопальников (Образовательная программа для врачей общей практики, Москва, 2009)

Ошибки антибактериальной терапии ВП у взрослых 2. По выбору препарата тяжелой ВП Назначение Комментарий Β-лактамы (в том числе Не перекрывают спектр потенциальных возбудителей, в цефотаксим, частности L. pneumophila цефтриаксон) в качестве монотерапии Карбопенемы Применение в качестве стартовой терапии экономически (имипенем, меропенем) не оправдано; могут использоваться только при аспирации и подозрении на инфекцию, вызванную P. aeruginosa (кроме эртапенема) Антисинегнойные цефалоспорины III поколения (цефтазидим, цефоперазон) Уступают по активности в отношении S. pneumoniae цефотаксиму и цефтриаксону; использование оправдвно только при подозрении на инфекцию, вызванную P. aeruginosa Ампициллин Не перекрывает спектр потенциальных возбудителей тяжелой ВП, в частности S. aureus и большинства

Ошибки антибактериальной терапии ВП у взрослых 3. По выбору пути введения Назначение Отказ от ступенчатой терапии Комментарий Ступенчатая терапия позволяет существенно сократить затраты на лечение, не ухудшая прогноз. В большинстве случаев перевод на пероральный прием антибиотиков возможен на 2 -3 день терапии Внутримышечное Нецелесообразно ввиду возможного снижения скорости введение антибиотиков и степени абсорбции препарата в системный кровоток при тяжелой ВП

Ошибки антибактериальной терапии ВП у взрослых 4. По срокам начала терапии Назначение Позднее начало антибактериальной терапии Комментарий Отсрочка с назначением антибиотиков с момента госпитализации на 4 часа и более существенно ухудшает прогноз

Ошибки антибактериальной терапии ВП у взрослых 5. По длительности терапии Назначение Комментарий Частая смена антимикробных препаратов в процессе лечения, «объясняемая» опасностью развития резистентности Смена антимикробной терапии в процессе лечения, за исключением случаев клинической неэффективности, и / или непереносимости является нецелесообразной. Показания для отмены антибиотиков: • Клиническая неэффективность, о которой можно судить через 48 -72 часа терапии • Развитие серьезных нежелательных явлений, требующих отмены антибиотика • Высокая потенциальная токсичность антибиотика, ограничивающая длительность его применения Продолжение антибактериальной терапии до полного исчезновения всех клинико-лабораторных показателей Основным критерием отмены антибиотика является обратное развитие клинических симптомов ВП: • Нормализация температуры тела • Уменьшение кашля • Уменьшение и / или улучшение характера мокроты и др. Сохранение отдельных лабораторных и / или

Вместо заключения Назначение некоторых антибиотиков в амбулаторной практике может провоцировать развитие резистентности Опубликовано: Пятница, 27 августа 2010 г. - 09: 05 Согласно результатам недавно завершённого исследования пациенты, получавшие антибиотики в амбулаторной практике для лечения инфекций дыхательных или мочевыводящий путей, имеют более высокий риск устойчивости микроорганизмов к применявшемуся антибиотику при последующих инфекциях. Исследователями из Великобритании был выполнен систематический обзор 4373 публикаций, представленных в Medline, Embase и в Кокрановской базах банных, с целью определения тенденций антибиотикорезистентности микроорганизмов у пациентов, получавших антибиотики в амбулаторной практике. В окончательный мета-анализ было включено 24 исследования со сходными анализируемыми исходами. Среди них было 22 исследования, в которые включались пациенты с инфекциями, и 2 исследования, выполненные у здоровых добровольцев. В анализ были включены 19 обсервационных исследований (из них 2 проспективных) и 5 рандомизированных исследований. Были проанализированы объединённые результаты 5 исследований у 14348 пациентов с инфекциями мочевыводящих путей (ИМП). Объединённый показатель отношения шансов (ОШ) для наличия резистентных бактерий в данной популяции составил 2, 5 (95% доверительный интервал — ДИ от 2, 1 до 2, 9) в течение 2 месяцев после применения антибиотиков и 1, 33 (95% ДИ от 1, 2 до 1, 5) в течение 12 месяцев после лечения. В 7 исследованиях у 2605 участников изучалась антибиотикорезистентность возбудителей инфекций дыхательных путей. Объединённый показатель ОШ для наличия резистентных бактерий в данной популяции составил 2, 4 (95% ДИ от 1, 4 до 3, 9) в течение 2 месяцев после применения антибиотиков и 2, 4 (95% ДИ от 1, 3 до 4, 5) в течение 12 месяцев после лечения. По данным нескольких исследований, в которых было указано количество применявшихся антибиотиков, более длительное лечение и проведение нескольких курсов антимикробной терапии были связаны с более высокой частотой развития резистентности. В одном проспективном исследовании, включённом в мета-анализ, были определены показатели ОШ наличия резистентности после лечения в динамике на протяжении длительного периода наблюдения. Объединённые показатели ОШ составили: 12, 2 (95% ДИ от 6, 8 до 22, 1) через 1 неделю после применения антибиотиков; 6, 1 (2, 8 -3, 4) — через 1 месяц; 3, 6 (2, 2 -6, 0) — через 2 месяца и 2, 2 (1, 3 -3, 6) — через 6 месяцев после лечения. Таким образом, каждый случай применения антибиотиков приводит к достоверному повышению риска антибиотикорезистентности микроорганизмов и распространению носительства резистентных бактерий в популяции, что требует в последующем терапии антибиотиками «второй линии» при лечении инфекций в амбулаторной практике. Полученные результаты ещё раз подчеркивают важность предельно обоснованного и разумного применения антибиотиков при лечении инфекций в амбулаторной практике. Costelloe C. , et al. Effect of antibiotic prescribing in primary care on antimicrobial resistance in individual patients: systematic review and meta-analysis. BMJ 2010; 340: c 2096.

Вместо заключения Приобретённая антибиотикорезистентность, не связанная с применением антибиотиков Опубликовано: Четверг, 28 октября 2004 г. - 09: 15 Глобальное возникновение антибиотикорезистентности часто связывают с широким использованием антибиотиков. Однако данные о резистентности в удалённых районах заставляют пересмотреть подобное предположение. Исследование, предпринятое A. Bartoloni и соавт. (Италия), было проведено в небольшой деревне, расположенной в горах на высоте 1700 м и находящейся в 3 часах пути от ближайшей больницы. Жители деревни проживают в хижинах, централизованное водоснабжение отсутствует. В 1999 г. у 108 человек (около 80% населения деревни) был произведён одномоментный забор образцов кала для определения содержащихся в нем бактерий и их чувствительности к антибиотикам. У 29 (26, 9%) из обследованных лиц выделенные штаммы Escherichia coli были чувствительны ко всем наиболее часто использующимся антибиотикам. Остальные штаммы были резистентны к одному или более препарату, включая тетрациклин (64%), ампициллин (58%), триметоприм-сульфаметоксазол (50%) и хлорамфеникол (41%). 34% изолятов оказались резистентны ко всем 4 препаратам. При опросе выяснилось, что только 8 из 108 обследованных лиц когда-либо принимали антибактериальные препараты, 6 когда-либо посещали больницу и 4 были госпитализированы хотя бы один раз за жизнь. Животные в данной деревне никогда не получали антибиотики. Авторы сочли полученные результаты достаточно неожиданными, учитывая отсутствие селективного давления антибиотиков в данной местности, а также невозможность контаминации источника водоснабжения. Согласно предварительному заключению, резистентные штаммы E. сoli были занесены в деревню и широко распространились среди населения, однако авторы признают, что длительная персистенция резистентных микроорганизмов остаётся необъяснимой. Дальнейшие исследования в других отдаленных регионах могут помочь в разъяснении этих интригующих данных. Bartoloni A. , Bartalesi F. , Mantella A. , Dell'Amico E. , Roselli M. , Strohmeyer M. et al. High prevalence of acquired antimicrobial resistance unrelated to heavy antimicrobial consumption. J Infect Dis 2004; 189: 1291 -4.


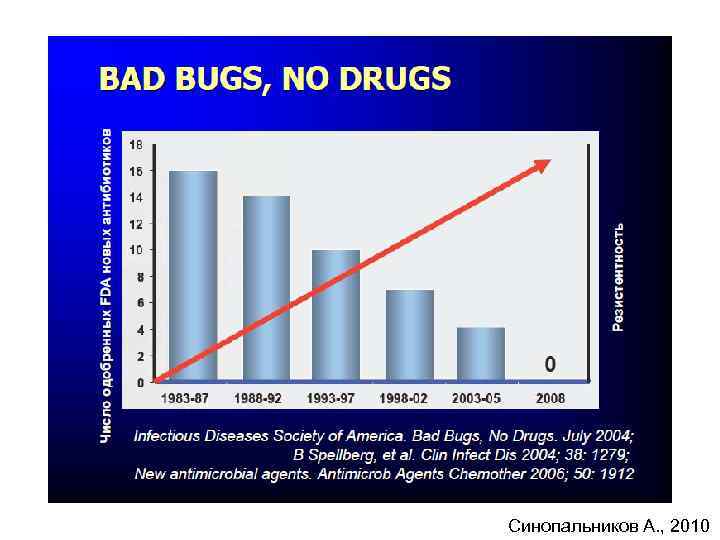
Синопальников А. , 2010

И пусть эта безграничная сила, которая управляет судьбами Вселенной, ведет нас к тому, что называется лучшим, и наставляет нас, как обеспечить вам мир и процветание Томас Джефферсон (1743– 1826)

Спасибо за внимание!
Pnevmonii-Krasnoyarsk_2012.ppt