Пневмония 2011.ppt
- Количество слайдов: 102
 Пневмония Малишевский Михаил Владимирович Тюменская медицинская академия
Пневмония Малишевский Михаил Владимирович Тюменская медицинская академия

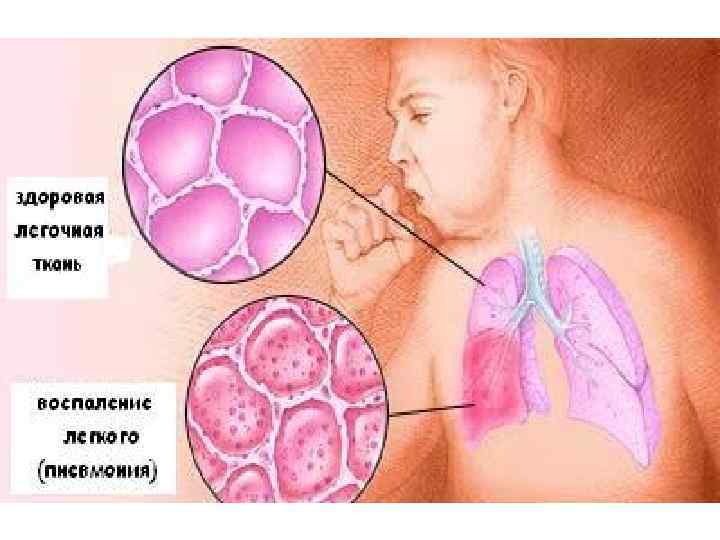
 Пневмонии – это группа различных по этиологии, патогенезу, морфологической характеристике острых инфекционных (преимущественно бактериальных) заболеваний, характеризующихся очаговым поражением респираторных отделов легких с обязательным наличием внутриальвеолярной экссудации
Пневмонии – это группа различных по этиологии, патогенезу, морфологической характеристике острых инфекционных (преимущественно бактериальных) заболеваний, характеризующихся очаговым поражением респираторных отделов легких с обязательным наличием внутриальвеолярной экссудации
 Особенности современной пневмонии
Особенности современной пневмонии
 1. Рост заболеваемости пневмонией
1. Рост заболеваемости пневмонией
 2. Гиподиагностика пневмоний
2. Гиподиагностика пневмоний
 3. Рост смертности от пневмоний
3. Рост смертности от пневмоний




 4. Возрастной и половой аспекты пневмоний
4. Возрастной и половой аспекты пневмоний
 5. Теория модифицирующих факторов
5. Теория модифицирующих факторов
 6. Увеличение частоты тяжелого течения пневмоний
6. Увеличение частоты тяжелого течения пневмоний
 7. Спектр ключевых возбудителей пневмоний
7. Спектр ключевых возбудителей пневмоний
 Классификация пневмоний 1. Внебольничная (приобретенная вне лечебного учреждения) пневмония (синонимы: домашняя, амбулаторная) 2. Нозокомиальная (приобретенная в лечебном учреждении) пневмония (синонимы: госпитальная, внутрибольничная) 3. Аспирационная пневмония 4. Пневмония у лиц с тяжелыми нарушениями иммунитета (врожденный иммунодефицит, ВИЧ-инфекция, ятрогенная иммуносупрессия) Чучалин А. Г. , 2006
Классификация пневмоний 1. Внебольничная (приобретенная вне лечебного учреждения) пневмония (синонимы: домашняя, амбулаторная) 2. Нозокомиальная (приобретенная в лечебном учреждении) пневмония (синонимы: госпитальная, внутрибольничная) 3. Аспирационная пневмония 4. Пневмония у лиц с тяжелыми нарушениями иммунитета (врожденный иммунодефицит, ВИЧ-инфекция, ятрогенная иммуносупрессия) Чучалин А. Г. , 2006
 Классификация пневмоний (Чучалин А. Г. и др. , 2010 г. ) Внебольничная пневмония I. Типичная (у пациентов с отсутствием выраженных нарушений иммунитета): а) бактериальная; б) вирусная; в) грибковая; г) микобактериальная; д) паразитарная. II. У пациентов с выраженными нарушениями иммунитета: а) синдром приобретенного иммунодефицита (СПИД); б) прочие заболевания/патологические состояния. III. Аспирационная пневмония/абсцесс легкого. Нозокомиальная пневмония Пневмония, связанная с оказанием медицинской помощи I. Собственно нозокомиальная I. Пневмония у обитателей домов пневмония. престарелых II. Вентиляторассоциированная II. Прочие категории пациентов: пневмония. а) антибактериальная терапия в III. Нозокомиальная пневмония у предшествующие 3 мес. ; пациентов с выраженными б) госпитализация (по любому нарушениями иммунитета: поводу) в течение ≥ 2 суток в а) у реципиентов донорских предшествующие 90 дней; органов; в) пребывание в других б) у пациентов, получающих учреждениях длительного ухода; цитостатическую терапию. г) хронический диализ в течение ≥ 30 суток; д) обработка раневой поверхности в домашних условиях; е) иммунодефицитные состояния/заболевания.
Классификация пневмоний (Чучалин А. Г. и др. , 2010 г. ) Внебольничная пневмония I. Типичная (у пациентов с отсутствием выраженных нарушений иммунитета): а) бактериальная; б) вирусная; в) грибковая; г) микобактериальная; д) паразитарная. II. У пациентов с выраженными нарушениями иммунитета: а) синдром приобретенного иммунодефицита (СПИД); б) прочие заболевания/патологические состояния. III. Аспирационная пневмония/абсцесс легкого. Нозокомиальная пневмония Пневмония, связанная с оказанием медицинской помощи I. Собственно нозокомиальная I. Пневмония у обитателей домов пневмония. престарелых II. Вентиляторассоциированная II. Прочие категории пациентов: пневмония. а) антибактериальная терапия в III. Нозокомиальная пневмония у предшествующие 3 мес. ; пациентов с выраженными б) госпитализация (по любому нарушениями иммунитета: поводу) в течение ≥ 2 суток в а) у реципиентов донорских предшествующие 90 дней; органов; в) пребывание в других б) у пациентов, получающих учреждениях длительного ухода; цитостатическую терапию. г) хронический диализ в течение ≥ 30 суток; д) обработка раневой поверхности в домашних условиях; е) иммунодефицитные состояния/заболевания.
 Классификация пневмоний (Чучалин А. Г. и др. , 2010 г. ) 1. Внебольничная пневмония: I. Типичная (у пациентов с отсутствием выраженных нарушений иммунитета): а) бактериальная; б) вирусная; в) грибковая; г) микобактериальная; д) паразитарная. II. У пациентов с выраженными нарушениями иммунитета: а) синдром приобретенного иммунодефицита (СПИД); б) прочие заболевания/патологические состояния. III. Аспирационная пневмония/абсцесс легкого.
Классификация пневмоний (Чучалин А. Г. и др. , 2010 г. ) 1. Внебольничная пневмония: I. Типичная (у пациентов с отсутствием выраженных нарушений иммунитета): а) бактериальная; б) вирусная; в) грибковая; г) микобактериальная; д) паразитарная. II. У пациентов с выраженными нарушениями иммунитета: а) синдром приобретенного иммунодефицита (СПИД); б) прочие заболевания/патологические состояния. III. Аспирационная пневмония/абсцесс легкого.
 Классификация пневмоний (Чучалин А. Г. и др. , 2010 г. ) 2. Нозокомиальная пневмония: I. Собственно нозокомиальная пневмония. II. Вентиляторассоциированная пневмония. III. Нозокомиальная пневмония у пациентов с выраженными нарушениями иммунитета: а) у реципиентов донорских органов; б) у пациентов, получающих цитостатическую терапию.
Классификация пневмоний (Чучалин А. Г. и др. , 2010 г. ) 2. Нозокомиальная пневмония: I. Собственно нозокомиальная пневмония. II. Вентиляторассоциированная пневмония. III. Нозокомиальная пневмония у пациентов с выраженными нарушениями иммунитета: а) у реципиентов донорских органов; б) у пациентов, получающих цитостатическую терапию.
 Классификация пневмоний (Чучалин А. Г. и др. , 2010 г. ) 3. Пневмония, связанная с оказанием медицинской помощи: I. Пневмония у обитателей домов престарелых II. Прочие категории пациентов: а) антибактериальная терапия в предшествующие 3 мес. ; б) госпитализация (по любому поводу) в течение ≥ 2 суток в предшествующие 90 дней; в) пребывание в других учреждениях длительного ухода; г) хронический диализ в течение ≥ 30 суток; д) обработка раневой поверхности в домашних условиях; е) иммунодефицитные состояния/заболевания.
Классификация пневмоний (Чучалин А. Г. и др. , 2010 г. ) 3. Пневмония, связанная с оказанием медицинской помощи: I. Пневмония у обитателей домов престарелых II. Прочие категории пациентов: а) антибактериальная терапия в предшествующие 3 мес. ; б) госпитализация (по любому поводу) в течение ≥ 2 суток в предшествующие 90 дней; в) пребывание в других учреждениях длительного ухода; г) хронический диализ в течение ≥ 30 суток; д) обработка раневой поверхности в домашних условиях; е) иммунодефицитные состояния/заболевания.
 Назначение некоторых антибиотиков в амбулаторной практике может провоцировать развитие резистентности Опубликовано: Пятница, 27 августа 2010 г. - 09: 05 Согласно результатам недавно завершённого исследования пациенты, получавшие антибиотики в амбулаторной практике для лечения инфекций дыхательных или мочевыводящий путей, имеют более высокий риск устойчивости микроорганизмов к применявшемуся антибиотику при последующих инфекциях. Исследователями из Великобритании был выполнен систематический обзор 4373 публикаций, представленных в Medline, Embase и в Кокрановской базах банных, с целью определения тенденций антибиотикорезистентности микроорганизмов у пациентов, получавших антибиотики в амбулаторной практике. В окончательный мета-анализ было включено 24 исследования со сходными анализируемыми исходами. Среди них было 22 исследования, в которые включались пациенты с инфекциями, и 2 исследования, выполненные у здоровых добровольцев. В анализ были включены 19 обсервационных исследований (из них 2 проспективных) и 5 рандомизированных исследований. Были проанализированы объединённые результаты 5 исследований у 14348 пациентов с инфекциями мочевыводящих путей (ИМП). Объединённый показатель отношения шансов (ОШ) для наличия резистентных бактерий в данной популяции составил 2, 5 (95% доверительный интервал — ДИ от 2, 1 до 2, 9) в течение 2 месяцев после применения антибиотиков и 1, 33 (95% ДИ от 1, 2 до 1, 5) в течение 12 месяцев после лечения. В 7 исследованиях у 2605 участников изучалась антибиотикорезистентность возбудителей инфекций дыхательных путей. Объединённый показатель ОШ для наличия резистентных бактерий в данной популяции составил 2, 4 (95% ДИ от 1, 4 до 3, 9) в течение 2 месяцев после применения антибиотиков и 2, 4 (95% ДИ от 1, 3 до 4, 5) в течение 12 месяцев после лечения. По данным нескольких исследований, в которых было указано количество применявшихся антибиотиков, более длительное лечение и проведение нескольких курсов антимикробной терапии были связаны с более высокой частотой развития резистентности. В одном проспективном исследовании, включённом в мета-анализ, были определены показатели ОШ наличия резистентности после лечения в динамике на протяжении длительного периода наблюдения. Объединённые показатели ОШ составили: 12, 2 (95% ДИ от 6, 8 до 22, 1) через 1 неделю после применения антибиотиков; 6, 1 (2, 8 -3, 4) — через 1 месяц; 3, 6 (2, 2 -6, 0) — через 2 месяца и 2, 2 (1, 3 -3, 6) — через 6 месяцев после лечения. Таким образом, каждый случай применения антибиотиков приводит к достоверному повышению риска антибиотикорезистентности микроорганизмов и распространению носительства резистентных бактерий в популяции, что требует в последующем терапии антибиотиками «второй линии» при лечении инфекций в амбулаторной практике. Полученные результаты ещё раз подчеркивают важность предельно обоснованного и разумного применения антибиотиков при лечении инфекций в амбулаторной практике. Costelloe C. , et al. Effect of antibiotic prescribing in primary care on antimicrobial resistance in individual patients: systematic review and meta-analysis. BMJ 2010; 340: c 2096.
Назначение некоторых антибиотиков в амбулаторной практике может провоцировать развитие резистентности Опубликовано: Пятница, 27 августа 2010 г. - 09: 05 Согласно результатам недавно завершённого исследования пациенты, получавшие антибиотики в амбулаторной практике для лечения инфекций дыхательных или мочевыводящий путей, имеют более высокий риск устойчивости микроорганизмов к применявшемуся антибиотику при последующих инфекциях. Исследователями из Великобритании был выполнен систематический обзор 4373 публикаций, представленных в Medline, Embase и в Кокрановской базах банных, с целью определения тенденций антибиотикорезистентности микроорганизмов у пациентов, получавших антибиотики в амбулаторной практике. В окончательный мета-анализ было включено 24 исследования со сходными анализируемыми исходами. Среди них было 22 исследования, в которые включались пациенты с инфекциями, и 2 исследования, выполненные у здоровых добровольцев. В анализ были включены 19 обсервационных исследований (из них 2 проспективных) и 5 рандомизированных исследований. Были проанализированы объединённые результаты 5 исследований у 14348 пациентов с инфекциями мочевыводящих путей (ИМП). Объединённый показатель отношения шансов (ОШ) для наличия резистентных бактерий в данной популяции составил 2, 5 (95% доверительный интервал — ДИ от 2, 1 до 2, 9) в течение 2 месяцев после применения антибиотиков и 1, 33 (95% ДИ от 1, 2 до 1, 5) в течение 12 месяцев после лечения. В 7 исследованиях у 2605 участников изучалась антибиотикорезистентность возбудителей инфекций дыхательных путей. Объединённый показатель ОШ для наличия резистентных бактерий в данной популяции составил 2, 4 (95% ДИ от 1, 4 до 3, 9) в течение 2 месяцев после применения антибиотиков и 2, 4 (95% ДИ от 1, 3 до 4, 5) в течение 12 месяцев после лечения. По данным нескольких исследований, в которых было указано количество применявшихся антибиотиков, более длительное лечение и проведение нескольких курсов антимикробной терапии были связаны с более высокой частотой развития резистентности. В одном проспективном исследовании, включённом в мета-анализ, были определены показатели ОШ наличия резистентности после лечения в динамике на протяжении длительного периода наблюдения. Объединённые показатели ОШ составили: 12, 2 (95% ДИ от 6, 8 до 22, 1) через 1 неделю после применения антибиотиков; 6, 1 (2, 8 -3, 4) — через 1 месяц; 3, 6 (2, 2 -6, 0) — через 2 месяца и 2, 2 (1, 3 -3, 6) — через 6 месяцев после лечения. Таким образом, каждый случай применения антибиотиков приводит к достоверному повышению риска антибиотикорезистентности микроорганизмов и распространению носительства резистентных бактерий в популяции, что требует в последующем терапии антибиотиками «второй линии» при лечении инфекций в амбулаторной практике. Полученные результаты ещё раз подчеркивают важность предельно обоснованного и разумного применения антибиотиков при лечении инфекций в амбулаторной практике. Costelloe C. , et al. Effect of antibiotic prescribing in primary care on antimicrobial resistance in individual patients: systematic review and meta-analysis. BMJ 2010; 340: c 2096.

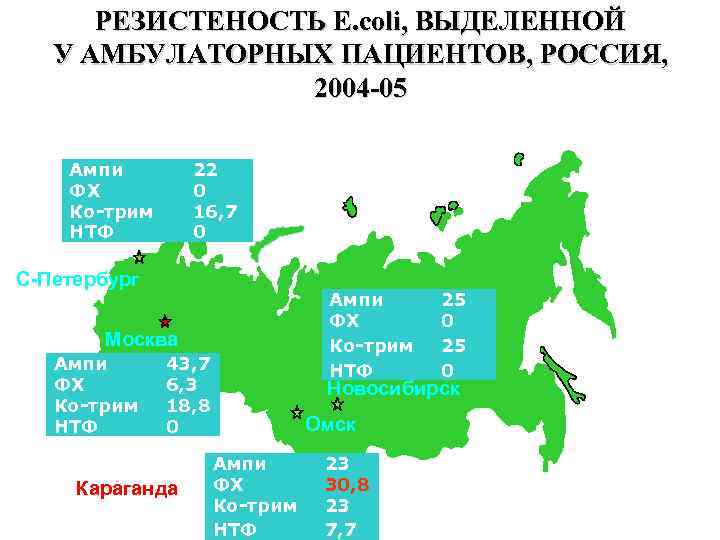 РЕЗИСТЕНОСТЬ E. coli, ВЫДЕЛЕННОЙ У АМБУЛАТОРНЫХ ПАЦИЕНТОВ, РОССИЯ, 2004 -05 Ампи ФХ Ко-трим НТФ 22 0 16, 7 0 С-Петербург Ампи ФХ Ко-трим НТФ Москва Ампи ФХ Ко-трим НТФ 43, 7 6, 3 18, 8 0 Караганда 25 0 Новосибирск Омск Ампи ФХ Ко-трим НТФ 23 30, 8 23 7, 7
РЕЗИСТЕНОСТЬ E. coli, ВЫДЕЛЕННОЙ У АМБУЛАТОРНЫХ ПАЦИЕНТОВ, РОССИЯ, 2004 -05 Ампи ФХ Ко-трим НТФ 22 0 16, 7 0 С-Петербург Ампи ФХ Ко-трим НТФ Москва Ампи ФХ Ко-трим НТФ 43, 7 6, 3 18, 8 0 Караганда 25 0 Новосибирск Омск Ампи ФХ Ко-трим НТФ 23 30, 8 23 7, 7
 Классификация пневмоний (Чучалин А. Г. и др. , 2010 г. ) 3. Пневмония, связанная с оказанием медицинской помощи: I. Пневмония у обитателей домов престарелых II. Прочие категории пациентов: а) антибактериальная терапия в предшествующие 3 мес. ; б) госпитализация (по любому поводу) в течение ≥ 2 суток в предшествующие 90 дней; в) пребывание в других учреждениях длительного ухода; г) хронический диализ в течение ≥ 30 суток; д) обработка раневой поверхности в домашних условиях; е) иммунодефицитные состояния/заболевания.
Классификация пневмоний (Чучалин А. Г. и др. , 2010 г. ) 3. Пневмония, связанная с оказанием медицинской помощи: I. Пневмония у обитателей домов престарелых II. Прочие категории пациентов: а) антибактериальная терапия в предшествующие 3 мес. ; б) госпитализация (по любому поводу) в течение ≥ 2 суток в предшествующие 90 дней; в) пребывание в других учреждениях длительного ухода; г) хронический диализ в течение ≥ 30 суток; д) обработка раневой поверхности в домашних условиях; е) иммунодефицитные состояния/заболевания.
 Внебольничная пневмония – острое заболевание, возникшее во внебольничных условиях (вне стационара) или диагностированное в первые 48 часов от момента госпитализации или развившееся у пациента, не находящегося в домах сестринского ухода/отделениях длительного медицинского наблюдения ≥ 14 суток, - сопровождающееся симптомами инфекции нижних дыхательных путей (лихорадка, кашель, выделение мокроты, возможно гнойной, боль в грудной клетке, одышка) и рентгенологическими признаками «свежих» очаговоинфильтративных изменений в легких при отсутствии очевидной диагностической альтернативы.
Внебольничная пневмония – острое заболевание, возникшее во внебольничных условиях (вне стационара) или диагностированное в первые 48 часов от момента госпитализации или развившееся у пациента, не находящегося в домах сестринского ухода/отделениях длительного медицинского наблюдения ≥ 14 суток, - сопровождающееся симптомами инфекции нижних дыхательных путей (лихорадка, кашель, выделение мокроты, возможно гнойной, боль в грудной клетке, одышка) и рентгенологическими признаками «свежих» очаговоинфильтративных изменений в легких при отсутствии очевидной диагностической альтернативы.
 Этиология • S. pneumoniae (30 -50% случаев заболевания)
Этиология • S. pneumoniae (30 -50% случаев заболевания)
 Этиология • S. pneumoniae (30 -50% случаев заболевания) • Атипичные микроорганизмы (8 -30% случаев заболевания)
Этиология • S. pneumoniae (30 -50% случаев заболевания) • Атипичные микроорганизмы (8 -30% случаев заболевания)
 Этиология • S. pneumoniae (30 -50% случаев заболевания) • Атипичные микроорганизмы (8 -30% случаев заболевания): • Clamydophila pneumoniae
Этиология • S. pneumoniae (30 -50% случаев заболевания) • Атипичные микроорганизмы (8 -30% случаев заболевания): • Clamydophila pneumoniae
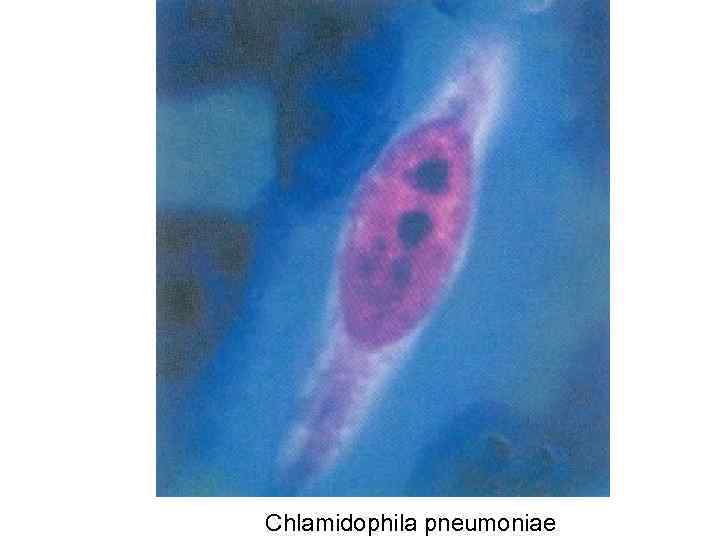 Chlamidophila pneumoniae
Chlamidophila pneumoniae
 Этиология • S. pneumoniae (30 -50% случаев заболевания) • Атипичные микроорганизмы (8 -30% случаев заболевания): • Clamydophila pneumoniae • Mycoplasma pneumoniae
Этиология • S. pneumoniae (30 -50% случаев заболевания) • Атипичные микроорганизмы (8 -30% случаев заболевания): • Clamydophila pneumoniae • Mycoplasma pneumoniae
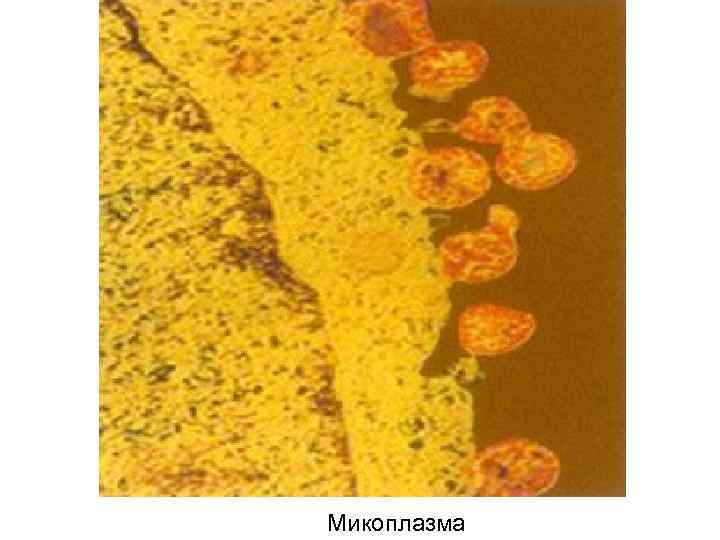 Микоплазма
Микоплазма
 Этиология • S. pneumoniae (30 -50% случаев заболевания) • Атипичные микроорганизмы (8 -30% случаев заболевания): • Clamydophila pneumoniae • Mycoplasma pneumoniae • Legionella pneumophila
Этиология • S. pneumoniae (30 -50% случаев заболевания) • Атипичные микроорганизмы (8 -30% случаев заболевания): • Clamydophila pneumoniae • Mycoplasma pneumoniae • Legionella pneumophila
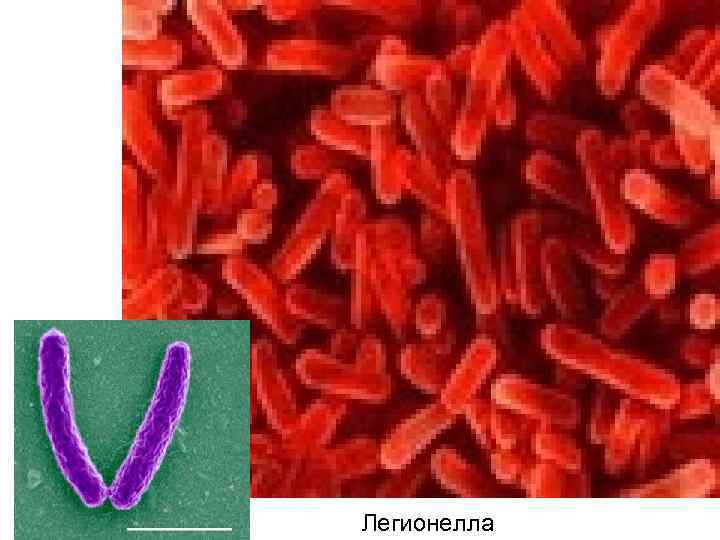 Легионелла
Легионелла
 Возбудитель Ligionella pneumophila открыт в 1976 г. , после того как в Филадельфии на съезде легионеров (ветеранов, воевавших в Индокитае) из 221 участника заболело 220, причем в 30 случаях исход был летальным. В 90 -е годы эпидемические вспышки “болезни легионеров” были зафиксированы в Грузии и Прибалтике. Спорадическая заболеваемость, по данным разных авторов, составляет от 1, 5% до 15% всех случаев этиологически верифицированных пневмоний. Восприимчивость к инфекции более 70%. Болеют все, но чаще старики и дети. Легионелла — это грамотрицательная палочка размером до 3 мкм, имеющая жгутики. Место естественного обитания бактерии — пресная вода, организм человека является для возбудителя легионеллеза биологическим тупиком. Последнее ставит под сомнение возможность непосредственной передачи инфекции от человека к человеку. Пути передачи легионеллеза — алиментарный и ингаляционный, сезонность — летне-осенняя. Эпидемическая заболеваемость связывается с контаминацией возбудителем водных систем. Групповые вспышки возможны при проживании вблизи открытых водоемов, посещении бассейнов, контакте с кондиционерами, увлажнителями воздуха, системами принудительной вентиляции (метро, вокзалы, аэропорты, универмаги и др. ). Таким образом, легионеллез — это болезнь больших городов индустриально развитых стран.
Возбудитель Ligionella pneumophila открыт в 1976 г. , после того как в Филадельфии на съезде легионеров (ветеранов, воевавших в Индокитае) из 221 участника заболело 220, причем в 30 случаях исход был летальным. В 90 -е годы эпидемические вспышки “болезни легионеров” были зафиксированы в Грузии и Прибалтике. Спорадическая заболеваемость, по данным разных авторов, составляет от 1, 5% до 15% всех случаев этиологически верифицированных пневмоний. Восприимчивость к инфекции более 70%. Болеют все, но чаще старики и дети. Легионелла — это грамотрицательная палочка размером до 3 мкм, имеющая жгутики. Место естественного обитания бактерии — пресная вода, организм человека является для возбудителя легионеллеза биологическим тупиком. Последнее ставит под сомнение возможность непосредственной передачи инфекции от человека к человеку. Пути передачи легионеллеза — алиментарный и ингаляционный, сезонность — летне-осенняя. Эпидемическая заболеваемость связывается с контаминацией возбудителем водных систем. Групповые вспышки возможны при проживании вблизи открытых водоемов, посещении бассейнов, контакте с кондиционерами, увлажнителями воздуха, системами принудительной вентиляции (метро, вокзалы, аэропорты, универмаги и др. ). Таким образом, легионеллез — это болезнь больших городов индустриально развитых стран.
 Этиология • S. pneumoniae (30 -50% случаев заболевания) • Атипичные микроорганизмы (8 -30% случаев заболевания) • Clamydophila pneumoniae • Mycoplasma pneumoniae • Legionella pneumophila • Редкие возбудители (3 -5%) • Hemophilus influenza • Staphylococcus aureus • Klebsiella pneumoniae
Этиология • S. pneumoniae (30 -50% случаев заболевания) • Атипичные микроорганизмы (8 -30% случаев заболевания) • Clamydophila pneumoniae • Mycoplasma pneumoniae • Legionella pneumophila • Редкие возбудители (3 -5%) • Hemophilus influenza • Staphylococcus aureus • Klebsiella pneumoniae
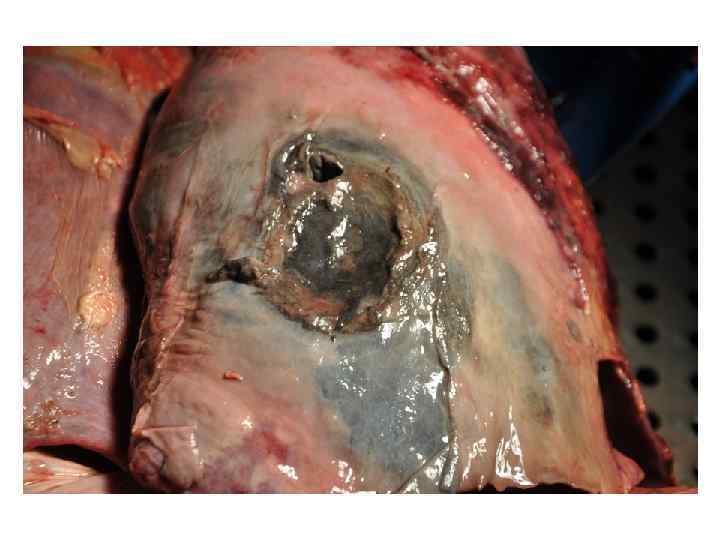
 В последнее время наблюдается рост числа ВП, вызываемых внебольничными штаммами MRSA. Продукция данным возбудителем лейкоцидина Panton-Valentine и других токсинов обусловливает развитие осложнений пневмонии (деструкция / абсцедирование легочной ткани, эмпиема плевры, шок, дыхательная недостаточность). Предположение о внебольничном MRSA следует допускать у больных с абсцедированием легочных инфильтратов при отсутствии факторов риска аспирационной пневмонии (злоупотребление алкоголем, нарушение моторики пищевода, нарушение сознания, инсульт, заболевания десен)
В последнее время наблюдается рост числа ВП, вызываемых внебольничными штаммами MRSA. Продукция данным возбудителем лейкоцидина Panton-Valentine и других токсинов обусловливает развитие осложнений пневмонии (деструкция / абсцедирование легочной ткани, эмпиема плевры, шок, дыхательная недостаточность). Предположение о внебольничном MRSA следует допускать у больных с абсцедированием легочных инфильтратов при отсутствии факторов риска аспирационной пневмонии (злоупотребление алкоголем, нарушение моторики пищевода, нарушение сознания, инсульт, заболевания десен)
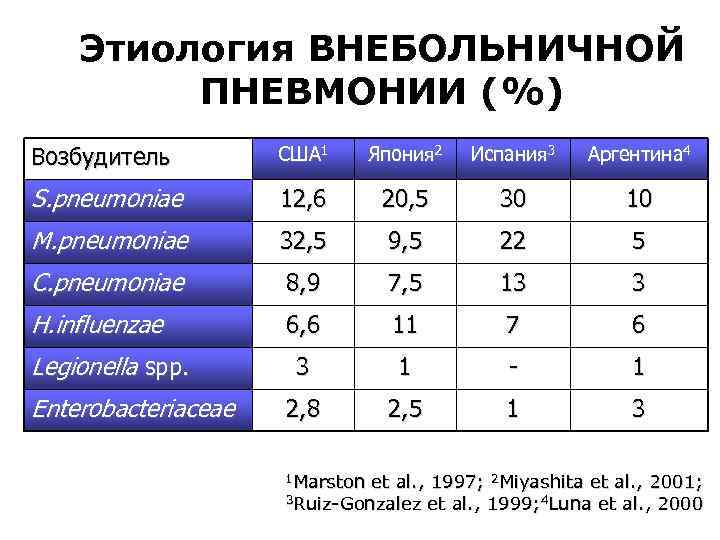 Этиология ВНЕБОЛЬНИЧНОЙ ПНЕВМОНИИ (%) Возбудитель США 1 Япония 2 Испания 3 Аргентина 4 S. pneumoniae 12, 6 20, 5 30 10 M. pneumoniae 32, 5 9, 5 22 5 C. pneumoniae 8, 9 7, 5 13 3 H. influenzae 6, 6 11 7 6 3 1 - 1 2, 8 2, 5 1 3 Legionella spp. Enterobacteriaceae 1 Marston et al. , 1997; 2 Miyashita et al. , 2001; 3 Ruiz-Gonzalez et al. , 1999; 4 Luna et al. , 2000
Этиология ВНЕБОЛЬНИЧНОЙ ПНЕВМОНИИ (%) Возбудитель США 1 Япония 2 Испания 3 Аргентина 4 S. pneumoniae 12, 6 20, 5 30 10 M. pneumoniae 32, 5 9, 5 22 5 C. pneumoniae 8, 9 7, 5 13 3 H. influenzae 6, 6 11 7 6 3 1 - 1 2, 8 2, 5 1 3 Legionella spp. Enterobacteriaceae 1 Marston et al. , 1997; 2 Miyashita et al. , 2001; 3 Ruiz-Gonzalez et al. , 1999; 4 Luna et al. , 2000
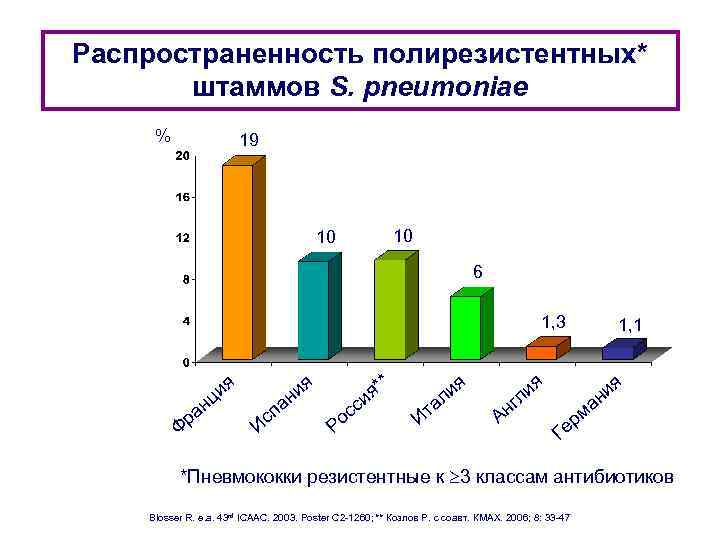 Распространенность полирезистентных* штаммов S. pneumoniae % 19 10 10 6 1, 3 ия ц ан р Ф Ис ия н па * я* и Р сс о Ит ия ал Ан и гл 1, 1 я я и ан рм е Г *Пневмококки резистентные к 3 классам антибиотиков Blosser R. e. a. 43 rd ICAAC. 2003. Poster C 2 -1260; ** Козлов Р. с соавт. КМАХ. 2006; 8: 33 -47
Распространенность полирезистентных* штаммов S. pneumoniae % 19 10 10 6 1, 3 ия ц ан р Ф Ис ия н па * я* и Р сс о Ит ия ал Ан и гл 1, 1 я я и ан рм е Г *Пневмококки резистентные к 3 классам антибиотиков Blosser R. e. a. 43 rd ICAAC. 2003. Poster C 2 -1260; ** Козлов Р. с соавт. КМАХ. 2006; 8: 33 -47

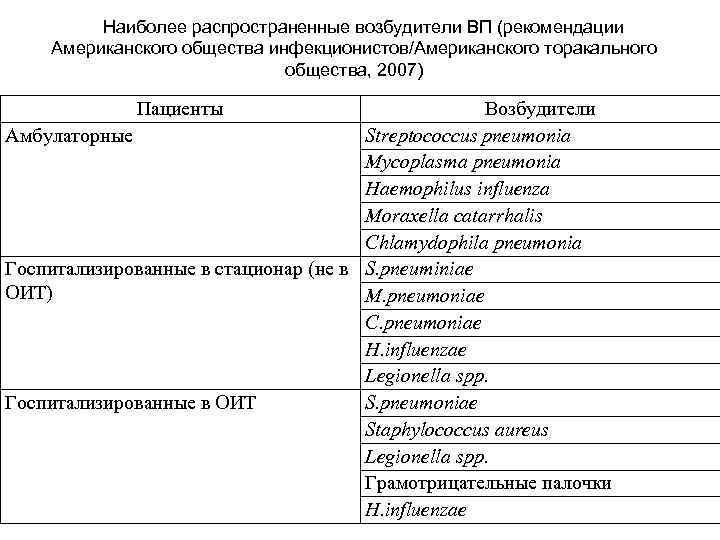 Наиболее распространенные возбудители ВП (рекомендации Американского общества инфекционистов/Американского торакального общества, 2007) Пациенты Возбудители Амбулаторные Streptococcus pneumonia Mycoplasma pneumonia Haemophilus influenza Moraxella catarrhalis Chlamydophila pneumonia Госпитализированные в стационар (не в S. pneuminiae ОИТ) M. pneumoniae C. pneumoniae H. influenzae Legionella spp. Госпитализированные в ОИТ S. pneumoniae Staphylococcus aureus Legionella spp. Грамотрицательные палочки H. influenzae
Наиболее распространенные возбудители ВП (рекомендации Американского общества инфекционистов/Американского торакального общества, 2007) Пациенты Возбудители Амбулаторные Streptococcus pneumonia Mycoplasma pneumonia Haemophilus influenza Moraxella catarrhalis Chlamydophila pneumonia Госпитализированные в стационар (не в S. pneuminiae ОИТ) M. pneumoniae C. pneumoniae H. influenzae Legionella spp. Госпитализированные в ОИТ S. pneumoniae Staphylococcus aureus Legionella spp. Грамотрицательные палочки H. influenzae
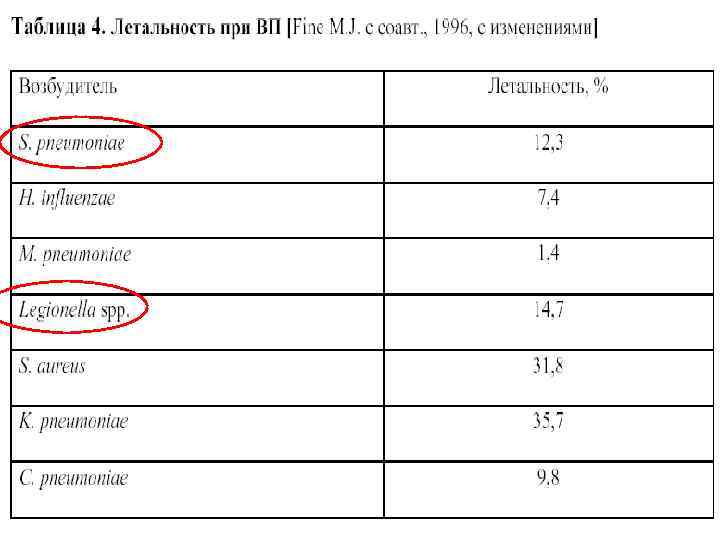
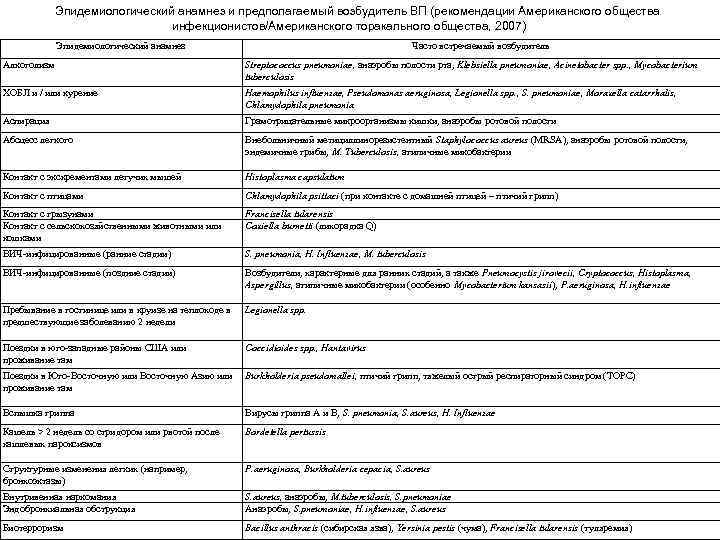 Эпидемиологический анамнез и предполагаемый возбудитель ВП (рекомендации Американского общества инфекционистов/Американского торакального общества, 2007) Эпидемиологический анамнез Часто встречаемый возбудитель Алкоголизм Streptococcus pneumoniae, анаэробы полости рта, Klebsiella pneumoniae, Acinetobacter spp. , Mycobacterium tuberculosis ХОБЛ и / или курение Haemophilus influenzae, Pseudomonas aeruginosa, Legionella spp. , S. pneumoniae, Moraxella catarrhalis, Chlamydophila pneumonia Аспирация Грамотрицательные микроорганизмы кишки, анаэробы ротовой полости Абсцесс легкого Внебольничный метициллинорезистентный Staphylococcus aureus (MRSA), анаэробы ротовой полости, эндемичные грибы, M. Tuberculosis, атипичные микобактерии Контакт с экскрементами летучих мышей Histoplasma capsulatum Контакт с птицами Chlamydophila psittaci (при контакте с домашней птицей – птичий грипп) Контакт с грызунами Контакт с сельскохозяйственными животными или кошками Francisella tularensis Coxiella burnetti (лихорадка Q) ВИЧ-инфицированные (ранние стадии) S. pneumonia, H. Influenzae, M. tuberculosis ВИЧ-инфицированные (поздние стадии) Возбудители, характерные для ранних стадий, а также Pneumocystis jirovecii, Cryptococcus, Histoplasma, Aspergillus, атипичные микобактерии (особенно Mycobacterium kansasii), P. aeruginosa, H. influenzae Пребывание в гостинице или в круизе на теплоходе в предшествующие заболеванию 2 недели Legionella spp. Поездки в юго-западные районы США или проживание там Coccidioides spp. , Hantavirus Поездки в Юго-Восточную или Восточную Азию или Burkholderia pseudomallei, птичий грипп, тяжелый острый респираторный синдром (ТОРС) проживание там Вспышка гриппа Вирусы гриппа А и В, S. pneumonia, S. aureus, H. Influenzae Кашель > 2 недель со стридором или рвотой после кашлевых пароксизмов Bordetella pertussis Структурные изменения легких (например, бронхоэктазы) P. aeruginosa, Burkholderia cepacia, S. aureus Внутривенная наркомания Эндобронхиальная обструкция S. aureus, анаэробы, M. tuberculosis, S. pneumoniae Анаэробы, S. pneumoniae, H. influenzae, S. aureus Биотерроризм Bacillus anthracis (сибирская язва), Yersinia pestis (чума), Francisella tularensis (туляремия)
Эпидемиологический анамнез и предполагаемый возбудитель ВП (рекомендации Американского общества инфекционистов/Американского торакального общества, 2007) Эпидемиологический анамнез Часто встречаемый возбудитель Алкоголизм Streptococcus pneumoniae, анаэробы полости рта, Klebsiella pneumoniae, Acinetobacter spp. , Mycobacterium tuberculosis ХОБЛ и / или курение Haemophilus influenzae, Pseudomonas aeruginosa, Legionella spp. , S. pneumoniae, Moraxella catarrhalis, Chlamydophila pneumonia Аспирация Грамотрицательные микроорганизмы кишки, анаэробы ротовой полости Абсцесс легкого Внебольничный метициллинорезистентный Staphylococcus aureus (MRSA), анаэробы ротовой полости, эндемичные грибы, M. Tuberculosis, атипичные микобактерии Контакт с экскрементами летучих мышей Histoplasma capsulatum Контакт с птицами Chlamydophila psittaci (при контакте с домашней птицей – птичий грипп) Контакт с грызунами Контакт с сельскохозяйственными животными или кошками Francisella tularensis Coxiella burnetti (лихорадка Q) ВИЧ-инфицированные (ранние стадии) S. pneumonia, H. Influenzae, M. tuberculosis ВИЧ-инфицированные (поздние стадии) Возбудители, характерные для ранних стадий, а также Pneumocystis jirovecii, Cryptococcus, Histoplasma, Aspergillus, атипичные микобактерии (особенно Mycobacterium kansasii), P. aeruginosa, H. influenzae Пребывание в гостинице или в круизе на теплоходе в предшествующие заболеванию 2 недели Legionella spp. Поездки в юго-западные районы США или проживание там Coccidioides spp. , Hantavirus Поездки в Юго-Восточную или Восточную Азию или Burkholderia pseudomallei, птичий грипп, тяжелый острый респираторный синдром (ТОРС) проживание там Вспышка гриппа Вирусы гриппа А и В, S. pneumonia, S. aureus, H. Influenzae Кашель > 2 недель со стридором или рвотой после кашлевых пароксизмов Bordetella pertussis Структурные изменения легких (например, бронхоэктазы) P. aeruginosa, Burkholderia cepacia, S. aureus Внутривенная наркомания Эндобронхиальная обструкция S. aureus, анаэробы, M. tuberculosis, S. pneumoniae Анаэробы, S. pneumoniae, H. influenzae, S. aureus Биотерроризм Bacillus anthracis (сибирская язва), Yersinia pestis (чума), Francisella tularensis (туляремия)
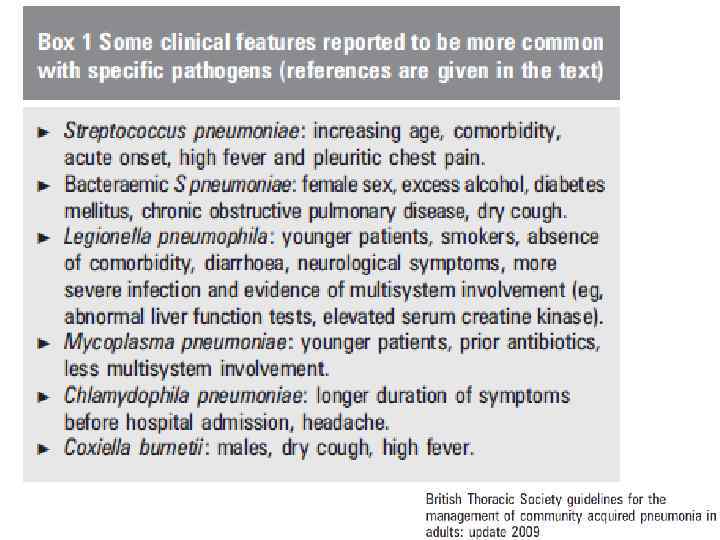
 Пневмококк: повышение возраста, сопутствующие заболевания, острое начало, высокая температура и плевральная боль. Бактериемия пневмококковая: женский пол, злоупотребление алкоголем, диабет, хроническая обструктивная болезнь легких, сухой кашель. Легионелла: молодые пациенты, курильщики, отсутствие сопутствующей патологии, понос, неврологической симптоматики, более тяжелый инфекционный процесс и полиорганное поражение (например, нарушение функции печени, повышенный уровень креатинкиназы). Микоплазма: молодые пациенты, предшествующий прием антибиотиков, меньше мультисистемного участия. Хламидофила: большая продолжительность симптомов до госпитализации, головная боль. Q лихорадка: мужчины, сухой кашель, высокая температура.
Пневмококк: повышение возраста, сопутствующие заболевания, острое начало, высокая температура и плевральная боль. Бактериемия пневмококковая: женский пол, злоупотребление алкоголем, диабет, хроническая обструктивная болезнь легких, сухой кашель. Легионелла: молодые пациенты, курильщики, отсутствие сопутствующей патологии, понос, неврологической симптоматики, более тяжелый инфекционный процесс и полиорганное поражение (например, нарушение функции печени, повышенный уровень креатинкиназы). Микоплазма: молодые пациенты, предшествующий прием антибиотиков, меньше мультисистемного участия. Хламидофила: большая продолжительность симптомов до госпитализации, головная боль. Q лихорадка: мужчины, сухой кашель, высокая температура.
 Патогенез • Аспирация секрета ротоглотки • Вдыхание аэрозоля, содержащего микроорганизмы • Гематогенное распространение инфекции из внелегочного очага • Непосредственное распространение из соседних пораженных органов
Патогенез • Аспирация секрета ротоглотки • Вдыхание аэрозоля, содержащего микроорганизмы • Гематогенное распространение инфекции из внелегочного очага • Непосредственное распространение из соседних пораженных органов
 Патогенез В 1 мл слюны содержится до 1 млрд. бактерий, поэтому аспирация даже одной капли слюны может внести в дыхательные пути большое количество микроорганизмов.
Патогенез В 1 мл слюны содержится до 1 млрд. бактерий, поэтому аспирация даже одной капли слюны может внести в дыхательные пути большое количество микроорганизмов.
 Патогенез Пневмококки различных серотипов могут бессимптомно персистировать на слизистых оболочках полости рта и верхних дыхательных путей. Проникновению их в дистальные отделы респираторного тракта препятствуют защитные структуры организма: • лимфоидные миндалины, • бактерицидные свойства слюны и носовой слизи, • мукоцилиарный аппарат трахеобронхиального дерева, • фагоцитарная активность нейтрофилов и альвеолярных макрофагов, • гуморальные факторы бронхиального секрета (иммуноглобулины А и G, система комплемента, лизоцим, интерферон, лактоферрин, ингибиторы протеаз).
Патогенез Пневмококки различных серотипов могут бессимптомно персистировать на слизистых оболочках полости рта и верхних дыхательных путей. Проникновению их в дистальные отделы респираторного тракта препятствуют защитные структуры организма: • лимфоидные миндалины, • бактерицидные свойства слюны и носовой слизи, • мукоцилиарный аппарат трахеобронхиального дерева, • фагоцитарная активность нейтрофилов и альвеолярных макрофагов, • гуморальные факторы бронхиального секрета (иммуноглобулины А и G, система комплемента, лизоцим, интерферон, лактоферрин, ингибиторы протеаз).
 Патогенез Ведущее значение в патогенезе пневмоний приобретают факторы, нарушающие динамическое равновесие между макро- и микроорганизмами. К таким неблагоприятным обстоятельствам относятся: • переохлаждение (расстройства микроциркуляции и нарушение мукоцилиарного клиренса), • острые респираторные заболевания (угнетение системы местных защитных факторов), • переутомление, • гиповитаминоз, • стрессовые ситуации, • десинхронозы • другие факторы, нарушающие резистентность организма
Патогенез Ведущее значение в патогенезе пневмоний приобретают факторы, нарушающие динамическое равновесие между макро- и микроорганизмами. К таким неблагоприятным обстоятельствам относятся: • переохлаждение (расстройства микроциркуляции и нарушение мукоцилиарного клиренса), • острые респираторные заболевания (угнетение системы местных защитных факторов), • переутомление, • гиповитаминоз, • стрессовые ситуации, • десинхронозы • другие факторы, нарушающие резистентность организма
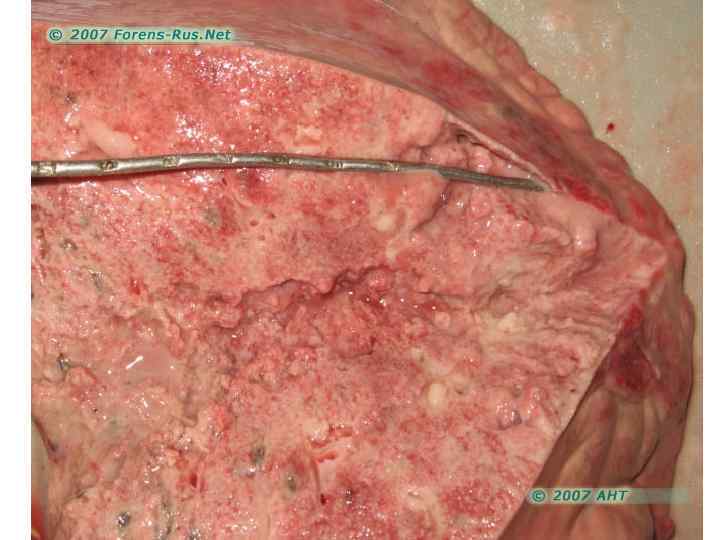
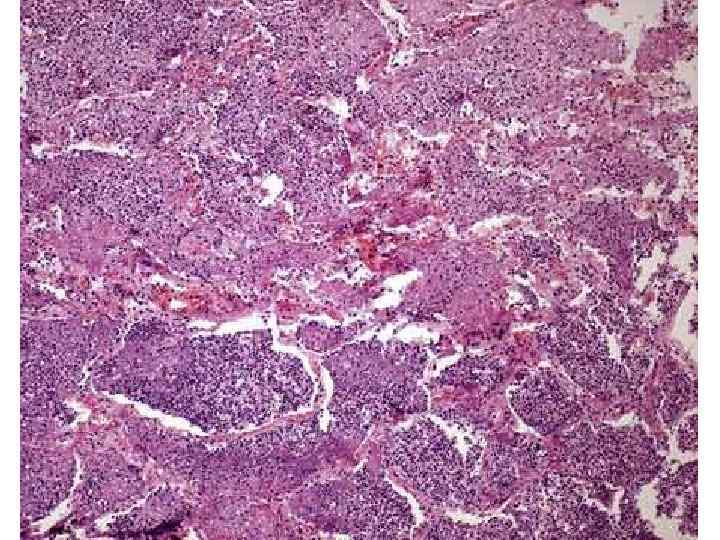
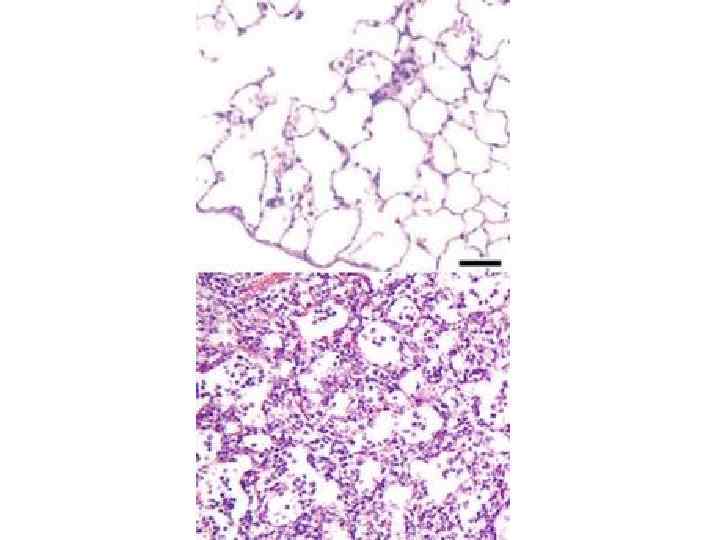
 Клиника пневмоний • Легочные проявления • Внелегочные проявления
Клиника пневмоний • Легочные проявления • Внелегочные проявления
 Клиника пневмоний • Легочные проявления • одышка; • кашель; • выделение мокроты (слизистая, слизисто-гнойная, «ржавая» и т. д. ); • боли при глубоком дыхании; • локальные клинические признаки (притупление перкуторного звука, бронхиальное дыхание, крепитация, шум трения плевры); • локальные рентгенологические признаки • Внелегочные проявления
Клиника пневмоний • Легочные проявления • одышка; • кашель; • выделение мокроты (слизистая, слизисто-гнойная, «ржавая» и т. д. ); • боли при глубоком дыхании; • локальные клинические признаки (притупление перкуторного звука, бронхиальное дыхание, крепитация, шум трения плевры); • локальные рентгенологические признаки • Внелегочные проявления
 Клиника пневмоний • Легочные проявления • Внелегочные проявления • • • лихорадка; ознобы и потливость; миалгии; головная боль; цианоз; тахикардия; herpes labialis; кожная сыпь, поражения слизистых (конъюнктивит); спутанность сознания; диарея; желтуха; изменения со стороны периферической крови (лейкоцитоз, сдвиг формулы влево, токсическая зернистость нейтрофилов, повышение СОЭ).
Клиника пневмоний • Легочные проявления • Внелегочные проявления • • • лихорадка; ознобы и потливость; миалгии; головная боль; цианоз; тахикардия; herpes labialis; кожная сыпь, поражения слизистых (конъюнктивит); спутанность сознания; диарея; желтуха; изменения со стороны периферической крови (лейкоцитоз, сдвиг формулы влево, токсическая зернистость нейтрофилов, повышение СОЭ).
 Критерии диагноза • Рентгенологически подтвержденная очаговая инфильтрация легочной ткани • Плюс хотя бы 2 клинических признака: – Острая лихорадка в начале заболевания (to>38, 0 o. C) – Кашель с мокротой – Физические признаки (укорочение перкуторного звука, жесткое везикулярное или бронхиальное дыхание, фокус крепитации и/или мелкопузырчатые хрипы) – Лейкоцитоз > 10 х 109/л и/или палочкоядерный сдвиг (>10%) Чучалин А. Г. , 2010
Критерии диагноза • Рентгенологически подтвержденная очаговая инфильтрация легочной ткани • Плюс хотя бы 2 клинических признака: – Острая лихорадка в начале заболевания (to>38, 0 o. C) – Кашель с мокротой – Физические признаки (укорочение перкуторного звука, жесткое везикулярное или бронхиальное дыхание, фокус крепитации и/или мелкопузырчатые хрипы) – Лейкоцитоз > 10 х 109/л и/или палочкоядерный сдвиг (>10%) Чучалин А. Г. , 2010
 Критерии диагноза Диагноз ВП является определенным при наличии у больного рентгенологически подтвержденной очаговой инфильтрации легочной ткани и, по крайней мере, двух клинических признаков из числа следующих: а) острая лихорадка в начале заболевания (t 0 > 38, 0°С); б) кашель с мокротой; в) физические признаки (фокус крепитации и/или мелкопузырчатые хрипы, жесткое бронхиальное дыхание, укорочение перкуторного звука); г) лейкоцитоз > 10· 109/л и/или палочкоядерный сдвиг (> 10%). В этой связи следует по возможности стремиться к клинико-рентгенологическому подтверждению диагноза ВП. При этом необходимо учитывать и вероятность известных синдромосходных заболеваний/патологических состояний.
Критерии диагноза Диагноз ВП является определенным при наличии у больного рентгенологически подтвержденной очаговой инфильтрации легочной ткани и, по крайней мере, двух клинических признаков из числа следующих: а) острая лихорадка в начале заболевания (t 0 > 38, 0°С); б) кашель с мокротой; в) физические признаки (фокус крепитации и/или мелкопузырчатые хрипы, жесткое бронхиальное дыхание, укорочение перкуторного звука); г) лейкоцитоз > 10· 109/л и/или палочкоядерный сдвиг (> 10%). В этой связи следует по возможности стремиться к клинико-рентгенологическому подтверждению диагноза ВП. При этом необходимо учитывать и вероятность известных синдромосходных заболеваний/патологических состояний.
 Критерии диагноза Отсутствие или недоступность рентгенологического подтверждения очаговой инфильтрации в легких (рентгенография или крупнокадровая флюорография органов грудной клетки) делает диагноз ВП неточным/неопределенным. При этом диагноз заболевания основывается на учете данных эпидемиологического анамнеза, жалоб и соответствующих локальных симптомов.
Критерии диагноза Отсутствие или недоступность рентгенологического подтверждения очаговой инфильтрации в легких (рентгенография или крупнокадровая флюорография органов грудной клетки) делает диагноз ВП неточным/неопределенным. При этом диагноз заболевания основывается на учете данных эпидемиологического анамнеза, жалоб и соответствующих локальных симптомов.
 Критерии диагноза Если при обследовании пациента с лихорадкой, жалобами на кашель, одышку, отделение мокроты и/или боли в грудной клетке рентгенологическое исследование оказывается недоступным и отсутствует соответствующая локальная симптоматика (укорочение/тупость перкуторного звука над пораженным участком легкого, локально выслушиваемое бронхиальное дыхание, фокус звучных мелкопузырчатых хрипов или инспираторной крепитации, усиление бронхофонии и голосового дрожания), то предположение о ВП становится маловероятным.
Критерии диагноза Если при обследовании пациента с лихорадкой, жалобами на кашель, одышку, отделение мокроты и/или боли в грудной клетке рентгенологическое исследование оказывается недоступным и отсутствует соответствующая локальная симптоматика (укорочение/тупость перкуторного звука над пораженным участком легкого, локально выслушиваемое бронхиальное дыхание, фокус звучных мелкопузырчатых хрипов или инспираторной крепитации, усиление бронхофонии и голосового дрожания), то предположение о ВП становится маловероятным.
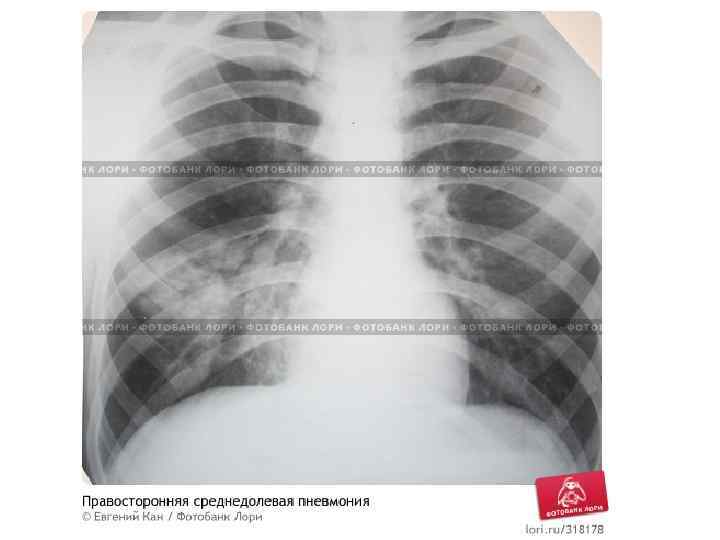
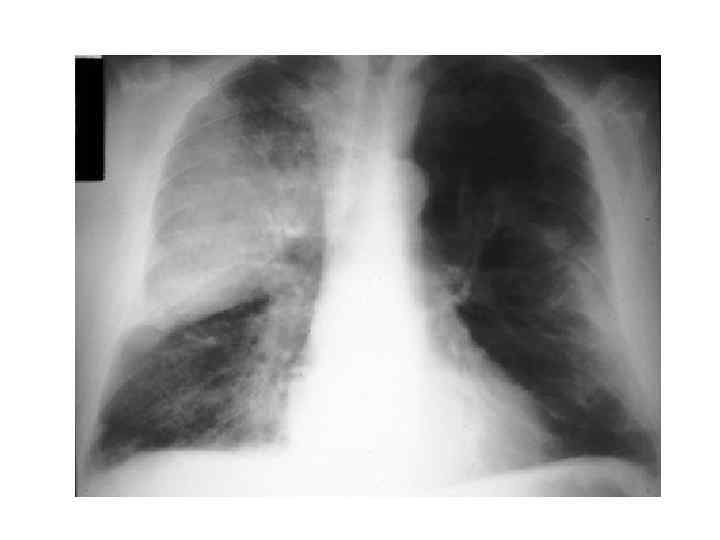
 Осложнения пневмоний • • Плевральный выпот Эмпиема плевры Деструкция/абсцедирование легочной ткани Острый респираторный дистресс-синдром Острая дыхательная недостаточность Септический шок Вторичная бактериемия, сепсис, гематогенные очаги отсева • Перикардит, миокардит • Нефрит и др.
Осложнения пневмоний • • Плевральный выпот Эмпиема плевры Деструкция/абсцедирование легочной ткани Острый респираторный дистресс-синдром Острая дыхательная недостаточность Септический шок Вторичная бактериемия, сепсис, гематогенные очаги отсева • Перикардит, миокардит • Нефрит и др.
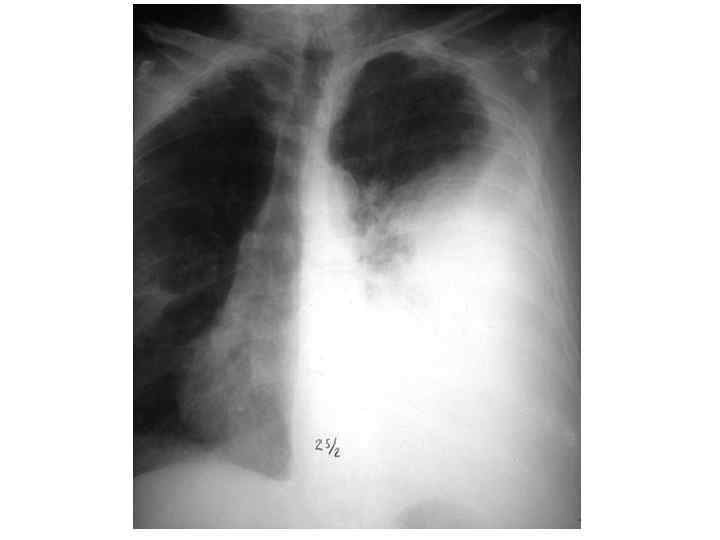
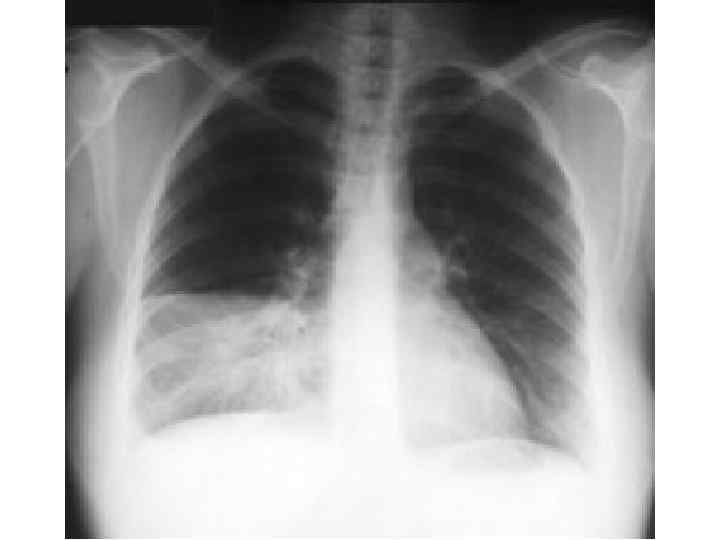
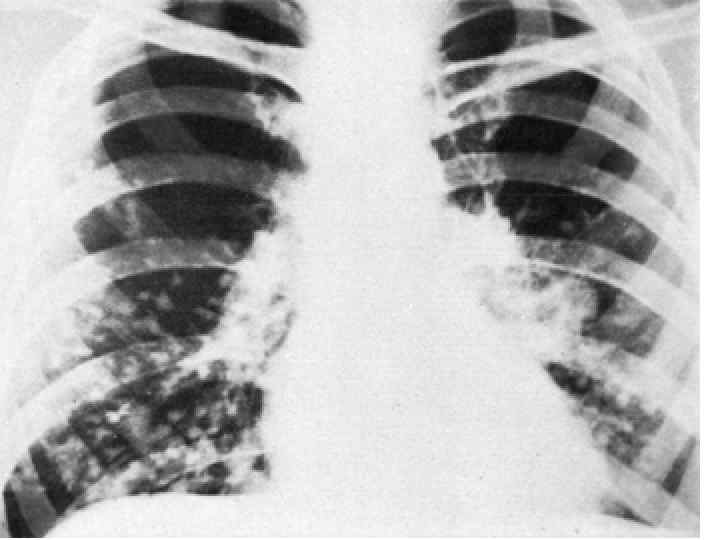
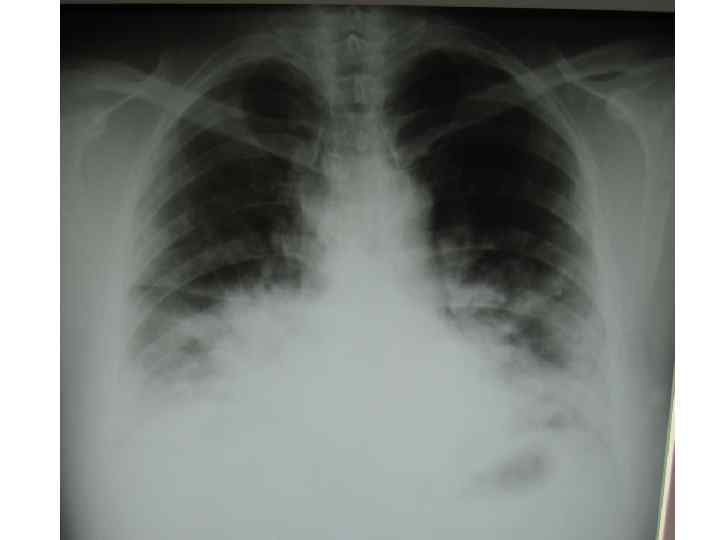
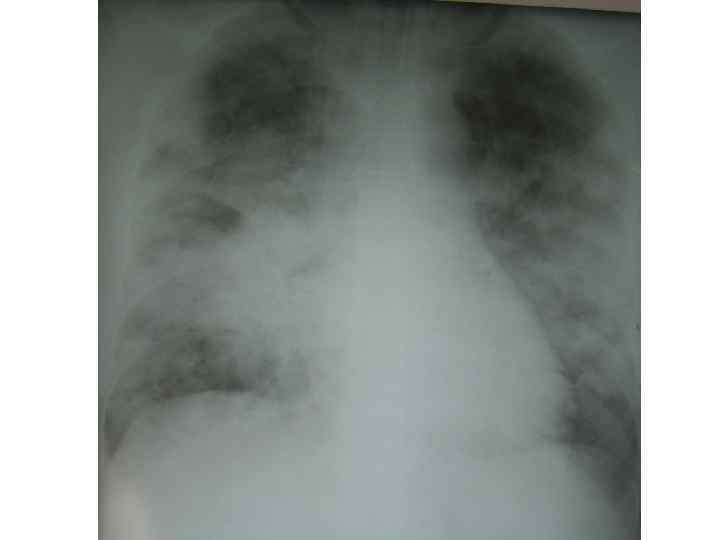
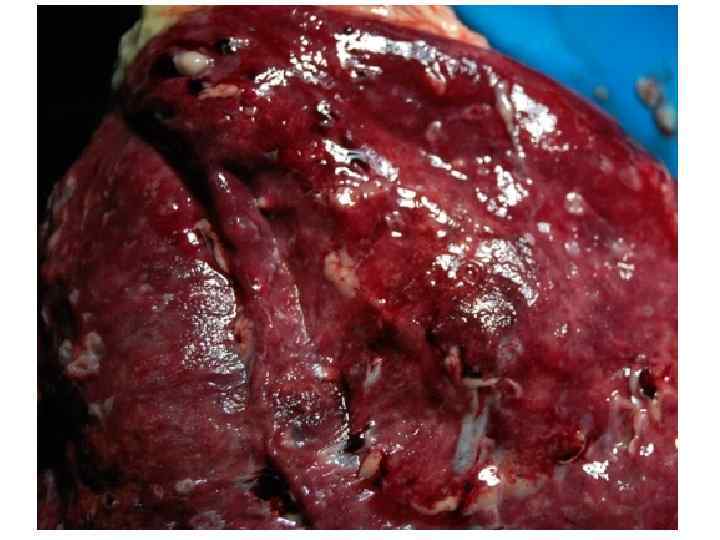
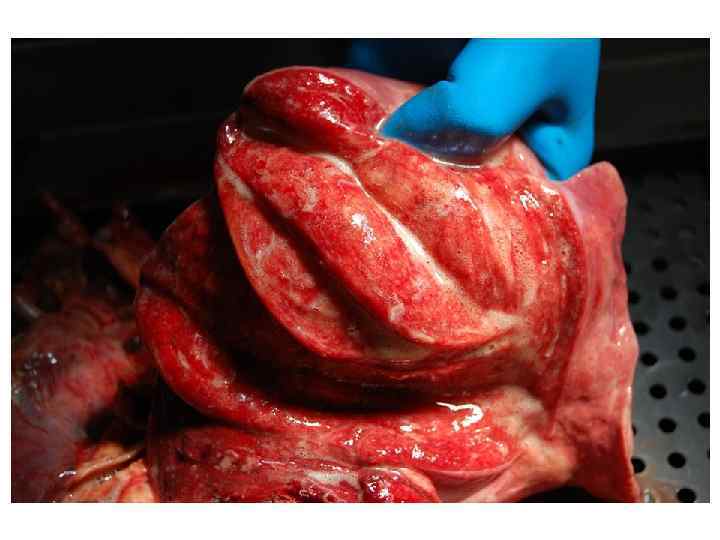
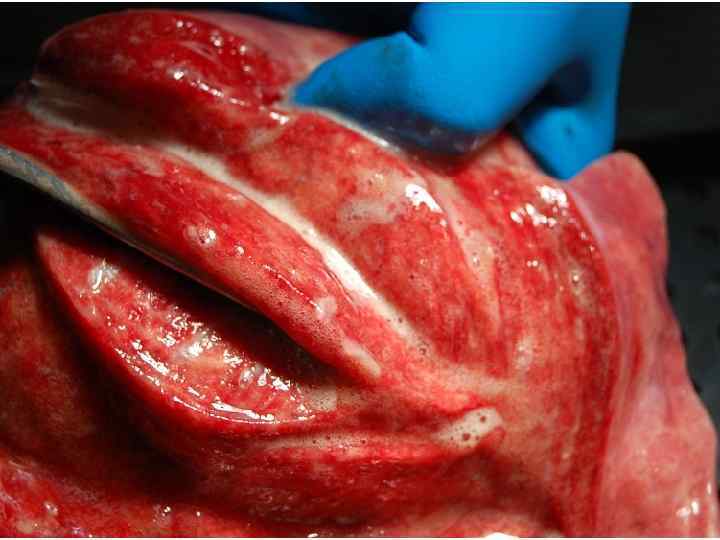

 Epidemiological report of pandemic (H 1 N 1) 2009 in the UK; April 2009 – May 2010
Epidemiological report of pandemic (H 1 N 1) 2009 in the UK; April 2009 – May 2010
 Параллельные бактериальные инфекции 1. Параллельное бактериальные инфекции (ПБИ) не были определены в качестве одной из главных особенностей пандемии. 2. Среди 20288 случаев английской пандемии гриппа (H 1 N 1) в общей сложности 76 связаны с ПБИ (0, 4%). 3. Среди инфекционных агентов были определены: • 39 случаев S. pneumoniae, • 34 случаев S. aureus, • 3 случая S. pyogenes. 4. 24 больных из этих случаев, связанных с ПБИ (0, 9%), были госпитализированы, и 16 (67%) закончились смертельным исходом. Epidemiological report of pandemic (H 1 N 1) 2009 in the UK; April 2009 – May 2010
Параллельные бактериальные инфекции 1. Параллельное бактериальные инфекции (ПБИ) не были определены в качестве одной из главных особенностей пандемии. 2. Среди 20288 случаев английской пандемии гриппа (H 1 N 1) в общей сложности 76 связаны с ПБИ (0, 4%). 3. Среди инфекционных агентов были определены: • 39 случаев S. pneumoniae, • 34 случаев S. aureus, • 3 случая S. pyogenes. 4. 24 больных из этих случаев, связанных с ПБИ (0, 9%), были госпитализированы, и 16 (67%) закончились смертельным исходом. Epidemiological report of pandemic (H 1 N 1) 2009 in the UK; April 2009 – May 2010
 Критерии тяжелого течения Клинические Лабораторные • Острая дыхательная недостаточность (ЧДД≥ 30 в мин) • Гипотензия (АДсист<90 мм рт. ст. ) • Двух- и многодолевое поражение • Нарушение сознания • Внелегочный очаг инфекции • Лейкопения (< 4 х 109/л) • Гипоксемия (Sa. O 2<90%, PO 2<60 мм рт. ст. ) • Гемоглобин < 100 г/л • Гематокрит < 30% • Острая почечная недостаточность (анурия, мочевина > 7, 0 ммоль/л) При наличии хотя бы одного критерия пневмония расценивается как тяжеля!
Критерии тяжелого течения Клинические Лабораторные • Острая дыхательная недостаточность (ЧДД≥ 30 в мин) • Гипотензия (АДсист<90 мм рт. ст. ) • Двух- и многодолевое поражение • Нарушение сознания • Внелегочный очаг инфекции • Лейкопения (< 4 х 109/л) • Гипоксемия (Sa. O 2<90%, PO 2<60 мм рт. ст. ) • Гемоглобин < 100 г/л • Гематокрит < 30% • Острая почечная недостаточность (анурия, мочевина > 7, 0 ммоль/л) При наличии хотя бы одного критерия пневмония расценивается как тяжеля!
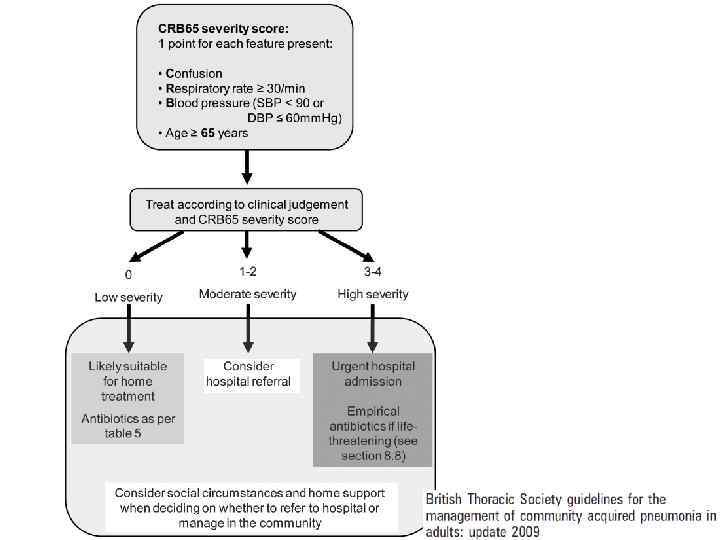
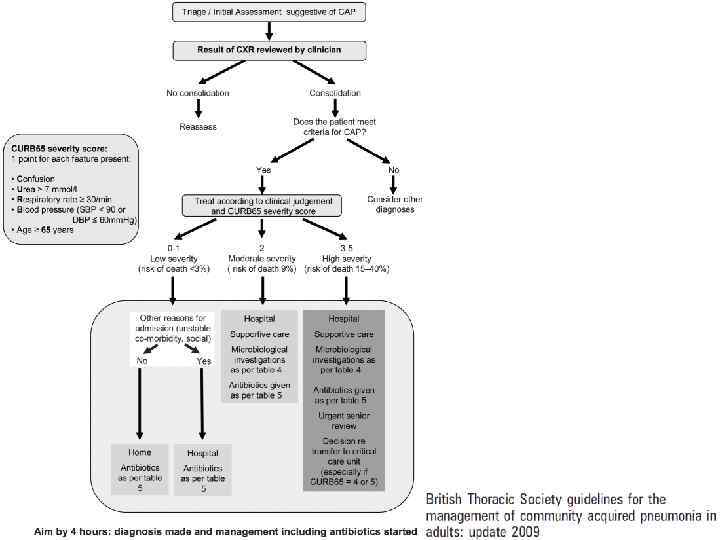
 Критерии тяжести ВП При поступлении пациента с ВП в стационар необходимо, прежде всего, оценить тяжесть его состояния и решить вопрос о месте лечения (амбулаторно, стационарно в отделении общего профиля или ОРИТ). Для отбора больных ВП, которые могут лечиться амбулаторно, рекомендуется использовать шкалы определения тяжести ВП, такие как критерии Британского торакального общества (CURB-65) либо Американские критерии Pneumonia Severe Index – PSI. Оценка неблагоприятного исхода по шкале CURB-65: 1) Нарушение сознания (Confusion) 2) уровень мочевины крови > 7 ммоль/л (Urea) 3) частота дыхания ≥ 30 в мин (Respiratory rate) 4) низкое АД (систолическое < 90 мм рт. ст. или диастолическое ≤ 60 мм рт. ст. ) (Blood pressure) 5) возраст ≥ 65 лет (65). Суммарная оценка по шкале CURB-65 в пределах 0 -1 баллов предполагает лечение ВП в амбулаторных условиях, 2 балла – в стационаре в условиях отделения общего профиля, 3 и более баллов – в ОИТ.
Критерии тяжести ВП При поступлении пациента с ВП в стационар необходимо, прежде всего, оценить тяжесть его состояния и решить вопрос о месте лечения (амбулаторно, стационарно в отделении общего профиля или ОРИТ). Для отбора больных ВП, которые могут лечиться амбулаторно, рекомендуется использовать шкалы определения тяжести ВП, такие как критерии Британского торакального общества (CURB-65) либо Американские критерии Pneumonia Severe Index – PSI. Оценка неблагоприятного исхода по шкале CURB-65: 1) Нарушение сознания (Confusion) 2) уровень мочевины крови > 7 ммоль/л (Urea) 3) частота дыхания ≥ 30 в мин (Respiratory rate) 4) низкое АД (систолическое < 90 мм рт. ст. или диастолическое ≤ 60 мм рт. ст. ) (Blood pressure) 5) возраст ≥ 65 лет (65). Суммарная оценка по шкале CURB-65 в пределах 0 -1 баллов предполагает лечение ВП в амбулаторных условиях, 2 балла – в стационаре в условиях отделения общего профиля, 3 и более баллов – в ОИТ.
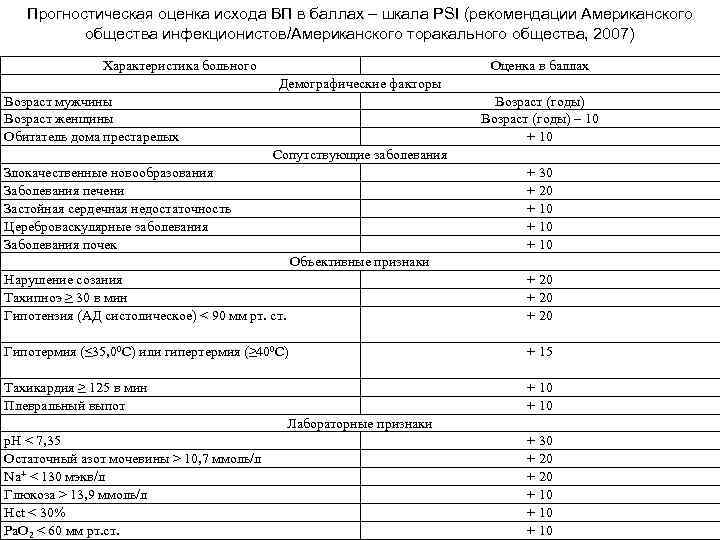 Прогностическая оценка исхода ВП в баллах – шкала PSI (рекомендации Американского общества инфекционистов/Американского торакального общества, 2007) Характеристика больного Оценка в баллах Демографические факторы Возраст мужчины Возраст женщины Обитатель дома престарелых Возраст (годы) – 10 + 10 Сопутствующие заболевания Злокачественные новообразования Заболевания печени Застойная сердечная недостаточность Цереброваскулярные заболевания Заболевания почек + 30 + 20 + 10 Объективные признаки Нарушение созания Тахипноэ ≥ 30 в мин Гипотензия (АД систолическое) < 90 мм рт. ст. + 20 Гипотермия (≤ 35, 00 С) или гипертермия (≥ 400 С) + 15 Тахикардия ≥ 125 в мин Плевральный выпот + 10 Лабораторные признаки p. H < 7, 35 Остаточный азот мочевины > 10, 7 ммоль/л Na+ < 130 мэкв/л Глюкоза > 13, 9 ммоль/л Hct < 30% Pa. O 2 < 60 мм рт. ст. + 30 + 20 + 10
Прогностическая оценка исхода ВП в баллах – шкала PSI (рекомендации Американского общества инфекционистов/Американского торакального общества, 2007) Характеристика больного Оценка в баллах Демографические факторы Возраст мужчины Возраст женщины Обитатель дома престарелых Возраст (годы) – 10 + 10 Сопутствующие заболевания Злокачественные новообразования Заболевания печени Застойная сердечная недостаточность Цереброваскулярные заболевания Заболевания почек + 30 + 20 + 10 Объективные признаки Нарушение созания Тахипноэ ≥ 30 в мин Гипотензия (АД систолическое) < 90 мм рт. ст. + 20 Гипотермия (≤ 35, 00 С) или гипертермия (≥ 400 С) + 15 Тахикардия ≥ 125 в мин Плевральный выпот + 10 Лабораторные признаки p. H < 7, 35 Остаточный азот мочевины > 10, 7 ммоль/л Na+ < 130 мэкв/л Глюкоза > 13, 9 ммоль/л Hct < 30% Pa. O 2 < 60 мм рт. ст. + 30 + 20 + 10
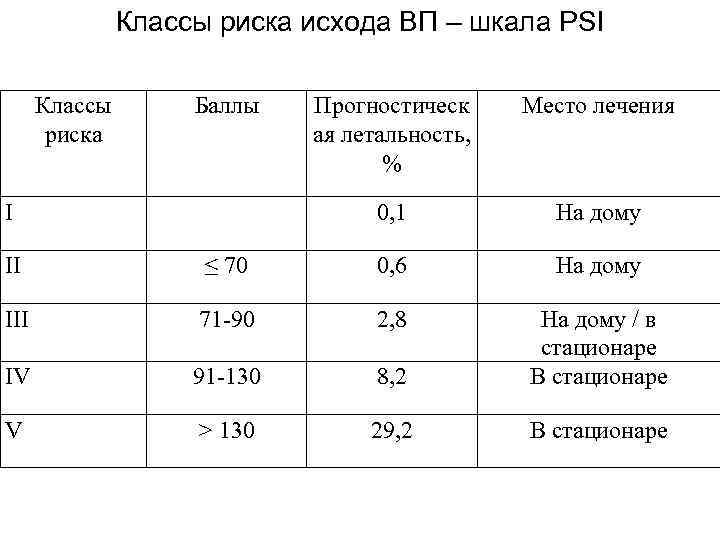 Классы риска исхода ВП – шкала PSI Классы риска Баллы Место лечения 0, 1 I Прогностическ ая летальность, % На дому II ≤ 70 0, 6 На дому III 71 -90 2, 8 IV 91 -130 8, 2 На дому / в стационаре В стационаре V > 130 29, 2 В стационаре
Классы риска исхода ВП – шкала PSI Классы риска Баллы Место лечения 0, 1 I Прогностическ ая летальность, % На дому II ≤ 70 0, 6 На дому III 71 -90 2, 8 IV 91 -130 8, 2 На дому / в стационаре В стационаре V > 130 29, 2 В стационаре
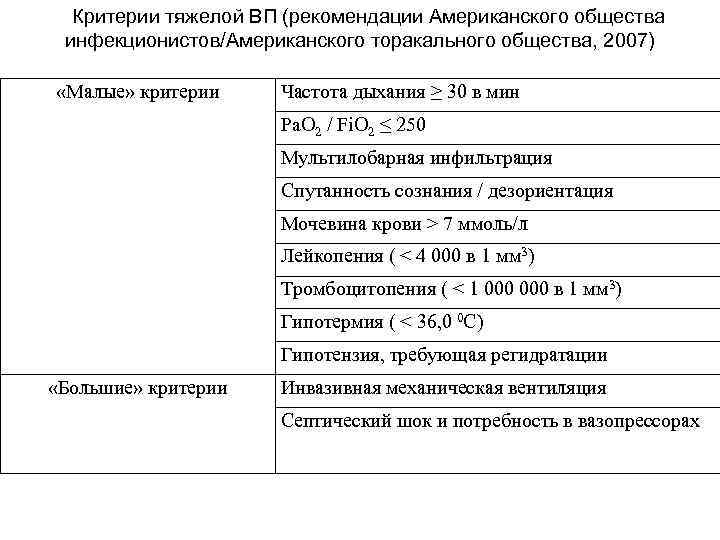 Критерии тяжелой ВП (рекомендации Американского общества инфекционистов/Американского торакального общества, 2007) «Малые» критерии Частота дыхания ≥ 30 в мин Pa. O 2 / Fi. O 2 ≤ 250 Мультилобарная инфильтрация Спутанность сознания / дезориентация Мочевина крови > 7 ммоль/л Лейкопения ( < 4 000 в 1 мм 3) Тромбоцитопения ( < 1 000 в 1 мм 3) Гипотермия ( < 36, 0 0 С) Гипотензия, требующая регидратации «Большие» критерии Инвазивная механическая вентиляция Септический шок и потребность в вазопрессорах
Критерии тяжелой ВП (рекомендации Американского общества инфекционистов/Американского торакального общества, 2007) «Малые» критерии Частота дыхания ≥ 30 в мин Pa. O 2 / Fi. O 2 ≤ 250 Мультилобарная инфильтрация Спутанность сознания / дезориентация Мочевина крови > 7 ммоль/л Лейкопения ( < 4 000 в 1 мм 3) Тромбоцитопения ( < 1 000 в 1 мм 3) Гипотермия ( < 36, 0 0 С) Гипотензия, требующая регидратации «Большие» критерии Инвазивная механическая вентиляция Септический шок и потребность в вазопрессорах
 Тяжелая внебольничная пневмония Это особая форма заболевания различной этиологии, проявляющаяся выраженной дыхательной недостаточностью и/или признаками тяжелого сепсиса или септического шока, характеризуется плохим прогнозом и требует проведения интенсивного лечения
Тяжелая внебольничная пневмония Это особая форма заболевания различной этиологии, проявляющаяся выраженной дыхательной недостаточностью и/или признаками тяжелого сепсиса или септического шока, характеризуется плохим прогнозом и требует проведения интенсивного лечения
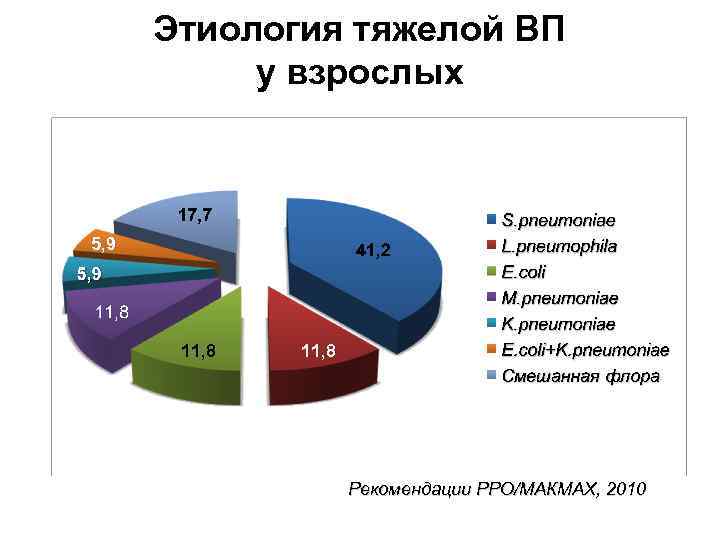 Этиология тяжелой ВП у взрослых 5, 9 11, 8 Рекомендации РРО/МАКМАХ, 2010
Этиология тяжелой ВП у взрослых 5, 9 11, 8 Рекомендации РРО/МАКМАХ, 2010
 Лечение • Этиотропное • Незамедлительное (в течение первых 4 -х часов) • Де-эскалационное • Ступенчатое
Лечение • Этиотропное • Незамедлительное (в течение первых 4 -х часов) • Де-эскалационное • Ступенчатое
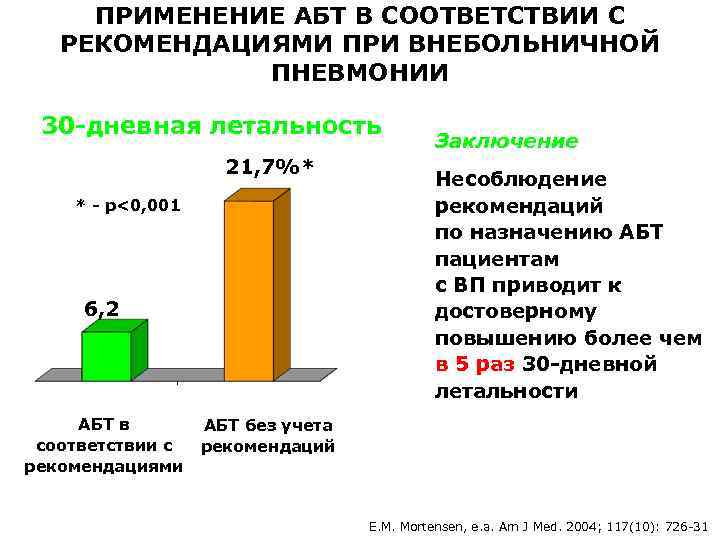 ПРИМЕНЕНИЕ АБТ В СООТВЕТСТВИИ С РЕКОМЕНДАЦИЯМИ ПРИ ВНЕБОЛЬНИЧНОЙ ПНЕВМОНИИ 30 -дневная летальность 21, 7%* * - р<0, 001 6, 2% АБТ в соответствии с рекомендациями Заключение Несоблюдение рекомендаций по назначению АБТ пациентам с ВП приводит к достоверному повышению более чем в 5 раз 30 -дневной летальности АБТ без учета рекомендаций E. M. Mortensen, е. а. Am J Med. 2004; 117(10): 726 -31
ПРИМЕНЕНИЕ АБТ В СООТВЕТСТВИИ С РЕКОМЕНДАЦИЯМИ ПРИ ВНЕБОЛЬНИЧНОЙ ПНЕВМОНИИ 30 -дневная летальность 21, 7%* * - р<0, 001 6, 2% АБТ в соответствии с рекомендациями Заключение Несоблюдение рекомендаций по назначению АБТ пациентам с ВП приводит к достоверному повышению более чем в 5 раз 30 -дневной летальности АБТ без учета рекомендаций E. M. Mortensen, е. а. Am J Med. 2004; 117(10): 726 -31
 Эмпирическая антибактериальная терапия антибиотиком широкого спектра действия с последующей де-эскалацией не приводит к селекции резистентности у грам(-) патогенов у пациентов с вентиляторассоциированной пневмонией Опубликовано: Пятница, 17 сентября 2010 г. - 09: 05 Приверженность тактике де-эксалации (т. е. смена антибактериальной терапии с учётом выделенных патогенов в течение 96 ч) составила 78% для имипенема/циластатина, 77, 2% для тобрамицина и 59% для левофлоксацина. Когда инфекционные заболевания, потребовавшие назначения имипенема/циластатина, были удалены из анализа, комплаентность увеличилась до 92%. Таким образом, ранее начало эмпирической антибактериальной терапии антибиотиком широкого спектра действия с последующей сменой на антибиотик узкого спектра действия в соответствии с выделенным бактериальным возбудителем не приводит к росту антибиотикорезистентности и является обоснованной тактикой ведения пациентов. Hibbard M. L. , Kopelman T. R. , O'Neill P. J. , Maly T. J. , Matthews M. R. , Cox J. C. , Vail S. J. , Quan A. N. , Drachman D. A. Empiric, Broad-Spectrum Antibiotic Therapy with an Aggressive De. Escalation Strategy Does Not Induce Gram-Negative Pathogen Resistance in Ventilator. Associated Pneumonia. Surg Infect (Larchmt). 2010 Sep 6
Эмпирическая антибактериальная терапия антибиотиком широкого спектра действия с последующей де-эскалацией не приводит к селекции резистентности у грам(-) патогенов у пациентов с вентиляторассоциированной пневмонией Опубликовано: Пятница, 17 сентября 2010 г. - 09: 05 Приверженность тактике де-эксалации (т. е. смена антибактериальной терапии с учётом выделенных патогенов в течение 96 ч) составила 78% для имипенема/циластатина, 77, 2% для тобрамицина и 59% для левофлоксацина. Когда инфекционные заболевания, потребовавшие назначения имипенема/циластатина, были удалены из анализа, комплаентность увеличилась до 92%. Таким образом, ранее начало эмпирической антибактериальной терапии антибиотиком широкого спектра действия с последующей сменой на антибиотик узкого спектра действия в соответствии с выделенным бактериальным возбудителем не приводит к росту антибиотикорезистентности и является обоснованной тактикой ведения пациентов. Hibbard M. L. , Kopelman T. R. , O'Neill P. J. , Maly T. J. , Matthews M. R. , Cox J. C. , Vail S. J. , Quan A. N. , Drachman D. A. Empiric, Broad-Spectrum Antibiotic Therapy with an Aggressive De. Escalation Strategy Does Not Induce Gram-Negative Pathogen Resistance in Ventilator. Associated Pneumonia. Surg Infect (Larchmt). 2010 Sep 6
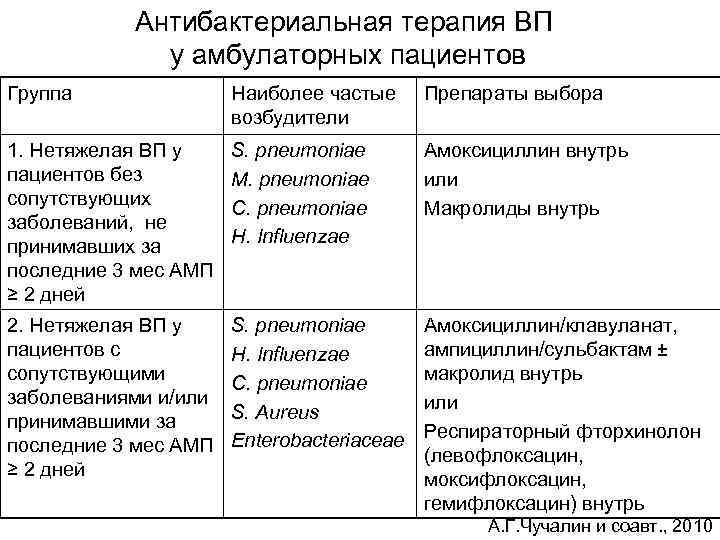 Антибактериальная терапия ВП у амбулаторных пациентов Группа Наиболее частые возбудители Препараты выбора 1. Нетяжелая ВП у пациентов без сопутствующих заболеваний, не принимавших за последние 3 мес АМП ≥ 2 дней S. pneumoniae M. pneumoniae C. pneumoniae H. Influenzae Амоксициллин внутрь или Макролиды внутрь 2. Нетяжелая ВП у пациентов с сопутствующими заболеваниями и/или принимавшими за последние 3 мес АМП ≥ 2 дней S. pneumoniae H. Influenzae C. pneumoniae S. Aureus Enterobacteriaceae Амоксициллин/клавуланат, ампициллин/сульбактам ± макролид внутрь или Респираторный фторхинолон (левофлоксацин, моксифлоксацин, гемифлоксацин) внутрь А. Г. Чучалин и соавт. , 2010
Антибактериальная терапия ВП у амбулаторных пациентов Группа Наиболее частые возбудители Препараты выбора 1. Нетяжелая ВП у пациентов без сопутствующих заболеваний, не принимавших за последние 3 мес АМП ≥ 2 дней S. pneumoniae M. pneumoniae C. pneumoniae H. Influenzae Амоксициллин внутрь или Макролиды внутрь 2. Нетяжелая ВП у пациентов с сопутствующими заболеваниями и/или принимавшими за последние 3 мес АМП ≥ 2 дней S. pneumoniae H. Influenzae C. pneumoniae S. Aureus Enterobacteriaceae Амоксициллин/клавуланат, ампициллин/сульбактам ± макролид внутрь или Респираторный фторхинолон (левофлоксацин, моксифлоксацин, гемифлоксацин) внутрь А. Г. Чучалин и соавт. , 2010
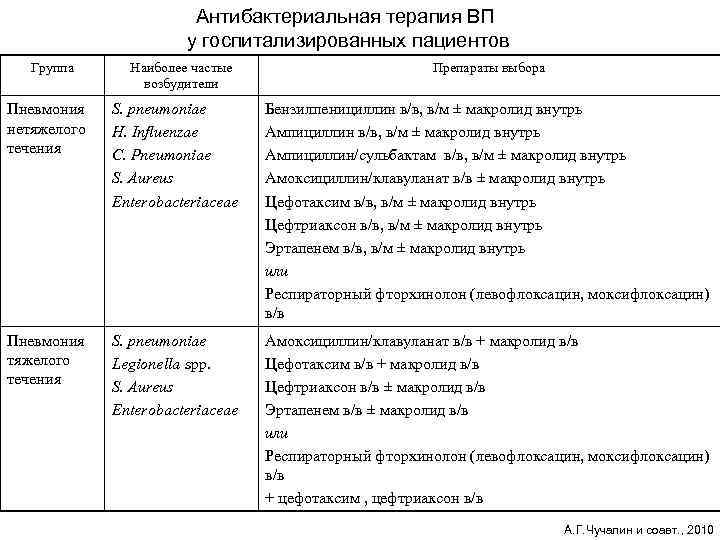 Антибактериальная терапия ВП у госпитализированных пациентов Группа Наиболее частые возбудители Препараты выбора Пневмония нетяжелого течения S. pneumoniae H. Influenzae C. Pneumoniae S. Aureus Enterobacteriaceae Бензилпенициллин в/в, в/м ± макролид внутрь Ампициллин/сульбактам в/в, в/м ± макролид внутрь Амоксициллин/клавуланат в/в ± макролид внутрь Цефотаксим в/в, в/м ± макролид внутрь Цефтриаксон в/в, в/м ± макролид внутрь Эртапенем в/в, в/м ± макролид внутрь или Респираторный фторхинолон (левофлоксацин, моксифлоксацин) в/в Пневмония тяжелого течения S. pneumoniae Legionella spp. S. Aureus Enterobacteriaceae Амоксициллин/клавуланат в/в + макролид в/в Цефотаксим в/в + макролид в/в Цефтриаксон в/в ± макролид в/в Эртапенем в/в ± макролид в/в или Респираторный фторхинолон (левофлоксацин, моксифлоксацин) в/в + цефотаксим , цефтриаксон в/в А. Г. Чучалин и соавт. , 2010
Антибактериальная терапия ВП у госпитализированных пациентов Группа Наиболее частые возбудители Препараты выбора Пневмония нетяжелого течения S. pneumoniae H. Influenzae C. Pneumoniae S. Aureus Enterobacteriaceae Бензилпенициллин в/в, в/м ± макролид внутрь Ампициллин/сульбактам в/в, в/м ± макролид внутрь Амоксициллин/клавуланат в/в ± макролид внутрь Цефотаксим в/в, в/м ± макролид внутрь Цефтриаксон в/в, в/м ± макролид внутрь Эртапенем в/в, в/м ± макролид внутрь или Респираторный фторхинолон (левофлоксацин, моксифлоксацин) в/в Пневмония тяжелого течения S. pneumoniae Legionella spp. S. Aureus Enterobacteriaceae Амоксициллин/клавуланат в/в + макролид в/в Цефотаксим в/в + макролид в/в Цефтриаксон в/в ± макролид в/в Эртапенем в/в ± макролид в/в или Респираторный фторхинолон (левофлоксацин, моксифлоксацин) в/в + цефотаксим , цефтриаксон в/в А. Г. Чучалин и соавт. , 2010
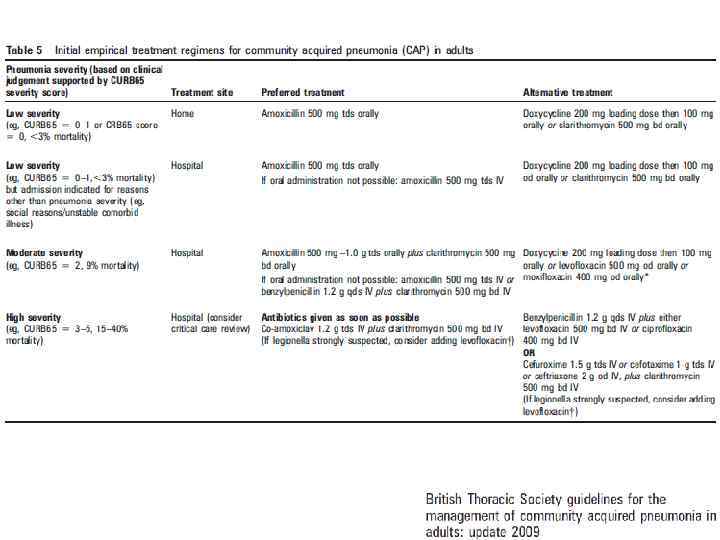
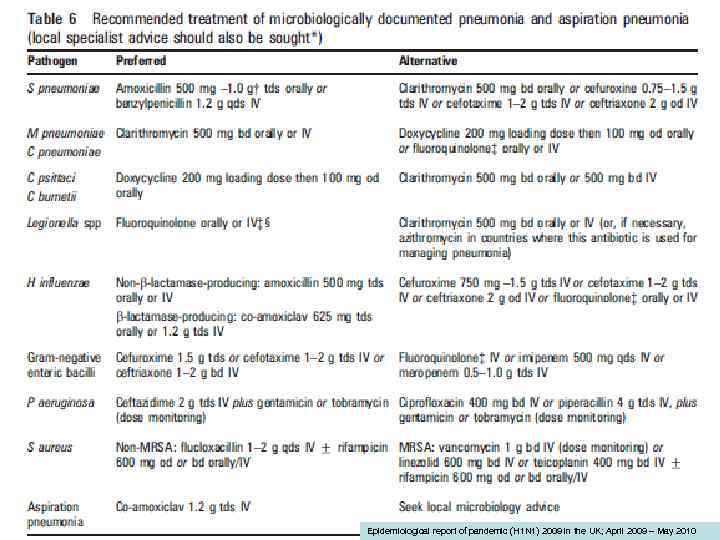 Epidemiological report of pandemic (H 1 N 1) 2009 in the UK; April 2009 – May 2010
Epidemiological report of pandemic (H 1 N 1) 2009 in the UK; April 2009 – May 2010
 В последнее время наблюдается рост числа ВП, вызываемых внебольничными штаммами MRSA. Продукция данным возбудителем лейкоцидина Panton-Valentine и других токсинов обусловливает развитие осложнений пневмонии (деструкция / абсцедирование легочной ткани, эмпиема плевры, шок, дыхательная недостаточность). Предположение о внебольничном MRSA следует допускать у больных с абсцедированием легочных инфильтратов при отсутствии факторов риска аспирационной пневмонии (злоупотребление алкоголем, нарушение моторики пищевода, нарушение сознания, инсульт, заболевания десен)
В последнее время наблюдается рост числа ВП, вызываемых внебольничными штаммами MRSA. Продукция данным возбудителем лейкоцидина Panton-Valentine и других токсинов обусловливает развитие осложнений пневмонии (деструкция / абсцедирование легочной ткани, эмпиема плевры, шок, дыхательная недостаточность). Предположение о внебольничном MRSA следует допускать у больных с абсцедированием легочных инфильтратов при отсутствии факторов риска аспирационной пневмонии (злоупотребление алкоголем, нарушение моторики пищевода, нарушение сознания, инсульт, заболевания десен)
 Epidemiological report of pandemic (H 1 N 1) 2009 in the UK; April 2009 – May 2010
Epidemiological report of pandemic (H 1 N 1) 2009 in the UK; April 2009 – May 2010
 Критерии достаточности антибактериальной терапии ВП • Температура < 37, 5 о. С • Отсутствие интоксикации • Отсутствие дыхательной недостаточности (ЧДД<20 в мин) • Отсутствие гнойной мокроты • Количество лейкоцитов в крови <10 х 109/л • Отсутствие отрицательной динамики на рентгенограмме
Критерии достаточности антибактериальной терапии ВП • Температура < 37, 5 о. С • Отсутствие интоксикации • Отсутствие дыхательной недостаточности (ЧДД<20 в мин) • Отсутствие гнойной мокроты • Количество лейкоцитов в крови <10 х 109/л • Отсутствие отрицательной динамики на рентгенограмме
 Индикаторы качества клинической работы с госпитализированным больным ВП (Чучалин А. Г. и др. , 2010): 1. Рентгенологическое исследование органов грудной клетки при наличии клинических признаков ВП в течение 24 ч с момента госпитализации (если не выполнялось на амбулаторном этапе). 2. Бактериологическое исследование мокроты до назначения антибиотиков. 3. Бактериологическое исследование крови до назначения антибиотиков (у пациентов с тяжелой ВП). 4. Введение первой дозы системного антибиотика в первые 4 ч с момента госпитализации. 5. Соответствие стартового режима антибактериальной терапии национальным рекомендациям. 6. Использование ступенчатой антибактериальной терапии (для пациентов, нуждающихся в парентеральном назначении антибиотиков). 7. Наличие рекомендаций по вакцинации пненвмококковой вакциной пациентам из группы риска. 8. Наличие рекомендаций по вакцинации гриппозной вакциной (в осеннезимний сезон) пациентам из группы риска.
Индикаторы качества клинической работы с госпитализированным больным ВП (Чучалин А. Г. и др. , 2010): 1. Рентгенологическое исследование органов грудной клетки при наличии клинических признаков ВП в течение 24 ч с момента госпитализации (если не выполнялось на амбулаторном этапе). 2. Бактериологическое исследование мокроты до назначения антибиотиков. 3. Бактериологическое исследование крови до назначения антибиотиков (у пациентов с тяжелой ВП). 4. Введение первой дозы системного антибиотика в первые 4 ч с момента госпитализации. 5. Соответствие стартового режима антибактериальной терапии национальным рекомендациям. 6. Использование ступенчатой антибактериальной терапии (для пациентов, нуждающихся в парентеральном назначении антибиотиков). 7. Наличие рекомендаций по вакцинации пненвмококковой вакциной пациентам из группы риска. 8. Наличие рекомендаций по вакцинации гриппозной вакциной (в осеннезимний сезон) пациентам из группы риска.
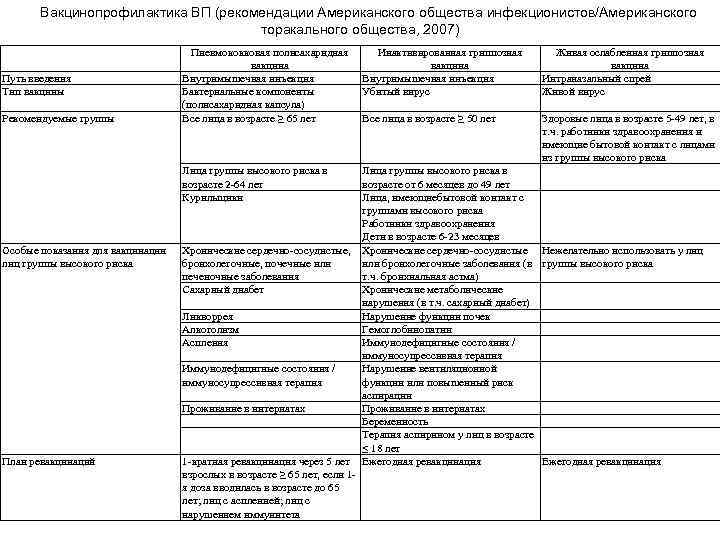 Вакцинопрофилактика ВП (рекомендации Американского общества инфекционистов/Американского торакального общества, 2007) Путь введения Тип вакцины Рекомендуемые группы Пневмококковая полисахаридная вакцина Внутримышечная инъекция Бактериальные компоненты (полисахаридная капсула) Все лица в возрасте ≥ 65 лет Лица группы высокого риска в возрасте 2 -64 лет Курильщики Особые показания для вакцинации лиц группы высокого риска План ревакцинаций Инактивированная гриппозная вакцина Внутримышечная инъекция Убитый вирус Живая ослабленная гриппозная вакцина Интраназальный спрей Живой вирус Все лица в возрасте ≥ 50 лет Здоровые лица в возрасте 5 -49 лет, в т. ч. работники здравоохранения и имеющие бытовой контакт с лицами из группы высокого риска Лица группы высокого риска в возрасте от 6 месяцев до 49 лет Лица, имеющиебытовой контакт с группами высокого риска Работники здравоохранения Дети в возрасте 6 -23 месяцев Хронические сердечно-сосудистые, Хронические сердечно-сосудистые Нежелательно использовать у лиц бронхолегочные, почечные или бронхолегочные заболевания (в группы высокого риска печеночные заболевания т. ч. бронхиальная астма) Сахарный диабет Хронические метаболические нарушения (в т. ч. сахарный диабет) Ликворрея Нарушение функции почек Алкоголизм Гемоглобинопатии Аспления Иммунодефицитные состояния / иммуносупрессивная терапия Иммунодефицитные состояния / Нарушение вентиляционной иммуносупрессивная терапия функции или повышенный риск аспирации Проживание в интернатах Беременность Терапия аспирином у лиц в возрасте ≤ 18 лет 1 -кратная ревакцинация через 5 лет Ежегодная ревакцинация взрослых в возрасте ≥ 65 лет, если 1 я доза вводилась в возрасте до 65 лет; лиц с аспленией; лиц с нарушением иммунитета
Вакцинопрофилактика ВП (рекомендации Американского общества инфекционистов/Американского торакального общества, 2007) Путь введения Тип вакцины Рекомендуемые группы Пневмококковая полисахаридная вакцина Внутримышечная инъекция Бактериальные компоненты (полисахаридная капсула) Все лица в возрасте ≥ 65 лет Лица группы высокого риска в возрасте 2 -64 лет Курильщики Особые показания для вакцинации лиц группы высокого риска План ревакцинаций Инактивированная гриппозная вакцина Внутримышечная инъекция Убитый вирус Живая ослабленная гриппозная вакцина Интраназальный спрей Живой вирус Все лица в возрасте ≥ 50 лет Здоровые лица в возрасте 5 -49 лет, в т. ч. работники здравоохранения и имеющие бытовой контакт с лицами из группы высокого риска Лица группы высокого риска в возрасте от 6 месяцев до 49 лет Лица, имеющиебытовой контакт с группами высокого риска Работники здравоохранения Дети в возрасте 6 -23 месяцев Хронические сердечно-сосудистые, Хронические сердечно-сосудистые Нежелательно использовать у лиц бронхолегочные, почечные или бронхолегочные заболевания (в группы высокого риска печеночные заболевания т. ч. бронхиальная астма) Сахарный диабет Хронические метаболические нарушения (в т. ч. сахарный диабет) Ликворрея Нарушение функции почек Алкоголизм Гемоглобинопатии Аспления Иммунодефицитные состояния / иммуносупрессивная терапия Иммунодефицитные состояния / Нарушение вентиляционной иммуносупрессивная терапия функции или повышенный риск аспирации Проживание в интернатах Беременность Терапия аспирином у лиц в возрасте ≤ 18 лет 1 -кратная ревакцинация через 5 лет Ежегодная ревакцинация взрослых в возрасте ≥ 65 лет, если 1 я доза вводилась в возрасте до 65 лет; лиц с аспленией; лиц с нарушением иммунитета
 Вместо заключения Назначение некоторых антибиотиков в амбулаторной практике может провоцировать развитие резистентности Опубликовано: Пятница, 27 августа 2010 г. - 09: 05 Согласно результатам недавно завершённого исследования пациенты, получавшие антибиотики в амбулаторной практике для лечения инфекций дыхательных или мочевыводящий путей, имеют более высокий риск устойчивости микроорганизмов к применявшемуся антибиотику при последующих инфекциях. Исследователями из Великобритании был выполнен систематический обзор 4373 публикаций, представленных в Medline, Embase и в Кокрановской базах банных, с целью определения тенденций антибиотикорезистентности микроорганизмов у пациентов, получавших антибиотики в амбулаторной практике. В окончательный мета-анализ было включено 24 исследования со сходными анализируемыми исходами. Среди них было 22 исследования, в которые включались пациенты с инфекциями, и 2 исследования, выполненные у здоровых добровольцев. В анализ были включены 19 обсервационных исследований (из них 2 проспективных) и 5 рандомизированных исследований. Были проанализированы объединённые результаты 5 исследований у 14348 пациентов с инфекциями мочевыводящих путей (ИМП). Объединённый показатель отношения шансов (ОШ) для наличия резистентных бактерий в данной популяции составил 2, 5 (95% доверительный интервал — ДИ от 2, 1 до 2, 9) в течение 2 месяцев после применения антибиотиков и 1, 33 (95% ДИ от 1, 2 до 1, 5) в течение 12 месяцев после лечения. В 7 исследованиях у 2605 участников изучалась антибиотикорезистентность возбудителей инфекций дыхательных путей. Объединённый показатель ОШ для наличия резистентных бактерий в данной популяции составил 2, 4 (95% ДИ от 1, 4 до 3, 9) в течение 2 месяцев после применения антибиотиков и 2, 4 (95% ДИ от 1, 3 до 4, 5) в течение 12 месяцев после лечения. По данным нескольких исследований, в которых было указано количество применявшихся антибиотиков, более длительное лечение и проведение нескольких курсов антимикробной терапии были связаны с более высокой частотой развития резистентности. В одном проспективном исследовании, включённом в мета-анализ, были определены показатели ОШ наличия резистентности после лечения в динамике на протяжении длительного периода наблюдения. Объединённые показатели ОШ составили: 12, 2 (95% ДИ от 6, 8 до 22, 1) через 1 неделю после применения антибиотиков; 6, 1 (2, 8 -3, 4) — через 1 месяц; 3, 6 (2, 2 -6, 0) — через 2 месяца и 2, 2 (1, 3 -3, 6) — через 6 месяцев после лечения. Таким образом, каждый случай применения антибиотиков приводит к достоверному повышению риска антибиотикорезистентности микроорганизмов и распространению носительства резистентных бактерий в популяции, что требует в последующем терапии антибиотиками «второй линии» при лечении инфекций в амбулаторной практике. Полученные результаты ещё раз подчеркивают важность предельно обоснованного и разумного применения антибиотиков при лечении инфекций в амбулаторной практике. Costelloe C. , et al. Effect of antibiotic prescribing in primary care on antimicrobial resistance in individual patients: systematic review and meta-analysis. BMJ 2010; 340: c 2096.
Вместо заключения Назначение некоторых антибиотиков в амбулаторной практике может провоцировать развитие резистентности Опубликовано: Пятница, 27 августа 2010 г. - 09: 05 Согласно результатам недавно завершённого исследования пациенты, получавшие антибиотики в амбулаторной практике для лечения инфекций дыхательных или мочевыводящий путей, имеют более высокий риск устойчивости микроорганизмов к применявшемуся антибиотику при последующих инфекциях. Исследователями из Великобритании был выполнен систематический обзор 4373 публикаций, представленных в Medline, Embase и в Кокрановской базах банных, с целью определения тенденций антибиотикорезистентности микроорганизмов у пациентов, получавших антибиотики в амбулаторной практике. В окончательный мета-анализ было включено 24 исследования со сходными анализируемыми исходами. Среди них было 22 исследования, в которые включались пациенты с инфекциями, и 2 исследования, выполненные у здоровых добровольцев. В анализ были включены 19 обсервационных исследований (из них 2 проспективных) и 5 рандомизированных исследований. Были проанализированы объединённые результаты 5 исследований у 14348 пациентов с инфекциями мочевыводящих путей (ИМП). Объединённый показатель отношения шансов (ОШ) для наличия резистентных бактерий в данной популяции составил 2, 5 (95% доверительный интервал — ДИ от 2, 1 до 2, 9) в течение 2 месяцев после применения антибиотиков и 1, 33 (95% ДИ от 1, 2 до 1, 5) в течение 12 месяцев после лечения. В 7 исследованиях у 2605 участников изучалась антибиотикорезистентность возбудителей инфекций дыхательных путей. Объединённый показатель ОШ для наличия резистентных бактерий в данной популяции составил 2, 4 (95% ДИ от 1, 4 до 3, 9) в течение 2 месяцев после применения антибиотиков и 2, 4 (95% ДИ от 1, 3 до 4, 5) в течение 12 месяцев после лечения. По данным нескольких исследований, в которых было указано количество применявшихся антибиотиков, более длительное лечение и проведение нескольких курсов антимикробной терапии были связаны с более высокой частотой развития резистентности. В одном проспективном исследовании, включённом в мета-анализ, были определены показатели ОШ наличия резистентности после лечения в динамике на протяжении длительного периода наблюдения. Объединённые показатели ОШ составили: 12, 2 (95% ДИ от 6, 8 до 22, 1) через 1 неделю после применения антибиотиков; 6, 1 (2, 8 -3, 4) — через 1 месяц; 3, 6 (2, 2 -6, 0) — через 2 месяца и 2, 2 (1, 3 -3, 6) — через 6 месяцев после лечения. Таким образом, каждый случай применения антибиотиков приводит к достоверному повышению риска антибиотикорезистентности микроорганизмов и распространению носительства резистентных бактерий в популяции, что требует в последующем терапии антибиотиками «второй линии» при лечении инфекций в амбулаторной практике. Полученные результаты ещё раз подчеркивают важность предельно обоснованного и разумного применения антибиотиков при лечении инфекций в амбулаторной практике. Costelloe C. , et al. Effect of antibiotic prescribing in primary care on antimicrobial resistance in individual patients: systematic review and meta-analysis. BMJ 2010; 340: c 2096.
 Спасибо за внимание!
Спасибо за внимание!


